法莫替丁杂质列表-杂质对照品
《药物分析》期末复习题(第三章至第四章)

《药物分析》期末复习题(第三章至第四章)第三章药物的杂质检查一、填空题1.药物在生产过程中可能引入的氯离子,氯离子对人体_______,但它能反映药物的_______及生产过程_______,因此氯化物常作为_______杂质检查。
药物中的微量氯化物检查的条件是在______比色管中,在_________条件下与__________反应,生成氯化银胶体微粒而显白色浑浊,与一定量的_____________溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合________规定。
比较时,比色管同置______背景上,从比色管__________观察,比较,即得。
氯化物浓度以50ml 中含_________μg的Cl-为宜,此范围内氯化物所显浑浊度明显,便于比较。
供试品溶液如不澄清,应________;如带颜色,可采用____________解决。
2. “一般杂质检查”收载于《中国药典》的________ 中,而特殊杂质检查收载于_______的各药品项下。
3.砷盐检查的古蔡氏法原理是金属锌与________反应产生________________,与药物中微量砷盐反应生成具有挥发性的____________,遇溴化汞试纸,产生黄色至棕色的________。
二、单项选择题1.药物中氯化物杂质检查的一般意义在于它( )A. 是有疗效的物质B. 是对药物疗效有不利影响的物质C. 是对人体健康有害的物质D. 可以考核生产工艺和企业管理是否正常E. 可能引起制剂的不稳定性2.检查磺胺嘧啶或苯巴比妥中的重金属可以选用( )A.硫代乙酰胺法(第一法)B.炽灼残渣法C.硫化钠法D.微孔滤膜法3.用古蔡法检砷时,产生的砷化氢气体与下列哪种物质作用生成砷斑( )A.氯化汞B.溴化汞C.碘化汞D.硫化汞4.在用古蔡氏检查砷盐时,导气管中塞入醋酸铅棉花的目的是除去供试品及试剂中的( )A.防止砷化氢逸失B.AS H3干扰 C.H2S干扰D.将五价砷还原为三价砷E. 防止H2逸失5.《中国药典》规定检查有机溶剂残留的方法为( )A. GC法B. HPLC法C. UV法D. TLC法6. 药物有关物质检查时,常首选色谱法,其中TLC不适用的检查法是( )A. 杂质对照品法适用于已知杂质并能制备杂质对照品的情况。
法莫替丁注射液的研制

法莫替丁注射液的研制目的:制备法莫替丁注射液,建立其质量控制方法,并考察其稳定性和安全性。
方法:优化处方组成与制备工艺,并进行性状、鉴别、检查等质量研究,采用高效液相色谱法测定有关物质和含量,影响因素试验、加速试验和长期试验考察其稳定性,血管刺激性试验、溶血性试验以及过敏性试验评价其用药的安全性。
结果:样品经酸、碱、氧化、热、光照破坏后所产生的杂质峰均能与主峰有效分离,最低检测限为1.0 ng。
法莫替丁在80.32~120.48 μg/ml的浓度范围内与峰面积成良好的线性关系,平均回收率为99.76%,RSD为0.73%。
恒温加速试验6个月和长期留样试验12个月,其性状、pH值、有关物质、可见异物、含量等均未见明显改变。
结论:该制剂处方合理,制备工艺简便可行,质量可控,稳定性良好,用药安全。
[Abstract] Objective: To prepare famotidine injection,establish its quality control and determine its stability and safety.Methods: Some work was done to optimize the prescription and preparation technology. The character, identification and examination et al were tested.The content and the related materials of famotidine injection were determined by HPLC.Stress testing, accelerated testing and long-term testing were done to study its stability. The safety was evaluated by testing the vessel stimulation, haemolyticus and hypersensitivity.Results:The method had an effective separation of the main component from impurities which produced after a series of destruction test,such as acid, alkalization,oxidation,light and thermal destruction.The detective limit was 1.0 ng. The linear relation of famotidine was excellent within the range of 80.32-120.48 μg/ml, and the average recovery rate was 99.76% with RSD was 0.73%. No obvious changes were observed at 6 month of an accelerated test or 12 month of long-term storage test. Conclusion: The preparation is reasonable in formulation, simple and convenient in preparation technique, accurate in quality control, good in stablility, and safe in application.[Key words] Famotidine injection; Preparation; Quality control; Stability; Safety法莫替丁为哌基噻唑类的H2受体拮抗剂,具有对H2受体亲和力高的特点,对胃酸分泌具有明显的抑制作用,对基础分泌及因给予各种刺激而引起的胃酸及胃蛋白酶增加有抑制作用。
非洛地平全套杂质汇总

项目报批 纯度高于98%
非洛地平EP杂质6 Felodipine Impurity 6 138279-32-0
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
非洛地平
Felodipine
72509-76-3
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
项目报批 纯度高于98%
非洛地平EP杂质4 Felodipine Impurity 4 105580-45-8
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
非洛地平EP杂质5 Felodipine Impurity 5
N/A
10mg 25mg 50mg 100mg 更大规格请咨询
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑 杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢! 专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。
非洛地平EP杂质B
(Felodipine EP
91189-59-2
Impurity B)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Felodipine Impurity 3
非洛地平EP杂质C
(Felodipine EP
欧洲药典总体结构中pdf

Claude Coune
疫苗
• 用于公众免疫的产品,专论提供了获取的公 共标准
• 专论作为质控当局官方批放行的依据 • 欧洲药典有所有儿童用和成人用疫苗的全部
专论 • 研发了参照制剂,使官方实验室能够进行独
立的批放行检验
Claude Coune
血液制品
• 专论作为质控当局官方批放行的依据 • 欧洲药典有所有工业化生产的血液制品(白
Claude Coune
注意事项 (5)
• 检验项目的缺省
– 在某些情况下某些检验项目不需要进行,因 为经过验证或有其他合理解释证明可以不做 该项检验
– 如果与工艺相关的杂质在实际工艺中不会产 生,可以不进行该杂质的检验
Claude Coune
注意事项 (6)
• 什么物质必须符合药典要求?
– 对所有药品是强制要求的 – 制剂的成分 – 制剂中含有的/或用来制备制剂的溶剂、缓
Claude Coune
FRCs的地位 (2)
• “以下检验项目不是强制性的要求,但 考虑到达到药品生产、质量和功效的一 致性是十分重要的,建议生产商确证这 些特性,并将所用的分析方法和结果提 供给使用者。以下方法已经证明是适用 的,但也可以使用其它方法。”
Claude Coune
FRCs的一些重要类别
– 粒度分布 – 堆密度和振实密度 – α-和β-乳糖 – 干燥失重
Claude Coune
乳糖一水化物的FRCs
• 它的用途与无水化物稍有区别,其FRC限 于以下两个方面:
– 粒度分布 – 堆密度和振实密度
Claude Coune
第2部分
个论和杂质控制
更多案例研究
法莫替丁EP杂质全套汇总
法莫替丁EP杂质G
Famotidine Impurity 7(Famotidine EP Impurity G)
76823-97-7
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
法莫替丁EP杂质I
Famotidine Impurity 8(Famotidine EP 1020719-36-1 Impurity I)
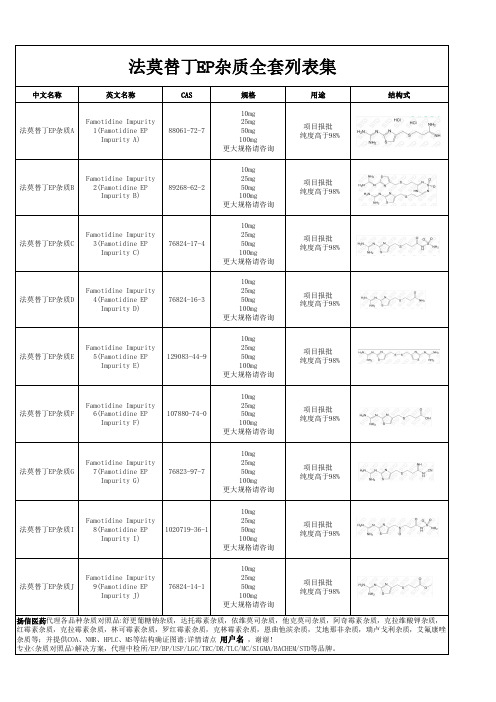
法莫替丁EP杂质全套列表集
中文名称
英文名称
CAS
法莫替丁EP杂质A
Famotidine Impurity 1(Famotidine EP Impurity A)
88061-72-7
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
法莫替丁EP杂质B
Famotidine Impurity 2(Famotidine EP Impurity B)
129083-44-9
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
法莫替丁EP杂质F
Famotidine Impurity 6(Famotidine EP Impurity F)
107880-74-0
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
89268-62-2
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
法莫替丁EP杂质C
Famotidine Impurity 3(Famotidine EP Impurity C)
76824-17-4
头孢唑肟Ceftizoxime杂质汇总列表

N/A
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
头孢唑肟杂质5 Ceftizoxime Impurity 5
N/A
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Ceftizoxime Impurity
头孢唑肟杂质10
10
79226-66-7
头孢唑肟Ceftizoxime杂质汇总列表
中文名称
英文名称
CAS
头孢唑肟杂质1 Ceftizoxime Impurity 1 929101-91-7
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
头孢唑肟杂质2 Ceftizoxime Impurity 2
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
头孢唑肟rity 11(E-Ceftizoxime Sodium Salt)
97164-53-9
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
唐 1814- 扬信医药 代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉
志 -064- 维酸钾杂质,红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非;
康
-3157 瑞卢戈利杂质,艾康氟康唑杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢!
扬信医药专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/ STD 等品牌。
Famotidine USP42 法莫替丁USP42标准 汉语版

法莫替丁USP42标准C8H15N7O2S3337.45UNII: 5QZO15J2Z8.定义包含98.5%-101.0%的法莫替丁(以C8H15N7O2S3)以干品计。
鉴别•A.红外吸收法〈197〉[注:方法在197K中介绍了,197M或者197A可能用不到]含量•步骤样品制备:溶解250mg法莫替丁至80ml冰醋酸中。
分析:使用合适的无水电极系统,用0.1 N高氯酸VS滴定(见滴定法541)。
进行空白测定,并进行必要的校正。
每毫升0.1 N高氯酸相当于16.87毫克C8H15N7O2S3。
可接受限度98.5%–101.0% ,以干品计。
杂质•炽灼残渣〈281〉:不超过0.1%•有机杂质缓冲液: 配成1.882 g/L 1-己磺酸钠的水溶液,用乙酸调节至pH值至3.5。
溶液A:乙腈, 甲醇, 和缓冲液 (94:6:900)溶液B:乙腈流动相:见表1. [注-如有必要,调整流动相,使法莫替丁峰的保留时间为19-23分钟,法莫替丁相关化合物E峰的保留时间最长为48分钟。
]表1标准储备液: 0.5 mg/mL的USP法莫替丁标准品溶于溶液A标准溶液: 0.5 µg/mL USP法莫替丁标准品在溶液A中。
系统适用性储备溶液: 0.25mg/ml的USP法莫替丁有关物质D标品的甲醇溶液系统适用性溶液:将1ml系统适用性储备液和0.5ml标准储备液移入100毫升容量瓶中,用溶液A稀释至刻度。
样品溶液:0.5 mg/mL 的法莫替丁在溶液A鉴别溶液:0.5 mg/mL 的USP法莫替丁标准品,和1.5 µg/mL的杂质B标品,杂质C标品,杂质D标品,杂质E标品,杂质F标品,分别于溶液A中。
(杂质标品均为USP法莫替丁相关物质标准品)[注:为了解决USP法莫替丁相关化合物F在溶液A中溶解度差的问题,可首先将其溶解在最小量的0.1N氢氧化钠中。
]气相色谱系统(见气相色谱《621》,系统适应性)型号: LC检测器: UV 265 nm色谱柱: 4.6-mm × 25-cm; 5-µm 填料L1柱温: 50°流速: 见表1.进样量: 20 µL系统适应性样品: 系统适应性溶液适应性要求分离度: 法莫替丁和杂质D的分离度,不低于3.5分析样品: 标准溶液、样品溶液、鉴别溶液用色谱仪对鉴别液进行色谱分析,并根据表2中给出的相对保留时间鉴定成分。
法莫替丁-溶出曲线资料

【法莫替丁】日文名:ファモチジン英文名:Famotidine 结构式:解离常数:pKa = 7.06在各溶出介质中的溶解度(37℃):pH1.2:29.0mg/ml pH4.0:15.7mg/mlpH 6.8:2.8mg/ml 水:1.9mg/ml在各溶出介质中的稳定性:水:未测定。
在各pH值溶出介质中:在pH1.2溶出介质中,24小时降解86.5%。
光:未测定。
《四条标准溶出曲线》溶出度试验条件:桨板法/50转、溶出介质中不添加表面活性剂。
< 1g:20mg规格散剂>< 1g:100mg规格散剂>< 10mg规格片剂>< 20mg规格片剂>《质量标准》●1g:20mg规格和1g:100mg规格散剂取本品,混匀,精密称取适量【相当于法莫替丁(CH15N7O2S3)20mg】,照溶出度测定8法(桨板法),以0.05mol/L醋酸-醋酸钠缓冲液(pH4.0)900ml为溶剂,转速为每分钟50转,依法操作,经15分钟时,取溶液适量滤过,弃去至少10ml初滤液,取续滤液作为供试品溶液。
另精密称取经五氧化二磷干燥剂80℃减压干燥4小时的对照品40mg,置100ml 量瓶中,加溶出介质溶解并稀释至刻度,摇匀,精密量取5ml,置100ml量瓶中,加溶出介质稀释至刻度,摇匀,作为对照品溶液。
取上述两种溶液照紫外-可见分光光度法,在266nm的波长处测定吸光度,计算出每袋溶出量,限度分别为标示量的80%或85%,应符合规定。
0.05mol/L醋酸-醋酸钠缓冲液(pH4.0) 取冰醋酸3.0g,加水1000ml,混匀,加0.68%醋酸钠三水合物溶液500ml,并调节pH值至4.0,即得。
●10mg规格和20mg规格片剂取本品,照溶出度测定法(桨板法),以0.05mol/L醋酸-醋酸钠缓冲液(pH4.0)900ml 为溶剂,转速为每分钟50转,依法操作,分别经45分钟或60分钟时,取溶液适量滤过,弃去至少10ml初滤液,取续滤液作为供试品溶液。
红霉素杂质列表

1
产品名称
红霉素杂质 1
红霉素杂质列表(部分)
英文名称
Erythromycin Impurity 1
(Erythromyc in EP Impurity
A)
CAS 号
82230-93 -1
规格
10mg-25mg-50mg -100mg
纯度
≥99
2
红霉素杂质 2
Erythromycin Impurity 2
6
红霉素杂质 6
≥99
Impurity 6
1
-100mg
结构式
广州隽沐生物主营各种杂质对照品:紫杉醇杂质,莫西沙星杂质,达托霉素杂质,
阿奇霉素杂质,帕拉米韦杂质,克拉霉素磷酸酯杂质,西格列汀杂质,林可霉素
杂质,奥拉帕利杂质,阿加曲班杂质,法莫替丁杂质,他达拉非杂质,厄洛替尼
杂质,替格瑞洛杂质等;并提供 COA、NMR、HPLC、MS、定量核磁等结构确证
527-75-3
10mg-25mg-50mg -100mg
≥99
Erythromycin
3
红霉素杂质 3
Impurity 3(Erythromyci n EP Impurity
41451-9100mg
≥99
C)
Erythromycin
4
红霉素杂质 4
Impurity 4(Erythromyci n EP Impurity
图谱。
177 二 813 八 655
代理中检所/EP/BP/USP/LGC/TRC/TLC/MC/SIGMA/等品牌。
124412-5 8-4
10mg-25mg-50mg -100mg
≥99
法莫替丁胃内滞留片的制备及体外释放度研究

法莫替丁胃内滞留片的制备及体外释放度研究摘要:目的:探讨法莫替丁胃内滞留片的制备工艺及体外释放特性。
方法:采用正交试验设计对法莫替丁胃内滞留片处方进行优化,按照最佳处方工艺制备胃内滞留片,以人工胃液为体外释放度测定介质,检测滞留片体外累积释放量,考察体外药物释放时间及体外释放行为。
结果:正交试验设计进行处方优化后制备的法莫替丁胃内滞留片,体外累积释放百分率符合Higychi方程,累积体外释放时间长。
结论:本文实验制备的胃内滞留片体外释放缓释效果良好,制备工艺简单。
关键词:法莫替丁;胃内滞留片;体外释放度;研究胃内滞留片是通过特殊制备工艺使口服片剂长时间滞留于胃液中的一种新型制剂,该类制剂在延长胃内滞留时间的基础上,能有效促进药物的吸收,进而提高药物的生物利用度,此剂型特别适用于生物利用度不高的药物[1],本文实验采用的法莫替丁传统剂型生物利用度低,因此制备法莫替丁胃内滞留片可提高药物的吸收利用度。
1实验材料1试剂和仪器骨架材料为羟丙甲纤维素和果胶,稀释剂为乳糖,阻滞剂为十八醇,法莫替丁原料药(购自上海现代药物有限公司),对照品(购自中检院,含量为99.07%),本实验中所用其他试剂均为分析纯级。
单冲压片机,体外溶出度检测仪,紫外分光光度计。
2方法与结果2.1处方优化采用正交试验设计优化处方工艺,选择骨架材料、稀释剂及阻滞剂作为影响滞留片质量的影响因素,进行4因素3水平进行正交试验[2],结果显示7号处方为最优处方工艺,骨架材料选择羟丙甲纤维素250mg,果胶30mg,稀释剂乳糖为50mg,阻滞剂十八醇为45mg,法莫替丁为40mg,具体正交试验结果见表1。
2.2滞留片制备按照7号处方工艺精密称取法莫替丁、骨架材料、阻滞剂及稀释剂充分搅匀,搅匀粉末过5号筛,用90%的乙醇将过筛粉末制成软材,于50℃下烘干后整粒,加入硬脂酸镁混匀后压片,片剂重量为415mg,其中含有法莫替丁40mg。
2.3测定波长选择精密称取干燥恒重的法莫替丁对照品,以人工胃液为介质配置浓度为20μg/ml的标准液,同时以各种赋形剂配置人工胃液溶液,两者均在一定波长范围内进行紫外扫描,扫描结果显示,标准液在264.5nm波长处有最大吸收,人工胃液及赋形剂在此波长处均无吸收。
西咪替丁杂质全套列表

中文名
CAS号
用途
结构式
西咪替丁杂质1(西咪替丁EP 杂质A)
52378-40-2
新药研发申报注册/ 鉴别、检查、含量测定
等 181+7164+1670
西咪替丁杂质2(西咪替丁EP 杂质B)来自138035-55-9
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质3(西咪替丁EP 杂质C)
52568-80-6
西咪替丁杂质列表
【怕发补,找扬信】 【怕发补,就用STD标准物质】
规格:10mg-25mg-50mg-100mg-200mg 随货提供氢谱、质谱、液相、COA,也可以提供CNMR、IR、UV、二维谱、水分、含量图谱等资料
杂质会实时更新,如列表没有您需要的产品可随时联系我 扬信医药小周 Q&VX3003379697
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质7(西咪替丁EP 杂质G)
31857-31-5
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质8(西咪替丁EP 杂质H)
74886-59-2
新药研发申报注册/ 鉴别、检查、含量测定
等
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质4(西咪替丁EP 杂质D)
59660-24-1
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质5(西咪替丁EP 杂质E)
54237-72-8
新药研发申报注册/ 鉴别、检查、含量测定
等
西咪替丁杂质6(西咪替丁EP 杂质F)
55272-86-1
地塞米松杂质整理列表(重点部分)
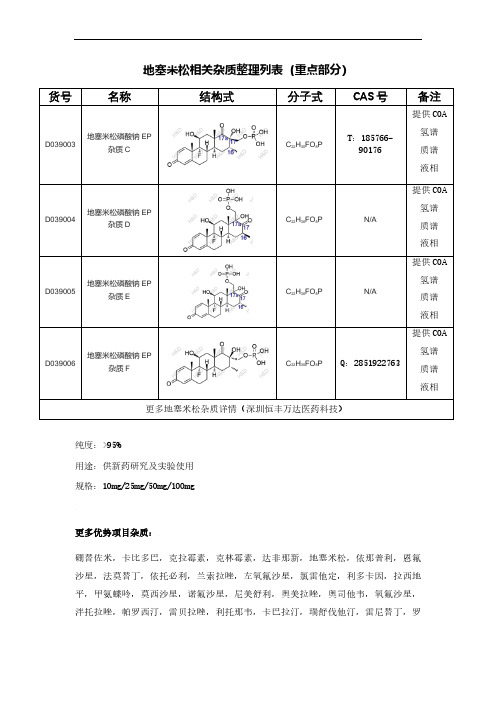
地塞米松相关杂质整理列表(重点部分)
货号
名称
结构式 分子式 CAS 号 备注
D039003 地塞米松磷酸钠EP
杂质C
C 22H 30FO 8P
T :185766-90176
提供COA 氢谱 质谱 液相 D039004
地塞米松磷酸钠EP
杂质D
C 22H 30FO 8P
N/A
提供COA
氢谱
质谱 液相 D039005
地塞米松磷酸钠EP
杂质E
C 22H 30FO 8P
N/A
提供COA
氢谱
质谱 液相 D039006
地塞米松磷酸钠EP
杂质F
C 22H 30FO 8P
Q :2851922763
提供COA
氢谱
质谱 液相
更多地塞米松杂质详情(深圳恒丰万达医药科技)
纯度:>95%
用途:供新药研究及实验使用 规格:10mg/25mg/50mg/100mg
更多优势项目杂质:
硼替佐米,卡比多巴,克拉霉素,克林霉素,达非那新,地塞米松,依那普利,恩氟沙星,法莫替丁,依托必利,兰索拉唑,左氧氟沙星,氯雷他定,利多卡因,拉西地平,甲氨蝶呤,莫西沙星,诺氟沙星,尼美舒利,奥美拉唑,奥司他韦,氧氟沙星,泮托拉唑,帕罗西汀,雷贝拉唑,利托那韦,卡巴拉汀,瑞舒伐他汀,雷尼替丁,罗
红霉素,沙丁胺醇,西他列汀,舍曲林,索菲那新,舒马曲坦,辛伐他汀,西洛多辛,托莫西汀,氨甲环酸,替卡格雷,替卡西林,替米沙坦,伐地那非等。
法莫替丁杂质整理总结文档

法莫替丁杂质18
Famotidine Impurity 18
47518F 503-66-2
10mg-25mg50mg-100mg
法莫替丁杂质19
Famotidine Impurity 19
47519F 542-76-7
10mg-25mg50mg-100mg
法莫替丁杂质20
Famotidine Impurity 20
法莫替丁杂质列表
湖北扬信医药科技有限公司经营上万种杂质对照品(优势供应①溴已新葡萄糖 ②奥司他韦葡萄糖加合物 ③替洛 福韦乳糖 ④阿德福韦酯乳糖加合物 ⑤硫酸羟氯喹杂质 ⑥硝苯地平杂质 ⑦沙丁胺醇杂质 ⑧达格列净杂质 ⑨厄贝 沙坦杂质 ⑩阿莫西林克拉维酸钾杂质 ⑪利伐沙班杂质 ⑫阿托伐他汀钙杂质 ⑬西格列汀杂质 ⑭利格列汀杂质 ⑮他 克莫司杂质 ⑯舒更葡糖钠杂质等),并代理销售中检所、STD、LGC、TLC、EP、USP、TRC等多个品牌产品, 提供上万种标准品对照品,真诚为您服务。杂质会实时更新,如列表没有您需要的产品可随时联系我 扬信医药小
法莫替丁杂质4 (法莫替丁EP杂
质D)
Famotidine Impurity
4(Famotidine EP Impurity D)
4754F 76824-16-3
10mg-25mg50mg-100mg
法莫替丁杂质5 (法莫替丁EP杂
质E)
Famotidine Impurity
5(Famotidine EP Impurity E)
Famotidine Impurity
7(Famotidine EP Impurity G)
4757F 76823-97-7
10mg-25mg50mg-100mg
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
序号杂质名称或编号英文名CAS
1法莫替丁杂质A Famotidine Impurity A
2法莫替丁杂质B Famotidine Impurity B
3法莫替丁杂质C Famotidine Impurity C
4法莫替丁杂质D Famotidine Impurity D
5法莫替丁杂质E Famotidine Impurity E
6法莫替丁杂质F Famotidine Impurity F
7法莫替丁杂质G Famotidine
Impurity G
法莫替丁杂质列表-杂质对照品
结构式及CAS
相关杂质1、阿考替胺杂质 2、维格列汀杂质 3、厄洛替尼杂质 4、利伐沙班杂质 5、索拉非尼杂质 6、阿伐那非杂质 7、替卡格雷杂质 8、阿哌沙班杂质 9、米格列奈杂质 10、普拉克索杂质 11、氨氯地平杂质 12、非不司他杂质 13、托法替尼杂质 14、达比加群酯杂质 15、埃索美拉唑钠杂质 16、盐酸氨溴索杂质 17、卡格列净杂质 18 索菲布韦杂质 19、依托考昔杂质
及代理其他品牌杂质标准品(EP、USP、LGC、TRC、TLC、MC、SINCO)等。
QQ:2850183206 联系电话:0755-2334 9667 手机:189******** 深圳菲斯——专注于标准品、杂质对照品。
