碱度与硬度的关系
总硬度和总碱度

总硬度和总碱度
总硬度是指水中钙、镁离子含量的总和,是衡量水质的一个重要指标。
它不仅关系到水的质量,还对水体的生态环境产生影响。
总硬度包括暂时硬度和永久硬度两种类型。
暂时硬度是由于水中含有碳酸钙和碳酸镁等矿物质,在加热或加入酸后会形成沉淀物,使硬度暂时消失。
而永久硬度则是由硫酸盐、氯化物等其他矿物质引起的,不会因加热或加入酸而消失。
总碱度则是指水中能够接受氢离子的一类物质的总量。
它包括强碱、弱碱、强碱弱酸盐等物质。
总碱度对于水体的pH值起到调节作用,从而影响水体的化学平衡和生态平衡。
总硬度与总碱度之间存在密切的关系。
当总碱度小于总硬度时,水体中的钙和镁不仅以碳酸盐和碳酸氢盐的形式存在,还会以硫酸盐、氯化物等非碳酸盐的形式存在。
这种水质的硬度较为复杂,处理难度较大。
当总碱度等于总硬度时,水体中的钙和镁只以碳酸盐和碳酸氢盐的形式存在,水质相对较为单一,处理起来也较为容易。
当总碱度大于总硬度时,水体中的钙和镁除了以碳酸盐和碳酸氢盐的形式存在外,还会以钾盐和钠盐等其他形式存在。
这种水质可能因含盐量较高而导致口感不佳,同时也会对水体的生态平衡产生一定的影响。
为了维护水质的健康和生态平衡,需要针对不同的总硬度与总碱度关系采取相应的处理措施。
同时,加强水质监测和生态保护也是非常重要的。
只有这样,才能确保水质的优良,为人类的生产和生活提供安全可靠的水资源。
标准之各种硬度单位换算表以及水质硬度范围
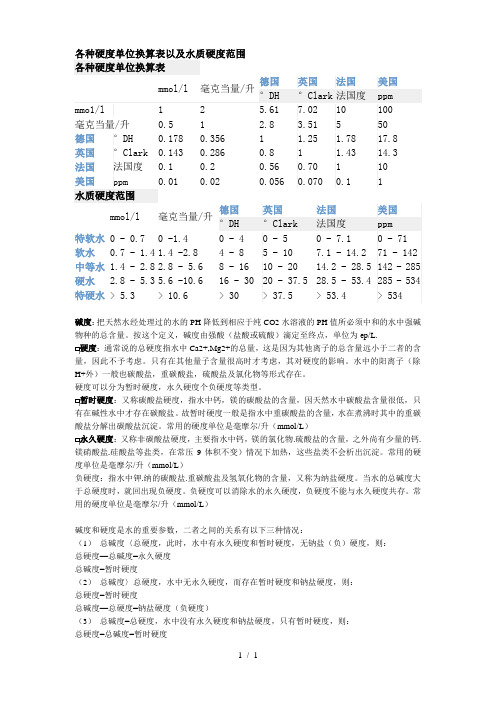
各种硬度单位换算表以及水质硬度范围各种硬度单位换算表mmol/l 毫克当量/升德国英国法国美国°DH°Clark法国度ppmmmo1/l 1 2 5.61 7.02 10 100 毫克当量/升0.5 1 2.8 3.51 5 50 德国°DH0.178 0.356 1 1.25 1.78 17.8 英国°Clark0.143 0.286 0.8 1 1.43 14.3 法国法国度0.1 0.2 0.56 0.70 1 10 美国ppm 0.01 0.02 0.056 0.070 0.1 1水质硬度范围mmol/l 毫克当量/升德国英国法国美国°DH°Clark法国度ppm特软水 0 - 0.7 0 -1.4 0 - 4 0 - 5 0 - 7.1 0 - 71软水0.7 - 1.4 1.4 -2.8 4 - 8 5 - 10 7.1 - 14.2 71 - 142 中等水 1.4 - 2.8 2.8 - 5.6 8 - 16 10 - 20 14.2 - 28.5 142 - 285 硬水 2.8 - 5.3 5.6 -10.6 16 - 30 20 - 37.5 28.5 - 53.4 285 - 534 特硬水 > 5.3 > 10.6 > 30 > 37.5 > 53.4 > 534碱度:把天然水经处理过的水的PH降低到相应于纯CO2水溶液的PH值所必须中和的水中强碱物种的总含量。
按这个定义,碱度由强酸(盐酸或硫酸)滴定至终点,单位为ep/L.硬度:通常说的总硬度指水中Ca2+,Mg2+的总量,这是因为其他离子的总含量远小于二者的含量,因此不予考虑。
只有在其他量子含量很高时才考虑,其对硬度的影响。
水中的阳离子(除H+外)一般也碳酸盐,重碳酸盐,硫酸盐及氯化物等形式存在。
硬度可以分为暂时硬度,永久硬度个负硬度等类型。
总碱度与碳酸盐硬度及pH 间的关系

随着社会经济的不断发展,污废水不经处理大量排放,河流水体受到了人类活动的严重影响,改变了原来的水化学特征,污染日趋严重。
这种变化了的形势,对水质监测工作提出了新的课题。
水质监测目的是及时、准确、全面地反映水环境质量状况及其发展趋势,为水环境管理、规划、污染治理等提供科学依据,它是国家合理开发利用和保护水资源的一项重要的基础工作,是控制水污染、保护水环境、改善水环境的哨兵与耳目。
水环境科学研究,对发展国民经济和保障人民健康等具有十分重要的意义。
1概述1)碱度:把天然水经处理过的水的PH降低到相应于纯CO2水溶液的PH值所必须中和的水中强碱物种的总含量。
2)暂时硬度:又称碳酸盐硬度,指水中钙,镁的碳酸盐的含量,因天然水中碳酸盐含量很低,只有在碱性水中才存在碳酸盐。
故暂时硬度一般是指水中重碳酸盐的含量,水在煮沸时其中的重碳酸盐分解出碳酸盐沉淀。
3)pH:表示溶液酸性或碱性程度的数值,是指溶液中氢离子的总数和总物质的量的比。
2检测方法2.1总碱度方法原理水样用标准酸溶液滴定至规定的pH值,其终点由加入的酸碱指示剂在该pH值时颜色的变化来判断。
当滴定至酚酞指示剂由红色变为无色时,溶液pH值为8.3,表明指示剂水中氢氧根离子已被中和,碳酸盐均变为重碳酸盐;当滴定至甲基橙指示剂由淡桔黄色变成桔红色时,溶液的pH值为4.4~4.5,指示水中的重碳酸盐被中和,包括原油的和由碳酸盐转化成。
根据上述2个终点到达时所消耗的盐酸标准滴定溶液的量,计算出水中碳酸盐、重碳酸盐含量及总碱度。
以酚酞作指示剂时,滴定至颜色变化消耗的盐酸标准溶液的量为P(ml),以甲基橙为指示剂时,滴定至颜色变化消耗的盐酸标准溶液的量为M(ml)。
2.2暂时硬度方法原理水中所含重碳酸盐(及碳酸盐)在用甲基橙为指示剂时与算起反应如下:Ca(HCO3)2+2HCl→CaCl2+2CO2↑+2H2O如有碳酸盐也起反应:CaCO3+2HCl→CaCl2+CO2↑+H2O如水中含有机酸、重碳酸或碳酸钠(或钾)等,均能消耗盐酸,因此在测定碳酸盐硬度以前,必要时应确定上述各物的含量而将所得结果加以校正,否则,计算的碳酸盐硬度便较实际数值高。
碱度和硬度的测定原理

碱度和硬度的测定原理
碱度和硬度是水质检测中常用的参数。
下面是碱度和硬度的测定原理。
碱度的测定原理:
碱度反映了水中碱性物质的含量,常用指标是水中的碳酸盐硬度。
常见的测定方法有酚酞法和酸碱滴定法。
酚酞法:该方法通过酚酞指示剂的变色反应来测定水中的碱度。
首先,将酚酞指示剂加入待测水样中,逐滴加入盐酸溶液直到溶液转为红色。
通过计算所使用的盐酸溶液的体积,可以确定水样中的碱度。
酸碱滴定法:该方法通过滴定剂和酸碱指示剂的反应来测定水中的碱度。
首先,将滴定剂(例如盐酸或硝酸)滴入待测水样中,滴定至溶液的pH值达到指示剂的变色点。
通过计算所使用的滴定剂的体积,可以确定水样中的碱度。
硬度的测定原理:
硬度是水中钙和镁离子的含量,可以分为总硬度和临时硬度两种。
常见的测定方法有EDTA滴定法和复合指示剂法。
EDTA滴定法:该方法通过EDTA (乙二胺四乙酸)与水样中的钙、镁离子生成络合物的滴定反应来测定水中的硬度。
首先,将专用指示剂(例如二甲基黄)加入水样中,直到溶液转为蓝色。
然后,滴定EDTA溶液直至溶液由蓝色转变为粉红
色。
通过计算所使用的EDTA溶液的体积,可以确定水样中的硬度。
复合指示剂法:该方法将复合的指示剂(例如酞菁T)与水样中的钙、镁离子生成络合物的反应来测定水中的硬度。
复合指示剂可在不同硬度的水样中产生颜色的变化,根据颜色的变化可以确定水样中的硬度。
总的来说,碱度和硬度的测定原理基于滴定反应或指示剂的变色反应,通过计算所使用的试剂体积,可以确定水样中的碱度和硬度。
永久硬度

永久硬度又称非碳酸盐硬度,主要指水中钙,镁的氯化物.硫酸盐的含量,之外尚有少量的钙.镁硝酸盐.硅酸盐等盐类,在常压9体积不变)情况下加热,这些盐类不会析出沉淀。
常用的硬度单位是毫摩尔/升(mmol/L)负硬度:指水中钾.纳的碳酸盐.重碳酸盐及氢氧化物的含量,又称为纳盐硬度。
当水的总碱度大于总硬度时,就回出现负硬度。
负硬度可以消除水的永久硬度,负硬度不能与永久硬度共存。
常用的硬度单位是毫摩尔/升(mmol/L)碱度和硬度是水的重要参数,二者之间的关系有以下三种情况:(1)总碱度〈总硬度,此时,水中有永久硬度和暂时硬度,无钠盐(负)硬度,则:总硬度—总碱度=永久硬度总碱度=暂时硬度(2)总碱度〉总硬度,水中无永久硬度,而存在暂时硬度和钠盐硬度,则:总硬度=暂时硬度总碱度—总硬度=钠盐硬度(负硬度)(3)总碱度=总硬度,水中没有永久硬度和钠盐硬度,只有暂时硬度,则:总硬度=总碱度=暂时硬度碱度basicity又称盐基度。
(1)中与的摩尔比。
一般用符号来代表碱度%。
它是的重要,它直接决定着的结构形态和许多特性,如、分子电荷数、混凝能力、贮存稳定性、等。
碱度是指中吸收的能力,水中碱度的形成主要是由于重碳酸盐、及的存在,、和也会产生一些碱度。
此外还有等。
各种碱度用标准酸滴定时可起下列:0H-十H+=H20CO32-十H+=HC03-;HC03-+H+=Hz0十CO2当至酚酞指示剂由红色变为无色时,溶液pH值即为8.3,指示水中离子(0H-)已被,碳酸盐均被转化为重碳酸盐,此时的滴定结果称为“酚酞碱度”。
当滴定至甲基橙指示剂由黄色度为橙红色时,溶液的pH值为4.4—4.5,指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和,此时的滴定结果称为“”。
通过计算可求出相应的碳酸盐、重碳酸盐和氢氧根的含量。
但对于、,则由于复杂,这种计算是无实际意义的。
(2)鞣性络合物鞣革性能的一个重要指标。
定义为,用表示的无机,如铬络合物中OH基的总当量数对的总当量数的。
硬度与碱度的关系

水处理中硬度与碱度的关系•水中离子的假想结合在水溶液中的无烟煤滤料硬度和碱度都是以离子状态单独存在的,有时为了研究问题方便起见,人为地将水中阳、阴离子结合起来,写成假想化合物的形态。
称为水中离子的假想结合。
•假想化合物的组成原则水体在蒸发浓缩时,阴、阳离子是按形成化合物时的溶解度由小至大的顺序排列的,这是因为无烟煤滤料溶解度小的先结合,故溶解度小的离子排在前面。
这样,阳离子按Ca2+、Mg2+、•Na+、K+的次序排列,阴离子按HCO3-、SO23-、Cl-的次序排列,如图1-2所示。
••在图1-2中,因HCO3-量大于Ca2+量,故所有的Ca2+都看作是由Ca(HCO3)2形成的,因此图1-2中AB段代表Ca(HCO3)2,同理,可以推知BC段代表Mg(HCO3)2,CD段代表MgSO4,余下的DE段代表Na+和K+的硫酸盐类,EF段代表Na+和K+的氯化盐类等。
这种表示法的原理是:钙和镁的碳酸氢盐最易转化成难溶的沉淀物,所以令它们首先假想结合;其次是钙、镁的硫酸盐;而阳离子Na+和K+以及阴离子Cl-都不易生成沉淀物,所以列在了最后。
•碱度和硬度的关系根据水中假想化合物组合的原则,无烟煤滤料厂家可以列出硬度和碱度的组合顺序,如表1-13所示。
由表1-13可知:•硬度与碱度的组合关系表1-13指标名称阳离子组合顺序假象化合物组合顺序阴离子组合顺序指标名称硬度Ca2+ + Mg2+ HCO3- 碱度钠离子Na+ + K+ SO24- Cl- 强酸根•(1)水中的硬度和碱度首先结合为碱性硬度,即Ca(HCO3)2、Mg(HCO3)2(2)当硬度大于碱度时,水中的离子才组成非碱性硬度,即CaSO4、MgSO4、CaCl2、MgCl2等。
(3)当硬度小于碱度时,水中的离子组合成的假想化合物除了碱性硬度以外,还含有NaHCO3、KHCO3,这种组合常称为有过剩碱度,也称为负硬度水。
•碱性水和非碱性水根据硬度和碱度之间的关系,天然水也可分为碱性水和非碱性水。
水的总碱度俗称水的硬度 什么是水的硬度

水的总碱度俗称水的硬度什么是水的硬度?水中有些金属阳离子,同一些阴离子结合在一起,在水被加热的过程中,由于蒸发浓缩,容易形成水垢,附着在受热面上而影响热传导,我们抒水中这些金属离子的总浓度称为水的硬度。
如在天然水中最常见的金属离子是钙离子(Ca2+)和镁离子(Mg2+),它与水中的阴离子如碳酸根离子(CO32-)、碳酸氢根离子(HCO3-)、硫酸根离子(SO42-)、氯离子(CL-)、以及硝酸根离子(NO3-)等结合在一起,形成钙镁的碳酸盐、碳酸氢盐、硫酸盐、氯化物、以及硝酸盐等硬度。
水中的铁、锰、钭等金属离子也会形成硬度,但由于它们在天然水中的含量很少,可以略去不计。
因此,通常就把Ca2+、Mg2+的总浓度看作水的硬度。
水的硬度对锅炉用水的影响很大,因此,应根据各种不同参数的锅炉对水质的要求对水进行软化或除盐处理。
测定方法1原理用酸碱中和滴定法测定总碱量,反应产物为NaCl+H2CO3,选用甲基橙作指标剂,用标准H2SO4溶液滴定至溶液由黄色变橙色,即为终点。
2试剂2.1甲基橙指示剂:0.1%(m/v)2.2 标准H2SO4溶液:0.1N3测定步骤3.1量取100.0ml澄清水样,注入250 ml锥形瓶中;3.2加入2滴甲基橙指标剂;3.3用0.1N标准H2SO4溶液滴定至溶液由橙色变黄色,记下标准H2SO4溶液用量Vml。
4计算结果总碱度=C×V /0.1=10 C×V (毫克当量/升)公式中C----标准H2SO4溶液浓度,N;V----标准H2SO4溶液用量V,ml;水的PH值,是指水的酸碱度什么是水的pH值?它有什么意义?pH值是水溶液最重要的理化参数之一。
凡涉及水溶液的自然现象。
化学变化以及生产过程都与pH值有关,因此,在工业、农业、医学、环保和科研领域都需要测量pH值。
水的pH值是表示水中氢离子活度的负对数值,表示为:pH=-lgaH+pH值有时也称氢离子指数,由于氢离子活度的数值往往很小,在应用上很不方便,所以就用pH值这一概念来作为水溶液酸性、碱性的判断指标。
盐度、硬度、碱度区别

盐度,总固体量,硬度,和碱度四个概念的区别一次和朋友聊起当地的水质,上面几个概念之间大家互相关联又有点混淆,所以觉得有必要对自己再进行一次水质科普。
于是找来了几本参考书,终于明白了他们之间的不同。
在此,结合一些健康知识和大家分享。
盐度(Salinity):主要指NaCl(盐)的成分,不包括其他溶解性离子成分。
盐有杀菌作用,有偶尔细菌性腹泻的人喝盐水能减轻症状。
但盐度太高除了给人的味觉感觉不太好,如果经常饮用也会给肾脏造成负担。
其水源主要是未经反渗透处理的海水。
总固体量(Total Dissolved Solids):顾名思义误以为是颗粒(particulate solid)的成分,但其实不然。
其主要指所有溶解性离子的总量,包括钠,钙,镁,锌,氯,硫酸盐,碳酸根,硝酸根,等物质,但不包括氢根阳离子和氢氧根阴离子。
美国环保署的二级标准(不要求所有人都遵守的规定)规定TDS不能超过500mg/L,其具体危害还在研究中。
但该指标是所有四个指标中唯一被明文限定的指标。
硬度(Hardness):仅仅指钙镁两种阳离子的总量,但表达单位却是CaCO3。
太少管道容易腐蚀,太多则容易起垢堵塞。
因为两者都易形成硬质沉淀,所以长期饮用高硬度水的人容易得胆结石。
此外,高硬度水也能降低洗涤剂的效果。
硬度的成分主要取决于水源经过的岩石或土壤层,有些地表水的硬度也会比地下水的硬度高。
碱度(Alkalinity):单位也是CaCO3,和硬度相同。
但在饮用水体中其成分主要指的是碳酸根,碳酸氢根离子,和少量的氢氧根。
适量的碱度能中和酸,起到平衡酸碱的作用,对人体有好处。
但碱度太大水会显得较浊,一般地下水水源的碱度比地表水的碱度高。
总体说,总固体量(TDS)表述的离子种类最多最广。
如果它的数量大,一般其他指标也会大。
但反之不然。
过大的硬度,碱度,和TDS 都可能导致沉淀,在管道内结垢,或者对人体产生结石,造成负面影响。
但另一方面,所有离子成分都是人体微量元素的重要组成部分,缺一不可。
什么叫水的碱度?

水中主要阳离子 水中主要阴离子 离子组成
Ca2+ Ca(HCO3)2
Mg2+ HCO3-
Mg(HCO3)2
B.碱度<硬度 这里面有两种情况:
NaHCO3 KHCO3
Na+ + K+ SO42Na2SO4 K2SO4
ClNaCl KCl
①HCO3- <[Ca2+ +Mg2+]<[HCO3- + SO42-] 这种类型水被称为硫酸盐型水。
硬度高,水质差,属于盐碱水范围
水中主要阳离 子
水中主要阴离 子
离子组成
Ca2+ HCO3Ca(HCO3)2
Mg2+
SO42MgSO4 CaSO4
Na+ + K+
Cl-
MgCl2
NaCl KCl
可能有两种情况:一种是 Ca2+>HCO3-的钙硬水;另一种是 Ca2+<HCO3-的 镁硬水。
水中主要阳 离子
Ca2+ > HCO3-的钙硬水离子组成
Ca2+
Mg2+
Na+ + K+
水中主要阴 离子
HCO3-
SO42-
Cl-
离子组成
Ca(HCO3)2
CaSO4 MgSO4
Na2SO4 K2SO4
NaCl KCl
Ca2+ < HCO3-的镁硬水离子组成
水中主要阳离
Ca2+
Mg2+子Na + K+水中主要阴离 子
HCO3-
SO42-
Cl-
水质中各检测指标的关系

水质中各检测指标得关系一、水质检测中各指标得定义:1.悬浮物:水中得悬浮物质就是颗粒直径在10-4mm以上得微粒,肉眼可见。
2.浑浊度:由于水中含有悬浮及胶体状态得微粒,使得原就是无色透明得水产生浑浊现象,使浑浊得程度称为浑浊度、1L水中含有1mgSiO2所构成得浊度为一个标准浊度单位,简称1度。
浑浊度就就是指浊度。
3.总硬:水中金属离子得总含量称为水得硬度。
(碳酸盐硬度与非碳酸盐硬度之与称为总硬)4.碱度:就是指水中CO32—、HCO3 -、OH—及其她一些弱酸盐类得总与、5.总铁:铁在水中有几种不同得存在形式,比如二价得亚铁(Fe2+),三价铁(Fe3+),铁得配合物(如铁与EDTA形成得配合物),铁得氧化物(如铁锈)。
以上水中各种形态得铁称为总铁、6.总磷:总磷包括水中溶解物质得含磷与悬浮物中得含磷。
7.电导率:电导率就是物质传送电流得能力,就是电阻率得倒数。
单位电导率(C)简单得说就是所测电导率(G)与电导池常数(L/A)得乘积、这里得L为两块极板之间得液柱长度,A为极板得面积。
一般通过对溶液电导得测量可掌握水中所溶解得总无机盐类得浓度指标。
8.CL- :水中游离态氯离子得总与。
水中氯离子降低方法:沉淀法、离子交换法、电渗析、膜过滤等。
9.PH值:二、水质中各种指标之间得关系1。
悬浮物与浑浊度得关系:悬浮物主要由泥沙、原生动物、澡类、细菌、病毒以及高分子有机物等组成,常常悬浮水流之中,产生水得浑浊度。
浑浊度与悬浮物得质量浓度大小有相关关系,因为颗粒得大小、形状、折射指数也影响悬浮体得光学性质、2、PH值与总碱之间得关系:总碱度M=[HCO3 - ]+2[CO32—]+[OH-]-[H+]PH≤8。
3时,水中只有HCO3-8、3≤PH<9.4时,水中只有CO32-、HCO3 —PH=9、4时,水中只有CO32—9、4〈PH<11.0时,水中只有CO32-、OH-PH≥11、0时,水中只有OH-3.电导率与总硬得关系:水溶液得电导率直接与溶解固体量浓度成正比,而且固体量浓度越高,电导率越大。
硬度的计算

硬度和碱度的计算一、硬度是指溶解在水中的盐类物质的含量,即钙盐与镁盐含量的多少。
钙镁离子的总合相当于10毫克氯化钙称之为1“度”。
硬度常以CaCO3(分子量=100)的当量来表示,并以水质中含1ppmCaCO3为1度。
计算硬度时,通常引起硬度的离子可用下列公式计算:硬度(ppmCaCO3)=M2+(ppm)×100/M2+的当量(公式中的M2+代表任一的二价金属离子)例如,若水质中含有10ppm的镁离子(Mg2+),以及15ppm的钙离子(Ca2+),则它的总硬度值计算如下:总硬度=镁硬度+钙硬度镁硬度=10ppm×100/24.4=41.0ppm钙硬度=15ppm×100/40.0=37.5ppm总硬度=41.0ppm+37.5ppm=78.5ppm(计算公式中的24.4为镁的当量重,40.0为钙的当量重)二、碱度是指水中吸收质子的能力,水中碱度的形成主要是由于重碳酸盐、碳酸盐及氢氧化物的存在,硼酸盐、磷酸盐和硅酸盐也会产生一些碱度。
此外还有有机碱等。
各种碱度用标准酸滴定时可起下列反应:0H-十H+=H20CO32-十H+=HC03-;HC03-+H+=H z0十CO2当滴定至酚酞指示剂由红色变为无色时,溶液pH值即为8.3,指示水中氢氧根离子(0H-)已被中和,碳酸盐均被转化为重碳酸盐,此时的滴定结果称为“酚酞碱度”。
当滴定至甲基橙指示剂由黄色度为橙红色时,溶液的pH值为4.4—4.5,指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和,此时的滴定结果称为“总碱度”。
一般把中和100克试样中的酸性物质所需要的OH-的物质的量n (OH-)用毫摩尔作单位的数值称为酸度。
水质中各检测指标的关系

水质中各检测指标的关系一、水质检测中各指标的定义:1.悬浮物:水中的悬浮物质是颗粒直径在10-4mm以上的微粒,肉眼可见。
2.浑浊度:由于水中含有悬浮及胶体状态的微粒,使得原是无色透明的水产生浑浊现象,使浑浊的程度称为浑浊度。
1L水中含有1mgSiO2所构成的浊度为一个标准浊度单位,简称1度。
浑浊度就是指浊度。
3.总硬:水中金属离子的总含量称为水的硬度。
(碳酸盐硬度和非碳酸盐硬度之和称为总硬)4.碱度:是指水中CO32-、HCO3 -、OH-及其他一些弱酸盐类的总和。
5.总铁:铁在水中有几种不同的存在形式,比如二价的亚铁(Fe2+),三价铁(Fe3+),铁的配合物(如铁与EDTA形成的配合物),铁的氧化物(如铁锈)。
以上水中各种形态的铁称为总铁。
6.总磷:总磷包括水中溶解物质的含磷和悬浮物中的含磷。
7.电导率:电导率是物质传送电流的能力,是电阻率的倒数。
单位电导率(C)简单的说是所测电导率(G)与电导池常数(L/A)的乘积.这里的L为两块极板之间的液柱长度,A为极板的面积。
一般通过对溶液电导的测量可掌握水中所溶解的总无机盐类的浓度指标。
8.CL- :水中游离态氯离子的总和。
水中氯离子降低方法:沉淀法、离子交换法、电渗析、膜过滤等。
9.PH值:二、水质中各种指标之间的关系1.悬浮物与浑浊度的关系:悬浮物主要由泥沙、原生动物、澡类、细菌、病毒以及高分子有机物等组成,常常悬浮水流之中,产生水的浑浊度。
浑浊度与悬浮物的质量浓度大小有相关关系,因为颗粒的大小、形状、折射指数也影响悬浮体的光学性质。
2.PH值与总碱之间的关系:总碱度M=[HCO3 - ]+2[CO32-]+[OH-]-[H+]PH≤8.3时,水中只有HCO3 -8.3≤PH<9.4时,水中只有CO32-、HCO3 -PH=9.4时,水中只有CO32-9.4<PH<11.0时,水中只有CO32-、OH-PH≥11.0时,水中只有OH-3.电导率与总硬的关系:水溶液的电导率直接和溶解固体量浓度成正比,而且固体量浓度越高,电导率越大。
碱度与硬度

水中的碱度和硬度的关系水中的硬度的大小与碱度的大小之比,能判别是碱性水或非碱性水。
当碱度大于硬度,(A>H)即[HCO3-]>[1/2Ca2+]+[1/2Mg2+],是碱性水。
水中的钙、镁离子都形成碳酸氢盐,没有非碳酸盐硬度,水中还有钠离子和钾离子的碳酸氢盐,这个碳酸氢盐量称为过剩碱度,即“负硬”。
当硬度大于碱度,(H>A)此时水中有非碳酸盐硬度存在,是非碱性水。
它们可分为钙硬水和镁硬水。
钙硬水[1/2Ca2+]>[HCO3-],水中有钙的非碳酸盐硬度而没有镁的碳酸盐硬度。
镁硬水[1/2Ca2+]<[HCO3-],水中有镁的碳酸盐硬度,而没有钙的非碳酸盐硬度。
离子交换树脂的吸附选择性离子交换树脂对溶液中的不同离子有不同的亲和力,对它们的吸附有选择性。
各种离子受树脂交换吸附作用的强弱程度有一般的规律,但不同的树脂可能略有差异。
主要规律如下:(1) 对阳离子的吸附高价离子通常被优先吸附,而低价离子的吸附较弱。
在同价的同类离子中,直径较大的离子的被吸附较强。
一些阳离子被吸附的顺序如下:Fe3+ > Al3+ > Pb2+ > Ca2+ > Mg2+ > K+ > Na+ > H+(2) 对阴离子的吸附强碱性阴离子树脂对无机酸根的吸附的一般顺序为:SO42-> NO3- > Cl- > HCO3-> OH-弱碱性阴离子树脂对阴离子的吸附的一般顺序如下:OH-> 柠檬酸根3- > SO42- > 酒石酸根2- >草酸根2- > PO43- >NO2- > Cl- >醋酸根- > HCO3-(3) 对有色物的吸附糖液脱色常使用强碱性阴离子树脂,它对拟黑色素(还原糖与氨基酸反应产物)和还原糖的碱性分解产物的吸附较强,而对焦糖色素的吸附较弱。
这被认为是由于前两者通常带负电,而焦糖的电荷很弱。
通常,交联度高的树脂对离子的选择性较强,大孔结构树脂的选择性小于凝胶型树脂。
水硬度的测定方法

水硬度的测定方法
水硬度的测定方法有以下几种:
1. 碱度法:采用碱度计,测定水样中溶解性碱质(碳酸根、氢氧根和氯离子)的总量,以毫摩尔(mmol/L)为单位,称为
碱度。
根据碱度和水中离子的类型,可以计算出水硬度的大小。
2. 氢氧化钙法:采用滴定法,分析水样中的氢氧化钙,以毫克每升(mg/L)为单位,称为氢氧化钙浓度,根据氢氧化钙浓
度可以计算出水硬度的大小。
3. 电导率法:采用电导率仪,测定水样的电导率,根据电导率可以计算出水硬度的大小。
4. 氢氧化锌法:采用滴定法,分析水样中的氢氧化锌,以毫克每升(mg/L)为单位,称为氢氧化锌浓度,根据氢氧化锌浓
度可以计算出水硬度的大小。
食品酸碱度对糖果硬度的影响研究

食品酸碱度对糖果硬度的影响研究糖果作为一种常见的零食,各种各样的颜色、口味和口感广受欢迎。
而糖果的硬度是在食用过程中最能直接感受到的一种特性。
人们喜欢各种不同硬度的糖果,而这种硬度与食品酸碱度之间的关系备受关注。
本文将探讨食品酸碱度对糖果硬度的影响,并分析其中的原因。
首先,我们需要了解什么是食品酸碱度。
食物的酸碱度是指其酸碱度值,也叫pH值。
pH值的范围是从0到14,其中7为中性,小于7为酸性,大于7为碱性。
酸碱度对于糖果的硬度有着一定的影响。
酸性食品一般具有较酸的口味,如柠檬、柚子等。
这类食品中的酸度会增加糖果的硬度。
原理是酸性物质能与糖分子发生反应,改变糖的结构,使其凝固得更紧密。
这就是为什么酸性糖果更容易嚼碎的原因。
可以通过加入柠檬汁或其他酸性成分来提高糖果硬度。
然而,过度酸度会使糖果过于硬,影响口感。
相反,碱性食品更容易溶解,如泡泡糖。
泡泡糖具有较高的碱性,其主要成分是碳酸氢钠。
碱性物质能中和酸性物质,使之变为盐和水。
因此,泡泡糖在口中会出现起泡的现象,表现为咀嚼感较软,而最终溶解于口中。
这是由于碱性物质与糖的分子结构相互作用,使其变得松散而不再凝固。
除了食品酸碱度,还有其他因素会影响糖果的硬度。
例如,糖的含量和结晶度也会对硬度产生影响。
高糖含量的糖果更容易结晶并变硬,而低糖含量的糖果则相对较软。
此外,制作过程中的温度、湿度和操作技巧也会对糖果的硬度产生影响。
在研究食品酸碱度对糖果硬度影响的过程中,我们还发现了一些有趣的现象。
例如,酸碱度还与糖果的保质期有关。
酸性糖果的保质期较短,因为酸性物质易导致糖果变质。
而碱性糖果因其成分特性,保质期相对较长。
总结起来,食品酸碱度对糖果硬度有着一定的影响。
酸性食品增加糖果硬度,而碱性食品则降低糖果的硬度。
这与食物的化学反应以及糖的结构有关。
然而,我们还需要深入研究糖果硬度的影响因素,包括制作工艺、温度、湿度等,以便进一步提高糖果的口感和质量。
对于糖果制造商和消费者来说,了解酸碱度与糖果硬度之间的关系对于改善产品和满足消费者口感需求至关重要。
碱度与硬度的关系

碱度与硬度的关系:a.总碱度>总硬度此时,永硬为0总碱度-总硬度=负硬度此时,水呈碱性(pH>7);b.总碱度=总硬度此时,总碱度=暂时硬度;c.总碱度<总硬度此时,总硬度-总碱度=永硬pH值与碱度的关系:碱度相同的水(或溶液),其pH值不一定相同。
反之,pH值相同的水(或溶液),其碱度也不一定相同。
原因是pH值直接反映水中H+或OH-的含量,而碱度除包括OH-外,还包括CO3-2、HCO3-等碱性物质的含量。
如:碱度L的NaOH液,pH=13碱度L的NaHCO3液,pH=碱度L的NH3-H2O液,pH=11水的碱度是指水中能够接受H+离子与强酸进行中和反应的物质含量。
水中产生碱度的物质主要由碳酸盐产生的碳酸盐碱度和碳酸氢盐产生的碳酸氢盐碱度,以及由氢氧化物存在和强碱弱酸盐水解而产生的氢氧化物碱度。
所以,碱度是表示水中CO32-、HCO3-、OH-及其他一些弱酸盐类的总和。
这些盐类的水溶液都呈碱性,可以用酸来中和。
然而,在天然水中,碱度主要是由HCO3-的盐类所组成。
可认为:总碱度M=[HCO3-]+2[CO32-]+[OH-]-[H+] 当pH值大于时,[H+]可略去,故,M=c(Bx-)=[HCO3-]+[2CO32-]+[OH-]mol/L 形成水中碱度的物质碳酸盐和碳酸氢盐可以共存,碳酸盐和氢氧化物也可以共存。
然而,碳酸氢盐与氢氧化物不能同时存在,它们在水中能起如下反应:HCO3-+OH-==CO32-+H2O 由此可见,碳酸盐、碳酸氢盐、氢氧化物可以在水中单独存在,除此之外,还有两种碱度的组合,所以,水中的碱度有五种形式存在,即:(1)碳酸氢盐碱度HCO3-;(2)碳酸盐碱度CO32-;(3)氢氧化物碱度OH-;(4)碳酸氢盐和碳酸盐碱度HCO3-+ CO32-;(5)碳酸盐和氢氧化物碱度CO32-+ OH-。
简而言之:碱度是水介质与氢离子反应的定量能力,通过用强酸标准溶液将一定体积的水样滴定至某一pH值而定量确定。
水的硬度与碱度的测定

水硬度的测定实验目的:1 .了解水的硬度的概念,测定水硬度的意义,以及水的硬度的表示方法;2 .理解EDTA测定水中钙、镁含量的原理和方法,包括酸度控制和指示剂的选择;3 .测定过程中加入Mg-EDTA的作用及其对测定结果的影响。
实验原理:水的硬度最初是指钙、镁离子沉淀肥皂的能力。
水的总硬度指水中钙、镁离子的总浓度,其中包括碳酸盐硬度( 即通过加热能以碳酸盐形式沉淀下来的钙、镁离子,故又叫暂时硬度) 和非碳酸盐硬度( 即加热后不能沉淀下来的那部分钙、镁离子,又称永久硬度) 。
硬度的表示方法尚未统一,目前我国使用较多的表示方法有两种:一种是将所测得的钙、镁折算成CaO 的质量,即每升水中含有CaO 的毫克数表示,单位为mg·L-1 ;另一种以度( °) 计:1硬度单位表示10 万份水中含1份CaO( 即每升水中含10mgCaO) ,1°=10ppm CaO 。
这种硬度的表示方法称作德国度。
【工业用水和生活饮用水对水的硬度的要求】我国生活饮用水卫生标准规定以CaCO3 计的硬度不得超过450mg·L-1 。
Ca2+ + EDTA = Ca-EDTAMg2+ + EDTA = Mg-EDTA实验预习:了解配制和标定EDTA标准溶液的方法;了解测定的水的总硬度的原理和方法。
基本操作:EDTA标准溶液的配制和标定;酸式滴定管的基本操作。
实验步骤:在一份水样中加入pH=10.0 的氨性缓冲溶液和少许铬黑T 指示剂,溶液呈红色;用EDTA标准溶液滴定时,EDTA先与游离的Ca2+ 配位,再与Mg2+ 配位;在计量点时,EDTA 从MgIn- 中夺取Mg2+ ,从而使指示剂游离出来,溶液的颜色由红变为纯蓝,即为终点。
当水样中Mg2+ 极少时,由于CaIn- 比MgIn- 的显色灵敏度要差很多,往往得不到敏锐的终点。
为了提高终点变色的敏锐性,可在EDTA标准溶液中加入适量的Mg2+ (在EDTA 标定前加入,这样就不影响EDTA与被测离子之间的滴定定量关系),或在缓冲溶液中加入一定量的Mg—EDTA盐。
水质中各检测指标的关系

水质中各检测指标得关系一、水质检测中各指标得定义:1.悬浮物:水中得悬浮物质就是颗粒直径在1 0利mm以上得微粒,肉眼可见。
2.浑浊度:由于水中含有悬浮及胶体状态得微粒,使得原就是无色透明得水产生浑浊现象,使浑浊得程度称为浑浊度、1L水中含有1 mgS i 0 2所构成得浊度为一个标准浊度单位,简称1度。
浑浊度就就是指浊度。
3.总硬:水中金属离子得总含量称为水得硬度。
(碳酸盐硬度与非碳酸盐硬度之与称为总硬)4.碱度:就是指水中CO3 2—、HCO3-、OH—及其她一些弱酸盐类得总与、5.总铁:铁在水中有几种不同得存在形式,比如二价得亚铁(Fe2+),三价铁(Fe 3 +),铁得配合物(如铁与EDTA形成得配合物),铁得氧化物(如铁锈)。
以上水中各种形态得铁称为总铁、6•总磷:总磷包括水中溶解物质得含磷与悬浮物中得含磷。
7.电导率:电导率就是物质传送电流得能力,就是电阻率得倒数。
单位电导率(C)简单得说就是所测电导率(G)与电导池常数(L/A)得乘积、这里得L为两块极板之间得液柱长度,A为极板得面积。
一般通过对溶液电导得测量可掌握水中所溶解得总无机盐类得浓度指标。
8.CL-:水中游离态氯离子得总与。
水中氯离子降低方法:沉淀法、离子交换法、电渗析、膜过滤等。
9.P II 值:二、水质中各种指标之间得关系1。
悬浮物与浑浊度得关系:悬浮物主要由泥沙、原生动物、澡类、细菌、病毒以及高分子有机物等组成,常常悬浮水流之中,产生水得浑浊度。
浑浊度与悬浮物得质量浓度大小有相关关系,因为颗粒得大小、形状、折射指数也影响悬浮体得光学性质、2、P H值与总碱之间得关系:总碱度M=[IIC03-]+2[CO32~] +[OH_]-[H+]PHW8。
3时,水中只有II C 0 3_8、3W PH<9.4 时冰中只有CO32\ IICO3-PH=9、4时冰中只有CO32-9、4〈PH<11. 0 时,水中只有C 0 32\ OilPHN11、0时,水中只有OH3.电导率与总硬得关系:水溶液得电导率直接与溶解固体量浓度成正比,而且固体量浓度越高,电导率越大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碱度与硬度的关系:
a.总碱度>总硬度此时,永硬为0
总碱度-总硬度=负硬度此时,水呈碱性(pH>7);
b.总碱度=总硬度此时,总碱度=暂时硬度;
c.总碱度<总硬度此时,总硬度-总碱度=永硬
pH值与碱度的关系:
碱度相同的水(或溶液),其pH值不一定相同。
反之,pH值相同的水(或溶液),其碱度也不一定相同。
原因是pH值直接反映水中H+或OH-的含量,而碱度除包括OH-外,还包括CO3-2、HCO3-等碱性物质的含量。
如:碱度0.1mmol/L的NaOH液,pH=13
碱度0.1mmol/L的NaHCO3液,pH=8.3
碱度0.1mmol/L的NH3-H2O液,pH=11
水的碱度是指水中能够接受H+离子与强酸进行中和反应的物质含量。
水中产生碱度的物质主要由碳酸盐产生的碳酸盐碱度和碳酸氢盐产生的碳酸氢盐碱度,以及由氢氧化物存在和强碱弱酸盐水解而产生的氢氧化物碱度。
所以,碱度是表示水中CO32-、HCO3-、OH-及其他一些弱酸盐类的总和。
这些盐类的水溶液都呈碱性,可以用酸来中和。
然而,在天然水中,碱度主要是由HCO3-的盐类所组成。
可认为:总碱度M=[HCO3-]+2[CO32-]+[OH-]-[H+] 当pH 值大于7.0时,[H+]可略去,故, M=c( Bx-)=[HCO3-]+[2CO32-]+[OH-]mol/L 形成水中碱度的物质碳酸盐和碳酸氢盐可以共存,碳酸盐和氢氧化物也可以共存。
然而,碳酸氢盐与氢氧化物不能同时存在,它们在水中能起如下反应: HCO3-+OH-==CO32-+H2O 由此可见,碳酸盐、碳酸氢盐、氢氧化物可以在水中单独存在,除此之外,还有两种碱度的组合,所以,水中的碱度有五种形式存在,即:(1)碳酸氢盐碱度HCO3-;(2)碳酸盐碱度CO32-;(3)氢氧化物碱度OH-;(4)碳酸氢盐和碳酸盐碱度HCO3-+ CO32-;(5)碳酸盐和氢氧化物碱度CO32-+ OH-。
简而言之:碱度是水介质与氢离子反应的定量能力,通过用强酸标准溶液将一定体积的水样滴定至某一pH值而定量确定。
测定结果用相当于碳酸钙的质量溶液,
mg/L为单位表示。
