高分子化学第二章逐步聚合反应
合集下载
高分子课件第二章 逐步聚合反应

五、线型缩聚机理
许多缩聚物都是通过逐步聚合的机理聚合得到的。
单体(一聚体)
二聚体
三聚体
......
低聚体 + 低聚体
高聚体
低聚体 + 高聚体
高聚体
大多数缩聚反应都是可逆平衡反应
OH +
k1 COOH k-1
OCO
+ H2O
平衡常数
K
k1 k1
OCO H2O OH COOH
酯化反应的K=4。在实际生产中,为使反应尽量 向生成高聚物的方向移动,通常要采取措施将副产 物小分子尽量排除。如:通入惰性气体或抽真空。
a
a
AA
n
+n
A
如: a
b
b
BB
B b
AA A
B B BA A
A
B B BA
B AB B
A
B BB
3、按照热力学特征分 ⑴ 平衡缩聚
具有可逆变化特性的缩聚反应
如:
nHOROH + nHOOCR'COOH
H
OROOCR'CO n OH + (2n-1)H 2O
⑵ 不平衡缩聚反应
在缩聚反应的条件下不发生逆反应的缩聚反应
NH2(CH2)3COOH
成环—单分子反应 缩聚—双分子反应
O
( 内
C
CH3 CH
O
交 酯
/
O
H2C H2C
CH CH3
内
C
环
O
酯 )(
CH2
环
C O +H2O 酰
N
胺
H
)
故增加单体浓度,有利于缩聚反应
高分子化学-第二章 缩聚和逐步聚合
N0
N0
反应程度与转化率的区别
转化率:参加反应的单体量占起始单体量的分数,是指已 经参加反应的单体的数目
反应程度:则是指已经反应的官能团的数目
例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体,就 单体转化率而言,转化率达100%;而官能团的反应程度 仅50%
反应程度与平均聚合度的关系
聚合度是指高分子中含有的结构单元的数目
聚加成:形式上是加成反应,但反应机理是逐步反应。 如聚氨酯的合成(p17)。
开环反应:部分开环反应为逐步反应,如水、酸引发的己内 酰胺的开环反应。
氧化-偶合:单体与氧气的缩合反应, 如 2,6-二甲基苯酚和氧 气形成聚苯撑氧,也称聚苯醚。
2 逐步聚合反应的特点
官能团间的反应,无特定的活性中心;无所谓的引发、 增长、终止等基元反应;反应逐步进行,每一步的反 应速率和活化能大致相同;
[ H + ][ A- ] KHA =
[ HA ]
[ HA ] [ H + ] [ A- ] = KHA
代入式
-d [ COOH ] = k1k3[ COOH ][OH ][ H+]
dt
k 2KHA
催化用酸HA:可以是二元酸本身,但反应较慢,也可以是 外加酸,如H2SO4,大大加速
自催化缩聚反应
无外加酸,二元酸单体催化剂,[HA] = [COOH]
Flory对此进行了解释:
官能团等活性理论是近似的,不是绝对的,这一理论大大简化了研 究处理,可用同一平衡常数表示,整个缩聚过程可以用两种官 能团之间的反应来表征
COOH + HO
k1
OCO
k1
2. 线型缩聚动力学
不可逆条件下的缩聚动力学
高分子化学第二章-缩聚及逐步聚合

2.2.2 缩聚反应分类
l 按反应热力学的特征分类 平衡缩聚反应 指平衡常数小于 103 的缩聚反应 不平衡缩聚反应 平衡常数大于 103
l按生成聚合物的结构分类 线型缩聚 体型缩聚
2.2.3 特点
缩聚反应是缩合聚合反应的简称,是缩合反应多 次重复结果形成缩聚物的过程。 1、典型缩合反应——形成低分子化合物
3 、反应程度与数均聚合度的关系
数均聚合度是指高分子中含有的结构单元的数目。
Xn
起始单体数目
=
达到平衡时同系物数目(大分子数)
N0 N
代入反应程度关系式
P = N0-N = 1- N
N0
N0
P = 1- 1 Xn
1 Xn = 1-P
一般 Xn 100~200 P提高到
0.99~0.995
300 250 200
a. 密闭体系中,nw=P
Xn
1 P
K=
1 nw
K
当M n 104 , P 1, X n
K nw
平衡缩聚中数均聚合度与平衡常数
及小分子副产物浓度三者关系
Xn只与温度有关,与其他无关。(因为nw平衡时为定值)
b. 敞开体系,水排出,则 nw为体系中剩余的。
说明:X
的影响因素
n
密闭体系,只与T有关 敞开体系,与排出的水有关
3、缩聚中的副反应 副反应
消去反应 化学降解 链交换反应
消去反应
HOOC(CH2)nCOOH
HOOC(CH2)nH + CO2
二元酸脱羧温度(℃)
己二酸 300~320 庚二酸 290~310 辛二酸 340~360 壬二酸 320~340 癸二酸 350~370
l 按反应热力学的特征分类 平衡缩聚反应 指平衡常数小于 103 的缩聚反应 不平衡缩聚反应 平衡常数大于 103
l按生成聚合物的结构分类 线型缩聚 体型缩聚
2.2.3 特点
缩聚反应是缩合聚合反应的简称,是缩合反应多 次重复结果形成缩聚物的过程。 1、典型缩合反应——形成低分子化合物
3 、反应程度与数均聚合度的关系
数均聚合度是指高分子中含有的结构单元的数目。
Xn
起始单体数目
=
达到平衡时同系物数目(大分子数)
N0 N
代入反应程度关系式
P = N0-N = 1- N
N0
N0
P = 1- 1 Xn
1 Xn = 1-P
一般 Xn 100~200 P提高到
0.99~0.995
300 250 200
a. 密闭体系中,nw=P
Xn
1 P
K=
1 nw
K
当M n 104 , P 1, X n
K nw
平衡缩聚中数均聚合度与平衡常数
及小分子副产物浓度三者关系
Xn只与温度有关,与其他无关。(因为nw平衡时为定值)
b. 敞开体系,水排出,则 nw为体系中剩余的。
说明:X
的影响因素
n
密闭体系,只与T有关 敞开体系,与排出的水有关
3、缩聚中的副反应 副反应
消去反应 化学降解 链交换反应
消去反应
HOOC(CH2)nCOOH
HOOC(CH2)nH + CO2
二元酸脱羧温度(℃)
己二酸 300~320 庚二酸 290~310 辛二酸 340~360 壬二酸 320~340 癸二酸 350~370
高分子化学第二章-精品.ppt

注意:在书写这类聚合物的结构式时,一般要求其重复结构单元 的表达式必须反映功能基反应机理,如聚酯化反应时,其反应机理 是羧基和羟基之间的脱水反应,羧基失去的是-OH,羟基失去的是 -H:
OO HOCRCO HHOR' O H
因此聚酯分子结构式更准确的表达式应为2-1,而不是式2-2:
OO H OCRCO R 'O n H
高分子化学
第二章 逐步聚ห้องสมุดไป่ตู้反应
2.1 概 述
2.1.1 逐步聚合反应的一般性特征
以二元羧酸与二元醇的聚合反应为例:
H O O C - R - C O O H + H O - R ' - O H H O O C - R - C O O - R ' - O H + H 2 O 二 聚 体
H O O C - R - C O O H H O O C - R - C O O - R '- O O C - R - C O O H + H 2 O
(2)聚酰胺化反应,包括二元胺与二元羧酸、二元酯或二元酰氯等
之间的聚合反应,如
O O
O O
n C lC R 'C C l+ n H 2 N - R '- N H 2 C l( C R C N H R 'N H ) n H + ( 2 n - 1 ) H C l
(3)聚醚化反应,二元醇和二元醇之间的聚合反应
线形逐步聚合单体为双功能基单体,聚合产物分子链只会向两个 方向增长,生成线形高分子。
非线形逐步聚合反应的聚合产物分子链不是线形的,而是支化或 交联的。此时必须在聚合体系中加入含三个以上功能基的单体。
2.2 逐步聚合反应的分类
第二章 逐步聚合反应

………………
+二 酸 二 胺 HO [OC(CH 2)4CONH(CH 2)6NH]n H -(2n-1)H 2O
一、 缩聚反应的定义
官能团间经过多次缩合形成聚合物的反 应,即缩合聚合反应的简称。 即缩合聚合反应的简称。
特点: 特点: 缩聚物有特征结构官能团 有低分子副产物 缩聚物和单体分子量不成整数倍
线形缩聚
一、平衡线形缩聚
指缩聚过程中生成的产物可被反应中伴生 的小分子降解, 的小分子降解,单体分子与聚合物分子之间存 在可逆平衡的逐步聚合反应。 在可逆平衡的逐步聚合反应。
例如: 例如:聚酯化反应
线形缩聚的机理: 线形缩聚的机理:逐步和可逆
机理特征:逐步、 机理特征:逐步、可逆
是官能团间的逐步反应,且每一步都是可逆的。 是官能团间的逐步反应,且每一步都是可逆的。
第二章 逐步聚合反应
stepwise polymerization
第一节 引言
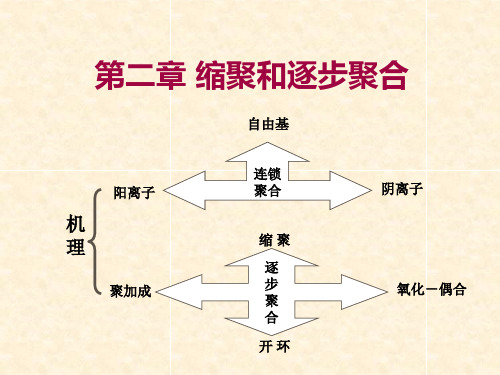
按聚合机理或动力学分类: 按聚合机理或动力学分类: ★连锁聚合(chain polymerization) 连锁聚合( ) ------活性中心(active center)引发单体,迅 活性中心( )引发单体, 活性中心 速连锁增长 ★逐步聚合(stepwise polymerization) 逐步聚合( ) ------无活性中心,单体所带的不同官能团间相 无活性中心, 无活性中心 互反应而逐步增长 互反应而逐步增长
缩聚反应的分类(本章就以缩聚反应为代表) 缩聚反应的分类(本章就以缩聚反应为代表)
1)按反应热力学分类: )按反应热力学分类:
平衡缩聚(或可逆缩聚) 平衡缩聚(或可逆缩聚) K<103 如聚酯 K=4 不平衡缩聚(不可逆缩聚) K>103 如聚碳酸酯 不平衡缩聚(不可逆缩聚)
高分子化学 第2章 逐步聚合反应1

是参加反应的官能团数占起始官能团数的分数,用P 表示 反应程度可以对任何一种参加反应的官能团而言 对于等物质量的二元酸和二元醇的缩聚反应,设: 体系中起始二元酸和二元醇的分子总数为N0 等于起始羧基数或羟基数 t 时的聚酯分子数为N,等于残留的羧基或羟基数
N0-N N P= =1 - N0 N0
17
解:当己二酸过量时,尼龙-66的分子结构为
HO CO(CH2)4CONH(CH2)6NH n CO(CH2)4COOH
112 114
q+2 ( Na+Nb ) / 2 1 +r Xn = = = ( Na+Nb-2 NaP ) / 2 1 +r-2rP q+2( 1 -P )
表示了Xn与P、r或q之间的定量关系式
21
q+2 1 +r Xn = = 1 +r-2rP q+2( 1 -P )
讨论两种极限情况:
当原料单体等当量比时 即r=1或q=0
n HORCOOH
2-3、2-4官能度体系 如:苯酐和甘油反应 苯酐和季戊四醇反应
体形缩聚物
双官能度体系的成环反应
2-2或 2 官能度体系是线形缩聚的必要条件,但 不是充分条件 在生成线形缩聚物的同时,常伴随有 成环反应
9
2.2.3 平均官能度(f)
体系中可能反应的官能团总数(总当量数)被体系 分子数所除而得的结果。
与醛缩合,官能度为 3
官能度与官能团的关系?
如: 乙炔
7
对于不同的官能度体系,其产物结构不同
1-n官能度体系 一种单体的官能度为 1,另一种单体的官能度大 于1 ,即 1-1、1-2、1-3、1-4体系 只能得到低分子化合物,属缩合反应 2-2官能度体系 每个单体都有两个相同的官能团 可得到线形聚合物,如
N0-N N P= =1 - N0 N0
17
解:当己二酸过量时,尼龙-66的分子结构为
HO CO(CH2)4CONH(CH2)6NH n CO(CH2)4COOH
112 114
q+2 ( Na+Nb ) / 2 1 +r Xn = = = ( Na+Nb-2 NaP ) / 2 1 +r-2rP q+2( 1 -P )
表示了Xn与P、r或q之间的定量关系式
21
q+2 1 +r Xn = = 1 +r-2rP q+2( 1 -P )
讨论两种极限情况:
当原料单体等当量比时 即r=1或q=0
n HORCOOH
2-3、2-4官能度体系 如:苯酐和甘油反应 苯酐和季戊四醇反应
体形缩聚物
双官能度体系的成环反应
2-2或 2 官能度体系是线形缩聚的必要条件,但 不是充分条件 在生成线形缩聚物的同时,常伴随有 成环反应
9
2.2.3 平均官能度(f)
体系中可能反应的官能团总数(总当量数)被体系 分子数所除而得的结果。
与醛缩合,官能度为 3
官能度与官能团的关系?
如: 乙炔
7
对于不同的官能度体系,其产物结构不同
1-n官能度体系 一种单体的官能度为 1,另一种单体的官能度大 于1 ,即 1-1、1-2、1-3、1-4体系 只能得到低分子化合物,属缩合反应 2-2官能度体系 每个单体都有两个相同的官能团 可得到线形聚合物,如
高分子化学第二章 缩聚和逐步聚合

O=
C
H2C─C O H2C─CH2
H2C O
H2C CH2 CH2
20
• HO–(CH2)n–COOH缩聚
n=1,2HOCH2COOH HOCH2COOCH2COOH O=C-CH2O-C=O + H2O OCH2
21
• n=2
HO(CH2)2COOH
CH2=CH-COOH+H2O
• n=3 HO(CH2)3COOH
CH2-C=O CH2-CH2-O + H2O
22
• n=4 HO(CH2)4COOH
CH2-CH2-C=O CH2-CH2-O + H2O
• n>=5,成链,形成线形聚合物。
23
• 成环倾向大小,主要取决于单体的结构, 受反应条件的影响较小。
• 环上取代基或环上元素改变时,环的稳定 性也相应变化。
• 在工业上:锦纶大量用来制造轮胎帘子 布、工业用布、缆绳、传送带、帐篷、 鱼网等,还可用作降落伞。
64
• 还可用于制造轴承、齿轮、滚子、 滑轮、辊轴、风扇叶片、涡轮、垫 片等。
65
全芳聚酰胺
• 是20世纪60年代由美国的杜邦公司首先开 发成功的。
13
自由基聚合
线型缩聚
③只有链增长才使聚 ③任何物种间都能反应, 合度增加,从一聚体 使分子量逐步增加。反应 增长到高聚物,时间 可以停留在中等聚合度阶 极短,中途不能暂停。段,只在聚合后期,才能 聚合一开始,就有高 获得高分子量产物。 聚物存在。
④在聚合过程中,单 ④聚合初期,单体几乎全
体逐渐减少,转化率 部缩聚成低聚物,以后再
(2—23式)
• 水部分排出时:
-dC/d t =k1 [ (1-P)2-P•nW/ K]
高分子化学第二章

3.3
聚合度与平衡常数的关系
O
COOH
+
HO
C
O
+ H2O
设t=0时 平衡时
N。 N
N。 N
0 (N。—N)
0 Nw
N —— 平衡时未反应的羧基或羟基数 N0–N —— 也是已反应的羟基或羧基的mol数即是平 衡时生成的酯基数; Nw —— 体系中H2O的mol数
K=
_ _ [ OCO ][H2O] _ _ [ COOH][ OH]
_ _ H [ORCO]n OH
该反应事实上包括 n-1 个反应,当然就存在 n-1个平 衡常数。
aRb+aRb aRRb+ab aRRb+ aRb aRRRa+ab aRRRb+ aRb bRRRRb+ab 单体+单体 单体+二聚体 单体+三聚体 二聚体+三聚体 反应速率R1 R2 R3 R4 Rn-1 平衡常数K1 K2 K3 K4 Kn-1
第二章
逐步聚合反应
(stepwise polymerization)
第一节
引言
逐步聚合: 是具有两个或两个以上官能团的低分之化合物 相互反应而逐步生成高分子化合物的反应。
研究意义:
1、大多数杂链聚合物都是靠这类聚合合成的。 如:聚碳酸酯 (聚2,2双[4,4′羟基苯基] 丙烷碳酸酯):
_ n HO CH3 _C _ CH3 O _ _ _ n Cl C Cl OH +
_
_
-H2O
+己二酸
HO [OC(CH2)4CONH(CH2)6NH] H
_
_
_ _ -H2O HO [OC(CH2)4CONH(CH2)6NH] OC(CH2)4COOH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高分子化学第二章逐步聚合反应
2.1 缩合反应与缩聚反应
O
酯 化
CH3C_ OH + H_OCH2CH3
反
O
应
CH3C_OCH2CH3 + H2O
酰 胺 化
O CH3C_OH + H_NHCH2CH3
反
O
应
CH3C_NHCH2CH3 + H2O
双官能团单体的多步缩合反应:
H O O C(CH 2)4CO_O H+H _N H (CH 2)6N H 2
3、单体通式 a–R–c
H2N(CH2) 5OH 仅参加前面二类型的均缩聚或混缩聚反应而不能单独进行 聚合,这叫共缩聚反应,产物叫做共缩聚物。
合成一种线型缩聚物一般可有多种聚合反应路线和相应的 单体,但是按照这些单体的合成难易、聚合反应的难易以 及聚合物相对分子质量的高低,通常只有一两种单体是最 符合条件的。
2 与官能团所处的空间环境有关 对苯二胺 + 对Biblioteka 二甲酰氯 反应活性较低H2N_
_NH 2+CO l C _ _COl C 全芳聚酰胺
间苯二胺 + 间苯二甲酰氯 反应活性较高
H2N_ _NH 2+CO l C _ _COl C 全 芳 聚 酰 胺
3 环化反应倾向大小 羟基酸的聚合-环化反应倾向与碳原子数
由带两个或两个以上官能团的单体之间连续、重复进行的缩 合反应称为缩合聚合反应,简称缩聚反应。
2.2 逐步聚合反应单体
2.2.1 线型缩聚反应单体的类型
1、单体通式 a–R–b
HO(CH2)5COOH
H2N(CH2) 5COOH
属于均缩聚反应,得到均缩聚物。
2、单体通式 a–R–a + b–R'–b HOOCC6H4COOH + HO(CH2) 2OH HOOC(CH2) 4COOH + H2N(CH2) 6NH2 属于混缩聚反应,得到混缩聚物。
mHOOC(CH2)nOH
HO_[OC(CH2)nO]m _H mOC(CH2)nO
结论 ◆ 5、6元环的张力是最小,最容易环化。 ◆ 7、12元环的张力中等,稍有环化倾向 ◆ 其余环张力均较大 ,不容易环化
因此:
凡是能够生成5、6元环的双官能团单体的环化反应占主导 地位,无法进行聚合!。
4-羟基丁酸 HO(CH2) 3COOH
如,合成涤纶(聚对苯二甲酸乙二醇酯)理论上有下列3 条合成路线可以选择,但是第3中路线才是工业化的。
① 对苯二甲酸与乙二醇进行混缩聚反应 n HOOCC6H4COOH + n HO(CH2) 2OH
= HO–[OCC6H4COO(CH2) 2O]n–H + (2n –1) H2O
②.对苯二甲酸二甲酯与乙二醇进行酯交换聚合反应 n CH3OOCC6H4COOCH3 +(n+1)HO(CH2) 2OH = HO (CH2) 2O–[OCC6H4COO(CH2) 2O]n–H+2n CH3OH
③ 对苯二甲酸双β羟乙酯进行分子间的酯交换聚合反应
n HO(CH2) 2OOCC6H4COO(CH2) 2OH= HO(CH2) 2O–[OCC6H4COO(CH2) 2O]n–H+(n –1) HO(CH2) 2OH
2.2.2 单体的聚合反应活性
单体缩聚反应活性规律 ◆ 遵守有机化合物相应缩合反应的活性规律 ◆ 与官能团所处的空间环境有关 ◆ 碳原子数与环化反应倾向大小
- H 2 O H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] _ H
+ - 己 H 二 2 O 酸 H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] _ O C ( C H 2 ) 4 C O O H
+ - 己 H 二 2 O 胺 H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] 2 _ H
+ - 己 H 2 二 O 酸 ? H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] 2 _ O C ( C H 2 ) 4 C O O H - + ( 2 二 n 酸 - 1 二 H 胺 2 O · ) H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] n _ H
1、官能团活性规律举例 酰卤活性 > 羧酸活性 > 酯活性 ClOCC6H4COCl > HOOCC6H4COOH > HO(CH2) 2OOCC6H4COO(CH2) 2OH 聚合反应的活性递减 –Cl > –OH > –O(CH2) 2OH,电负性递减
HCl > HOH > HO(CH2) 2OH ,酸性递减
5-羟基戊酸 4-氨基丁酸 5-氨基戊酸
HO(CH2) 4COOH H2N(CH2) 3COOH H2N(CH2) 4COOH
特别注意:含4、5个碳原子的氨基酸和羟基酸具有强烈的 环化倾向而不能聚合。
谢谢!
2.1 缩合反应与缩聚反应
O
酯 化
CH3C_ OH + H_OCH2CH3
反
O
应
CH3C_OCH2CH3 + H2O
酰 胺 化
O CH3C_OH + H_NHCH2CH3
反
O
应
CH3C_NHCH2CH3 + H2O
双官能团单体的多步缩合反应:
H O O C(CH 2)4CO_O H+H _N H (CH 2)6N H 2
3、单体通式 a–R–c
H2N(CH2) 5OH 仅参加前面二类型的均缩聚或混缩聚反应而不能单独进行 聚合,这叫共缩聚反应,产物叫做共缩聚物。
合成一种线型缩聚物一般可有多种聚合反应路线和相应的 单体,但是按照这些单体的合成难易、聚合反应的难易以 及聚合物相对分子质量的高低,通常只有一两种单体是最 符合条件的。
2 与官能团所处的空间环境有关 对苯二胺 + 对Biblioteka 二甲酰氯 反应活性较低H2N_
_NH 2+CO l C _ _COl C 全芳聚酰胺
间苯二胺 + 间苯二甲酰氯 反应活性较高
H2N_ _NH 2+CO l C _ _COl C 全 芳 聚 酰 胺
3 环化反应倾向大小 羟基酸的聚合-环化反应倾向与碳原子数
由带两个或两个以上官能团的单体之间连续、重复进行的缩 合反应称为缩合聚合反应,简称缩聚反应。
2.2 逐步聚合反应单体
2.2.1 线型缩聚反应单体的类型
1、单体通式 a–R–b
HO(CH2)5COOH
H2N(CH2) 5COOH
属于均缩聚反应,得到均缩聚物。
2、单体通式 a–R–a + b–R'–b HOOCC6H4COOH + HO(CH2) 2OH HOOC(CH2) 4COOH + H2N(CH2) 6NH2 属于混缩聚反应,得到混缩聚物。
mHOOC(CH2)nOH
HO_[OC(CH2)nO]m _H mOC(CH2)nO
结论 ◆ 5、6元环的张力是最小,最容易环化。 ◆ 7、12元环的张力中等,稍有环化倾向 ◆ 其余环张力均较大 ,不容易环化
因此:
凡是能够生成5、6元环的双官能团单体的环化反应占主导 地位,无法进行聚合!。
4-羟基丁酸 HO(CH2) 3COOH
如,合成涤纶(聚对苯二甲酸乙二醇酯)理论上有下列3 条合成路线可以选择,但是第3中路线才是工业化的。
① 对苯二甲酸与乙二醇进行混缩聚反应 n HOOCC6H4COOH + n HO(CH2) 2OH
= HO–[OCC6H4COO(CH2) 2O]n–H + (2n –1) H2O
②.对苯二甲酸二甲酯与乙二醇进行酯交换聚合反应 n CH3OOCC6H4COOCH3 +(n+1)HO(CH2) 2OH = HO (CH2) 2O–[OCC6H4COO(CH2) 2O]n–H+2n CH3OH
③ 对苯二甲酸双β羟乙酯进行分子间的酯交换聚合反应
n HO(CH2) 2OOCC6H4COO(CH2) 2OH= HO(CH2) 2O–[OCC6H4COO(CH2) 2O]n–H+(n –1) HO(CH2) 2OH
2.2.2 单体的聚合反应活性
单体缩聚反应活性规律 ◆ 遵守有机化合物相应缩合反应的活性规律 ◆ 与官能团所处的空间环境有关 ◆ 碳原子数与环化反应倾向大小
- H 2 O H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] _ H
+ - 己 H 二 2 O 酸 H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] _ O C ( C H 2 ) 4 C O O H
+ - 己 H 二 2 O 胺 H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] 2 _ H
+ - 己 H 2 二 O 酸 ? H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] 2 _ O C ( C H 2 ) 4 C O O H - + ( 2 二 n 酸 - 1 二 H 胺 2 O · ) H O _ [ O C ( C H 2 ) 4 C O N H ( C H 2 ) 6 N H ] n _ H
1、官能团活性规律举例 酰卤活性 > 羧酸活性 > 酯活性 ClOCC6H4COCl > HOOCC6H4COOH > HO(CH2) 2OOCC6H4COO(CH2) 2OH 聚合反应的活性递减 –Cl > –OH > –O(CH2) 2OH,电负性递减
HCl > HOH > HO(CH2) 2OH ,酸性递减
5-羟基戊酸 4-氨基丁酸 5-氨基戊酸
HO(CH2) 4COOH H2N(CH2) 3COOH H2N(CH2) 4COOH
特别注意:含4、5个碳原子的氨基酸和羟基酸具有强烈的 环化倾向而不能聚合。
谢谢!
