影响化学位移的因素共20页文档
仪器分析-影响化学位移的因素-2

主讲教师:胡高飞 7.4 影响化学位移的因素(2)三、氢键对δ的影响Hydrogen Bonding Deshields Protons分子形成氢键后,氢核周围的电子云密度降低,产生去屏蔽效应,化学位移移向低场, δ增大。
分子内氢键:O O O HC H 3•在水杨酸甲酯中,由于强的分子内氢键作用,NMR 吸收信号中 O-H 约为 14 ppm ,处于非常低场。
•注意形成了一个新的六元环分子间氢键:化学位移取决于形成了多少氢键 醇的化学位移可以在0.5 ppm (自由OH )至约5.0ppm (形成大量氢键)间变化氢键拉长了O-H 化学键并 降低了质子周围的价电子密度 - 去屏蔽效应导致NMR 谱中化学位移移向低场OH R O R H HO R(a)10kg/L ,(b) 5kg/L ,(c) 0.5kg/L ,乙醇溶剂CCl4,T =40℃OCO R H H C O O R •羧酸具有强的氢键 – 形成了二聚体 •对于羧酸 O-H 吸收在NMR 谱中化学位移位于10 ~ 12 ppm ,一般处于最低场四、H核交换对δ的影响化合物的质子分为可交换氢和不可交换氢与 N、O、S等原子连接的氢称为可交换氢,又称活泼氢与C、Si、P等原子连接的氢称为不可交换氢CH3COOH a+H b OH b CH3COOH b+H a OH bδ观察=N aδa+N bδbN-摩尔分数δa、δb-分别为H a与H b纯品的化学位移值四、H核交换对δ的影响活泼氢:R-OH δ=0.5-5.5Ar-OH δ=4.0-7.7RCOOH δ=10.0-13.0R-NH2δ=5.0-8.0Ar-NH2δ=3.5-6.0R-CO-NH2δ=5.0-8.5R-SH δ=1.0-2.0Ar-SH δ=2.8-3.6五、溶剂对δ的影响采用不同的溶剂,化学位移也会发生变化,强极性溶剂的作用更加明显。
溶质与溶剂间相互作用(如形成氢键)。
影响化学位移的因素
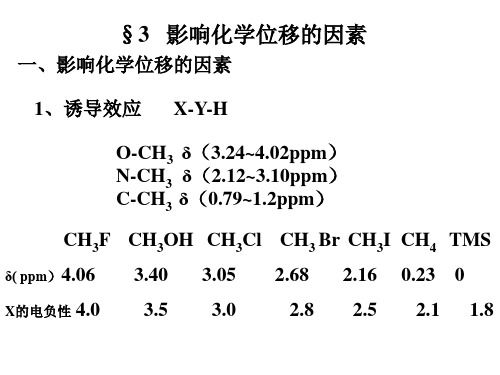
X的电负性 4.0 3.5 3.0
2.8 2.5 2.1 1.8
2、共轭效应 CH3 O
CH3 O
δ-
δδ-
CH3
O
δ 6.84 ppm
δ 7.18 ppm δ 6.90 ppm
δ 7.27ppm
NO2
NO2 δ+ δ+
δ+
NO2 δ 8.21ppm
δ 7.45ppm δ 7.66ppm
4.74
5、溶剂效应
O C
..
N
CH3β
H
CH3α
O C
H
N+ CH3 β CH3α
O C
H
+ CH3β N
CH3 α
从(a)到(d)苯逐渐加入DMF的氯仿溶液中
6、交换反应 (1)、位置交换
同类分子间的交换: R1OHa + R2OHb = R1OHb + R2OHa
溶质与溶剂之间的质子交换: ROHa + HOHb = ROHb + HOHa
1.1~1.2
RNH2,R2NH
0.4~ 3.5
ArNH2,Ar2NH
2.9~4.8
RCONH2,ArCONH2 5~ 6.5
RCONHR,ArCONHR 6~8.2
RCONHAr
7.8 ~9.4
ArCONHAr
7.8 ~9.4
H H
C=C
OCOCH3 H
H
H
C=C
H H
4.31
7.18
5.25
6.38
H C=C COOCH3
H
H
5.82
6.20
3、化学键的各向异性 A、三键的各向异性效应
程鹏-1H 化学位移及其影响

国际关系学院
程鹏
(一)1H-NMR的化学位移 NMR的
化学位移(Chemical 化学位移(Chemical shift) ——由于化学环境 ——由于化学环境 不同所引起的NMR信号位置的变化。 不同所引起的NMR信号位置的变化。 化学位移常用δ表示。 化学位移常用δ表示。 δ取决于氢原子周围的电子云密度,而电子 云密度是由核所处的结构环境决定的。因此 分子中的氢的化学位移是确定分子结构的重 分子中的氢的化学位移是确定分子结构的重 要线索。 要线索。
产生以上现象的原因:
芳环
H0
H0
C H C C
C C C H
C H CC
+
C
-C H
C
+
H感
双键( 双键(C=C、C=O):
三键: 三键:
• 炔烃三键上的π电子云围绕三键运行,形成π电子的环电子 炔烃三键上的π电子云围绕三键运行,形成π 流,因此生成的磁场与三键之间两个氢核平行,正好与外 加磁场相对抗,故其屏蔽作用较强。(三)化学位移的表示方法
• (1)位移的标准 位移的标准 • 没有完全裸露的氢核,没有绝对的标准。 • 相对标准:四甲基硅烷 Si(CH3)4 (TMS)(内标) • 位移常数 δTMS=0
• (2) 为什么用 为什么用TMS作为基准 作为基准? 作为基准 • a. 12个氢处于完全相同的化学环境,只产生一个尖峰; • b.屏蔽强烈,位移最大。与有机化合物中的质子峰不重叠; • c.化学惰性;易溶于有机溶剂;沸点低,易回收。
• 为什么乙酸苄酯中三个基团的氢产生不同的NMR峰呢? 为什么乙酸苄酯中三个基团的氢产生不同的NMR峰呢? 乙酸苄酯中三个基团的氢产生不同的NMR峰呢 • 分子结构是怎样影响NMR信号的位置? 分子结构是怎样影响NMR信号的位置? NMR信号的位置
影响化学位移的因素

影响化学位移的因素
1.温度:温度是一个重要的因素,它影响了反应速率和化学位移。
温
度的升高可以增加反应速率,并促使化学位移发生。
2.压力:压力也可以影响化学反应的速率和化学位移。
增加压力可以
促使反应向高位移的方向进行,而减少压力则使反应朝低位移的方向进行。
3.浓度:反应物的浓度可能会影响反应速率和化学位移。
增加反应物
的浓度可以加快反应速率,并可能导致更高的化学位移。
4.催化剂:催化剂是一种可以增加反应速率而不参与反应的物质。
催
化剂可以通过改变反应的路径或减少反应物之间的能量差异来影响化学位移。
5.光照:光照可以引起许多化学反应,并且可以改变化学位移。
一些
反应在光照下会更快或更慢发生,并且可能会导致不同的化学位移。
6.物理性质:物理性质,例如溶剂的性质、溶液的颜色、密度等的改变,可以影响化学反应和化学位移。
7.原子结构:原子结构可以通过原子间的连接和键长来确定反应的进
行和化学位移的方向。
8.核外电子:化学位移可以受到核外电子的影响。
核外电子的数量和
运动方式可能会改变反应速率和化学位移。
此外,还有其他一些因素可以影响化学位移,例如反应物的尺寸、表
面积、电场和磁场等。
化学位移是一个复杂的过程,需要综合考虑多种因
素来理解。
无论哪个因素,都可以对化学位移产生重要的影响,并决定反
应的进行和观察到的化学变化。
核磁共振氢谱(化学位移)

精选课件
3
化学位移的产生
•核外电子的影响,屏蔽效应,化学位移
修正的核磁共振条件
:
h
h
2
B0(1
)
1
2
B0(1
)
核外电子在外加磁场作用下产生电子环
流,电子环流产生相应的感应磁场,感
应磁场的方向与原外加磁场的方向相反
,磁场强度等于σB0,此时原子核实际 受到的磁场强度小于原外加磁场强度B0 ,这种核外电子对原子核的影响称为屏
核磁共振氢谱(1H-NMR)
——化学位移(chemical shifts)
Produced by Jiwu Wen
精选课件
1
内容提要
化学位移的产生 化学位移的表示方法与测定 影响化学位移的因素 不同质子的化学位移
精选课件
2
化学位移的产生
•核磁共振条件及面临的问题
1. 核磁共振的条件小结:
(1)自旋核(I≠0)
蔽效应,σ称为屏蔽常数。
由于屏蔽效应不同导致化学环境不同的 原子核共振频率不同,因而在不同的位 置上出现吸收峰,这种现象称为化学位 移。
精选课件
4
化学位移的表示方法与测定
•高场与低场的区分
•化学位移的表示方法——位移常数
•测定和计算方法——标准物质(通常用TMS,即四甲基 硅)对照法:
样品TMS 106 仪器
精选课件
6
化学位移的表示方法与测定
2.05 3.66
精选课件
7
影响化学位移的因素
1. 诱导效应:吸电子诱导效应降低原子核周围的电子云 密度,化学位移向低场移动,增大。
CH3X中甲基和各种取代基连接后的化学位移
-X
三核磁共振氢谱2化学位移
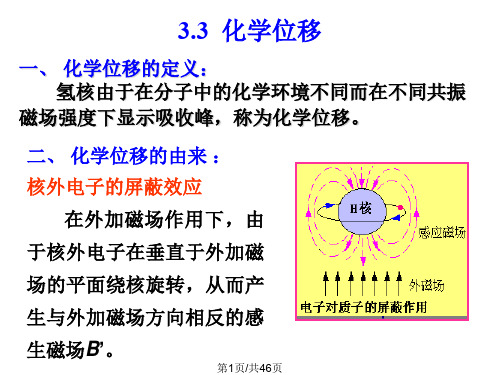
一、 化学位移的定义: 氢核由于在分子中的化学环境不同而在不同共振
磁场强度下显示吸收峰,称为化学位移。
二、 化学位移的由来 :
核外电子的屏蔽效应
在外加磁场作用下,由
于核外电子在垂直于外加磁
Байду номын сангаас
场的平面绕核旋转,从而产
生与外加磁场方向相反的感
生磁场B’。
第1页/共46页
H核的实际感受到的磁场强度为:
第14页/共46页
化合物 δ
CH4 0.23
CH3Cl CH2Cl2 CHCl3
3.05
5.33
7.27
化合物 电负性
δ
C-CH3 C: 2.5 0.7~1.9
N-CH3 N: 3.0 2.1~3.1
O-CH3 O: 3.5 3.2~4.2
第15页/共46页
CH3—CH2—CH2—X
γ βα
0.93 1.53 3.49 —OH 1.06 1.81 3.47 —Cl
Beff = B0 -σ·B0 = Bo(1-σ)
σ 为屏蔽常数
核的共振频率为:
=
2
·B0(1-σ)
• 核外电子云密度高,屏蔽作用大(σ 值大),核的 共振吸收向高场(或低频)移动,化学位移减小。
• 核外电子云密度低,屏蔽作用小(σ 值小) ,核的 共振吸收向低场(或高频)移动,化学位移增大。
增强,δ值向低场移动。
第17页/共46页
H
OH
C=O
H
7.27
H
6.73
H
7.81
5.25
H
H
C=C
H
H
4.03
H
影响化学位移的因素
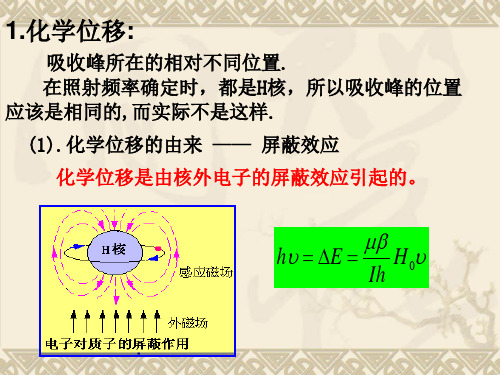
1.化学位移:吸收峰所在的相对不同位置.在照射频率确定时,都是H 核,所以吸收峰的位置应该是相同的,而实际不是这样.(1).化学位移的由来——屏蔽效应化学位移是由核外电子的屏蔽效应引起的。
υμβυ0H IhE h =∆=H 核在分子中是被价电子所包围的。
因此,在外加磁场的同时,还有核外电子绕核旋转产生感应磁场H ’。
如果感应磁场与外加磁场方向相反,则H 核的实际感受到的磁场强度为:)1('H 0000σσ-=-=-=H H H H H 实式中:σ为屏蔽常数核外电子对H 核产生的这种作用,称为屏蔽效应(如果产生磁场与外加磁场同向,称之为去屏蔽效应)。
显然,核外电子云密度越大,屏蔽效应越强,要发生共振吸收就势必增加外加磁场强度,共振信号将移向高场区;,共振信号将移向低场区。
H0低场高场屏蔽效应,共振信号移向高场屏蔽效应,共振信号移向低场去(2).化学位移的表示方法化学位移的差别约为百万分之十,精确测量十分困难,现采用相对数值。
以四甲基硅(TMS )为标准物质,规定:它的化学位移为零,然后,根据其它吸收峰与零点的相对距离来确定它们的化学位移值。
6010⨯-=νννTMS 试样化学位移试样的共振频率标准物质TMS 的共振频率感生磁场H'非常小,只有外加磁场的百万分之几,为方便起见,故×106仪器频率为什么选用TMS (四甲基硅烷)作为标准物质?(1)屏蔽效应强,共振信号在高场区(δ值规定为0),绝大多数吸收峰均出现在它的左边。
(2)结构对称,是一个单峰。
(3)容易回收(b.p 低),与样品不反应、不缔合。
SiCH 3CH 3H 3C CH 3分子结构因素(质子的化学环境)外部因素(测试条件)影响化学位移的因素诱导效应共轭效应化学键各向异性效应范德华效应分子内氢键效应溶剂效应分子间氢键效应影响化学位移的因素:(3).影响化学位移(电子云密度)的因素:1.取代基电负性:元素的电负性↑,通过诱导效应,使H核的核外电子云密度↓,屏蔽效应↓,共振信号→低场。
第三章:1H-NMR-2

核相连的原子或基团的电负性大小将影响其电子云密度。
HN=H0(1-σ)
3 影响化学位移的因素
由于诱导效应,取代基电负性越强,与取代基连接在同一碳原子上氢 核外围电子云密度越低,共振峰移向低场,化学位移增大;
X X的电负性 F 4.0 OCH3 3.5 Cl 3.1 Br 2.8 NH2 3.0 CH3 2.5 H 2.1 SiMe3 1.9 Li 0.98
RCOOHa HOHb
RCOOHb HOHa
obs na a nbb
δ obs: 观察到的化学位移;na和nb为Ha和Hb的摩尔数
3. 影响化学位移的因素
11.6 5.2
δ obs = nδ a a + nδ b b
增加温度或有酸碱存在,均可加快交换反应速度。 一般说来,交换速率-OH>-NH>-SH。- SH通常能 保持自己的化学环境,具有独立的共振信号。
3. 影响化学位移的因素
β α 0.55 -0.77
3. 影响化学位移的因素
b. 芳环的磁各向异性
+
+
苯环上的6个电子产生较强的诱导磁场,质子位 于其磁力线上,与外磁场方向一致,去屏蔽。
δ : (6.0~9.0)
3. 影响化学位移的因素
9.28 H H H H H H
H H
H H-2.9 H H H H H H
1.80
H C C H
1.73-1.88
H C C R
2.71-3.37
H C C Ar
2.23
H C C CO2H
环丙烷<CH3 <CH2 <CH。
• 但当与氢相连的碳上同时连有强吸电子原子,如氧、 氯、氮等,或者邻位有各向异性基团,如双键、羰 基、苯基等时,它们的化学位移值会大幅度增加, 往往超出此范围。
知识点6-影响化学位移的因素

Aromatic Hydrogens
Aromatic hydrogens resonate between 7 - 8 ppm.
Aldehyde Hydrogens
Aldehyde protons resonate between 9 - 10 ppm. This further downfield shift is due to the additional effect of the electron withdrawing oxygen atom nearby.
氢键效应
无论是分子内还是分子间氢键的形成都使氢受到去 屏蔽作用,羧基形成强的氢键,因此其δ值一般都 超过10ppm。 甲醇的化学位移值与温度的关系: -54C -10C 15C ~ 4.8 ppm ~ 3.8 ppm ~ 2.8 ppm
温度升高,氢键减弱,化学位移值减小。
v
Chemically equivalent protons in ethyl acetate.
2.Integration
The NMR spectrometer can integrate all peaks (determine the area under each peak) to determine the relative numbers of protons responsible for all peaks.
sp Hydrogens
Acetylenic hydrogens resonate between 2 - 3 ppm due to the anisotropy of the carboncarbon triple bond.
Hydrogen Bonding Effects
化学位移

4.2.1 1H 的化学位移
1.影响化学位移的因素 2. 各类1H的化学位移
1.影响化学位移的因素
(1)电子效应 • 诱导效应
化学位移随着相邻电负性基团的电负性的增大而增大
X
X的电负 性
F OCH3 Cl 4.0 3.5 3.1
a )沿环单键的互变
环己烷:-89℃测定:Ha与Hb显示两个峰 常温下测定:显示一个峰
温度低于-89oC时,正己烷构象 固定,2-3键和5-6键的作用使Ha 处于屏蔽区,而Hb处于去屏蔽区
。 Hb - Ha ≈ 0.5ppm
甲基环己烷:室温下以直立和平伏质子的形式存在, 这些构象是不可重合的,低温下,一张谱图包含了这 两种形式。
4.2 核磁共振氢谱(1H NMR)
—发展最早,研究得最多,应用最为广泛。 —质子的旋磁比 较大,天然丰度接近100%,核磁共振
测定的绝对灵敏度最大; —1H是有机化合物中最常见的同位素,1H NMR谱是有机物
结构解析中最有用的核磁共振谱之一。
CH3CH2CONH2
低场
高场
• 化学位移值,代表谱峰位置—化学环境
CH3 CH3 H C O C Hb
CH3 CH3 a
HH I C C Cl
HH ab
CH3CH2CH2I a bc
a<b
a<b
a<b<c
• 下面化合物中所标出的质子其1H NMR化学位移从低场
到高C O CH2CH3
ab
cd
c 、 b 、d 、a
•共轭效应
(2) 相连碳原子的杂化态影响
化学位移

4. 3
4.3.1 4.3.2 4.3.3 4.3.4
化学位移
chemical shift
屏蔽效应 化学位移及其表示方法 影响化学位移的因素 各类H核的化学位移
4.3.1
屏蔽效应
(shielding effect)
对于理想化的、裸露的氢核,
实现核磁共振的条件:
0 = B0 / (2 )
实际上,氢核受外围不断运动着的电子影响。 在外磁场作用下,运动着的电子产生与外磁场相对 抗的感生磁场( B0),对H核起到屏蔽作用,使氢 核实际受到的外磁场作用减小。
二. 共轭效应
在共轭效应中,推电子基和吸电子基的影响各 不相同。 推电子基—— p -π共轭——电子云密度 ——δ 。 吸电子基——π-π共 轭——电子云密度 ——δ 。
三. 磁各向异性效应(magnetic anisotropic effect)
实验表明: CH2=CH2 CH=CH CH3-CH3
当用固定频率的射频照射时,不同H核共振所 需要的外磁场强度B0也不相同。 因此,不同化学环境的 H 核的共振峰将出现 在 NMR 谱图上的不同磁场强度的位置。 例如,CH3-CH2-Cl 中,两种不同环境的H核 将不同场强处产生共振吸收峰。
由此可得出以下结论:
如果H核外围的电子云密度减小,则其屏蔽效
剂效应。 通常,溶剂的极性、磁化率、磁各向异性等性质,都 会对溶质H核产生一定的影响,使其δ变化。 氘代溶剂不含H核,不会干扰样品H核的谱图。 常用氘代溶剂: O O
七.
溶剂效应
D2O 、 CDCl3 、 CD3-C-CD3 、 CD3-S-CD3 ....等。
试解释酚羟基在氯仿中时,δ =7.3ppm,
的化学位移值相等。
影响化学位移的因素.

2、烯烃的化学位移 5~6.5ppm 5~6.5ppm δ=5.25 + Z同 + Z顺 + Z反
Ar H2 C=C
H1 COOH
δ1=5.25+0.97+0.36+0=6.58 ppm (实测值 6.46ppm ) δ2=5.25+1.36+1. 41+0=8.02 ppm (实测值 7.83ppm )
B0
含双键的基团如碳碳双键、羰基、碳氮双 键、碳硫双键等都有同样的效应
C、芳环的各向异性效应
D、单键的各向异性效应
H 3 5 4 2 6 1 H
4、氢键的影响
X-H· · · · · · Y
12.3 ppm 12.40 ppm
H O O
H
O
O OH 9.52 ppm
O
OCH3
H3CO
O
OH 9.30 ppm OCH3
5、溶剂效应
O H C
.. N
CH3β CH3α
O H
C
N
+
CH3β CH3 α
O H
C
N
+
CH3 β CH3α
从(a)到(d)苯逐渐加入DMF的氯仿溶液中
6、交换反应 (1)、位置交换 同类分子间的交换: R1OHa + R2OHb = R1OHb + R2OHa
溶质与溶剂之间的质子交换:
ROHa + HOHb = ROHb + HOHa ROH + DOD = ROD + HOD (δH ∽5.0ppm)
4、稠环及杂环质子的化学位移
H 7.46 H N H 6.30 7.06 O H 7.40 S H 7.19 H 7.04
核磁共振氢谱(1H NMR)
第二十二页,共53页。
c)围绕部分双键(受阻旋转)的互变 DMF:
第二十三页,共53页。
• 活泼氢的快速交换反应
分子中的-OH、-NH2、-SH和-COOH等活泼氢可在分子间进行快速交
换。
因此, 酸3
第四页,共53页。
-CH3 ,δ = 1.8,出现在高场 -CH2I,δ= 3.1, 出现在低场
第五页,共53页。
第六页,共53页。
• 判断下列化合物中Ha,Hb化学位移的大小
CH3 CH3 HC OC Hb
CH3 CH3 a
HH I C C Cl
HH ab
CH3CH2CH2I a bc
➢ 邻氯苯酚形成微弱的氢键δ 5.6~6.5,位移范围较宽,但
较苯酚的窄。
第四十二页,共53页。
d) 烯醇
➢ 普通酮类化合物,烯醇含量极少,呈现酮的吸收峰。 ➢ 乙酰丙酮,存在稳定的烯醇式,且室温下酮式和烯醇式
交换缓慢,观察到两种形式的NMR特征。 ➢ 2,3-丁二酮在谱图上只观察到酮式结构。但如下所示环状
➢ 巯基质子和烯醇质子并不与羧酸质子发生交换而观察到 各自的吸收峰。
第四十四页,共53页。
f) 氮原子上的质子
氮原子上质子的交换速率和14N核的电四极矩使谱图复杂。
➢ 交换快速时,NH表现为尖锐单峰,相邻CH上质子不被NH裂分
。大多数脂肪族胺属此种情况。δ= 0.5 ~ 3.0 ➢ 中等交换速率时,NH部分去耦表现为一个宽峰,但相邻CH上质
α-二酮只有稳定的烯醇式出现在NMR谱中。
第四十三页,共53页。
e) 羧酸
影响化学位移的因素
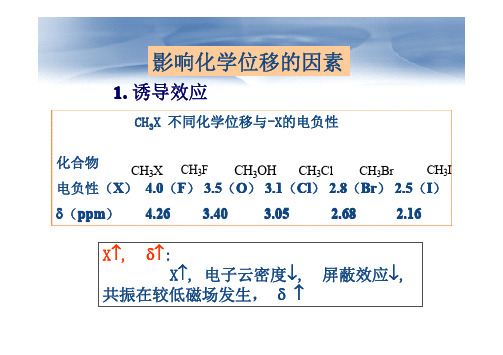
影响化学位移的因素1. 诱导效应X 不同化学位移与-X的电负性CH3化合物CH3X CH3F CH3OH CH3Cl CH3Br CH3I 电负性(X) 4.0(F) 3.5(O) 3.1(Cl) 2.8(Br) 2.5(I)δ(ppm) 4.26 3.40 3.05 2.68 2.16 X↑, δ↑:X↑, 电子云密度↓, 屏蔽效应↓,共振在较低磁场发生, δ↑拉电子基团越多, 这种影响越大CH2Cl HCHCl2HCCl3H δ=3.05δ=5.30δ=7.27基团距离越远,受到的影响越小CH 2CH 3CH 2Br 1.25 1.69 3.30αβγδ2. 各向异性(1) 芳环的各向异性δ 7.3感应磁场: 与外磁场方向在环内相反(抗磁的),在环外相同(顺磁的)对环吩(2) 双键化合物的各向异性乙烷质子 0.96乙烯质子 5.841) 烯碳sp2杂化, C-H键电子更靠近碳,对质子的屏蔽↓*2) 产生感应磁场,质子恰好在去屏蔽区(3) 三键化合物的各向异性1)炔碳为sp杂化,相对sp2和sp3杂化的C-H键电子更靠近碳,使质子周围的电子云密度减少,质子共振吸收向低场移动* 2)炔碳质子处在屏蔽区,炔氢共振应出现在较高的磁场强度区炔质子的化学位移值为2.883. 氢键的影响氢键的形成可以削弱对氢键质子的屏蔽,使共振吸收移向低场醇羟基 0.5~5酚 4~7胺 0.5~5羧酸 10~13二聚体形式(双分子的氢键)分子内氢键同样可以影响质子的共振吸收β-二酮的烯醇式可以形成分子内氢键该羟基质子的化学位移δ为11~164.3.3 化学等价与磁等价1. 化学等价化学等价又称为化学位移等价。
若分子中两个相同原子(或基团)处于相同的化学环境时,则称它们是化学等价的一般说来,若两个相同基团可通过二次旋转轴互换,则它们无论在何种溶剂中均是化学等价的。
若两个相同基团是通过对称面互换的。
则它们在非手性溶剂中是化学等价的,而在手性溶剂中则不是化学等价的。
氢谱中影响化学位移的因素
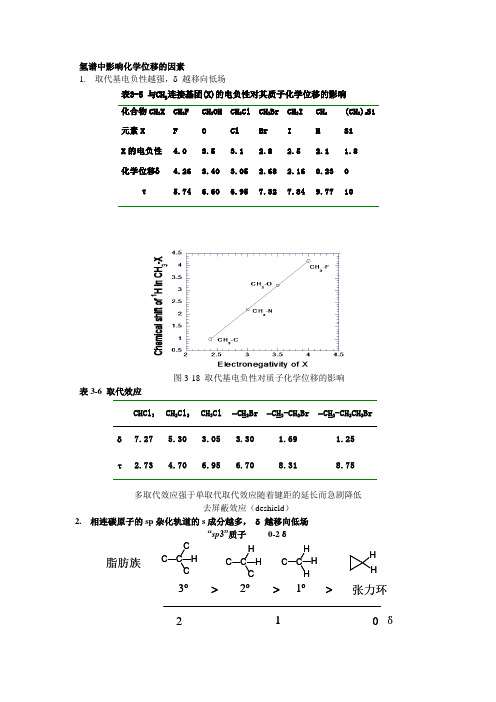
氢谱中影响化学位移的因素1. 取代基电负性越强,δ越移向低场表3-5 与CH3连接基团(X)的电负性对其质子化学位移的影响化合物CH3X CH3F CH3OH CH3Cl CH3Br CH3I CH4(CH3)4Si 元素X F O Cl Br I H SiX的电负性 4.0 3.5 3.1 2.8 2.5 2.1 1.8化学位移δ 4.26 3.40 3.05 2.68 2.16 0.23 0τ 5.74 6.60 6.95 7.32 7.84 9.77 10图3-18 取代基电负性对质子化学位移的影响表3-6 取代效应CHCl3CH2Cl2CH3Cl -CH2Br -CH2-CH2Br -CH2-CH2CH2Br δ7.27 5.30 3.05 3.30 1.69 1.25τ 2.73 4.70 6.95 6.70 8.31 8.75多取代效应强于单取代取代效应随着键距的延长而急剧降低去屏蔽效应(deshield)2. 相连碳原子的sp杂化轨道的s成分越多,δ越移向低场“sp3”质子0-2δ321C CCCH C CHCH C CHHHHH0 δ12脂肪族o o o张力环>>>“sp 2”质子 4.5-7δ“sp ”质子 2-3δ3. 酸性质子 10-12δR C OO HRC OO H作用和O 电负性拉电子效应的双重影响氢键的影响和可交换质子 能够形成氢键的质子(-OH ,-NH2)化学位移可变表3-7 可变化学位移的质子Acids RCOOH 10.5-12.0δ Phenols ArOH 4.0-7.0 Alcohols ROH 0.5-5.0 Amines RNH 2 0.5-5.0 Amides RCONH 2 5.0-8.0 EnolsCH=CH-OH≥15形成氢键的数目越多,质子的去屏蔽效应越强 氢键数目通常是浓度和温度的函数R OOHO R O H δδδ游离羟基(稀溶液)0.5-1.0δ 形成氢键(浓溶液)4-5δ可交换质子(活泼氢)H H R O H a+R'O H b R O H b+R'O H aR O +R O H+H SOLVSOLVR O +SOLV SOLVR O+3. 共轭效应sp 2-1s C-H 键,C 原子具有更多的s 特征,s 轨道的吸电子能力大于p 轨道C H 4.03C H H OCH 33.886.27C C HHC HO CH 35.90OH H6.73C HO H7.81p-π共轭,邻位H 的电子密度增加(正屏蔽),δ值减少π-π共轭,邻位H 的电子密度减少(去屏蔽),δ值增加CH 2H 2CH 2C H 2C H 2CH 2CCH 2CH 2CH 2H 2C2.631.551.080.700.515. 相邻基团电偶极矩和范德华力的影响 当分子内有强极性基团时,它在分子内产生电场,影响分子内其余部分的电子云密度,从而影响其它核的屏蔽常数。
