第二章分子识别元件及其反应基础
蛋白质结构与功能——受体

• α亚基具有GTP酶活性,能催化所结合的GTP水解, 恢复无活性的三聚体状态
G蛋白偶联系统的组成:膜结合机器
效应物 蛋 白 分 子 开 关
G
G蛋白循环(G protein cycle)
磷脂酶C-β催化PIP2水解生成DAG和IP3
处于静息状态的磷脂肌醇信号转导系统
IP3和DG的作用
用于PIP2再合成
胞质溶胶中IP3的命运
Ca2+信号的消除
蛋白激酶C激活特定基因转录的两种途径
肝细胞中两个第二信使 的协同作用,促进糖原 分解并抑制糖原合成
某些激活磷脂酶C的信号分子
信号分子 肾上腺素 加压素 PDGF 乙酰胆碱 凝血酶
phosphodiesterase)。
cAMP途径的信号解除方式
• 通过cAMP磷酸二酯酶(cAMP phosphodiesterase,PDE)将cAMP的环破坏,形成 5’-AMP。
• 通过抑制型的信号作用于Ri,然后通过Gi起作用。
• 在某些细胞中,G蛋白不仅可激活其效应物酶的 活性,也可抑制其活性。因此,G蛋白偶联系统
• 离子通道偶联型受体又可分为阳离子通道,如乙酰胆碱、谷氨酸和五羟色胺 的受体以及阴离子通道,如甘氨酸和γ-氨基丁酸的受体
乙酰胆碱受体结构模型
乙酰胆碱受体的三种构象
神经肌肉接点处的离子通道型受体
γ- 氨基丁酸(GABA)受体结构
离
①动作电位到达突触末 端,引起暂时性的去极
子 化;②去极化作用打开
G蛋白偶联受体信号转导系统的特点
• 系统由三个部分组成:7次跨膜的受体、G蛋白和 效应物(酶)
生物信号检测及传感器第一节

第二章 传感器生物材料
第一节 分子识别元件及其生物 反应基础
一、分子识别元件
• 生物传感器的分子识别元件又称敏感元件,主要指来 源于生物体的生物活性物质(包括酶、抗原、抗体和 各种功能蛋白质、核酸、微生物细胞、细胞器、动植 物组织)、生物衍生材料以及或生物模拟材料等.
• 生物传感器的分子识别元件的生物反应原理:
• 酶能够区分对称分子中等价的潜手性基团。
3.反应条件温和
• 酶促反应一般在pH 5-8 水溶液中进行,反应温度范围 为20-40C。
• 高温或其它苛刻的物理或化学条件,将引起酶的失活。
4.酶活力可调节控制
• 如抑制剂调节、共价修饰调节、反馈调节、酶原激活 及激素控制等。
5.某些酶催化活力与辅酶、辅基及金属离 子有关。
缺点: 标准难建立,反应途径繁多, 易受环境干扰
不同点:
•微生物细胞的膜系统为酶反 应提供了天然的适宜环境
•在多底物反应时,微生物更适 宜
•细胞本身能提供所需的各种 辅助因子和能量
•更方便,更廉价
(二)微生物反应类型
1、根据细菌的营养类型分类
自养菌
以简单的无机物为原 料,合成菌体成分
以多种有机物为原料, 合成菌体成分并获能 量
化酶) OH
O
OH邻苯二酚氧化酶
O
2
+ O2
2
+ 2H2O
邻苯二酚
邻苯醌
葡萄糖氧化酶
(2)脱氢酶类:直接催化底物脱氢
A·2H + B
A + B·2H
例:乳酸脱氢酶(EC 1.1.1.27,L-乳酸:NAD+氧化还原酶)
COOH
COOH
有机化学中的分子识别与生物传感

有机化学中的分子识别与生物传感在有机化学领域,分子识别和生物传感是两个关键领域,它们在药物研发、生物医学、材料科学等众多领域中发挥着重要作用。
本文将深入探讨有机化学中的分子识别和生物传感,介绍其原理、应用和前景。
一、分子识别的原理分子识别是指分子之间通过非共价相互作用,如氢键、范德华力、离子键等,特异性地识别和结合的过程。
这一过程在生物体内广泛存在,例如,酶与底物的特异性结合就是通过分子识别实现的。
在有机化学中,分子识别通常涉及配体和受体之间的相互作用。
分子识别的原理可以总结如下:1. 氢键:氢键是分子识别中常见的非共价相互作用,通常涉及氢原子与氮、氧或氟原子之间的相互作用。
2. 范德华力:范德华力是分子之间的瞬时相互作用力,它们可以导致分子的短时吸引和排斥。
3. 离子键:离子键是由正电荷和负电荷之间的相互作用引发的,通常涉及阳离子和阴离子之间的吸引。
4. 疏水作用:疏水作用是疏水性分子在水中聚集的趋势,通过排斥水分子来实现特异性结合。
二、分子识别在生物传感中的应用分子识别在生物传感领域具有广泛的应用,其中包括但不限于以下方面:1. 药物开发:药物设计中的分子识别是关键步骤,研究人员通过设计特异性配体,以实现对靶分子的选择性识别和结合,从而开发出更有效的药物。
2. 生物传感器:生物传感器是用于检测生物分子的装置,通过利用分子识别原理,可以实现对生物分子的高灵敏检测,用于医学诊断、环境监测等领域。
3. 分子探测器:在化学分析中,分子识别可用于检测和测定目标分子的存在和浓度,如气相色谱和液相色谱等技术。
4. 生物催化:酶作为生物催化剂,通过分子识别实现对底物的特异性识别和催化,广泛应用于生物合成和工业生产。
三、生物传感的原理生物传感是一种利用生物分子与分子识别原理相结合的技术,用于检测目标分子的存在、浓度或活性。
生物传感的原理包括以下几个方面:1. 生物元件:生物传感器通常包括生物元件,如酶、抗体、DNA 等,这些生物元件能够与目标分子特异性结合。
分子机器分类及其工作原理

分子机器分类及其工作原理
分子机器是一种超分子结构,它利用分子之间的相互作用和能量转化,以执行特定任务。
按照结构和功能的差异,分子机器可以分成多种类型,例如分子齿轮、分子轮船、分子电梯等。
分子机器的工作原理主要基于分子识别和能量转换。
首先,每种类型的分子机器都有特定的识别元件,可以识别外界的特定信号,比如光、电、化学物质等。
当这些信号与识别元件结合时,会引发一系列的化学反应,改变分子机器的结构和状态。
这些变化会进一步传递和放大,最终导致分子机器的运动和行为。
以分子齿轮为例,其工作原理如下:当特定的外界信号与识别元件结合后,会引起分子齿轮的构型改变,使得分子齿轮的“齿”与另一个分子齿轮的“齿槽”结合或分离,从而驱动齿轮的运动。
这种运动可以是旋转、平移等,取决于具体的分子结构和相互作用。
再比如分子轮船,它由多个分子机器组成,如发动机、转向器和推进器等。
当发动机识别到特定的化学物质后,会引发一系列的化学反应,改变发动机的旋转速度和方向。
转向器则会根据发动机的旋转方向和速度,调整轮船的前进方向。
推进器则会根据发动机的旋转速度,调整轮船的前进速度。
以上就是分子机器分类及其工作原理的基本概述。
虽然目前的技术还无法制造出宏观意义上的机器,但随着科技的不断进步,未来有望利用这些原理创造出更加高效和微型化的机器设备。
第二章 药物设计的基本原理和方法

O 青蒿素
H H CH3 OCOCH2CH2COOH 青蒿琥酯
2.微生物来源
美伐他汀和洛伐他汀,来源于青霉菌属、红
曲霉菌和土曲霉菌,羟甲戊二酰辅酶A还原
酶抑制剂的Lead Compound。后开发了人工合 成的阿托伐他汀(No. 1)
HO O H3C H3C H O H O H CH3 H3C H3C
NH2 N HO N O O HO HO
CHO HO OH OH CH2OH HO O O HO N
NH
. HCl
NH3.H2O MeOH
. HCl
N
D-阿拉伯糖
安西他滨
阿糖胞苷
第二节 分子的互补性-先导化合物的 发现
又称:基于结构的药物设计 一、分子识别 配体与受体相互作用的本质是分子识别。 分子识别是由于两个分子的多个特定的原子或基团性质的 互补性和空间的适配所驱动的,这种特异性的本质是双方 的互补性。 药物与受体的分子识别和相互作用,大都形成非共价键作 用,与维持机体的生物大分子的空间结构的键合力在本质 上是相似的(氢键、静电引力和疏水作用)。 药物和受体分子构象变化,诱导契合。
H2N
N=N NH2
SO2NH2
H2N
SO2NH2
活性代谢产物---磺胺 先导化合物
H2N
SO2NH N O CH3
磺胺甲恶唑 磺胺类抗菌药
从代谢产物开发的新药:
(1)非索那定
(2)诺阿司咪唑
(3)地氯雷他定
五、从临床药物的副作用或者老药新用中发(From SideEffect or New Purpose of Medicine)
1、 1929年青霉素的发现
2、异丙肾上腺素:β -受体激动剂,结构改造,发现 β -受体阻断剂--普萘洛尔,
化学生物学相互作用与分子识别PPT课件
第四节 超分子化学与分子识别
分子印迹聚合物与分子识别
概念: 分子印迹技术(molecular imprinting technique, MIT)是为获得在空间结构和结合点位上与某一分子(通常称为 模板分子)完全匹配的聚合物的实验制备技术,所得到的具有识别模板分子的聚合物被称为分子印迹聚合物(也 叫分子烙印聚合物,molecularly imprinted polymers, MIP)。
[A][B] =
[AB]
Koff
= Keq Kon
Keq 为平衡常数,又称亲和常数
三、分子识别的特性
1 作用的专一性 (1)酶与底物作用的专一性 (2)抗原-抗体相互作用的专一性
抗原:能够刺激机体产生免疫应答,并能与免疫应答产物发生特异性结合的物质。 抗体:肌体的免疫系统接受抗原物质刺激后,由浆细胞合成和分泌的一类能与抗原发生特异性结合的球蛋白。
抗原
抗体
抗原与抗体特异性 结合,表现出溶菌、 杀菌、促进吞噬、 中和毒素等作用。
(3)受体与配体 相互作用的特异性
受体
膜受体 胞内受体 核受体
配体
信号分子
(4)蛋白质与糖链相互作用的专一性
(5)蛋白质与核酸相互作用的专一性
锌指结构是指由至少三个在结构上不同的、由锌离子稳定的超小结构域组成的蛋白质基元,锌指 结构与DNA大沟结构时主要涉及三个碱基对,锌指结构之间的连接区悬于大沟之上,不直接参与 DNA的结构。
2 运动
振动
共价连接的原子相对另一原子做快速往复运动
旋转
三种运动形式对相互作用分子表面的接近都是极其重要的
二、分子识别过程的动力学
1 结合与解离 2 平衡常数
若分子A可特异识别分子B,则平衡时:
化学与生物传感 2
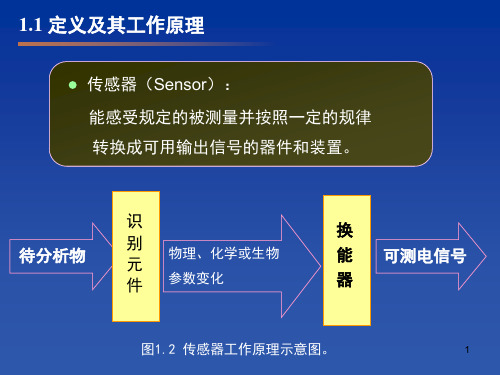
NAD+和NADP+ FMN和FAD 铁卟啉
脱氢酶 氧化酶 过氧化物酶
辅助因子通常存在酶的活性中心部位,对酶的催化起 重要作用。
18
以铁卟啉为辅基的
细胞色素c
肌红蛋白 (Mb)
血红蛋白(Hb)、辣根过氧化物酶(HRP)等
19
2.3.1 酶及酶反应 二、 酶的特性
1. 高效性;
生物催化剂
2. 高度专一性 3. 反应条件温和,一般在常温、常压;
的反应。
33
2.3.2 微生物及微生物反应
微生物传感器的工作原理
微生物的特征
微生物具有新陈代谢机能(物质的合成与分解)和呼吸机 能(O2的消耗),菌体内具有复合酶、能量再生系统等。
34
2.3.2 微生物及微生物反应 微生物传感器的工作原理
(a) 呼吸机能型
环境废水BOD分析仪
图2.8 微生物传感器的工作原理
49
2.3.4 核酸及核酸反应
DNA杂交
50
2.3.4 核酸及核酸反应 DNA传感器的分类
根据传感器DNA识别模型的不同 (1)单链DNA (ssDNA) 传感器
利用固定化单链 DNA探针,在碱基配对原则基础上进行分子识 别检测系统,通过DNA分子杂交反应,直接或间接产生的信号变化检
是一种利用对特定化合物具有的预定选择性来制备合成识别位点的 技术。
图2. 4 MIP制备的一般步骤
11
2.2.2 分子印迹
已制备分子印迹传感器 尼古丁、吗啡、对硫磷、氯霉素 敌草净等等 例如:尼古丁检测 在弱酸性条件下,以邻氨基酚为单体,尼古丁为模 板分子,用循环伏安法电聚合成膜制备传感器。 检测浓度: 4.010-7 3.3 10-5 mol/L
分子间相互作用与分子识别

分子间相互作用与分子识别(北京大学化学与分子工程学院张驰窦萌徐迟胡田骁)摘要:化学的研究几百年来主要集中在分子层次,针对分子的组成、结构和性质。
分子的微观结构决定了其宏观性质,而联系宏观性质和微观结构的就是分子之间的相互作用和反应。
自从1987年诺贝尔奖获得者J.M.Lehn提出超分子的概念以来,这一学科迅速发展,在现代材料、催化剂等领域起着极大的作用。
超分子的性质和结构主要由分子间相互作用决定,分子间相互作用的一种特异选择性表现在分子识别上。
本文通过介绍分子间相互作用的类型和分子识别的基本原理,简单阐述了超分子化学的基础内容和一些实例。
关键词:分子间力Van der Waals力次级键氢键分子识别原理应用超分子一、分子间相互作用1.什么是分子间相互作用分子间相互作用就是基团或分子间除去共价键、离子键、和金属键外一切相互作用力的总称。
物质凝聚态的存在是分子间存在相互作用的最简单的证据。
分子间相互作用的强弱可以用分子间相互作用能U的大小来衡量,它是一个势能量,为分子间距离R的函数。
如图1.1.1所示:它有一个在长程相互吸引的区域,其力为-∂V/∂R它在较劲的范围是排斥区;式中R m是相应于能量最低点的分子间距离,σ表示分子间势能为零的距离,ε表示吸引势阱的深度。
V(R)函数曲线的形式会因分子的不同而略有差异,但它们是具有共同的特征的。
图1.1.1典型分子间作用势能函数2.分子间相互作用的组成分子间相互作用主要包括:离子或电荷基团,偶极子,诱导偶极子等之间的相互作用力,氢键力,疏水基团相互作用力及非键电子推迟力等,大多数分子间作用能在10kJ.mol-1以下,比通常的共价键键能小一、二个数量级,作用范围约为0.3-0.5nm,除氢键外,一般没有方向性和饱和性。
各种分子间相互作用能的大小与距离r的函数关系如下:表1.2.1一些分子间相互作用能与分子间距离的函数关系(1)Van der Waals力以上表1.2.1中作用能与1/r6成正比的三种作用力统称Van der Waals 力。
生物传感器

• 热生物传感器(calorimetricbiosensor)
• 压电晶体生物传感器(piezoelectricbiosensor)
3.3 以待测物与分子识别元件的相互作用方式进行分类
5.3 发酵工业
(1)原材料及代谢产物的测定 微生物传感器可用于测量发酵工业中的原材料和代谢产 物。测量的装置基本上都是由适合的微生物电极与氧电极组 成,原理是利用微生物的同化作用耗氧,通过测量氧电极电 流的变化量来测量氧气的减少量,从而达到测量底物浓度的 目的。 (2)微生物细胞数目的测定 人们发现在阳极表面上,菌体可以直接被氧化并产生电流。 这种电化学系统可以应用于细胞数目的侧定。侧定结果与常 规的细胞计数法测定的数值相近。利用这种电化学微生物细 胞数传感器可以实现菌体浓度连续、在线的测定。
• 生物亲合型生物传感器(affinitybiosensor)
4.1 速度快,成本低 采用固定化酶膜作为分析工具, 酶法分析试剂可 以反复使用数千次, 其分析成本大大降低,分析速度快, 不到20s可以获得准确的分析结果 4.2 专一性强 生物传感器只对特定的底物起反应,而且不受颜色 和浊度的影响, 因此一般不需要进行样品的预处理, 干 扰少
我国自主研发生物传感器产品及跨国企业集团在中国推出的产品
共存并相互竞争。
一些掌握生物传感器技术的跨国大企业集团,看好被称为“世界
工厂”的中国市场,采取技术输出的途径,吸收我国的技术力量 和销售途径,在我国市场上进行生物传感器的开发、产品制造和 销售。
一部份海外留学归国的生物传感器专门人才也将自己的成果在中
生 物 传 感 器
化学生物学中的分子识别与探测

化学生物学中的分子识别与探测化学生物学是将化学原理与生物学相结合的跨学科领域,旨在研究生物分子之间的相互作用及其在生物系统中的功能。
分子识别和探测是化学生物学中的重要研究领域之一,它涉及了分子识别的原理、方法和应用。
本文将探讨化学生物学中的分子识别与探测的基本概念、技术和应用。
一、分子识别的原理分子识别是指分子之间通过非共价相互作用,以特异性和选择性地辨识和识别目标分子。
这些非共价相互作用包括氢键、范德华力、静电作用、疏水作用等。
而分子识别的选择性则取决于目标分子的化学结构、空间构型以及周围环境等因素。
二、分子识别的方法在化学生物学中,常用的分子识别方法包括荧光探针法、质谱分析法、核磁共振法、表面等离子共振法等。
荧光探针法是一种常用的分子识别方法,它利用合成的荧光染料与目标分子发生特异性相互作用,从而产生荧光信号来检测和识别目标分子。
质谱分析法是一种通过对样品分子的质量和荷质比进行测量,从而确定其分子结构和组成的方法。
核磁共振法则是利用核磁共振现象来研究分子结构和动态行为的一种方法。
表面等离子共振法则是通过检测生物分子与表面上固定的配体相互作用时引起的光信号变化来进行分子识别的方法。
三、分子探测的原理分子探测是指通过某种方法或技术来检测和测量样品中存在的目标分子。
其原理主要涉及到分子与探测器之间的特定相互作用以及信号的转化和放大。
例如,荧光探针法中,当荧光探针与目标分子结合时,荧光强度会发生变化,这种变化可以被光谱仪等仪器测量和记录。
四、分子探测的方法和应用在化学生物学中,有多种分子探测方法被广泛应用。
例如,酶活性探测法可通过测量酶对底物的催化活性来检测和确定样品中底物的存在或浓度。
荧光探针法则是利用荧光染料与目标分子结合形成复合物,产生荧光信号用于分子的检测和测量。
另外,生物传感器和纳米技术也被广泛应用于分子探测领域。
生物传感器是一种将生物分子识别元件和传感器技术结合起来实现目标分子检测的设备。
化学生物学导论新版教学大纲-终

《化学生物学导论》教学大纲课程编码:课程名称:化学生物学导论(Foundation of Chemical Biology)课程地位及意义:该课程类型为学科平台课程,学分:2;学时:36;开课学期:第三学年学年。
随着生命科学领域研究的不断深入,生物功能分子机制研究水平进入了单细胞、单分子层次。
特别是人类基因组计划的完成,人们需要在分子水平上认识生命的过程,发现并阐明不同基因以及相应的蛋白质的结构和功能。
摆在化学家的面前的任务是如何利用化学的理论、研究方法和手段更加深入的理解和解释更多的生命现象,这就是新的一门交叉学科-化学生物学。
目前,化学生物学已经成为化学学科与生命科学交叉的一个重要发展方向,是一个充满活力和应用前景的研究领域。
近年来,化学生物学领域已取得了长足的发展,化学生物学研究的基本问题已经集中于生物大分子(蛋白质、核酸、多糖)与小分子的相互识别、作用和酶、模拟酶催化的有机合成及生物转化的研究。
化学生物学被定义为“发展和应用化学手段研究生命现象”。
无可置疑,化学生物学不但要突出化学学科在化学与生命科学结合中的作用,还要强调化学在为生命科学的发展作出贡献的同时也为化学学科本身发展提供更大的发展空间。
化学学科除了让学生掌握化学专业基础课知识外,还应该掌握化学生物学这门交叉学科的基础知识,以培养合格具有创新能力的现代复合化学人才。
因此,我们面向化学学科所有专业本科生开设《化学生物学导论》课程。
该课程主要培养目标就是要学生能够掌握化学生物学的基础。
具体要求学生牢固掌握组成生物体中的主要物质蛋白质、酶、核酸、聚糖、脂和膜的化学组成、结构、功能和主要性质;掌握化学物质与各种生物分子的相互作用及其在生命过程中的各种分子间作用机制。
为从分子水平上探究了生命的本质,为解决重大生物医学问题提供工具、方向和资源,造福于人类。
教学内容及课时分配绪论(2学时)Introduction知识点:了解化学生物学的起源,定义及其主要研究内容;了解化学生物学与生物化学、分子生物学的区别。
生物传感器的工作原理及检测流程

生物传感器的工作原理及检测流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!生物传感器的工作原理及其检测流程揭秘生物传感器是一种先进的技术,它巧妙地结合了生物学、物理学和工程学,用于快速、准确地检测各种生物和化学物质。
第二章分子识别元件及其反应基础

2.4 免疫学反应
4、免疫学分析:
1)沉淀法 2)放射免疫测定法 3)免疫荧光测定法 4)酶联免疫测定法
32
2.5 核酸与核酸反应
1、核酸组成与结构
• 核酸的组成成分 核酸有两大类:一是主要分布于细胞核中的脱氧核糖核
酸(简写DNA);另一是主要分布于细胞质中的核糖核酸 (简写RNA)。它们是由许多单核苷酸组成的多聚物,核酸 分子中核苷酸序列组成密码,用于储存和传输遗传信息, 指导各类蛋白质合成,两类核酸的差异是组成核酸的单 位——单核苷酸的化学组成不同。
6
2.2 酶及酶反应
酶的作用机理
4)酶的活性中心
1、特殊催化能力只局限于一定区域 2、活性中心往往位于凹穴处
活性中心有2个功能部位: • 结合域 • 催化域
酶 (Enzyme)
7
2.2 酶及酶反应
酶的作用机理
5)邻近效应和定向效应
邻近效应:底物在活性中心的浓度极高 定向效应:反应基团的分子轨道交叉,使分子间反应
29
2.4 免疫学反应
• 抗体结构
抗体的结构-有4条多肽链的对称结构
30
2.4 免疫学反应
3、抗原-抗体反应:
指抗原与相应抗体之间所发生的特异性结合反应。伴随 产生凝聚、沉淀、溶解和促进吞噬抗原颗粒的现象。
结合点位于Fab段,即抗体活性中心 结合的两个条件: 1)形状互补 2)电荷相反 抗原抗体的结合是可逆的。
2.2 酶及酶反应
酶:由生物体产生的具有催化能力的蛋白质 酶的蛋白质性质: 酶的催化性质:
1)高度专一性,锁和钥匙的关系。这种关系在生物大分子的 相互作用中具有普遍性
1
2.2 酶及酶反应
2)催化效率高,是其它催化剂的107-1013倍。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1)高度专一性,锁和钥匙的关系。这种关系在生物大分子的 相互作用中具有普遍性
第二章分子识别元件及其反应基础
2
2.2 酶及酶反应
2)催化效率高,是其它催化剂的107-1013倍。
3)催化条件要温和,极端条件下会失活。
4)有些酶催化时需要辅酶
根据微生物反应对氧的需求分为:
好氧型 枯草杆菌、青霉菌
新
陈 厌氧型 破伤风菌
代
谢 兼氧型 大肠杆菌、酵母菌
第二章分子识别元件及其反应基础
20
2.3 微生物反应
微生物反应的类型:
细胞能量的产生与转移
高能化合物:ATP
来源:
1)代谢物脱氢或脱水引起分子内能量重新分布,而形成 的高能磷酸键转移给ADP生成ATP
5)酶在体内的活力受多种方式调控
6)酶促反应产生多种形式的信息变化
第二章分子识别元件及其反应基础
3
2.2 酶及酶反应
酶量表示方法
酶活力单位IU,一个活力单位指特定条件下,1min内能转化 1μM底物分子的酶量。
酶比活力,指1mg酶所具有的酶活力,单位IU/mg
酶含量指每克或每毫升酶制剂中含有的活力单位数,IU/g或 IU/ml
2)氧化磷酸化产生ATP,是指电子从NADH或FADH2经 电子传递链传递给分子氧生成水,并偶联ADP和Pi生成 ATP的过程。它是需氧生物合成ATP的主要途径。
第二章分子识别元件及其反应基础
21
2.3 微生物反应
分析微生物学:
定义:利用微生物完成定量分析任务的学科 1)细胞增殖法的原理
2)呼吸法的原理
7
2.2 酶及酶反应
酶的作用机理
4)酶的活性中心
1、特殊催化能力只局限于一定区域 2、活性中心往往位于凹穴处
活性中心有2个功能部位: • 结合域 • 催化域
酶 (Enzyme)
第二章分子识别元件及其反应基础
8
2.2 酶及酶反应
酶的作用机理
5)邻近效应和定向效应
邻近效应:底物在活性中心的浓度极高 定向效应:反应基团的分子轨道交叉,使分子间反应
第二章分子识别元件及其反应基础
22
2.4 免疫学反应
第二章分子识别元件及其反应基础
23
2.4 免疫学反应
第二章分子识别元件及其反应基础
24
2.4 免疫学反应
免疫学经历了四个迅速发展阶段
1876年后,多种病原菌被发现,用已灭活及减毒的病原体 制成疫苗,预防多种传染病,使疫苗得以广泛发展和使用。
微生物反应的类型:
根据物质代谢流向分为:
第二章分子识别元件及其反应基础
18
2.3 微生物反应
微生物反应的类型:
根据对营养的要求分为:
光能自养型:如:绿硫细菌 新 自养型
陈 代
化能自养型: 如:硝化细菌
谢 异养型 动物,寄生腐生的细胞与
真菌
第二章分子识别元件及其反应基础
19
2.3 微生物反应
微生物反应的类型:
近似于分子内反应
第二章分子识别元件及其反应基础
9
2.2 酶及酶反应
酶的作用机理
6)诱导契合假说
第二章分子识别元件及其反应基础
10
催化反应
2.2 酶及酶反应
酶的作用机理
7)酶催化的化学形式
共价催化:形成过渡态的中间物
E+S
ES
E+P
酸碱催化:质子供体与质子受体的催化
相关功能基团:羧基、氨基等
为了要解释这一现象,Michaelis & Menten 提出 了中间复合物学说。
第二章分子识别元件及其反应基础
13
2.2 酶及酶反应
酶促反应的米氏动力学
经推导后得出底物浓度与反应速度的关系方程
Km—— 米氏常数 由于 Km= (k2+k3)/k1 , ∴ 为复合常数。 Km是酶的特征常数,经常表示酶与底物的亲和力。
Km值越大,亲和力越小。
第二章分子识别元件及其反应基础
14
2.2 酶及酶反应
酶促反应的米氏动力学
酶动力学稳态期反应物质浓度变化
第二章分子识别元件及其反应基础
15
2.2 酶及酶反应
酶促反应的米氏动力学
Vmax ·[S]
V=------------------
Km + [S] 根据米氏方程可以说明以下关系:
第二章 分子识别元件及其反应基础
2.1 概述
分子识别元件又称敏感元件,是具有分子识 别能力的生物活性物质(如组织切片、细胞、 细胞器、细胞膜、酶、抗体、核酸、有机物 分子等),是生物传感器最重要的组成部分;
特点是能对靶分子(待测对象)具有特异 性识别功能
第二章分子识别元件及其反应基础
1
2.2 酶及酶反应
包括族专一性和键专一性。 绝对专一性:有些酶只作用于一种底物,催化一个反
应, 而不作用于任何其它物质。 立体专一性:这类酶不仅要求底物有一定的化学结构,
而且要求有一定立体结构。只对其中的某一种构型起作用, 而不催化其他异构体。
第二章分子识别元件及其反应基础
6
2.2 酶及酶反应
酶的作用机理
3)酶的辅助因子
酶的辅因子有辅酶或辅基,其主要作用是作为电子、原 子或某些基团的载体参与反应并促进整个催化过程。 (1)传递电子体:如 卟啉铁; (2)传递氢(递氢体):如 黄素单核苷酸(FMN) (3)金属酶:Zn2+ Mg2+ (4)传递碳基团:如 四氢叶酸; (5)传递磷酸基:如 ATP,GTP;
第二章分子识别元件及其反应基础
第二章分子识别元件及其反应基础
4
2.2 酶及酶反应
酶的作用机理 1)降低反应活化能
活化能的定义
第二章分子识别元件及其反应基础
5
2.2 酶及酶反应
酶的作用机理
2)结构专一性
即酶只能对特定的一种或一类底物起作用,这种专一性是由酶蛋 白的结构特性所决定的。
可分为: 相对专一性:这类酶对结构相近的一类底物都有作用。
在中性条件下,有一半是酸形式、一半是碱形式。因此既可 进行酸催化,又可进行碱催化,所以咪唑基是酶分子最有效、 最活泼的一个功能基团。
第二章分子识别元件及其反应基础
11
2.2 酶及酶反应 酶促反应Biblioteka 米氏动力学Vmax2
Km
第二章分子识别元件及其反应基础
12
2.2 酶及酶反应
酶促反应的米氏动力学
当[S]<<Km时,
Vmax [S]
Vmax
v = ──── = ─── [S] = K [S]
Km
Km
这时底物浓度低,酶没有全部被底物所饱和。
第二章分子识别元件及其反应基础
16
2.3 微生物反应
微生物反应的特点: 1)与酶促反应的共同点 2)特殊性
第二章分子识别元件及其反应基础
17
2.3 微生物反应
