最新整理特征质子的化学位移培训资料
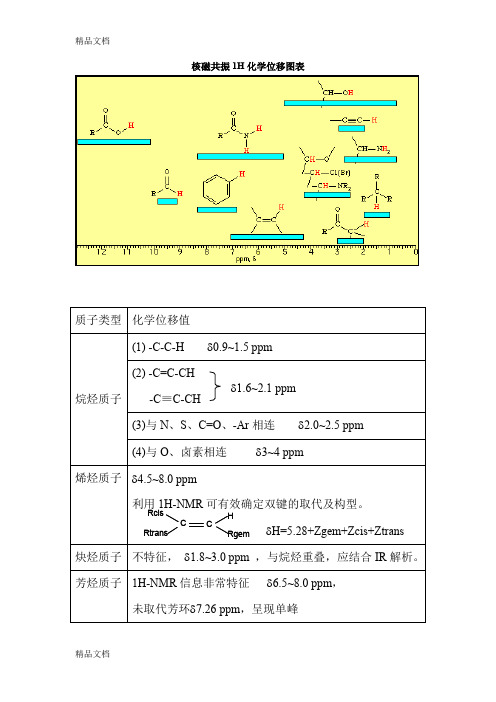
不同类型质子的化学位移

B0
C16
16
O
C
O (C)
C
C
三、影响化学位移的因素
3. 炔键的磁各向异性效应 炔键的电子环流在键轴方向附近产生反屏蔽区域,化学位移向高 场方向移动。如下图所示:
17
17
三、影响化学位移的因素
三、氢键效应 连接在杂原子(如O、N、S)上的质子容易形成氢键,氢键状态 对形成氢键质子化学位移的影响称为氢键效应。活泼氢形成氢键后, 所受的屏蔽效应变小,化学位移值移向低场。 分子间氢键形成的程度与试样浓度、温度以及溶剂的种类有关。 分子内氢键的特点是不随非极性溶剂的稀释而改变其缔合程度,据此 可与分子间氢键相区别。
CH3X X 的电负性 δ CH3F 4.0 4.26 CH3Cl 3.1 3.05
12
CH3Br 2.8 2.68
CH3I 2.5 2.16
CH4 2.1 0.23
12
三、影响化学位移的因素
一、电性效应
2. 共轭效应 共轭取代基可使与之共轭结构中的价电子分布发生改变,从而引起质 子的化学位移变化。如醛基(-CHO)与苯环间呈吸电子共轭效应, 使苯环上总的电子云密度减少,苯环上各质子δ 值都大于未取代苯上 质子的δ 值。
2
B0 标准 - 样品
共振频率差(Δν ,Hz)与外磁场强度B0成正比。同一样品的同一磁性核
用不同MHz仪器测得的共振频率差不同。如我们假定一个峰在300
MHz仪器上对于频率为1200 Hz9 ,如果换作600 MHz的仪器,我们 指定的峰将会是2400 Hz的位置。
9
二、化学位移标准物质和化学位移的表示
6
6
二、化学位移标准物质和化学位移的表示
化学位移ppt课件

31
4.2.2.各类1H的化学位移
1~2:相邻没有电负性基团的饱和碳上的氢(CCHn)、烯烃或 炔烃α-H 2~4.5:相邻有电负性基团(如:C=O、O、N、S、Cl、Br等) 的饱和碳上的氢 (XCHn)、苯环α-H 其它氢核:炔氢:2~3 烯氢:4.5~8 芳氢(ArH): 6.0~9.0
23
c)围绕部分双键(受阻旋转)的互变 DMF:
24
• 活泼氢的快速交换反应
分子中的-OH、-NH2、-SH和-COOH等活泼氢可在分子间进行 快速交换。
因此, 酸性氢核的化学位移是不稳定的,与交换快慢、 交换是否进行有关。
交换速率:-OH > -NH > -SH
25
(5) 氢键的影响
两个电负性基团与氢相连,产生吸电子诱导作用,共振发 生在低场。
O
C
.. N
CH3 b
H
CH3 a
OC
+ N
CH3 b
H
CH3 a
在氘代氯仿溶剂中,b2.88;a2.97。
逐步加入各向异性溶剂苯,a和b甲基的化学位移逐渐
靠近,然后交换位置。
29
30
溶剂效应的产生是由于溶剂的磁各向异性造成或者是 由于不同溶剂极性不同,与溶质形成氢键的强弱不同引 起的.
27
(6) 范德华效应
当两个质子在空间结构上非常靠近时,电子云就会互相排 斥,从而使这些质子周围的电子云密度减少,屏蔽作用下降, 共振信号向低场移动,这种效应称为范德华效应。这种效应 与相互影响的两个原子之间的距离密切相关。
28
特征质子的化学位移

R2CHCOOR
2~2、2
RCH2F
4~4、5
RCOOCH3
3、7~4
RCH2Cl
3~4
RC≡CCOCH3
2~3
RCH2Br
3、5~4
RNH2或R2NH
0、5~5(峰不尖锐,常呈馒头形)
RCH2I
3、2~4
ROH
0、5~5、5(温度、溶剂
、浓度改变时影响很大)
RCONRH或ArCONRH
5~9、4
[1]
烷烃
甲烷氢的化学位移值为0、23,其它开链烷烃中,一级质子在高场δ≈9处出现,二级质子移向低场在δ≈1、33处出现,三级质子移向更低场在δ≈1、5处出现。例如:
烷烃
CH4
CH3—CH3
CH3—CH2—CH3
(CH3)3CH
δ
0、23
0、86
0、86
0、91
1、33
0、91
0、86
1、50
甲基峰一般具有比较明显的特征,亚甲基峰与次甲基峰没有明显的特征,而且常呈很复杂的峰形,不易辨认。当分子中引人其它官能团后,甲基、次甲基及亚甲基的化学位移会发生变化,但其δ值极少超出0、7~4-5这一范围。
特征质子的化学位移
由于不同类型的质子化学位移不同,因此化学位移值对于分辨各类质子就是重要的,而确定质子类型对于阐明分子结构就是十分有意义的。下表列出了一些特征质子的化学位移,表中黑体字的H就是要研究的质子。
核磁共振氢谱化学位移ppt正式完整版

化从学核位 磁移共的振表条示件方式法可与以测看定出,磁性原子核的共振频率ν只和效磁旋应比,γ和σ外称加磁为场屏强度蔽B0常有关数。。
核σB外0,电此子时在原修外子加核正磁实场的际作受用核到下的磁产磁生共场电强子振度环小条流于,件原电外子:加环磁流由场产强生于度相B屏应0,的蔽这感种应效核磁外应场电,不子感对应同原磁子导场核的致的方影向化响与称学原为外环屏加蔽磁境效场应不的,方同σ向称相为的反屏,蔽磁常场数强。度等于
不同质子的化学位移
不同质子的化学位移
不同质子的化学位移
5. 氢键:分子形成氢键后,氢核周围的电子云密度降低, 产生去屏蔽作用,化学位移向低场移动,增大。
6. 温度:大多数信号的共振位置受温度影响很小,但-OH, -NH和-SH在升高温度时形成氢键的程度降低,化学位移 移向高场,降低。 7. 溶剂效应:溶剂的磁各向异性和溶质与溶剂之间形成 氢键将对溶质中不同位置的氢核的化学位移产生影响。
影响化学位移的因素
(2)苯环的磁各向异性效应
环内氢 = -2.99 环外氢 = 9.28
影响化学位移的因素
(3)叁键的磁各向异性效应
影响化学位移的因素
(4)单键的磁各向异性效应
直立键上的氢核处于屏蔽区,在较高场,平伏键上的氢核处于去屏 蔽区,在较低场,化学位移值大约相差0.5 ppm。
影响化学位移的因素
核磁共振氢谱化学位移
内容提要
化学位移的产生 化学位移的表示方法与测定 影响化学位移的因素 不同质子的化学位移
化学位移的产生
•核磁共振条件及面临的问题
1. 核磁共振的条件小结:
(1)自旋核(I≠0)
(2)外加磁场B0 (3)外加射频的能量hv等于自旋核磁能级的能量差:
化学位移

二. 共轭效应
在共轭效应中,推电子基和吸电子基的影响各 不相同。 推电子基—— p -π共轭——电子云密度 ——δ 。 吸电子基——π-π共 轭——电子云密度 ——δ 。
三. 磁各向异性效应(magnetic anisotropic effect)
实验表明: CH2=CH2 CH=CH CH3-CH3
规定
四甲基硅的
TMS
= 0
用TMS作为基准的原因: (1) 12个氢处于完全相同的化学环境,只产生一个尖峰; (2) 屏蔽强烈,位移最大,共振峰在最高场区,与其他有 机化合物中的质子峰不重迭; (3) 化学性质稳定;易溶于有机溶剂;沸点低,易回收。
当用重水作溶剂时,标准物质可选用:
DSS (2,2-二甲基-硅戊烷-5磺酸钠)
分子中处于不同化学环境的氢核的外围电子云 密度不同,使它们产生共振需要不同大小的外磁场 强度来抵消屏蔽效应的影响。 当用同一射频照射样品时,样品分子中处于不 同化学环境的氢核 ,所产生的共振峰将出现在不 同磁场强度的区域。这种共振峰位置的差异称为化 学位移。
一. 化学位移的表示方法
用待测核共振峰所在位置的场强 Bs 和某标准 物质磁性核共振峰所在位置的场强 Br 进行比较,用
3.4. 各类有机化合物的化学位移
一. 烷烃
-CH3: -CH2: -CH: CH3= 0.791.10ppm CH2 = 0.981.54ppm CH = CH3 +(0.5 0.6)ppm H=3.2~4.0ppm H=2.2~3.2ppm
O CH3 N CH3 C C CH3 O C CH3 CH3
对于理想化的、裸露的氢核,
实现核磁共振的条件:
0 = B0 / (2 )
第二节 化学位移

常见结构单元化学位移范围
O ~2.1
H3C C
~3.0
~1.8
H 3C N H3C C C
~3.7 H H3C O
O
H
C OH C O
H CC
~0.9 H3C C
15 14 13 12 11 10 9 8 7 6 5 4 3 2 1 0 »¯ ѧλ ÒÆ Ä¦ (ppm)
一、化学位移的产生
理想化的、裸露的氢核; 满足共振条件:
0 2B0 h
产生单一的吸收峰; 实际上,氢核受周围 不断运动着的电子影响。 在外磁场作用下,运动着 的电子产生与外磁场反向的感应磁场,起到屏蔽作用,使氢核实际 受到的外磁场作用减小。
B=(1- )B0 :屏蔽常数。 越大,屏蔽效应越大。
如:在乙醚分子中,CH3CH2—O—CH2CH3由于吸电子原子O的 影响, 使CH2质子的外围电子云密度低于甲基质子的外围电子云密度, 屏蔽常数σ(CH3)>σ(CH2), 所以δ(CH3)<δ(CH2)
③ 1H核相邻的电负性原子数越多,则δ其值越大.
如: 化合物 δH
CH3Cl 3.05
CH2Cl2 5.33
π电子产生诱导磁场,质子位于其磁力线中,磁3;
-
Be +
B0
因为感应磁力线具有闭合性质双键区内感应磁场Be与外磁场B0 反向,称此区域为屏蔽区 + ;在屏蔽区实际感应强度减小。 反 之,去屏蔽区 - ,实受感应强度增大,共振吸收信号移向低场, δ增大。
CH2=CH2中的四个1H均位于去屏蔽区,所以其化学位移 (δ=5.25)比乙烷的(δ=0.9)大的多。醛质子的δ值在7.8~10.5范 围内,又比乙烯质子大,因为醛质子既受双键的磁各向异性效应
03_化学位移

Cl
Ha
CC
Cl
Hb
A
Cl Ha C
Cl
Hb
B
O
H3C
CH 3
a
b
C
H3C
Cl Ha
Cl
CH 3
Hb
D
Ha
O
Hb
Br
Br
E
Cl
Ha
CC
Hc
Hb
2020/9I/25
Br Ha C
Cl Hb
F
a CH3 b H3C C OCH 3 CH 3
J
Ha
Hb
CH 3
CH 3
G
NO 2
Ha
Ha
Hb
Hb
Hc
K
H3C
某组环境相同的氢,若分别与 n 个 和 m 个环 境不同 的氢发生偶合,则被裂分为( n+1 )×(m+1)重峰。
CH3CH2CH3 CH3CH2CH2NO2
两组峰,裂分峰的数目分别为3和7 三组峰,裂分峰的数目分别为3、12、3
2020/9/25
42
2、裂分峰强度比(面积比)
等于二项式的展开式系数之比 1
:屏蔽常数;
H0: 外磁场强度
H H 0H 感 ( 应 1-) H 0
H(1)H0
2 2
2020/9/25
6
由于屏蔽作用的存在: 1)如果外磁场强度不变,氢核的共振频率降低; 2)如果保持共振频率不变,需要更大的外磁场强度(相对于 裸露的氢核)。
在有机化合物中,氢核受核外电子的屏蔽作用, 使其共振频率发生变化,即引起共振吸收峰的位移,
3
第三节: 化学位移(chemical shift)
最新核磁共振1H化学位移图表
核磁共振1H化学位移图表杂质峰种类:测试核磁的样品一般要求比较纯,并且能够溶解在氘代试剂中,这样才能测得高分辨率的图谱。
为不干扰谱图,所用溶剂分子中的氢都应被氘取代,但难免有氢的残余(1%左右),这样就会产生溶剂峰;除了残存的质子峰外,溶剂中有时会有微量的H2O而产生水峰,而且这个H2O峰的位置也会因溶剂的不同而不同;另外,在样品(或制备过程)中,也难免会残留一些杂质,在图谱上就会有杂质峰,应注意识别。
常用氘代溶剂和杂质峰在1H谱中的化学位移单位:ppm溶剂— CDCl3 (CD3)2CO (CD3)2SO C6D6 CD3CN CD3OH D2O溶剂峰— 7.26 2.05 2.49 7.16 1.94 3.31 4.80水峰— 1.56 2.84 3.33 0.40 2.13 4.87 —乙酸— 2.10 1.96 1.91 1.55 1.96 1.99 2.08丙酮— 2.17 2.09 2.09 1.55 2.08 2.15 2.22乙腈— 2.10 2.05 2.07 1.55 1.96 2.03 2.06苯— 7.36 7.36 7.37 7.15 7.37 7.33 —叔丁醇CH3 1.28 1.18 1.11 1.05 1.16 1.40 1.24 OH —— 4.19 1.55 2.18 ——叔丁基甲醚CCH3 1.19 1.13 1.11 1.07 1.14 1.15 1.21OCH3 3.22 3.13 3.08 3.04 3.13 3.20 3.22氯仿— 7.26 8.02 8.32 6.15 7.58 7.90 —环己烷— 1.43 1.43 1.40 1.40 1.44 1.45 —1,2-二氯乙烷 3.73 3.87 3.90 2.90 3.81 3.78 —二氯甲烷— 5.30 5.63 5.76 4.27 5.44 5.49 —乙醚CH3(t) 1.21 1.11 1.09 1.11 1.12 1.18 1.17CH2(q) 3.48 3.41 3.38 3.26 3.42 3.49 3.56二甲基甲酰胺CH 8.02 7.96 7.95 7.63 7.92 7.79 7.92CH3 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3 2.88 2.78 2.73 1.86 2.77 2.86 2.85二甲基亚砜— 2.62 2.52 2.54 1.68 2.50 2.65 2.71二氧杂环— 3.71 3.59 3.57 3.35 3.60 3.66 3.75乙醇CH3(t) 1.25 1.12 1.06 0.96 1.12 1.19 1.17CH2(q) 3.72 3.57 3.44 3.34 3.54 3.60 3.65OH(s) 1.32 3.39 3.63 — 2.47 ——乙酸乙酯CH3CO 2.05 1.97 1.99 1.65 1.97 2.01 2.07OCH2(q) 4.12 4.05 4.03 3.89 4.06 4.09 4.14CH3(t) 1.26 1.20 1.17 0.92 1.20 1.24 1.24甲乙酮CH3CO 2.14 2.07 2.07 1.58 2.06 2.12 2.19CH2(q) 2.46 2.45 2.43 1.81 2.43 2.50 3.18CH3(t) 1.06 0.96 0.91 0.85 0.96 1.01 1.26乙二醇—3.76 3.28 3.34 3.41 3.51 3.59 3.65润滑脂CH3(m) 0.86 0.87 — 0.92 0.86 0.88 —CH2(br) 1.26 1.29 — 1.36 1.27 1.29 —正己烷CH3(t) 0.88 0.88 0.86 0.89 0.89 0.90 —CH2 (m) 1.26 1.28 1.25 1.24 1.28 1.29 —甲醇CH3 3.49 3.31 3.16 3.07 3.28 3.34 3.34OH 1.09 3.12 4.01 2.16 ——正戊烷CH3(t) 0.88 0.88 0.86 0.87 0.89 0.90 —CH2(m) 1.27 1.27 1.27 1.23 1.29 1.29 —异丙醇CH3(d) 1.22 1.10 1.04 0.95 1.09 1.50 1.17CH 4.04 3.90 3.78 3.67 3.87 3.92 4.02硅脂— 0.07 0.13 — 0.29 0.08 0.10 —四氢呋喃CH2 1.85 1.79 1.76 1.40 1.80 1.87 1.88CH2O 3.76 3.63 3.60 3.57 3.64 3.71 3.74甲苯 CH3 2.36 2.32 2.30 2.11 2.33 2.32 —CH(o/p) 7.17 7.20 7.18 7.02 7.30 7.16 — ortho邻,para对CH(m) 7.25 7.20 7.25 7.13 7.30 7.16 —meta对三乙基胺CH3 1.03 0.96 0.93 0.96 0.96 1.05 0.99CH2 2.53 2.45 2.43 2.40 2.45 2.58 2.57石油醚— 0.5-1.5 0.6-1.9 —————。
最新核磁共振1H化学位移图表

核磁共振1H化学位移图表杂质峰种类:测试核磁的样品一般要求比较纯,并且能够溶解在氘代试剂中,这样才能测得高分辨率的图谱。
为不干扰谱图,所用溶剂分子中的氢都应被氘取代,但难免有氢的残余(1%左右),这样就会产生溶剂峰;除了残存的质子峰外,溶剂中有时会有微量的H2O而产生水峰,而且这个H2O峰的位置也会因溶剂的不同而不同;另外,在样品(或制备过程)中,也难免会残留一些杂质,在图谱上就会有杂质峰,应注意识别。
常用氘代溶剂和杂质峰在1H谱中的化学位移单位:ppm溶剂— CDCl3 (CD3)2CO (CD3)2SO C6D6 CD3CN CD3OH D2O溶剂峰— 7.26 2.05 2.49 7.16 1.94 3.31 4.80水峰— 1.56 2.84 3.33 0.40 2.13 4.87 —乙酸— 2.10 1.96 1.91 1.55 1.96 1.99 2.08丙酮— 2.17 2.09 2.09 1.55 2.08 2.15 2.22乙腈— 2.10 2.05 2.07 1.55 1.96 2.03 2.06苯— 7.36 7.36 7.37 7.15 7.37 7.33 —叔丁醇CH3 1.28 1.18 1.11 1.05 1.16 1.40 1.24 OH —— 4.19 1.55 2.18 ——叔丁基甲醚CCH3 1.19 1.13 1.11 1.07 1.14 1.15 1.21OCH3 3.22 3.13 3.08 3.04 3.13 3.20 3.22氯仿— 7.26 8.02 8.32 6.15 7.58 7.90 —环己烷— 1.43 1.43 1.40 1.40 1.44 1.45 —1,2-二氯乙烷 3.73 3.87 3.90 2.90 3.81 3.78 —二氯甲烷— 5.30 5.63 5.76 4.27 5.44 5.49 —乙醚CH3(t) 1.21 1.11 1.09 1.11 1.12 1.18 1.17CH2(q) 3.48 3.41 3.38 3.26 3.42 3.49 3.56二甲基甲酰胺CH 8.02 7.96 7.95 7.63 7.92 7.79 7.92CH3 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3 2.88 2.78 2.73 1.86 2.77 2.86 2.85二甲基亚砜— 2.62 2.52 2.54 1.68 2.50 2.65 2.71二氧杂环— 3.71 3.59 3.57 3.35 3.60 3.66 3.75乙醇CH3(t) 1.25 1.12 1.06 0.96 1.12 1.19 1.17CH2(q) 3.72 3.57 3.44 3.34 3.54 3.60 3.65OH(s) 1.32 3.39 3.63 — 2.47 ——乙酸乙酯CH3CO 2.05 1.97 1.99 1.65 1.97 2.01 2.07OCH2(q) 4.12 4.05 4.03 3.89 4.06 4.09 4.14CH3(t) 1.26 1.20 1.17 0.92 1.20 1.24 1.24甲乙酮CH3CO 2.14 2.07 2.07 1.58 2.06 2.12 2.19CH2(q) 2.46 2.45 2.43 1.81 2.43 2.50 3.18CH3(t) 1.06 0.96 0.91 0.85 0.96 1.01 1.26乙二醇—3.76 3.28 3.34 3.41 3.51 3.59 3.65润滑脂CH3(m) 0.86 0.87 — 0.92 0.86 0.88 —CH2(br) 1.26 1.29 — 1.36 1.27 1.29 —正己烷CH3(t) 0.88 0.88 0.86 0.89 0.89 0.90 —CH2 (m) 1.26 1.28 1.25 1.24 1.28 1.29 —甲醇CH3 3.49 3.31 3.16 3.07 3.28 3.34 3.34OH 1.09 3.12 4.01 2.16 ——正戊烷CH3(t) 0.88 0.88 0.86 0.87 0.89 0.90 —CH2(m) 1.27 1.27 1.27 1.23 1.29 1.29 —异丙醇CH3(d) 1.22 1.10 1.04 0.95 1.09 1.50 1.17CH 4.04 3.90 3.78 3.67 3.87 3.92 4.02硅脂— 0.07 0.13 — 0.29 0.08 0.10 —四氢呋喃CH2 1.85 1.79 1.76 1.40 1.80 1.87 1.88CH2O 3.76 3.63 3.60 3.57 3.64 3.71 3.74甲苯 CH3 2.36 2.32 2.30 2.11 2.33 2.32 —CH(o/p) 7.17 7.20 7.18 7.02 7.30 7.16 — ortho邻,para对CH(m) 7.25 7.20 7.25 7.13 7.30 7.16 —meta对三乙基胺CH3 1.03 0.96 0.93 0.96 0.96 1.05 0.99CH2 2.53 2.45 2.43 2.40 2.45 2.58 2.57石油醚— 0.5-1.5 0.6-1.9 —————。
核磁共振氢谱(化学位移)ppt课件

编辑版pppt
13
不同质子的化学位移
编辑版pppt
14
不同质子的化学位移
编辑版pppt
15
不同质子的化学位移
编辑版pppt
16
Thank You!
编辑版pppt
17
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
18
编辑版pppt
6
化学位移的表示方法与测定
2.05 3.66
编辑版pppt
7
影响化学位移的因素
1. 诱导效应:吸电子诱导效应降低原子核周围的电子云 密度,化学位移向低场移动,增大。
CH3X中甲基和各种取代基连接后的化学位移
-X
F OCH3 Cl Br CH3 H
4.26 3.24 3.05 2.68 0.88 0.2
编辑版pppt
3
化学位移的产生
•核外电子的影响,屏蔽效应,化学位移
修正的核磁共振条件
:
h
h
2
B0(1
)
1
2
B0(1
)
核外电子在外加磁场作用下产生电子环
流,电子环流产生相应的感应磁场,感
应磁场的方向与原外加磁场的方向相反
,磁场强度等于σB0,此时原子核实际 受到的磁场强度小于原外加磁场强度B0 ,这种核外电子对原子核的影响称为屏
核磁共振氢谱(1H-NMR)
——化学位移(chemical shifts)
Produced by Jiwu Wen
编辑版pppt
1
内容提要
化学位移的产生 化学位移的表示方法与测定 影响化学位移的因素 不同质子的化学位移
编辑版pppt
不同类型质子的化学位移

不同类型质子的化学位移在核磁共振(NMR)技术中,质子(H)的化学位移是一个重要的参数。
不同的物质由于其分子结构的不同,其质子的化学位移值也各有差异。
化学位移反应了质子周围的电子环境对其磁矢量产生的影响,是NMR 谱图中区分不同化合物的重要依据。
根据分子结构和电子分布的不同,质子可以大致分为两类:一类是氢原子,它通常存在于非极性环境中;另一类是重氢原子,它通常存在于极性环境中。
这两类质子的化学位移值存在显著的差异。
氢原子的化学位移值通常较低,主要受其周围电子环境的影响。
在有机化合物中,氢原子的化学位移值通常在0-2ppm之间。
在脂溶性维生素和生物膜中,氢原子的化学位移值较低,通常在5-5ppm之间。
而在水溶性维生素和核酸中,氢原子的化学位移值则较高,通常在5-0ppm之间。
重氢原子的化学位移值则较高,主要受其周围电子环境的影响。
在有机化合物中,重氢原子的化学位移值通常在2-4ppm之间。
在醇、酚和羧酸等化合物中,重氢原子的化学位移值通常在3-4ppm之间。
而在胺、酮和醛等化合物中,重氢原子的化学位移值则较低,通常在2-3ppm之间。
不同类型质子的化学位移对于解析NMR谱图至关重要。
通过分析质子的化学位移值,我们可以推断出其所在的分子环境和电子环境,从而进一步解析化合物的结构。
质子的化学位移也广泛应用于药物研发、材料科学、生物学等领域,对于研究分子的性质和行为具有重要意义。
不同类型质子的化学位移是NMR谱分析中的关键参数,对于解析分子结构和性质具有重要意义。
通过深入理解质子化学位移的原理和影响因素,我们可以更好地利用NMR技术进行物质分析和研究。
化学实验是化学教学的重要组成部分,对于培养学生的科学素养和创新实践能力具有至关重要的作用。
然而,不同类型的化学实验具有不同的教学重点和难点,因此需要针对不同类型的实验进行教学优化,以提高教学效果。
基础操作型实验主要是为了让学生掌握基本的化学实验操作方法和技能,如药品的取用、仪器的使用、实验数据的记录和处理等。
化学位移-生物物理

• 费米接触作用:两个核磁矩通过共价键传 递的相互作用
是形成液体谱精细结构的原因
自旋耦合造成的能级和谱线分裂
在简单谱中谱线的位置与JAX的符号无关。在复杂的波谱中,则耦合常数的符号会很大 程度地影响谱线的相对位置。
偶合常数
偶合常数——反映两核之间自旋偶合作用大小的量度, 用J表示。
J常常等于两裂分峰之间的裂距,一般在20Hz以下。
偶合常数也是重要的结构信息。例如:
Ha CC
Hb
CC
Ha
Hb
Ha CC Hb
Jab=0-3.5Hz
Jab=5-14Hz
Jab=12-18Hz
偶合常数的特点: ① J与H0无关。不同H0作用下或不同场强的仪器测得的J值相同。 ② 两组相互干扰的核J值相同。 例如,CH2ClCHCl2中三重峰间裂距等于二重峰间裂距。 ③ 在复杂体系中,J≠裂距!解析图谱时,需进行繁杂的计算以求得δ和J。
δ
= ν 样品-ν 标样 ν0
×
10
6=
437 60 ×10
6
× 10 6=7.28
chemical shifts分布
O
H
C OH C O
O ~2.1
H3C C
~3.0
~1.8
H 3C N H3C C C
~3.7
H
H3C O
H CC
~0.9 H3C C
15 14 13 12 11 10 9 8 7 6 5 4 3 2 1 0 化学位移 δ(ppm)
θ
r
ΔH
局部逆磁作用-2
诱导效应即相连原子或基团的电负性对核化学位移的影响:
• 附近的吸电子基团使核周围的电子云密度降低,屏蔽效应也降低,去屏蔽增加, 化学位移向低场移动 • 附近的推电子基团使核周围的电子云密度增加,屏蔽效应也增加,化学位移向高 场移动
化学位移

4.2.1 1H 的化学位移
1.影响化学位移的因素 2. 各类1H的化学位移
1.影响化学位移的因素
(1)电子效应 • 诱导效应
化学位移随着相邻电负性基团的电负性的增大而增大
X
X的电负 性
F OCH3 Cl 4.0 3.5 3.1
a )沿环单键的互变
环己烷:-89℃测定:Ha与Hb显示两个峰 常温下测定:显示一个峰
温度低于-89oC时,正己烷构象 固定,2-3键和5-6键的作用使Ha 处于屏蔽区,而Hb处于去屏蔽区
。 Hb - Ha ≈ 0.5ppm
甲基环己烷:室温下以直立和平伏质子的形式存在, 这些构象是不可重合的,低温下,一张谱图包含了这 两种形式。
4.2 核磁共振氢谱(1H NMR)
—发展最早,研究得最多,应用最为广泛。 —质子的旋磁比 较大,天然丰度接近100%,核磁共振
测定的绝对灵敏度最大; —1H是有机化合物中最常见的同位素,1H NMR谱是有机物
结构解析中最有用的核磁共振谱之一。
CH3CH2CONH2
低场
高场
• 化学位移值,代表谱峰位置—化学环境
CH3 CH3 H C O C Hb
CH3 CH3 a
HH I C C Cl
HH ab
CH3CH2CH2I a bc
a<b
a<b
a<b<c
• 下面化合物中所标出的质子其1H NMR化学位移从低场
到高C O CH2CH3
ab
cd
c 、 b 、d 、a
•共轭效应
(2) 相连碳原子的杂化态影响
化学位移

化学位移
1.化学位移是由于电子的屏蔽作用,核磁共振吸收位置的移动。
2.化学位移的绝对值差异很小,因此很难精确测量。
因此,需要选择一种标准物质,将其NMR吸收峰的位置设为零,用相对数值表示法来表示化合物吸收峰的位置。
3.常用的标准物质为四甲基硅烷(TMS),化学位移=0。
原因:
(1)TMS为对称分子,四个甲基上所连H化学环境相同,属于化学等价质子,其吸收峰只有一个;
(2)硅与碳属于同一主族元素,电负性相差不大,TMS中的质子所受屏蔽作用较大,共振吸收峰出现在高场。
4.绝大多数有机物中质子所受屏蔽效应比TMS 小,吸收峰处于低场,在TMS吸收峰的左侧。
5.影响化学位移的因素
(1) 电负性:
吸电子基团使得H核周围的电子云密度降低,屏蔽效应减小,化学位移值增大;
给电子基团使得H核周围的电子云密度升高,屏蔽效应增大,化学位移值减小。
(2) 值会随着H核与吸电子基团距离的增大而减小。
(可理解为:H核距离吸电子基团越远,H核周围电子云密度降低得越少,屏蔽效应越大,化学位移越小)
总结:
(1)化学位移与H核周围的电子云密度有关,可根据H核周围的电子云密度判断化合物吸收峰与标准物质吸收峰的位置关系。
(2)屏蔽区的质子向高场化学移动;未掩蔽区域中的质子化学移动到低场。
(3)高场位于参考材料的右侧,低场位于参考材料的左侧。
例如:卤素原子为吸电子基团,H核周围的电子云密度降低,屏蔽效应减小,化学位移值增大,位于低场,在标准物质吸收峰的左边。
祝各位小伙伴们端午节快乐!过节也不忘学习哦~~~。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.3
R3CH
1.5
R2C=CR—OH
15~19(分子内缔合)
0.22
RCH2OH
3.4~4
R2C=CH2
4.5~5.9
ROCH3
3.5~4
R2C=CRH
5.3
RCHO
9~10
R2C=CR—CH3
1.7
RCOCR2—H
2~2.7
RC≡CH
7~3.5
HCR2COOH
2~2.6
ArCR2—H
2.2~3
环己烷的各向异性屏蔽效应[1]
环烷烃能以不同构象形式存在,未被取代的环烷烃处在一确定的构象中时,由于碳碳单键的各向异性屏蔽作用,不同氢的δ值略有差异。例如,在环己烷的椅型构象中,由于C-I上的平伏键氢处于C⑵—C⑶键及C⑸—C⑹键的去屏蔽区,而C-I上的直立键氢不处在去屏蔽区,(图环己烷的各向异性屏蔽效应)。所以平伏键氢比直立键氢的化学位移略高0.2~0.5。在低温(-100℃)构象固定时,NMR谱图上可以清晰地看出两个吸收峰,一个代表直立键氢,一个代表平伏键氢。但在常温下,由于构象的迅速转换(图环己烷构象的转换),一般只看到一个吸收峰(见右图)。
R2CHCOOR
2~2.2
RCH2F
4~4.5
RCOOCH3
3Hale Waihona Puke 7~4RCH2Cl3~4
RC≡CCOCH3
2~3
RCH2Br
3.5~4
RNH2或R2NH
0.5~5(峰不尖锐,常呈馒头形)
RCH2I
3.2~4
ROH
0.5~5.5(温度、溶剂
、浓度改变时影响很大)
RCONRH或ArCONRH
5~9.4
[1]
其他
醇的核磁共振谱的特点参见后文。醚α-H的化学位移约在3.54附近。
酚羟基氢的核磁共振的δ值很不固定,受温度、浓度、溶剂的影响很大,只能列出它的大致范围。一般酚羟基氢的δ值在4~8范围内,发生分子内缔合的酚羟基氢的δ值在10.5~16范围内。
羧酸H的化学位移在2~2.6之间。羧酸中羧基的质子由于受两个氧的吸电子作用,屏蔽大大降低,化学位移在低场。R2CHCOOHδH=10~12。
环己烷构象的转换[1]
其它未取代的环烷烃在常温下也只有一个吸收峰。环丙烷的δ值为0.22,环丁烷的δ值为1.96,别的环烷烃的δ值在1.5左右。取代环烷烃中,环上不同的氢有不同的化学位移,它们的图谱有时呈比较复杂的峰形,不易辨认。[1]
C6D11H在不同温度下的1H-NMR谱[1]
烯烃
烯氢是与双键碳相连的氢,由于碳碳双键的各向异性效应,烯氢与简单烷烃的氢相比δ值均向低场移动3~4乙烯氢的化学位移约为5.25,不与芳基共轭的取代烯氢的化学位移约在4.5~6.5范围内变化,与芳基共轭时δ值将增大。乙烯基对甲基、亚甲基、次甲基的化学位移也有影响。例如:
化合物
CH4
CH3—CH=CH2
CH3—CH3
CH3—CH2—CH=CH2
(CH3)2CH2
(CH3)2CH—CH=CH2
δ
0.23
1.71
0.86
0.86
1.00
2.00
1.33
1.73
从上面的数据可以看出,同碳上有乙烯基的氢δ值约在1.59~2.14之间,变化较大,邻碳上有乙烯基的氢,δ值变化较小。[1]
烷烃
甲烷氢的化学位移值为0.23,其它开链烷烃中,一级质子在高场δ≈9处出现,二级质子移向低场在δ≈1.33处出现,三级质子移向更低场在δ≈1.5处出现。例如:
烷烃
CH4
CH3—CH3
CH3—CH2—CH3
(CH3)3CH
δ
0.23
0.86
0.86
0.91
1.33
0.91
0.86
1.50
甲基峰一般具有比较明显的特征,亚甲基峰和次甲基峰没有明显的特征,而且常呈很复杂的峰形,不易辨认。当分子中引人其它官能团后,甲基、次甲基及亚甲基的化学位移会发生变化,但其δ值极少超出0.7~4-5这一范围。
炔烃
炔基氢是与三键碳相连的氢,由于炔键的屏蔽作用,炔氢的化学位移移向高场,一般δ=1.7~3-5处有一吸收峰。例如,HC≡CH(1.80),RC≡CH(1.73~1.88),ArC≡CH(2.71~3-37),—CH=CH-C≡CH(2.60~3.10),—C≡C—C≡CH(1.75~2.42),CH3-C≡C-C≡C-C≡CH(1.87)。HC≡C—若连在一个没有氢的原子上,则炔氢显示一个尖锐的单峰。炔基对甲基、亚甲基的化学位移有影响,与炔基直接相连的碳上的氢化学位移影响最大,其δ值约为1.8~2.8。[1]
特征质子的化学位移
由于不同类型的质子化学位移不同,因此化学位移值对于分辨各类质子是重要的,而确定质子类型对于阐明分子结构是十分有意义的。下表列出了一些特征质子的化学位移,表中黑体字的H是要研究的质子。
特征质子的化学位移
质子的类型
化学位移
质子的类型
化学位移
RCH3
0.9
ArOH
4.5-4.7(分子内缔合10.5~16)
芳烃
由于受π电子环流的去屏蔽作用,芳氢的化学位移移向低场,苯上氢的δ=7.27。萘上的质子受两个芳环的影响δ值更大,α质子的δ为7.81,β质子的δ为7.46。一般芳环上质子的在δ值在6.3~8.5范围内,杂环芳香质子的δ值在6.0~9.0范围内。[1]
卤代烃
由于卤素电负性较强,因此使直接相连的碳和邻近碳上质子所受屏蔽降低,质子的化学位移向低场方向移动,影响按F,Cl,Br,I的次序依次下降。与卤素直接相连的碳原子上的质子化学位移一般在δ=2.16~4.4之间,相邻碳上质子所受影响减小,δ=1.25~1.55之间,相隔一个碳原子时,影响更小,δ= 1.03~1.08之间。[1]
羧酸衍生物
酯中烷基上的质子RCOOCH2R的化学位移δH=3.7~4。酰胺中氮上的质子RCONHR的化学位移,一般在δ= 5~9.4之间,往往不能给出一个尖锐的峰。
羰基或氮基附近α碳上的质子具有类似的化学位移= 2~3,例如,CH3COClδH=2.67,CH3COOCH3δH=2.03,RCH2COOCH3δH=2.13,CH3CONH2δH= 2.08,RCH2CONH2δH=2.23,CH3CNδH=1.98,RCH2CNδH=2.30。[1]
胺中,氮上质子一般不容易鉴定,由于氢键程度不同,改变很大,有时N—H和C一H质子的化学位移非常接近,所以不容易辨认。一般情况在α-HδH=2.7~3.1,β-Hδ=1.1~1.71。N-Hδ=0.5~5,RNH2,R2NH的δ值的大致范围在0.4~3.5,ArNH2,ArzNH,ArNHR的δ值的大致范围在2.9~4.8之间。[1]
