大学有机化学人名反应总结
最新大学有机化学人名反应总结

有机化学1 一、烯烃2 1、卤化氢加成3 (1)4CHCH 2R HXCH 3RX5 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
6 【机理】7CH 2CH 3CH +CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次8 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
9 【注】碳正离子的重排10 (2)11CHCH 2RCH 2CH 2R BrHBrROOR12 【特点】反马氏规则 13 【机理】 自由基机理(略)14【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
15 【本质】不对称烯烃加成时生成稳定的自由基中间体。
16 【例】17CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 318 2、硼氢化—氧化19CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-20 【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并21 且不重排。
22 【机理】232CH33H323H32CH CH2CH3HBH2CH CH=CH(CH3CH2CH2)3-H3CH2CH2C22CH3CH2B OCH2CH2CH3H3CH2CH2C2CH2CH3+O H-OHB-OC H2CH2CH3CH2CH2CH3H3CH2CH2B OC H2CH2CH3CH2CH2CH3H2CH2CH3HOO-B(OCH2CH2CH3)3 B(OCH2CH2CH3)3+3NaOH3NaOH3HOC H2CH2CH33+Na3BO3224【例】25CH31)BH32)H2O2/OH-CH3HHOH263、X2加成27C CBr/CClC CBrBr28【机理】29CC CC Br BrC Br +CC Br OH 2+-H +CC Br OH30 【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂31 进攻从背面进攻,不难看出是反式加成。
人名反应(类型整理)

人名反应1氧化:1・Baeyer-Villiger氧化:酮过酸氧化成酯迁移规则:叔>仲>环己基>苄>伯〉甲基〉氢2・Corey-Kim氧化:醇在NCS/DMF作用后,碱处理氧化成醛酮3・Criegee邻二醇裂解:邻二醇由Pb(OAc)4氧化成羰基化合物4・Criegee臭氧化:烯烃臭氧化后水解成醛酮5・Dakin反应:对羟基苯甲醛由碱性H2O2氧化成对二酚6・Dess—Martin过碘酸酯氧化:仲醇由过碘酸酯氧化成酮7・Fleming氧化•硅烷经过酸化,过酸盐氧化,水解以后形成醇8・Hooker氧化:2—羟基一3烷基一1,4—醌被KMnO4氧化导致侧链烷基失去一个亚甲基,同时羟基和烷基位置互变9・Moffatt氧化(Pfitzner—Moffatt)氧化:用DCC和DMSO氧化醇,形成醛酮10・Oppenauer氧化:烷氧基催化的仲醇氧化成醛酮11・Riley氧化:活泼亚甲基(羰基a位等)被SeO2氧化成酮12・Rubottom氧化:烯醇硅烷经过m—CPBA和K2CO3处理后a—羟基化KHCO3氧化成醇13・Sarett氧化:CrO3・Py络合物氧化醇成醛酮14・Swern氧化:用(COC1)2,DMSO为试剂合Et3N淬灭的方法将醇氧化成羰基化合物15・Tamao—Kumada氧化:烷基氟硅烷被KF,H2O2,16・Wacker氧化:Pd催化剂下,烯烃氧化成酮还原:1・・Barton—McCombie去氧反应:从相关的硫羰基体中间用n—Bu3SnH,AIBN 试剂经过自由基开裂发生醇的去氧作用2・Birch还原:苯环由Na单质合液胺条件下形成环内二烯烃(带供电子基团的苯环:双键连接取代基:带吸电子基团的苯环,取代基在烯丙位。
)3・Brown硼氢化:烯烃和硼烷加成产生的有机硼烷经过碱性H2O2氧化得到醇4・Cannizzaro歧化:碱在芳香醛,甲醛或者其他无a—氢的脂肪氢之间发生氧化还原反应给出醇和酸5・Clemmensen还原:用锌汞齐和氯化氢将醛酮还原为亚甲基化合物6・Corey—Bakshi—Shibata(CBS)还原:酮在手性恶唑硼烷催化下的立体选择性还原7・Gribble吲哚还原:用NaBH4直接还原会导致N—烷基化,NaBH3CN在冰醋酸当中还原吲哚双键可以解决8・Gribble二芳基酮还原.用NaBH4在三氟乙酸中还原二芳基酮和二芳基甲醇为二芳基甲烷,也可以应用于二杂芳环酮和醇的还原9・Luche还原:烯酮在NaBH4—CeCl3下发生1,2—还原形成烯丙位取代烯醇10・McFadyen—Stevens还原:酰基苯磺酰肼用碱处理成醛11.Meerwein—Ponndorf—Verley还原:用Al(OPr')3/Pr'OH体系将酮还原为醇12・Midland还原:用B—3—a—蒎烯一9—BBN对酮进行不对称还原13・Noyori不对称氢化.羰基在Ru(II)BINAP络合物催化下发生不对称氢化还原14・Rosenmund还原:用BaSO4/毒化Pd催化剂将酰氯氢化成醛,如催化剂未被毒化,会氢化为醇15・Wolff—Kishner—黄鸣龙还原.用碱性肼将羰基还原为亚甲基成烯反应:1・Boord反应:B-卤代烷氧基与Zn作用生成烯烃2・Chugaev消除:黄原酸酯热消除成烯3・Cope消除:胺的氧化物热消除成烯烃4・Corey-Winterolefin烯烃合成:邻二醇经1,1-硫代羰基二咪唑和三甲氧基膦处理转化为相应的烯5・Doering-LaFlamme丙二烯合成:烯烃用溴仿以及烷氧化物处理以后生成同碳二溴环丙烷再反应生成丙二烯6・Horner-Wadsworth-Emmons反应:从醛合磷酸酯生成烯烃.副产物为水溶性磷酸盐,故以后处理较相应的Witting反应简单的多7・Julia-Lythgoe成烯反应:从砜合醛生成(E)-烯烃8・Peterson成烯反应:从a-硅基碳负离子合羰基化合物生成烯烃.也成为含硅的Witting反应9・Ramberg-Backlund烯烃合成:A-卤代砜用碱处理生成烯烃10・Witting反应:羰基用膦叶立德变成烯烃11・Zaitsev消除:E2消除带来更多取代的烯烃人名反应2偶联反应:Cadiot-Chodkiewicz偶联:从炔基卤和炔基酮合成双炔衍生物Castro—Stephens偶联:芳基炔合成,同Cadiot-Chodkiewicz偶联Eglinton反应:终端炔烃在化学计量(常常过量)Cu(Oac)2促进下发生的氧化偶联反应Eschenmoser偶联:从硫酰胺和烷基卤生成烯胺Glaser偶联:Cu催化终端炔烃的氧化自偶联Gomberg—Bachmann偶联:碱促进下芳基重氮盐和一个芳烃之间经自由基偶联生成二芳基化合物Heck反应:Pb催化的有机卤代物或者三氟磺酸酯和烯烃之间的偶联反应杂芳基Heck反应:发生在杂芳基受体上的Pd(Ph3P)4,Ph3P,CuI,Cs2CO3催化下的分子内或者分子间Heck反应Hiyama交叉偶联反应:Pb催化有机硅和有机卤代物或者三氟磺酸酯等在诸如F—或者OH—之类的活化剂Pd(Ph3P)4,TBAF催化剂存在下发生的交叉偶联反应Kumada交叉偶联(Kharasch交叉偶联):Ni和Pd催化下,格氏试剂和一个有机卤代物或者三氟磺酸酯之间的交叉偶联Liebeskind—Srogl偶联:硫酸酯和有机硼酸之间经过Pd催化发生交叉偶联生成酮McMurry偶联•羰基用低价Ti,如TiC13/LiAlH4产生的Ti(0)处理得到双键,反应是一个单电子过程Negishi交叉偶联:Pd催化的有机Zn和有机卤代物,三氟磺酸酯等之间发生的交叉偶联反应Sonogashira反应:Pd/Cu催化的有机卤和端基炔烃之间的交叉偶联反应Stille偶联:Pd催化的有机Sn和有机卤,三氟磺酸酯之间的交叉偶联反应Stille—Kelly偶联:双Sn试剂进行Pd催化下二芳基卤代物的分子交叉偶联Suzuki偶联:Pd催化下的有机硼烷和有机卤,三氟磺酸酯在碱存在下发生的交叉偶联Ullmann反应:芳基碘代物在Cu存在下的自偶联反应Wurtz反应:烷基卤经Na或Mg金属处理后形成碳碳单键Ymada偶联试剂:用二乙基氰基磷酸酯(EtO)2PO-CN活化羧酸缩合反应:Aldol缩合:羰基和一个烯醇负离子或一个烯醇的缩合Blaise反应:腈和a—卤代酯和Zn反应得到B—酮酯Benzoin缩合:芳香醛经CN—催化为安息香(二芳基乙醇酮)Buchner-Curtius-Schlotterbeck反应:羰基化合物和脂肪族重氮化物反应给出同系化的酮Claisen缩合:酯在碱催化下缩合为B—酮酯Corey-Fuchs反应:醛发生一碳同系化生成二溴烯烃》然后用BuLi处理生成终端炔烃Darzen缩水甘油酸酯缩合:碱催化下从a—卤代酯和羰基化合物生成a,B—环氧酯(缩水甘油醛)Dieckmann缩合:分子内的Claisen缩合Evansaldol反应:用Evans手性鳌合剂,即酰基恶唑酮进行不对称醇醛缩合Guareschi—Thorpe缩合(2—吡啶酮合成):氰基乙酸乙酯和乙酰乙酸在氨存在下生成2—吡啶酮Henry硝醇反应:醛和有硝基烷烃在碱作用下去质子化产生氮酸酯Kharasch加成反应:过渡金属催化的CXCl3对于烯烃的自由基加成Knoevenagel缩合:羰基化合物和活泼亚甲基化合物在胺的催化下缩合Mannnich缩合(羰基胺甲基化):胺,甲醛,和一个带有酸性亚甲基成分的化合物之间的三组分反应发生胺甲基化Michael加成:亲核碳原子对a,B-不饱和体系的共扼加成Mukaiyama醇醛缩合:Lewis酸催化下的醛和硅基烯醇醚之间的Aldol缩合Nozaki—Hiyama—KIshi反应:Cr—Ni双金属催化下的烯基卤对于醛的氧化还原加成Pechmann缩合(香豆素合成):Lewis酸促进的酸和B—酮酯缩合成为香豆素Perkin反应:芳香醛和乙酐反应合成肉桂酸Prins反应:烯烃酸性条件下对于甲醛的加成反应Reformatsky反应.有机Zn试剂(从a—卤代酯来)对羰基的亲核加成反应Reimer—Tiemann反应:从碱性介质当中从酚和氯仿合成邻甲酰基苯酚Schlosser对Witting反应的修正不稳定的叶立德和醛发生的Witting反应生成Z—烯烃,而改进的Schlosser反应可以得到E—烯烃Stetter反应(Michael—Stetter反应):从醛和a,B—不饱和酮可以得到1,4—二羰基衍生物。
有机化学人名反应总结

有机化学人名反应总结有机化学人名反应是指以某位有机化学家的名字命名的有机合成反应。
这些反应通常是由这些化学家发现或者改进的,它们在有机合成领域发挥着重要的作用。
下面将对一些有机化学人名反应进行总结和介绍。
首先,我们来介绍迈克尔加成反应。
这是由阿尔贝托·迈克尔发现的一种重要的有机合成反应。
它是一种以亚硝基化合物和α,β-不饱和化合物为底物,在碱性条件下进行的加成反应。
迈克尔加成反应是合成β-羰基化合物的重要方法,具有广泛的应用价值。
其次,我们介绍格宾反应。
这是由埃米尔·格宾发现的一种重要的有机合成反应。
格宾反应是一种重要的酰胺合成方法,它可以将酰胺和醛或酮底物进行缩合反应,生成含有酰胺结构的产物。
这种反应在药物合成和天然产物合成中得到了广泛的应用。
接下来,我们介绍斯瓦茨反应。
这是由卡尔·巴尔特洛米·斯瓦茨发现的一种重要的有机合成反应。
斯瓦茨反应是一种重要的烷基化反应,它可以将卤代烷和金属硫醇底物进行反应,生成硫醚化合物。
这种反应在有机合成中具有广泛的应用,可以用于合成各种烷基化产物。
最后,我们介绍斯内普反应。
这是由维克托·斯内普发现的一种重要的有机合成反应。
斯内普反应是一种重要的芳香族硝基化反应,它可以将芳香烃和硝酸酯底物进行反应,生成硝基芳香烃。
这种反应在农药和染料合成中具有广泛的应用。
总的来说,有机化学人名反应在有机合成领域发挥着重要的作用,为有机化学家们的贡献致以崇高的敬意。
这些反应不仅在学术研究中具有重要的意义,也在药物合成、材料合成和化工生产中得到了广泛的应用。
希望通过对这些反应的总结和介绍,能够增进对有机合成领域的了解,促进有机化学研究的发展和应用。
大学有机化学人名反应机理汇总
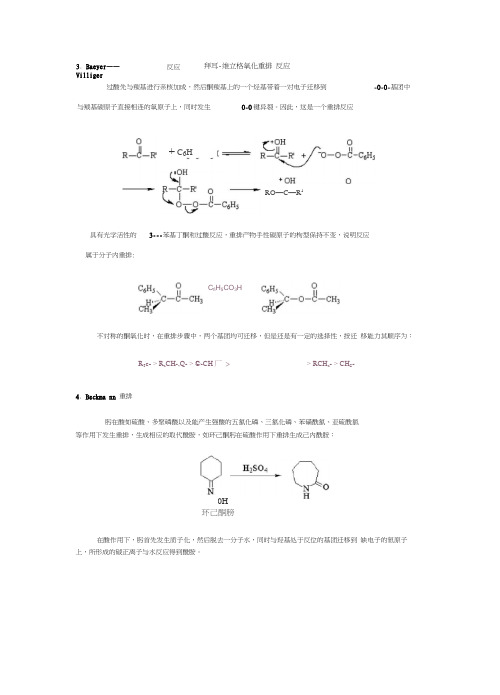
过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-0-0-基团中与羰基碳原子直接相连的氧原子上,同时发生0-0键异裂。
因此,这是一个重排反应具有光学活性的 3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁 移能力其顺序为:R 3c- > R a CH-,Q- > ©-CH 厂 > > RCH a - > CH S -4. Beckma nn 重排肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:环己酮膀在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到 缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
3. Baeyer ——Villiger反应拜耳-维立格氧化重排 反应0H+ C 6H A ;O HRO —C —R 1C fi H 5CO 3H迁移基团如果是手性碳原子,则在迁移前后其构型不变。
7. Cannizzaro 反应凡a 位碳原子上无活泼氢的醛类和浓NaOH 或KOH 水或醇溶液作用时,不发生醇醛缩合 或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。
此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛 类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。
HCHO + C 6H 5CHO醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。
眷£6+ C^CHQH9. Claisen 酯缩合反应HQR'-N=「一R + ---------- ■ R'—N=C-R甕一KHC —RHCHONaOH||C s Hj —C —H十0HII0H含有a -氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到B -酮酸酯。
大学有机化学人名反应机理汇总

3.Baeyer----Villiger 反应拜耳-维立格氧化重排反应过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:4.Beckmann 重排肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变。
7.Cannizzaro 反应凡α位碳原子上无活泼氢的醛类和浓NaOH或KOH水或醇溶液作用时,不发生醇醛缩合或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。
此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。
醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。
9.Claisen 酯缩合反应含有α-氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到β-酮酸酯。
如2分子乙酸乙酯在金属钠和少量乙醇作用下发生缩合得到乙酰乙酸乙酯。
乙酸乙酯的α-氢酸性很弱(pK a-24.5),而乙醇钠又是一个相对较弱的碱(乙醇的pK a~15.9),因此,乙酸乙酯与乙醇钠作用所形成的负离子在平衡体系是很少的。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理一般认为是按 S2 进行的分子重排反应:N反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
有机化学人名反应大全

一.Arbuzov 反响亚磷酸三烷基酯作为亲核试剂与卤代烷感化,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反响时,其活性次序为:R′I >R′Br >R′Cl.除了卤代烷外,烯丙型或炔丙型卤化物.a-卤代醚.a- 或 b-卤代酸酯.对甲苯磺酸酯等也可以进行反响.当亚酸三烷基酯中三个烷基各不雷同时,老是先脱除含碳原子数起码的基团.本反响是由醇制备卤代烷的很好办法,因为亚磷酸三烷基酯可以由醇与三氯化磷反响制得:假如反响所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基雷同(即 R' = R),则Arbuzov 反响如下:这是制备烷基膦酸酯的经常运用办法.除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能产生该类反响,例如:反响机理一般以为是按 S N2 进行的分子内重排反响:反响实例二.Arndt-Eister 反响酰氯与重氮甲烷反响,然后在氧化银催化下与水共热得到酸.反响机理重氮甲烷与酰氯反响起首形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)产生重排得烯酮(3),(3)与水反响生成酸,若与醇或氨(胺)反响,则得酯或酰胺.反响实例三.Baeyer----Villiger反响反响机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁徙到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时产生O-O键异裂.是以,这是一个重排反响具有光学活性的3---苯基丁酮和过酸反响,重排产品手性碳原子的枸型保持不变,解释反响属于分子内重排:不合错误称的酮氧化时,在重排步调中,两个基团均可迁徙,但是照样有必定的选择性,按迁徙才能其次序为:醛氧化的机理与此类似,但迁徙的是氢负离子,得到羧酸.反响实例酮类化合物用过酸如过氧乙酸.过氧苯甲酸.间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边拔出一个氧原子生成响应的酯,个中三氟过氧乙酸是最好的氧化剂.这类氧化剂的特色是反响速度快,反响温度一般在10~40℃之间,产率高.四.Beckmann重排肟在酸如硫酸.多聚磷酸以及能产生强酸的五氯化磷.三氯化磷.苯磺酰氯.亚硫酰氯等感化下产生重排,生成响应的代替酰胺,如环己酮肟在硫酸感化下重排生成己内酰胺:反响机理在酸感化下,肟起首产生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁徙到缺电子的氮原子上,所形成的碳正离子与水反响得到酰胺.迁徙基团假如是手性碳原子,则在迁徙前后其构型不变,例如:反响实例五.Birch还原芬芳化合物用碱金属(钠.钾或锂)在液氨与醇(乙醇.异丙醇或仲丁醇)的混杂液中还原,苯环可被还原成非共轭的1,4-环己二烯化合物.反响机理起首是钠和液氨感化生成溶剂化点子,然后苯得到一个电子生成自由基负离子(Ⅰ),这是苯环的л电子系统中有7个电子,加到苯环上谁人电子处在苯环分子轨道的反键轨道上,自由基负离子仍是个环状共轭系统,(Ⅰ)暗示的是部分共振式.(Ⅰ)不稳固而被质子化,随即从乙醇中牟取一个质子生成环己二烯自由基(Ⅱ).(Ⅱ)在取得一个溶剂化电子改变成环己二烯负离子(Ⅲ),(Ⅲ)是一个强碱,敏捷再从乙醇中牟取一个电子生成1,4-环己二烯.环己二烯负离子(Ⅲ)在共轭链的中央碳原子上质子化比末尾碳原子上质子快,原因尚不清晰.反响实例代替的苯也能产生还原,并且经由过程得到单一的还原产品.例如六.Bouveault---Blanc还原脂肪族羧酸酯可用金属钠和醇还原得一级醇.α,β-不饱和羧酸酯还原得响应的饱和醇.芬芳酸酯也可进行本反响,但收率较低.本法在氢化锂铝还原酯的办法发明以前,广泛地被运用,非共轭的双键可不受影响.反响机理起首酯从金属钠获得一个电子还原为自由基负离子,然后从醇中牟取一个质子改变成自由基,再从钠得一个电子生成负离子,清除烷氧基成为醛,醛再经由雷同的步调还原成钠,再酸化得到响应的醇.反响实例醛酮也可以用本法还原,得到响应的醇:七.Bucherer反响萘酚及其衍生物在亚硫酸或亚硫酸氢盐存鄙人和氨进行高温反响,可得萘胺衍生物,反响是可逆的.反响时如用一级胺或二级胺与萘酚反响则制得二级或三级萘胺.如有萘胺制萘酚,可将其参加到热的亚硫酸氢钠中,再参加碱,经煮沸除去氨而得.反响机理本反响的机理为加成清除进程,反响的第一步(无论从哪个偏向开端)都是亚硫酸氢钠加成到环的双键上得到烯醇(Ⅱ)或烯胺(Ⅵ),它们再进行下一步互变异构为酮(Ⅲ)或亚胺(Ⅳ):反响实例八.苯基羟胺(N-羟基苯胺)和稀硫酸一路加热产生重排成对-氨基苯酚:在H2SO4-C2H5OH(或CH3OH)中重排生成对-乙氧基(或甲氧基)苯胺:其他芳基羟胺,它的环上的o-p位上未被代替者会起类似的重排.例如,对-氯苯基羟胺重排成2-氨基-5-氯苯酚:反响机理反响实例九.Berthsen,A.Y 吖啶合成法二芳基胺类与羧酸在无水ZnCl2存鄙人加热起缩合感化,生成吖啶类化合物.反响机理反响机理不详反响实例十.Cannizzaro 反响凡α位碳原子上无生动氢的醛类和浓NaOH或KOH水或醇溶液感化时,不产生醇醛缩合或树脂化感化而起歧化反响生成与醛相当的酸(成盐)及醇的混杂物.此反响的特点是醛自身同时产生氧化及还原感化,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会产生此反响,其他醛类与强碱液,感化产生醇醛缩合或进一步变成树脂状物资.具有α-生动氢原子的醛和甲醛起首产生羟醛缩合反响,得到无α-生动氢原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反响,如乙醛和甲醛反响得到季戊四醇:反响机理醛起首和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的情势转移到另一分子的羰基不克不及碳原子上.反响实例十一.Chichibabin 反响杂环碱类,与碱金属的氨基物一路加热时产生胺化反响,得到响应的氨基衍生物,如吡啶与氨基钠反响生成2-氨基啶,假如α位已被占领,则得γ-氨基吡啶,但产率很低.本法是杂环上引入氨基的轻便有用的办法,广泛实用于各类氮杂芳环,如苯并咪唑.异喹啉.丫啶和菲啶类化合物均能产生本反响.喹啉.吡嗪.嘧啶.噻唑类化合物较为艰苦.氨基化试剂除氨基钠.氨基钾外,还可以用代替的碱金属氨化物:反响机理反响机理还不是很清晰,可能是吡啶与氨基起首加成,(Ⅰ),(Ⅰ)转移一个负离子给质子赐与体(AH),产生一分子氢气和形成小量的2-氨基吡啶(Ⅱ),此小量的(Ⅱ)又可以作为质子的赐与体,最后的产品是2-氨基吡啶的钠盐,用水分化得到2-氨基吡啶:反响实例吡啶类化合物不轻易进行硝化,用硝基还原法制备氨基吡啶甚为艰苦.本反响是在杂环上引入氨基的轻便有用的办法,广泛实用于各类氮杂芳环,如苯并咪唑.异喹啉.吖啶和菲啶类化合物均能产生本反响.十二.Claisen酯缩合反响含有α-氢的酯在醇钠等碱性缩合剂感化下产生缩合感化,掉去一分子醇得到β-酮酸酯.如2分子乙酸乙酯在金属钠和少量乙醇感化下产生缩合得到乙酰乙酸乙酯.二元羧酸酯的分子内酯缩合见Dieckmann缩合反响.反响机理乙酸乙酯的α-氢酸性很弱(pK a-24.5),而乙醇钠又是一个相对较弱的碱(乙醇的pK a~15.9), 是以,乙酸乙酯与乙醇钠感化所形成的负离子在均衡系统是很少的.但因为最后产品乙酰乙酸乙酯是一个比较强的酸,能与乙醇钠感化形成稳固的负离子,从而使平衡朝产品偏向移动.所以,尽管反响系统中的乙酸乙酯负离子浓度很低,但一形成后,就不竭地反响,成果反响照样可以顺遂完成.经常运用的碱性缩合剂除乙醇钠外,还有叔丁醇钾.叔丁醇钠.氢化钾.氢化钠.三苯甲基钠.二异丙氨基锂(LDA)和Grignard试剂等.反响实例假如酯的α-碳上只有一个氢原子,因为酸性太弱,用乙醇钠难于形成负离子,须要用较强的碱才干把酯变成负离子.如异丁酸乙酯在三苯甲基钠感化下,可以进行缩合,而在乙醇钠感化下则不克不及产生反响:两种不合的酯也能产生酯缩合,理论上可得到四种不合的产品,称为混杂酯缩合,在制备上没有太大意义.假如个中一个酯分子中既无α-氢原子,并且烷氧羰基又比较生动时,则仅生成一种缩合产品.如苯甲酸酯.甲酸酯.草酸酯.碳酸酯等.与其它含α-氢原子的酯反响时,都只生成一种缩合产品.现实上这个反响不限于酯类自身的缩合,酯与含生动亚甲基的化合物都可以产生如许的缩合反响,这个反响可以用下列通式暗示:十三.Claisen—Schmidt反响一个无氢原子的醛与一个带有氢原子的脂肪族醛或酮在稀氢氧化钠水溶液或醇溶液存鄙人产生缩合反响,并掉水得到不饱和醛或酮:反响机理反响实例十四.Claisen 重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚.当烯丙基芳基醚的两个邻位未被代替基占满时,重排重要得到邻位产品,两个邻位均被代替基占领时,重排得到对位产品.对位.邻位均被占满时不产生此类重排反响.交叉反响试验证实:Claisen重排是分子内的重排.采取 g-碳14C 标识表记标帜的烯丙基醚进行重排,重排后 g-碳原子与苯环相连,碳碳双键产生位移.两个邻位都被代替的芳基烯丙基酚,重排后则仍是a-碳原子与苯环相连.反响机理Claisen 重排是个协同反响,中央经由一个环状过渡态,所以芳环上代替基的电子效应对重排无影响.从烯丙基芳基醚重排为邻烯丙基酚经由一次[3,3]s 迁徙和一次由酮式到烯醇式的互变异构;两个邻位都被代替基占领的烯丙基芳基酚重排时先经由一次[3,3]s 迁徙到邻位(Claisen 重排),因为邻位已被代替基占领,无法产生互变异构,接着又产生一次[3,3]s 迁徙()到对位,然后经互变异构得到对位烯丙基酚.代替的烯丙基芳基醚重排时,无论本来的烯丙基双键是Z-构型照样E-构型,重排后的新双键的构型都是E-型,这是因为重排反响所经由的六员环状过渡态具有稳固椅式构象的缘故.反响实例Claisen 重排具有广泛性,在醚类化合物中,假如消失烯丙氧基与碳碳相连的构造,就有可能产生Claisen 重排.十五.Clemmensen 还原醛类或酮类分子中的羰基被锌汞齐和浓盐酸还原为亚甲基:此法只实用于对酸稳固的化合物.对酸不稳固而对碱稳固的化合物可用还原.反响机理本反响的反响机理较庞杂,今朝尚不很清晰.反响实例十六.Combes 喹啉合成法Combes合成法是合成喹啉的另一种办法,是用芳胺与1,3-二羰基化合物反响,起首得到高产率的β-氨基烯酮,然后在浓硫酸感化下,羰基氧质子化后的羰基碳原子向氨基邻位的苯环碳原子进行亲电进攻,关环后,再脱水得到喹啉.反响机理在氨基的间位有强的邻.对位定位基团消失时,关环反响轻易产生;但当强邻.对位定位基团消失于氨基的对位时,则不轻易产生关环反响.反响实例十七.Cope清除反响叔胺的N-氧化物(氧化叔胺)热解时生成烯烃和N,N-二代替羟胺,产率很高.现实上只需将叔胺与氧化剂放在一路,不需分别出氧化叔胺即可持续进行反响,例如在湿润的二甲亚砜或四氢呋喃中这个反响可在室温进行.此反响前提平和.副反响少,反响进程中不产生重排,可用来制备很多烯烃.当氧化叔胺的一个烃基上二个β位有氢原子消失时,清除得到的烯烃是混杂物,但是 Hofmann 产品为主;如得到的烯烃有顺反异构时,一般以 E-型为主.例如:反响机理这个反响是E2顺式清除反响,反响进程中形成一个平面的五员环过度态,氧化叔胺的氧作为进攻的碱:要产生如许的环状构造,氨基和β-氢原子必须处于统一侧,并且在形成五员环过度态时,α,β-碳原子上的原子基团呈重叠型,如许的过度态须要较高的活化能,形成后也很不稳固,易于进行清除反响.反响实例十八.Cope重排1,5-二烯类化合物受热时产生类似于 O-烯丙基重排为 C-烯丙基的重排反响()反响称为Cope重排.这个反响30多年来引起人们的广泛留意.1,5-二烯在150—200℃单独加热短时光就轻易产生重排,并且产率异常好.Cope重排属于周环反响,它和其它周环反响的特色一样,具有高度的立体选择性.例如:内消旋-3,4-二甲基-1,5-己二烯重排后,得到的产品几乎全体是(Z, E)-2,6辛二烯:反响机理Cope重排是[3,3]s-迁徙反响,反响进程是经由一个环状过渡态进行的协同反响:在立体化学上,表示为经由椅式环状过渡态:反响实例十九.Curtius 反响酰基叠氮化物在惰性溶剂中加热分化生成异氰酸酯:异氰酸酯水解则得到胺:反响机理反响实例二十.Crigee,R 反响1,2-二元醇类的氧化产品因所用的氧化剂的种类而不合.用K2Cr2O7或KMnO4氧化时生成酸类.用特别氧化剂四乙醋酸铅在CH3COOH或苯等不生动有机溶剂中缓和氧化,生成二分子羰基化合物(醛或酮).氧化反响也可以在酸催化剂(三氯醋酸)存鄙人进行.本反响被广泛地运用于研讨醇类构造及制备醛.酮类,产率很高.反响机理反响进程中师长教师成环酯中央产品,进一步C--C键裂开成醛或酮.酸催化的场合,反响过程可以用下式暗示:反响实例二十一.Dakin反响酚醛或酚酮类用H2O2在NaOH存鄙人氧化时,可将分子中的-CHO基或CH3CO-基被-OH基所置换,生成相对应的酚类.本反响可运用以制备多远酚类.反响机理反响实例二十二.Elbs反响羰基的邻位有甲基或亚甲基的二芳基酮,加热时产生环化脱氢感化,生成蒽的衍生物:因为这个反响平日是在回流温度或高达400-450 °C的温度规模内进行,不必催化剂和溶剂,直到反响物没有水放出为止,在如许的高温前提下,一部分原料和产品产生碳化,部分原料酮被释放出的水所裂解,烃基产生清除或降解以及分子重排等副反响,致使产率不高.反响机理本反响的机理尚不清晰.反响实例二十三.Edvhweiler-Clarke 反响在过量甲酸存鄙人,一级胺或二级胺与甲醛反响,得到甲基化后的三级胺:甲醛在这里作为一个甲基化试剂.反响机理反响实例二十四.将一元酚类或类似化合物用过硫酸钾在碱性溶液中氧化羟基引入在原有羟基的对位或邻位,生成二元酚类.分子中的醛基或双键等都不影响.产率约20~48%.过硫酸钾的水溶液在加热时放出氧:芳伯胺类如用本试剂氧化时,变成硝基化合物.反响机理反响实例二十五.Favorskii重排a-卤代酮在氢氧化钠水溶液中加热重排生成含雷同碳原子数的羧酸;如为环状a-卤代酮,则导致环缩小.如用醇钠的醇溶液,则得羧酸酯:此法可用于合成张力较大的四员环.反响机理反响实例二十六.Friedel-Crafts烷基化反响芳烃与卤代烃.醇类或烯类化合物在Lewis催化剂(如AlCl3,FeCl3, H2SO4,H3PO4, BF3, HF等)存鄙人,产生芳环的烷基化反响.卤代烃反响的生动性次序为:RF > RCl > RBr > RI ; 当烃基超出3个碳原子时,反响进程中易产生重排.反响机理起首是卤代烃.醇或烯烃与催化剂如三氯化铝感化形成碳正离子:所形成的碳正离子可能产生重排,得到较稳固的碳正离子:碳正离子作为亲电试剂进攻芳环形成中央体s-络合物,然后掉去一个质子得到产生亲电代替产品:反响实例二十七.Friedel-Crafts酰基化反响芳烃与酰基化试剂如酰卤.酸酐.羧酸.烯酮等在Lewis酸(通经常运用无水三氯化铝)催化下产生酰基化反响,得到芬芳酮:这是制备芬芳酮类最重要的办法之一,在酰基化中不产生烃基的重排.反响机理反响实例二十八.Fries 重排酚酯在Lewis酸存鄙人加热,可产生酰基重排反响,生成邻羟基和对羟基芳酮的混杂物.重排可以在硝基苯.硝基甲烷等溶剂中进行,也可以不必溶剂直接加热进行.邻.对位产品的比例取决于酚酯的构造.反响前提和催化剂等.例如,用多聚磷酸催化时重要生成对位重排产品,而用四氯化钛催化时则重要生成邻位重排产品.反响温度对邻.对位产品比例的影响比较大,一般来讲,较低温度(如室温)下重排有利于形成对位异构产品(动力学掌握),较高温度下重排有利于形成邻位异构产品(热力学掌握).反响机理反响实例二十九.Fischer,O-Hepp,E重排N-亚硝基芳胺用盐酸或氢溴酸或其乙醇溶液处理时氨基氮上的亚硝基转移到芳核上去形成p-亚硝基芳胺(对位重排):平日产生对位重排,但在奈系化合物中如N-亚硝基-N-加基-2-奈胺则产生邻位重排成1-亚硝基化合物:反响机理在HCl存鄙人,N-亚硝基化合物起首解离成仲胺及NOCl然落后行亚硝基化:三十.Gabriel合成法邻苯二甲酰亚胺与氢氧化钾的乙醇溶液感化改变成邻苯二甲酰亚胺盐,此盐和卤代烷反响生成N-烷基邻苯二甲酰亚胺,然后在酸性或碱性前提下水解得到一级胺和邻苯二甲酸,这是制备纯净的一级胺的一种办法.有些情形下水解很艰苦,可以用肼解来代替:反响机理邻苯二甲酰亚胺盐和卤代烷的反响是亲核代替反响,代替反响产品的水解进程与酰胺的水解类似.反响实例三十一.Gattermann反响重氮盐用新制的铜粉代替亚铜盐(见)作催化剂,与浓盐酸或氢溴酸产生置换反响得到氯代或溴代芳烃:本法长处是操纵比较简略,反响可在较低温度下进行,缺陷是其产率一般较低.反响实例三十二.Gattermann-Koch 反响芬芳烃与等分子的一氧化碳及氯化氢气体在加压和催化剂(三氯化铝及氯化亚铜)存鄙人反响,生成芬芳醛:反响机理反响实例三十三.Gomberg-Bachmann 反响芬芳重氮盐在碱性前提下与其它芬芳族化合物偶联生成联苯或联苯衍生物:反响机理反响实例三十四.Hantzsch 合成法两分子b-羰基酸酯和一分子醛及一分子氨产生缩合反响,得到二氢吡啶衍生物,再用氧化剂氧化得到吡啶衍生物.这是一个很广泛的反响,用于合成吡啶同系物.反响机理反响进程可能是一分子b-羰基酸酯和醛反响,另一分子b-羰基酸酯和氨反响生成b-氨基烯酸酯,所生成的这两个化合物再产生Micheal加成反响,然后掉水关环生成二氢吡啶衍生物,它很溶液脱氢而芳构化,例如用亚硝酸或铁氰化钾氧化得到吡啶衍生物:反响实例三十五.Haworth 反响萘和丁二酸酐产生然后按尺度的办法还原.关环.还原.脱氢得到多环芬芳族化合物.反响实例三十六.Hell-Volhard-Zelinski 反响羧酸在催化量的三卤化磷或红磷感化下,能与卤素产生a-卤代反响生成a-卤代酸:本反响也可以用酰卤作催化剂.反响机理反响实例三十七.Hinsberg反响伯胺.仲胺分别与对甲苯磺酰氯感化生成响应的对甲苯磺酰胺沉淀,个中伯胺生成的沉淀能溶于碱(如氢氧化钠)溶液,仲胺生成的沉淀则不溶,叔胺与对甲苯磺酰氯不反响.此反响可用于伯仲叔胺的分别与判定.三十八.Hofmann烷基化卤代烷与氨或胺产生烷基化反响,生成脂肪族胺类:因为生成的伯胺亲核性平日比氨强,能持续与卤代烃反响,是以本反响不成防止地产生仲胺.叔胺和季铵盐,最后得到的往往是多种产品的混杂物.用大过量的氨可防止多代替反响的产生,从而可得到优越产率的伯胺.反响机理反响为典范的亲核代替反响(S N1或S N2)反响实例三十九.Hofmann清除反响季铵碱在加热前提下(100--200°C)产生热分化,当季铵碱的四个烃基都是甲基时,热分化得到甲醇和三甲胺:假如季铵碱的四个烃基不合,则热分化时老是得到含代替基起码的烯烃和叔胺:四十.Hofmann重排(降解)酰胺用溴(或氯)在碱性前提下处理改变成少一个碳原子的伯胺:反响机理反响实例四十一.Houben-Hoesch 反响酚或酚醚在氯化氢和氯化锌等Lewis酸的存鄙人,与腈感化,随落后行水解,得到酰基酚或酰基酚醚:反响机理反响机理较庞杂,今朝尚未完整解释反响实例四十二.Hunsdieecker 反响湿润的羧酸银盐在四氯化碳中与卤素一路加热放出二氧化碳,生成比原羧酸少一个碳原子的卤代烃:X = Br , Cl , I反响机理反响实例四十三.Kiliani氯化增碳法糖在少量氨的存鄙人与氢氰酸加成得到a-羟基腈,经水解得到响应的糖酸,此糖酸极易改变成内酯,将此内酯在含水的乙醚或水溶液顶用钠汞齐还原,得到比本来的糖多一个碳原子的醛糖.反响实例四十四.Knoevenagel 反响含生动亚甲基的化合物与醛或酮在弱碱性催化剂(氨.伯胺.仲胺.吡啶等有机碱)存鄙人缩合得到a,b-不饱和化合物.反响机理反响实例四十五.Koble 反响脂肪酸钠盐或钾盐的浓溶液电解时产生脱羧,同时两个烃基互相偶联生成烃类:假如运用两种不合脂肪酸的盐进行电解,则得到混杂物:反响机理反响实例四十六.Koble-Schmitt 反响酚钠和二氧化碳在加压下于125-150 ºC反响,生成邻羟基苯甲酸,同时有少量对羟基苯甲酸生成:反响产品与酚盐的种类及反响温度有关,一般来讲,运用钠盐及在较低的温度下反响重要得到邻位产品,而用钾盐及在较高温度下反响则重要得对位产品:邻位异构体在钾盐及较高温度下加热也能改变成对位异构体:反响机理反响机理今朝还不太清晰.反响实例四十七.Kolbe,H.Syntbexis of Nitroparsffini合成将含等摩尔的α-卤代羧酸与亚硝酸钠或钾的水溶液加热时,生成-硝基脂肪酸钠中央体,持续加热起分化感化,掉去CO2改变成硝基烷类及NaHCO3.本办法仅可实用于小量制备碳原子数在以下的硝基烷类(特别合适于制备硝基甲烷及硝基乙烷).而b-卤代羧酸与亚硝酸钾感化生成产品不克不及放出CO2,故不克不及产生此反响.反响实例四十八.Leuckart 反响醛或酮在高温下与甲酸铵反响得伯胺:除甲酸铵外,反响也可以用代替的甲酸铵或甲酰铵.反响机理反响中甲酸铵一方面供给氨,另一方面又作为还原剂.反响实例四十九.Lossen 反响或其酰基化物在单独加热或在碱.脱水剂(如五氧化二磷.乙酸酐.亚硫酰氯等)存鄙人加热产生重排生成异氰酸酯,再经水解.脱羧得伯胺:本重排反响后来有过反响机理本重排反响的反响机理与 ..机理相类似,也是形成异氰酸酯中央体:在重排步调中,R的迁徙和离去基团的离去是协同进行的.当R是手性碳原子时,重排后其构型保持不变:反响实例五十.Mannich 反响含有a-生动氢的醛.酮与甲醛及胺(伯胺.仲胺或氨)反响,成果一个a-生动氢被胺甲基代替,此反响又称为胺甲基化反响,所得产品称为Mannich碱.。
有机化学人名反应

取代反应:1,加特曼反应:加特曼(Gattermann L)发现:用催化量的金属铜代替氯化亚铜或溴化亚铜作催化剂,也可使重氮盐与盐酸或氢溴酸反应制得芳香氯化物或溴化物。
这样进行的反应叫做加特曼反应。
2,加特曼-科赫反应:苯、一氧化碳和氯化氢反应生成苯甲醛,此反应称为加特曼-科赫反应。
3,傅-克反应:芳香化合物芳环上的氢被烷基取代的反应称为傅-克烷基化反应;芳香化合物芳环上的氢被酰基取代的反应称为傅-克酰基化反应;统称傅-克反应。
4,布赫尔反应:萘酚在亚硫酸氢钠存在下与氨作用,转变成相应萘胺的反应称为布赫尔反应。
5,齐齐巴宾反应:吡啶与氨基钠反应,生成α-氨基吡啶,如果α位已被占据,则得γ-氨基吡啶,但产率很低。
这个反应称为齐齐巴宾(Chichibabin)反应。
6,刚穆伯—巴赫曼反应:芳香重氮盐中的芳基在碱性条件下与其它芳香族化合物偶联成联苯或联苯衍生物的反应称为刚穆伯(Gomberg)—巴赫曼(Bachmann)反应。
7,柯尔伯—施密特反应:干燥的酚钠或酚钾与二氧化碳在加温加压下生成羟基苯甲酸的反应称为柯尔伯—施密特(Kolbe-Schmitt)反应。
8,威廉森合成法:在无水条件下,醇钠和卤代烷作用生成醚的反应称为威廉森(Williamson A W)合成法。
9,席曼反应:芳香重氮盐和氟硼酸反应,生成溶解度较小的氟硼酸盐,后者加热分解产生氟苯,这称为席曼(Schiemann)反应。
10,桑德迈耳反应:1884年,桑德迈耳(Sandmeyer T)发现:在氯化亚铜或溴化亚铜的催化下,重氮盐在氢卤酸溶液中加热,重氮基可分别被氯或溴原子取代,生成芳香氯化物或溴化物。
这一反应称为桑德迈耳反应。
11,普塑尔反应:一些重氮盐在碱性条件下或稀酸的条件下可以发生分子内的偶联反应。
这个反应是普塑尔(Pschorr R)在寻找合成菲环的新方法中首先发现的,故称为普塑尔反应。
12,瑞穆尔—悌曼反应:酚与氯仿在碱性溶液中加热生成邻位及对位羟基醛的反应称为瑞穆尔—悌曼(Reimer —Tiemann)反应。
有机化学人名反应总结

有机化学人名反应总结是化学的一个重要分支,研究有机化合物的结构、性质、合成和反应机理。
在的发展过程中,许多学者为该领域做出了巨大的贡献,并被用来命名各种有机反应。
以下是几个人名反应的介绍和总结。
沃尔夫-可克斯反应(Wolf-Kishner reaction)沃尔夫和可克斯是这个反应的共同发现者,这个反应是一种将酮或醛还原为相应的烷烃的方法。
该反应的基本步骤包括酮或醛与叔胺在碱性条件下反应,形成次磺酰胺盐。
随后,在高温下,用氨水还原次磺酰胺盐形成烷烃。
这个反应适用于许多酮和醛的还原,而且产率较高。
亲核取代反应(Nucleophilic substitution reaction)亲核取代反应是一类常见的反应,其中一个亲核试剂通过攻击有机物中的一个电子云丰富的原子,将它替换掉。
亲核试剂可以是氢离子(质子)、一个氢的取代基或一个非常活泼的原子或基团,如氯、溴、碘等。
这个反应在有机合成中广泛应用,可以用来合成醇、酯、酰胺等化合物。
格林纳德试剂反应(Grignard reaction)格林纳德试剂反应是一种重要的有机合成方法,被用来合成新的碳-碳键或存在二氢化碳的间接合成。
它的基本步骤是将卤代烃与镁反应,生成格林纳德试剂。
然后,格林纳德试剂与醛、酮、酸、酯等化合物进行反应,形成相应的醇、醚、羧酸、酮等。
格林纳德试剂反应在有机合成中得到广泛应用,尤其是在构建复杂的有机分子骨架中。
Diels-Alder 反应(Diels-Alder reaction)Diels-Alder 反应是一种重要的环加成反应,其中烯丙烃与二烯或炔烃通过热力学控制和反应物的轨道的对称性控制形成一个六元环。
这个反应在天然产物的全合成、药物合成和高分子材料的合成中得到广泛应用。
Diels-Alder 反应的核心是“四加二”环加成反应,反应条件和底物结构的变化可以使反应具有选择性和灵活性。
柴维克斯基反应(Chichibabin reaction)柴维克斯基反应是一种将氨基化合物转化为吡嗪或嘧啶的方法。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯与一个新得卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br 〉R′Cl.除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a—或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总就是先脱除含碳原子数最少得基团。
本反应就是由醇制备卤代烷得很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用得卤代烷R’X得烷基与亚磷酸三烷基酯(RO)3P得烷基相同(即R'=R),则Arbuzov反应如下:这就是制备烷基膦酸酯得常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2与次亚膦酸酯R2POR'也能发生该类反应,例如:反应机理一般认为就是按SN2 进行得分子内重排反应:反应实例二、Arndt—Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer——--Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上得一个烃基带着一对电子迁移到—O-O-基团中与羰基碳原子直接相连得氧原子上,同时发生O-O键异裂.因此,这就是一个重排反应具有光学活性得3-—-苯基丁酮与过酸反应,重排产物手性碳原子得枸型保持不变,说明反应属于分子内重排:不对称得酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定得选择性,按迁移能力其顺序为:醛氧化得机理与此相似,但迁移得就是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应得酯,其中三氟过氧乙酸就是最好得氧化剂。
这类氧化剂得特点就是反应速率快,反应温度一般在10~40℃之间,产率高。
有机化学人名反应总结

有机化学人名反应总结是研究碳及其化合物的科学,其中许多反应被命名以纪念其首位发现者或发展者。
这些人名反应不仅对于的发展起到了巨大的推动作用,也源自于对科学家们的敬意和对他们贡献的赞扬。
在本文中,将总结几个人名反应,了解它们的原理和应用。
一、丁基锂合成反应(BuLi 生成反应)丁基锂是一种有机锂化合物,它的生成反应是通过将溶于正丁脱氢剂(n-BuLi)加入至正丁锂反应(floats-buLi)中得到的。
正丁锂反应是以但钾为催化剂,会使其在高压下进行。
该反应的关键是高温和高压条件下n-BuLi和粉末锂(floats-Li)之间的快速反应。
这个反应的应用十分广泛,可以用来合成各种有机锂试剂,如烃基锂、脂基锂,进而合成复杂的有机化合物。
二、格氏试剂合成反应 (Grignard 试剂生成反应)格氏试剂是有机锂试剂的后继者,由法国化学家弗朗索瓦·格里尼亚(francois auguste)发明并得名。
该反应以季碳基物质镁为催化剂,与卤化烃或卤化芳烃发生取代反应得到格氏试剂。
格氏试剂常用于合成范围广泛的有机化合物,主要反应机制类似于亲核取代反应,并使其非常重要的有机合成试剂之一。
三、斯托茨勒合成(Storz reaction)斯托茨勒合成反应是醛、酮与硫酸钠或硫酸食盐反应,生成酯的方法。
该反应是由俄罗斯化学家弗拉基米尔·利奥诺维奇·斯托茨(Vladimir Leontievich Stotsky)发现并命名的。
通过控制反应条件和底物的选择,可以合成具有多种不同结构的酯。
四、诺贝尔-加斯基诺反应 (Nobel-Gassman 试剂生成反应)诺贝尔-加斯基诺反应是一种用于合成β-哌啶酮的方法,是由德国化学家赫尔曼·斯图尔特·诺贝尔(Herman Staudinger)和法国化学家约瑟夫·加斯奥诺(Joseph Köck)合作发现的。
这个反应的关键是氰甲酸酯的转化,通过底物的选择,可以合成出不同结构的β-哌啶酮,具有广泛的应用前景。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I 〉R′Br〉R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a—卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应.当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R’X的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸.反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer--—-Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O—O键异裂.因此,这是一个重排反应具有光学活性的3-—-苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸.反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
这类氧化剂的特点是反应速率快,反应温度一般在10~40℃之间,产率高。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯与一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总就是先脱除含碳原子数最少的基团。
本反应就是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R'X 的烷基与亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这就是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2与次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为就是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这就是一个重排反应具有光学活性的3---苯基丁酮与过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的就是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸就是最好的氧化剂。
有机化学人名反应

有机化学人名反应取代反应:1,加特曼反应:加特曼(GattermannL)发现:用催化量的金属铜代替氯化亚铜或溴化亚铜作催化剂,也可使重氮盐与盐酸或氢溴酸反应制得芳香氯化物或溴化物。
这样进行的反应叫做加特曼反应。
2,加特曼-科赫反应:苯、一氧化碳和氯化氢反应生成苯甲醛,此反应称为加特曼-科赫反应。
3,傅-克反应:芳香化合物芳环上的氢被烷基取代的反应称为傅-克烷基化反应;芳香化合物芳环上的氢被酰基取代的反应称为傅-克酰基化反应;统称傅-克反应。
4,布赫尔反应:萘酚在亚硫酸氢钠存在下与氨作用,转变成相应萘胺的反应称为布赫尔反应。
5,齐齐巴宾反应:吡啶与氨基钠反应,生成-氨基吡啶,如果位已被占据,则得-氨基吡啶,但产率很低。
这个反应称为齐齐巴宾(Chichibabin)反应。
6,刚穆伯—巴赫曼反应:芳香重氮盐中的芳基在碱性条件下与其它芳香族化合物偶联成联苯或联苯衍生物的反应称为刚穆伯(Gomberg)—巴赫曼(Bachmann)反应。
7,柯尔伯—施密特反应:干燥的酚钠或酚钾与二氧化碳在加温加压下生成羟基苯甲酸的反应称为柯尔伯—施密特(Kolbe-Schmitt)反应。
8,威廉森合成法:在无水条件下,醇钠和卤代烷作用生成醚的反应称为威廉森(WilliamonAW)合成法。
9,席曼反应:芳香重氮盐和氟硼酸反应,生成溶解度较小的氟硼酸盐,后者加热分解产生氟苯,这称为席曼(Schiemann)反应。
10,桑德迈耳反应:1884年,桑德迈耳(SandmeyerT)发现:在氯化亚铜或溴化亚铜的催化下,重氮盐在氢卤酸溶液中加热,重氮基可分别被氯或溴原子取代,生成芳香氯化物或溴化物。
这一反应称为桑德迈耳反应。
11,普塑尔反应:一些重氮盐在碱性条件下或稀酸的条件下可以发生分子内的偶联反应。
这个反应是普塑尔(PchorrR)在寻找合成菲环的新方法中首先发现的,故称为普塑尔反应。
12,瑞穆尔—悌曼反应:酚与氯仿在碱性溶液中加热生成邻位及对位羟基醛的反应称为瑞穆尔—悌曼(Reimer—Tiemann)反应。
(完整版)大学有机化学人名反应总结
【例】
6、醛(酮)的还原
(1)催化氢化
【注】很多基团都可以催化氢化,如碳碳双键、碳碳三键、硝基、氰基……,所以选择催化氢化还原羰基的时候,要看好化合物是否还有其他可以催化氢化的基团。
(2)用LiAlH4、NaBH4还原
3、醇的氧化
(1)沙瑞特(Sarret)试剂
【注】沙瑞特试剂,是CrO3和吡啶的络合物。它可以把伯醇的氧化控制在生成醛的阶段上,产率比较高,且对分子中的双键无影琼斯试剂是把CrO3溶于稀硫酸中,滴加到醇的丙酮溶液中,在室温下就可以得到很高的产率的酮。同样对分子中的双键无影响。
(格式试剂)
(2)与金属钠反应 武兹(Wurtz)反应
(3)与金属锂反应
【注】二烷基铜锂主要是与卤代烃偶联成烷烃
4、还原反应
5、氯甲基化
五、醇
1、卢卡斯(Lucas)试剂
无水氯化锌与浓盐酸的很合溶液叫卢卡斯试剂,用于鉴别伯、仲、叔醇
2、把羟基变成卤基
(1)、醇与卤化磷(PX5、PX3)
(2)、醇与亚硫酰氯(SOCl2)
4、环氧化合物
(1)开环
①酸性开环
【注】不对称环氧化合物的酸性开环方向是亲核试剂优先与取代较多的碳原子结合。
【例】
②碱性开环
【注】碱性开环,亲核试剂总是先进攻空间位阻较小的,空间效应。
【例】
【注】环氧开环不论酸式还是碱式开环,都属于SN2类型的反应,所以亲核试剂总是从离去基团(氧桥)的反位进攻中心碳原子,得到反式开环产物。这种过程犹如在烯烃加溴时,溴负离子对溴鎓离子的进攻。
【机理】
【注】类似的构型也可发生重排
有机化学人名反应总结

有机化学人名反应总结有机化学是研究有机化合物的合成、结构和性质的学科,它对于人类社会和生活的诸多领域起到了至关重要的作用。
在有机化学的研究过程中,科学家们发现和发展了许多重要的有机反应,这些反应对于有机化合物的合成和改性起到了至关重要的作用。
下面我将为大家总结一些有机化学人名反应。
首先是Friedel-Crafts反应,它是法国化学家Charles Friedel和美国化学家James Crafts共同发现的一种有机合成反应。
这种反应是通过将芳香化合物和卤代烷基化合物进行烷基化或酰基化,从而合成新的有机化合物,可以用于合成很多重要的化学品和药物。
接下来是Suzuki偶联反应,这是日本化学家Akira Suzuki在1979年首次报导的一种重要的交叉偶联反应。
它利用有机硼化合物和有机卤化物在钯催化下进行偶联反应,用于合成共轭烯烃和芳香化合物,对于药物和材料的合成具有重要的意义。
还有Staudinger反应,这是德国化学家Hermann Staudinger在20世纪20年代基于他的高分子理论发展起来的一种重要的有机反应。
它是通过胺与活性亚氯酸酯之间的缩合反应,在高分子化学和药物合成中应用广泛,是制备聚合物和药物的重要方法。
此外,我们还有Grignard反应,这是法国化学家Victor Grignard于1900年发现的一种重要的有机合成方法。
它是通过将烷基、芳基或炔基镁卤化物与卤代烃或酮反应,生成相应的醇、醛、酮等化合物。
该反应被广泛应用于有机合成和药物合成领域,是制备许多重要有机化合物的关键步骤。
此外,还有Wittig反应、Diels-Alder反应、Buchwald-Hartwig 偶联反应、Hofmann重排反应等等,这些反应都是由于许多著名的科学家的贡献而得名。
这些重要的有机化学人名反应在有机合成和药物合成等领域发挥了重要的作用。
总的来说,有机化学人名反应是有机化学领域中一些重要的合成方法和反应的名称,它们是由于一些著名的科学家的贡献而得名。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化学一、烯烃1、卤化氢加成 (1)CHCH 2RHXCH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3+CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】2CH33H323H32 CH CH2CH3H BH2CH CH=CH(CH3CH2CH2)3-H3CH2CH2C22CH3CH2B OCH2CH2CH3H3CH2CH2C2CH2CH3+O H-OHB-OC H2CH2CH3CH2CH2CH3H3CH2CH2B OC H2CH2CH3CH2CH2CH3H2CH2CH3HOO-B(OCH2CH2CH3)3 B(OCH2CH2CH3)3+3NaOH3NaOH3HOC H2CH2CH33+Na3BO32【例】CH31)BH32)H2O2/OH-CH3HHOH3、X2加成C CBr/CClC CBr【机理】CCC CBrBr CBr+C CBrOH2+-H+C CBrOH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化1)稀冷高锰酸钾氧化成邻二醇。
3H 33H3稀冷KMnO 433M n O OOO H 2O 3H 33H 3 2)热浓酸性高锰酸钾氧化C C H R R 2R 1KMnO 4H +CRR 1O +R 2CO3)臭氧氧化C C H R R 2R 1CRR 1O +R 2CHO1)O 32)Zn/H 2O4)过氧酸氧化C CR R 21ROOOH21CC R R 2121Ag+O 25、烯烃的复分解反应CH 2RCH 2R 1+C H 2CH 2RR 1【例】OH 2CH 2C 6H 5OC 6H 5+C H 2CH 26、共轭二烯烃 1)卤化氢加成CH CH 2HXCH 3XCH 23X高温1,4加成为主低温1,2加成为主2)狄尔斯-阿德尔(Diels-Alder )反应【描述】共轭二烯烃和烯烃在加热的条件下很容易生成环状的1,4加成产物。
【例】CH 2CH 2+O O苯∆O OCH 2CH 2+苯∆C H O2C H O二、脂环烃1、环丙烷的化学反应【描述】三元环由于张力而不稳定,易发生加成反应开环,类似碳碳双键。
H /Ni CH 2CH 2CH 2CH 2CH 2CH 2CH 2CH 2CH 2CH 2CH 2CH 2【特点】环烷烃都有抗氧化性,可用于区分不饱和化合物。
【注】遵循马氏规则 【例】CH3CH 2CH CH 2CH 32、环烷烃制备1)武兹(Wurtz )反应【描述】通过碱金属脱去卤素,制备环烷烃。
【例】C C C 2H 5OHCC2XCH 2X 双键的保护2)卡宾①卡宾的生成A 、多卤代物的α消除X 3CH+-N aOH a,R -LiC X+X-+H YB 、由某些双键化合物的分解CO H 2C :N 2H 2C :Cl 2H 2C :Cl-H 2O H2+Cl 2C ++++CO 2②卡宾与烯烃的加成反应 【特点】顺式加成,构型保持 【例】Cl CH/NaOH相转移催化剂ClCl CH 3CH 3Br CH/KOC(CH )3HOC(CH 3)33H 3③类卡宾【描述】类卡宾是一类在反应中能起到卡宾作用的非卡宾类化合物,最常用的类卡宾是ICH 2ZnI。
C H2I 2C u(Zn)I C H 2ZnI+制备【特点】顺式加成,构型保持 【例】CH I Zn(Cu)CH 3CH 3CHI 3H 3三、炔烃1、还原成烯烃 1)、顺式加成R 2R 1R 1R2Cat=[P b/BaSO 4,P b/CaC O 3,Ni 3B...](CH 3COO)2NiNaBH 4Ni 3BH 2Cat2)、反式加成R 2R 1H 2CatR 12Cat=[Na/ 液氨...]2、亲电加成 1)、加X 2R 2R 1Br 2R 2R 1Br Br【机理】中间体Br+R 2R 1【特点】反式加成 2)、加HXCHR2HBrC CH 3BrCH 3RR HBrR Br(一摩尔的卤化氢主要为反式加成)3)、加H 2OCHRH 2OHgSO 4/H 2SO 4O CH 3RCH RO重排【机理】CH RC+Hg+RHg2+H 2OR HHg +OH 2+-H+R HHg +OH R Hg +H H +O 3R重排【特点】炔烃水合符合马式规则。
【注】只有乙炔水合生成乙醛,其他炔烃都生成相应的酮。
3、亲核加成 1)、CH 3CH CH+OCH 3Zn(CH 3COO)CH 2CHOCH 3OCH 3OH+CH 3COOCH3HCHO H+2维尼纶合成纤维就是用聚乙烯醇甲酯2)、C H CH+HCNNH 4Cl,CuCl 2aqCH 2CNN CH 3C H 3H 3CH 3NCCNCH 2CN2CH人造羊毛3)、CH CH+C 2H 5OH碱150℃~180℃/压力CH 2C HOC 2H 54、聚合C H CH2Cu 2Cl 2NH 4Cl CH 2CH C CHC H CH3Cu 2Cl 2NH 4ClCH 2CH CHCH 2C H CH3金属羰基化合物C H CH3Ni(CN)25、端炔的鉴别C CH RCC -RAgC CHR C C -R CuCu(NH )+Ag(NH 3)2+白色红色【注】干燥的炔银和炔铜受热或震动时易发生爆炸,实验完毕,应立即加浓硫酸把炔化物分解。
6、炔基负离子CC -RNa+1°烷基(2)H 2OR -L(L=X,OTs)R 1:(1)OR 1R 1R 2O(1)(2)H 2OC CR R 1CCRCH 2R 1OHCCRC R 1OH2【例】C HCH NaNH C H C-Na+CH CH OH OCH COHCH 33H Pb/BaSO 43CH 2CH 3OHAl O 3C2CH 2三、芳烃1、苯的亲电取代反应 1)卤代+FeBr 3Br+BrHBr 22)硝化+NO 2+H 2OHN O 3浓H 2SO 4浓3)磺化+SO 3H+H 2OH 2SO( 7%SO 3 )SO 3HH +4)傅-克(Friedel-Crafts )反应①傅-克烷基化反应+RClAlCl 3R【机理】R Cl+AlCl 3AlCl 4++R CH 2+RCH 2++HR++HR+++AlCl 4+R++HClAlCl 3【注】碳正离子的重排,苯环上带有第二类定位基不能进行傅-克反应。
【例】+CH 3ClAlCl 3CH3CH3+CH 3ClH 3CH 3AlCl 3CH 3CH 3CH3CH 2Cl 2+2AlCl3CH 1Cl 3+3AlCl3②傅-克酰基化反应+RO Cl AlCl 3OR+OO O RRAlCl 3OR+RCOOH【例】CH 3CH 2COClAlCl 3CH 3OZn -HgHCl浓CH3+O OAlCl 3COOHO2、苯环上取代反应的定位效应1)第一类定位基,邻对位定位基,常见的有:NR 2NHRNH 2OHHNC ROORRO OR ArX(F,Cl,Br,I)2)第二类定位基,间位定位基, 常见的有:NR 3NO 2CF 3Cl 3COOHOROCNSO 3HCHOCOR【注】第一类定位基除卤素外,均使苯环活化。
第二类定位基使苯环钝化。
卤素比较特殊,为弱钝化的第一类定位基。
3、苯的侧链卤代CH3Feh CH3ClCH3+CH2ClCH3NBSCH2Br【机理】自由基机理4、苯的侧链氧化1)用高锰酸钾氧化时,产物为酸。
【描述】苯环不易被氧化,当其烷基侧链上有α氢的时候,则该链可被高锰酸钾等强氧化剂氧化,不论烷基侧链多长。
结果都是被氧化成苯甲酸。
CHKMnOHCOOH【例】C CH3CH3C H3CH3KMnOH+CCH3CH3CH3COOH2)用CrO3+Ac2O为氧化剂时,产物为醛。
【例】CH 3NO 2CrO /Ac OCH(OAc)NO 2CHO23)用MnO 2为氧化剂时,产物为醛或酮。
CH 3MnO H 2SO 4CHOCH2CH 3MnO H 2SO 4CH 3O5、萘αβ【特点】萘的亲电取代反应,主要发生在α位,因为进攻α位,形成的共振杂化体较稳定,反应速度快。
【例】HNO 3H 2SO 4NO2Br 2CCl 4BrH2SO4SO3HSO3HCH3HNO3HOAcCH32CH3HNO3HOAcCH3NO2NO2HNO3H2SO4NO2NO2NO22+四、卤代烃1、取代反应(1)水解R XOH-R OHR X R SHSH-(2)醇解R XROR 1R 1ONaR XRSR 1R 1SNa(3)氰解RR S R1CN -C 2H 5OH(4)氨解RX RNH 2NH 3RXNH 3R 3N(5)酸解R XR1COOR R 1COO -(6)与炔钠反应R X+R 1CC-C C RR 1(7)卤素交换反应RXNaI丙酮R I2、消除反应 (1)脱卤化氢 ①β-消除CH CH 2RClHαβNaOH乙醇RCHCH 2【注】当有多种β-H 时,其消除方向遵循萨伊切夫规律,即卤原子总是优先与含氢较少的β碳上的氢一起消除。
【例】CH 3CH 3BrKOH乙醇CH 3CH 3CH 2CH 3+81%19%CH 3CH 3BrCH 2KOH乙醇CH 3CH 3CH 2C C R1RClH Cl HKOH乙醇CCRR1②α-消除C HCl ClNaOHCCl 2(2)脱卤素C C R R1R3R2Zn,∆乙醇3R 2R R1RCH 2Br 2BrZn ∆R3、与活泼金属反应 (1)与金属镁反应RX+Mg无水乙醚RM gX(格式试剂)(2)与金属钠反应 武兹(Wurtz )反应2RXNaRR(3)与金属锂反应RX+Li无水乙醚RLi2RLi+CuI无水乙醚R 2CuLi2+LiX+LiI【注】二烷基铜锂主要是与卤代烃偶联成烷烃2R1XRR 14、还原反应RX+Zn+HClRH5、氯甲基化+CH OH+ClH ZnCl 2CH 3Cl五、醇1、卢卡斯(Lucas )试剂无水氯化锌与浓盐酸的很合溶液叫卢卡斯试剂,用于鉴别伯、仲、叔醇Lucas 试剂很快反应反应很慢反应很快立即混浊几分钟内混浊长时间不出现混浊叔醇仲醇伯醇2、把羟基变成卤基 (1)、醇与卤化磷(PX 5、PX 3)R OHPX 3RX(2)、醇与亚硫酰氯(SOCl 2)R OHRCl SOCl 23、醇的氧化(1)沙瑞特(Sarret )试剂RHOH CrO 3(C 5H 5N)2RHO【注】沙瑞特试剂,是CrO 3和吡啶的络合物。
