急性慢性和亚慢性毒性实验
毒理学——4

24
3.经皮肤染毒 脱毛:化学法脱毛或机械法脱毛 (体表面积的10%)。 染毒:局部涂敷受试物或大鼠、 小鼠浸尾法染毒。
25
4.经注射途径染毒
静脉注射或滴注;
腹腔注射; 肌肉注射; 皮下注射; 皮内注射; 椎管内注射
究和将研究结果外推到人提供依据。
58
(三)亚慢性毒性试验方法的要点
1. 实验动物的选择
(1) 物种和品系 实验动物对受试物的生物转化、生理生 化、毒性反应与人类相当或相似。
两种实验动物,啮齿类和非啮齿类。
59
(2) 性别、年龄和动物数 两种性别,每组雌雄各半;
13
适宜容积染毒
① 经口:20ml/kg(空腹动物); ② 经皮:2ml/kg; ③ 静脉:1ml/kg(5min以上); ④ 肌肉注射:0.5ml/kg(一个部位); ⑤ 眼睛:0.01ml/每眼; ⑥ 直肠:0.5ml/kg; ⑦ 阴道:大鼠0.2ml,兔lml; ⑧ 吸入:2mg/L; ⑨ 鼻:猴或犬每鼻孔0.1ml。
吞咽胶囊:将受试物装入胶囊中,放至舌 后部,迫使动物咽下。 喂饲:将受试物掺入动物饲料或饮水中供 实验动物自行摄入。
18
2.经呼吸道染毒 吸入染毒 静式吸入染毒;
动式吸入染毒。
气管内注入
19
静式吸入染毒 方法:将实验动物置于有一定体积的密 闭容器中,加入液态或气态受试物,形成 一定浓度的受试物空气环境进行染毒。 优点:简单、方便、受试物消耗少,适 合于小鼠。 缺点:氧气减少;浓度不稳定;经皮吸 收;不适合稍大动物;挥发性。
毒理学实验对比
毒性作用评价
LD50标志着一个化合物毒性的大小,所以常用作急性毒性分级。极毒、剧毒、中等毒、低毒、实际无毒、无毒。 LD50<人的可能摄入量的10倍,则放弃; LD50>10倍,进入下一阶段
蓄积毒性产生的因素:蓄积毒性作用产生的因素:与接触剂量大小和时间间隔有关;与毒物本身的性质有关(脂溶性还是水溶性,体内的贮存库);与动物种属的代谢特点有关
①检测外源化学物的致突变性,预测其对哺乳动物和人的致癌性; ②检测外源化学物对哺乳动物生殖细胞的遗传毒性,预测其对人体的遗传危害性。
了解外源化学物及其代谢产物对机体成年哺乳动物的生殖功能和生育力的影响。
通过计数胚胎或胎仔吸收或死亡数,测量胎仔的重量和性别比,检查外观、内脏和骨骼的形态,来识别受试物有无对胚胎或胎仔的致死、致畸或其他毒性作用。
作用机制:一是以DNA为靶点的直接诱变,引起基因突变和染色体畸变;二是不以DNA为靶点的间接诱变,即基因组突变。
①三代两窝生殖试验;②两代一窝和一代一窝生殖试验。
最佳试验方案是对成年动物进行染毒并包括子代从受精卵到性成熟所有生长发育阶段。观察期应贯穿一个完整的生命周期,以检测近、远期效应。最常选用的方案为三阶段试验。
哺乳动物致癌试验:哺乳动物致癌试验是鉴定化学致癌物的标准体内试验。哺乳动物致癌试验用来确定受试物对实验动物的致癌性、剂量-反应关系及诱发肿瘤的靶器官。
实验设计
实验动物、染毒途径、染毒剂量、观察周期、观察指标的选择、计算方法和评价
蓄积系数法、生物半减期法
在遗传毒理学及一些前期的试验难以做出明确评价时需要进行亚慢性毒性试验。在整个亚慢性试验期间,动物均应摄食试验饲料。受试物可掺入饲料中,也可掺入饮水中。不得已时可采用灌胃法进行。
药理毒理学实验

药理毒理学实验
药理毒理学实验是指研究药物对机体生理和病理过程的影响以及药物的毒性和安全性的实验研究。
这些实验常用于药物的开发、评价和监管。
药理学实验常包括以下方面的研究:
1. 药物在体内的吸收、分布、代谢和排泄过程;
2. 药物对生理系统和器官的作用机制和效应;
3. 药物对生理参数(如血压、心率、血糖等)的影响;
4. 药物的药效学研究,如测定最小有效剂量、最大耐受剂量等。
毒理学实验主要研究药物对机体引起的毒性反应,包括急性毒性、慢性毒性和亚慢性毒性等。
常用的毒理学实验包括:
1. 急性毒性实验:用于确定药物对动物的一次性剂量引起的毒性反应;
2. 慢性毒性实验:用于评估长期接触药物对动物的毒性效应;
3. 亚慢性毒性实验:用于评估中长期接触药物对动物的毒性效应;
4. 各种毒性指标的测定,如致死剂量、半数致死剂量、致畸性、致癌性等。
药理毒理学实验通常在动物模型中进行,常用的动物包括小鼠、大鼠、猴等。
实验设计需要符合伦理规范,并进行必要的安全措施,以确保实验过程安全且可靠。
值得注意的是,药理毒理学实验虽然可以提供药物效果和毒性的初步评估信息,但实验结果在转化到人类临床应用方面仍需要进行更进一步的研究和验证。
环境毒理学常用实验方法

方法
通常将动物长期暴露于毒物,观察肿 瘤发生情况、类型和恶性程度等指标。
03
细胞培养实验方法
细胞毒性实验
01
02
03
MTT法
通过检测活细胞线粒体中 的琥珀酸脱氢酶来反映细 胞活性,评估毒物对细胞 的毒性作用。
LDH释放法
检测细胞损伤时释放的乳 酸脱氢酶,用于评估毒物 对细胞膜的损伤程度。
中性红摄取法
06
数据分析和结果解读
数据统计和分析方法
描述性统计
对数据进行整理、分类、汇总,通过图表展示数据的分布、中心 趋势和离散程度。
推论性统计
通过假设检验、方差分析等方法,推断样本数据所代表的总体特征, 评估不同处理组之间的差异显著性。
多元统计分析
运用主成分分析、聚类分析、判别分析等方法,挖掘数据间的内在 联系和规律,简化数据结构。
研究动物在长时间内暴露于低 剂量毒物后的毒性反应和潜在 危害。
方法
通常将动物长期暴露于低剂量 毒物,观察生长、发育、繁殖 和器官损害等指标。
应用
用于评估毒物的慢性毒性,了 解毒物对机体的长期影响,如 致癌、致畸、致突变等。
致癌性实验
目的
应用
研究动物在长时间内暴露于毒物后是 否诱发肿瘤。
用于评估毒物的致癌性,为环境毒理 学和公共卫生领域提供重要依据。
04
分子生物学实验方法
基因毒性实验
02
01
03
单细胞凝胶电泳(彗星实验)
检测DNA链断裂,评估遗传物质损伤。
基因突变实验
通过观察基因突变频率,评估化学物质的致突变性。
报告基因实验
利用报告基因的表达变化,间接反映目标基因毒性。
蛋白表达实验
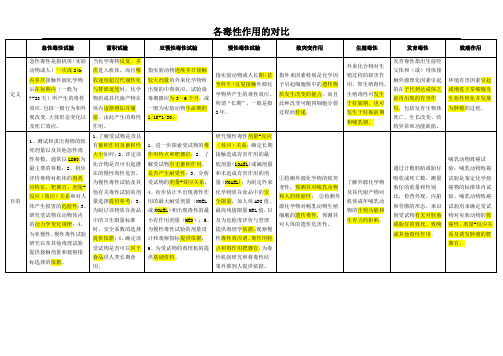
急性毒性、蓄积毒性、亚慢性毒性、亚急性毒性、慢性毒性资料区分

易混知识
毒性概念区分 亚慢性毒性试验
试验目的: 1.观察长期不同剂量受试物对动物的毒性作用; 2.测试靶器官; 3.获取亚慢性毒性参数NOEL值和MTD值,估计阀剂量或阈浓度 ; 4.了解受试物对成年动物生殖机能影响及子代致畸作用; 5.为慢性毒性和致癌试验提供剂量筛选和数据参考。 评价方式: 1.一般性指标:体重、饲料利用率、中毒症状。 2.生理生化指标:肝脏功能、肾脏功能、血液生化指标。 3.病理学检查:尸检、脏器系数、组织学检查。 4.特异性指标:尿液、粪便、毛发、呼出气体及各器官功能。
3
易混知识
兽药易混知识点 2.毒性概念区分 (临床资料22号-26号)
毒性:指外源化学物质在一定剂量、一定接触时间和一定接触方式下,对 动物机体产生的总体毒效应的能力,又称作一般毒性作用。 毒性分类 1.一般毒性根据外源化学物质剂量大小和时间长短分为:急性毒性、蓄积 毒性、亚慢性毒性、亚急性毒性、慢性毒性等。 442公告中中兽药要求的23号资料要求长期毒性试验(化药为亚慢性毒 性),长期毒性即包括:亚慢性毒性和慢性毒性试验! 2.相对特殊毒性根据观察目标不同可分为:遗传毒性、生殖发育毒性、致 癌性、免疫毒性、神经毒性和神经行为毒性等。
11
易混知识
亚慢性、慢性毒性试验检测点
12
The End
谢谢大家宝贵时间!
请批评指正。
13
6
易混知识
毒性概念区分 亚慢性毒性
亚慢性毒性:是指人或实验动物连续较长时间(相当于生命周期的1/10,如大鼠为3 个月)接触较大剂量(相对于低剂量,无剂量下限,但低于LD50,动物无死亡或极少死 亡)外源化合物所产生的毒性效应。 亚慢性毒性试验期限“较长时间”确切天数至今尚无完全统一认识。一般认为在环境 毒理学与药品、食品毒理学中所要求的连续接触为3~6个月,而在工业毒理学中认为 1~3月即可。 现有学者主张进行实验动物90天喂饲试验为亚慢性毒性试验,即将受试物混合物饲 料或饮水中,动物自然摄取连续90天。这是由于有研究报道认为动物连续接触外来化 合物3个月,其毒性效应往往与再延长接触时间所表现的毒性效应基本相同,故不必 再延长接触期限。
6 第6章 一般毒性作用及其试验与评价方法

2、剂量设计与分组
• 根据受试物或其近似物的物理、化学性质选择与本实 验相同动物物种或品系,相同染毒途径的LD50值作为 参考值,选择剂量系列。 • 一般分四组:高中低三个剂量组及一个阴性对照组
3、确定实验动物染毒方法: 灌胃
4、观察周期及观察内容
观察周期:一般为14天或24h,但计算出LD50时应注明
• 品种、品系的选择 • 健康状况:健康成年动物
小鼠、大鼠测半数致死量,狗观察毒性反应。
• 年龄:大鼠180-240g,小鼠18-25g(35-50日 龄),家兔2-2.5kg,豚鼠200-250g,狗10-15kg。 • 性别:雌、雄各半,雌性实验动物要求是未 经交配和受孕的。 • 各剂量组动物数: 小动物数量为每组 10 只,大动物也应每组 6 只。
‘一次接触’
(P122)
经口接触和各种方式的注射接触,“一次接触”,是指 在瞬间将受试化合物输入实验动物的体内;
而经呼吸道吸入与经皮肤接触,“一次接触”是指在一
个特定的期间内实验动物持续地接触受试化合物的过程; 此外,当化学物毒性较低时,需要给予动物较大剂量时, 可在 24 小时内分多次给予,这时的急性接触即为“多 次”。
免费茶水的重金属严重超标
一份外国学者的研究指出, 中国13个品牌的香烟重金属含量超标
第二节 蓄积毒性
一、基本概念 P138
当化学毒物连续、反复进入机体,而且进 入的速度(或总量)超过代谢转化与排出的速度 (或总量)时,物质就有可能在体内逐渐增加并 贮留的现象--蓄积作用(accumulation) 化学毒物容易蓄积的组织和器官——贮存库
急 以性 死毒 亡性 为的 终上 点限 参 数 急 非性 毒 作致 性 用死 的 为性 下 终急 限 点性 毒参 性数 ,
毒理学实验

毒理学实验毒理学实验是一项重要的科学研究方法,用于评估化学物质对生物体的毒性。
通过实验可以了解化学物质对人体的潜在危害以及其对环境的影响,从而制定相应的防护措施和规定。
本文将介绍毒理学实验的基本原理、常见的实验设计和评估方法,并探讨其在毒理学研究中的应用。
毒理学实验的基本原理:毒理学实验是通过将动物或细胞系统暴露于不同剂量的化学物质中,观察其对生物体造成的伤害和影响来评估其毒性。
实验中通常包括急性毒性、亚慢性毒性和慢性毒性等不同类型的实验。
常见的实验设计:1.急性毒性实验:该实验通过口服、注射或吸入等途径将化学物质暴露给动物,观察其可能导致的突发反应和致死效应。
实验通常在短时间内完成,并根据动物的反应判断化学物质的急性毒性。
2.亚慢性毒性实验:该实验通过连续或间歇地将化学物质暴露给动物一段较长时间,观察其对生物体各个器官和系统的影响。
实验通常持续几周或几个月,并通过检测血液生化指标、器官病变和行为变化等来评估化学物质的亚慢性毒性。
3.慢性毒性实验:该实验通过长期暴露动物或细胞系统于化学物质,观察其对生物体的长期影响。
实验通常持续数月至数年,并通过观察癌症发生率、器官功能变化等来评估化学物质的慢性毒性。
评估方法:1. LD50(半致死量):通过给动物不同剂量的化学物质,观察其在一定时间内造成50%动物死亡的剂量,从而评估其急性毒性。
2.组织病理学:通过组织切片和显微镜观察,评估化学物质对动物器官和组织结构的病变情况。
3.血液生化指标:通过检测动物体内的生物标志物,如肝功能指标、肾功能指标等,评估化学物质对生物体各个系统的影响。
4.外部观察和行为测定:通过观察动物的外貌和行为变化,评估化学物质对其行为、神经系统的影响。
毒理学实验在毒理学研究中的应用:1.安全评估:毒理学实验可用于确定化学物质的安全剂量和无效剂量范围,从而为制定相关安全规定和生产标准提供科学依据。
2.毒性机制研究:通过毒理学实验可以了解化学物质对生物体的具体作用机制,从而推测其毒性途径和潜在的毒性效应。
毒性试验

遗传毒性研究在药物研发中处于比较的重要位置,尤其是在药物筛选阶段,在很大程度上遗传毒性试验结果将影响到药物开发的进程。
一般而言,根据其检测的遗传学终点可分为4种类型:检测基因突变;检测染色体畸变;检测染色体组畸变;检测DNA原始损伤。
长期毒性试验
长期细胞毒性试验一般是在急性毒性试验结果的基础上,观察评价动物反复给予受试物后,机体产生毒性反应的特征及其毒性损害的严重程度,以及主要毒性靶器官及其损害的可逆性。
急性毒性试验
急性毒性试验是指在24小时内动物接受药物1-2次(间歇时间为6-8小时),观察给药后动物7-14天内所产生的急性中毒反应。
急性毒性试验可确定被研究药物的毒性程度,即剂量和不良反应之间的关系,亦可以比较被研究对象与其他已知急性毒性物的相对毒性程度,通过对不同给药途径出现毒性作用的比较研究, 就可以确定药物不同接触途径的相对危害。
受试物长期毒性试验的目的是提供受试物的无毒性反应剂量和临床主要检测指标,为制定人用安全剂量提供参考资料。
因此长期毒性试验的设计 最好能包括神经病理学、生理学、生物化学及相关的形态学指标的监测,还应注意受试物再组织中可能的蓄积,以及通过其他机制产生的延缓毒性作用等。
北校区北门2205师母,13515209736
致畸敏感期毒性试验大鼠致畸敏感期毒性试验:按受试品剂量分组,对雌性大鼠受孕后的第6-15天连续给药。观察受试品对胎仔外观、体重、身长、尾长、内脏和骨骼等的影响,并与生理盐水对照组比较。
围产期毒性试验大鼠围产期毒性试验:按受试品剂量分组皮下注射给药,给药时间为孕鼠妊娠15天开始至分娩后28天,观察受试品大、中、小三个剂量组,对大鼠胚胎后期生长发育、母鼠分娩、以及新生F1代大鼠的生理发育指标、神经反射发育指标和生殖功能,并与生理盐水对照组比较。
毒性作用名词解释毒理学

毒性作用名词解释毒理学
毒性作用的定义
毒性作用是指化学物质、生物制品或其他外部因素对生物体产生的危害效应。
这些危害效应可能会损害生物体的组织、器官或生命体征,从而引起多种生理和病理变化。
毒性作用是毒理学研究的重要内容之一。
毒性作用的分类
根据毒性作用的表现形式和机理,可将其分为急性毒性和慢性毒性两种:
急性毒性
急性毒性是指一次或短期内暴露于高浓度的毒物后,引起的急剧中毒反应。
症
状多发生在暴露后的24小时内,可导致中毒死亡或严重的急性疾病。
慢性毒性
慢性毒性是指长时间接触低浓度的毒物后,累积引起的长期或持续的毒物作用。
慢性毒性作用常常比急性毒性作用更隐匿,症状可能在较长时间内逐渐显现,影响生命质量和健康。
毒性作用的评估
对毒性作用的评估是毒理学研究的核心环节,通常包括以下几个方面:
毒性试验
毒性试验是通过实验方法,评估毒物对生物体的毒性效应和危险性。
常见的毒
性试验包括急性毒性试验、慢性毒性试验、亚急性毒性试验等。
毒性动力学
毒性动力学研。
短期、亚慢性和慢性毒性

15
常用大鼠或小鼠 染毒途径多用灌胃或者腹腔注射
16
B 剂量递增法
动物及分组:常用大或小鼠,40(或更多)分染毒组和对 照组,每组至少20只,雌雄各半。 终止时间:试验组累计发生一半动物死亡。在第21天也可结 束,因累计剂量已达5.26 LD50。
17
剂量递增20天法: 20天法 C 剂量递增20天法:
11
K值越小:表示化学物的蓄积性越大 K<1 K=1 K>=5 实验动物对化学毒物发生过敏 化合物在体内完全蓄积或每次 染毒后毒效应叠加 化合物蓄积性弱
12
蓄积系数分级标准 蓄积系数(K) <1 1~ 3~ 5~ 蓄积毒级分级 高度蓄积 明显蓄积 中等蓄积 轻度蓄积
13
1.2 蓄积系数法常用试验方案
7
功能蓄积(func accumulation): 3.2 功能蓄积(functional accumulation): 化学毒物反复多次染毒实验动物后, 化学毒物反复多次染毒实验动物后,机体内虽不能 检出化学毒物,然而机体可以出现慢性中毒现象。 检出化学毒物,然而机体可以出现慢性中毒现象。 注:功能蓄积是损害效应累计的结果。也可能是由于存留 功能蓄积是损害效应累计的结果。
短期、 短期、亚慢性和慢性毒性作用
1
一、概
述
急性毒性试验的局限性: 急性毒性试验的局限性: 1.外源性化学物在长期重复染毒时可产生与急性 1.外源性化学物在长期重复染毒时可产生与急性 毒性试验完全不同的毒作用。 毒性试验完全不同的毒作用。如:苯 2.动物的衰老可影响毒作用的性质和程度 2.动物的衰老可影响毒作用的性质和程度 3.许多重要疾病均与年龄增长有关 3.许多重要疾病均与年龄增长有关
38
波棱瓜子总木脂素的急性和亚慢性毒性试验

波棱瓜子总木脂素的急性和亚慢性毒性试验目录一、内容简述 (2)1.1 研究背景与意义 (2)1.2 国内外研究现状 (3)1.3 研究目的与内容 (4)二、材料与方法 (5)2.1 实验材料 (6)2.2 实验仪器与试剂 (7)2.3 实验设计 (7)2.4 样本制备与剂量设置 (8)2.5 数据采集与分析方法 (9)三、急性毒性试验结果与分析 (10)3.1 实验动物与剂量选择 (11)3.2 急性毒性症状观察 (12)3.3 生物毒性评价指标 (13)3.4 急性毒性试验结论 (13)四、亚慢性毒性试验结果与分析 (14)4.1 实验动物与剂量选择 (15)4.2 亚慢性毒性症状观察 (16)4.3 亚慢性毒性生理指标变化 (17)4.4 亚慢性毒性组织器官损伤评估 (17)4.5 亚慢性毒性试验结论 (18)五、波棱瓜子总木脂素的安全性评价 (18)5.1 急性和亚慢性毒性综合分析 (19)5.2 安全性评价标准与方法 (20)5.3 波棱瓜子总木脂素的安全性评级 (21)5.4 安全性应用建议 (21)六、结论与展望 (22)6.1 研究成果总结 (23)6.2 存在问题与不足 (24)6.3 未来研究方向与应用前景 (25)一、内容简述本试验旨在研究波棱瓜子总木脂素(total oleanolic acid,TOA)的急性和亚慢性毒性。
通过观察不同剂量下波棱瓜子提取物对实验小鼠的生长、行为、器官功能以及血液生化指标的影响,评价TOA的毒性水平。
本试验采用3种不同剂量和200 mgkg)的波棱瓜子提取物,分别进行急性和亚慢性毒性试验。
在试验过程中,对各组小鼠进行定期观察,记录生长情况、活动能力、食欲、体重变化等指标,并对主要器官如肝脏、肾脏、心脏、肺等进行病理学检查。
测定血液生化指标如血清谷丙转氨酶(ALT)、血清谷草转氨酶(AST)、肌酐(Cr)、尿素氮(BUN)等,以评估TOA对小鼠的肝肾功能的影响。
食品添加剂使用的安全性评估方法

食品添加剂使用的安全性评估方法食品添加剂是一种用于改善食品质量和保持食品新鲜度的物质。
在现代食品加工中,添加剂被广泛使用,以提高食品的口感、外观和营养价值。
然而,由于添加剂的广泛应用,人们对其是否安全的担忧也日益增加。
因此,食品添加剂的安全性评估方法成为了一个重要的研究领域。
食品添加剂的安全性评估是通过一系列的实验和研究来确定添加剂对人体健康的潜在风险。
这些评估方法通常包括以下几个方面:1. 急性毒性评估:急性毒性评估是通过给动物大剂量投放添加剂来评估其对动物的毒性。
这种评估方法可以快速确定添加剂是否具有明显的毒性效应。
实验中通常使用小鼠或大鼠作为实验动物,观察其在给予添加剂后的行为、生理和生化指标的变化。
2. 亚慢性和慢性毒性评估:亚慢性和慢性毒性评估是通过将添加剂长期投放给动物来评估其对动物的慢性毒性效应。
这种评估方法可以更准确地评估添加剂在长期暴露下对动物的潜在危害。
实验中通常使用大鼠或小鼠作为实验动物,观察其在长期接触添加剂后的生理、生化和病理变化。
3. 基因毒性评估:基因毒性评估是通过一系列的实验来评估添加剂对基因的损伤程度。
这种评估方法可以确定添加剂是否具有致突变或致癌的潜力。
实验中通常使用细菌、哺乳动物细胞或实验动物进行基因毒性实验,观察添加剂对DNA的损伤程度。
4. 长期暴露评估:长期暴露评估是通过将添加剂添加到动物的日常饮食中,评估其对动物的长期健康影响。
这种评估方法可以模拟人类长期暴露于添加剂的情况,更准确地评估其对人体的潜在危害。
除了以上实验方法,还有一些其他的评估方法也被广泛应用于食品添加剂的安全性评估中。
例如,流行病学研究可以通过调查人群暴露于添加剂后的健康状况,评估添加剂对人体的潜在影响。
体外试验可以通过使用细胞或组织模型,评估添加剂对人体的毒性效应。
此外,还有一些计算模型和预测方法可以根据添加剂的结构和生物活性,预测其对人体的潜在危害。
需要指出的是,食品添加剂的安全性评估是一个复杂的过程,需要多学科的专家共同参与。
第7章一般毒性作用及其实验与评鉴方法

第7章⼀般毒性作⽤及其实验与评鉴⽅法第六章⼀般毒性作⽤及其试验与评价⽅法⼀般毒性作⽤:是指毒物对动物机体产⽣的综合毒性效应,也称基本毒性作⽤根据接触毒物的时间长短可将产⽣的毒性作⽤分为急性毒性、亚慢性毒性和慢性毒性。
第⼀节急性毒性作⽤及其试验与评价⽅法⼀、急性毒性试验的概念急性毒性试验是指动物机体⼀次或24h内多次接触受试物后在短期内所产⽜的毒性效应及反应。
观察内容⼀般包括⾏为变化、外观改变以及致死效应。
观察时间⼀般为7d,观察范围可为7~28d(迟发毒性效应)。
凡经⼝或经注射给毒,“⼀次”的含义是指瞬间将受试物输⼊试验动物体内;若经呼吸或⽪肤给毒,“⼀次”则指在⼀个特定的时间内,使试验动物持续接受受试物的过程。
“24h内多次接触受试物”的概念是指当受试物毒性很低,⼀次接触还不能达到充分了解该受试物的毒性作⽤,或⼀次不能导⼊设计剂量的受试物时,需在24h内分次染毒。
⼆、急性毒性试验的⽬的(1)测定和计算出受试物的致死量及其他急性毒试参数,主要获得受试物对某种实验动物以某种接触途径的LD50值;(2)了解受试物对动物机体的急性毒性特征,靶器官和剂量⼀反应关系;(3)研究受试物在动物体内的动⼒学变化规律;(4)为下⼀步的亚慢性、慢性毒性试验及其他毒理学试验的剂量设计和观察指标选择提供依据。
三、急性毒性试验⽅法1.实验动物的选择和要求(1)品种、品系的选择实验动物选择的原则是以哺乳动物为主,选择两种或两种以上的动物,包括啮齿类(rodentspecies)和⾮啮齿类(nonrodenl species),其中⾄少有⼀种⾮啮齿类动物。
啮齿类多选⽤⼩⿏和⼤⿏,⾮啮齿类常选⽤⽝或猴。
(2)性别和年龄或体重的要求对于实验动物的性别⼀般要求雌雄(早6)各半。
如果试验仅为某些特殊试验研究⽬标,也可选⽤单⼀性别。
如致畸试验可仅选雌性动物,对精⼦毒性试验可仅选雄性动物。
急性毒性试验通常要求刚成年的动物。
⼀般按体重选购,通常要求⼩⿏18~25g、⼤⿏180~240g、豚⿏.200~250g、家兔2~2.5kg、猫1.5~2kg、⽝4~6kg(⽝⼀般为1岁左右)。
亚慢性和慢性毒理实验

❖ ②动物的饲料消耗
❖ 记录动物的饲料消耗,并计算食物利用率(实验动 物每食入100克饲料所增长的体重克数)。
❖ 比较各染毒组与对照组实验动物的食物利用率, 有助于分析受试物对实验动物的生物学效应。
❖ 急性毒性试验和慢性毒性试验分别代表了人一次 染毒和长期反复染毒这两种暴露特征的毒性试验 方法。
❖ 慢性毒性试验耗费大量的人力、物力和时间,亚 急性、亚慢性毒性试验就具有预备或筛选试验的 性质。
慢性毒性实验
❖ 由于人体接触外源化学物往往是长期、反复接触, 利用急性毒性试验的资料难以预测慢性毒性。
❖ Weil等(1969)报告,112种受试物中,大鼠染毒90d 后才出现毒性效应的只有3种(占2.5%),其他受试 物均在90d内已出现毒性效应,故认为大鼠90d毒 性试验即可确定受试物的未观察到有害作用水平 (NOAEL)。
❖ 尽管还有争论,亚慢性毒性试验(90d亚慢性试验) 已成为比较常用的重复染毒毒性试验;从科学上 和经济上考虑,慢性毒性试验就倾向于和致癌试 验合并进行。
❖ 当外源化学物在亚急性、亚慢性毒性试验中有严 重的毒作用时,此受试物就应考虑放弃,只有在 必要时才进行慢性毒性试验。
❖ Parkinson等(1995)报告117种药品狗亚慢性(90d) 和慢性(24月)毒性试验结果与大鼠(短期或长期毒 性试验)的结果比较,几乎没有发现新的毒性资料。 因此,Parkinson等认为,动物毒性试验长于6个 月没有必要,除非是研究致癌作用。
❖ 在慢性毒性研究中,工业毒理学要求每天吸入4~ 6h,环境毒理学一般要求每天吸入8h。
毒理学评价的四个阶段和内容

毒理学评价的四个阶段和内容通常包括以下:
1. 急性毒性试验(Acute Toxicity Testing):
这是毒理学评价的第一阶段,主要目的是确定物质在短时间内(通常是一次或几次接触后)对生物体产生的有害效应。
内容包括:经口、皮肤接触和吸入途径的急性毒性试验,计算LD50(半数致死剂量),即导致一半实验动物死亡的剂量。
2. 遗传毒性试验(Genotoxicity Testing):
这个阶段评估物质是否能够引起遗传物质(DNA)的损伤,这可能导致突变、癌症或其他遗传疾病。
内容包括:Ames试验(细菌回复突变试验)、染色体畸变试验和微核试验等。
3. 亚慢性毒性试验(Subchronic T oxicity Testing):
在这个阶段,物质的毒性效应在较长时间内(几周到几个月)被研究。
内容包括:重复剂量毒性试验,观察动物的行为变化、体重变化、血液学参数、生化指标、器官重量和病理学改变等。
4. 慢性毒性试验和致癌性试验(Chronic T oxicity and Carcinogenicity Testing):
这是最长的一个试验阶段,通常持续数月到数年,旨在评估物质长期暴露对生物体的影响,包括潜在的致癌性。
内容包括:生命周期研究,观察生长发育、生殖能力、寿命以及肿瘤发生率等。
在这些试验中,除了直接的毒性效应外,还会考虑物质的代谢途径、蓄积效
应、剂量-反应关系以及敏感群体(如孕妇、儿童和老人)的特殊反应。
这些信息对于全面评估物质的安全性和风险管理至关重要。
值得注意的是,具体的试验设计和要求可能会根据监管机构的指导原则和物质的特性进行调整。
毒理学染毒时间选择

急性毒性:实验动物一次接触或者24小时内多次接触某一化合物而引起的毒效应,甚至死亡。
亚慢性毒性:人或者动物连续接触较长时间、较大剂量的外源性化学物质所出现的中毒效应。
接触时间介于单次染毒和10%动物寿命的范围。
没有严格的界限,通常为1-6个月。
慢性毒性:指人或者实验动物长期(甚至终生)反复接触低剂量的外源化合物所出现的毒性效应。
一般是2年。
对于大鼠相当于终身,兔相当于生命的36%,狗20%,猴13%。
《毒理学基础第5版》90天亚慢性毒性试验来判断慢性毒性效应基本得到认可。
保健食品安全性毒理学评价试验的四个阶段和内容

保健食品安全性毒理学评价试验的四个阶段和内容SANY GROUP system office room 【SANYUA16H-保健食品安全性毒理学评价试验的四个阶段和内容毒理试验的四个阶段和内容1第一阶段:急性毒性试验经口急性毒性:LD50,联合急性毒性,一次最大耐受量试验。
2第二阶段:遗传毒性试验,30天喂养试验,传统致畸试验2.1基因突变试验:鼠伤寒沙门氏菌/哺乳动物微粒体酶试验(Ames试验)为首选,其次考虑选用V79/HGPRT基因突变试验,必要时可另选其它试验。
2.2骨髓细胞微核试验或哺乳动物骨髓细胞染色体畸变试验。
2.3TK基因突变试验。
2.4小鼠精子畸形分析或睾丸染色体畸变分析。
2.5其它备选遗传毒性试验:显性致死试验、果蝇伴性隐性致死试验,非程序性DNA合成试验。
2.630天喂养试验。
2.7传统致畸试验。
3第三阶段:亚慢性毒性试验----90天喂养试验、繁殖试验、代谢试验4第四阶段:慢性毒性试验(包括致癌试验)1、药物的毒性试验分为两类,其一特殊毒性试验,包含致癌、致残、致突变,号称三致试验;作此试验的单位必须是国家指定并认可的;一般单位即使做了也不被国家认可!通常一类创新药必须做的。
无论一个药物的药效如何好,只要含有三致试验的特殊毒性(动物若干代繁殖后,查看),该药物将不会允许上市的。
2、其二,一般毒性试验,通常用老鼠或兔子去做,主要是测定半数致死量;若某个药物的半数致死量是有效使用剂量的2倍以上,通常认为是临床使用安全的,若半数致死量比有效剂量略大一点,那就谁也不敢使用了,万一略微超一点量就会导致患者死亡!。
苍朴乌梅散对大鼠的急性毒性及亚慢性毒性研究

苍朴乌梅散对大鼠的急性毒性及亚慢性毒性研究目录一、内容简述 (2)1. 研究背景与目的 (2)2. 研究意义 (3)3. 文献综述 (4)二、材料与方法 (5)1. 实验动物与分组 (7)2. 药品与试剂 (7)3. 实验仪器与设备 (8)4. 实验方法 (8)5. 数据采集与分析 (9)三、急性毒性实验研究 (10)1. 给药剂量与途径 (11)2. 观察指标与时间点 (11)3. 数据处理与结果分析 (12)四、亚慢性毒性实验研究 (13)1. 给药剂量与周期 (14)2. 观察指标与时间点 (15)3. 数据处理与结果分析 (16)五、讨论 (17)1. 急性毒性实验结果讨论 (18)2. 亚慢性毒性实验结果讨论 (19)3. 与其他研究的比较 (20)4. 本研究的局限性与未来展望 (21)六、结论 (22)1. 研究成果总结 (23)2. 对后续研究的建议 (24)一、内容简述本研究旨在探讨苍朴乌梅散对大鼠的急性毒性及亚慢性毒性作用。
苍朴乌梅散作为一种具有特定药理活性的中药制剂,在广泛应用前,对其安全性评价至关重要。
本实验通过构建大鼠急性毒性模型和亚慢性毒性模型,对苍朴乌梅散进行系统的毒性研究,以评估其潜在风险,为药物的安全使用提供科学依据。
急性毒性研究:通过给予大鼠不同剂量的苍朴乌梅散,观察其在短时间内的毒性反应,如生命体征变化、行为异常、死亡率等,并计算药物的半数致死量(LD,以评估药物的急性毒性。
亚慢性毒性研究:在较长时间内给予大鼠苍朴乌梅散,观察其对大鼠的生长、发育、繁殖、器官功能、生化指标等方面的影响,以评估药物在长期使用下的潜在毒性。
研究方法包括实验设计、实验动物的选择与分组、药物剂量的设定、观察指标的确定以及数据收集与分析等。
实验过程中将严格遵守动物实验伦理规范,确保实验结果的准确性和可靠性。
本研究旨在为苍朴乌梅散的安全性和合理用药提供科学依据,为其临床应用提供参考。
1. 研究背景与目的随着人们生活节奏的加快和饮食结构的改变,脾胃虚弱、消化不良等问题日益普遍,乌梅作为一种传统的中药药材,因其具有涩肠止泻、生津止渴、安蛔止痛等功效,在中医临床应用中受到广泛关注。
急性慢性和亚慢性毒性实验

急性毒性试验一经典的急性致死性毒性试验通过试验得到化合物引起动物死亡的剂量—反应关系并求得LD50LC501、实验动物常用的实验动物是小鼠或大鼠;一般受试动物应是雌、雄各半;若雌、雄动物对待测化学物毒性的敏感程度有明差异,则应分别求出各自的LD50;如果试验是为畸形试验做剂量准备,也可仅做雌性动物的LD50试验;小动物每组10只,狗等大动物可每组6只;2、染毒剂量设计首先要了解化学毒物的结构式、分子量、常温常压下的状态、纯度、杂质成分与含量、溶解度、挥发度、PH等理化性质;对于新的受试化学物,找出与受试化学毒物结构与理化性质近似的化学物的毒性资料,并以文献资料中相同的动物种系和相同接触途径所测得的LD50LC50值作为受试化学物的预期毒性中值,先用少量动物,以较大的剂量间隔一般按几何级数染毒,找出找出10%~90%或0%~100%的致死剂量范围,然后在这个剂量范围内设几个剂量组;改良寇氏法最好设5个剂量组,每组10只动物,雌雄各半,剂量组要求以等比级数设置;根据以下公式计算出剂量分组:i=lgLD90-lgLD10/n-1 或:i=lgLD100-lgLD0/n-1式中i为组距相邻的两个剂量组对数剂量之差;n为设计的剂量组数;有的毒性较小,此时可不再求其LD50,而应进行限量试验;在用大鼠或小鼠进行试验时,一般用20只动物,雌雄各半;单次染毒剂量一般限定为5g/kg体重,对于食品毒理学试验,限量要求为15g/kg体重;如果实验动物无死亡或仅有个别动物死亡死亡率低于50%,则可得出LD50大于限量的结论;3、观察染毒后一般要求观察14天,依据14天内动物的总死亡情况计算LD50;在实际工作中,依据受试物有关测试规程要求确定观察期的长短;观察内容包括:(1)动物死亡情况:包括动物死亡数及各自的死亡时间;(2)动物体重:于染毒前、染毒后每周和死亡时测定体重;(3)中毒反应症状:临床观察每天至少一次,观察皮肤、被毛、眼睛和粘膜改变,呼吸、循环、自主和中枢神经系统以及四肢活动和行为方式的变化等,特别要注意有无震颤、惊厥、腹泻、嗜睡等现象;神经毒性:惊厥、共济失调和死亡;植物神经兴奋:腹泻或竖毛;(4)病理学检查:解剖进行尸检,观察各器官有无改变,对肉眼观察有变化的脏器需进行组织病理学检查;4、LD50计算(1)霍恩氏法(2)简化寇氏法M = X – iΣp –式中: m— log LD50,X—最高剂量组剂量对数值,p—死亡率用小数表示,Σp—死亡率总和,i—相邻两组剂量对数之差;3直接回归法:死亡频率呈正态分布,则变化曲线为典型的“钟罩”型;死亡频率化为累积死亡频率,反应曲线呈S形;累积死亡频率化为概率单位时,反应曲线呈直线;二急性毒性试验的其他方法1.固定计量法2.急性毒性分级法3.上、下移动法亚慢性毒性和慢性毒性的评价方法1、实验动物要求选拔两种实验动物,一种为啮齿类,首选是大鼠,另一种为非啮齿类,首选是狗;亚慢性毒性试验一般每个剂量组20只大鼠,或每组4~6只狗;慢性毒性试验每组40只大鼠,狗每组8只或以上;2、染毒途径常用的染毒途径是经胃肠道、经呼吸道和经皮肤染毒;3、染毒期限工业毒理学—— 3-6个月食品毒理学—— 6个月-1年环境毒理学—— 6个月-1年致癌试验——接近或等于动物的预期寿命4、剂量分组1亚慢性毒性的剂量选择:阴性对照组,低剂量组,中剂量组,高剂量组急性毒性的阈剂量:1/20~1/5 LD50组距:3~10倍,最低不小于2倍2慢性毒性的剂量选择阴性对照组,低剂量组,中剂量组,高剂量组亚慢性阈剂量:1/50~1/5LD50组距:2~5倍,最低不小于2倍5、观察指标(1)中毒症状行为和外观(2)体重:每周称量一次(3)食物利用率试验动物每食入100g饲料所增长的体重克数4实验室检查1血液学检查2尿液检查3血液生化学检查5病理及病理组织学检查对濒死动物进行解剖;试验结束及恢复期结束时,活杀实验动物;1系统解剖:消化道、肺、肝、肾、淋巴腺、眼、皮肤等,记录有无肉眼可见的异常变化;2脏器系数:是指某个脏器质量与体重的比值,又称脏体比值;常以100 g体重或1g体重计;需称量脏器湿重并计算其脏器系数;3组织病理学检查6特异性指标6、结果分析:选择适当的统计学方法进行各剂量组与阴性对照组的比较;。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
急性慢性和亚慢性毒性实
验
The Standardization Office was revised on the afternoon of December 13, 2020
急性毒性试验
(一)经典的急性致死性毒性试验
通过试验得到化合物引起动物死亡的剂量—反应关系并求得LD50(LC50)
1、实验动物
常用的实验动物是小鼠或大鼠。
一般受试动物应是雌、雄各半;若雌、雄动物对待测化学物毒性的敏感程度有明差异,则应分别求出各自的LD50;如果试验是为畸形试验做剂量准备,也可仅做雌性动物的LD50试验。
小动物每组10只,狗等大动物可每组6只。
2、染毒剂量设计
首先要了解化学毒物的结构式、分子量、常温常压下的状态、纯度、杂质成分与含量、溶解度、挥发度、PH等理化性质。
对于新的受试化学物,找出与受试化学毒物结构与理化性质近似的化学物的毒性资料,并以文献资料中相同的动物种系和相同接触途径所测得的LD50(LC50)值作为受试化学物的预期毒性中值,先用少量动物,以较大的剂量间隔(一般按几何级数)染毒,找出找出10%~90%(或0%~100%)的致死剂量范围,然后在这个剂量范围内设几个剂量组。
改良寇氏法最好设5个剂量组,每组10只动物,雌雄各半,剂量组要求以等比级数设置。
根据以下公式计算出剂量分组:
i=(lgLD90-lgLD10)/(n-1) 或:i=(lgLD100-lgLD0)/(n-1)
式中i为组距(相邻的两个剂量组对数剂量之差);
n为设计的剂量组数。
有的毒性较小,此时可不再求其LD50,而应进行限量试验。
在用大鼠或小鼠进行试验时,一般用20只动物,雌雄各半。
单次染毒剂量一般限定为5g/kg(体
重),对于食品毒理学试验,限量要求为15g/kg(体重)。
如果实验动物无死亡或仅有个别动物死亡(死亡率低于50%),则可得出LD50大于限量的结论。
3、观察
染毒后一般要求观察14天,依据14天内动物的总死亡情况计算LD50。
在实际工作中,依据受试物有关测试规程要求确定观察期的长短。
观察内容包括:
(1)动物死亡情况:包括动物死亡数及各自的死亡时间。
(2)动物体重:于染毒前、染毒后每周和死亡时测定体重。
(3)中毒反应症状:临床观察每天至少一次,观察皮肤、被毛、眼睛和粘膜改变,呼吸、循环、自主和中枢神经系统以及四肢活动和行为方式的变化等,特别要注意有无震颤、惊厥、腹泻、嗜睡等现象。
神经毒性:惊厥、共济失调和死亡。
植物神经兴奋:腹泻或竖毛。
(4)病理学检查:解剖进行尸检,观察各器官有无改变,对肉眼观察有变化的脏器需进行组织病理学检查。
4、LD50计算
(1)霍恩氏法
(2)简化寇氏法
M = X – i(Σp –
式中: m— log LD50,
X—最高剂量组剂量对数值,
p—死亡率(用小数表示),
Σp—死亡率总和,
i—相邻两组剂量对数之差。
(3)直接回归法:
死亡频率呈正态分布,则变化曲线为典型的“钟罩”型;死亡频率化为累积死亡频率,反应曲线呈S形;累积死亡频率化为概率单位时,反应曲线呈直线。
(二)急性毒性试验的其他方法
1.固定计量法
2.急性毒性分级法
3.上、下移动法
亚慢性毒性和慢性毒性的评价方法
1、实验动物
要求选拔两种实验动物,一种为啮齿类,首选是大鼠,另一种为非啮齿类,首选是狗。
亚慢性毒性试验一般每个剂量组20只大鼠,或每组4~6只狗。
慢性毒性试验每组40只大鼠,狗每组8只或以上。
2、染毒途径
常用的染毒途径是经胃肠道、经呼吸道和经皮肤染毒。
3、染毒期限
工业毒理学—— 3-6个月
食品毒理学—— 6个月-1年
环境毒理学—— 6个月-1年
致癌试验——接近或等于动物的预期寿命
4、剂量分组
(1)亚慢性毒性的剂量选择:
阴性对照组,低剂量组,中剂量组,高剂量组
急性毒性的阈剂量:1/20~1/5 LD50
组距:3~10倍,最低不小于2倍
(2)慢性毒性的剂量选择
阴性对照组,低剂量组,中剂量组,高剂量组
亚慢性阈剂量:1/50~1/5LD50
组距:2~5倍,最低不小于2倍
5、观察指标
(1)中毒症状(行为和外观)
(2)体重:每周称量一次
(3)食物利用率(试验动物每食入100g饲料所增长的体重克数)
(4)实验室检查
1)血液学检查
2)尿液检查
3)血液生化学检查
(5)病理及病理组织学检查
对濒死动物进行解剖。
试验结束及恢复期结束时,活杀实验动物。
1)系统解剖:消化道、肺、肝、肾、淋巴腺、眼、皮肤等,记录有无肉眼可见的异常变化。
2)脏器系数:是指某个脏器质量与体重的比值,又称脏体比值。
常以100 g体重或1g体重计。
需称量脏器湿重并计算其脏器系数。
3)组织病理学检查
(6)特异性指标
6、结果分析:选择适当的统计学方法进行各剂量组与阴性对照组的比较。
