2020届高考化学二轮复习 高考选择客观题:电解质溶液有关图像题型的专题复习
高考化学二轮复习专题检测七电解质溶液

专题检测七 电解质溶液一、选择题(每小题6分,共60分)1.水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图像,模型见右图。
下列关于水的说法正确的是( )A .水是弱电解质B .可燃冰是可以燃烧的水C .氢氧两种元素只能组成水D .0 ℃时冰的密度比液态水的密度大解析:可燃冰是甲烷水合物,不是水,B 错误;氢氧两种元素除组成水外,还能组成H 2O 2,C 错误;水结成冰后密度减小,D 错误。
答案:A2.下列有关电解质溶液中粒子浓度关系正确的是( )A .pH =1的NaHSO 4溶液:c (H +)=c (SO 2-4)+c (OH -)B .含有AgCl 和AgI 固体的悬浊液:c (Ag +)>c (Cl -)=c (I -)C .CO 2的水溶液:c (H +)>c (HCO -3)=2c (CO 2-3)D .含等物质的量的NaHC 2O 4和Na 2C 2O 4的溶液:3c (Na +)=2[c (HC 2O -4)+c (C 2O 2-4)+c (H 2C 2O 4)]解析:因为NaHSO 4溶液中存在c (Na +)=c (SO 2-4),依据电荷守恒:c (Na +)+c (H +)=2c (SO 2-4)+c (OH -),可知c (H +)=c (SO 2-4)+c (OH -),A 项正确;AgCl 的溶解度比AgI 的大,所以c (Ag +)>c (Cl -)>c (I -),B 项错误;CO 2水溶液中存在:H 2CO 3++HCO -3,HCO -3++CO 2-3和H 2++OH -,H 2CO 3的第一步电离远大于第二步电离,所以c (H +)>c (HCO -3)>c (CO 2-3),C 项错误;假设NaHC 2O 4和Na 2C 2O 4均为1 mol ,则n (Na +)=3 mol ,依据物料守恒n (HC 2O -4)+n (C 2O 2-4)+n (H 2C 2O 4)=2 mol ,同一溶液中存在2c (Na +)=3[c (HC 2O -4)+c (C 2O 2-4)+c (H 2C 2O 4)],D 项错误。
2020高考化学课标二轮(天津专用)热点专攻:10 电解质溶液图像题

热点专攻10 电解质溶液图像题1.(2019天津理综)某温度下,HNO 2和CH 3COOH 的电离常数的值分别为5.0×10-4和1.7×10-5。
将pH 和体积均相同的两种酸溶液分别稀释,其pH 随加水体积的变化如图所示。
下列叙述正确的是( )A.曲线Ⅰ代表HNO 2溶液B.溶液中水的电离程度: N 点>P 点C.从P 点到Q 点,溶液中保持不变(其中HA 、A -分别代表相应的酸和酸根离子)c (HA )·c (OH -)c (A -)M 点的两溶液分别与NaOH 恰好中和后,溶液中n (Na +)相同,酸性:HNO 2>CH 3COOH,pH 相同的两种酸稀释相同倍数,pH 变化大的是相对较强的酸,即曲线Ⅱ表示HNO 2溶液的稀释,A 项错误;pH 越小酸性越强,对水电离的抑制程度越大,因此溶液中水的电离程度:N 点<P 点,B 项错误;题给表达式可看作,K W K a 稀释时温度不变,则K W 、K a 均不变,C 项正确;起始pH 相同时c (CH 3COOH)大,则与NaOH 恰好中和时,CH 3COOH 溶液消耗氢氧化钠多,对应溶液中n (Na +)大,D 项错误。
2.已知t ℃时的K sp (AgCl)=1.6×10-10,K sp (AgBr)=7.8×10-13;在t ℃时,Ag 2CrO 4在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是( )A.t ℃时,K sp (Ag 2CrO 4)=1×10-9B.t ℃时,在饱和Ag 2CrO 4溶液中加入AgNO 3可使溶液由Z 点到X 点C.t ℃时,溶解度的大小顺序为AgCl>Ag 2CrO 4>AgBrD.t ℃时,取一定量的KCl 和KBr 的混合溶液,向其中滴加AgNO 3溶液,当AgCl 开始沉淀时,c (Cl -)c (Br -)=K sp (AgCl )K sp (AgBr )℃时,K sp (Ag 2CrO 4)=(10-3)2×10-6=1×10-12,A 项错误;在饱和Ag 2CrO 4溶液中加入AgNO 3可使溶液由Z 点到Y 点,处于饱和状态,不能由Z 点到X 点,B 项错误;由K sp 可以计算AgCl 、Ag 2CrO 4、AgBr 在水中c (Ag +)的数量级是10-5、10-3、10-6.5,故溶解度的大小顺序为Ag 2CrO 4>AgCl>AgBr,C 项错误;t ℃时,取一定量的KCl 和KBr 的混合溶液,向其中滴加AgNO 3溶液,当AgCl 开始沉淀时,AgBr 已经沉淀,,D 项正确。
高考化学二轮复习难点专题:电解质溶液曲线(附答案与详解)

高考化学二轮复习难点专题电解质溶液曲线分析【命题规律】本专题的考查点主要是弱电解质的电离平衡和盐类水解相结合,进行综合考察。
为高考的中频考点,命题形式以选择题为主,试题难度中等。
考查的核心素养以证据推理与模型认知为主。
【备考建议】2020年高考备考应重点关注数形结合与分析推理型选择题。
【限时检测】(建议用时:30分钟)1.(2019-安徽省六安市第一中学高考模拟)常温下用NaOH溶液滴定H2C2O4溶液溶液中和-lgc(HC2O4)[或-lgc(H')c(HC2O;)和-lgc(C2O42)]的关系如图所示。
下列说法正确的是('Mcxcqm'tgoth123458r(H/:,OJ*e(HC,OJc(H+)A.曲线N表示-lg—气和-lgc(C2O42_)的关系c(HC2O;)B.K al(H2C2O4)W数量级为101C.向NaHC2O4溶液中加少量NaOH至c(HC2O「)和c(C2O42-)ffl^.此时溶液pH约为4D.在Na2C2O4和NaHC2O4物质的量为1:1的混合溶液中c(Na+)>c(C2O42)>c(HC2O4)>c(H2C2O4)>c(OH)>c(H+)2.(2019-黑龙江省大庆一中高考模拟)用0.1mol-L1NaOH溶液滴定40mL0.1mol-L^1H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。
下列叙述错误的是()A.K a2(H2SO3)的数量级为IO®B.若滴定到第一反应终点,可用甲基橙作指示剂C,图中Z点对应的溶液中:c(Na+)>c(SO32_)>c(HSO3_)>c(OH-)D,图中Y点对应的溶液中:3c(SO32-)=c(Na+)+c(H+)-c(OH^)3.(2019.东北育才学校科学高中部高考模拟)常温下向2OmLO.lmol/L氨水中通入HC1气体,溶液中由水电离出的氢离子浓度随通入HC1气体的体积变化如图所示。
2020届高考化学提分攻略 题型14 电解质溶液图像题(含解析)
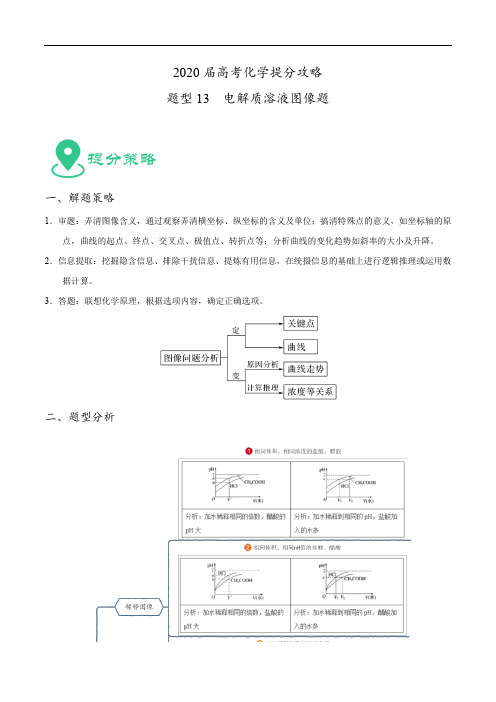
2020届高考化学提分攻略题型13 电解质溶液图像题一、解题策略1.审题:弄清图像含义,通过观察弄清横坐标、纵坐标的含义及单位;搞清特殊点的意义,如坐标轴的原点,曲线的起点、终点、交叉点、极值点、转折点等;分析曲线的变化趋势如斜率的大小及升降。
2.信息提取:挖掘隐含信息、排除干扰信息、提炼有用信息,在统摄信息的基础上进行逻辑推理或运用数据计算。
3.答题:联想化学原理,根据选项内容,确定正确选项。
二、题型分析【典例1】【2019·课标全国Ⅱ,12】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。
硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。
下列说法错误的是()A.图中a和b分别为T1、T2温度下CdS在水中的溶解度B.图中各点对应的K sp的关系为:K sp(m)=K sp(n)<K sp(p)<K sp(q)C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动【答案】B【解析】a、b分别表示温度为T1、T2时溶液中Cd2+和S2-的物质的量浓度,可间接表示对应温度下CdS在水中的溶解度,A项正确;K sp只受温度影响,即m、n、p三点对应的K sp相同,又T1→T2,c(S2-)、c(Cd2+)都增大,故K sp(m)=K sp(n)=K sp(p)<K sp(q),B项错误;向m点的溶液中加入少量Na2S固体,溶液中c(S2-)增大,温度不变,K sp不变,则溶液中c(Cd2+)减小,溶液组成由m点沿mpn线向p方向移动,C 项正确;温度降低时,CdS的溶解度减小,q点的饱和溶液的组成由q沿qp线向p方向移动,D项正确。
【典例2】【2018·课标全国Ⅲ,12】用0.100 mol·L-1 AgNO3滴定50.0 mL 0.050 0 mol·L-1 Cl-溶液的滴定曲线如图所示。
高中化学二轮复习电解质溶液选择题通关六离子平衡图像的分析与应用

2.(酸碱中和反应曲线)常温下,用 0.100 mol·L-1 的 NaOH 溶液分别滴定 20.00 mL 0.100 mol·L-1 的盐酸和 0.100 mol·L-1 的醋酸,得到两条滴定曲 线,如图所示: 下列说法正确的是( ) A.滴定盐酸的曲线是图 2 B.两次滴定均可选择甲基橙或酚酞做指示剂
酸碱中和滴定图像分析
氢氧化钠溶液滴定等浓度等体积 盐酸滴定等浓度等体积的氢氧化
的盐酸、醋酸的滴定曲线
钠溶液、氨水的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴 定强碱、弱碱的曲线,强碱起点高 突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变 化范围大于强碱与弱酸反应(强酸与弱碱反应) 室温下 pH=7 不一定是终点:强碱与强酸反应时,终点是 pH=7; 强碱与弱酸(强酸与弱碱)反应时,终点不是 pH=7(强碱与弱酸反应 的终点是 pH>7,强酸与弱碱反应的终点是 pH<7)
C.物质的量浓度c= = = mol/L,故C错误;
A.曲线①代表 δ(H A),曲线②代表 δ(HA ) 1【2.详下 解列】离综子合方分程析式工不艺正流确程的图是可知,试剂X只能是氢氧化钠溶液,Al2O3溶于氢氧化钠溶液得到NaAlO2-溶液,Fe2O3与氢氧化钠溶液不反应,所以反应①、过滤后所得溶液乙为
(4)①+6价的Cr具有氧化性,能氧化碘离子,生成单质碘,则BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式为2BaCrO4+6I-+16H+=3I2+2Ba2++2Cr3++8H2O;
【解析】
2-
比如A 的分布系数:δ(A )= c(A ) 1试,0.题所已分 以知析关某:闭+2①所价煤有离、化子2石工的-油企电等业子燃是排料不布的现式燃实为烧的1s产,22生不s2二符2p氧合6,化题该硫意元等.素有错在害误周气;期体③表,提中开倡所发使2属-新用的能一族源次是,性减发少泡矿塑物料燃餐料具的和燃塑烧 料,袋也,就会减造少成了白污色染污物染的,排不放符,合符题-合意题.意错.误正;确④;废②旧现电代池社属2会于-很电多子的污产染品,来开自发化生工产
2020届高考化学二轮复习教师用书:微专题七 电解质溶液图像题

电解质溶液图像题[知识必备] 电解质溶液图像题的分类和解题方法与技巧1.一强一弱溶液的稀释图像相同体积、相同浓度的盐酸和醋酸相同体积、相同pH的盐酸、醋酸加水稀释相同的倍数,醋酸的pH大加水稀释相同的倍数,盐酸的pH大pH与稀释倍数的线性关系(1)pH与lgVV a变化相等的是强酸;HY为强酸;HX为弱酸(2)a、b两点的溶液中:c(X-)=c(Y-)(3)水的电离程度:d>c>a=b(1)同理、MOH为强碱、ROH为弱碱(2)c(ROH)>c(MOH)(3)水的电离程度:a>b用0.1 mol·L-1 NaOH溶液滴定20 mL0.1 mol·L-1 CH3COOH用0.1 mol·L-1 NaOH溶液滴定10 mL0.1 mol·L-1 H2SO3溶液(1)巧妙抓住“一半”“恰好”“中性”“过量”“二倍”点,突破“粒子”浓度关系(2)抓住“关键点”中以下问题:①参加反应溶质量的关系②溶质的成分③溶质中各成分量的关系④溶液的酸碱性等(3)正确使用电荷守恒和物料守恒解决问题3.分布系数与pH关系曲线图像一元弱酸(以CH3COOH为例) 二元酸(以草酸H2C2O4为例)δ0为CH3COOH分布系数,δ1为CH3COO-分布系数δ0为H2C2O4分布系数、δ1为HC2O-4分布系数、δ2为C2O2-4分布系数利用曲线的交点确定弱电解质每步的电离常数K1、K2、K3…根据图像确定不同pH点微粒间的关系H2Y与NaOH溶液的反应H2X与NaOH溶液的反应(1)识图像:观察横坐标、纵坐标含义,找到横坐标的零点,即lg c(HX-)c(H2X)=0和lgc(X2-)c(HX-)=0的点。
(2)找联系:二元弱酸H2X分步电离,H2X H++HX-,HX-H++X2-,第一步电离要远远大于第二步的电离,即K1>K2、c(H+)1>c(H+)2。
(3)思原理:涉及到电离平衡常数,写出K1(H2X)=c(H+)·c(HX-)c(H2X),K2(H2X)=c(H+)·c(X2-)c(HX-);横坐标在0点时,可以看出N曲线的pH小,酸性强,则曲线N表示pH与lgc(HX-)c(H2X)的关系,曲线M表示pH与lgc(X2-)c(HX-)的关系。
高考化学二轮复习精品 专题9 电解质溶液

专题九 电解质溶液
高考化学总复习(第2轮)人教版课件
热点题型突破
考情分析:电解质溶液是高考中考点分布较多的内容之一, 题型主要有选择题和填空题,其考查内容主要有: (1)外界条件对弱电解质电离平衡的影响。 (2)酸、碱混合后溶液酸碱性的判断及pH的简单计算。 (3)电解质溶液中离子浓度的大小比较。 (4)盐对水电离平衡的影响及盐溶液蒸干灼烧后产物的判断。
高考化学总复习(第2轮)人教版课件
4.施用的氮肥是铵盐时不宜与草木灰混合使用。 5.明矾净水:明矾溶于水,生成胶状物氢氧化铝,能吸附水里悬
浮的杂质,并形成沉淀使水澄清。 6.热的纯碱溶液有较好的去油污效果。因为升温能促进盐类的
水解,使纯碱溶液的碱性增强,去油污的效果更好。 7.将活泼金属放在强酸弱碱盐的溶液里,会有气体逸出。例如
高考化学总复习(第2轮)人教版课件
考点2 溶液的酸碱性及pH的计算 1.溶液的酸碱性——取决于溶液中c(H+)和c(OH-)的
相对大小 c(H+)>c(OH-) 酸性 c(H+)=c(OH-) 中性 c(H+)<c(OH-) 碱性
高考化学总复习(第2轮)人教版课件
(1)pH相同的酸(或碱),酸(或碱)性越弱,其物质的量浓度越大。 (2)pH相同的强酸和弱酸溶液,加水稀释相同的倍数,则强酸溶液pH变化大;碱也如此。 (3)酸与碱的pH之和为14,等体积混合时溶液的pH 若为强酸与强碱,则pH=7; 若为强酸与弱碱,则pH>7; 若为弱酸与强碱,则pH<7。
a<pH<a+n(即对于pH相同的强酸与弱酸稀释相同倍数,强 酸pH变化的程度大)。
Hale Waihona Puke 高考化学总复习(第2轮)人教版课件
高考化学专题复习电解质溶液中微粒变化图像题课件

) )
-
得意时应善待他人,因为你失意时会需要他们。
a
丈夫志不大,何以佐乾坤。
加入NaOH,促进电2-离,Ka不变
+
c(A )·c(H ) 图中a点与b点Ag2CrO4溶度积相等
+
-2
=c(H )=1.0×10 ,C 项正确;滴定终点时溶液中存在的离子有 根据图中pH数据,图中A、B、-C、D、E、F各点对应的溶液中水的电离程度大小顺序图示:
2.(2019·课标全国Ⅰ,11)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1= 1.1×10-3,Ka2=3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示, 其中b点为反应终点。下列叙述错误的是( ) A.混合溶液的导电能力与离子浓度和种类有关 B.Na+与A2-的导电能力之和大于HA-的 C.b点的混合溶液pH=7 D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
项正确;cc((HXX2--))=1
时,即
c(X2-) lgc(HX-)
=0,pH=5.4,c(H+)=1×10-5.4 mol·L-1,Ka2=c(Hc(+)H·cX(-)X2-)≈1×10-5.4,A 正
确;NaHX 溶液中,c(HX-)>c(X2-),即cc((HXX2--))<1,lgcc((HXX2--))<0,此时溶液呈酸
人生各有5志.(。2017·课标全国Ⅰ,13)常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液
雄追心踪壮 着志鹿是的的茫猎茫人p黑是H夜看中不与的见北山离斗的星。子。 浓度变化的关系如图所示。下列叙述错误的是(
)
志正则众邪不生。
鹰爱高飞,鸦栖一枝。
A.K (H X)的数量级为 男儿不展同云志,空负天生八尺躯。
2020年高考化学专题复习《电解质溶液中的图像分析》
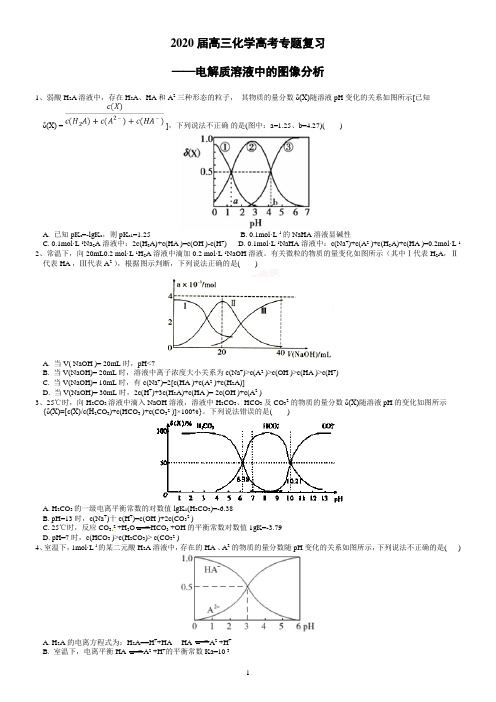
2020届高三化学高考专题复习——电解质溶液中的图像分析1、弱酸H2A 溶液中,存在H2A、HA-和A2-三种形态的粒子,其物质的量分数δ(X)随溶液pH变化的关系如图所示[已知δ(X) = ],下列说法不正确的是(图中:a=1.25、b=4.27)()A. 已知pK a=-lgK a,则pK a1=1.25B. 0.1mol·L-1的NaHA溶液显碱性C. 0.1mol·L-1Na2A溶液中:2c(H2A)+c(HA-)=c(OH-)-c(H+)D. 0.1mol·L-1NaHA溶液中:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol·L-12、常温下,向20mL0.2 mol·L-1H2A溶液中滴加0.2 mol·L-1NaOH溶液。
有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是()A. 当V( NaOH )= 20mL时,pH<7B. 当V(NaOH)= 20mL时,溶液中离子浓度大小关系为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)C. 当V(NaOH)= 10mL时,有c(Na+)=2[c(HA-)+c(A2-)+c(H2A)]D. 当V(NaOH)= 30mL时,2c(H+)+3c(H2A)+c(HA-)= 2c(OH-)+c(A2-)3、25℃时,向H2CO3溶液中滴入NaOH溶液,溶液中H2CO3、HCO3-及CO32-的物质的量分数δ(X)随溶液pH 的变化如图所示{δ(X)=[c(X)/c(H2CO3)+c(HCO3-)+c(CO32-)]×100%}。
下列说法错误的是()A. H2CO3的一级电离平衡常数的对数值lgK1(H2CO3)=-6.38B. pH=13时,c(Na+)十c(H+)=c(OH-)+2c(CO32-)C. 25℃时,反应CO32-+H2O HCO3-+OH-的平衡常数对数值1gK=-3.79D. pH=7时,c(HCO3-)>c(H2CO3)> c(CO32-)4、室温下,1mol·L-l的某二元酸H2A溶液中,存在的HA-、A2-的物质的量分数随pH变化的关系如图所示,下列说法不正确的是( )A. H2A的电离方程式为:H2A==H++HA-HA-A2-+H+C. 等物质的量浓度NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c(Na+)>c(HA-)>c(A2-)D. 在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA-)5、室温下,用0.1000mol/L盐酸分别滴定20.00mL浓度均为0.1000mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积V[HCl(aq)]的变化关系如图所示。
高三化学二轮复习:电解质溶液图像类题目分析课件

浓度小
CuS MnS
浓度大
浓度小
山东卷真题演练
1.(2022·山东,14)工业上以SrSO4(s)为原料生产SrCO3(s),对其工艺条件进行研 究。现有含SrCO3(s)的0.1 mol·L-1、1.0 mol·L-1 Na2CO3溶液,含SrSO4(s)的0.1 mol· L-1、1.0 mol·L-1 Na2SO4溶液。在一定pH范围内,四种溶液中lg [c(Sr2+)/mol· L-1]随pH的变化关系如图所示。下列说法错误的是 A.反应 SrSO4(s)+CO23-(aq) SrCO3(s)+
(2)写出pH由1到14依次发生反应的离子方程式:__H_3_P_O_4_+__O_H__-_=_=_=_H_2_P_O__- 4 _ +__H__2_O__、_H_2_P_O__-4 _+__O_H_-__=_=_=_H_P_O__24-_+__H__2_O_、_H_P__O_24-_+__O__H_-_=_=_=_P_O__34-_+__H_2_O__。 (3)Ka1=_1_0_-__2 _,Ka2=_1_0_-_7_.1_,Ka3=_1_0_-__12_.2_。
B
•
C. b点对应溶液中Q>KBsp
•
D. a、c点对应的Ksp相等
AgCl(s)
Ag+(aq)+Cl-(aq)
• 真题演练
(2022·广州期末)已知298 K时,Ksp(CuS)=6.3×10-36,Ksp(MnS)=2.5×10-13,随着温度的升高两者的Ksp 都增大。298 K时,饱和溶液中p(S2-)和p(M2+)的关系如图所示,其中p(S2-)=-lgc(S2-),p(M2+)=-lgc(Cu2+)
线下方为不饱和溶液 AgCl的沉淀溶解平衡图像
2020年高考化学专题复习《电解质溶液中强碱滴定二元弱酸曲线分析》

2020届高三化学高考专题复习:电解质溶液中强碱滴定二元弱酸曲线分析电解质溶液1、常温下,向10mL 0.2mol/L草酸溶液中逐滴加入等浓度的NaOH溶液,溶液中各微粒的物质的量与混合溶液pH的关系如图所示, 下列说法正确的是( )A.当V(NaOH溶液)< 10mL时,溶液中可能存在:c(Na+)=2c(C2O42-)+c(HC2O4-)B.当V(NaOH溶液)=10mL时,溶液中水的电离程度比纯水大C.当V(NaOH溶液) =15 mL时,溶液中存在: c(Na+)>c(HC2O4-)>c(C2O42-)D.当V(NaOH溶液)=20mL时,溶液中存在:c(OH-) =2c(H2C2O4)+c(H+)+c(HC2O4-)2、已知:pKa=-lgKa,25℃时,H2A的pK a1=1.85,pK a2=7.19,用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示。
下列说法正确的是( )A.c点所得溶液中: c(A2-)=c(HA-)B.b 点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)C.A2-水解平街常数K h(A2-)=10-7.19D.a点所得溶液中,V0=10mL3、常温下,向10mL 0.2mol·L-l草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液。
有关微粒的物质的量与混合溶液的pH有如右图关系,下列说法正确的是( )A.HC2O4-在溶液中水解程度大于电离程度B.当V (NaOH) =10 mL时溶液中存在:c(HC2O4-)+c(C2O42-)+c(H2C2O4)=0.1mol·L-lC.当V (NaOH) =15mL时,溶液中存在:c(Na+)>c(HC2O4-)>c(C2O42-)>c (OH-)>c(H+)D.当V (NaOH) =20 mL时,溶液中存在:c(OH-) =c (HC2O4-)+c (H2C2O4)+c(H+)4、已知:常温下,H2CO3K a1=4.2×10-7,K a2=5.6×10-11;某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(a)随溶液pH 变化关系如下图所示,下列叙述错误的是( )A.在pH=4.4 的溶液中:3c(HR-)=c(Na+)+c(H+)-c(OH-)B.向Na2CO3溶液中加入少量H2R溶液,发生反应:2CO32-+H2R==2HCO3-+R2-C.等体积等浓度的NaOH 溶液与H2R溶液混合,所得溶液中水的电离程度比纯水大D.在pH=3 的溶液中,三种微粒的浓度满足关系式: c(R2-)c(H2R)/c(HR-)2=10-3.15、常温下0.1mol/L的H2A溶液中H2A、HA-、A2-三者中所占物质的量分数随pH变化的关系如图所示.下列表述正确的是( )A.在含H2A、HA-、A2-的溶液中,通入少量HCl,HA-的物质的量分数一定变大B.将等物质的量的NaHA、Na2A溶于水中,所得溶液中存在:c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-)C.在0.1mol/L NaHA 溶液中,各离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)D.将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.26、常温下,向20mL0.2.L-1H2A溶液中滴另加0.2mol.L-1NaOH溶液。
2020最新版高考化学大二轮优选习题 考前强化练14 电解质溶液图像题

考前强化练14 电解质溶液图像题1.(2018安徽江淮十校高三联考)25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL a mol·L-1的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。
已知N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法不正确的是( )A.图上四点离子种类相同B.a=0.108C.N、Q两点的:N>QD.M点溶液中存在:c(H+)=c(OH-)+2c(NH3·H2O)+c(N)答案C解析盐酸与氨水混合后的溶液中只含有H+、N、OH-、Cl-四种离子,所以图上四点离子种类相同,故A项正确;N点溶液中存在的电荷守恒式为:c(H+)+c(N)=c(OH-)+c(Cl-),已知N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),联立得:c(NH3·H2O)+c(N)=c(Cl-),说明N点溶液中的溶质只有NH4Cl,即滴加10.8 mL氨水时恰好与盐酸完全中和,所得溶液为NH4Cl溶液,由NH3·H2O+HCl NH4Cl+H2O可知:0.10 mol·L-1×10.8×10-3L=a mol·L-1×10.00×10-3L,则a=0.108,故B项正确;,NH3·H2O的电离常数K b(NH3·H2O)只随温度的变化而变化,恒温下电离常数不变,即N、Q两点的值相等,故C项错误;M点滴加氨水5.4 mL,完全反应后所得溶液为等浓度的HCl和NH4Cl的混合溶液,溶液中存在电荷守恒c(H+)+c(N)=c(OH-)+c(Cl-)和物料守恒2c(NH3·H2O)+2c(N)=c(Cl-),联立可得c(H+)=c(OH-)+2c(NH3·H2O)+c(N),故D项正确。
2020届高考化学二轮复习 高考选择客观题:电解质溶液有关图像题型的专题复习(共11页)

•
3.书院除了要求学生熟读“四书五经”, 还锻炼 学生们 写八股 文的能 力,熟 悉八股 文的格 律、步 骤等。 唐朝和 宋朝的 科举考 试,策 问一科 是学生 们的重 点复习 对象。
•
4.文章通过对比,论证了只有完成由 传统经 济模式 到新动 能模式 的转型 升级, 中国经 济才有 无可限 量的未 来这一 观点。
•
7.小说结尾聚焦于父亲与林掌柜的三 举杯, 这一情 景极具 仪式感 ,既是 雪夜酒 叙情节 的收束 ,也是 全文的 升华, 带给读 者无限 遐想。
•
8.作者指出人之所以能适应人生境遇 的种种 变化, 就是因 为这些 变化是 在相当 长的时 间里达 到的。
•
9.时间之所以让人感到渺茫和不可思 议,是 因为和 空间相 比,时 间既无 法把握 ,又无 法挽留 。
选择客观题:电解质溶液有关图像题型的专题复习
全国卷Ⅰ近年来客观题电解质溶液的考查的知识点分布
年17 T11
弱电解质 电离平衡
▲
▲
▲
溶液稀释 及酸碱性
▲
▲
考点分布
水的离子 积及pH
▲
盐类水 难溶电
解
解质
▲
▲
形式:一般以图像题形式考查溶液中各种平衡的辨析, 溶液酸碱性的判断,离子浓度大小的比较或关系,及 溶度积常数的应用
A.曲线I和曲线II分别代表的 是CH3COOH和HCN B.点③和点⑤所示溶液中: c(CH3COO-)=c(CN-) C.点①和点②所示溶液中: c(CH3COO-)-c(CN-) =c(HCN)-c(CH3COOH) D.在点②和③之间(不包括端点) 存在关系 (Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子)
2020届高考化学二轮复习12题题型各个击破——沉淀溶解平衡曲线图形分析(选择专练)

2020届届届届届届届届届12届届届届届届届——沉淀溶解平衡曲线图形分析(大题专练)1.常温下,向10mL0.10mol/L CuCl2溶液中滴加0.10mol/L Na2S溶液,滴加过程中−lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。
下列说法正确的是()A. K sp(CuS)的数量级为10−21B. 曲线上a点溶液中,c(S2−)⋅c(Cu2+)>K sp(CuS)C. a、b、c三点溶液中,n(H+)和n(OH−)的积最小的为b点D. c点溶液中:c(Na+)>c(Cl−)>c(S2−)>c(OH−)>c(H+)2.已知pCa=−lgc(Ca2+),K sp(CaSO4)=9.0×10−6,K sp(CaCO3)=2.8×10−9,向10mL CaCl2溶液中滴加0.1mol/L的Na2SO4溶液时,溶液中pCa与Na2SO2溶液体积(V)的关系如图所示(实线),下列有关说法正确的是(已知lg3=0.48)A. Y值为3.48B. a与b两点c(Ca2+)之比为50:3C. 原CaCl2溶液浓度为1mol/LD. 若把0.1mol/L的Na2SO4溶液换成0.1mol/L的Na2CO3溶液则图象在终点后变为虚线部分3.常温下,用0.100mol·L−1的NH4SCN溶液滴定25.00mL0.100mol·L−1AgNO3溶液,以NH4Fe(SO4)2·12H2O为指示剂,测得溶液中pSCN=‒lgc(SCN−)、pAg=‒lgc(Ag+)随加入NH4SCN溶液的体积变化如图所示。
已知:Ag++SCN−⇌AgSCN↓,K sp(Ag2SO4)=1.4×10−5。
下列说法错误的是()A. 滴定至终点时溶液颜色变为红色,且振荡后不褪色B. 该温度下AgSCN的溶度积常数K sp=1.0×10−12C. 为防止指示剂失效,溶液应维持酸性D. 当加入15.00mLNH4SCN溶液时,溶液中c(SO42−)=0.14mol·L−14.某温度下,向20mL0.1mol·L−1BaCl2溶液中滴加0.1mol·L−1Na2CO3溶液,滴加过程中−lgc(Ba2+)与Na2CO3溶液体积的关系如图所示[已知:lg2=0.3,K sp(MgCO3)=3.5×10−8]。
高考化学二轮复习 电解质溶液各类图像的分析

3.滴定直线图像的分析与运用 常温下,向二元弱酸H2Y溶液中滴加NaOH溶液,所得混合溶液的pH与离 子浓度变化的关系如图所示: 回答下列问题: (1)向二元弱酸H2Y中滴加NaOH 溶液,顺次反应的离子方程式为 _H_2_Y_+__O__H_-__=_=_=_H_2_O_+__H__Y_-__、__H_Y__-_+__O_H__-_=_=_=_H__2_O_+__Y_2_-___。
2.滴定曲线图像中“交叉点”的分析与运用 [实例1] T ℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶 液中三种微粒H2C2O4、HC2O-4 、C2O24-的物质的量分数(δ)与pH的关系如图 所示:
回答下列问题:
(1)写出H2C2O4的电离方程式及电离安稳 常数表达式: ①_H_2_C_2_O_4____H__+_+__H_C_2_O_- 4__,
(2)NaHS溶液 水解方程式:_H_S__-_+__H_2_O____H__2S_+__O__H_-__; 离子浓度大小关系:_c_(_N_a_+_)_>_c_(_H_S_-__)>_c_(_O_H__-_)_>_c_(H__+_)_>_c_(_S_2-__)_; 电荷守恒:_c_(N__a_+_)_+__c_(H__+_)_=__c_(H__S_-_)_+__2_c_(S__2-__)+__c_(_O_H__-_)_; 物料守恒:__c_(N__a_+_)_=__c_(S_2_-_)_+__c_(_H_S_-_)_+__c_(_H_2_S_)_; 质子守恒:_c_(_O_H__-_)_=__c_(H__+_)_+__c_(H__2S__)-__c_(_S_2_-_)_。
[实例3] 硫酸钡是一种比碳酸钡更难溶的物质。常温下-lg c(Ba2+)随-lg c( CO23- ) 或-lg c( SO24-)的变化趋势如图所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、【2019年高考新课标Ⅰ卷】298K时,在20.0mL 0.10mol /L 氨水中滴入0.10 mol/L的盐酸,溶液的pH与 所加盐酸的体积关系如图所示。已知0.10 mol/L氨水的 电离度为1.32%,下列有关叙述正确的是( D )
酸碱中和滴定中 指示剂的选择、起始点、
溶液显中性的点所代 表的意义
lg
V V0
的变化如图所示,下列叙述错误的
考查弱电解质 的电离平衡, 横坐标、纵坐 标、起始点所 代表的意义
A.MOH的碱性强于ROH的碱性 B.ROH的电离程度:b点大于a点 C.若两溶液无限稀释,则它们的c(OH-)相等 c ( M )
D.当 lg V =2时,若两溶液同时升高温度,则 c ( R ) 增大
•
2朗读在短时记忆向长时记忆转化的过 程中充 当了刺 激物的 角色。 在读的 过程中 ,我们 需要将 更多的 注意力 集中在 所要记 忆的信 息上, 也更能 帮助我 们记住 它。
•
3朗读是加深记忆的有效方法,但并不 是唯一 的方法 。记忆 规律, 还有许 多未解 之谜, 有待我 们继续 探索和 发现。
(1)“一半点”:溶质: n(C物H3料CO守O恒Hc):(nC(HC3HC3OCOO-O)+Nca()C=1H:31COOH)=2 c(Na+)
因为Ka(CH3COOH)>Kh(CH3COO-) , CH3COOH的电离 CH3COO-的水解所以,离子浓度大小: c(CH3COO-)> c(Na+)> c(H+)>c(OH-)
例题3.【2018年高考浙江卷第12题】氯在饮用水处理中常用
作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体
系中存在以下平衡关系:
Cl2(g) Cl2(a3; H2O
HClO + H+ +Cl- K2=10-3.4
HClO
H+ + ClO-
Ka=?
•
4.草书特点是结构简省,笔画连绵; 楷书由 隶书逐 渐演变 而来, 更趋简 化,字 形由扁 改方, 平正而 不呆, 齐整而 不拘。
•
5.行书是在隶书的基础上发展起源的 ,介于 楷书、 草书之 间的一 种字体 ,是为 了弥补 楷书的 书写速 度太慢 和草书 的难于 辨认而 产生的 。
•
6.会赏析其语言,如从遣词、用句、 修辞等 方面揣 摩、推 敲、理 解作者 炼字达 意的技 巧;
例题1.常温下用0.10 mol·L-1 NaOH溶液分别滴定20.00mL 浓度均为0.10mol·L-1 CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如右图。下列说法正确的 是( C)
A.曲线I和曲线II分别代表的
是CH3COOH和HCN B.点③和点⑤所示溶液中: c(CH3COO-)=c(CN-) C.点①和点②所示溶液中: c(CH3COO-)-c(CN-) =c(HCN)-c(CH3COOH) D.在点②和③之间(不包括端点)
•
7.从作家作品的语言风格的比较中, 从用韵 、节奏 、音调 三个方 面去品 味其语 言的音 乐美、 节奏美 、韵律 美。
•
8.本题考查中心论点的提炼。从文章 的标题 “如何 看待数 字时代 的文学 评论” 来看, 文章的 中心论 点是对 这一论 题的回 答。解 答时, 我们要 在整体 阅读的 基础上 ,从文 中找出 最能回 答该问 题的句 子,作 为本文 的中心 论点。
V0
电解质溶液图像分析应抓住的几个点: 1、横坐标和纵坐标所代表的的物理量及单位。
2、曲线代表的物理量的走向
3、重要的几个点:起始点、交叉点、拐点; 酸碱中和反应的“恰好”反应点、呈“中性”的点、
反应“一半”的点、过量点
典例:向CH3COOH溶液中逐滴加入NaOH溶液,分析: 电荷守恒:c(Na+)+c(H+)= c(CH3COO -)+ c(OH-)
•
9.使用了举例论证,以人们对待周六 观点这 个电视 栏目的 态度为 例,具 体有力 的论证 了关于 评论的 影响力:评论是 否有效 取决于 其具体 内容, 评论也 绝不是 简单的 对与错 的问题 。为下 文引出 中心论 点作铺 垫。
•
10.培根是英国文艺复兴时期最重要 的散文 家、哲 学家之 一。从 他的散 文中我 们可以 感受到 文艺复 兴时期 的思想 者如何 在旧的 社会结 构和思 想体系 日趋瓦 解之际 ,致力 于探讨 并树立 新的信 念、规 范和道 德。
例题2.【2018广东理综化学】一定温度下,水溶液中 H+和OH-的浓度变化曲线如图2,下列说法正确的是 (C)
考查水的电 离平衡、水的 离子积常数
A.升高温度,可能引起有c向b的变化 B.该温度下,水的离子积常数为1.0×10-13 C.该温度下,加入FeCl3可能引起由b向a的变化 D.该温度下,稀释溶液可能引起由c向d的变化
选择客观题:电解质溶液有关图像题型的专题复习
全国卷Ⅰ近年来客观题电解质溶液的考查的知识点分布
年份 题 号
2019 T13 2018 T13 2017 T11
弱电解质 电离平衡
▲
▲
▲
溶液稀释 及酸碱性
▲
▲
考点分布
水的离子 积及pH
▲
盐类水 难溶电
解
解质
▲
▲
形式:一般以图像题形式考查溶液中各种平衡的辨析, 溶液酸碱性的判断,离子浓度大小的比较或关系,及 溶度积常数的应用
存在关系 (Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子)
(旧题重现)298K时,在100 mL 1 mol·L-1 H2R稀溶液中
滴入1 mol·L-1 NaOH溶液,溶液中HR一、R2-的物质的量随pH 变化的关系如下图所示。下列有关叙述正确的是( A )
A.pH=4时,溶液中c(HR一)∶c(R2一)=l∶10 B.滴入150 mL NaOH溶液时,溶液中c(Na+)>c(HR一)>c(R2一) C.a点溶液中存在c(Na+) +c(H+) =c(HR一)+c(R2一)+c(OH一) D.c点溶液中含R的微粒有HR-、H2R、R2-
(2)“恰好完全反应点”:溶质:CH3COONa
(3)“中性点” 溶质: CH3COONa和 CH3COOH(少量) c(H+)=c(OH-) ,利用电荷守恒得出c(CH3COO -)=c(Na+)
离子浓度大小: c(CH3COO-)= c(Na+)> c(H+)=c(OH-)
(4)“过量点” 溶质:CH3COONa和NaOH
A.该滴定过程应该选择酚酞作为指示剂 B.M点对应的盐酸体积为20.0 mL C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) D.N点处的溶液中pH<12
2.【2018新课标Ⅰ卷理综化学】浓度均为0.10mol/L、
体积均为V0的MOH和ROH溶液,分别加水稀释至体
积V,pH随 是( D ) :学,科,网]
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH 变化的关系如图所示。下列表述正确的是( C )
A.Cl2(g)+ H2O K=10-10.9
2H+ +ClO- +Cl-
B.在氯处理水体系中,c(HClO) +
c(ClO-) =c(H+)-c(OH-)
C.用氯处理饮用水时,pH=7.5时杀菌
效果比pH=6.5时差
D.氯处理饮用水时,在夏季的杀菌效
果比在冬季好
作业:练习卷P27、28并复习电解质 溶液的相关知识点
•
1记忆是在头脑中积累和保存个体经验 的心理 过程, 是人最 基本的 智慧之 一,联 结着我 们的过 去与现 在。一 切经验 都要经 过编码 、储存 和提取 才能形 成完整 的记忆 过程。
