第九章_羰基化合物红外光谱
羰基的红外吸收峰范围

羰基的红外吸收峰范围羰基是含有碳氧双键的有机官能团,是化学中十分常见的一种官能团。
羰基的红外吸收峰范围的研究是红外光谱领域的重要研究之一,因为它对于分析有机化合物和确定它们的结构非常有帮助。
本文将介绍羰基的红外吸收峰范围,包括其基本特性、红外光谱分析中的应用以及相关的研究成果。
羰基的基本特性羰基可以分为酮羰基和醛羰基两种类型。
酮羰基的化学式为R1COR2,其中R1和R2为有机基团;醛羰基的化学式为RCHO,其中R为有机基团。
羰基的红外吸收峰范围取决于它的化学结构、取代基的种类和位置、以及不同官能团之间的相互作用。
羰基的红外吸收峰范围通常在1600-1800 cm-1的波数区间内,这个范围被称为羰基伸缩振动区域。
在这个区域内,羰基的红外吸收峰可以分为两类:C=O伸缩振动和C-CO振动。
C=O伸缩振动通常在1700-1750 cm-1之间,而C-CO振动通常在800-1200 cm-1之间。
羰基的红外光谱分析中的应用羰基的红外吸收峰范围在有机化学中广泛应用。
下面将介绍一些具体的应用:1.功能化合物的鉴定羰基是许多有机化合物的重要结构单元。
通过红外光谱分析,我们可以观察到不同化合物中羰基的吸收峰,比较它们的差异,从而鉴定其结构类型。
例如,在酮类化合物中,C=O伸缩振动的吸收峰通常出现在1715-1735 cm-1之间,而在醛类化合物中,则出现在1660-1735 cm-1之间。
2.溶剂的鉴定溶剂也包含着许多有机官能团。
在分析含有溶剂的样品时,通常会出现来自溶剂中羰基的吸收峰。
这个峰可以用来确定所用溶剂的类型和浓度。
例如,DMSO中的C=O伸缩振动带出现在1730-1740 cm-1之间,而乙醇中的C=O伸缩振动带则在1700-1735 cm-1之间。
3.化学反应的监测化学反应通常会产生新的化学键,并在红外光谱上留下独特的吸收峰。
在研究化学反应动力学过程中,可以通过监测反应物和产物上的羰基吸收峰的变化,来研究反应的进展情况和反应速率等参数。
本科生有机课堂笔记(老师的重点提问)
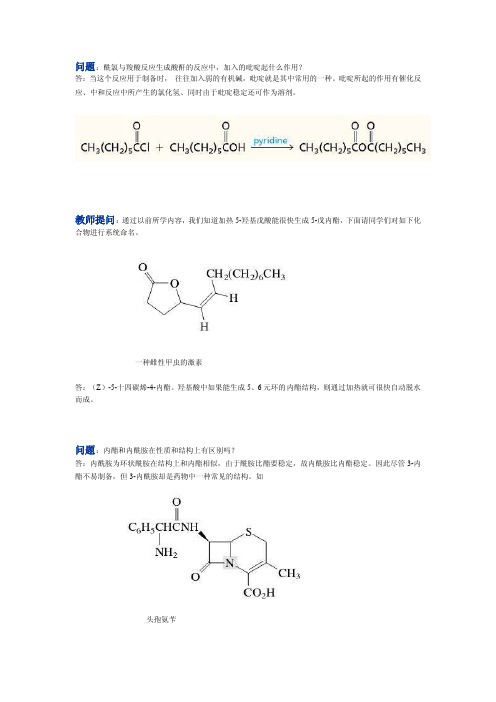
问题:酰氯与羧酸反应生成酸酐的反应中,加入的吡啶起什么作用?答:当这个反应用于制备时,往往加入弱的有机碱,吡啶就是其中常用的一种。
吡啶所起的作用有催化反应、中和反应中所产生的氯化氢、同时由于吡啶稳定还可作为溶剂。
教师提问:通过以前所学内容,我们知道加热5-羟基戊酸能很快生成5-戊内酯,下面请同学们对如下化合物进行系统命名。
一种雌性甲虫的激素答:(Z)-5-十四碳烯-4-内酯。
羟基酸中如果能生成5、6元环的内酯结构,则通过加热就可很快自动脱水而成。
问题:内酯和内酰胺在性质和结构上有区别吗?答:内酰胺为环状酰胺在结构上和内酯相似,由于酰胺比酯要稳定,故内酰胺比内酯稳定。
因此尽管3-内酯不易制备,但3-内酰胺却是药物中一种常见的结构。
如头孢氨苄在水溶液中能稳定存在,但由于四元环存在的张力,可以较为容易地与亲核试剂反应,从而达到消灭病菌的作用。
问题:《有机化学》第三版407页中提到只含一个a-氢原子的酯能否进行Claisen酯缩合反应?答:从Claisen酯缩合反应机理中可知当用醇钠作碱时,只含一个a-氢原子的酯由于在最后一步无法通过去质子生成稳定的负离子,因此在平衡中只存在痕量的Claisen酯缩合反应产物。
如在通常的Claisen酯缩合反应反应条件下,基本无缩合产物。
但如果用非常强的缩合剂如三苯甲基钠,也可进行。
原因在于缩合过程中,每一步反应的平衡在产物方,这是与用醇钠作缩合剂的区别。
教师提问:以下两种胺在Kb值上有显著差异,哪一个是更强的碱?为什么?四氢喹啉四氢异喹啉答:后者是更强的碱。
由于前者氮原子上的孤对电子会向苯环离域,降低了氮原子上的电子云密度。
而后者没有共轭,因此后者为更强的碱。
问题:在NMR中,3-硝基苯乙烯中Ha的偶合的情况如何?答:这是属于较为复杂的偶合模式。
乙烯基端位的两个H,对Ha来说是磁不全同,也就是说它们对Ha的偶合常数不同。
3-硝基苯乙烯中Ha在NMR中的裂分方式为“二重峰的二重峰”。
羰基的红外光谱特征峰

羰基的红外光谱特征峰羰基是一种常见的官能团,具有独特的红外光谱特征峰。
羰基是由碳和氧原子组成的双键,常见的有酮、醛、酰氯、酰胺、酸酐等。
它们在红外光谱中的特征峰是由于碳氧双键的振动和伸缩引起的。
酮和醛是两种常见的化合物类型,它们都含有羰基。
酮的特征峰通常在1700-1750 cm-1之间,对称拉伸振动峰位于1710-1720 cm-1,而不对称拉伸振动峰位于1740-1750 cm-1、醛的特征峰通常在1700-1780 cm-1之间,对称拉伸振动峰位于1710-1740 cm-1,而不对称拉伸振动峰位于1740-1780 cm-1、这些特征峰的位置由于分子结构的不同而略有变化。
酰氯是由羰基和氯原子组成的化合物。
酰氯的特征峰通常在1770-1810 cm-1之间,对称拉伸振动峰位于1790-1810 cm-1,而不对称拉伸振动峰位于1770-1790 cm-1酰胺是由羰基和氮原子组成的化合物。
酰胺的特征峰通常在1640-1690 cm-1之间,对称拉伸振动峰位于1660-1690 cm-1,而不对称拉伸振动峰位于1640-1660 cm-1酸酐是由羰基和羧基组成的化合物。
酸酐的特征峰通常在1700-1780 cm-1之间,对称拉伸振动峰位于1710-1740 cm-1,而不对称拉伸振动峰位于1740-1780 cm-1需要注意的是,以上提到的特征峰的位置是一般性的参考值,可能会因分子结构的不同而有所变化。
其他因素,如溶剂和实验条件等,也可能会对特征峰位置产生影响。
除了特征峰的位置,特征峰的强度和形状也是红外光谱中的重要信息。
特征峰的强度反映了羰基的吸收强度,而特征峰的形状则可以提供关于分子结构和键的对称性的信息。
总的来说,羰基的红外光谱特征峰提供了一种用于确定羰基化合物的常见官能团的方法。
通过分析这些特征峰的位置、强度和形状,可以确定羰基化合物的结构和功能基团,从而在有机化学、药物化学和材料科学等领域中具有重要的应用价值。
各类有机化合物的红外光谱

4. 芳烃
芳烃的特征吸收:(与烯烃类似) 芳烃的特征吸收:(与烯烃类似) :(与烯烃类似
• υ=C-H 3000~3100 cm-1 (芳环C-H伸缩振动) 3000~ 芳环C 伸缩振动) =C- • υC=C =C 1650~ 芳环骨架伸缩振动) 1650~1450 cm-1(芳环骨架伸缩振动) • γ面外=C-H 900~650 cm-1 用于确定芳烃取代类型 900~ 用于确定 确定芳 取代类型 C 芳环取代基性质无关 而与取代个数有关, 取代基性质无关, (与芳环取代基性质无关,而与取代个数有关,取代 基个数越多, 芳环上氢数目越少, 基个数越多,即芳环上氢数目越少,振动频率越 低。) • γ面外=C-H C 2000~ 倍频 2000~1600 cm-1(w) 用于确定芳 用于确定芳烃取代类型
C4H9-O-C4H9 -
丁醚的红外光谱图
1210-1000cm –1是醚键的不对称伸缩振动 υC-O-C 是醚键的不对称伸缩振动 -
7. 胺和铵盐
CH3CH2CH2CH2NH2
丙胺的红外光谱图
CH3CH2CH2NH3+Cl-
丙胺盐的红外光谱图
8.羰基化合物 8.羰基化合物 • 因υC=O 非常特征,羰基化合物易与其他 非常特征, 有机物区分。 有机物区分。 • 不同的羰基化合物的区分主要依据: 不同的羰基化合物的区分主要依据: • υC=O 位置 • 其他辅助信息
3. 炔烃
端基炔烃有两个主要特征吸收峰: 端基炔烃有两个主要特征吸收峰: 一是叁键上不饱和C 伸缩振动υ 约在3300cm 一是叁键上不饱和C-H伸缩振动υ≡C-H约在3300cm-1处产 叁键上不饱和 生一个中强的尖锐峰 二是C 伸缩振动υ 吸收峰在2140 二是C≡C伸缩振动υ≡C-C吸收峰在2140 ~2100cm-1。 位于碳链中间则只有υ 若C≡C位于碳链中间则只有υ≡C-C在2200cm-1左右一个尖 在对称结构中, 峰,强度较弱。如果在对称结构中,则该峰不出现。 强度较弱。如果在对称结构中 则该峰不出现。
第九章 羰基化合物(有机)
6
第二节 醛酮的物理性质及光谱性质
由于羰基的偶极矩,增加了分子间的吸引力,因 此,醛酮的沸点比相应相对分子质量的烷烃高,但比 醇低。醛酮的氧原子可以与水形成氢键,因此低级醛 酮能与水混溶。脂肪族醛酮相对密度小于1,芳香族 醛酮相对密度大于1。
7
IR :
羰基的红外光谱在1750-1680 cm-1之间有一个非常强
内酯
羰基受OH- 进攻生成氧负离子的醛为氢的供体,被 氧化成酸,另一半醛为氢的受体,被还原成醇 甲醛总是还原剂
61
HCHO CH3CHO thin base HOCH2
CH2OH CHO
HCHO HOCH2
CH2OH CH2OH CH2OH
CH2OH thick base
五、其他的反应 一)、Wittig 反应
第九章 醛和酮 (carbonyl compounds)
H O H formaldehyde R aldehyde H O R O R` ketone
1
第一节 结构、分类和命名 一、结构
1 C=O双键是由一个键和一个键组成的。
2 C=O是一个极性基团,具有偶极矩。
2
二、分类 三、命名
一) 普通命名法
4
2、脂环酮的羰基在环内时,称环某酮,羰基在环 外时将环作为取代基。多元醛、酮的命名与多元 醇类似。
4-氧代戊醛
3-烯丙基-2,4-戊二酮
5
2’-氧代环己基甲醛
2-羟基环己酮
3、芳基作为取代基
4、多官能团,母体官能团的选择顺序:
RCOOH>RSO3H >(RCO)2O >RCOOR > RCOX >RCONHR >RCN >RCHO > RCOR >ROH >ArOH >RNHR >ROR
羰基化合物的红外光谱

O
O
O
丁酸酐的红外光谱图
I. C=O:1839,1750 cm-1(双峰); II. C-O-C:1050 cm-1 (b) III. 2960,2926,2850;IV.1450,1380;V. 760
p98,图2.112
O OO
C-O-C
1,8-萘二甲酸酐的红外光谱图(p98)
I. C=O:1772,1743(双带); II. 1308,1019 (环酸酐,双带); III. 1600, 1584, 1510, 1450;IV. =C-H: 781
1760(s)
1170~1050(s)
Cyclo anhydrides OOO
OOO
O O O
2020/5/16
1870~1820(s) 1800~1750(vs)
1800(s)1750(vs)
1805~1780(s) 1785~1755(vs)
1310~1210 952~909
(s,b) (双带)
II CHO中C-H伸缩振动与C-H面内弯曲倍频振动发生 Fermi共振,在2750cm-1和2850cm-1的有两个弱 峰。
注意,烷基中的C-H伸缩峰通常不会在光谱中延伸至这 样出若右现同的,时位而存置在27。ν5C02=c08峰m50-,1c峰几m在-乎1光峰可谱通以上常肯不以定与饱醛其和基它烃存νν在CC--。HH的峰肩重峰叠,
C=O正常伸缩峰出现在1715 cm-1 附近。共轭使吸收峰向 右移动。在3500~3350cm-1有时出现小的νC=0倍频峰。
2020/5/16
16
C4H10O
O
羰基的倍频吸
收3400 cm-1
丁酮的红外光谱图
I.
羰基化合物的红外光谱

2020/5/16
16
C4H10O
O
羰基的倍频吸
收3400 cm-1
丁酮的红外光谱图
I.
C=O:1720 cm-1;
II. C-C-C:1174 cm-1;
III. 2960,2850;IV. 1450,1380;V. 775
II CHO中C-H伸缩振动与C-H面内弯曲倍频振动发生 Fermi共振,在2750cm-1和2850cm-1的有两个弱 峰。
注意,烷基中的C-H伸缩峰通常不会在光谱中延伸至这 样出若右现同的,时位而存置在27。ν5C02=c08峰m50-,1c峰几m在-乎1光峰可谱通以上常肯不以定与饱醛其和基它烃存νν在CC--。HH的峰肩重峰叠,
III. 2960,2850;IV. 1450,1380
Lactone
R
O
O
-:1750~1735
ROO
-:1780~1754
R
O
O
-:1885~1820
R
O
O
-:1720
ROO
-:1750
,-不饱和内酯, 吸收右移
R
O
O
-:1760
2020/5/16
ROO
-:1800
双键与-O-连接 的内酯,吸收左移
2020/5/16
6
Acid halides
C=O:1815~1770 C=O(与其它基团共轭):1780~1750(s)
O Cl
O C RX
p44,图2.32
1774
875的倍频与C=O发生费米共振,羰基 的吸收有裂分,双峰相距40 cm-1
羰基化合物的分析(新)1

乙 酰 乙 酸 乙 酯 的 红 外 光 谱 图
乙酰乙酸乙酯的红外光谱分析
乙酰乙酸乙酯具两个羰基,并且这两个羰基碳连接的基团具有不同的性质,在图中这 两 个羰基都有明显的体现,接下来就通过红外光谱图来经行分析。 首先看到1731 1746处有两个最强吸收峰,可判断为羰基的吸收峰,对于为什么两个峰具 有差别,将会通过下面的结合物质结构经行分析,在看到1650于1632处出现了酯羰基与碳碳 双键的伸缩振动吸收,同样下面将通过结合物质结构来经行仔细分析,同时在1163处有一强 吸收峰,出现了酯基的C-O伸缩振动,同时在1042处也出现了C-O-C的伸缩振动,同样为酯基 的特征峰,剩下的峰都为甲基与亚甲基的C-H键伸缩振动吸收峰。 接下里通过结合物质结构来分析具体的峰位置与原因,先看到羰基的两个吸收峰,一个在 1731,一个在1746,在看到结构中,一个羰基为酮羰基,另一个为酯羰基,酯羰基的羰基碳 与氧相连,而氧上的孤对P电子与碳氧的π键产生P-π共轭,导致酯羰基的电子增多,极性增 强,吸收频率升高,而酮羰基的羰基为正常羰基,没有明显的影响,在看到酮羰基,有共振结 构式可以知道具有酮烯互变式异构,所以在图中出现了碳碳双键的吸收峰,再看到酯基的C-O 键,同样由于共轭作用也式其电子增多,导致频率升高,再看到物质中的甲基与亚甲基,可以 看到甲基与亚甲基中的C-H键都有与碳氧的π键产生σ-π超共轭效应,同样为供电子效应,导 致了吸收峰的多重重叠。
苯甲酸的RAMAN光谱图
苯甲酸的拉曼光谱分析
拉曼是通过激光的散射方法来测定化合物的结构信息的,并且可以检测到骨架结构,首 先看到图谱,在196为COOH面内摇摆振动,618 797为苯环的C-H面外弯曲振动,并且1003 为苯环的单取代特征峰,而1400~1800内的几个峰为苯环的环呼吸特征峰,剩下的3000左右 的几个峰都为C-H的伸缩振动,由此得出此物质为单取代苯,再看到1028为C-H的面内摇摆 与CO的伸缩振动,而1291可能为CO伸缩振动+C-OH面内弯曲振动,或者C-H面内摇摆,由 于羰基在拉曼散射中的强度非常弱,通常没法观察出,在结合苯甲酸的红外光谱图一起分析, 可以得出此物质为单取代的羧酸苯,由于拉曼中与红外中没有看出甲基与亚甲基的峰,所以 可以推测此物质为苯甲酸 接下来通过物质结构来分析拉曼谱图的峰位置,化合物中的共轭与诱导效应都会影响分 子偶极距的改变,导致拉曼图谱的改变,但影响都非常小,不同于在红外光谱中非常明显的 影响,所以在激光拉曼中并没有太大的结构导致的误差,而其他的误差出现则为样品的浓度 大小影响。 最后,通过苯甲酸的红外与拉曼光谱分析可得,通过拉曼与红外相结合,可以得出物质 的准确结构信息。
有机化学第九章__羰基化合物(三改)---《有机化学》人卫药学5版倪沛洲

第九章 羰基化合物碳原子以双键和氧原子相连 的官能团称羰基(carbonyl )。
有机分子中含有羰基的化合物称作羰基化合物(carbonyl compounds )。
羰基碳与一个烃基和一个氢相连的化合物称作醛(aldehyde,甲醛中的羰基碳与两个氢相连);羰基碳与两个烃基相连的化合物称作酮(ketone )。
C H HO C RHO 甲醛formaldehyde醛aldehy de酮k etoneC R R O1羧酸及其衍生物分子中也含有羰基,但它们与醛、酮的性质相差较大,将在第十一章二、四和第十二章二、三中另外讨论。
本章只讨论醛、酮。
一、结构和命名(一)结构醛、酮分子中的羰基碳以双键与氧结合,其成键情况与乙烯有些相似。
碳原子是sp 2杂化,三个sp 2杂化轨道处于一个平面内,其中一个杂化轨道与氧形成σ键。
碳原子上的p 轨道与氧的p 轨道彼此重叠形成π键,并与三个σ键所构成的平面垂直,因此,羰基的碳氧双键是由一个σ键和一个π键组成的,如图9-1(a )所示。
图9-1 羰基的结构示意图由于氧的电负性比碳大,成键处的电子云并不是均匀地分布在碳氧之间,而是偏向于氧,氧带部分负电荷(δ-),而碳带部分正电荷(δ+),所以,羰基是一个极性基团。
参见图9-1(b ),(c )。
这一点,从羰基化合物的偶极矩也可以反映出来。
例如:C O ( )R C H O 可简写作 R CHO 。
δ(b) 羰基的极性C O H 3CHC O H 3CCH 3×-30μm=9.4910C C 109.49=mμ-30×(二)命名1.普通命名法 简单醛、酮可采用普通命名法。
分子中含有芳环的醛则将芳基作为取代基,例如:苯基丙醛CH 3CH 2CHO丙醛propanalCHO苯(基)甲醛benzaldehy deCH CHO CH 3-phenylpropanal-22酮则按羰基所连接的两个烃基的名称来命名。
第九章_羰基化合物红外光谱

9.5 p-共轭(中介效应) 酰胺 O=C—N 羰基伸缩 1660 cm-1 酮 O=C—C 羰基伸缩 1715 cm-1 诱导效应X p-共轭
9.6 ketones 酮 RCR, 1715 cm-1,
O RCOCH3, CH3symmetric deformation 1370-1350 cm-1 RCH2COR, CH2 1440-1405 cm-1
1650 cm-1 六元环, 七元环 1750—1700 cm-1,五元环 1760—1730 cm-1,四元环 Cis N-H bending vibration at 1490--1440 cm-1 C-N stretching band at 1350-1310 cm-1
单取代酰胺顺反异构区分 Trans hydrogen bonded
ochbending相互作用只考红红量因素红振红红率稍微上升93红角影响红基化合物ccc红角度数通常情1715cm11745cm11775cm194红红效红1660cm11715cm1红红效红96ketonesrcr1715cm1rcochsymmetricdeformation13701350cm1rchcorch14401405cm1红红效红旋红98共红红红共红通常使红基伸红振红红率降低17001640cm117251705cm1ccco16851660cm1arco17001680cm1arcar16701660cm116701660cm1172010cm1cch2c17551695cm199共红同红形成红红的红红ohnh217071694cm117391725cm116301607cm116491646cm1910红红化合物中的红角效红红红力增加1719cm11719cm11746cm11788cm11822cm1911红红chcho脂肪红红28302810cm127202695cm11390cm1芳香红红28322812cm127452720cm11390cm1红米共振红米共振29002810cm127652747cm1低红吸收红红特征吸收912脂肪红17401720cm1芳香红17101685cm1cclcho
各类化合物的红外光谱特征

各类化合物的红外光谱特征有机化合物的数目非常大,但组成有机化合物的常见元素只有10种左右,组成有机化合物的结构单元即称为基团的原子组合数目约有几十种。
根据上述讨论,基团的振动频率主要取决于组成基团原子质量(即原子种类)和化学键力常数(即化学键的种类)。
一般来说,组成分子的各种基团如C-H、C-N 、C=C、C=O 、C-X等都有特定的红外吸收区域(特征吸收峰),根据特征吸收峰可以推断物质的结构。
所以,有必要对各类有机化合物的光谱特征加以总结。
一、烷烃1. νC-H 3000~2840 C-H伸缩振动频率2. δC-H 1460 和1380 C-H弯曲振动频率3.C-C 1250-800当化合物具有四个以上邻接的CH2基团时,几乎总是在(715-725,通常在720cm-1处)有谱带(CH2以内摇摆),它在鉴别上是有用的。
二、烯烃1. ν=C-H 3010-31002.νC=C1680-16003. δC-H1000-700三、炔烃1. ν≡C-H 3300-3250 峰形较窄,易于OH和NH区别开。
2. δ≡C-H 900-610 宽的谱带3. ν C≡C2140-2100 一元取代炔烃RC≡CH|| 2260-2190 二元取代炔烃四、芳香烃1.νC-H 3080-30102.νC-C 1650-1450 2~4个吸收峰3. 面外弯曲振动(g=C-H ) 900-650五、醇和酚羟基化合物1. νO-H 3700-3500(游离的醇和酚,峰尖、强)|| 3500-3200(缔和的羟基,峰形强而宽)2. δO-H 1500~13003. νC-O 1250~1000六、醚1.脂肪醚1150-10602.芳香醚1270 ~ 1230(为Ar-O 伸缩)1050 ~ 1000 cm-1(为R-O 伸缩)3.乙烯醚:1225-12005、在环氧乙烷类中有三条特征谱带可作为这种基团的存在的标志:1280-1240 环的不对称伸缩振动|| 950-810cm-1 环的对称伸缩振动|| 840-750cm-1七、羰基化合物(包括醛、酮、羧酸、酯、酸酐和酰胺等)1.酮1725-17052.醛1740-1720 2820-2720出现两个强度相等的吸收峰3.羧酸(1)νO-H 3200-2500(液体及固体羧酸)|| 3550(在气相或极稀的非极性溶剂溶液中)(2)nC=O 1730-1700(2)νC-O 1250附近(强峰)(3)δO-H 1400cm-1和920cm-1区域有两个强而宽的吸收峰(4)羧酸盐1580cm-1 和1400cm-1 之间的两个谱带4.酯(1) νC=O1750-1735(2) νC-O-C 1330-10305.酸酐(1)n C=O 在1860-1800cm-1和1800-1750cm-1出现两个强的吸收峰(2) n C-O-C 开链的在1180-1045cm-1,而环状酸酐在1310-1200cm-16.酰胺: 兼有胺和羰基化合物的特点(1)νN-H稀溶液中伯酰胺出现两个中等强度的峰,分别在3500cm-1和3400cm-1附近,浓溶液和固体中由于有氢键发生,将移向3350-3180cm-1低频区仲酰胺在很稀溶液中,在3460-3420cm-1处只出现一个谱带,浓溶液中或固体中缔和体出现在3330cm-1(3)δN-H弯曲振动(酰胺II带)伯酰胺游离态在1600cm-1处,缔合态在1650-1620处,仲酰胺游离态在1550-1510处;缔和体在1570-1515处(4)酰胺还有C-N吸收带(酰胺III带),它们的吸收位置如下:伯酰胺1420-1400cm-1(中);仲酰胺1305-1200cm-1(中)叔酰胺700-620cm-1(中)八、胺和胺盐1.胺:胺有三个特征吸收带即:nNH、δ N-H和nC-N吸收带(1)nNH 3550-3250(2)δ N-H 1650-15402.铵盐伯胺和仲胺的νNH νNH3+ 伯胺盐在3000-2800cm-1之间出现强和宽的吸收带伯胺盐的δNH3+出现在1600-1575cm-1和1550-1504cm-1处两个吸收带仲胺盐的νNH2+ 出现在2700-2250cm-1 区域;δ NH2+ 出现在1620-1560cm-1区域叔胺盐的νNH+ 在2700-2250cm-1 区域出现一个强的宽带或一组较尖的谱带。
红外光谱 主要官能团 分析-1

相关峰是指一组相互依存,相互佐证的吸收峰。
一个基团有数种振动形式,每种红外活性的振动都通常相应给出一个吸收峰。
如芳环化合物相关峰有五种振动形式:、泛频区、、和,可作为佐证苯环存在的依据。
第二节有机药物的典型红外吸收光谱一、脂肪烃类化合物(一)烷烃类化合物烷烃类化合物用于结构鉴定的吸收峰主要有碳—氢伸缩振动()和面内弯曲振动()吸收峰。
1.:在3000 cm-1~ 2845 cm-1范围内出现强的多重峰。
—CH3:2 970 cm-1~2 940 cm-1(s),2 875 cm-1~2 865 cm-1 (m)。
甲氧基中的甲基,由于氧原子的影响,一般在2 830 cm-1附近出现尖锐而中等强度的吸收峰。
—CH2—:2 932 cm-1~2 920 cm-1 (s),2 855 cm-1~2 850 cm-1 (s),环烷烃、与卤素等相连接的—CH2 向高频区移动。
—CH—:在2 890 cm-1附近,但通常被—CH3和—CH2—的伸缩振动所掩盖。
2.:面内弯曲振动出现在1 490 cm-1~1 350 cm-1。
—CH3:~ 1 450 cm-1 (m),~ 1 380 cm-1 (s),峰的出现是化合物中存在甲基的证明。
当化合物中存在有—CH(CH3)2或—C(CH3)3时,由于振动偶合,1380 cm-1峰发生分裂,出现双峰。
—CH2—:~ 1 465 cm-1 (m)。
3.:在有—(CH2)n—直链结构的化合物中,—CH2—的面内摇摆()在810 cm-1~720 cm-1内变化,n越大,越小,当n>4时,—CH2—的在720 cm-1。
(二)烯烃类化合物烯烃类化合物用于结构鉴定的吸收峰主要有碳—氢伸缩振动()、碳—碳伸缩振动()和碳—氢面外弯曲振动()吸收峰。
1.:出现在3 100 cm-1~3 010 cm-1范围内,强度都很弱。
2.:非共轭发生在1 680 cm-1~1 620 cm-1,强度较弱;共轭向低频方向移动,发生在1 600 cm-1附近,强度增大。
第九羰基化合物红外光谱概要

9.26 羧酸中 OH 伸缩振动
Strong, very broad, center 3000 cm-1,
非环共轭酸酐, 1775, 1720
---C—O—C---
O
O
高频吸收与低频吸收强度比值, 判断环的形成
9.24 peroxides 过氧化物
O=C—O—O—C=O 1816 –1787 cm-1, 1790—1765 cm-1 9.25 卤素取代的羰基化合物 R—C—Cl O 芳香酰氯 1785—1765 cm-1 气体 F2C=O 1928 cm-1, Cl2C=O 1827 cm-1 Br2C=O 1828 cm-1 1810—1795 cm-1
O
单键氧上吸电子基团, 频率升高
9.15 酯类C-O振动 (O=C-O)
甲酸酯 1724, 1214-1185 strong (C-C-O) 乙酸酯 1740, 1245(C-C-O) 丙酸酯 1740-1735, 1200-1190 strong (C-C-O) 丁酸酯 1735, 1190 strong (C-C-O) 异丁酸酯 1735, 1200 strong (C-C-O)
--C—C—
O O
1720±10 cm-1
1755—1695 cm-1
--C—CH2—C— O O
9.9 共轭同时形成氢键的酮类
X
X: OH, NH2
酮式 1707—1694 cm-1 反对称
1739—1725 cm-1 对称 烯醇式 1630---1607 cm-1 (氢键) 1649---1646 cm-1 (无氢键)
丙烯酸酯 1725 cm-1, 1640 cm-1, 1625 cm-1
1200 cm-1 C—O
红外光谱

第九章红外光谱学习要求:1、学会如何借助光学技术来分析化合物的结构。
2、掌握谱图分析,了解各个官能团的吸收峰位置,和吸收分的特点。
3、知道影响吸收峰位置的因素。
有机化合物分子结构的鉴定,是研究有机化合物的重要组成部分,也是有机化学工作者的一项重要任务。
有机化合物的结构、性质和合成的研究是相辅相成的,性质和合成的研究帮助人们对结构的认识,反过来,对结构的深入研究又必然会促进性质和合成研究的进展。
随着科学技术的进步,运用物理方法来研究有机化合物的结构有了巨大的发展,使有机化合物的鉴定以及结构的确定都大大简化了。
这些方法中特别重要的是波谱技术,它研究电磁辐射与分子的作用,为鉴定有机化合物和确定其结构提供了非常有价值的信息。
波谱方法具有分析速度快、用量少等优点,而且与经典官能团试验不同,样品经测试后常不会被破坏,可另作它用。
根据课程的要求和分工,本章将简要介绍常用的波谱方法:红外光谱、紫外光谱、核磁共振谱和质谱。
11.1电磁波电磁波或称电磁辐射,是一种空间传播着的交变电磁场,它的区域范围很广,从波长只有千万分之一纳米(nm)的宇宙线到波长用米,甚至千米计的无线电波都是电磁波(见图9-1)。
红外光(IR)、紫外光(UV)和可见光都是某一波长范围的电磁波。
电磁波具有相同的传播速度,即C=3×1010cm/s。
电磁波常用波长或频率来表示。
它们之间的关系为:ν=c/λ式中,ν为频率,单位是赫兹(Hz),λ是波长,单位是厘米(cm)、微米(μm)或纳米(nm)。
它们的关系是:1nm=10-9m=10-7cm=10-3μm。
在红外光谱中频率还常用波数(σ)来表示,即每一厘米长度中所含波的数目,其单位是厘米-1(cm-1)。
σ=1/λ=υ/c例如,波长为300nm的光,它的频率为:ν=c/λσ=1/λ光具有波动性和微粒性,因此电磁波还可以用光量子的能量来描述。
E=hν=hc/λ这里E是光量子能量,h=6.624×10-34J.s是普朗克(Plank)常数。
醛和酮亲和加成反应

CH3CH2CH2OH
97
10
3)水溶性:醛酮旳氧原子能够与水形成氢键,所 以低档醛酮能与水混溶,高级醛酮易溶于有机 溶剂;
4)IR:羰基旳红外光谱在1750-1680 cm-1之间有 一种非常强旳伸缩振动吸收峰。当羰基与双键 共轭,吸收向低波数位移。-CHO中旳C-H键在 2720 cm-1和2850 cm-1区域有两个非常特征旳 伸缩振动吸收峰。
36
2、卤仿反应
乙醛或甲基酮与次卤酸盐反应(实际是在碱催
化下旳α-H卤代反应),三个α-H均被卤代。
O
R-C-CH3 + X2 -OH
O R-C-CX3 -OH
OR-C-CX3
OH
~
RCOOH + X3C -
O
R C CH3+ 4NaOH + 3X2
RCOO- + CHX3
H+
RCOOH
RCOONa + CHX3 (卤仿)
H
O
O
稀碱
CH3C H + CH2C H
OH O CH3CHCH2C H -H2O
△
β-羟基醛
CH3CH CHCHO
O
O
O-
HO- + H CH2C H
CH2
CH
CH2
C H快
O
O
O-
CH3 C H + CH2 C H
CH3CHCH2CHO
慢
反应机理
O-
OH
CH3CHCH2CHO + H OH
CH3CHCH2CHO
鉴别醛; RCHO + Ag(NH3)2+OH- △ RCOONH4 + Ag + NH3 + H2O
NOB007常见化合物的红外光谱解析——按官能团分类说明(4)

IR NO.B-007
2019.07 常见化合物的红外光谱解析——按官能团分类说明(4)
常见的化合物,按照官能团的不同可以分为如下十大类,其红外光谱特征总结如下:
7.羰基化合物
羰基的吸收在红外光谱中很强,通常位于1800cm-1~1700cm-1之间,易于识别。
然而不同物质的羰基吸收位置差别较小,若要判断物质类别的归属,需要同时参考其他振动峰,例如,庚酮、庚醛及庚酸的羰基伸缩振动峰均在1715cm-1附近(参见图1-23~图1~25)。
先看醛,其C-H弯曲振动在2780cm-1~2680cm-1之间,这个区域很少有吸收峰,特征很强,很容易就与其他物质区分开来。
再看酸,由于酸类物质存在分子间氢键,因此羧酸会在3500cm-1-2500cm-1之间形成一个强宽峰,甲基和亚甲基的伸缩振动峰会被覆盖一部分,看上去会像是在一个大的羟基宽峰上冒出了几个小尖峰(甲基、亚甲基的伸缩振动),此外,羧酸在1420cm-1附近及1285cm-1附近还有COOH的伸缩/弯曲振动。
酯类化合物的羰基特征吸收峰通常位于1740cm-1附近(见图1-27),同时结合1350cm-1~1000cm-1附近C-O的伸缩振动峰(强峰),可以认为化合物中含有酯类的官能团;酸酐的羰基位置较高(见图1-26),在1870cm-1-1720cm-1区域内以双峰形式存在,易于判定;酰胺中C=O的伸缩振动吸收,以及部分。
羰基的红外特征吸收峰

羰基的红外特征吸收峰红外光谱是一种常用的分析手段,能够通过物质在红外光区的吸收特征峰来确定其结构和成分。
羰基是一种常见的官能团,具有明显的红外吸收特征峰。
本文将详细介绍羰基的红外特征吸收峰,并探讨其在有机化学中的应用。
1. 羰基的定义和结构羰基是由一个碳原子和一个氧原子通过双键连接而构成的官能团,常用C=O表示。
羰基可以存在于各种有机物中,包括酮、醛、酸、酯等。
羰基的结构决定了它在红外光谱中的吸收特征峰。
2. 羰基的红外吸收特征峰羰基的红外吸收特征峰通常出现在1700-1800 cm-1的波数范围内。
不同类型的羰基在具体位置和强度上会有所区别。
2.1 酮和酯的羰基酮和酯的羰基吸收峰通常出现在1710-1725 cm-1。
在酮中,羰基的吸收峰通常较强,位置在1710-1715 cm-1之间。
在酯中,羰基的吸收峰通常较弱,位置在1735-1745 cm-1之间。
2.2 醛的羰基醛的羰基吸收峰通常出现在1725-1740 cm-1。
醛中的羰基吸收峰相对较强,位置在1725-1735 cm-1之间。
2.3 酸的羰基酸的羰基吸收峰通常出现在1700-1725 cm-1。
酸中的羰基吸收峰相对较弱,位置在1705-1720 cm-1之间。
2.4 羰基的伸缩振动模式羰基的伸缩振动模式对应着羰基的红外吸收峰。
在羰基的伸缩振动中,氧原子向碳原子进行振动,导致了红外光谱中的特征吸收峰。
3. 羰基的应用羰基在有机化学中有广泛的应用。
通过红外光谱分析羰基的吸收峰,可以确定有机化合物的结构和成分。
羰基的红外吸收峰还可以用于鉴定和鉴别有机化合物中的酮、醛、酸、酯等官能团。
4. 羰基的红外光谱图解析为了更直观地解析羰基的红外光谱,我们可以借助红外光谱图。
在红外光谱图中,横轴表示波数,纵轴表示吸收强度。
羰基的吸收峰通常以峰高表示其强度,峰位表示其位置。
5. 总结羰基是一种常见的官能团,具有明显的红外吸收特征峰。
通过对羰基的红外吸收峰的分析,可以确定有机化合物的结构和成分。
红外光谱分析法3

酸酐化合物红外谱图
醇和酚的红外谱图(P179)
羟基化合物有三个特征吸收区:O-H伸缩振动吸收 区,C-O伸缩振动吸收区和O-H弯曲振动吸收区。其特 征吸收峰位置列于下表:
基 团 振动形式 吸收峰位置/cm-1
R OH
v OH δOH
OH vC-O-H
3700~3200 醇 1400~1250 酚 1300~1165 醇 1100~1000 酚 1260
(3)由于红外光谱的复杂性,并不是每一个红外谱峰 都是可以给出确切的归属,因为某些峰是分子作为一 个整体的吸收,而有的峰则是某些峰的倍频或合频。 另外有些峰则是多个基团振动吸收的叠加。在解析光 谱的时候,往往只要能给出10%~20%的谱峰的确切 归属,由这些谱峰提供的信息,通常可以推断分子中 可能含有的官能团。在分析特征吸收时,不能认为强 峰即是提供有用的信息,而忽略弱峰的信息。例如, 835cm-1的谱峰存在与否是区别天然橡胶与合成橡胶的 重要标志,前者有此峰,后者没有。
不饱和度的计算公式
已知分子式CxHyOz,计算不饱和度:所谓不饱 和度即是当一个化合物变为相应的烃时,和同碳的 饱和烃比较,每缺少二个氢为一个不饱和度。
2x 2 y 2
2 2n4 n3 n1 2
n1、n3、n4为分子式中一价(Cl和Br)、三价(P和N)和四 价(C和Si)原子的数目。
强度
s w s
s
备注 宽峰
醇类化合物红外谱图
酚类化合物红外谱图
醚类化合物红外谱图(P180)
醚类的特征是含有C-O-C的结构,有对称和反 对称(1150-1060 cm-1 )两种伸缩振动吸收。由于 氧的质量和碳的很接近,使醚键的C-O伸缩振动 吸收位置和C-C的类似,位于C-C伸缩振动的指纹 区,但C-O振动时偶极矩变化较大,有利于与C-C 键的区别,但任何含有C-O键的分子(例如醇, 酚,酯,酸等)都对醚键的特征吸收产生干扰, 因此要由红外光谱来单独确定醚键的存在与否是 比较困难的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
9.10 酮类化合物中的键角效应 环张力增加, 羰基伸缩振动频率,增加
丙酮: 1719 cm-1 环己酮: 1719 cm-1 环戊酮: 1746 cm-1 环丁酮: 1788 cm-1 环丙酮: 1822 cm-1
9.11 醛类CH振动(CHO) 脂肪醛类, 2830-2810 cm-1
2720-2695 cm-1 1390 cm-1 芳香醛类 2832-2812 cm-1 2745-2720 cm-1 1390 cm-1
羰基 In-phase stretch, higher frequency,
Out-of-phase, lower frequency
非环饱和酸酐, 1820, 1750
非环共轭酸酐, 1775, 1720
---C—O—C---
O
O
高频吸收与低频吸收强度比值, 判断环的形成
9.24 peroxides 过氧化物 O=C—O—O—C=O 1816 –1787 cm-1, 1790—1765 cm-1 9.25 卤素取代的羰基化合物 R—C—Cl 1810—1795 cm-1
9.17 酯中与羰基相连的基团 --C---O--
O 乙酸酯: CH3, sys 1374 cm-1 strong
as 1430 cm-1 weak 其它饱和酸酯, CH2, 1420 cm-1
9.18 酯中与氧相连的基团 --C---O--
O
CH3, 2960 cm-1, 1440 cm-1 sys deformation CH2CH3, CH2 1475 cm-1,
O
--C—C— 1720±10 cm-1
OO
--C—CH2—C— 1755—1695 cm-1
O
O
9.9 共轭同时形成氢键的酮类
X
X: OH, NH2
酮式 1707—1694 cm-1 反对称 1739—1725 cm-1 对称
烯醇式 1630---1607 cm-1 (氢键) 1649---1646 cm-1 (无氢键)
红外和拉曼光谱导论
长春应用化学研究所
王海水
Chapter 9 羰基化合物 9.1 简介 羰基化合物 1900-1550 cm-1, C=O 伸缩
9.2 X质量对X-C=O 振动的影响
当X有较大原子量时, C=O伸缩时, X 基本不动. C-X稍微收缩 H-C=O, C=O伸缩时, C-H键长基本不变化. O=C-H 面内 bending 相互作用 只考虑质量因素时, X质量大, C=O 振动频率稍微上升
费米共振 面内变角振动
费米共振 面内变角振动
邻位(卤素,硝基, 甲氧基)取代的苯甲醛 2900-2810 cm-1 2765-2747 cm-1
低频吸收醛类特征吸收
9.12 醛类的羰基振动 脂肪醛 1740—1720 cm-1 芳香醛 1710--1685 cm-1 CCl3CHO: 1768 cm-1 CHCl2CHO: 1748 cm-1 CH2ClCHO: 1730 cm-1
9.3 键角影响
羰基化合物, = 1279+68F-2.2 F, 力常数 , C-C-C键角度数, 通常情况下, 变化很小 环酮时, 张力环, 羰基伸缩振动频率增加.
环己酮1715 cm-1 环戊酮1745 cm-1 环丁酮1775 cm-1
9.4 诱导效应 吸电子基团, 高频移动, 兰移 给电子基团, 低频移动, 红移
9.14 酯类 C=O R-C-O-R
O C=O 伸缩振动 1750--1735 cm-1 C—O 伸缩, 1200 cm-1 HC-O-R 甲酸酯类 1725-1720 cm-1
O
R-C-O—X O
CH3-C-O—CH2CH3 1740 cm-1 O
CH3-C-O—CH=CH2 1770 cm-1 O
丙烯酸酯 1725 cm-1, 1640 cm-1, 1625 cm-1 1200 cm-1 C—O
异丁烯酸酯 1725 C=O, 1640 C=C, 1180 C—O
苯甲酸酯: 1725 (C=O), 1280 strong C—O, Ar—C—O—CH2—R, 1110 O--CH2
邻苯二甲酸酯: 1725, 1280, 1120 O--CH2
单键氧上吸电子基团, 频率升高
9.15 酯类C-O振动 (O=C-O) 甲酸酯 1724, 1214-1185 strong (C-C-O) 乙酸酯 1740, 1245(C-C-O) 丙酸酯 1740-1735, 1200-1190 strong (C-C-O) 丁酸酯 1735, 1190 strong (C-C-O) 异丁酸酯 1735, 1200 strong (C-C-O)
O 芳香酰氯 1785—1765 cm-1 气体 F2C=O 1928 cm-1, Cl2C=O 1827 cm-1
Br2C=O 1828 cm-1
9.26 羧酸中 OH 伸缩振动 Strong, very broad, center 3000 cm-1,
9.19 内酯 Lactones 环变小, 羰基伸缩振动频率增加
9.20 硫醇酯及相关化合物
9.21 碳酸酯及相关化合物
9.22 Oxalates 草酸酯
--O--CO—CO—O, 1765 cm-1, 1740 cm-1 脂肪酯
1795 cm-1, 1770 cm-1, 芳香酯
9.23 Anhydrides 酐
9.5 p-共轭(中介效应) 酰胺 O=C—N 羰基伸缩 1660 cm-1 酮 O=C—C 羰基伸缩 1715 cm-1 诱导效应X p-共轭
9.6 ketones 酮 RCR, 1715 cm-1,
O RCOCH3, CH3symmetric deformation 1370-1350 cm-1 RCH2COR, CH2 144.8 共轭酮类 共轭通常使羰基伸缩振动频率降低 1700-1640 cm-1 (1725—1705 cm-1) C=C-C=O 1685-1660 cm-1 Ar-C=O 1700-1680 cm-1 Ar-C-Ar 1670-1660 cm-1
O C=C-C-C=C 1670-1660 cm-1
