地下水的物理性质和化学成分资料
合集下载
地下水的物理性质和化学成分资料

强
福岛第一核电站运营商东京电力公司发言人松茂直
之3月31日说,东电3月30日11时10分从1号反应堆地下 15米处采集地下水样本。
检测结果显示,每千克样本碘131放射性活度为430 贝克勒尔,超过政府规定安全水平1万倍。
3.2
地下水的化学成分
各种气体、离子、胶体物质、有机质以及微生物等 3.2.1 地下水中主要气体成分 主要的气体组分:O2、N2、CO2、H2S、CH4、H2、
离子浓度越高,温度越高,导电性越强
根据地下水的导电性,可以区分含水层和隔水层、 矿水和淡水,也可以根据导电性圈定富水地带,寻找 断裂破碎带 (8)放射性
取决于其中放射性物质的含量
地下水按放射性元素的含量(g/L)分为强放射性 水,中等放射性水和弱放射性水
以镭为例
弱 10-10g/L
中等 >10-9g/L
温度每升高1℃所需增加的深度(m)称为【地热增温 级】(m/℃) 一般地区为:33m/℃ 近代火山活动地区为:1m/℃;如西藏羊八井达到0.3m/℃ 前寒武纪地区为:100m/℃
(2)颜色
由于含有某种离子较多,或者富集悬浮物质 和胶体物质 取决于水中溶解的盐类和有机质 二氧化碳——清凉可口 重碳酸钙——味美可口 氯化钠——咸味 硫酸钠——涩味
CH3COOH 8NO3 6H2O 10CO2 4N2 8OH 能量
5S 6KNO3 2H2O 3N2 K2 SO4 4KHSO4
2)氮(N2) ②分布特征 A)由于N2的化学性质不及氧活泼,它的分布随深度的减 少,不及O2明显 B)大气中的惰性气体(Ar/氩、Kr/氪、Xe/氙xiān)与N2 的比例恒定,即:(Ar+Kr+Xe)/N2=0.0118。 比值等于此数,说明N2是大气起价化合物而从中沉 淀; 反之,地下水中含O2少,形成低价态化合物而易于在 水中迁移
地下水的物理性质及化学成分
不同地区的地温梯度变化于:
0.6~10℃/100m之间。
地下水的温度对地下水的化学成分有很
大影响。水温增高,化学反应速度和溶解度
也增高。
过冷水
<0℃
如:水温增高10℃时,冷 水
0~20℃
水分子的扩散速度约
低温热水
20~ 40℃
增加20%,化学反应 热 水 中温热水
40~ 60℃
速度增加2~3倍。
中高温热水
第一节 地下水的物理性质
地下水的物理性质包括温度、颜色、透明度、 嗅、味、相对密度、导电性及放射性等。
它在一定程度上反映了地下水的化学成分及 其存在的环境条件。
一、地下水的温度 二、地下水的颜色 三、地下水的透明度 四、地下水的嗅(气味) 五、地下水的味(味道) 六、地下水的比重
一、地下水的温度 水温变化范围可达100℃以上。在寒带和多年
无 有少量 有较多, 半透明状
有大量,似乳状
60cm水深 >30cm水深
<30cm水深 水深很小 也看不见
四、地下水的嗅(气味)
地下水的气味取决于水中所含的气体成分和有
机物质。一般地下水是无嗅的。
“气味”的强弱 与温度有关,
含气体 或有机质
鉴别气味时,
一般将水加热 至40℃时,
H2S 含低铁Fe2+
的风化溶滤。此外:废水、污水的渗入,动物排泄物 和动物尸体腐烂是Cl- 的有机来源之一。
一般在居民点、工业区及其附近,地下水中Cl-含
放射性取决于其中放射性物质的含量,地下 水不同程度上或多或少地都具有放射性,但其 含量一般极微,循环于放射性矿床的地下水
其放射性相应增强。
第二节 地下水的化学成分
一、地下水的化学成分(有60多种) (一)地下水中的主要离子成分 (二)地下水中的主要气体成分 (三)地下水中的胶体成分 (四)地下水中的有机质及细菌成分
0.6~10℃/100m之间。
地下水的温度对地下水的化学成分有很
大影响。水温增高,化学反应速度和溶解度
也增高。
过冷水
<0℃
如:水温增高10℃时,冷 水
0~20℃
水分子的扩散速度约
低温热水
20~ 40℃
增加20%,化学反应 热 水 中温热水
40~ 60℃
速度增加2~3倍。
中高温热水
第一节 地下水的物理性质
地下水的物理性质包括温度、颜色、透明度、 嗅、味、相对密度、导电性及放射性等。
它在一定程度上反映了地下水的化学成分及 其存在的环境条件。
一、地下水的温度 二、地下水的颜色 三、地下水的透明度 四、地下水的嗅(气味) 五、地下水的味(味道) 六、地下水的比重
一、地下水的温度 水温变化范围可达100℃以上。在寒带和多年
无 有少量 有较多, 半透明状
有大量,似乳状
60cm水深 >30cm水深
<30cm水深 水深很小 也看不见
四、地下水的嗅(气味)
地下水的气味取决于水中所含的气体成分和有
机物质。一般地下水是无嗅的。
“气味”的强弱 与温度有关,
含气体 或有机质
鉴别气味时,
一般将水加热 至40℃时,
H2S 含低铁Fe2+
的风化溶滤。此外:废水、污水的渗入,动物排泄物 和动物尸体腐烂是Cl- 的有机来源之一。
一般在居民点、工业区及其附近,地下水中Cl-含
放射性取决于其中放射性物质的含量,地下 水不同程度上或多或少地都具有放射性,但其 含量一般极微,循环于放射性矿床的地下水
其放射性相应增强。
第二节 地下水的化学成分
一、地下水的化学成分(有60多种) (一)地下水中的主要离子成分 (二)地下水中的主要气体成分 (三)地下水中的胶体成分 (四)地下水中的有机质及细菌成分
地下水的物理性质和化学成分

(2)颜色。纯水是无色 的,而地下水的颜色取决于水 中的化学成分及悬浮物。
1.1地下水的物理性质
(4)嗅味。纯水无嗅、无味 ,但当水中含有某些气体或有机质 时就会有某种气味。例如,水中含 H2S时有臭鸡蛋味,含腐殖质时有 霉味,等等。
(5)口味。地下水的味道主 要取决于水中的化学成分。
(6)比重。地下水的比重取 决于所含各种成分的含量。纯水比 重为1,但当水中溶解的各种成分 较多时可达1.2~1.3。
(1)主要离子成分。地下水中的阳离子 主 要 有 H+ 、 Na+ 、 K+ 、 NH4+ 、 Ca2+ 、 Mg2+ 、 Fe3+ 和 Fe2+ 等 , 阴 离 子 主 要 有 OH- 、 Cl- 、 SO42-、NO2-、NO3-、HCO3-、CO32-、SiO32和PO43-等。一般情况下,在地下水化学成分 中占主要地位的是Na+、 K+ 、 Ca2+ 、 Mg2+ 、 Cl- 、 SO42-和HCO3-离子。它们是人们评价地 下水化学成分的主要项目。
1.2地下水的化学成分
(2)主要分子成分。地下水中的主要 分 子 成 分 有 Fe ( OH ) 3 、 Al ( OH ) 3 和 H2SiO3等。
(3)主要气体成分。地下水中常见的 气体有N2、O2、CO2、H2S。一般情况下, 地下水的气体含量每升只有几毫克到几十毫 克。
工程地质
工程地质
1.1地下水的物理性质
地下水的物理性质包括温 度、颜色、透明度、嗅味、口 味、比重、导电性及放射性等。
(3)透明度。纯水是透明 的,但当水中含有矿物质、机械 混合物、有机质及胶体物质时, 水的透明度就会改变,所含各种 成分越多,透明度越差。
1.1地下水的物理性质
(4)嗅味。纯水无嗅、无味 ,但当水中含有某些气体或有机质 时就会有某种气味。例如,水中含 H2S时有臭鸡蛋味,含腐殖质时有 霉味,等等。
(5)口味。地下水的味道主 要取决于水中的化学成分。
(6)比重。地下水的比重取 决于所含各种成分的含量。纯水比 重为1,但当水中溶解的各种成分 较多时可达1.2~1.3。
(1)主要离子成分。地下水中的阳离子 主 要 有 H+ 、 Na+ 、 K+ 、 NH4+ 、 Ca2+ 、 Mg2+ 、 Fe3+ 和 Fe2+ 等 , 阴 离 子 主 要 有 OH- 、 Cl- 、 SO42-、NO2-、NO3-、HCO3-、CO32-、SiO32和PO43-等。一般情况下,在地下水化学成分 中占主要地位的是Na+、 K+ 、 Ca2+ 、 Mg2+ 、 Cl- 、 SO42-和HCO3-离子。它们是人们评价地 下水化学成分的主要项目。
1.2地下水的化学成分
(2)主要分子成分。地下水中的主要 分 子 成 分 有 Fe ( OH ) 3 、 Al ( OH ) 3 和 H2SiO3等。
(3)主要气体成分。地下水中常见的 气体有N2、O2、CO2、H2S。一般情况下, 地下水的气体含量每升只有几毫克到几十毫 克。
工程地质
工程地质
1.1地下水的物理性质
地下水的物理性质包括温 度、颜色、透明度、嗅味、口 味、比重、导电性及放射性等。
(3)透明度。纯水是透明 的,但当水中含有矿物质、机械 混合物、有机质及胶体物质时, 水的透明度就会改变,所含各种 成分越多,透明度越差。
工程地质学-地下水

Ca OH2 +2H+ Ca 2+ +2H2O 碳酸性侵蚀: 由于CaCO3在侵蚀性CO2作用下溶解使砼遭受破坏
CaCO3 H2O CO2 CaHCO3 2 Ca 2 2HCO3
Ca OH 2 +CO2 CaCO3 +2H 2O
②结晶性侵蚀:
②分解类腐蚀
③结晶分解复合类腐蚀
当 地 下 水 中 NH4- , NO3- , Cl- 和 由 于 地 下 水 中 含 有 超 量 Mg2+ 离子的含量超过一定数量时, CO2 时混凝土中的 CaCO3 被 与混凝土中的 Ca(OH) 发生反应, 2 溶解而受腐蚀,即为分解 Ca(OH) 与镁盐作用的生成物中, 2 类腐蚀。地下水的酸度过 除 Mg(OH) 不易溶解外, CaCl 则 2 2 大,即pH值小于某一数值, 易溶于水并随之流失 。硬石膏 那 么 混 凝 土 中 的 Ca(OH)2 CaSO 一方面与混凝土中的水化 4 也要分解,特别是当反应 铝酸钙反应生成水泥杆菌;另一 生成物为易溶于水的氯化 方面,硬石膏遇水生成二水石膏。 物时,对混凝土的分解腐 二水石膏在结晶时体积膨胀,破 蚀很强烈。 坏混凝土的结构。
主要是硫酸盐侵蚀,是含有硫酸盐的水与砼发生反应,在砼的孔洞中形成石 膏和硫酸铝盐晶体;由于结晶膨胀作用使砼的强度降低以致破坏。
生成硫酸铝盐的反应式为: 3CaO.Al2O3.6H2O+3CaSO4 25H2O 3CaO.Al2O3.3CaSO4.31H2O 石膏是形成硫酸铝盐的中间产物。 ③结晶分解复合性侵蚀
第5章 地下水
内容提要
5.1概述
5.2地下水的类型及其主要特征
5.3地下水的性质
第3章 地下水的物理性质和化学成分

早期, 早期,Cl盐最易溶于水中→随水带走,岩土贫Cl盐继续作用,较易溶
后期溶滤作用—长期强烈溶滤作用的结果是难溶成分的低矿化水 后期 去考察,去分析与研究问题!!
(二)浓缩作用
定义:地下水在蒸发排泄条件下,水分不断失去,盐分相对浓集 浓缩作用(过程)——理想的蒸发浓缩模式
水份失去过程→盐分相对浓集,化学成分的变化 (实际上与上述理想模式是不同的)
水中以哪种阴、阳离子为主?
Company Logo
(一)溶滤作用——结果 结果
长期、强烈溶滤作用的结果,地下水以低矿化度的难溶离子为主 这是由溶滤作用的阶段性决定!在由多种盐类组成的岩石中: 因此,分析溶滤作用及其地下水的成分特征:
① 要从地质历史发展的眼光(角度)来理解—它是地质历史长期作用的结果 ② 地下水是不断运动的—溶解的组分会被带去(岩土组分变化) 前期溶滤作用—溶滤什么组分 溶滤什么组分, 前期溶滤作用 溶滤什么组分,水中获得相应组分
0.5L水 水
蒸发(2)
0.25L 1400mg/L
蒸发(3)
0.125L 2800mg/L
0.25L 水
Company Logo
地下水化学特征具有分带性
由于地下水化学成分形成作用受区域自然地理与地质条件的影响, 由于地下水化学成分形成作用受区域自然地理与地质条件的影响, 地下水的化学特征往往具有一定的分带性(空间上的)。 地下水的化学特征往往具有一定的分带性(空间上的)。
Company Logo
(二)主要离子成分
这与主要离子构成的盐类溶解度有关:
硫酸盐类 < 氯化物 常见离子在水中的相对含量与地下水中的总固体溶解物(TDS 矿化度(g/L) : 低(<1) 阴 阳 离 离 子: 子: HCO-3 Ca2+ 中(1-10) 高(10-30) SO2-4 Ca2+,Mg2+ ClNa+,K+
地下水的物理性质、化学成分及其形成作用

饮用水水质评价 工业用水水质评价 农业用水水质评价 工程建设项目用水水质评价
§2 地下水的物理性质
地下水的物理性质包括水温、颜色、透明度、味道、气味、比 重、放射性、导电性。它在一定程度上反映了地下水的化学成分及其 存在的环境条件。
一、地下水的温度
水温变化范围-5℃以下-100℃以上。在寒带和多年积雪地带,浅层的 地下水温可低达-5℃以下;在温带和亚热带的平原、丘陵区浅层地下水的年 平均温度一般接近于当地年平均气温;在火山活动地区及地壳深处,地下水的 温度很高,可超过100℃。如我国广东丰良地区在地下800m深处,打出了 103.5℃的热水。
③增温带:
❖ 常温带以下,地温受地球内热影响,随深度加大而有规律地升高—— 增温带。 深度每增加100m温度增加的值称地热增温率(地温梯度, 单位:℃/100m),温度每增加一度深度增加的值称地热增温级。 各地增温级不同, 华北:33-43m;北方山区:50m;古老结晶岩区:1000m; 近火山区:1m;一般山区:33m,由于变化不大,故地下水“冬 暖夏凉”。
地下水的温度受其赋存与循环所处的地温控制:
❖ 变温带中浅埋地下水显示微小的水温季节变化。 ❖ 常温带地下水温与当地年平均气温很接近。(地温年变化幅度小于
0.1℃) ❖ 增温带地下水随其赋存与循环深度的加大而提高,成为热水甚至蒸汽。 ❖ 利用年平均气温t、年常温带深度h、地温梯度r,可计算某一深度H的
❖ 如地下水中含有重碳酸钙、重碳酸镁及碳酸时,水味便爽快、适口, 人们称这种水为“甜水”
❖ 如含氯化物会使水发咸味 ❖ 含硫酸钠、硫酸镁使水变苦,而且常引起饮用者呕吐、腹痛和腹泻
❖ 含盐分过多时水味发涩
❖ H2S与碳酸气同时存在有酸味,有机质有甜味,但不适饮用。
§2 地下水的物理性质
地下水的物理性质包括水温、颜色、透明度、味道、气味、比 重、放射性、导电性。它在一定程度上反映了地下水的化学成分及其 存在的环境条件。
一、地下水的温度
水温变化范围-5℃以下-100℃以上。在寒带和多年积雪地带,浅层的 地下水温可低达-5℃以下;在温带和亚热带的平原、丘陵区浅层地下水的年 平均温度一般接近于当地年平均气温;在火山活动地区及地壳深处,地下水的 温度很高,可超过100℃。如我国广东丰良地区在地下800m深处,打出了 103.5℃的热水。
③增温带:
❖ 常温带以下,地温受地球内热影响,随深度加大而有规律地升高—— 增温带。 深度每增加100m温度增加的值称地热增温率(地温梯度, 单位:℃/100m),温度每增加一度深度增加的值称地热增温级。 各地增温级不同, 华北:33-43m;北方山区:50m;古老结晶岩区:1000m; 近火山区:1m;一般山区:33m,由于变化不大,故地下水“冬 暖夏凉”。
地下水的温度受其赋存与循环所处的地温控制:
❖ 变温带中浅埋地下水显示微小的水温季节变化。 ❖ 常温带地下水温与当地年平均气温很接近。(地温年变化幅度小于
0.1℃) ❖ 增温带地下水随其赋存与循环深度的加大而提高,成为热水甚至蒸汽。 ❖ 利用年平均气温t、年常温带深度h、地温梯度r,可计算某一深度H的
❖ 如地下水中含有重碳酸钙、重碳酸镁及碳酸时,水味便爽快、适口, 人们称这种水为“甜水”
❖ 如含氯化物会使水发咸味 ❖ 含硫酸钠、硫酸镁使水变苦,而且常引起饮用者呕吐、腹痛和腹泻
❖ 含盐分过多时水味发涩
❖ H2S与碳酸气同时存在有酸味,有机质有甜味,但不适饮用。
0417-第四章 地下水的物理性质和化学成分

地下水在运动过程中的各种作用
(2)水中阳离子的浓度 水中某种阳离子浓度越大,则其交替吸附能力就越强, 甚至可以发生吸附能力小的交替岩土颗粒表面吸附能力 大的阳离子 例如,海水入侵大陆时可以发生如下反应 (3)岩土本身吸附能力的大小 主要取决于其比表面积,比表面积越大,则岩土本身 吸附能力越大,交替吸附能力越强;反之,交替吸附能 力越弱
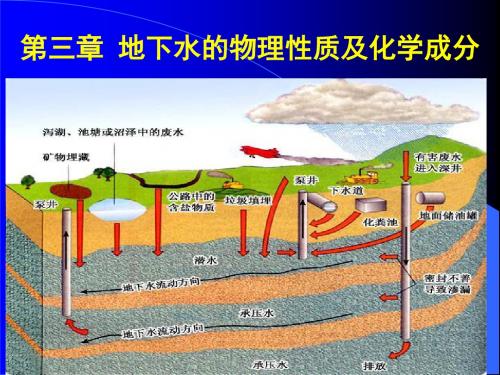
第四章 地下水的物理性质 和化学成分
4.1 地下水的物理性质
地下水的物理性质、化学成分特征是地下水与环境 (自然地理、地质背景及人类活动)长期作用的结果。 地下水的化学性质为认识和了解地下水形成的地质历史 条件和过程提供依据 地下水在岩石的孔隙、裂隙或溶洞中储存和运动时, 溶滤和溶解着岩石的可溶成份,使地下水变成了含有各 种矿物质的天然溶液,而且随着运动环境和运动过程的 变化,地下水的化学成分也不断地更迭着
本章完
地下水在运动过程中的各种作用
• 离子交换与吸附作用 指岩土颗粒表面因静电作用而吸附的阳离子在一定条 件下部分转入水中,而书中的某些阳离子转入吸附到岩 土颗粒表面的过程 影响因素: (1)阳离子本身吸附能力的大小 水中吸附能力大小的阳离子可以交替岩土颗粒表面吸 附能力小的阳离子。阳离子吸附能力由大到小的顺序:
地下水中常见的化学成分
(2) 硫化氢(H2S) 处于还原环境,一般存在于封闭地质构造的地下水中,特 别是油田水中(SO42-将被微生物还原成H2S) (3)甲烷(CH4) 一般存在于封闭地质构造的地下水中,特别是油田水中 (4)二氧化碳(CO2) 地下水中的二氧化碳主要有两个来源: 一种由有机物的氧化(植物的呼吸作用及有机质残骸的发 酵作用)形成。这种作用发生于大气、土壤及地表水中,生成 后随同水一起入渗补给地下水,浅部地下水中的主要是这种 成因的 ;另一种是深部变质造成的。含碳酸盐类的岩石,在 深部高温影响下,分解生成CO2,即:
水文地质学基础:地下水的物理性质和化学特征

3.地下水的化学成分
– 溶解气体意义: • 气体成分能够说明地下水所处的地球化学环境 – O2、N2:主要来源于大气;指示地下水是大气起源, 若只有N2说明地下水起源于大气且处于还原环境 – CH4、H2S:来源于封闭还原环境下微生物参与的生 • 会物增化加学地作下用水;溶指解示某还些原矿环物境组分的能力 - CO2主要来自与土壤中有机质残骸的发酵作用与植 物的呼吸作用,可增加水对碳酸盐岩等的溶解能力
地下水的物理性质和化学特征
目录
1 概述
目录 CONTEN
TS
2 地下水的物理性质 3 地下水的化学成分
3 地下水的化学成性质
1.概述
• 地下水含有各种组分具有一定的物理性质和化学组特征。 • 水是良好的溶剂,在空隙中运移时,可溶解岩石中的成分。
在自然界水循环过程中,地下水与大气圈、水圈与生物圈 同时发生着水量和化学成分的交换。
• 中等矿化的地下水中,阴离子常以
SO42-为主,阳离子则以Na+或
谢பைடு நூலகம்观看 !
3.地下水的化学成分
离子成分
阴离子:Cl-、SO2-4、HCO-3 阳离子:Na+、K+、Ca2+、Mg2+
来源于相应矿物、岩石的溶解风化
3.地下水的化学成分
其他成分
• H+、Fe2+、F3+、Mn2+、NH4+、OH-、NO2、NO3、 CO32-、SiO3-及PO43-等。
• 微量组分,有Br、I、F、B、Sr等。 • 胶体Fe(OH)3、Al(OH)3、H2SiO3等。 • 有机质:经常以胶体的方式存在于地下水中。有机质
• 意义:水质评价,水化学找矿;地震预报等
第六章地下水的化学成分、物理性质及其形成作用

五、地下水中的其它成分
1.次要离子:H+、Fe2+、Fe3+、Mn2+、NH4+、OH-、NO2-、NO3-、 CO32-、 SiO3-、PO43-等。
2.微量组分:Br、I、F、B、Sr 、Ba等。其作用:
1)说明地下水的形成环境;
2)对人体健康有明显影响。
3.未离解的化合物构成的胶体:如Fe(OH)3、A1(OH)3、H2SiO3等。
3.二氧化碳(CO2)
1)来源:
a.主要来源于土壤。有机质残骸的发酵作用与植物的呼吸作用使土壤不 断产生CO2,并溶入流经土壤的地下水中。
b.深部变质来源。含碳酸盐类的岩石,在深部高温下,也可以变质生成 CO2。
在少数情况下,地下水中可能富含CO2 甚至高达1g/L 以上。
c.少量来源于降水和地表水,但含量通常较 低。
d.人为来源。
2)作用:地下水中含CO2 愈多,其溶解碳酸盐岩与对结晶岩进行风化 作用的能力便愈强。
四、地下水中主要离子成分
1.总体特征
1)主要离子成分:氯离子(C1-)、硫酸根离子(SO42-)、重碳酸根 离子(HCO3-)、钠离子(Na+)、钾离子(K+)、钙离子(Ca2+) 及镁离子(Mg2+)。
3.地下水化学成分对于用于各种地下水利用的目的,水质评价都具有决定性 意义。
4.地下水化学成分的确定,有助于查明地下水有关物质的迁移、分散规律, 对寻找矿产资源,确定矿床或污染源位置具有重要意义。
三、地下水化学成分研究理论及特征
1. 理论基础:水文地质学的分支——水文地球化学,研 究地下水中化学元素迁移、集聚与分散的规律,地下水 水质演变的学科。
地壳中钾的含量与钠相近,钾盐的溶解度也相当大。但是,在地下水中 K+的含量要比Na+少得多。原因: a.K+大量地参与形成不溶于水的次生矿物(水云母、蒙脱石、绢云母); b.易为植物所摄取。
第三章 地下水的物理性质和化学成分

3.2.2地下水化学成分的性质 3.2.2.1总含盐量与总溶解固体
TDS是反映地下水化学成分的主要指标,一般情 况下地下水随着TDS的变化,主要离子的种类也 相应地改变
TDS含量低的淡水常以HCO3-为其主要成分 TDS 含量中等的盐质水常以SO42-为其主要成分 TDS 含量高的盐水和卤水则常常是以以Cl-为其主 要成分
3.1地下水的物理性质 3.1.1.1 地壳的温度带
常温带以下的地温,主要受地球内部热力影响, 随着深度的增加而有规律地升高,称为增温带。 温度每增加l℃所需要的深度(m)称为地热增温级, 一般平均每33m升高1℃(用33m/ ℃表示) 由于岩石的导热性、地壳运动和水文地质条件的 不同,各地的地热增温级有很大差异
3.1地下水的物理性质
3.1.1.2地下水的温度
地下水的温度一般和它所在地区的地温状况是相 适应的 1)变温带地下水的水温 整个变温带的地下水温度有年变化,变温带上部 (地表以下1~3m)的地下水温度还有昼夜变化
不论是地下水温度的年变化还是昼夜变化都较气 温变化幅度为小,而且落后于气温的变化时间
3.1.6 地下水的导电性
地下水导电能力的大小取决于水中所含电解质的 数量与性质(各种离子的含量与离子价)。离子 含量越多,离子价越高.则水的导电性越强。
3.1.7 地下水的放射性
地下水的放射性的强弱决定于其中所含放射性元 素的数量。 一般地下水的放射性极微弱,在与放射性矿床有 关时,放射性含量相应增强。
3 地下水的物理性质与化学成分 3.1地下水的物理性质 地下水的物理性质一般指:温度、颜色、 透明度、嗅、味、比重、导电性、放射性等 3.1.1温度 地下水的温度变化主要是受气温和地温的 影响,尤其是地温。 原因:地下水存在于地壳中,且停留时间长 3.1.1.1地壳的温度带 地壳按热力状态从上而下分为变温带、年常温 带、增温带
水文地质学 第3章 地下水的物理性质和化学成分

溶滤作用——岩石中的某些可溶部分被溶解转入地下水中而成为 溶液的作用。
溶滤作用的强度取决于下列因素: 1)组成岩土的矿物盐类 2)岩土的空隙特征 3)水的溶解能力 4)水中CO2、O2等气体成分的含量 5)水的流动状况
地下水在运动过程中的作用
浓缩作用——地下水在运动的过程中由干水分不断地蒸发(当埋藏 较浅时),地下水中的含盐量便会相对地增加,这种作用即称为浓 缩作用。
地下水在运动过程中的作用
脱碳酸作用 碳酸盐类在地下水中的溶解度决定子水中的CO2的含量。当
地下水在运动过程中由于环境改变使地下水的温度增高或压力 减小时,水中的CO2便会从水中逸出,这时水中的HCO3-就会 与Ca2+、Mg2+结合形成CaCO3或MgCO3沉淀析出,从而改变 了地下水的化学成分,这种作用即脱碳酸作用。
1组成岩土的矿物盐类2岩土的空隙特征3水的溶解能力4水中co等气体成分的含量5水的流动状况地下水在运动过程中的作用浓缩作用地下水在运动的过程中由干水分不断地蒸发当埋藏较浅时地下水中的含盐量便会相对地增加这种作用即称为浓缩作用
第三章
地下水的物理性质和化学成分
1 地下水的物理性质 2 地下水的化学成分 3 地下水化学成分的形成与演变 4 与人类生存的关系
地下水在运动过程中的作用
脱硫酸作用 在缺氧的还原环境中,地下水含的SO42-在有机物存在的条件
下,由于微生物(脱硫细菌)作用的结果,使水中的SO42-可被还原 成为H2S,这样地下水中的SO42-就会减少甚至消失,而H2S气体 与HCO3-的含量则会增加,这种作用即脱硫酸作用
产生条件:1)缺氧;2)存在有机物。
地下水化学成分性质
➢ 总含盐量——存在于地下水中的离子、分子和微粒(不含气 体)之总含量,用“g/L”表示。
溶滤作用的强度取决于下列因素: 1)组成岩土的矿物盐类 2)岩土的空隙特征 3)水的溶解能力 4)水中CO2、O2等气体成分的含量 5)水的流动状况
地下水在运动过程中的作用
浓缩作用——地下水在运动的过程中由干水分不断地蒸发(当埋藏 较浅时),地下水中的含盐量便会相对地增加,这种作用即称为浓 缩作用。
地下水在运动过程中的作用
脱碳酸作用 碳酸盐类在地下水中的溶解度决定子水中的CO2的含量。当
地下水在运动过程中由于环境改变使地下水的温度增高或压力 减小时,水中的CO2便会从水中逸出,这时水中的HCO3-就会 与Ca2+、Mg2+结合形成CaCO3或MgCO3沉淀析出,从而改变 了地下水的化学成分,这种作用即脱碳酸作用。
1组成岩土的矿物盐类2岩土的空隙特征3水的溶解能力4水中co等气体成分的含量5水的流动状况地下水在运动过程中的作用浓缩作用地下水在运动的过程中由干水分不断地蒸发当埋藏较浅时地下水中的含盐量便会相对地增加这种作用即称为浓缩作用
第三章
地下水的物理性质和化学成分
1 地下水的物理性质 2 地下水的化学成分 3 地下水化学成分的形成与演变 4 与人类生存的关系
地下水在运动过程中的作用
脱硫酸作用 在缺氧的还原环境中,地下水含的SO42-在有机物存在的条件
下,由于微生物(脱硫细菌)作用的结果,使水中的SO42-可被还原 成为H2S,这样地下水中的SO42-就会减少甚至消失,而H2S气体 与HCO3-的含量则会增加,这种作用即脱硫酸作用
产生条件:1)缺氧;2)存在有机物。
地下水化学成分性质
➢ 总含盐量——存在于地下水中的离子、分子和微粒(不含气 体)之总含量,用“g/L”表示。
第3章地下水的物理性质及化学成分
中阳离子发生交换
(6)混合作用— 2种不同类型地下水混合时发生 (7)人类活动的作用——影响越来越大
19
3.3.1 溶滤作用
(1)定义
水与岩土相互作用下,岩土中某些组分向地下水中 转移的过程。其结果是:岩土失去部分可溶物质,地下 水中获得相应的化学成分使水中TDS↑。
CaCO3 + H2O + CO2 → 2HCO-3 + Ca2+ (固) (水) (气)
21
地下水是如何保持它的溶解能力的?
地下水的流动(交替)性: 地下水的径流速度和交替强度( V 与 Q ) 停滞与流动很缓慢的地下水,溶解能力最终 会降为零, 溶滤作用停止。 水如果流动速度快,水交替(更新)迅速, CO2,O2不断被补充, 低TDS水不断更新—溶解能力已降低的水 如果某地区地下水流动很快,水交替(循环)
25
浓缩作用的结果
溶滤作用将岩土中的某些成分溶入水中,地下水的流
动又把这些溶解物质带到排泄区。在半干旱干旱地区的平 原与盆地的低洼处,地下水埋藏不深,蒸发成为地下水的 主要排泄去路。由于蒸发作用只排走水分,盐分仍保留在 余下的地下水中,随着时间的延续,地下水溶液逐渐浓缩 ,矿化度不断增大。
浓缩作用的必备条件: (1)半干旱干旱的气候; (2)低平地势控制下较浅的地下水埋深; (3)有利于毛细作用的松散岩土; (4)地下水流动系统的势汇。
溶SO42-盐类被溶入中→随水带走,贫SO42-盐类持续(岩 土中)只剩
较难溶的碳酸盐类。
因此,分析溶滤作用及其地下水的成分特征:
① 要从地质历史发展的眼光(角度)来理解—它是
地质历史长期作用的结果
23
3.3.2 浓缩作用
定义:地下水在蒸发排泄条件下,水分不断 失去,盐分相对浓
(6)混合作用— 2种不同类型地下水混合时发生 (7)人类活动的作用——影响越来越大
19
3.3.1 溶滤作用
(1)定义
水与岩土相互作用下,岩土中某些组分向地下水中 转移的过程。其结果是:岩土失去部分可溶物质,地下 水中获得相应的化学成分使水中TDS↑。
CaCO3 + H2O + CO2 → 2HCO-3 + Ca2+ (固) (水) (气)
21
地下水是如何保持它的溶解能力的?
地下水的流动(交替)性: 地下水的径流速度和交替强度( V 与 Q ) 停滞与流动很缓慢的地下水,溶解能力最终 会降为零, 溶滤作用停止。 水如果流动速度快,水交替(更新)迅速, CO2,O2不断被补充, 低TDS水不断更新—溶解能力已降低的水 如果某地区地下水流动很快,水交替(循环)
25
浓缩作用的结果
溶滤作用将岩土中的某些成分溶入水中,地下水的流
动又把这些溶解物质带到排泄区。在半干旱干旱地区的平 原与盆地的低洼处,地下水埋藏不深,蒸发成为地下水的 主要排泄去路。由于蒸发作用只排走水分,盐分仍保留在 余下的地下水中,随着时间的延续,地下水溶液逐渐浓缩 ,矿化度不断增大。
浓缩作用的必备条件: (1)半干旱干旱的气候; (2)低平地势控制下较浅的地下水埋深; (3)有利于毛细作用的松散岩土; (4)地下水流动系统的势汇。
溶SO42-盐类被溶入中→随水带走,贫SO42-盐类持续(岩 土中)只剩
较难溶的碳酸盐类。
因此,分析溶滤作用及其地下水的成分特征:
① 要从地质历史发展的眼光(角度)来理解—它是
地质历史长期作用的结果
23
3.3.2 浓缩作用
定义:地下水在蒸发排泄条件下,水分不断 失去,盐分相对浓
