完全互溶双液系的平衡相图
二组分完全互溶双液系气-液平衡相图

课程名称:大学化学实验(P)指导老师:成绩:_______________实验名称:二组分完全互溶双液系气-液平衡相图实验类型:物性测试同组学生姓名:【实验目的】1.学习测定气-液平衡数据及绘制二组分系统相图的方法,加深理解相律和相图等概念。
2.掌握正确测量纯液体和液体混合物沸点的方法。
3.熟悉阿贝折光仪的原理及操作,熟练掌握超级恒温超的使用和液体折射率的测定。
4.了解运用物理化学性质确定混合物组成的方法。
【实验原理】两种液态物质若能以任意比例混合,则称为二组分完全互溶液态混合物系统。
当纯液体或液态混合物的蒸气压与外压相等时就会沸腾,此时的温度就是沸点。
在一定外压下,纯液体的沸点有确定值,通常说的液体沸点指101.3kPa下的沸点。
对于完全互溶的混合物系统,沸点不仅与外压有关,还与系统的组成有关。
在一定压力下,二组分完全互溶液态混合物系统的沸点与组成的关系可分为三类:(1)液态混合物的沸点介于两纯组分的沸点之间,如苯-甲苯系统;(2)液态混合物有沸点极大值,如丙酮-氯仿系统;(3)液态混合物有沸点极小值,如水-乙醇系统、苯-乙醇系统。
对于第(1)类,在系统处于沸点时,气液两相的组成不相同,可以通过精馏使系统的两个组分完全分离。
第(2)、(3)类是由实际系统与拉乌尔定律产生严重偏差导致。
正偏差很大的系统,如第(3)类,在T-x图上呈现极小值,负偏差很大时,如第(2)类,则会出现极大值。
相图中出现极致的那一点,称为恒沸点,恒沸点温度和组成都是非常重要的平衡数据。
具有恒沸点组成的二组分混合物,在蒸馏时的气相组成和液相组成完全一样,整个蒸馏过程中沸点恒定不变,因此称为恒沸混合物,如要获得两纯组分,则需采取其他方法。
液态混合物组成的分析是相平衡实验的关键。
组分分析常采用折射率法、密度法等物理方法和色谱分析法等。
本实验采用折射率法。
在一定温度下的折射率是物质的一个特征参数,液态混合物的折射率与组成有关,一般呈简单的函数关系。
4.3完全互溶双液系统讲解

T x1
x2
x3 x4
A
xB
B
一、理想的完全互溶的双液系统
T-p-x图
T
液 pA*
TA*
液
A
xB
pB* 气
气 气
TB* B
一、理想的完全互溶的双液系统
T-p-x图
二、杠杆规则
T g
TB*
DC E
l TA*
B
x1
xA x2
A
xA
物系点:系统物质的总组成点(不管相的存在状态)
二、杠杆规则
假设某压力下液态混合物沸腾时气液平衡的物系点为C点,那 么有: n总 nA nB nl ng
三、非理想的完全互溶双液系统
1. 正负偏差不大的体系
气液相图与理想液态混合物气液相图基本类似
p
p
T
A
xB
(a) p-x图
BA
xB
BA
xB
B
(b) p-x-y图
(c) T-x-y图
三、非理想的完全互溶双液系统
2. 正偏差很大的体系 有最高点
p-液相组成线
p
p
p-气相组成线
A
xB
B
(a) p-x图
A
xB
B
(b) p-x-y图
pA、pB偏离拉乌尔定律都很大,p-x图上形成最高点。
三、非理想的完全互溶双液系统
2. 正偏差很大的体系
g
T lg lg
(c) T-x-y图
l
l
A
x1
B
xB
在p-x图上有最高点,在T-x图上就有最低点,称最低恒沸点。 最低恒沸点对应的组成称最低恒沸组成。在此组成下蒸馏双 液系:yA = xA , yB= xB,A与B达不到分离目的,类似蒸馏 具有恒定沸点的纯物质,所以此点上混合物称恒沸混合物。
完全互溶双液系的平衡相图

7-目镜;
8-望远镜筒;
9-示值调节螺钉;
10-阿米西棱镜手轮;
11-色散值刻度圈;
12-棱镜锁紧扳手;
13-棱镜组;
14-温度计座;
15-恒温器接头;
16-保护罩;
17-主轴;
18-反光镜
阿贝折射仪是一种精密的
光学仪器,使用时注意以下几点:
☻使用时要注意保护棱镜,清洗时只能用擦镜纸而不 能用滤纸等。加 试样时不能将滴管口触及镜面。对于酸碱等腐蚀性液体不得用阿贝折射 仪。 ☻每次测定时,试样不可加地太多,一般加需加2-3滴即可。
在每一份样品的蒸馏过程中,正常回流1~2min后,即可 取样测定,不宜等待时间过长。
每次取样量不宜过多,取样时毛细滴管一定要干燥,不能 留有上次的残液,并且气相部分的样品要取干净。
使用阿贝折光仪时,棱镜上不能触及硬物(如滴管)。
六 数据处理
1. 将测得的折射率-组成数据列表,并绘 制成工作曲线。
恒温槽1台;阿贝折射仪1台;沸点仪1 套; 移液管(1mL2支、10mL1支);具塞小 试管9支。 环己烷(A.R.);无水乙醇(A.R.)
沸点仪原理图
1-温度计; 2-进样口; 3-加热丝; 4-气相冷凝液取样口 5-气相冷凝液
四 实验步骤
1. 调节恒温槽温度比室温高5℃,通恒温水于阿贝折射仪中。 2. 测定折射率与组成的关系,绘制工作曲线。
完全互溶双液系统气-液平衡相图的绘制(2)误差分析

大学化学实验Ⅱ实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业:环境科学091*名:***学号:**********指导教师:**实验成绩:实验编号:十四实验项目名称:完全互溶双液系统气-液平衡相图的绘制报告人:岳凡耀同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:2011年4月 28日一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X图或沸点-组成图。
B恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(а)所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1(b)所示。
(3)最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1(c)所示。
图1 完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
压力不同,同一双液系统的相图不同,恒沸点及恒沸组成也不同。
本实验采用回流冷凝的方法绘制乙醇-环己醇体系的T-X图。
完全互溶双液系的气-液平衡相图
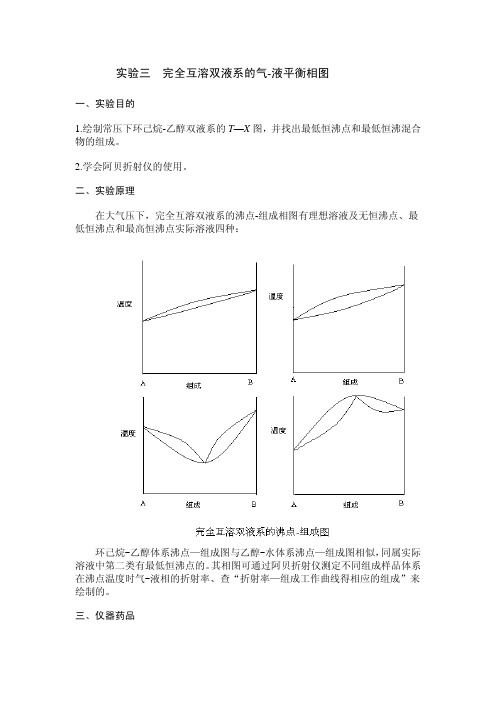
实验三完全互溶双液系的气-液平衡相图一、实验目的1.绘制常压下环己烷-乙醇双液系的T—X图,并找出最低恒沸点和最低恒沸混合物的组成。
2.学会阿贝折射仪的使用。
二、实验原理在大气压下,完全互溶双液系的沸点-组成相图有理想溶液及无恒沸点、最低恒沸点和最高恒沸点实际溶液四种:环己烷-乙醇体系沸点—组成图与乙醇-水体系沸点—组成图相似,同属实际溶液中第二类有最低恒沸点的。
其相图可通过阿贝折射仪测定不同组成样品体系在沸点温度时气-液相的折射率、查“折射率—组成工作曲线得相应的组成”来绘制的。
三、仪器药品1、仪器阿贝折射仪1台; 沸点仪1套; 恒温槽1台;0.1刻度水银温度计(0-100℃)2支;带磨口塞子的小样品管(2mL)16支;移液管(2mL)2支;胶头滴管2个; 50mL 烧杯10只(公用);50mL量筒10只(公用)。
2、药品(1)无水乙醇(AR);环己烷(AR); 二次蒸馏水。
(2)在样品瓶中依次加入环己烷10mL、20mL、30mL、40mL、50mL、60mL、70mL、80mL、90mL和乙醇90mL、80mL、70mL、60mL、50mL、40mL、30mL、20mL、20mL已知浓度的标准溶液(按纯样品的密度,换算成物质的量分数)9份。
(3)环己烷物质的量分数约为0.05、0.15、0.30、0.45、0.55、0.65、0.80、0.95的环己烷-乙醇溶液样品。
四、实验步骤1、测已知浓度的标准的折射率,作环己烷-乙醇的折射率-组成工作曲线(1)调节超级恒温槽水浴温度,使阿贝折射仪上的温度为250.1±℃左右。
(2)依次测已知浓度的标准溶液及纯乙醇和环己烷的的折射率(棱镜不能触及硬物如滴管,擦拭棱镜用擦镜纸)。
2、按图安装好沸点仪-沸点仪将一干燥、洁净的磁子放入已洗涤、干燥的沸点仪内,按图安装在实验室特制的磁力加热电热套内(250mL、只可覆盖圆底烧瓶底部1/5);一支温度计离圆底烧瓶约0.5cm,另一支温度计水银球上沿与支管口下沿相齐。
完全互溶双液系统气 液平衡相图的绘制2 误差分析

完全互溶双液系统气-液平衡相误差分析(2)------图的绘制.大学化学实验Ⅱ实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业环境科091岳凡耀姓名: 0908100121 学号:谭指导教师:蕾实验成绩:实验项目名称:完全互溶双液系统气十四-液平衡相图的绘制实验编号:同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:报告人:岳凡耀日月 28年20114一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X 图或沸点-组成图。
B液-恒定压力下,真实的完全互溶双液系的气.平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(а)所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1(b)所示。
(3)最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1(c)所示。
图1 完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
压力不同,同一双液系统的相图不同,恒沸点及恒沸组成也不同。
实验5 完全互溶双液系的平衡相图

实验5 完全互溶双液系定压气液液相平衡图【实验目的】1.掌握阿贝折光仪的使用方法并通过测定混和物折光率确定其组成。
2.学习常压下完全互溶双液系定压气液液相平衡图的测绘方法,加深对相律、恒沸点的理解。
3.绘制常压下环己烷-乙醇双液系的T—X图,并找出恒沸点混合物的组成和最低恒沸点。
【实验原理】相图:描述相平衡系统温度、压力、组成之间关系的图形,通过实验测定相平衡系统的组成来绘制。
由液态物质混合而成的二组分系统称为双液系统。
若两液体能以任意比例互溶,称其为完全互溶双液系;若两液体只能部分互溶,称其为部分互溶双液系。
纯液体或液态混合物的蒸气压与外压相等时就会沸腾,此时气液两相呈平衡,所对应的温度为沸点。
双液系的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系气液两相平衡时温度与组成关系的图称为Tx图或沸点组成图。
定压下完全互溶双液系的沸点组成图可分为三类:(1)各组分对拉乌尔定律的偏差不大,溶液的沸点介于两纯液体的沸点之间。
如苯与甲苯系统,其T-x图如图5.1 (a)所示;(2)各组分对拉乌尔定律有较大负偏差,其溶液有最高沸点。
如丙酮与氯仿系统,其T-X图如图5.1 (b)所示;(3)各组分对拉乌尔定律有较大正偏差,其溶液有最低沸点。
如乙醇与环己烷等系统,其T-X图如图5.1 (c)所示。
图5.1 完全互溶双液系的相图恒沸点与恒沸组:在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加,液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
压力不同,同一双液系的相图不同,恒沸点及恒沸组成也不同。
平衡数据测定:配制不同组成的溶液,大气压下加热至沸腾,测定不同组分的体系在沸点温度时气相、液相的折射率,再从折射率—组成工作曲线上查得相应的组成,然后绘制T—x图。
图5.2 沸点测定装置1进样口 2气相冷凝液取样口 3气相冷凝液 4数字温度计5电加热套实验装置如图。
完全互溶双液系气液平衡相图的绘制

完全互溶双液系气液平衡相图的绘制一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3.掌握阿贝折射仪的使用方法及原理。
4.了解和掌握沸点仪的测定原理及方法。
5.加深对完全互溶双液系气液平衡相图的理解和增强个人动手能力。
二.实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-x图),根据体系对拉乌尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。
(2)最大负偏差:存在一个最小蒸气压值,比两个纯液体的蒸气压都小,混合物存在着最高沸点,如盐酸-水体系,如图1 (b)所示。
(3)最大正偏差:存在一个最大蒸气压值,比两个纯液体的蒸气压都大,混合物存在图1 二组分真实液态混合物气-液平衡相图(T-x图)着最低沸点,如正丙醇—水体系,如图1(c))所示。
对于后两种情况,为具有恒沸点的双液系相图。
它们在最低或最高恒沸点时的气相和液相组成相同,因而不能象第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。
为了绘制双液系的T -x 相图,需测定几组原始组成不同的双液系在气-液两相平衡后的沸点和液相、气相的平衡组成。
本实验以环己烷-乙醇为体系,该体系属于上述第三种类型。
在沸点仪(如图2所示)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T -x 相图。
本实验中气液两相的组成均采用折光率法测定。
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。
物理化学 第四章 第三节 完全互溶双液体系

若将P=P*A+(P*B-P*A) xB 代入PyB=P*BxB 可得
Px yB * PA ( P P ) xB
理想溶液的 p-x-y 图
* B B * * B A
(xA= 1-xB) (yA =1-yB)
据此可以分别求得气相和液相的组成。
如果要全面描述溶液蒸气压与气、液两相 平衡组成的关系,可根据在P-x图上画出液相线, 然后从液相线上取不同的xB值代入上式求出相应 的气相组成yB值,把它们连接起来即构成气相线。 气相线总是在液相线的下面(见图)
四、蒸馏、分馏与精馏
x t
8
y8 x7 x6 x5
y7 y6
y5 x4
x3 x2 x1 y4 y3 y2
x0
y1 y0
B
A
x xB
根据上面讨论,对于完全互溶的二组分液液体系,把气相不断地部分冷凝,或将液相不 断地部分气化,都能在气相中浓集易挥发组 分,在液相中浓集难挥发组分。这样进行一连 串的部分气化和冷凝,可将混合液A、B完全 分离,这就是精馏原理。 工业上和实验室中这种部分气化和冷凝是在 精馏塔和精馏柱中进行的。精馏实际上是简单 蒸馏的多次组合。所以塔板数越多,蒸馏的次 数亦越多,分离的效果亦就越好(见下图所示)。
塔板上气-液两项重新分配
精馏塔中,塔顶得低沸点物, 塔底得高沸点物。
四、蒸馏、分馏与精馏
如果溶液介于A和C之 间,假定为x1,则经 精馏后,从塔顶蒸出 组成 的是具有最低恒沸 x1 x2 B A C 点的恒沸物C,流入 塔釜的是沸点高的纯组分A。如果溶液组成介于C和B之间, 设为x2 ,则经分离后得到的馏出液为C与残液为纯B。
四、蒸馏、分馏与精馏
进料
加 热 棒 精馏塔示意图
双液系的气-液平衡相图

双液系的气—液平衡相目的要求(1) 绘制在pΘ下环己烷-乙醇双液系的气-液平衡相图,了解相图和相律的基本概念。
(2) 掌握测定双组分液体沸点及正常沸点的方法。
(3) 掌握用折光率确定二元液体组成的方法。
基本原理一、气-液相图两种液态物质混合而成的二组分体系称为双液系。
两种组分若能按任意比例互相溶解,称为完全互溶双液系。
液体的沸点是指液体的蒸气压与外界压力相等时的温度。
在一定的外压力下,纯液体的沸点有其确定的值。
但双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。
根据相律,自由度=组分数-相数+2因此,一个气-液共存的二组分体系,其自由度为2.只要任意再确定一个变量,整个体系的存在状态就可以用二维图形来描述。
例如,在一定温度下,可以画出体系的压力p和组分x的关系图,如体系的压力确定,则可作温度T对x的关系图。
这就是相图。
在T-x相图上,还有温度,液相组成和气相组成三个变量,但只有一个自由度。
一旦设定某个变量,则其他两个变量必有相应的确定值。
图Ⅱ-5-1以苯-甲苯为例表明,温度T这一水平线指出了在此温度时处于平衡的液相组分x和气相组分y的相应值。
苯与甲苯这一双液系基本上接近理想溶液,然而绝大多数实际体系与拉乌尔定律有一定偏差。
偏差不大时,温度-组分相图与图Ⅱ-5-1相似,溶液的沸点仍介于两纯物质的沸点之间。
但是,有些体系的偏差很大,以至其相图将出现极值。
正偏差很大的体系在T-x图上呈现极小值,负偏差很大时则会有极大值。
这样的极值称为恒沸点,其气,液两相的组成相同。
例如,H2O-HCl体系的最高恒沸点在P0时为108.5,恒沸物的组成含HCl20.242%。
通常,测定一系列不同配比溶液的沸点及气、液两相组成,就可绘制气-液体系的相图。
压力不同时,双液系相图将略有差异。
本实验要求将外压校正到1个大气压力。
二、沸点测定仪各种沸点仪的具体构造虽各有特点,但其设计思想则都集中于如何正确测定沸点、便于取样分析、防止过热及避免分馏等方面。
完全互溶双液系的平衡相图

实验目的1. 绘制常压下环己烷-乙醇双液系的T—X图,并找出恒沸点混合物的组成和最低恒沸点。
2. 掌握阿贝折射仪的使用方法。
实验原理常温下,任意两种液体混合组成的体系称为双液体系。
假设两液体能按任意比例相互溶解,那么称完全互溶双液体系;假设只能局部互溶,那么称局部互溶双液体系。
双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
恒压下将完全互溶双液体系蒸馏,测定馏出物〔气相〕和蒸馏液〔液相〕的组成,就能找出平衡时气、液两相的成分并绘出T—X图。
通常,如果液体与拉乌尔定律的偏差不大,在T—X图上溶液的沸点介于A、B二纯液体的沸点之间见图2-4-1 (a)。
而实际溶液由于A、B二组分的相互影响,常与拉乌尔定律有较大偏差,在T—X图上就会有最高或最低点出现,这些点称为恒沸点,其相应的溶液称为恒沸点混合物,如图2-4-1(b),〔c)所示。
恒沸点混合物蒸馏时,所得的气相与液相组成一样,因此通过蒸馏无法改变其组成。
图1 完全互溶双液系的相图本实验采用回流冷凝的方法绘制环己烷-乙醇体系的T—X图。
其方法是用阿贝折射仪测定不同组分的体系在沸点温度时气相、液相的折射率,再从折射率-组成工作曲线上查得相应的组成,然后绘制T—X图。
实验试剂环己烷(A.R);无水乙醇(A.R)。
实验仪器沸点仪1套;恒温槽1台;阿贝折射仪1台;移液管(1mL,2支;10mL,1支);具塞小试管9支。
实验装置a原始数据测定折射率与混合液浓度的关系环己烷0 0.100 0.200 0.300 0.400 0.500 0.600 0.700 0.800 0.900 1.000无水乙醇1.000 0.900 0.800 0.700 0.600 0.500 0.400 0.300 0.200 0.100 0W%0 10 20 30 40 50 60 70 80 90 100折光率1.34721.361711.36861.37451.38191.38791.39571.40541.40921.41911.5010体积单位为毫升右半部沸点-组成关系的测定20毫升无水乙醇液中参加环己烷的体积0.5 1.0 1.5 2.0 4.0 14.0温度℃79.5 77.8 74.9 71.5 69.0 67.8液相折射率Nl1.3598 1.3605 1.3600 1.3656 1.3742 1.3909液相W% 8.03 11.04 10.29 11.04 14.50 41.86气相折射率Ng1.3628 1.3731 1.3775 1.3811 1.3930 1.3981气相W% 12.39 19.01 10.29 28.33 40.35 62.15左半部沸点-组成关系的测定25毫升环己烷参加无水乙醇的体积0.1 0.2 0.3 0.4 1.0 5.0温度℃75.0 76.1 74.9 73.9 69.8 66.8液相折射率Nl1.4192 1.4150 1.4126 1.4075 1.4040 1.3971液相W% 100 100 100 100 100 80.20气相折射率Ng1.4115 1.4224 1.4220 1.4216 1.4196 1.4010气相W% 95.97 96.73 98.98 99.28 84.10 69.22试验数据处理折射率-组成数据图沸点与组成的关系204060801001200.00020.00040.00060.00080.000100.000120.000组成沸点系列1系列2系列3系列4系列5系列6系列7系列8系列9系列10系列11系列12。
完全互溶双液系气液平衡相图的绘制实验报告

完全互溶双液系气液平衡相图得绘制。
一.实验目得1。
测定常压下环己烷一乙醉二元系统得气液平衡数据,绘制沸点一组成相图。
2。
掌握双组分沸点得测定方法,通过实验进一步理解分镉原理。
3。
堂握阿贝折射仪得使用方法。
二.实验原理两种液体物质混合而成得两组分体系称为双液系、根据两组分间溶解度得不同,可分为完全互溶、部分互溶与完全不互溶三种情况、两种挥发性液体混合形成完全互溶体系时,如果该两组分得蒸气压不同,则混合物得组成与平衡时气相得组成不同。
出压力保持一定,混合物沸点与两组分得相对含量有关。
恒定压力下,真实得完全互溶双液系得气一液平衡相图(r-x),根据体系对拉乌尔定律得偏差情况,可分为3类:(1)一般偏差:混合物得沸点介于两种纯组分之间,如甲苯一苯体系,如图2 o 7(a)所示。
(2 )垠大负偏差:存在一个最小蒸汽压值,比两个纯液体得蒸汽压都小,混合物存在着最髙沸点,如盐酸-水体系,如图2.7(b)所示。
(3 )最大正偏差:存在一个战大蒸汽压值,比两个纯液体得蒸汽圧都大,混合物存在着最低沸点如图2、7 (c)) 所示。
X B(a)(b)图2。
7二组分真实液态混合物气一液平衡相图(Tn图)后两种情况为具有恒沸点得双液系相图、它们在昴低或最岛恒沸点时得气相与液相组成相同,因而不能象第一类那样通过反复蒸馆得方法而使双液系得两个组分相互分离,而只能采取精懾等方法分离出一种纯物质与另一种恒沸混合物、为了测定双液系得T—x相图,需在气一液平衡后,同时测定双液系得沸点与液相、气相得平衡组成、木实验以环己烷■乙醇为体系,该体系属于上述第三种类型,在沸点仪(如图2、8 )中蒸锚不同组成得混合物,测定其沸点及相应得气、液二相得组成, 即可作出T—x相图。
木实验中两相得成分分析均采用折光率法测定。
折光率就是物质得一个持征数值,它与物质得浓度及温度有关,因此在测虽物质得折光率时耍求温度恒定、溶液得浓度不同、组成不同,折光率也不同、因此可先配制一系列已知组成得溶液,在恒定温度下测其折光率,作岀折光率 -组成匸作曲线,便可通过测折光率得大小在匸作曲线上找出未知溶液得组三.仪器与试剂沸点仪,阿贝折射仪,调斥变斥器,超级恒温水浴,溫度测定仪,长短取样管。
完全互溶双液系统气-液平衡相图的绘制(2)误差分析

大学化学实验Ⅱ实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业:环境科学091姓名:岳凡耀学号: 01指导教师:谭蕾实验成绩:实验编号:十四实验项目名称:完全互溶双液系统气-液平衡相图的绘制报告人:岳凡耀同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:2011年4 月 28 日一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X B图或沸点-组成图。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(а)所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1(b)所示。
(3)最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1(c)所示。
图1 完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
压力不同,同一双液系统的相图不同,恒沸点及恒沸组成也不同。
本实验采用回流冷凝的方法绘制乙醇-环己醇体系的T-X B图。
完全互溶双液系统气 液平衡相图的绘制2误差分析

大学化学实验□实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业:_________ 环境科学091姓名:__________ 岳凡耀学号:_________ 0908100121指导教师:_____________ 谭蕾实验成绩:_____________________________实验编号:十四实验项目名称:完全互溶双液系统气-液平衡相图的绘制报告人:岳凡耀同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:2011年4月28日一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X B图或沸点-组成图。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1 ( a ) 所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1 ( b)所示。
(3 )最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1 (c)所示。
图1完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
........word...完美整理精品文档
实
沸点仪 1 套;恒温槽 1 台;阿贝折射仪 1 台;移液管(1mL,2 支;10mL,1 支);具塞
验
仪 小试管 9 支。
器
a
b
实 验 装 置
.......专业资料供学习分享下载
........word...完美整理精品文档
1. 调节恒温槽温度 30℃,通恒温水于阿贝折射仪中。 2. 测定折射率与组成的关系,绘制工作曲线:将 9 支小试管编号,依次移入 0.100mL、 0.200mL、…、0.900mL 的环己烷,然后依次移入 0.900mL、0.800mL、…、0.100mL 的无水 乙醇,轻轻摇动,混合均匀,配成 9 份已知浓度的溶液。用阿贝折射仪测定每份溶液的折射 率及纯环己烷和纯无水乙醇的折射率。以折射率对浓度作图(按纯样品的密度,换算成质量 百分浓度或者摩尔浓度),即得工作曲线。 3. 测定环己烷-乙醇体系的沸点与组成的关系
实
1. 绘制常压下环己烷-乙醇双液系的 T—X 图,并找出恒沸点混合物的组成和最低恒沸
验 点。
目 的
2. 掌握阿贝折射仪的使用方法。
.......专业资料供学习分享下载
........word...完美整理精品文档
常温下,任意两种液体混合组成的体系称为双液体系。若两液体能按任意比例相互溶解, 则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。双液体系的沸点不仅与 外压有关,还与双液体系的组成有关。恒压下将完全互溶双液体系蒸馏,测定馏出物(气相) 和蒸馏液(液相)的组成,就能找出平衡时气、液两相的成分并绘出 T—X 图。
系列1 系列2 系列3 系列4 系列5 系列6 系列7 系列8 系列9 系列10 系列11 系列12
.......专业资料供学习分享下载
........word...完美整理精品文档
1. 该实验中,测定工作曲线时折射仪的恒温温度与测定样品时折射仪的恒温温度是否
ቤተ መጻሕፍቲ ባይዱ需要保持一致?为什么?
答:需要保持一致,因为折射率是温度的函数,样品中气液相组成是通过折射率曲线查
1. 间歇法测定完全互溶双液体系的 T—X 图
测定沸点与组成的关系时,也可以用间歇方法测定。先配好不同质量百分数的溶液,按
实 顺序依次测定其沸点及气相、液相的折射率。
将配好的第一份溶液加入沸点仪中加热,待沸腾稳定后,读取沸点温度,立即停止加热。
验
取气相冷凝液和液相液体分别测其折射率。用滴管取尽沸点仪中的测定液,放回原试剂瓶中。
本实验是以恒沸点为界,把相图分成左右两半支,分两次来绘制相图。具体方法如下: (1) 右半支 沸点-组成关系的测定 取 20mL 无水乙醇加入沸点仪中,然后依次加入环己烷 0.5mL、1.0mL、1.5mL、2.0mL、 4.0mL、14.0mL。用前述方法分别测定溶液沸点及气相组分折射率 ng、液相组分折射率 nL。 实验完毕,将溶液倒入回收瓶中。 (2) 左半支 沸点-组成关系的测定 取 25mL 环己烷加入沸点仪中,然后依次加入无水乙醇 0.1mL、0.2mL、0.3mL、0.4mL、 1.0mL、5.0mL,用前述方法分别测定溶液沸点及气相组分折射率 ng、液相组分折射率 nL。
实验 名称
实验者 姓名
实验 日期
室温
指导 教师
评语
........word...完美整理精品文档
完全互溶双液系的平衡相图
合作者
xxx
姓名
xxx xxx xx
2011-09-27
25.1 ℃
气压
101.78
Pa
杨静
成绩
.......专业资料供学习分享下载
........word...完美整理精品文档
........word...完美整理精品文档 .......专业资料供学习分享下载
如图 2 所示。安装好沸点仪,打开冷却水,加热使沸点仪中溶液沸腾。最初冷凝管下端 袋状部的冷凝液不能代表平衡时的气相组成。将袋状部的最初冷凝液体倾回蒸馏器,并反复 实 2~3 次,待溶液沸腾且回流正常,温度读数恒定后,记录溶液沸点。用毛细滴管从气相冷 验 步 凝液取样口吸取气相样品,把所取的样品迅速滴入阿贝折射仪中,测其折射率 ng。再用另 骤 一支滴管吸取沸点仪中的溶液,测其折射率 nL。
0.1
75.0 1.4192 100 1.4115
0.2
76.1 1.4150 100 1.4224
0.3
74.9 1.4126 100 1.4220
.......专业资料供学习分享下载
体积单位为毫升
2.0
4.0
71.5 1.3656 11.04 1.3811 28.33
69.0 1.3742 14.50 1.3930 40.35
99.28
84.10
69.22
.......专业资料供学习分享下载
........word...完美整理精品文档
折射率-组成数据图
试
验
数
据
处
理
沸点
120 100 80 60 40 20
0 0.000
沸点与组成的关系
20.000
40.000
60.000 组成
80.000 100.000 120.000
.......专业资料供学习分享下载
........word...完美整理精品文档
测定折射率与混合液浓度的关系
环0 己
0.100 0.200 0.300 0.400 0.500 0.600 0.700 0.800 0.900 1.000
烷
无 1.000 0.900 0.800 0.700 0.600 0.500 0.400 0.300 0.200 0.100 0 水 乙
通常,如果液体与拉乌尔定律的偏差不大,在 T—X 图上溶液的沸点介于 A、B 二纯液 体的沸点之间见图 2-4-1 (a)。而实际溶液由于 A、B 二组分的相互影响,常与拉乌尔定律有 较大偏差,在 T—X 图上就会有最高或最低点出现,这些点称为恒沸点,其相应的溶液称为 恒沸点混合物,如图 2-4-1(b),(c)所示。恒沸点混合物蒸馏时,所得的气相与液相组成相同, 因此通过蒸馏无法改变其组成。
讨 在沸点仪中再加入新的待测液,用上述方法同样依次测定。(注意:更换溶液时,务必用滴
论 管取尽沸点仪中的测定液,以免带来误差。)
与
2. 具有最低恒沸点的完全互溶双液体系很多,除了上面介绍的环己烷-乙醇体系外,再
介绍一个异丙醇-环己烷体系。实验中两个体系的工作曲线及 T—X 图的绘制方法完全相同,
总 只是样品的加入量有所区别,现介绍如下:
得到。
思
2. 过热现象对实验产生什么影响?如何在实验中尽可能避免?
考
答:过热现象导致相图区域变窄,液相线上移。可以通过每次加入少量沸石或者通入新
题 鲜空气避免。实验中我们通过调节加热电流得大小使沸腾得缓和来避免。
3. 在连续测定法实验中,样品的加入量应十分精确吗?为什么?
答:不需要,因为样品的组成是通过工作曲线查的而不是通过样品的加入量计算得到的。
醇
W0
10
20
30
40
50
60
70
80
90
100
%
折
光 1.34 1.36 1.36 1.37 1.38 1.38 1.39 1.40 1.40 1.41 1.50
率
72 171 86 45 19 79 57 54 92 91 10
原 右半部沸点-组成关系的测定
20 毫升无 0.5
1.0
1.5
始 水乙醇液 中加入环
数 己烷的体 积
据 温度 ℃ 79.5
77.8
74.9
液相折射 率 Nl 液相 W% 气相折射 率 Ng 气相 W%
1.3598
8.03 1.3628
12.39
1.3605
11.04 1.3731
19.01
1.3600
10.29 1.3775
10.29
左半部沸点-组成关系的测定
25 毫升环 己烷加入 无水乙醇 的体积 温度 ℃ 液相折射 率 Nl 液相 W% 气相折射 率 Ng
实 验 原 理
图 1 完全互溶双液系的相图
本实验采用回流冷凝的方法绘制环己烷-乙醇体系的 T—X 图。其方法是用阿贝折射仪测 定不同组分的体系在沸点温度时气相、液相的折射率,再从折射率-组成工作曲线上查得相 应的组成,然后绘制 T—X 图。
实
验
环己烷(A.R);无水乙醇(A.R)。
试
剂
.......专业资料供学习分享下载
0.4
1.0
73.9 1.4075
100 1.4216
69.8 1.4040
100 1.4196
14.0
67.8 1.3909 41.86 1.3981 62.15
5.0
66.8 1.3971 80.20 1.4010
气相 W% 95.97
........word...完美整理精品文档
96.73
98.98
结
右半分支: 先加入 20mL 异丙醇,然后依次加入 1mL 、1.5mL、2.0mL、2.5mL、3.0mL、
6.0mL、25.0mL 环己烷。
左半分支: 加入 50mL 环己烷,依次加入 0.3mL、0.5mL、0.7mL、1.0mL、2.5mL、5.0mL、
12.0mL 的异丙醇。
.......专业资料供学习分享下载
