第3章 自由基聚合-2
第三章自由基聚合

HC CH
Cl
O O O
C H
C H
Cl
(3) 三取代、四取代,一般不能聚合,但也有例外:取 代基为小体积的氟代乙烯 。
F F C H C H F F C H C F F F H2C C F F C C F
F
(1) 1, 1 双取代烯类单体CH2=CXY ,通常,比单取代更 易聚合,若两个取代基均体积较大(如1,1-2苯基乙烯), 则只能形成二聚体。
(2) 具有共轭效应的烯类单体 ∏电子云流动性大,易诱导极化,可随进攻试剂 性质的不同而取不同的电子云流向,可进行多种机 理的聚合反应(自由基、阴离子和阳离子聚合)。 如苯乙烯、甲基苯乙烯、丁二烯及异戊二烯等等 。 + + R H2C CH R H2C CH
+
单烯CH2=CHX中取代基电负性不同和聚合倾向的关系图
(二) 位阻效应
位阻效应是由取代基的体积、数量、位置等 所引起的。在动力学上它对聚合能力有显著的影 响,但它不涉及对活性种的选择。
(1) 1, 1 双取代烯类单体CH2=CXY ,通常,比单取代更
易聚合,但两个取代基均体积较大(如1,1-2苯基乙烯),
则只能形成二聚体。
H2C
C
(2) 1,2 双取代的烯类化合物,因结构对称,极化程度
第三章 自由基聚合
1. 单体聚合的选择性 2. 四种基元反应及自由基聚合的特征 3. 引发反应、引发剂种类及其使用条件 4. 聚合速率方程的推导、公式、使用 5. 聚合速率以及分子量的影响因素 6. 分子量的公式及其使用条件 7. 阻聚剂和烯丙基的自阻聚作用
高分子化学课件第三章 自由基共聚合

m1= d[M1] = k11[M1*][M1] + k21[M2*][M1] (i)
m2 d[M2]
k12[M1*][M2] + k22[M2*][M2]
第三章 自由基共聚合
(3)假设共聚反应是一个稳态过程,即总的活性中心的浓 度[M1*+M2*]恒定,[M1*]和[M2*]的消耗速率等于[M1*]和 [M2*]的生成速率,并且 M1* 转变为M2*的速率等于M2*转 变为M1*的速率;
二元共聚合的理论研究较系统深入,而三元及三元以上共 聚合复杂,理论研究很少,但实际应用的例子颇多。ABS, SBS
三元以上聚合,一般以两种单体确定主要性质,另外单体 改性。
二元共聚物根据两单体单元在分子链上的排列方式可分四 类:
第三章 自由基共聚合
(1)无规共聚物(random copolymer) 两种单体单元的排列没有一定顺序,A单体单元相邻的单
第三章 自由基共聚合
四种竞争链增长反应:
k11 M1* + M1
k12 M1* + M2
k21 M2* + M1
k22 M2* + M2
M1* R11 = k11[M1*][M1]
M2* R12 = k12[M1*][M2]
M1*
R21 = k21[M2*][M1]
M2* R22 = k22[M2*][M2]
若含一段A链与一段B链,如~AAAAAAA-BBBBBBBBBB~, 称AB型二嵌段共聚物;如果是由一段A链接一段B链再届一 段A链,如~AAAAAA-BB~BBB-AAAAAAA~,则称ABA型 三嵌段共聚物;若由多段A链和多段B链组成,则称(AB)n型 多嵌段共聚物。
第三章 自由基共聚合
高分子化学第三章 自由基聚合

• 链转移反应前后,自由基的数目未变。
35
1. 向单体转移
· ~~CH2-CH + CH2=CH Cl Cl
· ~~CH=CH + CH3-CH Cl Cl
• 注意CH2=CHCl单体
36
2. 向溶剂或链转移剂转移
X ~~CH2CH · + YS X ~~CH2CHY + S ·
• 溶剂:
• 链转移剂:有较强的链转移能力的化合
1 2
[I ]
1
2
[M ] (3—35式)
注意本方程的适用范围
73
二、温度对聚合速率的影响
• 阿累尼乌斯公式:K=Ae–Ea/RT
其中:K=kp(kd/kt)½ 则:Ea=Ep+Ed/2–Et/2
74
一般情况下: Ep≈29kJ•mol–1, Ed≈126kJ•mol–1 Et≈17kJ•mol–1
10
一、 聚合的可能性
• 主要取决于双键上取代基的空间 效应
11
1.烯类单体: CXY=CMN
(1)一取代( CH2=CHX)
可均聚合
12
(2)二取代
(CH2=CXY、CHX=CHY) (a)1,1——二取代:一般不考虑空 间位阻效应,可均聚合。
注意:CH2=C(Ar)2只能形成二聚体
13
(b)1,2——二取代
54
2.半衰期
[I] ln = Kd t [I0]
• 60℃
ln2 t½ = K d
(3—17)
t½ >6h,低活性引发剂 1h< t½ <6h,中活性引发剂 t½ <1h,高活性引发剂
55
3. 引发效率
3高分子化学 第三章 自由基聚合2

19
链引发反应
引发剂分解速率常数与温度之间的关系遵循阿累尼
乌斯(Arrhenius)经验公式。
kd
A e Ed/RT d
(3—18)
或
lnk d lnA d Ed /RT
(3—19)
不同温度测得某一引发剂的多个分解速率常数,作lnkd1/T 图,得一直线,由截距求得Ad,由斜率求Ed。 由于Ed 为正值,从式可知,随温度升高, kd增大。
RCH2 CH + CH2 CH
X
X
RCH2CHCH2CH XX
RCH2CH [ CH2CH ]n CH2CH
X
X
X
两个基本特征: (1)放热反应。 (2)链增长反应活化能低,反应速率极高。
5
自由基聚合机理
自由基聚合反应中,结构单元间的连接存在“头- 尾”、“头-头”(或“尾-尾”)两种可能的形式,一般 以头-尾结构为主。
诱导分解实际上是自由基向引发剂的转移反应。
O
O
O
O
Mx +
COOC
MxO C
+
CO
整个过程中自由基数量没有增加,但消耗了一个引发剂分子,
从而使引发剂效率降低。
过氧化物容易发生诱导分解。
Mx + ROOH
MxOH + RO
25
(2)笼蔽效应(cage effect) 当体系中引发剂浓度较低时,引发剂分子处于单体或溶 剂的包围中而不能发挥作用,称为笼蔽效应。 偶氮二异丁腈在笼子中可能发生的副反应:
HO OH 2HO
过氧化类引发剂的典型代表:过氧化二苯甲酰(dibenzoyl peroxide , BPO)。
BPO的分解分两步,第一步分解成苯甲酰自由基,第二 步分解成苯基自由基,并放出CO2。
第三章自由基聚合工艺

3.1 自由基聚合工艺基础 3.2 本体聚合生产工艺 3.3 悬浮聚合生产工艺 3.4 溶液聚合生产工艺 3.5 乳液聚合生产工艺
3.1 自由基聚合工艺基础
◆自由基聚合反应是当前高分子合成工业中应用最广泛 的化学反应之一
◆自由基聚合反应适用单体:乙烯基单体、二烯烃类单 体
影响聚合物平均分子量的主要因素:反应温度、引发 剂浓度和单体浓度、链转移剂的种类和用量
(1)聚合反应温度升高,所得聚合物的平均分子量降低 (2)引发剂用量对聚合物平均分子量发生显著的影响。
(动力学链长V=K[M]/[I]0.5
(3)链转移反应导致所得聚合物的分子量显著降低,对 获得高分子量聚合物不利,但可用来控制产品的平均 分子量,甚至还可用来控制产品的分子量。
混炼后用于成型 注塑成型用 假牙齿、牙托等
聚合物溶液 直接用于纺丝或溶解后
或颗粒
纺丝
聚合物溶液 直接用来转化为聚乙烯 醇
表2 四种聚合方法的工艺特点
聚合方法
聚合 主要操作方式 过程 反应温度控制
单体转换率 分离 工序复杂程度 回收 及后 动力消耗 处理 过程 产品纯度
废水废气
本体聚 乳液聚合 合
连续 连续
7.氯乙烯自由聚合时,聚合速率用 引发剂用量 调 节,而聚合物的相对分子质量用 聚合温度 控制。
第3章 自由基聚合生产工艺
3.1 自由基聚合工艺基础 3.2 本体聚合生产工艺 3.3 悬浮聚合生产工艺 3.4 溶液聚合生产工艺 3.5 乳液聚合生产工艺
3.2 本体聚合生产工艺
本体聚合:单体中加有少量引发剂或不加引发剂依赖热 引发,而无其他反应介质存在的聚合实施方法。
① 过氧化物类
通式:R-O-O-H 或 R-O-O-R (R可为烷基、芳基、酰基、碳酸酯基、磺酰基等)
3-自由基聚合(2)

[I] ln [ I ]0
-k t
四价铈盐和醇、醛、酮、胺等组成的氧化-还原体系, 可有效地引发烯类单体聚合或接枝聚合(如淀粉接枝丙烯 腈)。
Ce
4+
+
H C
H C
Ce 3+ +
OH OH
CH + CH O HO
+ H+
26
(ii)油溶性氧化—还原引发体系 氧化剂:氢过氧化物、二烷基过氧化物、二酰基过氧化 物等。 还原剂:叔胺、环烷酸盐、硫醇、有机金属化合物,如 [Al(C2H5)3]、 [B(C2H5)3] 等。
特征:放热反应、活化能低—20-34kJ/mol、速率 常数高、聚合度增大。
6
在链增长反应过程中,不仅研究反应速率,还需 考察增长反应对大分子微结构的影响。
在链增长反H2CH CH2 CH + CH2 X CH X X X or CHCH2 CH2CH X X
Rd
d [I] dt
k d [I]
负号—代表[I]随时间t的增加而减少; kd— 分解速率常数,单位为s-1。
29
将上式积分,得:
[I] ln [ I ]0
-k t
d
[I]0—引发剂的起始浓度, 单位为mol/L
[I] —时间为t时的引发剂 浓度,单位为mol/L
[I] e -k d t [ I ]0
2
C O
2
+ 2 CO2
BPO按两步分解。第一步均裂成苯甲酸基自由基, 有单体存在时,即引发聚合;无单体存在时,进一步 分解成苯基自由基,并放出CO2,但分解不完全。
21
3、无机过氧类引发剂
代表物:无机过硫酸盐,如过硫酸钾K2S2O8和 (NH4)2S2O8,这类引发剂能溶于水,多用于乳液聚合和 水溶液聚合。
《材化高分子化学》第3章 自由基聚合
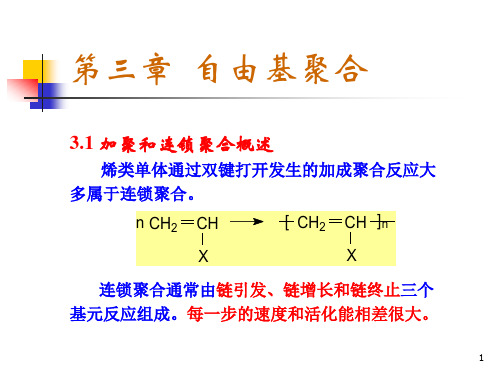
E = 105~150 kJ/mol (3—1)
kd = 10-4~10-6 s-1
(3—2)
19
第三章 自由基聚合
b. 单体自由基的形成
R + CH2 CH X
RCH2 CH X
由初级自由基与单体加成产生,为放热反应, 活
化能低,反应速度快。
E = 20 ~ 34 kJ/mol
(3—3)
20
第三章 自由基聚合
(CH3)2C N N C (CH3)2
2 (CH3)2C + N2
CN
CN
CN
优点:
(1)分解只形成一种自由基,无诱导分解。 (2)常温下稳定。80℃以上剧烈分解。
35
第三章 自由基聚合
(2)有机过氧化类引发剂
最简单的过氧化物:过氧化氢。活化能较高, 220kJ/mol,一般不单独用作引发剂。
HO OH 2HO
7
第三章 自由基聚合
分子中含有推电子基团,如烷基、烷氧基、苯基、乙 烯基等,碳=碳双键上电子云增加,有利于阳离子聚合进 行。
δ
CH2 CH Y
注意:丙烯分子上有一个甲基,具有推电子性和超共轭双 重效应,但都较弱,不足以引起阳离子聚合,也不能进行 自由基聚合。只能在配位聚合引发体系引发下进行配位聚 合。
30
第三章 自由基聚合
3.4.2 自由基聚合反应的特征
(1)可分为链引发、链增长、链终止等基元反应。 各基元反应活化能相差很大。其中链引发反应速率 最小,是控制聚合过程的关键。
慢引发、快增长、有转移,速终止。
与逐步缩聚机理特征比较见p75表3-6。
31
第三章 自由基聚合
(2)只有链增长反应使聚合度增加。从单体转化为 大分子的时间极短,瞬间完成。体系中不存在聚合 度递增的中间状态(p75图3-2)。聚合度与聚合时间 基本无关。
第3章 自由基共聚

k 12 [M1 ][ M 2 ] [M ] 2 k 21 [M1 ]
代入
d[M1 ] k11 M1 M1 k 21 M M1 2 d[M 2 ] k 22 M 2 M 2 k12 M1 M 2
得:
d[M 1 ] k 11k 21[M 1 ] k 12 k 21[M 1 ][ M 2 ] 2 d[M 2 ] k 22 k 12 [M 2 ] k 12 k 21[M 1 ][ M 2 ]
n CH2=CH + mCH2=CH Cl
共聚
[CH2 CH]n [CH2 CH ]m Cl OCOCH 3
OCOCH 3
根据参加反应单体的单元数,共聚反应可分为:
二元共聚: 三元共聚: 多元共聚: 两种单体 三种单体 3种或3种以上单体 共同进行反应
3.1 引言
二、 共聚物类型
共聚物按大分子链中单体链节的排列方式可分为下列四种: (1)无规共聚物(random copolymer)
链引发(initiation): 2个引发反应。
I R
R M1 RM
ki,1 1
Ri,1 ki ,1
R M
1
R M 2 RM
ki, 2
2
Ri,2 ki , 2 R M 2
3.2 二元共聚物组成
链增长(propagation):4个增长反应
3.2 二元共聚物组成
链终止(termination): 3个终止反应
M M1
M M2
2
1
死大分子
kt,11
Rt ,11 2kt ,11 M
第3章自由基聚合反应

tr,I Mx I Mx R
k
Rtr,I ktr,I [M ][I]
Rtr,S ktr,S[M ][S]
Rp Rt Rtr Rp C ( D) Rt Rtr 2
tr,S Mx S Mx S
k
聚合度的表达式应是:
高分子化学
3.5 聚合中期聚合反应速率
聚合初期的恒速阶段一般可持续到转化率达10~15%。
fkd 1/2 Rp k p [M ] [I ] kt
1/2
自动加速效应(autoacceleration)——聚合反应速率 自动加快的现象称为自动加速现象。
一般单体的聚合体系都会存在自动加速现象,差别是 体系不同,出现的早晚和程度不同。 主要原因 3.5.3.1 凝胶效应 ——由于反应过程体系粘度的增加引起的自动加速现象称为 凝胶效应(gel effect)。
Rp k p [M ][M ]
Rt 2kt [M ]2
ktr , M ktr , I [ I ] ktr , S [ S ] ktr , P [ P ] 2 kt R p 1 C ( D ) 2 2 2 k p [M ] kp k p [M ] k p [M ] k p [M ] Xn
凝胶效应的主要原因在于链终止反应是受扩散控制的反应。
高分子化学
第3章 自由基聚合反应
3.5-3.9
对于正常的双基终止,链自由基双基终止过程可以分为 三步:链自由基质心的平移、链段重排(控制步骤)和双基 碰撞发生反应。体系黏度是影响的主要因素。
fk R p k p [ M ] d [ I ]1/2 kt
k p [M ] (2kt )1/2 Ri1/2
自由基聚合习题参考答案
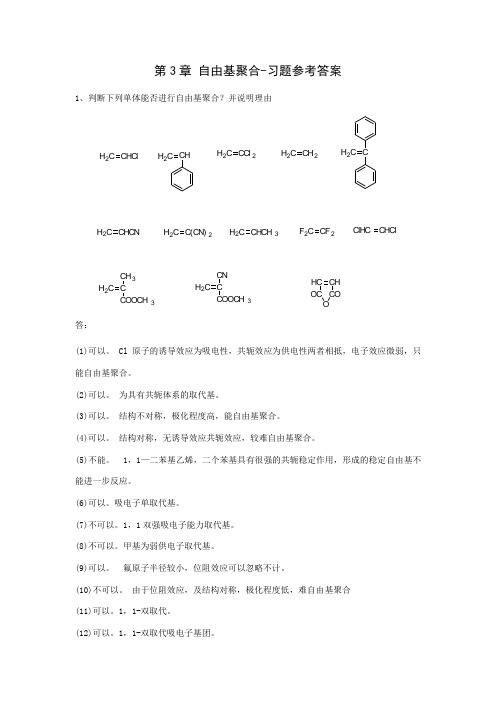
第3章自由基聚合-习题参考答案1、判断下列单体能否进行自由基聚合?并说明理由H2C CHCl H2C CH H2C CCl2H2C CH2H2C CH2C CHCN H2C C(CN)2H2C CHCH3F2C CF2ClHC CHClH2C CCH3COOCH3H2C CCNCOOCH3HC CHOC COO答:(1)可以。
Cl原子的诱导效应为吸电性,共轭效应为供电性两者相抵,电子效应微弱,只能自由基聚合。
(2)可以。
为具有共轭体系的取代基。
(3)可以。
结构不对称,极化程度高,能自由基聚合。
(4)可以。
结构对称,无诱导效应共轭效应,较难自由基聚合。
(5)不能。
1,1—二苯基乙烯,二个苯基具有很强的共轭稳定作用,形成的稳定自由基不能进一步反应。
(6)可以。
吸电子单取代基。
(7)不可以。
1,1双强吸电子能力取代基。
(8)不可以。
甲基为弱供电子取代基。
(9)可以。
氟原子半径较小,位阻效应可以忽略不计。
(10)不可以。
由于位阻效应,及结构对称,极化程度低,难自由基聚合(11)可以。
1,1-双取代。
(12)可以。
1,1-双取代吸电子基团。
(13) 不可以。
1,2-双取代,空间位阻。
但可进行自由基共聚。
2、试比较自由基聚合与缩聚反应的特点。
答:自由基聚合:(1)由链引发,链增长,链终止等基元反应组成,其速率常数和活化能均不等,链引发最慢是控制步骤。
(2)单体加到少量活性种上,使链迅速增长。
单体-单体,单体-聚合物,聚合物-聚合物之间均不能反应。
(3)只有链增长才是聚合度增加,从一聚体增加到高聚物,时间极短,中间不能暂停。
聚合一开始就有高聚物产生。
(4)在聚合过程中,单体逐渐减少,转化率相应增加(5)延长聚合时间,转化率提高,分子量变化较小。
(6)反应产物由单体,聚合物,微量活性种组成。
(7)微量苯酚等阻聚剂可消灭活性种,使聚合终止。
缩聚反应:(1)不能区分出链引发,链增长,链终止,各部分反应速率和活化能基本相同。
第三章-2:自由基聚合机理-基本反应

链终止
8-21
慢引发、快增长、速终止
重点内容
1、正确书写自由基聚合的基元反应 2、自由基聚合反应的特点 3、典型单体的双基终止方式
作业题
1、苯乙烯聚合制备聚苯乙烯,使用AIBN为引发剂,
问:在反应某一时刻,体系内的主要组成是什么? 所发生的主要基元反应是什么?特征是什么? 如果单体改为醋酸乙烯,差别在哪里?
2、下列因素中对聚氯乙烯的相对分子质量影响最大的是: 聚合温度、反应时间、引发剂用量
思考题: 图中1,2曲线是由怎样的基元反应特征造成的
1:(慢引发)
分子量 1 快增长 速终止 2
2:(快引发)
慢增长 无终止
反应时间
链引发
链增长
链终止
郑军峰
链式聚合机理与烯类单体结构小结
1)离子聚合对单体选择性高
CH3
正
负
CH2═C CH3
2)自由基聚合对单体选择性低,除电子效应太强单体 自+负
CH2═CH CL
自
3)1,1-二取代单体位阻大,难均聚,可共聚
4)共轭结构是百搭单体
第二节:自由基聚合机理
聚合 机理
反应快慢(动力学)
反应历程(基元反应) 特点
生成一个高分子,中间头-头,两段带引发剂残基
•双基歧化终止
生成两个高分子,其中一个高分子端基为引发剂残基, 一端带双键
终止特点:活化很低,速率常极高,受扩散控制,速率慢。
终止方式取决于单体结构和聚合物温度
•链自由基越活泼,越容易歧化终止
歧化
偶合
•温度升高有利于歧化终止
由温度而定
(4)链转移反应(Chain Transfer Reaction)
高分子化学-2(自由基聚合)

.
( 1)
水溶性氧化还原引发体系
常用的氧化剂:过氧化氢、过硫酸盐、氢过氧化物、Cu2+,Ag+, Fe3+ 无机还原剂:Fe2+,HSO3-,SO32常用的还原剂 有机还原剂:醇、胺、草酸、葡萄糖 如:无机-无机氧化还原引发体系
HO-OH + Fe2+
RO-OH + Fe2+
-.
Fe3+ +
Fe3+ +
温度升高,H-H连接形式的结构增加
怎样来合成H-H结构的聚合物?
-(CH2-CH=CH-CH2)- Cl2
n
Cl Cl -(CH2-CH-CH-CH2)n
H-H结构PVC
H2 -(CH2-C=C-CH2)n
-(CH2-CH-CH-CH2)n
H-H结构PS
(3) 链转移 ( Chain transfer) 在自由基聚合反应中,链自由基可能从单体、溶剂、 引发剂等低分子或大分子上夺取一个原子而终止,并使这 些失去原子的分子成为自由基,继续新链的增长,使聚合 反应继续下去,这一反应称链转移反应 可分为三种情况 a. 向单体的链转移
单体 转化率 聚合物
时间
(5) 少量阻聚剂(0.01-0.1%)足以使自由基聚合反应 终止
四、 链引发反应
1、引发剂和引发作用
(一)怎样的物质才能被选用作引发剂 分子结构上有弱键,易分解成自由基化合物
在聚合温度下(40-100º C),键离解能100-170KJ/mol,仅具有O-O, S-S,N-O键的一些化合物具备这一要求。 热分解型引发剂 引发剂类型 氧化还原型引发剂 低温游离基型引发剂:有机过氧化物和烷基金属 化物组合
第 三 章 自由基聚合2

3.自由基聚合反应 --连锁聚合反应概 3.自由基聚合反应 --连锁聚合反应概 述
根据引发活性种与链增长活性中心的不同, 根据引发活性种与链增长活性中心的不同, 引发活性种与链增长活性中心的不同 连锁聚合反应可分为自由基聚合 自由基聚合Free Radical、 连锁聚合反应可分为自由基聚合 阳离子聚合Cationic、阴离子聚合 阴离子聚合Anionic和 阳离子聚合 和 配位聚合Coordination Polymerization等。 配位聚合 等
(ii) X为吸电子基团 为吸电子基团electron withdrawing group 为吸电子基团
H2C CH X
降低电子云密度, 降低电子云密度, 易与富电性活性 种结合
R CH2
H C X
分散负电性, 分散负电性,稳定 活性中心
由于阴离子与自由基都是富电性electron rich的活性 由于阴离子与自由基都是富电性 的活性 种,因此带吸电子基团的烯类单体易进行阴离子聚合 与自由基聚合, 与自由基聚合,如X = -CN,-COOR,-NO2等; , , 但取代基吸电子性太强时一般只能进行阴离子聚合。 但取代基吸电子性太强时一般只能进行阴离子聚合。 如同时含两个强吸电子取代基的单体:CH2=C(CN)2 如同时含两个强吸电子取代基的单体: 等
R CH2 CH* + H2C CH X X
增长链
终止反应
CH2 CH* X 增长链
聚合物链
连锁聚合反应的基本特征 a. 聚合过程一般由多个基元反应组成; 聚合过程一般由多个基元反应组成; b. 各基元反应机理不同,反应速率和活化能差别 各基元反应机理不同, 大; c. 单体只能与活性中心反应生成新的活性中心, 单体只能与活性中心反应生成新的活性中心, 单体之间不能反应; 单体之间不能反应; d. 反应体系始终是由单体、聚合产物和微量引发 反应体系始终是由单体、 剂及含活性中心的增长链所组成; 剂及含活性中心的增长链所组成; e. 聚合产物的分子量一般不随单体转化率而变。 聚合产物的分子量一般不随单体转化率而变。 活性聚合除外)。 (活性聚合除外)。
第3章 自由基聚合

(2)偶氮类引发剂 带吸电子取代基的偶氮化合物,分对称和不对称两大类:
R
1
R2 R2 1 C N N C R X X 对称
R R2 R C N N C R1 X X 不对称
X为吸电子取代基:-NO2, -COOR, -COOH, -CN等
CH3 CH3 H3C C N N C CH3 CN CN 偶氮二异丁腈(AIBN) CH3 2 H3C C CN + N2
n = kp[M]/2(fktkd[I])1/2
动力学链长与平均聚合度的关系
无链转移反应时,每一条增长链都是由一个初级自由基引 发而成,因而ν=平均每条增长链所含的单体单元数: 当发生歧化终止时, 两条增长链生成两个聚合物分子,因而 聚合产物的 Xn = n; 当发生偶合终止时,两条增长链结合生成一个聚合物分子, 因而聚合产物的Xn = 2n 。
四、温度对聚合反应速率的影响 聚合反应速率常数与温度的关系遵守Arrhenius方程: k = Ae-E/RT Rp ∝ kp(kd/kt)1/2
表观聚合速率常数 k =kp(kd/kt)1/2 k = Ap(Ad/At)1/2exp{-[Ep - Et/2 + Ed/2]/RT} 式中:Ed 引发剂分解活化能;Ep 链增长活化能;Et 链终止 活化能; 总活化能 E= Ep -Et/2 + Ed/2 一般Ed = 126 kJ/mol, Ep =29 kJ/mol, Et = 17 kJ/mol,即 E = 84 kJ/mol, 聚合反应速率随温度升高而加快。
其中加入的能产生聚合反应活性中心的化合物常称为引发剂。 引发剂(或其一部分)在反应后成为所得聚合物分子的组成 部分。
(以乙烯基单体聚合为例)
分解 I 引发剂 R* + H2C CH X R CH2 CH* X 或离解 引发活性种(中心) R* 链增长活性中心
第三章 自由基聚合-2

3.4
自由基聚合反应动力学
当体系中存在阻聚剂时,引发剂开始分解后,并不能
马上引发单体聚合,必须在体系中的阻聚剂全部消耗完后
,聚合反应才会正常进行。即从引发剂开始分解到单体开 始转化存在一个时间间隔,称诱导期 (induction period, ti).
单体在贮存、运输过程中常加入阻聚剂以防止单体聚
3.4
自由基聚合反应动力学
曲线1—纯净单体聚合,无诱导期,聚合速率正常。
曲线2—典型的阻聚作用,存在诱导期,诱导期间聚合完 全停止。但诱导期过后,聚合速率正常(Rp与1相同)。
曲线3—典型的缓聚作用,无诱导期,不会使聚合反应停 止,但聚合速率降低。
曲线4—兼有阻聚作用与缓聚作用,既产生诱导期,诱导 期过后聚合速率又降低。 3.4.4.1 阻聚剂与阻聚机理
3.4
自由基聚合反应动力学
3.4.1.1 各基元反应速率方程 ( 1)链引发 M M· 链引发速率 Ri =d[M•]/dt (2)链增长 RM· k R MM· k R MMM· k p p p M ¨¨¨ RMi · k RMi+1 · (i=1→∞)
p
M
M
M
根据等活性假设,各步增长反应的速率常数相等。 链增长速率 Rp =kp[M] ∑[RMi•] = kp[M][M•] kp—链增长速率 常数 ( [M•]= ∑[RMi•] )
3.4
自 由 基 聚 合 反 应 动 力 学
3.4.1自由基聚合动力学方程 基本假设: (1)忽略链转移反应,终止方式为双基终止; (2)等活性理论:链自由基的活性与链长无关,即各步链 增长速率常数相等,用一个速率常数kp表示。 (3)聚合产物Xn 很大,链增长所消耗的单体远远大于链引 发反应,因此认为单体主要消耗于链增长反应,聚合总速率 可以用链增长速率表示 R = -d[M]/dt= Ri +Rp≈ Rp (4)稳态假设:反应开始很短一段时间后,链自由基的生 成速率等于其消失速率(Ri =Rt),即体系中自由基的浓度恒 定,进入“稳态”;
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CN
N2
BPO分解及其副反应更复杂。
C6H5COO OOCC6H5 C6H5COO 2 C6H5COO
+ C6H5 + CO2
2C6H5 + 2CO2 C6H5 C6H5
+
C6H5COOC6H5 + CO2
2CO2
引发剂效率随单体、溶剂和引发剂的特性、种类有不同 程度的变化。
3 自由基聚合 3.5 引发剂
消耗掉一分子引发剂,而自由基数目并没有增加。
3 自由基聚合 3.5 引发剂
19
3.5.4 引发剂效率
诱导分解的影响因素:
引发剂种类:AIBN无诱导分解,ROOH容易诱导分解; 引发剂浓度:浓度大易诱导分解;������ 单体的相对活性:丙烯腈(AN)、St等活性较高的单体,能 迅速与引发剂作用引发增长,引发效率高。VAc等低活性
引发剂的温度选用范围
温度范围/℃ 高温 >100 中温 40~100 Ed/kJmol-1 138~188 110~138 引发剂举例 异丙苯过氧化氢,特丁基过氧化氢,过氧化二异丙苯,过 氧化二特丁基 过氧化苯甲酰,过氧化十二酰,AIBN,过硫酸盐 氧化还原体系:过氧化氢-亚铁盐,过硫酸盐-NaHSO3,异 丙苯过氧化氢-亚铁盐,过氧化苯甲酰-二甲基苯胺
第3章
自由基聚合 主要内容
单体对不同连锁聚合机理的选择性;
自由基聚合反应机理及其特征; 主要热引发剂种类、引发机理和引发剂分解动力学; 自由基聚合反应动力学及影响自由基聚合反应速率和分子 量的因素;
掌握引发效率、稳态、自由基等活性理论、自动加速、
动力学链长、聚合度、链转移、阻聚及缓聚等基本概念。
常用的有机过氧化物引发剂有烷基过氧化氢(RC-OO-H)、二烷基过氧化物(R-O-O-R’)、过氧化酯 (RCOOOR’)、过氧化二酰(RCOOOCOR’)和过氧化二碳
酸酯(ROOC-O-O-COOR’)等。
3 自由基聚合 3.5 引发剂
8
(2)有机过氧类引发剂 过氧化物受热分解时,过氧键均裂生成两个自由基,如:
kd Ad e
Ed RT
lnkd lnAd Ed RT
3 自由基聚合 3.5 引发剂
16
工业上衡量引发剂活性的定量指标: 过氧化二碳酸二环己酯 60℃下t1/2:
t1/2< 1h:高活性引发剂,如DCPD (1h); 1h<t1/2< 6h:中活性引发剂,如BPPD (2.1h); t1/2> 6h:低活性引发剂,如AIBN (16h) 过氧化二碳酸二苯氧乙酯
高-低(中)活性引发剂复合使用
常温聚合一定时间后,提高聚合温度进行后聚合
3 自由基聚合 3.5 引发剂
25
3.5.5 引发剂的选择 选择引发剂时还须考虑的因素: 与体系中其他组分有无反应;������
是否易着色、有无毒性等;������
贮存、运输安全、使用方便、经济效益等。 引发剂用量的确定需经过大量的试验。
3 自由基聚合 3.5 引发剂
17
3.5.4 引发剂效率 引发剂分解后,只有一部分能够引发聚合,而另一部分
由于诱导分解和笼蔽效应伴随的副反应而消耗。
引发聚合的部分引发剂占引发剂分解或消耗总量的分数 称为引发剂效率 (f)。 引发剂分解速率 Rd=kd[I], 引发速率 Ri = 2fkd[I] 副反应:使引发剂效率下降。
O C O +
O C O
3 自由基聚合 3.5 引发剂
14
3.5.3 引发剂分解动力学
R O O R' R N N R' RO + R'O R + R' + N2
单分子一级反应
引发剂分解速率
d[I] Rd k d [I ] dt
注意kd的单位 s-1,min-1,h-1
t=0 时引发剂浓度为[I]0,上式积分得
CH3 CH3 H3C C N N C CH3 CN CN 偶氮二异丁腈 (AIBN) CH3 2 H3C C CN + N2
45~80℃
3 自由基聚合 3.5 引发剂
5
(1)偶氮类引发剂
在45~80℃使用,一级反应,无诱导分解,产生一种
自由基,分解产生氮气;稳定,存储安全;
因为氰基的共轭,甲基的超共轭,自由基稳定,无脱 氢能力,故不能作接枝聚合引发剂。
大多数引发剂可观察到这些现象,偶氮类引发剂易发生。
AIBN分解形成自由基后,可能偶合成稳定分子。
3 自由基聚合 3.5 引发剂
21
(CH3)2C C(CH3)2 +N2 (CH3)2CN NC(CH3)2 CN CN [2(CH3)2C
+
N2 ]
CN CN (CH3)2C C N C(CH3)2 CN
[I] ln kd t [I]0
3 自由基聚合 3.5 引发剂
15
3.5.3 引发剂分解动力学
引发剂半衰期( t1/2): 引发剂分解至起始浓度一半所需的时间
t1 2
[I]0 1 ln 2 0.693 ln kd [I]0 /2 kd kd
kd与温度有关,t1/2与温度有关,同一引发剂在不同温度 下有不同的t1/2。
低温 -10~40
极低温 < -30
63~110
<63
过氧化物-烷基金属(三乙基铝,三乙基硼,二乙基铅),氧烷基金属
3 自由基聚合 3.5 引发剂
24
3.5.5 引发剂的选择 为了控制聚合速率,使之均速反应,常采用高 - 低 ( 中 ) 活性引发剂复合使用的方法; 若体系具有还原性 ( 如 NaCNS 的水溶液聚合 ) 则不宜使 用过氧类引发剂。 工业上,通常:
的单体,对自由基的捕捉能力较弱,使引发效率降低。
3 自由基聚合 3.5 引发剂
20
3.5.4 引发剂效率 笼蔽效应(Cage Effect) 引发剂的浓度相对很低,处于单体或溶剂的笼子包围中。
引发剂分解产生的初级自由基,处于周围分子(如单体和溶剂
分子)的包围,像处在笼子中一样,形成稳定分子,使引发剂 效率降低。这一现象称之为笼蔽效应。
3 自由基聚是聚合动力学的主要研究内容。聚 合速率的研究目的:在理论上探明聚合机理,实际上为生 产控制提供依据。 定义:Rp——单位时间内单体消耗量或聚合物的生成量。
d[M] d[P] Rp dt dt
转化率(Conversion):参加反应的单体量占总单体量的百分比。
22
3.5.5 引发剂的选择 1. 由聚合方法选择引发剂类型。 本体、悬浮和溶液聚合选用偶氮类和过氧类油溶性引
发剂,乳液聚合和水溶液聚合则选用水溶性过硫酸盐引 发剂或氧化-还原引发剂。
2. 由聚合温度选择活化能或半衰期适当的引发剂,使自由
基形成速率和聚合速率适中。
3 自由基聚合 3.5 引发剂
23
3 自由基聚合 3.5 引发剂
18
3.5.4 引发剂效率
引发自由基的再结合: 以BPO为例
O Ph C O + Ph O Ph C O Ph 2 Ph Ph Ph
诱导分解 (induced decomposition) 自由基向引发剂的链转移反应。
O O Ph C O O C Ph + Ph O O Ph C O Ph + Ph C O
3 自由基聚合 3.5 引发剂
11
无机物/无机物氧化还原体系
HO OH + Fe
2+
水溶性
-
HO + OH + Fe3+
竞争反应 HO + H2O2 H O O + H2O2 HO + Fe
2+
H O O + H2O HO + H2O + O2 HO + Fe
3+
影响H2O2的效率和反应重现性,多被过硫酸盐体系代替。 属于双分子反应,1分子氧化剂只形成一个自由基; 若还原剂过量,则进一步与自由基反应,使活性消失。 故还原剂用量一般较氧化剂少 。
总的原则为:低活性用量多,高活性用量少,一般为
单体量的0.01%~0.1%。
3 自由基聚合 3.5 引发剂
26
3.7 聚 合 速 率
自由基聚合各基元反应对总聚合速率都有所贡献。链
转移反应一般不影响聚合速率,可暂不考虑。 从三个基元反应的动力学方程推导出发,依据等活性、 长链和稳态三个基本假设推导聚合反应总的动力学方程。 分析影响聚合反应速率的一些因素。
Δ[M] [M]0 [M] C 100% 即 [M] [M]0 (1 C ) [M]0 [M]0
33.7 自由基聚合 聚合速率
28
3.7.1 概述
d[M] dC Rp [M]0 dt dt
可用C ~ t 曲线表示聚合过程中速率的变化 通常呈S型。据此,
可将聚合过程分为:
3 自由基聚合 3.5 引发剂
12
无机物/无机物氧化还原体系 常用的是:过硫酸盐 + 低价盐
-
O3SOOSO3- + HSO3O3SOOSO3- + Fe
2+
SO42- + SO4- + HSO3 SO4 + SO4
2-
-
+ Fe
3+
有机物/无机物氧化还原体系:有机过氧化物 + 低价盐
R-O-O-R + Fe2+ R-O-O-H + Fe2+ R-O-O C R' + Fe O
O O C O O C 过氧化苯甲酰(BPO) O C O + CO2 2 O C O
