食品保藏学实验汇总
食物实验报告

一、实验目的1. 了解食物保鲜的基本原理和方法。
2. 探究不同保鲜方法对食物保鲜效果的影响。
3. 为家庭和餐饮业提供有效的食物保鲜建议。
二、实验原理食物保鲜是指通过各种方法减缓或抑制微生物的生长繁殖,降低食物的腐败速度,延长食物的保质期。
常见的食物保鲜方法有低温保存、真空包装、添加防腐剂等。
三、实验材料1. 食物:苹果、黄瓜、牛肉、面包等。
2. 保鲜方法:低温保存、真空包装、添加防腐剂。
3. 实验工具:冰箱、真空包装机、防腐剂、计时器等。
四、实验方法1. 低温保存:将食物放入冰箱中,分别记录不同温度下的保鲜效果。
2. 真空包装:将食物放入真空包装袋中,抽真空后封口,记录保鲜效果。
3. 添加防腐剂:将食物加入适量的防腐剂,记录保鲜效果。
五、实验步骤1. 低温保存实验(1)将苹果、黄瓜、牛肉、面包分别放入四个不同的保鲜盒中。
(2)将保鲜盒放入冰箱中,分别设定为0℃、5℃、10℃、15℃。
(3)每隔一天观察食物的变化,记录保鲜效果。
2. 真空包装实验(1)将苹果、黄瓜、牛肉、面包分别放入四个真空包装袋中。
(2)用真空包装机抽真空,封口。
(3)将真空包装袋放入冰箱中,记录保鲜效果。
3. 添加防腐剂实验(1)将苹果、黄瓜、牛肉、面包分别放入四个保鲜盒中。
(2)向每个保鲜盒中加入适量的防腐剂,搅拌均匀。
(3)将保鲜盒放入冰箱中,记录保鲜效果。
六、实验结果与分析1. 低温保存实验结果(1)0℃:食物保鲜效果较好,细菌生长缓慢。
(2)5℃:食物保鲜效果较好,细菌生长速度适中。
(3)10℃:食物保鲜效果一般,细菌生长速度较快。
(4)15℃:食物保鲜效果较差,细菌生长速度较快。
2. 真空包装实验结果(1)真空包装:食物保鲜效果较好,细菌生长缓慢。
3. 添加防腐剂实验结果(1)添加防腐剂:食物保鲜效果较好,细菌生长缓慢。
七、实验结论1. 低温保存是食物保鲜的有效方法,其中0℃和5℃的保鲜效果较好。
2. 真空包装也是食物保鲜的有效方法,可以减缓细菌生长。
食品贮藏与保鲜实验
实验一果蔬一般物理性状测定一、实验目的及意义物理性状的测定是用一些物理测定方法来表示果蔬的重量、大小、容重、硬度等物理性状。
其中也包含了某些感官的反映,色泽、新鲜度和成熟度等。
果实在成熟、采收、运输、贮藏及加工期间的物理特性的变化,反映其组织内部一系列复杂的生理生化变化的结果。
因此对物理性状的测定是进行化学测定的基础。
果蔬的物理性状测定是确定采收成熟度,识别品种特性,进行产品标准化的必要措施。
新鲜果实是活的有机体,与外界环境条件的统一是保证贮藏特性的主要因素。
欲控制适合于新鲜果蔬的环境,首先就要通过在贮藏期中进行物理性状的测定,是了解其加工适应性与拟定加工技术条件的依据。
二、实验原理1、硬度计使用方法在每个被测果实的中部取两个对称点两面薄薄地削去果皮,用果实压力硬度计,测定果肉的硬度。
(1) FT327(Fruit Tester 3-27Lbs)。
测定范围为3~27磅/(cm)2。
测定时,左手紧握果实,右手持硬度计于拇指和食指间,将测头慢慢压入果肉至测头槽凹处(进果线)后读数。
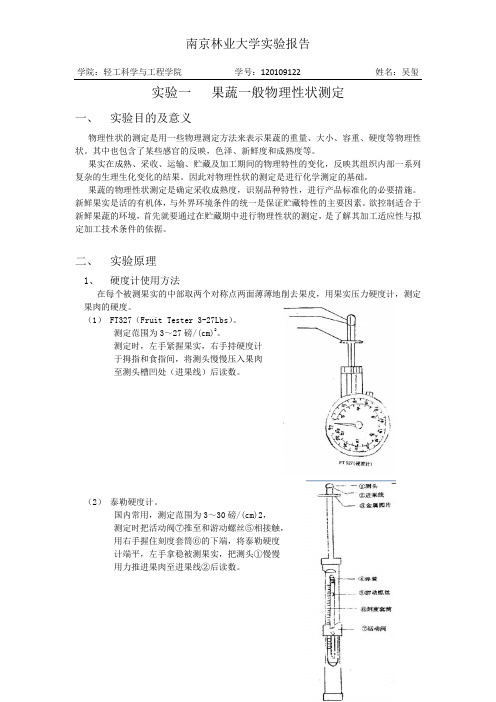
(2)泰勒硬度计。
国内常用,测定范围为3~30磅/(cm)2,测定时把活动阀⑦推至和游动螺丝⑤相接触,用右手握住刻度套筒⑥的下端,将泰勒硬度计端平,左手拿稳被测果实,把测头①慢慢用力推进果肉至进果线②后读数。
2、可溶性固形物测定(1)测定原理由于溶质是单一的,所以可由折射率直接换算出溶液浓度。
果蔬汁液成分复杂,故用手持糖量计测定的实是可溶性固形物的含量。
(2)手持糖量计的使用原理(3)手持糖量计使用方法a、调零。
使用时掀开照明棱镜盖板,用柔软的绒布仔细将折光棱镜拭净,取蒸馏水数滴,置于折光棱镜的镜面上,合上照明棱镜盖板,使蒸馏水遍布于折光棱镜的表面。
将仪器进光窗对向光源或明亮处,调节视度圈,使视野内分划刻度清晰可见,并观察视野中明暗分界线是否对准刻度0%,若有偏离,可旋动校正螺丝,使分界线指示于0%处。
最后把蒸馏水拭净,进行试样测定。
食品的保藏实验报告

食品的保藏实验报告实验目的本实验旨在探究不同保藏条件对食品保鲜的影响,分析各种保藏方法的优缺点,并为消费者提供合理的食品保藏建议。
实验材料和方法材料- 鸡蛋*10- 酸奶*2杯- 牛奶*2袋- 苹果*5个- 面包*1袋实验方法1. 将材料分为5组,每组材料数量相同。
2. 对比以下保藏条件:- 组A:常温下(25C)放置2天- 组B:冷藏(4C)放置2天- 组C:真空密封冷藏(4C)放置2天- 组D:冷冻(-18C)放置2天- 组E:真空密封冷冻(-18C)放置2天3. 每组保藏后的材料进行观察和记录。
实验结果鸡蛋- 组A:2天后,鸡蛋壳开始变黄,出现异味。
- 组B:2天后,鸡蛋壳的颜色和气味都没有变化。
- 组C:2天后,鸡蛋壳的颜色和气味都没有变化。
- 组D:2天后,鸡蛋壳出现裂纹,蛋黄变得稀薄。
- 组E:2天后,鸡蛋壳有些发霉,蛋黄变得稀薄。
酸奶- 组A:2天后,酸奶的颜色变得黯淡,出现分离现象。
- 组B:2天后,酸奶的颜色和质地都没有变化。
- 组C:2天后,酸奶的颜色和质地都没有变化,分离现象消失。
- 组D:2天后,酸奶的颜色变得黯淡,质地变得不均匀。
- 组E:2天后,酸奶的颜色变得黯淡,质地变得不均匀。
牛奶- 组A:2天后,牛奶的颜色变得黯淡,出现异味。
- 组B:2天后,牛奶的颜色和味道都没有变化。
- 组C:2天后,牛奶的颜色和味道都没有变化。
- 组D:2天后,牛奶的颜色变得黯淡,味道有些变化。
- 组E:2天后,牛奶的颜色变得黯淡,味道有些变化。
苹果- 组A:2天后,苹果的外皮开始出现皱纹,有些变得软。
- 组B:2天后,苹果的外皮变得稍微松散,但仍然硬。
- 组C:2天后,苹果的外皮变得稍微松散,但仍然硬。
- 组D:2天后,苹果的外皮变得非常松散,质地变得软。
- 组E:2天后,苹果的外皮变得非常松散,质地变得软。
面包- 组A:2天后,面包变得有些干硬,口感下降。
- 组B:2天后,面包的外表没有变化,但口感稍微松软。
热处理保藏实验报告

一、实验目的1. 了解热处理保藏的基本原理和方法;2. 掌握热处理保藏过程中的关键技术参数;3. 通过实验,验证热处理保藏的效果,为食品保藏提供理论依据。
二、实验原理热处理保藏是一种利用高温对食品进行杀菌、灭酶、降低食品中的微生物数量,从而延长食品保质期的方法。
热处理保藏主要包括巴氏杀菌、高温杀菌和超高温杀菌等。
三、实验材料1. 原料:鲜牛奶、鲜猪肉、鲜鸡肉;2. 仪器设备:电热恒温培养箱、高压蒸汽灭菌器、电子天平、温度计、计时器等;3. 药品:氯化钠、柠檬酸、磷酸氢二钠、磷酸二氢钠等。
四、实验方法1. 巴氏杀菌实验(1)将鲜牛奶在60℃下保温30分钟,然后降至室温;(2)将鲜牛奶在75℃下保温15分钟,然后降至室温;(3)将鲜牛奶在90℃下保温10分钟,然后降至室温;(4)将鲜牛奶在95℃下保温5分钟,然后降至室温;(5)将鲜牛奶在100℃下保温2分钟,然后降至室温;(6)对杀菌后的鲜牛奶进行微生物检测,比较不同杀菌温度对微生物数量的影响。
2. 高温杀菌实验(1)将鲜猪肉、鲜鸡肉分别切成小块;(2)将猪肉和鸡肉放入高压蒸汽灭菌器中,分别设置不同压力和时间进行杀菌;(3)将杀菌后的猪肉和鸡肉进行微生物检测,比较不同杀菌压力和时间对微生物数量的影响。
3. 超高温杀菌实验(1)将鲜牛奶、鲜猪肉、鲜鸡肉分别进行超高温杀菌;(2)将杀菌后的食品进行微生物检测,比较不同杀菌温度对微生物数量的影响。
五、实验结果与分析1. 巴氏杀菌实验从实验结果可以看出,随着杀菌温度的升高,微生物数量逐渐减少。
在60℃下保温30分钟,微生物数量减少了约80%;在75℃下保温15分钟,微生物数量减少了约90%;在90℃下保温10分钟,微生物数量减少了约95%;在95℃下保温5分钟,微生物数量减少了约98%;在100℃下保温2分钟,微生物数量减少了约99%。
由此可见,巴氏杀菌效果随温度升高而增强。
2. 高温杀菌实验从实验结果可以看出,随着杀菌压力和时间增加,微生物数量逐渐减少。
冻藏实验报告

一、实验目的1. 探究不同冻藏条件下食品品质的变化;2. 评估不同冻藏方法对食品品质的影响;3. 为食品冻藏提供科学依据。
二、实验材料与仪器1. 实验材料:新鲜蔬菜、肉类、鱼类等;2. 仪器:冰箱、电子秤、温度计、食品品质检测仪器等。
三、实验方法1. 实验分组:将实验材料分为四组,分别采用不同的冻藏方法: A组:常温冻藏(0℃-5℃)B组:低温冻藏(-18℃)C组:快速冻藏(-40℃)D组:普通冻藏(-20℃)2. 实验过程:(1)将新鲜蔬菜、肉类、鱼类等分别称重,记录初始质量;(2)按照不同冻藏方法进行冻藏,记录冻藏时间;(3)冻藏结束后,取出实验材料,进行感官评价和品质检测。
3. 感官评价:(1)观察实验材料的外观、颜色、质地等;(2)品尝实验材料的口感、味道等;(3)记录感官评价结果。
4. 品质检测:(1)测定实验材料的物理指标,如水分含量、蛋白质含量等;(2)测定实验材料的微生物指标,如菌落总数、大肠菌群等;(3)记录品质检测结果。
四、实验结果与分析1. 感官评价结果:A组:外观、颜色、质地较好,口感、味道一般;B组:外观、颜色、质地较好,口感、味道较好;C组:外观、颜色、质地较好,口感、味道较好;D组:外观、颜色、质地较好,口感、味道一般。
2. 品质检测结果:A组:水分含量较高,蛋白质含量较低,菌落总数较高,大肠菌群较多;B组:水分含量较高,蛋白质含量较高,菌落总数较低,大肠菌群较少;C组:水分含量较高,蛋白质含量较高,菌落总数较低,大肠菌群较少;D组:水分含量较高,蛋白质含量较低,菌落总数较高,大肠菌群较多。
3. 结果分析:(1)低温冻藏(B、C组)相较于常温冻藏(A组)和普通冻藏(D组),食品品质较好,水分含量和蛋白质含量较高,菌落总数和大肠菌群较少;(2)快速冻藏(C组)相较于低温冻藏(B组),食品品质略好,但差异不大;(3)常温冻藏(A组)和普通冻藏(D组)的食品品质较差,水分含量和蛋白质含量较低,菌落总数和大肠菌群较多。
食品贮运学实验报告

一、实验目的1. 了解食品贮运的基本原理和操作方法。
2. 掌握食品贮运过程中的质量控制要点。
3. 培养实验操作技能,提高对食品贮运学知识的实际应用能力。
二、实验原理食品贮运学是研究食品在储存、运输、销售过程中保持品质、延长货架期的一门学科。
本实验旨在通过实际操作,了解食品贮运过程中的关键技术,如温度控制、湿度控制、气体控制等,以及如何通过合理的包装和运输方式来延长食品的保质期。
三、实验材料与设备1. 实验材料:苹果、梨、黄瓜、猪肉、大米、面粉等。
2. 实验设备:冰箱、冷库、温度计、湿度计、包装材料、运输工具等。
四、实验步骤1. 温度控制实验(1)将苹果、梨、黄瓜、猪肉、大米、面粉等食品分别放入冰箱和冷库中,设置不同的温度(如0℃、5℃、10℃、15℃等)。
(2)观察并记录食品在不同温度下的保质期变化。
2. 湿度控制实验(1)将苹果、梨、黄瓜、猪肉、大米、面粉等食品分别放入不同湿度的环境中,如干燥、潮湿、常湿等。
(2)观察并记录食品在不同湿度下的保质期变化。
3. 气体控制实验(1)将苹果、梨、黄瓜、猪肉、大米、面粉等食品分别放入充满氮气、二氧化碳、氧气的环境中。
(2)观察并记录食品在不同气体环境下的保质期变化。
4. 包装实验(1)将食品分别用不同材质的包装材料进行包装,如塑料袋、纸箱、玻璃瓶等。
(2)观察并记录食品在不同包装材料下的保质期变化。
5. 运输实验(1)将食品分别用不同运输工具进行运输,如汽车、火车、飞机等。
(2)观察并记录食品在不同运输工具下的保质期变化。
五、实验结果与分析1. 温度控制实验实验结果显示,食品在低温环境下保质期较长,而在高温环境下保质期较短。
如苹果在0℃环境下保质期为30天,而在15℃环境下保质期仅为7天。
2. 湿度控制实验实验结果显示,食品在干燥环境下保质期较长,而在潮湿环境下保质期较短。
如大米在干燥环境下保质期为6个月,而在潮湿环境下保质期仅为3个月。
3. 气体控制实验实验结果显示,食品在氮气环境下保质期较长,而在氧气环境下保质期较短。
食品冻藏实验报告

食品冻藏实验报告实验目的本次实验旨在研究不同温度下食品的冻藏效果,为食品储存和保鲜提供科学依据。
具体目标如下:1. 比较不同温度对食品的冻藏效果;2. 分析食品在冻藏过程中的变化。
实验器材与试剂- 冰箱- 温度计- 试验样品:苹果、肉类、蔬菜等实验方法1. 准备不同种类的食品样品;2. 将样品放入冰箱中,设置不同的冻藏温度:- 温度A:-18;- 温度B:-10;- 温度C:-5。
3. 定期观察和记录各温度下食品的变化情况,包括其外观、口感、营养成分等。
实验结果与分析温度A:-18- 苹果:在-18的温度下,苹果的外观呈现冻结状态,果肉松软度较高,口感相对较差。
但由于较低的温度能有效抑制细菌和酵母菌的繁殖,苹果的保鲜期较长,并且保留了大部分营养成分。
- 肉类:肉类在-18的温度下很快被冻结,其外观和口感变硬,但由于因冰晶形成对细胞的破坏,会导致肉质变得稍显粗糙。
然而,低温能够有效延缓细菌和酵母菌的生长速度,从而延长肉类的保鲜期。
- 蔬菜:在-18下,蔬菜的水分会以冰晶形式结冻,导致其口感变软。
尽管会出现一定的失水现象,但蔬菜的色泽和维生素成分得以保留,保持较好的食用价值。
温度B:-10- 苹果:在-10的温度下,苹果仍有部分冻结,果肉较硬,口感会略有改善。
然而,由于冻结程度不够彻底,食品的保鲜期相对较短,不宜过多存放时间。
- 肉类:肉类在-10的温度下冻结较慢,所以部分组织仍然保持着较好的口感。
然而,这种温度下细菌的生长速度仍然较快,因此肉类的保鲜期相对较短。
- 蔬菜:在-10下,蔬菜的水分结冻程度较轻,因此其口感仍然较硬。
但由于较低的温度会影响维生素C的含量,蔬菜的营养价值相对较低。
温度C:-5- 苹果:在-5的温度下,苹果的冻结程度较轻,果肉较为脆嫩,口感较好。
然而,由于温度不够低,细菌和酵母仍然能够生长,使得苹果的保鲜期相对较短。
- 肉类:肉类在-5的温度下无法完全冻结,因此肉质较为柔软,口感较好。
食品保鲜技术实验报告

实验一果蔬呼吸强度的测定【实验目的和原理】呼吸作用是农产品收获后进行的重要的生理活动,呼吸强度代表农产品生命活动和品种的耐藏性能,当农产品收获后进行呼吸代谢时,消耗糖、酸、呼吸氧,放出二氧化碳。
反应如下:C6H12O6 + 6O2 6O2 + 6H2O + 674千卡热量。
呼吸强度可以单位时间内单位重量的样品吸收O2或放出CO2的量来衡量。
呼吸强度的测定通常是采用定量碱液吸收农产品在一定时间内呼吸所释放出来的CO2,再用酸滴定剩余的碱,即可计算出呼吸所释放出来的CO2量,求出其呼吸强度。
单位通常用每公斤每小时释放CO2毫克数(CO2mg/kg·h)表示。
本次实验所用碱为NaOH,酸为HCL,反应如下:2NaOH + CO2 Na2CO3+ H2ONa2CO3+ BaCL2BaCO3+2NaCLNaOH + HCI NaCl + H2O【仪器和用品】果蔬样品、0.4NHCL、饱和BaCL2、0.1NaOH、酚酞溶液、7%KOH溶液、7%NaOH溶液、正丁醇玻璃真空干燥器、大气采样器等。
【实验步骤】1、按照图连接好大气采样器,用少量凡士林密封呼吸室,检查气密性。
启动大气采样器,调节气体流量,装有7%NaOH溶液和7%KOH溶液的净化瓶中不断有气泡产生,则说明整个系统气密性良好,否则应检查各接口是否漏气。
2.空白测定确保装置气密性后开始空白值的测定。
先将呼吸室与安全瓶连接,拨动开关,调节空气流量,将定时旋钮反时钟方向旋转时,先使呼吸室抽空平衡20min~30min,然后连接吸收瓶(内装有25mL0.1NNaOH溶液和一滴正丁醇)开始测定。
吸收30min后,将洗出液无损移入250mL洗瓶,用蒸馏水少量多次洗涤吸收瓶,洗出液移入同一三角瓶。
加5mL饱和BaCI2溶液和一滴酚酞溶液,用0.4NHCI 滴定至终点,记录数据。
3、样品测定样品称重后装入呼吸室,先使呼吸室抽空平衡20~30min (与空白相同), 然后连接吸收瓶开始测定。
食品储藏保鲜实验报告

一、实验目的本实验旨在探究不同储藏方式对食品保鲜效果的影响,分析不同温度、湿度、包装方法等因素对食品品质的保持作用,为食品储藏保鲜提供理论依据和实践指导。
二、实验材料与设备1. 实验材料:- 新鲜蔬菜(如黄瓜、西红柿、菠菜等)- 新鲜水果(如苹果、橙子、草莓等)- 熟食(如肉类、海鲜等)- 空气包装袋- 保鲜膜- 冷藏柜- 冷冻柜- 温湿度计- 计时器2. 实验设备:- 电子天平- 色差仪- 水分测定仪- 显微镜三、实验方法1. 实验分组:- A组:常温储藏- B组:冷藏储藏(0-4℃)- C组:冷冻储藏(-18℃以下)- D组:真空包装储藏- E组:保鲜膜包装储藏2. 实验步骤:(1)将新鲜蔬菜、水果、熟食分别按照实验分组进行预处理,包括清洗、切割等。
(2)将预处理好的食品分别放入对应的储藏方式中,如A组放入常温环境,B组放入冷藏柜,C组放入冷冻柜,D组使用真空包装袋包装后储藏,E组使用保鲜膜包装后储藏。
(3)每隔一定时间(如3天、7天、14天等)对各组食品进行品质检测,包括外观、口感、水分、营养成分等指标。
(4)记录实验数据,并进行统计分析。
四、实验结果与分析1. 外观变化:- A组食品在常温下储藏,易出现霉变、腐烂等现象,外观品质下降明显。
- B组食品在冷藏条件下储藏,外观品质较好,但部分蔬菜出现轻微失水现象。
- C组食品在冷冻条件下储藏,外观品质保持良好,但部分水果出现冻伤现象。
- D组食品在真空包装条件下储藏,外观品质保持良好,无霉变、腐烂等现象。
- E组食品在保鲜膜包装条件下储藏,外观品质较好,但部分蔬菜出现轻微失水现象。
2. 口感变化:- A组食品口感较差,易出现霉味、异味等现象。
- B组食品口感较好,但部分蔬菜口感略差。
- C组食品口感较好,但部分水果口感略差。
- D组食品口感保持良好,无异味、霉味等现象。
- E组食品口感较好,但部分蔬菜口感略差。
3. 水分变化:- A组食品水分流失明显,水分含量降低。
食品保鲜试验设计实验报告

食品保鲜试验设计实验报告1. 实验目的本实验旨在探究不同保鲜方式对食品保质期的影响,以寻找最佳的保鲜方式。
2. 实验材料和设备- 鸡蛋- 新鲜牛奶- 面包- 空气密封袋- 保鲜膜- 冰箱- 实验室温度计3. 实验步骤3.1 实验组设置1. 将鸡蛋分成三组,每组十个。
2. 第一组的鸡蛋放置在常温环境下,作为对照组。
3. 第二组的鸡蛋放入保鲜膜包裹后放置在常温环境下。
4. 第三组的鸡蛋放入空气密封袋后放入冰箱内。
3.2 记录观察数据1. 开始实验后,每天记录每组鸡蛋的状态,包括硬度、外观、气味等因素。
2. 每天检查一次各组鸡蛋的变化,并记录数据。
3.3 实验周期与观察时间在实验开始后的连续两周内,每天记录一次数据。
4. 实验数据日期对照组(常温)保鲜膜组(常温)空气密封袋组(冰箱):: :: :: ::Day 1 硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 2 硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 3 硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 4 硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 5 硬度:变软外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 6 硬度:变软外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:正常外观:正常气味:正常Day 7 硬度:变软外观:正常气味:正常硬度:正常外观:正常气味:正常硬度:稍软外观:正常气味:正常Day 8 硬度:变软外观:正常气味:正常硬度:稍软外观:正常气味:正常硬度:稍软外观:正常气味:正常Day 9 硬度:变软外观:正常气味:正常硬度:稍软外观:正常气味:正常硬度:稍软外观:正常气味:正常Day 10 硬度:变软外观:正常气味:正常硬度:稍软外观:正常气味:正常硬度:软外观:正常气味:正常Day 11 硬度:变软外观:正常气味:正常硬度:软外观:正常气味:正常硬度:软外观:正常气味:正常Day 12 硬度:变软外观:正常气味:正常硬度:软外观:正常气味:正常硬度:软外观:正常气味:正常Day 13 硬度:变软外观:正常气味:正常硬度:软外观:正常气味:正常硬度:软外观:正常气味:正常Day 14 硬度:变软外观:正常气味:正常硬度:软外观:正常气味:正常硬度:变软外观:正常气味:正常5. 结果分析凭借实验数据,可以得出以下结论:- 对照组的鸡蛋在两周内出现了明显的软化现象,表明鸡蛋的保质期受到了环境条件的影响。
食品冻藏实验报告

一、实验目的1. 探究不同冻藏条件下食品质量的变化。
2. 分析食品冻藏过程中冰晶生长对食品品质的影响。
3. 评估不同冻藏方法对食品品质的保持效果。
二、实验材料1. 实验食品:新鲜蔬菜(如胡萝卜、黄瓜)、水果(如苹果、香蕉)、肉类(如猪肉、鸡肉)。
2. 冻藏设备:家用冰箱、冻藏箱。
3. 测量工具:电子秤、温度计、计时器。
4. 其他材料:食品包装袋、标签纸、记录表。
三、实验方法1. 食品准备:将新鲜蔬菜、水果和肉类分别清洗干净,并切成相同大小和形状的样本。
2. 分组:将样本分为若干组,每组样本数量相同。
3. 冻藏处理:- A组:常温放置(不进行冻藏)。
- B组:低温冻藏(-18℃,24小时)。
- C组:快速冻藏(-35℃,30分钟)。
- D组:超速冻藏(-60℃,10分钟)。
4. 冻藏后处理:- 分别将各组样本从冻藏设备中取出,恢复至室温。
- 观察并记录样本的外观、质地、色泽和口感变化。
- 测量样本的重量变化。
- 使用电子秤测量样本的冰晶大小。
四、实验结果与分析1. 外观变化:- A组样本外观无明显变化。
- B组样本出现轻微冻伤,色泽略暗。
- C组样本外观完好,色泽接近新鲜。
- D组样本外观完好,色泽最佳。
2. 质地变化:- A组样本质地略软,口感较差。
- B组样本质地较硬,口感较差。
- C组样本质地适中,口感较好。
- D组样本质地最佳,口感最佳。
3. 色泽变化:- A组样本色泽无明显变化。
- B组样本色泽略暗。
- C组样本色泽接近新鲜。
- D组样本色泽最佳。
4. 口感变化:- A组样本口感较差。
- B组样本口感较差。
- C组样本口感较好。
- D组样本口感最佳。
5. 重量变化:- A组样本重量无明显变化。
- B组样本重量略有下降。
- C组样本重量略有下降。
- D组样本重量略有下降。
6. 冰晶大小:- A组样本无冰晶形成。
- B组样本冰晶较大。
- C组样本冰晶较小。
- D组样本冰晶最小。
五、实验结论1. 快速冻藏和超速冻藏可以有效保持食品的品质,降低冰晶生长对食品的影响。
食品保存探究实验报告

食品保存探究实验报告实验目的本实验旨在探究不同保存方法对食品新鲜度的影响,为人们正确选择食品保存方法提供科学依据。
实验材料- 鸡蛋- 青椒- 纸巾- 温度计- 显微镜- 计时器- 保鲜袋- 冰箱- 室温环境实验步骤1. 鸡蛋保存实验:- 实验1:将鸡蛋分别放入保鲜袋、冰箱和常温环境中,观察并记录鸡蛋在不同环境下的变化。
- 实验2:用显微镜观察不同保存环境下鸡蛋的蛋壳微观结构。
- 实验3:使用温度计测量不同保存环境下鸡蛋的温度变化。
2. 青椒保存实验:- 实验1:将青椒分别放入保鲜袋、冰箱和常温环境中,观察并记录青椒在不同环境下的变化。
- 实验2:用显微镜观察不同保存环境下青椒表面的微观结构。
- 实验3:使用计时器记录青椒在不同环境下出现腐烂的时间。
实验结果鸡蛋保存实验结果- 实验1观察到,放在保鲜袋内的鸡蛋保存时间较长,呈现良好的新鲜度;放在冰箱内的鸡蛋保存时间稍短,但仍然保持较好的新鲜度;放在常温环境下的鸡蛋很快出现变质。
- 实验2观察到,在显微镜下,放在保鲜袋内的鸡蛋蛋壳微观结构完整,放在冰箱内的鸡蛋蛋壳微观结构略有变化,放在常温环境下的鸡蛋蛋壳微观结构变化明显。
- 实验3测量到,放在保鲜袋内的鸡蛋平均温度为10C,放在冰箱内的鸡蛋平均温度为4C,放在常温环境下的鸡蛋平均温度为25C。
青椒保存实验结果- 实验1观察到,放在保鲜袋内的青椒保存时间较长,外观无明显变化;放在冰箱内的青椒保存时间稍短,但外观仍然保持良好;放在常温环境下的青椒很快变软并出现腐烂。
- 实验2观察到,在显微镜下,放在保鲜袋内的青椒表面微观结构完整,放在冰箱内的青椒表面微观结构略有变化,放在常温环境下的青椒表面微观结构变化明显。
- 实验3记录到,在常温环境下的青椒平均腐烂时间为3天,放在冰箱内的青椒平均腐烂时间延长至7天,放在保鲜袋内的青椒保持良好的新鲜度直到实验结束。
实验分析通过本次实验的结果分析,可以得出以下结论:1. 保鲜袋是一种较好的食品保存方式,可以有效延缓食品变质的速度。
食品安全保藏学实验心得

食品安全保藏学实验心得食品安全保藏学实验心得1今年以来,__镇人民政府按照《__市食品安全委员会办公室关于进一步加强农村食品安全治理工作的通知》(武食安办[__年]2号)和《关于__年__市治理“餐桌污染”建设“食品放心工程”实施方案的通知》(__办[__年85]号)要求,在市食安办的安排部署和各成员单位的共同努力下,与时俱进,从食品安全专项整治、食品抽检、风险监测、食品违法案件办理、食品安全宣传、监督检查等方面,结合我镇实际,总结汇报如下:一、食品安全专项整治工作根据《__市食品安全委关于开进一步加强农村食品安全治理工作的通知》,__镇迅速开展专项整治行动:我镇主要以个体经营和墟市经营,本次专项整治工作以粮、油、肉、水产品、蔬菜等“菜篮子”食用农产品为重点检查对象,截至__年10月28日,我镇共出动执法车1辆次,出动执法人员4人次,检查食用农产品经营户2户次,检查墟市食用农产品摊点8户次,开展快速检测22批次。
积极开展农村食品安全“扫雷”专项行动,截至__年11月7日,我镇会同各相关部门共出动执法人员106人次,检查各类食品经营主体225户次,其中校园周边食品经营户31户次;检查食品生产企业40户次,其中食品加工小作坊6户次;检查餐饮服务单位63户次,其中学校食堂9户次;开展食品快速检测90批次,检测合格率为100%。
2、为确保__年元旦食品安全,保护消费者和经营者合法权益,根据《南平市食品药品监督管理局关于加强__年元旦春节期间流通环节食品监管工作的通知》(南食药监食流〔__〕253号)文件精神,我镇积极开展专项执法检查行动。
共出动执法人员9人次,检查各类食品经营主体97户次,开展食品快速检测12批次,检测合格率为100%。
3、根据南平市食品药品监督管理局《关于加强“五一”及汛期食品药品安全监管工作的通知》的工作要求,我镇积极开展食品保障工作,努力营造让群众放心的食品安全氛围,切实维护消费者合法权益。
食品保藏实验总结

食品保藏实验总结引言食品保藏是指为了延长食品的保质期和保持食品的质量,采取一系列的措施来保护食品。
在食品加工和储存过程中,食品会面临微生物污染、氧化变质、异味传递等问题,因此,采取合适的保藏措施对于保持食品的安全和品质至关重要。
本文将总结一系列针对不同类型食品进行的保藏实验。
实验一:冷藏储存对乳制品的影响实验目的探究冷藏储存对乳制品的保质期和质量的影响。
实验步骤1.选取三种不同类型的乳制品:牛奶、酸奶和奶酪。
2.将每种乳制品分为两组,一组进行冷藏储存,另一组不进行储存。
3.每隔两天,对储存样品和对照样品进行外观检查、pH值测定和微生物总数检测。
实验结果经过一周的实验观察,我们得到了以下结果:•冷藏储存的牛奶保质期较长,外观无明显变化,pH值基本稳定,微生物总数较低。
•酸奶在冷藏储存后,质地有所改变,pH值有轻微上升,微生物总数有所增加。
•奶酪在冷藏储存后,外观无明显变化,pH值有轻微下降,微生物总数有所增加。
结论冷藏储存可以显著延长牛奶的保质期,对于酸奶和奶酪的保藏效果相对较弱。
因此,在乳制品保藏过程中,冷藏储存是一种较好的保藏方法。
实验二:真空包装对鲜肉保鲜的影响实验目的探究真空包装对鲜肉保鲜的效果。
实验步骤1.将新鲜鸡胸肉分为两组,一组进行真空包装,另一组不进行包装。
2.每隔两天,对包装和未包装样品进行外观检查、pH值测定和微生物总数检测。
实验结果经过一周的实验观察,我们得到了以下结果:•真空包装的鸡胸肉外观保持较好,颜色鲜亮,无污染和异味。
•未包装的鸡胸肉表面容易失水,颜色较暗,微生物总数较高。
结论真空包装能有效地保持鲜肉的外观和质量,延长其保鲜期。
因此,在鲜肉保藏过程中,真空包装是一种有效的保藏方式。
实验三:盐腌对蔬菜保藏的影响实验目的研究盐腌对蔬菜保藏的效果。
实验步骤1.选择新鲜胡萝卜和黄瓜,将其分为两组,一组进行盐腌处理,另一组不进行处理。
2.每隔三天,对处理和未处理样品进行外观检查、pH值测定和微生物总数检测。
食品保鲜技术实验报告

实验一果蔬呼吸强度的测定【实验目的和原理】呼吸作用是农产品收获后进行的重要的生理活动,呼吸强度代表农产品生命活动和品种的耐藏性能,当农产品收获后进行呼吸代谢时,消耗糖、酸、呼吸氧,放出二氧化碳。
反应如下:C6H12O6 + 6O2 6O2 + 6H2O + 674千卡热量。
呼吸强度可以单位时间内单位重量的样品吸收O2或放出CO2的量来衡量。
呼吸强度的测定通常是采用定量碱液吸收农产品在一定时间内呼吸所释放出来的CO2,再用酸滴定剩余的碱,即可计算出呼吸所释放出来的CO2量,求出其呼吸强度。
单位通常用每公斤每小时释放CO2毫克数(CO2mg/kg·h)表示。
本次实验所用碱为NaOH,酸为HCL,反应如下:2NaOH + CO2 Na2CO3+ H2ONa2CO3+ BaCL2BaCO3+2NaCLNaOH + HCI NaCl + H2O【仪器和用品】果蔬样品、0.4NHCL、饱和BaCL2、0.1NaOH、酚酞溶液、7%KOH溶液、7%NaOH溶液、正丁醇玻璃真空干燥器、大气采样器等。
【实验步骤】1、按照图连接好大气采样器,用少量凡士林密封呼吸室,检查气密性。
启动大气采样器,调节气体流量,装有7%NaOH溶液和7%KOH溶液的净化瓶中不断有气泡产生,则说明整个系统气密性良好,否则应检查各接口是否漏气。
2.空白测定确保装置气密性后开始空白值的测定。
先将呼吸室与安全瓶连接,拨动开关,调节空气流量,将定时旋钮反时钟方向旋转时,先使呼吸室抽空平衡20min~30min,然后连接吸收瓶(内装有25mL0.1NNaOH溶液和一滴正丁醇)开始测定。
吸收30min后,将洗出液无损移入250mL洗瓶,用蒸馏水少量多次洗涤吸收瓶,洗出液移入同一三角瓶。
加5mL饱和BaCI2溶液和一滴酚酞溶液,用0.4NHCI 滴定至终点,记录数据。
3、样品测定样品称重后装入呼吸室,先使呼吸室抽空平衡20~30min (与空白相同), 然后连接吸收瓶开始测定。
食品保藏技术实验报告心得

食品保藏技术实验报告心得一、实验介绍本次实验旨在探索常见食品的保藏技术,通过学习和实践掌握不同的食品保藏方法,以延长食物的保鲜期和保持其营养价值。
实验内容包括常见食材的冷藏、冷冻、真空包装等保藏方式。
二、实验过程1. 冷藏保藏在实验中,我们将常见的食材如牛奶、新鲜蔬菜、水果等放置在冰箱中冷藏,观察并记录其保鲜效果。
2. 冷冻保藏将一部分食物放入冷冻室进行冷冻保藏,比如鸡胸肉、切片面包等。
同时,我们在记录了食材的保藏前后体积、颜色、质地等变化。
3. 真空包装利用真空包装机将剩下的一部分食物进行真空包装,如饼干、虾仁等。
在包装前后比较这些食物的保鲜程度。
三、实验结果1. 冷藏保藏通过冷藏保藏,我们发现牛奶的保鲜效果非常好,没有出现变质的情况。
而新鲜蔬菜和水果在冷藏后质地变软,颜色也稍有改变,但整体保鲜效果较好。
2. 冷冻保藏经过冷冻保藏,鸡胸肉的质地变得更硬,但仍然保存得较好。
而切片面包在解冻后质地有所改变,口感较差。
这可能是因为冷冻导致面包内部水分结冰,影响了其质地。
3. 真空包装真空包装后的食物保鲜效果最好。
饼干依然保持了脆脆的口感,虾仁也没有出现变质的情况。
与冷冻方式相比,真空包装能更好地保持食物的原始质地和口感。
四、心得体会通过本次实验,我对食品保藏技术有了一定的了解。
冷藏是最常见的保藏方式,能够延长食物的保鲜期,但需要注意对蔬菜和水果等容易被冷藏影响质地的食物进行适当处理。
冷冻是一种较为激进的保藏方式,适用于一些肉类和糕点等食物,但在解冻过程中要注意保持食物的质量。
真空包装则是一种非常有效的保鲜方法,能够保持食物原本的口感和质地。
在实验中,我也发现不同食材对不同保藏方式的适应性不同。
因此,在实际生活中,我们需要根据食材的特性选择合适的保藏方法。
同时,合理控制食物的保藏时间也很重要,过长的保藏可能影响食物的营养价值。
总之,食品保藏技术对于现代生活至关重要。
通过学习和应用食品保藏技术,我们能够更好地保持食物的新鲜度和质量,减少食材的浪费,同时也能够更好地享受美食。
鸡蛋的保藏实验报告

一、实验目的1. 探究不同条件下鸡蛋的保鲜效果。
2. 了解影响鸡蛋保鲜的因素。
3. 学习并掌握鸡蛋保鲜的方法。
二、实验材料1. 新鲜鸡蛋:10个2. 鸡蛋箱:1个3. 冰箱:1台4. 温度计:1个5. 计时器:1个6. 纸张:若干7. 笔:1支三、实验方法1. 将10个新鲜鸡蛋随机分成三组,每组3个。
2. 第一组鸡蛋(A组)置于室温下(约25℃)保存。
3. 第二组鸡蛋(B组)放入冰箱冷藏层(约4℃)保存。
4. 第三组鸡蛋(C组)放入冰箱冷冻层(约-18℃)保存。
5. 每隔一天记录鸡蛋的保存情况,包括外观、气味、蛋黄、蛋白等。
6. 在实验过程中,观察并记录鸡蛋的变化,分析保鲜效果。
四、实验步骤1. 实验开始前,将10个鸡蛋编号,以便区分。
2. 将A组鸡蛋放入鸡蛋箱中,置于室温下保存。
3. 将B组鸡蛋放入冰箱冷藏层保存。
4. 将C组鸡蛋放入冰箱冷冻层保存。
5. 每天观察鸡蛋的变化,记录如下信息:- 外观:鸡蛋壳是否有裂痕、破损等。
- 气味:鸡蛋是否有异味。
- 蛋黄:蛋黄是否上浮、变形等。
- 蛋白:蛋白是否变稀、发黄等。
6. 持续观察记录,直至鸡蛋变质。
五、实验结果与分析1. 实验开始后,A组鸡蛋在室温下保存,第三天出现异味,第五天蛋黄上浮,第七天蛋白变稀,第九天鸡蛋变质。
2. B组鸡蛋在冰箱冷藏层保存,第五天出现异味,第七天蛋黄上浮,第九天蛋白变稀,第十二天鸡蛋变质。
3. C组鸡蛋在冰箱冷冻层保存,第五天出现异味,第七天蛋黄上浮,第九天蛋白变稀,第十三天鸡蛋变质。
六、实验结论1. 鸡蛋在室温下保存容易变质,建议在冰箱中保存。
2. 冷藏层和冷冻层对鸡蛋的保鲜效果有一定影响,冷藏层比室温保存时间更长,但冷冻层效果最佳。
3. 在保存鸡蛋时,注意观察鸡蛋的变化,及时处理变质鸡蛋。
七、实验总结本次实验通过对鸡蛋在不同条件下保存效果的探究,发现冰箱冷藏层和冷冻层对鸡蛋的保鲜效果较好。
在日常生活中,我们应该注意鸡蛋的保存方法,以保证食品安全和营养。
食品加工与保藏原理实验

食品加工与保藏原理实验实验一食品的腌渍保藏(一)、实验目的和要求1.了解食品在腌渍条件下的保藏期,验证腌渍保藏效果;2.熟悉常规腌渍保藏操作;3.掌握常规腌渍保藏条件;4理论与实践相结合,提高同学们的动手能力;(二)、实验原理:通过降低水分活性而达到抑制微生物和酶的活性而延长食品保藏期;(三)、仪器、设备和材料1.仪器、设备:瓷罐(带盖);刀;盆;塑料桶;切菜板等;2.材料:鲜鸡蛋;黄瓜;白萝卜;芥菜;食盐;醋;酱油;糖;香辛料;黄粘土等;(四)、实验内容:1.实验操作(1). 水腌五香咸鸡蛋的腌制保藏:取花椒、八角、白芷、良姜、桂皮、茴香、生姜、精盐,用适量水煮沸20min(制成饱和食盐水,10℃时的饱和浓度为35/(100+35)=25.926%,20℃时的饱和浓度为36/(100+36)=26.47%)→冷却后倒入瓷坛内,将洗净的鸡蛋泡入(水要能淹没鸡蛋)→密封坛口,置通风处→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存;30天左右即可开坛取蛋煮食;(蛋水比=1�s1.3具体随容器等而异)(2)黄泥腌蛋的腌制保藏法:取花椒、八角、白芷、良姜、桂皮、茴香、生姜等用适量水煮沸20min→冷却后和选择好的深层黄土(晒干捣碎)调成浆糊状→用干布擦净鸡蛋(切勿用生水洗)→将鸡蛋在泥浆里打滚后→把食盐摊在平面上将鸡蛋在食盐上打滚→使鸡蛋外面的黄泥上包裹好一层食盐→然后将沾满食盐的鸡蛋装坛密封即可→在坛子上贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存→30天即可食用;(3). 对照→取鲜鸡蛋适量→装坛封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存;(做为对照);2.实验观察:每隔5天观察一次,观察不同腌制条件下的风味、色泽和质地变化;(五)、小节:要求:通过实验比较腌制处理条件下鸡蛋保存期,以及鸡蛋的风味、色泽、质地的变化,比较不同腌制处理条件的优劣;3、也可选用黄瓜;白萝卜;芥菜;大蒜为原料进行腌制保藏;如选用白萝卜干法腌制保藏:(1)原料选择和预加工处理(原料选取收成较晚、鲜嫩、肉实、皮厚、水分充足的白萝卜,将萝卜洗净后进行腌制)→装坛(一层盐一层萝卜,最下面和最上面都是食盐→封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存;(2)对照→取相同条件的白萝卜原料适量→装坛封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存;(做为对照);(3)实验观察:每隔10天观察一次,观察不同贮存条件下的风味、色泽和质地变化;(4)、小节:要求:通过实验比较腌制处理条件下白萝卜的保存期,以及白萝卜的风味、色泽、质地的变化,比较腌制保藏和常规保藏的保藏期;实验二食品的化学保藏(一)、实验目的1.了解食品在化学处理保藏条件下的保藏期;2.熟悉常规化学保藏操作;3.掌握常规化学保藏条件;4.理论与实践相结合,提高同学们的动手能力;(二)、实验原理:利用化学防腐剂来抑制微生物的活性而延长食品保藏期(三)、仪器、设备和材料 1.仪器、设备:塑料桶(带盖);果汁机;盆;切菜板等;2.材料:苹果;西瓜;异抗坏血酸钠;乳酸链球菌素;山梨酸钾;保鲜膜等;(四)、实验内容:1.实验操作(1). 原料选择和预处理(选择新鲜的苹果或西瓜等)→洗净→切块(容易放在果汁机里)→果汁机捣汁→装瓶(要先洗净)→加适量的山梨酸钾(看说明或课本)→搅拌均匀→封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存(4瓶);(2). 原料选择和预处理(选择新鲜的苹果或西瓜等)→洗净→切块(容易放在果汁机里)→果汁机捣汁→装瓶(要先洗净)→加适量的异抗坏血酸钠(看说明或课本)→搅拌均匀→封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存(3瓶);(3). 原料选择和预处理(选择新鲜的苹果或西瓜等)→洗净→切块(容易放在果汁机里)→果汁机捣汁→装瓶(要先洗净)→封盖→贴标签(标明实验班组、实验条件、时间等)→放到保存处室温保存(做为对照)(1瓶);2.实验观察:每隔1天观察一次,观察不同化学处理条件下的果汁的气味色泽和质地变化;(五)、小节:要求:通过实验比较不同热处理条件下果汁保存期,以及果汁的风味、色泽、质地的变化,比较不同化学处理条件的优劣;感谢您的阅读,祝您生活愉快。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
食品保藏原理实验指导书(适用于食品科学与工程专业)实验一蔬菜的冷冻干燥保藏(2个学时)一、实验目的了解冷冻干燥的基本原理和冷冻干燥的特点,掌握冷冻干燥机械的基本构造和操作流程。
二、实验原理1、基本理论水有固态、液体、气态三种态相。
根据热力学中的相平衡理论,随压力的降低,水的冰点变化不大,而沸点却越来越低,向冰点靠近。
当压力降到一定的真空度时,水的沸点和冰点重合,冰就可以不经液态而直接汽化为气态,这一过程称为升华。
当冰周围的蒸汽压低于610.5Pa时,冰加热升温可以直接升华为水蒸气,这就是升华干燥的理论基础。
2、概念真空冷冻干燥是先将物料冻结到共晶点温度以下,使物料中的水分变成固态的冰,然后在适当的真空度下,使冰直接升华为水蒸气,再用真空系统中的水汽凝结器(捕水器)将水蒸汽冷凝,从而获得干燥制品的技术。
3、干燥过程食品的真空冷冻干燥,就是在水的三相点以下,即在低温低压条件下,使食品中冻结的水分升华而脱去,冷冻干燥过程分为预冻、升华干燥、解析干燥3个过程。
1)预冻过程预冻是产品在冻结干燥之前,作为单独的操作,用一般的冻结方法预先将产品冻成一定的形状。
2)升华干燥过程要维持升华干燥的不断进行,必须满足俩个基本条件,即热量的不断供给和生成蒸汽的不断排除。
干燥过程是由周围逐渐向内部中心干燥的,干燥过程中的传热驱动力为热源与升华界面之间的温差,而传质驱动力为升华界面与冷阱之间的蒸汽分压差,温差越大,传热速度就越快,蒸汽分压差越大,传质速率就越快。
在升华干燥中,加热温度不能超过物料的共熔点温度,若温度过高,导致冰晶熔化,会影响制品质量。
此外,在升华干燥过程中的加热方式直接影响了物料温度分布、升华界面温度、升华界面水蒸气通量和干燥时间等重要过程参数。
3)解析干燥过程解析干燥时升华干燥之后,去除分布在物料的基质内以游离态或结合水形式存在水分的过程。
物料的解析干燥一般要依靠比升华温度高得多的温度来完成。
4、冷冻干燥系统(略)三、实验材料及器材小白菜、胡萝卜,大葱,真空冷冻干燥机四、操作方法1、操作流程新鲜蔬菜原料---原料选择---预处理---预冻—真空冷冻干燥---成品2、操作要点1)原料选择:原料应新鲜无病虫害,大小一致。
2)原料预处理:新鲜原料应清洗和切片。
切片时厚度适当,切割面应垂直于纤维方向,使冻干时冰的升华界面的移动方向与纤维方向一致,以提高干燥速率。
3)预冻:装箱之前,先将处理后的原料放入冻干箱进行空箱降温,然后将产品放入冻干箱内进行预冻,在-35℃下冷冻2-4h,使水分充分冻结。
4)真空冷冻干燥:冷阱温度达到-50℃左右,设定真空冷冻干燥机的各种参数,进行真空冷冻干燥。
冷冻干燥分俩个阶段,冻干开始时,隔板不加热,通过外界辐射为升华过程提供热量,冻干10h左右,升华干燥阶段基本完结,进入解析干燥阶段,启动加热程序,使隔板温度达到40℃,当物料温度接近加热极温度时,表示物料已经冻干,结束冻干操作。
五、成品复水性实验准确称取冻干物料5-6g,在50-55℃水中浸泡20min左右,充分复水后,取出沥干,晾干表面水分后准确称重,按如下公式计算复水比。
复水比=(充分复水后产品重量/冻干后产品重量)×100%六、思考题1、真空冷冻干燥的特点。
2、讨论对冻干成品复水性的影响因素。
实验二、烫漂标准的确定(2个学时)一、目的要求烫漂是果蔬加工中一项重要的工序,通过本实验,达到两个目的:1、基本掌握烫漂的生化指标和感官指标;2、了解不同的原料,杀死过氧化物酶时需要不同的烫漂条件。
二、材料和用具菜豆、山楂、苹果、马铃薯等新鲜果蔬。
0.1%联苯胺、0.3%过氧化氢。
电炉、烧杯(50ml)、不锈钢刀、温度计、滴管。
三、烫漂标准确定原理原料烫漂后,在颜色、比重、酶活性等方面均有变化,其中酶活性较易测定,易于在实际工作中采用,原料组织酶系中,因过氧化物酶即比较耐热,又易引起产品的破坏。
因此,通常以使物料的过氧化物酶失活作为烫漂处理的生化标准,其反映过程如下:过氧化物酶,H2O2联苯胺(还原态)----------------------→联苯胺(蓝色)-H2O (氧化态)烫漂后的组织在联苯胺和过氧化氢试剂作用下,数分钟后,若变为蓝色,则证明过氧化物酶活性存在,原料烫漂不够,需要提高烫漂处理强度;若不变色,则证明烫漂处理达到了要求。
四、操作方法将果蔬原料洗涤干净,切分成适当的大小,放入沸水中处理若干分钟,取出,冷水冲洗冷透。
用不锈钢刀横切,在切面上依次滴1-2滴0.1%联苯胺和0.3%的过氧化氢试剂,观察颜色变化,将观察结果记入下表:五、试剂配制1、0.1%联苯胺:称取1g联苯胺,溶于1升95%乙醇中。
2、0.3%过氧化氢:取1ml 30%的过氧化氢,加100ml蒸馏水,摇匀。
六、思考题1、不同原料的烫漂条件为何不同?2、据你所观察的现象,叙述原料烫漂后的比重,颜色等方面的变化。
实验三、糖水桔子罐头的制作(4个学时)一、目的要求1、理解掌握食品罐藏原理和罐头食品概念;2、熟悉掌握全去瓤衣糖水橘子罐头的生产工艺流程和操作要点;3、了解认识酸性罐头的国家标准;4、熟悉掌握糖水橘子罐头理化检测的检测要求。
二、实验材料及设备1.材料:新鲜橘子,蔗糖,柠檬酸2.药品:浓盐酸,氢氧化钠,基准邻苯二甲酸氢纳,酚酞指示剂,草酸,抗坏血酸,碘化钾,碘酸钾,淀粉3.设备:罐头,打浆机,手持折光仪,离心机,恒温培养箱,分析实验和微生物实验常用仪器三、工艺流程选料→清洗→烫煮→剥皮、去络、分瓣→酸碱处理→漂洗→称量→装罐、注糖水→封罐、杀菌、冷却→成品→检测。
四、实验操作1.选料:选择完全成熟,容易剥皮,果实硬度较硬,未受机械损伤,无虫害,无霉烂,直径在4cm的中型果作糖水制品。
2.清洗:原料选择后,用清水洗净果实表面的泥沙、污物。
3.烫煮:将选好的橘子放入90℃水中烫煮30秒钟,以使外皮及橘络易于剥离而不影响橘肉为佳。
注意水温不能过高,时间也不能长,否则易造成果食烫熟,严重影响质量。
4. 剥皮、去络、分瓣:剥去果皮,不伤拮囊,逐瓣分开、撕净桔瓣上的拮络,不伤囊包,不出汁水,然后分瓣处理。
5.酸碱处理:浸酸使瓤衣与汁胞之间的果胶物溶解,并使之膨胀分离,大约浸至囊一起皱并与汁胞呈分离状态时,就可结束;强碱使囊衣溶解剥落,如果所浸的碱液浓度过大或时间过长,则也能使汁胞破裂和囊片破碎。
(1)酸处理:0.1%的盐酸溶液(1ml浓盐酸稀释到1000ml)于常温下搅拌处理30分钟,至嚼桔瓣无硬渣感,水发白时即放出酸水,流动水冲洗3次,然后进行碱处理。
(2)碱处理:将固态碱先配均匀,配成浓度0.20%的碱溶液(2g氢氧化钠溶于1000ml水)于常温下搅拌处理10分钟,达到粗囊去净,内层囊衣完整后即放碱液,注满清水进行充分清洗。
6.清洗:碱处理后应马上进行清洗,防止过度浸损囊衣。
应用流动水清洗至桔瓣无碱液残留,手感无滑腻感为宜。
7.装罐、注糖水:称取适量橘瓣,装于一定重量的(质量要先称量)玻璃罐内,注入18%浓度的热糖水(90g蔗糖加410g水加热溶解,并用柠檬酸调PH值为3.5),注满。
8.排气、封罐、杀菌、冷却:加注热糖液后排气约10min至罐中心温度达到80℃后趁热封罐,然后在100℃沸水中煮沸15mim,然后按80℃——60℃——40℃冷却,冷却时间不超过10min。
9.贴标储存:把经过处理的成品贴上标签,标签内容包括编号、时间、组名等;最后将成品置于阴凉处进行倒灌储存。
五、成品质量指标1.感官指标:(1)色泽:橘片表面具有与原果肉近似光泽,色泽较一致,糖水较透明。
(2)滋味及风味:具有品种糖水橘子罐头应有的风味,酸甜适口、无异味。
组织形态:橘片食之无硬渣感觉,形态饱满完整,大小大致均匀。
破碎率(以重量计)不超过固形物的3%。
(破碎片:指破碎部分超过桔片侧面积1/3的桔片。
均匀度:指同一罐中最大最厚的三片桔片的重量之和与最小最薄的三片枯片重量之和的比率。
均匀:比率不超过1.4倍;较均匀:不超过1.7倍;尚均匀:不超过2倍。
)(3)杂质:不允许存在。
2.理化指标:(1)净重:约300克(玻璃瓶)(毛重减去容器重)(2)固形物:果肉不低于净重的55%。
(控干水分后的物重与净重之比)(3)糖水浓度:开罐时(按折光率)为14~18%。
,优级品和一级品为14%-18%,合格品为12%-16%。
(4)重金属含量:每千克制品含锡(以Sn计)不超过200毫克,铜(以Cu计)不超过10毫克,铅(以Pb计)不超过2毫克。
3.微生物指标:无致病菌及微生物作用所以起的腐败征象。
六、各种指标的测定(一)总糖的测定(手持折光仪直接法):1.手持折光仪工作原理光线从一种介质进入另一种介质时会产生折射现象,且入射角正弦之比恒为定值,此比值称为折光率。
果蔬汁液中可溶性固形物含量与折光率在一定条件下(同一温度、压力)成正比例,故测定果蔬汁液的折光率,可求出果蔬汁液的浓度(含糖量的多少)。
常用仪器是手持式折光仪,也称糖镜、手持式糖度计,通过测定果蔬可溶性固形物含量(含糖量),可了解果蔬的品质,大约估计果实的成熟度。
2. 使用方法:打开盖板,用软布仔细擦净检测棱镜。
取待测溶液数滴,置于检测棱镜上,轻轻合上盖板,避免气泡产生,使溶液遍布棱镜表面。
将仪器进光板对准光源或明亮处,眼睛通过目镜观察视场,转动目镜调节手轮,使视场的蓝白分界线清晰。
分界线的刻度值即为溶液的浓度。
3. 使用注意事项:(1)在使用中必须细心谨慎,严格按说明使用,不得任意松动仪器各连接部分,不得跌落、碰撞,严禁发生剧烈震动。
(2)使用完毕后,严禁直接放入水中清洗,应用干净软布擦拭,对于光学表面,不应碰伤,划伤。
(3)仪器应放于干燥、无腐蚀气体的地方保管,同时避免零备件丢失。
(二)总酸的测定:1.原理:食品中的有机酸在用标准碱液滴定时,被中和生成盐类,用酚酞作指示剂,当滴定到终点(PH=8.2,指示剂显红色)时,根据耗用标准碱液的体积,可计算出样品中总酸含量。
其反应式为:RCOOH+NaOH→RCOONa+H2O2.使用范围:本法适用于各类色浅的食品中总酸含量的测定。
3.试剂:(1)NaOH标准溶液(0.1mol/L):称取4g分析纯氢氧化钠溶于200毫升水中,然后稀释至1000ml。
标定:精确称取3份约0.4g(准确至0.0002g)在120℃烘干的邻苯二甲酸氢钾基准试剂,分别置于250ml三角瓶中,加入50ml除去二氧化碳的蒸馏水,溶解后,加2~3滴酚酞指示剂,立即用0.1 mol/L氢氧化钠溶液滴定至粉红色30s不退色,记录体积:计算氢氧化钠标准溶液浓度C(NaOH)=m*1000/204.2(V2-V1)m—邻苯二甲酸氢钾的质量,g ;V2—氢氧化钠溶液的体积,ml;V1—空白试验中所耗用氢氧化钠溶液的体积,ml;(2)称取1%酚酞乙醇溶液:称取酚酞1g溶解于100ml95%乙醇中。
