α-淀粉酶的固定化以及淀粉水解作用的检测
《高三生物复习资料》实验6-α-淀粉酶的固定化及淀粉水解作用的检测-精选文档

六、实验步骤
5mg α-淀粉酶+4mL蒸馏水 +5g石英砂(搅拌30min)
装入下端接有气门心并 用夹子封住的注射器中 10倍体积蒸馏水洗涤注射器以除去 未吸附的淀粉酶,流速1mL/min 用滴管滴加淀粉溶液,以 0.3mL/min流速过柱 为什么要控制流速? 流出5mL溶液后接收0.5mL流出液,加 1~2滴过柱KI-I2溶液,观察颜色 10倍体积蒸馏水洗涤注射器4℃保存
一、基础知识 固定化酶:是将酶用物理或化学的方法 固定在某种介质上,使之成为不溶于水 而又有酶活性的制剂。 优点:固定化酶固定在一定的空间范围 内,可以重复使用,且能及时与产物分 离。
酶固定化的常用方法
吸附法
(1)物理吸附法 (基团与载体 共价结合。
交联法
酶蛋白的氨基以戊二醛 与载体相连。
四、实验材料 1、 α-淀粉酶,石英砂, 2、可溶性淀粉溶液 3、5mmol/LKI-I2溶液
五、实验原理
一定浓度的淀粉溶液经过固定酶柱后,
可使淀粉水解成糊精。用淀粉指示剂溶液测
试,流出物呈红色,表明水解产物糊精生成。
淀粉
α-淀粉酶
糊精
β-淀粉酶
麦芽糖
糖化淀粉酶
葡萄糖
遇碘显 蓝色
遇碘显 红色
遇碘不 显色
七、实验结果
淀粉溶液
吸附有α-淀粉酶的石英砂
1
2
3
4
1、2mL水+1~2滴KI-I2溶液 2、2mL淀粉液+1~2滴KI-I2溶液 3、2mL淀粉滤液+1~2滴KI-I2溶液 4、2mL淀粉滤液+1~2滴KI-I2溶液+稀释1倍
八、问题讨论
1.如何证明洗涤固定化酶柱的流出液中没有淀 粉酶?
高中生物 第2部分 酶的应用 实验6 α 淀粉酶的固定化及淀粉水解作用的检测教案 浙科版选修1

实验6 α-淀粉酶的固定化及淀粉水解作用的检测课标解读重点难点1.制备固定化α-淀粉酶。
2.进行淀粉水解的测定。
3.通过此实验探讨固定化酶的应用价值。
1.固定化酶的方法和优点。
2.固定化酶装柱后的使用。
一、酶与固定化酶1.酶活细胞产生的具有催化作用的一类有机物,它是生物体内各种化学反应的催化剂。
2.固定化酶将水溶性的酶用物理或化学的方法固定在某种介质上,使之成为不溶于水而又有酶活性的制剂。
3.将酶改造成固定化酶的原因由于酶在水溶液中很不稳定,且不利于工业化使用,所以要将酶改造成固定化酶。
4.酶固定化的方法吸附法、共价偶联法、交联法和包埋法等。
本实验用的是吸附法。
5.固定化酶作用的机理将固定化酶装柱,当底物经过该柱时,在酶的作用下转变为产物。
在酶固定化的各种方法中,哪一种方法对酶的作用影响较小?【提示】吸附法二、α-淀粉酶的固定化及淀粉水解作用检测的实验1.实验目的(1)制备固定化α-淀粉酶。
(2)进行淀粉水解作用的检测。
2.实验原理将α-淀粉酶固定在石英砂上,一定浓度的淀粉溶液经过固定化酶柱后,可使淀粉水解成糊精。
用淀粉指示剂测试,若流出物呈红色,表明糊精生成。
3.本实验使用的酶及特性本实验使用的酶是枯草杆菌的α-淀粉酶,其作用的最适pH为5.5~7.5,最适温度为50~75_℃。
4.实验材料及其制备(1)α-淀粉酶的固定化:在烧杯中将5 mg α-淀粉酶溶于4 mL蒸馏水中(由于酶不纯,可能有些不溶物)↓再加入5 g石英砂,不时搅拌30 min↓30 min后将上述溶液装入1支注射器中(该注射器的下端接有气门心,并用夹子封住)↓用10倍体积的蒸馏水洗涤此注射器,以除去未吸附的游离淀粉酶,流速为1 mL/min(2)可溶性淀粉溶液:取50 mg可溶性淀粉溶于100 mL热水中,搅拌均匀。
(3)KI-I2溶液:称取0.127 g碘和0.83 g碘化钾。
加蒸馏水100 mL,完全溶解后装入滴瓶中。
5.实验步骤(1)淀粉溶液流经固定化酶柱将灌注了固定化酶的注射器放在注射器架上,用滴管滴加淀粉溶液,使该溶液以0.3 mL/min的流速过柱。
α淀粉酶的固定化及淀粉水解作用的检测精品课件(一)

α淀粉酶的固定化及淀粉水解作用的检测精品课件(一)α淀粉酶是一种催化淀粉分解的酶,具有广泛的应用价值,在食品工业、饲料工业、医药工业和纺织工业都有重要的应用。
对于α淀粉酶的固定化和淀粉水解作用的检测具有重要的研究价值。
本文将介绍α淀粉酶的固定化及淀粉水解作用的检测精品课件。
一、α淀粉酶的固定化1. 研究目的α淀粉酶固定化的目的是利用固定化技术提高酶的稳定性和活性,使其在工业应用中更加优越。
2. 固定化方法(1)吸附法:将酶直接吸附在固体载体表面上,如硅胶、纤维素等。
(2)共价结合法:通过化学反应将酶共价结合在载体上,如聚酰胺凝胶。
(3)交联法:利用交联剂将酶与载体交联,形成固定化酶。
3. 固定化效果α淀粉酶经过固定化后,具有更好的稳定性和活性,可以提高酶的使用寿命和效率。
二、淀粉水解作用的检测1. 研究目的淀粉水解作用的检测旨在测定酶水解淀粉的效率,评价酶的性能和应用价值。
2. 检测方法(1)碘酒法:将淀粉样品与酶一起加入反应体系中,加入碘酒滴定,在淀粉被水解完全后,碘酒滴定出现无色。
(2)比色法:将淀粉样品与酶一起加入反应体系中,加入糖色再经比色,根据测试淀粉的浓度,推算出酶的效率。
(3)电化学法:利用电化学技术测定反应体系中的还原电位,根据反应体系的电化学响应来测定淀粉水解的效率。
3. 检测效果通过淀粉水解作用的检测,可以评估α淀粉酶的性能和应用价值,指导其在工业应用中的使用。
综上所述,α淀粉酶的固定化及淀粉水解作用的检测是酶学研究领域中的重要课题。
本文介绍了α淀粉酶的固定化方法、效果,以及淀粉水解作用的检测方法和效果,对于淀粉酶及其应用研究人员具有重要的参考价值。
a-淀粉酶的固定化及淀粉水解作用实验方案

实验:α-淀粉酶的固定化及淀粉水解作用背景资料一、酶酶(enzyme)催化特定化学反应的蛋白质、RNA或其复合体。
是生物催化剂,能通过降低反应的活化能加快反应速度,但不改变反应的平衡点。
绝大多数酶的化学本质是蛋白质。
具有催化效率高、专一性强、作用条件温和等特点。
1.高效性:酶的催化效率比无机催化剂更高,使得反应速率更快;2.专一性:一种酶只能催化一种或一类底物,如蛋白酶只能催化蛋白质水解成多肽;因此在食用酵素当今在功能上,主要有四种:高浓缩SOD酵素如复方天然酵素主要用于乳腺瘤、子宫肌瘤、卵巢囊肿等肿瘤方面;长生酵素直接补脾补肾补气血,全面调理;纤体酵素专门转化脂肪减肥;肠毒清酵素则专门清理肠皱褶的毒素。
3.多样性:酶的种类很多,大约有5000多种,其中可以通过食用补充的酵素达2000多种;形态上主要有三种:专业级酵素为酵素胶囊,其次为酵素粉,而液体酵素含量低、效价低、易腐败而安全性较差一些,食用风险较高。
4.温和性:是指酶所催化的化学反应一般是在较温和的条件下进行的,因此,纯正酵素是中性的,温和的,不存在副作用,或“好转反应”。
对于有刺激性而必然存的“好转反应”,除了本身腐败以外,也有可能有药品的添加。
5.活性可调节性:包括抑制剂和激活剂调节、反馈抑制调节、共价修饰调节和变构调节等。
6.易变性:大多数酶是蛋白质,因而会被高温、强酸、强碱等破坏;7.有些酶的催化性与辅助因子有关。
酶与无机催化剂的比较但酶易受环境影响而失活,包括温度、PH值等,例如一般来说动物体内的酶最适温度在35到40℃之间,植物体内的酶最适温度在40-50℃之间;细菌和真菌体内的酶最适温度差别较大,有的酶最适温度可高达70℃。
动物体内的酶最适PH大多在6.5-8.0之间,但也有例外,如胃蛋白酶的最适PH为1.8,植物体内的酶最适PH大多在4.5-6.5之间。
另外,反应中反应产物和酶的分工和回收困难等缺点限制了酶在工业上的广泛应用。
2013浙科版选修1第二部分《实验六 α-淀粉酶的固定化及淀粉水解作用的检测》word学案1

实验6:α—淀粉酶的固定化及淀粉水解作用的检测 导学一、酶和固定化酶1.酶:酶是生物体内催化各种反应的催化剂。
酶作为催化剂与一般的催化剂有共同特点:①用量少而催化效率高;②不改变化学反应的平衡点,酶本身在反应反应前后也不发生变化;③可降低反应的活化能。
酶作为生物催化剂的特性有:①催化效率高;②有高度的专一性;③易失活等。
通常情况下酶都是在水溶液中催化底物反应,因此酶在反应系统中是与底物、产物混在一起的,反应结束后,即使仍有较高活力,也很难再回收利用。
另外,在水溶液中起作用的酶也给产物进一步分离纯化带来了一定困难。
2.固定化酶:固定化酶又称固相酶、水不溶性酶,它是将水溶性的酶用物理或化学的方法固定在某种介质上,使之成为不溶于水而又有酶活性的制剂。
固定化酶与游离酶相比不但稳定性好,而且与底物和产物容易分离,且易于控制,能反复多次使用,便于运输和贮存,有利于自动化生产。
因此,固定化酶在工业、医学和生化分析等方面的应用发展较快。
直接使用酶和固定化酶催化的优缺点比较二、固定化酶的制作原理酶固定化方法由酶的性质和载体特性所决定,主要包括:吸附法、共价偶联法、交联法和包埋法等。
1.吸附法:有物理吸附法和离子交换法两种。
物理吸附法是将酶蛋白的分子吸附在惰性载体上,但要选择不引起变性且能保持一定酶活力的载体,对蛋白质有高度吸附能力的有机硅胶、活性碳和石英砂等。
离子交换法是利用蛋白质的两性性质,使其带有电荷的基团与离子交换剂形成离子键,而被交换结合至交换剂上。
2.共价偶联法(载体偶联法):酶蛋白的一些基团,包括羧基末端、氨基末端等,在温和的条件下能与载体共价结合,从而被固定。
但结合的部位必须不是酶的活性中心,也不是维持其空间结构的必需基团。
这种结合稳定性好,酶不易脱落,可使用较长时间。
3.交联法:是指通过双功能试剂,将酶和酶联结成网状结构的方法,交联法使用的交联剂是戊二醛等水溶性化合物。
4.包埋法:是指将酶包裹在多孔的载体中,如将酶包裹在聚丙烯酰胺凝胶等高分子凝胶中,或包裹在硝酸纤维素等半透性高分子膜中。
实验6-α-淀粉酶的固定化及淀粉水解作用的检测

固定化原生质体
注意:一般要添加渗透压稳定剂,以防止原生质体破裂。 ①由于去除了细胞壁的扩散障碍,有利于氧气和营养物 质的传递和吸收和胞内产物的分泌。 ②原生质体不稳定,容易破裂,固定化后,由于载体的 保护作用,稳定性提高,可反复使用和连续使用较长的 时间,利于连续化生产。 ③易于和发酵产物分开,有利于产物的分离纯化,提高 产品质量。
①溶解淀粉:50 mg 可溶性淀粉溶于100 mL热水 中,搅拌均匀。 ②过柱:使淀粉溶液以0.3 mL/min的流速过柱, 在流出5mL淀粉溶液后接收0.5 mL流出液。 ③检测:加入1-2滴KI-I2溶液,观察颜色变化。 用水稀释1倍后再观察颜色。
固 定 化 酶 柱
淀粉完全水解?
每分钟6滴
控制流速:让淀粉和淀粉酶充分接触反应。
关的问题:
(1)通常从腐烂的水果上分离产果胶酶的微生物,其
原因除水果中果胶含量较高外,还因为
。
ቤተ መጻሕፍቲ ባይዱ
(2)为了获得高产果胶酶微生物的单菌落,通常对分
离或诱变后的微生物悬液进行
。
腐烂的水果中含产果胶酶的微生物较多 涂布分离或划线分离
(3)在某种果汁生产中,用果胶酶处理显著增加了产量
,其主要原因是果胶酶水解果胶使
什么是固定化酶
固定化酶:将水溶性的酶用物理或化学的方法固定在某 种非水溶性介质上,使之成为不溶于水而又有酶活性的 制剂。
游离酶
酶在水溶液中很不稳定,且不利于工业化使用。
固定化酶的优点
①能提高酶的稳定性。 ②可以反复多次使用,大大降低生产成本。 ③反应后易于与产物分离,利于提高产品质量。 ④反应条件易于控制,生产可实现连续化和自 动化。
。果汁
生产中的残渣果皮等用于果胶生产,通常将其提取液浓
淀粉酶的固定化及淀粉水解作用的检测

• 方法: (1) α-淀粉酶的固定化:
遇碘显蓝色 遇碘显红色 遇碘不显色
(1)不稳定:酶通常对强酸、强碱、高温和有机溶剂等条件非常敏感,容易失活;
吸附法 将固定化酶装柱,当底物经过该柱时,在酶的作用下转变为产物。
贮于冰箱几天后重复实验:
3、设备及用品:
包埋法 5ml塑料注射器、50ml烧杯、滴管、自行车用气门芯及夹子、注射器架、试管或微量离心管3支
5ml塑料注射器、50ml烧杯、滴管、自行车用气 门芯及夹子、注射器架、试管或微量离心管3支
4、实验材料及其制备
(1) α-淀粉酶的固定化: 5mgα-淀粉酶+4ml蒸馏水+5g石英砂,搅拌,
30min
→装入层析柱→10倍体积的蒸馏水洗
涤此注射器,流速为1ml/min(约20滴) (2)可溶性淀粉溶液:
氨基相连处
酶的固定化方法
酶 物理吸附法 交联法 包埋法
固定化酶的性质
• 稳定性增加: 对热、蛋白酶及各种试剂的稳定性。 • pH活性曲线和最适pH的变化: 可能向酸性或碱性方向移动。需实验确定
• 底物的专一性变化:
三、α-淀粉酶的固定化及 淀粉水解作用检测的实验
1、实验目的:
(1)制备固定化α-枯淀草粉杆酶菌;的α-淀粉酶: (2)进行淀粉水解的最测适定p。H5.5~7.5
怎样解决这些问题呢?
——固定化酶技术
一、酶与固定化酶
• 酶 活细胞产生的具有生物催化作用的 生物大分子。
• 固定化酶 (固相酶)
将水溶性的酶用物理或化学 的方法固定在某种介质上, 使之成为不溶于水而又有酶 活性的制剂。
固定化酶的优点 • (1)使酶固定化后有一定的机械强度,催化
反应的过程可管道化、连续化和自动化; • (2)酶不溶解在催化反应的溶液中,产物更
_淀粉酶的固定化及淀粉水解作用的检测_实验改进_徐平珍

2014年第49卷第3期生物学通报51生物技术是一门既古老又现代的技术,而且涉及的范围极为广泛。
如酿造工业的产品———酱油、醋、酒等,是人们日常生活中的必需品。
由于生物技术的迅猛发展,每年都需要消耗大量的生物酶制剂,淀粉酶作为一类重要的生物催化剂,在医药、化工、食品及饲料添加剂等领域都有广泛的应用,其产量几乎占据整个酶制剂总产量的50%,且需求量越来越大[1]。
但是,酶在水溶液中很不稳定,容易受到酸、碱和有机溶剂的影响,而且溶液中的酶很难回收,不能再利用,反应后酶混在产品中又可能影响产品质量。
这些因素影响了酶工业化的应用,而固定化酶技术能很好地解决这些问题。
“α-淀粉酶的固定化及淀粉水解作用的检测”是浙科版生物学选修1“生物技术实践”模块中第2部分“酶的应用”实验6的内容,也是《浙江省生物教学指导意见》中提出的学生需要掌握的7个实验之一。
选修课“生物技术实践”,是一门以自己动手做实验为主的课程。
而本实验按照原实验步骤需要2h左右,在高中教学安排中很难满足此要求。
另外按照教材中的实验步骤进行实验,得不到理想的实验结果,本校教师和前几届学生在实验中观察到流出液加碘液混匀后溶液显黄色而非红色。
《生物课程标准》的基本理念之一是倡导探究性学习,实验是学习生物技术的有效途径之一。
教师应尽可能为学生提供或创造动手操作的机会,通过亲手操作,学生在实践中学习新知识,并使知识得到延伸,同时也能学习相关实验操作的技能。
笔者对本实验进行了适当改进,使学生能在课堂时间内完成相关实验,此外对以往实验中遇到的一些疑问进行了探讨。
1实验材料α-淀粉酶、可溶性淀粉、石英砂、碘、碘化钾、5mL一次性注射器、铁架台、烧杯、天平、滴瓶、玻璃棒、绳子、量筒、试管、试管架和冰箱。
2实验方法2.1试剂的配制①0.5%淀粉溶液:称取0.5g可溶性淀粉溶于100mL热水中,搅拌均匀。
②5mmol/L KI-I2溶液:称取0.127g碘和0.83g碘化钾,加蒸馏水100mL,完全溶解后装入滴瓶中。
α-淀粉酶的固定化及淀粉水解2

实验6 α-淀粉酶的固定化及淀粉水解作用的检测高二年级班姓名实验日期:____月日【知识准备】1.背景知识酶是生物体内各种化学反应的催化剂,它有高度的专一性和高效性。
但酶在水溶液中很不稳定,且不利于工业化使用。
固定化酶就是将水溶性的酶用物理或化学的方法固定在某种介质上,使之成为不溶于水而又有酶活性的制剂。
将固定化酶装柱,当底物经过该柱时,在酶作用下转变为产物。
2.实验原理本实验是采用吸附法制备固定化酶。
(1)使用的吸附剂是石英砂,石英砂是由天然矿石粉碎而成,它的化学成分是二氧化硅,其化学反应活性很低。
(2)使用的α-淀粉酶通常由枯草杆菌深层发酵制备,具有较强的液化淀粉的能力,可用于制备糊精,其最适pH5.5~7.5,最适温度50℃~75℃。
3.各种淀粉酶水解淀粉的反应如下:α-淀粉酶只将淀粉水解为糊精,淀粉溶液加入KI-I2指示溶液时显现蓝色,而转变成糊精后显现红色。
将吸附有α-淀粉酶的石英砂装柱,使淀粉溶液流过柱,若柱的流出液在加入KI-I2溶液时可看到溶液呈现红色,表明水解产物中有糊精。
α-淀粉酶制成不溶性的固定化酶后,酶的稳定性增加,包括酶对热的稳定性,对蛋白酶的抵抗能力、对各种试剂的稳定性都不同程度地增加。
由于稳定性增加,保存期也相应延长,数日内酶活力不减。
4.思考题①为什么使用石英砂作为酶的吸附剂?②如何证明α-淀粉酶已将淀粉水解?③如何证明洗涤固定化酶的流出液中没有淀粉酶?【实验目的】1.制备固定化的α-淀粉酶2.固定化的α-淀粉酶水解淀粉的测定【材料用具】α-淀粉酶溶液,0.5%淀粉溶液,石英砂,5mmol/L KI-I2溶液,蒸馏水5ml层析柱50mL烧杯,250mL烧杯,滴管,玻璃棒,点样板铁架台【实验步骤】一、新制淀粉固定化酶1.用50ml小烧杯称取5g石英砂,加入2ml α–淀粉酶溶液,浸泡10分钟,使α–淀粉酶固定到石英砂上。
在等候期间可以先完成实验步骤“二”。
2.用10~15ml的蒸馏水清洗石英砂后,取清洗液2滴加到点样板上,同时滴加0.5%淀粉溶液混匀,再加入1滴KI-I2溶液,若溶液变为蓝色,说明未固定到石英砂上的α–淀粉酶已完全除去。
a-淀粉酶的固定化及淀粉水解作用实验教案--
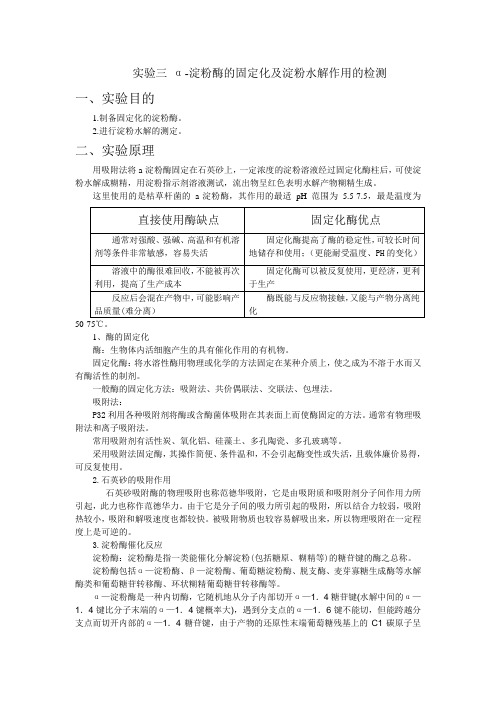
实验三 α-淀粉酶的固定化及淀粉水解作用的检测一、实验目的1.制备固定化的淀粉酶。
2.进行淀粉水解的测定。
二、实验原理用吸附法将a-淀粉酶固定在石英砂上,一定浓度的淀粉溶液经过固定化酶柱后,可使淀粉水解成糊精,用淀粉指示剂溶液测试,流出物呈红色表明水解产物糊精生成。
这里使用的是枯草杆菌的a-淀粉酶,其作用的最适pH 范围为 5.5-7.5,最是温度为50-75℃。
1、酶的固定化酶:生物体内活细胞产生的具有催化作用的有机物。
固定化酶:将水溶性酶用物理或化学的方法固定在某种介质上,使之成为不溶于水而又有酶活性的制剂。
一般酶的固定化方法:吸附法、共价偶联法、交联法、包埋法。
吸附法:P32利用各种吸附剂将酶或含酶菌体吸附在其表面上而使酶固定的方法。
通常有物理吸附法和离子吸附法。
常用吸附剂有活性炭、氧化铝、硅藻土、多孔陶瓷、多孔玻璃等。
采用吸附法固定酶,其操作简便、条件温和,不会引起酶变性或失活,且载体廉价易得,可反复使用。
2.石英砂的吸附作用石英砂吸附酶的物理吸附也称范德华吸附,它是由吸附质和吸附剂分子间作用力所引起,此力也称作范德华力。
由于它是分子间的吸力所引起的吸附,所以结合力较弱,吸附热较小,吸附和解吸速度也都较快。
被吸附物质也较容易解吸出来,所以物理吸附在一定程度上是可逆的。
3.淀粉酶催化反应 淀粉酶:淀粉酶是指一类能催化分解淀粉(包括糖原、糊精等)的糖苷键的酶之总称。
淀粉酶包括α—淀粉酶、β—淀粉酶、葡萄糖淀粉酶、脱支酶、麦芽寡糖生成酶等水解酶类和葡萄糖苷转移酶、环状糊精葡萄糖苷转移酶等。
α—淀粉酶是一种内切酶,它随机地从分子内部切开α—1.4糖苷键(水解中间的α—1.4键比分子末端的α—1.4键概率大),遇到分支点的α—1.6键不能切,但能跨越分支点而切开内部的α—1.4糖苷键,由于产物的还原性末端葡萄糖残基上的C1碳原子呈直接使用酶缺点固定化酶优点 通常对强酸、强碱、高温和有机溶剂等条件非常敏感,容易失活固定化酶提高了酶的稳定性,可较长时间地储存和使用;(更能耐受温度、PH 的变化) 溶液中的酶很难回收,不能被再次利用,提高了生产成本固定化酶可以被反复使用,更经济,更利于生产 反应后会混在产物中,可能影响产品质量(难分离) 酶既能与反应物接触,又能与产物分离纯化α—构型(光学),故称这种酶为α—淀粉酶。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《α-淀粉酶的固定化与淀粉水解作用的检测》实验方案第二实验班一组组长:张金昌组员:胡建军、朱恩梅、石仙竹、谢娟丽、李昀奕、郭天天2013.10.15α-淀粉酶的固定化与淀粉水解作用的检测一、实验背景资料:1、酶:活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质;具有高效性、专一性,同时,也有高度不稳定性,因为绝大多数酶的本质是蛋白质,凡是能使蛋白质变性的因素,如高温、高压、强酸、强碱等都会使酶丧失活性。
2、酶促反应:指由酶作为催化剂进行催化的化学反应;3、α-淀粉酶:为枯草杆菌的α-淀粉酶,其作用的最适PH为5.5~7.5,最适温度为50~70℃。
广泛分布于动物(唾液、胰脏等)、植物(麦芽、山萮菜)及微生物。
此酶既作用于直链淀粉,亦作用于支链淀粉,其特征是引起底物溶液粘度的急剧下降和碘反应的消失,最终产物在分解直链淀粉时以麦芽糖为主,此外,还有麦芽三糖及少量葡萄糖;在分解支链淀粉时,除麦芽糖、葡萄糖外,还生成分支部分具有α-1,6-键的α-极限糊精。
4、固定化酶:借助于物理和化学的方法把酶束缚在一定的空间内并仍具有催化活性的酶制剂。
酶更适合采用化学结合和物理吸附法固定化。
吸附法是酶分子吸附于水不溶性的载体上,它的优点是操作简便,条件温和,不会引起酶变性或失活,且载体廉价易得,可以反复使用。
5、吸附剂:常用的吸附剂有活性炭、氧化铝、硅藻土、多孔陶瓷、多孔玻璃等。
活性炭:活性炭是一种多孔性的含炭物质, 它具有高度发达的孔隙构造, 是一种极优良的吸附剂, 每克活性炭的吸附面积更相当于八个网球埸之多. 而其吸附作用是藉由物理性吸附力与化学性吸附力达成. 其組成物质除了炭元素外,尚含有少量的氢、氮、氧及灰份,其結构则为炭形成六环物堆积而成。
由于六环炭的不规则排列,造成了活性炭多微孔体积及高表面积的特性。
硅胶:硅胶是由硅酸凝胶mSiO2·nH2O适当脱水而成的颗粒大小不同的多孔物质。
具有开放的多孔结构,比表面(单位质量的表面积)很大,能吸附许多物质,是一种很好的干燥剂、吸附剂和催化剂载体。
硅胶的吸附作用主要是物理吸附,可以再生和反复使用。
在碱金属硅酸盐(如硅酸钠)溶液中加酸,使之酸化,再加入一定量的电解质进行搅拌,即生成硅酸凝胶;或者在较浓的硅酸钠溶液中加酸或铵盐也能生成硅酸凝胶。
将硅酸凝胶静置几小时使之老化,然后用热水洗去可溶性盐类,在60~70℃下烘干并在约300℃时活化,即可得硅胶。
氧化铝:影响活性氧化铝吸附性能的主要因素包括以下几方面:(1)颗粒粒径:粒径越小,吸附容量越高,但粒径越小,颗粒强度越低,影响其使用寿命。
(2)原水PH值:当PH值大于5时,PH值越低,活性氧化铝吸附容量越高。
⑶原水初始氟浓度:初始氟浓度越高,吸附容量较大。
(3)原水碱度:原水中重碳酸根浓度高,吸附容量将降低。
(4)氯离子和硫酸根离子。
(5)砷的影响:活性氧化铝对水中的砷有吸附作用,砷在活性氧化铝上的积聚造成对氟离子吸附容量的下降,且使再生时洗脱砷离子比较困难。
6、石英砂:是石英石经破碎加工而成的石英颗粒,石英石是一种非金属矿物质,是一种坚硬、耐磨、化学性能稳定的硅酸盐矿物,其主要矿物成分是SiO2,石英砂的颜色为乳白色、或无色半透明状,硬度7,石英砂是重要的工业矿物原料,非化学危险品,广泛用于玻璃、铸造、陶瓷及耐火材料、冶炼硅铁、冶金熔剂、冶金、建筑、化工、塑料、橡胶、磨料等工业。
因为其性质稳定、能耐酸、耐碱、耐磨,腐蚀性小,不易燃烧,廉价,所以选择石英砂作为酶的吸附剂。
7、为何选用石英砂?石英砂作为酶的吸附剂的优缺点:固定化酶有许多方法,本实验中采用的是吸附法。
吸附法有物理交换法和离子交换法两种。
其中本实验采用的又是物理交换法。
该方法是将酶蛋白的分子吸附在惰性载体上,但要选择不引起变性且能保持一定酶活力的载体,且对蛋白质要有高度吸附能力。
自然界中有机硅胶、活性炭和石英砂等都可以被用于做载体。
现已了解其中石英砂对固定化α-淀粉酶、胰蛋白酶作用较好。
优点:石英砂表面带正电荷,蛋白质为两性物质,在大于其等电点的条件下,蛋白质带负电荷,由此能吸附在石英砂表面,α-淀粉酶被石英砂吸附属于物理吸附法,将蛋白质分子吸附在惰性载体(石英砂)上,酶不会引起变性,且能保持一定酶活力,对蛋白质有高度吸附能力。
缺点:是非金属矿物质,不具有多孔结构,在吸附性上稍差,同时,石英砂质脆,坚硬,易磨细,不利于过滤。
吸附剂一般有孔结构,对吸附质有强烈吸附能力,一般不与吸附质和介质发生化学反应,有良好机械强度等,如活性炭、氧化铝、硅藻土、多孔陶瓷、多孔玻璃等。
8、固定化酶与游离酶的比较:9、淀粉遇碘变蓝:直链淀粉遇碘呈蓝色,支链淀粉遇碘呈紫红色,糊精遇碘呈蓝紫、紫、橙等颜色。
这些显色反应的灵敏度很高,可以用作鉴别淀粉的定量和定性的方法,也可以用它来分析碘的含量。
纺织工业上用它来衡量布匹退浆的完全度。
10、碘遇淀粉和糊精显不同的颜色:以前认为,淀粉能吸附碘,使碘吸收的可见光的波长向短的波长方向移动,棕色的碘液就变成蓝色。
同理,支链淀粉和糊精也能吸附碘,不过吸附的程度不同,因此呈现的颜色不同。
这种解释的有力根据是碘的淀粉液在加热时蓝色消失。
这就被认为是加热后分子动能增大,引起解吸的缘故。
近年来用先进的分析技术(如X射线、红外光谱等)研究碘跟淀粉生成的蓝色物,证明碘和淀粉的显色除吸附原因外,主要是由于生成包合物的缘故。
直链淀粉是由α-葡萄糖分子缩合而成螺旋状的长长的螺旋体,每个葡萄糖单元都仍有羟基暴露在螺旋外。
碘分子跟这些羟基作用,使碘分子嵌入淀粉螺旋体的轴心部位。
碘跟淀粉的这种作用叫做包合作用,生成物叫做包合物。
在淀粉跟碘生成的包合物中,每个碘分子跟6个葡萄糖单元配合,淀粉链以直径0.13 pm绕成螺旋状,碘分子处在螺旋的轴心部位。
淀粉跟碘生成的包合物的颜色,跟淀粉的聚合度或相对分子质量有关。
在一定的聚合度或相对分子质量范围内,随聚合度或相对分子质量的增加,包合物的颜色的变化由无色、橙色、淡红、紫色到蓝色。
例如,直链淀粉的聚合度是200~980或相对分子质量范围是32 000~160 000时,包合物的颜色是蓝色。
分支很多的支链淀粉,在支链上的直链平均聚合度20~28,这样形成的包合物是紫色的。
糊精的聚合度更低,显棕红色、红色、淡红色等。
11、对比中学课本上的这个实验步骤,和我们实验指导上的有何不同?中学课本在该实验的第六步添加了与样品2 做对比,课本没有这一步。
注意:加入“稀释1倍的流出液”这一步,目的是防止所取的流出液,由于流速没有控制好的原因,会导致所取的溶液中掺有淀粉,稀释一倍后,加入KI-I2,使更加偏红色,使其与对照组的颜色差异更明显。
二、实验目的1、中学中,在必修一中学习了“酶的作用和本质、酶的特性”,而此实验在选修一《生物技术实践》中出现,为了让同学通过实验来具体的了解酶的作用,化抽象为具象,对酶的作用加深理解;2、了解制备固定化酶的方法—吸附法,让中学生理解固定化酶对淀粉水解的作用;3、理解并掌握实验室中淀粉水解的测定方法;4、进一步掌握运用对照来观察实验结果。
三、实验原理1、淀粉(遇碘显蓝色)→【α-淀粉酶】→糊精(遇碘显红色)→【ß-淀粉酶】→麦芽糖(遇碘不显色)→【糖化淀粉酶】→葡萄糖(遇碘不显色)2、运用吸附法将α-淀粉酶固定在石英砂上。
一定浓度的淀粉溶液经过固定化的α-淀粉酶催化后,生成糊精,使流出液加入KI-I2指示液后呈红色,表明水解产物糊精生成。
3、固定化装置—层析柱四、实验器具和试剂1、α-淀粉酶的固定化及淀粉水解作用的检测试剂盒(α-淀粉酶、石英砂、可溶性淀粉、5mmol/L KI-I2溶液),固定化酶装柱(层析柱),滤布,电炉,水浴锅,50ml烧杯,5ml 试管4支,5ml量筒,胶头滴管,玻璃棒,电子天平,支架。
2、5mol/L KI-I2溶液的配置方法:碘化钾0.83g;蒸馏水100ml;碘0.127g。
先将碘化钾溶于蒸馏水中,待全部溶解后再加碘,振荡溶解。
(注:将此液保存在棕色玻璃瓶内。
)【注意:配置时KI的作用:在三种可溶于水中的卤素单质中碘的溶解度是最小的,不过由于在第四层有空的七个f轨道,这些轨道可以用来容纳其它能够为碘提供电子的原子、离子或原子团,而恰好,碘原子就是那个可以为碘提供电子的供体,每个碘原子可以为一个碘的阴离子提供一个电子,而每个碘的阴离子可以接受两个碘原子的两个电子,形成了一种I3-的原子团,而这种原子团和很多阴离子或酸根一样是可溶于水的,所以间接增加了碘单质在水中的溶解度。
稳定的碘化物(只要能电离出碘离子就可以和碘形成配合物——I3-离子)可以作为碘在水中的助溶剂,而且碘与碘离子不会因为形成I3-离子而使碘失去原有性质与功能是因为碘与碘离子的反应是可逆的(当碘在消耗过程中减少时,I3-离子就会逆过来变成碘离子和碘单质了,碘又变回来,并且随着碘的不断消耗,I3-离子会不断逆向进行直至接近完全分解成碘单质和碘离子,这样碘就不怕因反应而消耗掉了)所以增加碘化钾这类可以提供碘离子的可溶于水的溶质可以增大碘单质在水中的溶解度,否则试验配置的碘溶液浓度即便很小,但对于碘来说可能早就过饱和了,所以增加适量的像碘化钾这样的助溶剂才可得到试验要求的浓度的。
】五、实验步骤【配置→固定→洗→吸附→装柱→洗柱→溶解淀粉过柱→检测】1、配置可溶性淀粉溶液。
(已完成)取可溶性淀粉溶于沸水。
(可溶性淀粉先用冷水调成糊状,再加入沸水中。
这样溶解才会形成澄清的溶液)将配置好的淀粉溶液放置在60℃(酶的最适温度50℃~70℃,使后期淀粉酶经过时能达到酶的最高催化活性)的水浴锅(水浴锅中添加去离子水)中备用。
【此处淀粉浓度配置过低,有待预实验期间调试。
】调试方法:设置淀粉浓度梯度2、α-淀粉酶的固定化。
(材料已称量好,固定15min )在50ml 烧杯中将5mg α-淀粉酶溶于4ml 蒸馏水中。
(注意:由于酶不纯,可能有些不溶物。
)再加入5g 石英砂,不时搅拌(搅拌切忌太用力),固定15min 。
(使酶能吸附到石英砂表面)3、检验未吸附的游离淀粉酶。
(5min )小心倒掉上清液后(未吸附的游离淀粉酶应该在上清液中),用10~15ml 的蒸馏水小心清洗石英砂2~3次,每次取其上清液0.5ml 于试管中,同时滴加淀粉溶液充分混匀。
再加入1滴KI-I2溶液,若溶液变为蓝色,说明上清液中已无游离α-淀粉酶,如果溶液为红色,继续用蒸馏水清洗,直至淀粉溶液变为蓝色为止。
(检验未吸附的游离淀粉酶是否洗涤干净,每次蒸馏水洗涤都可以使未吸附的游离淀粉酶溶于上清液,而游离淀粉酶可以与加入的淀粉溶液反应,产生的糊精遇碘变红。
单纯的淀粉溶液与碘反应会变蓝色。
)4、先把滤布(可以考虑滤纸片,使石英砂不从注射器中漏出)放于固定化酶柱中,再装入有α-淀粉酶的石英砂约4ml ,装柱过程中可在装有石英砂的烧杯中加入少量蒸馏水(便于石英砂流入层析柱),同时适当打开层析柱的调节装置(使多余的液体流出)。
