进口兽药通关单
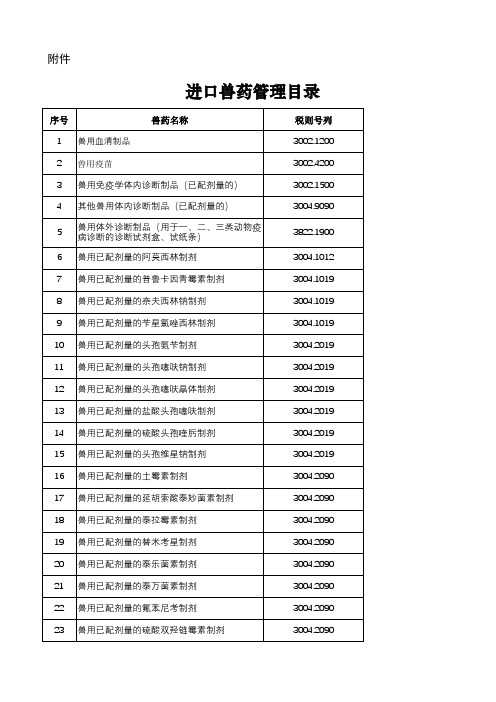
进口兽药管理目录
18 兽用已配剂量的泰拉霉素制剂
19 兽用已配剂量的替米考星制剂
20 兽用已配剂量的泰乐菌素制剂
21 兽用已配剂量的泰万菌素制剂
22 兽用已配剂量的氟苯尼考制剂
23 兽用已配剂量的硫酸双羟链霉素制剂
税则号列 3002.1200 3002.4200 3002.1500 3004.9090
3822.பைடு நூலகம்900
3004.1012 3004.1019 3004.1019 3004.1019 3004.2019 3004.2019 3004.2019 3004.2019 3004.2019 3004.2019 3004.2090 3004.2090 3004.2090 3004.2090 3004.2090 3004.2090 3004.2090 3004.2090
3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090 3004.9090
30049090.84 30049090.84 30049090.84 30049090.84 30049090.84 30049090.84 30049090.84 30049090.84 30049090.84
38089400.40
38089400.40 商品编号仅供通关参考。
课后作业答案

第二章/第三节:我国贸易管制主要措施(五)(有作业)(2014年新版)1、()统一管理、指导全国各发证机构的进出口许可证签发工作。
A.海关总署B.国务院C.商务部D.外汇管理局A B C D标准答案:C答案解析:进出口许可证的主管部门为商务部,故选C。
2、属于进口许可证管理的重点旧机电产品,其进口许可证的签发机构是()。
A.商务部配额许可证事务局B.各地特派员办事处C.自治区、直辖市商务厅D.自治区、直辖市外经贸委A B C D标准答案:A答案解析:商务部配额许可证事务局(简称“许可证局”)负责签发重点旧机电产品的进口许可证,故选A。
3、2014年实行出口许可证管理的商品有48种货物,分别实行出口配额许可证、出口配额招标和出口许可证管理,其中实行出口许可证管理的商品有()。
A.棉花B.原油C.焦炭D.镁砂A B C D标准答案:C答案解析:参考实行出口许可证管理的商品范围相关内容。
AB选项,实行出口配额许可证管理,故不正确;D选项,实行出口配额招标管理,故不正确。
4、进口许可证有效期为(),特殊情况需要跨年度使用的,有效期最长不得超过次年()。
年;3月31日个月;2月底个月;1月31日个月;3月31日A B C D标准答案:A答案解析:参考进口许可证报关规范相关规定。
进口许可证的有效期为1年,特殊情况需跨年度使用时,最长不得超过次年3月31日,故选A。
5、出口许可证的有效期最长不超过(),有效期截止时间不得超过()。
年,当年的12月31日个月,当年的12月31日年,次年的3月31日个月,次年的3月31日A B C D标准答案:B答案解析:出口许可证的有效期不超过6个月,且有效期截止时间不得超过当年12月31日,故选B。
6、进口许可证和出口许可证,如实行“非一批一证”,应在许可证的备注栏打印“非一批一证”字样,有效期内多次使用,但最多不超过()。
次次次次A B C D标准答案:D答案解析:参考进出口许可证报关规范相关规定。
兽药管理条例(2020年修订)-中华人民共和国国务院令第726号

兽药管理条例(2020年修订)正文:----------------------------------------------------------------------------------------------------------------------------------------------------兽药管理条例(2004年4月9日中华人民共和国国务院令第404号公布根据2014年7月29日《国务院关于修改部分行政法规的决定》第一次修订根据2016年2月6日《国务院关于修改部分行政法规的决定》第二次修订根据2020年3月27日《国务院关于修改和废止部分行政法规的决定》第三次修订)第一章总则第一条为了加强兽药管理,保证兽药质量,防治动物疾病,促进养殖业的发展,维护人体健康,制定本条例。
第二条在中华人民共和国境内从事兽药的研制、生产、经营、进出口、使用和监督管理,应当遵守本条例。
第三条国务院兽医行政管理部门负责全国的兽药监督管理工作。
县级以上地方人民政府兽医行政管理部门负责本行政区域内的兽药监督管理工作。
第四条国家实行兽用处方药和非处方药分类管理制度。
兽用处方药和非处方药分类管理的办法和具体实施步骤,由国务院兽医行政管理部门规定。
第五条国家实行兽药储备制度。
发生重大动物疫情、灾情或者其他突发事件时,国务院兽医行政管理部门可以紧急调用国家储备的兽药;必要时,也可以调用国家储备以外的兽药。
第二章新兽药研制第六条国家鼓励研制新兽药,依法保护研制者的合法权益。
第七条研制新兽药,应当具有与研制相适应的场所、仪器设备、专业技术人员、安全管理规范和措施。
研制新兽药,应当进行安全性评价。
从事兽药安全性评价的单位应当遵守国务院兽医行政管理部门制定的兽药非临床研究质量管理规范和兽药临床试验质量管理规范。
省级以上人民政府兽医行政管理部门应当对兽药安全性评价单位是否符合兽药非临床研究质量管理规范和兽药临床试验质量管理规范的要求进行监督检查,并公布监督检查结果。
报关实务——1、2单元综合复习

报关实务——1、2单元综合复习1.某进出口企业进口一批“已配剂量头孢菌素制剂”(同时列入《进口药品目录》和《进口兽药管理目录》),用于治疗畜禽疾病。
该企业向海关申报时应提交()。
[单选题] *A.进口药品通关单B.进口兽药通关单(正确答案)C.进口药品通关单和进口兽药通关单D.进口药品通关单或进口兽药通关单2. 海关管理的四项基本任务是(). *A.监管(正确答案)B.征税(正确答案)C.查缉走私(正确答案)D.编制海关统计(正确答案)3. 下列哪一选项不符合进出口货物收发货人报关行为规则() [单选题] *A.在海关注册登记后,可以在全国各口岸海关办理本单位报关业务B.自行办理报关业务,应当由本单位的报关员向海关办理C.可以委托在海关注册登记的报关企业,由报关企业的报关员代为办理报关业务D.可以接受委托签订进出口合同,并代为办理报关业务(正确答案)4. 我国出入境检验检疫制度内容包括()。
*A.进出口商品检验制度。
(正确答案)B.进出境动植物检疫制度(正确答案)C.国境卫生监督制度(正确答案)D.进出口商品质量公证鉴定制度5. 海关对进出境行李物品的监管原则是(). [单选题] *A.直接需要原则B.自用合理数量原则(正确答案)C.没有限制D.不能超过海关规定6. 报关单位有关登记事项的内容发生变更,应当()。
[单选题] *A.办理变更登记手续(正确答案)B.重新办理注册登记手续C.报关注册注销手续D.不必办理任何手续7. 国家禁止进口()。
*A.犀牛角(正确答案)B.天然砂C.旧服装(正确答案)D.木炭8.发证机关根据企业申请于2018年9月30日向企业签发了自动进口许可证。
该证截至()有效。
[单选题] *A.2018年12月31日(正确答案)B.2019年3月31日C. 2019年6月30日D.2019年9月30日9. 报关企业设立分支机构应当向其分支机构所在地海关提交的备案资料有(). *A.报关单位情况登记表(正确答案)B.报关企业“中华人民共和国海关报关单位注册登记证书”复印件(正确答案)C.分支机构营业执照副本复印件以及组织机构代码证书副本复印件(正确答案)D.报关服务营业场所所有权证明复印件或者使用权证明复印件(正确答案)10. 下述由国家生态环境部签发的进出口许可证件是())。
农业部442号补充公告

中华人民共和国农业部公告(讨论稿)为加强兽药管理,确保兽药安全有效,根据《兽药管理条例》规定,现就兽药注册管理补充规定公告如下:一、拟生产2009年11月30日前公布的进口兽药质量标准中的化学药品(含消毒剂,下同)的和本公告发布后新兽药监测期满(《新兽药注册证书》署名单位除外)化学药品的,实行兽药注册管理,并按下列要求提供资料:(一)申报原料药。
按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册项目中提交有关原料药的综述资料和相关药学研究资料。
(二)申报制剂。
按照“442号公告”中“化学药品注册分类及注册资料要求”提交综述资料、相关药学研究资料和错误!未指定书签。
原料药的合法来源证明文件,证明文件应当包括原料药生产企业资质证明文件(生产许可证、GMP 证书)和销售发票、检验报告、产品标准等资料复印件。
采用进口原料药的,应当提供《进口兽药注册证书》(或《兽药注册证书》)、《进口兽药通关单》、检验报告、兽药质量标准等复印件。
必要时,提供兽药残留消除研究试验资料,注射剂提供过敏性、溶血性和局部刺激性等试验资料。
缓(控)释制剂、混悬型制剂还应当提交血药法生物等效性试验资料,生物等效性试验对照药物应选已批准的同品种产品。
(三)申报抗生素全发酵品种。
申报注册抗生素全发酵品种的企业应具有抗生素发酵生产能力。
应按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”提交综述资料、相关药学研究资料,并提供菌种来源和菌种鉴定资料、标准物质来源及其制备考核方法等研究资料和相关毒理学试验资料。
多组分抗生素类全发酵品种还应提供主要组分及比例的试验数据和资料。
(四)申报在我国仅注册进口兽药制剂但未注册原料药、且国内原料药尚无药品标准或兽药标准的,应同时申报制剂和原料药,并按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册分类第二类要求提供资料。
二、拟生产2009年12月1日后首次公布化学药品进口兽药质量标准的化学药品,对国内原料药有药品或兽药标准的,申报该制剂应按“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册分类第五类要求提供资料。
兽药GSP现场检查操作程序

XX药店管理文件有关规定的要求。
2、依据:《兽药经营质量管理规范》第74、75条,《兽药经营质量管理规范实施细则》第67条。
3、适用范围:适用于企业购进兽药的验收工作。
4、责任:兽药质量验收员、保管员对本程序的实施负责。
5、内容:5.1 保管员收货:5.1.1 保管员依据兽药购进人员所做的“兽药购进记录”和供货单位“随货同行单”对照实物进行核对后收货,并在“兽药购进记录”和供货单位收货单上签章。
所收货的兽药为进口兽药时,应同时对照实物收取加盖有供货单位质量管理部门原印章的该批号兽药的《进口兽药检验报告书》或《进口兽药通关单》、《进口兽药注册证》(《医药产品注册证》或《生物制品进口批件》和《进口药材批件》)的复印件。
5.1.2 保管员应将属购进的兽药放置于待验区,及时通知验收员到场进行验收。
5.2 兽药验收:5.2.1 验收的内容:兽药质量验收包括兽药外观性状的检查和兽药包装、标签、说明书及标识的检查。
5.2.2 验收的标准:5.2.2.1 验收员依据兽药质量标准规定,逐批抽取规定数量的兽药进行外观性状的检查和包装、标签、说明书及标识的检查。
5.2.2.2 验收员依据兽药购进合同所规定的质量条款进行逐批验收。
5.2.2.3 各剂型的外观性状检查验收标准:(依照《中国药典》2000年版附录制剂通则该剂型项下的规定执行)5.2.2.3.1 片剂:检查有无变色、斑点、龟裂、脱壳、掉皮、粘瓶、溶化、发霉、松片、破碎、异物等现象。
①一般压制片:检查有无变色、松片、发霉等现象。
②包衣片(糖衣片、肠溶片、薄膜衣片):检查有无包衣褪色、结晶析出、粘连、粘瓶、脱壳、龟裂、掉皮(衣)、霉变等现象。
③含糖片(口含片等):检查有无溶化粘连及变形等现象。
5.2.2.3.2 胶囊剂:检查有无漏粉、破裂、漏油、粘软变形、粘结等项。
①硬胶囊:检查有无碎裂、漏粉、粘结、粘瓶、霉变等现象,内容物应无吸潮、变色、结块、霉变等异常现象,有色胶囊应检查有无变色现象。
兽药进口管理办法(2022年修订)

兽药进口管理办法(2022年修订)文章属性•【制定机关】农业农村部•【公布日期】2022.01.07•【文号】农业农村部令2022年第1号•【施行日期】2022.01.07•【效力等级】部门规章•【时效性】现行有效•【主题分类】畜牧业正文兽药进口管理办法(2007年7月31日农业部、海关总署令第2号公布,2019年4月25日农业农村部令2019年第2号、2022年1月7日农业农村部令2022年第1号修订)第一章总则第一条为了加强进口兽药的监督管理,规范兽药进口行为,保证进口兽药质量,根据《中华人民共和国海关法》和《兽药管理条例》,制定本办法。
第二条在中华人民共和国境内从事兽药进口、进口兽药的经营和监督管理,应当遵守本办法。
进口兽药实行目录管理。
《进口兽药管理目录》由农业农村部会同海关总署制定、调整并公布。
第三条农业农村部负责全国进口兽药的监督管理工作。
县级以上地方人民政府兽医主管部门负责本行政区域内进口兽药的监督管理工作。
第四条兽药应当从具备检验能力的兽药检验机构所在地口岸进口(以下简称兽药进口口岸)。
兽药检验机构名单由农业农村部确定并公布。
第二章兽药进口申请第五条兽药进口应当办理《进口兽药通关单》。
《进口兽药通关单》由中国境内代理商向兽药进口口岸所在地省级人民政府兽医主管部门申请。
申请时,应当提交下列材料:(一)兽药进口申请表;(二)代理合同(授权书)和购货合同复印件;(三)工商营业执照复印件;兽药生产企业申请进口本企业生产所需原料药的,提交工商营业执照复印件;(四)产品出厂检验报告;(五)装箱单、提运单和货运发票复印件;(六)产品中文标签、说明书式样。
申请兽用生物制品《进口兽药通关单》的,还应当向兽药进口口岸所在地省级人民政府兽医主管部门提交生产企业所在国家(地区)兽药管理部门出具的批签发证明。
第六条兽药进口口岸所在地省级人民政府兽医主管部门应当自收到申请之日起2个工作日内完成审查。
审查合格的,发给《进口兽药通关单》;不合格的,书面通知申请人,并说明理由。
兽药管理规定

兽药管理规定为规范兽药的管理,《兽药管理条例》已经2004年3月24日国务院第45次常务会议通过,下面店铺给大家介绍关于兽药管理规定的相关资料,希望对您有所帮助。
兽药管理规定如下第一章总则第一条为了加强兽药管理,保证兽药质量,防治动物疾病,促进养殖业的发展,维护人体健康,制定本条例。
第二条在中华人民共和国境内从事兽药的研制、生产、经营、进出口、使用和监督管理,应当遵守本条例。
第三条国务院兽医行政管理部门负责全国的兽药监督管理工作。
县级以上地方人民政府兽医行政管理部门负责本行政区域内的兽药监督管理工作。
第四条国家实行兽用处方药和非处方药分类管理制度。
兽用处方药和非处方药分类管理的办法和具体实施步骤,由国务院兽医行政管理部门规定。
第五条国家实行兽药储备制度。
发生重大动物疫情、灾情或者其他突发事件时,国务院兽医行政管理部门可以紧急调用国家储备的兽药;必要时,也可以调用国家储备以外的兽药。
第二章新兽药研制第六条国家鼓励研制新兽药,依法保护研制者的合法权益。
第七条研制新兽药,应当具有与研制相适应的场所、仪器设备、专业技术人员、安全管理规范和措施。
研制新兽药,应当进行安全性评价。
从事兽药安全性评价的单位应当遵守国务院兽医行政管理部门制定的兽药非临床研究质量管理规范和兽药临床试验质量管理规范。
省级以上人民政府兽医行政管理部门应当对兽药安全性评价单位是否符合兽药非临床研究质量管理规范和兽药临床试验质量管理规范的要求进行监督检查,并公布监督检查结果。
第八条研制新兽药,应当在临床试验前向省、自治区、直辖市人民政府兽医行政管理部门提出申请,并附具该新兽药实验室阶段安全性评价报告及其他临床前研究资料;省、自治区、直辖市人民政府兽医行政管理部门应当自收到申请之日起60个工作日内将审查结果书面通知申请人。
研制的新兽药属于生物制品的,应当在临床试验前向国务院兽医行政管理部门提出申请,国务院兽医行政管理部门应当自收到申请之日起60个工作日内将审查结果书面通知申请人。
农业部442号补充公告

中华人民共和国农业部公告(讨论稿)为加强兽药管理,确保兽药安全有效,根据《兽药管理条例》规定,现就兽药注册管理补充规定公告如下:一、拟生产2009年11月30日前公布的进口兽药质量标准中的化学药品(含消毒剂,下同)的和本公告发布后新兽药监测期满(《新兽药注册证书》署名单位除外)化学药品的,实行兽药注册管理,并按下列要求提供资料:(一)申报原料药。
按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册项目中提交有关原料药的综述资料和相关药学研究资料。
(二)申报制剂。
按照“442号公告”中“化学药品注册分类及注册资料要求”提交综述资料、相关药学研究资料和错误!未指定书签。
原料药的合法来源证明文件,证明文件应当包括原料药生产企业资质证明文件(生产许可证、GMP 证书)和销售发票、检验报告、产品标准等资料复印件。
采用进口原料药的,应当提供《进口兽药注册证书》(或《兽药注册证书》)、《进口兽药通关单》、检验报告、兽药质量标准等复印件。
必要时,提供兽药残留消除研究试验资料,注射剂提供过敏性、溶血性和局部刺激性等试验资料。
缓(控)释制剂、混悬型制剂还应当提交血药法生物等效性试验资料,生物等效性试验对照药物应选已批准的同品种产品。
(三)申报抗生素全发酵品种。
申报注册抗生素全发酵品种的企业应具有抗生素发酵生产能力。
应按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”提交综述资料、相关药学研究资料,并提供菌种来源和菌种鉴定资料、标准物质来源及其制备考核方法等研究资料和相关毒理学试验资料。
多组分抗生素类全发酵品种还应提供主要组分及比例的试验数据和资料。
(四)申报在我国仅注册进口兽药制剂但未注册原料药、且国内原料药尚无药品标准或兽药标准的,应同时申报制剂和原料药,并按照“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册分类第二类要求提供资料。
二、拟生产2009年12月1日后首次公布化学药品进口兽药质量标准的化学药品,对国内原料药有药品或兽药标准的,申报该制剂应按“农业部第442号公告”中“化学药品注册分类及注册资料要求”注册分类第五类要求提供资料。
报关水平测试:对外贸易管理、概述

报关水平测试:对外贸易管理、概述1、多选货物.技术进出口许可管理制度是我国进出口许可制度的主体,其管理范围包括A.禁止进出口货物和技术B.限制进出口货物和技术C.自由进出口的技术D.自由进出口中部分实行自动许可管理的货物答案:A, B, C, D2、多选国家外汇管理局对货物外汇的主要监督方式包括()。
A.企业名录登记管理B.非现场核查C.现场核查D.分类管理答案:A, B, C, D3、单选属于自由进出口的技术应当向国务院外经贸主管部门办理登记,国务院外经贸主管部门应当自收到规定的文件之日起()个工作日内对技术进口合同进行登记,颁发技术进出口合同登记证。
A.2B.3C.5D.7答案:B4、单选“农药进出口登记管理放行通知单”实行“一批一证”制,证面内容不得更改,如需更改应在有效期内将原证交回(),并重新办理新证。
A.商务部B.林业局农药检定所C.农业部农药检定所D.出入境检验检疫局答案:C5、单选临时反倾销措施实施的期限,自临时反倾销措施决定公告规定实施之日起,不超过()个月,特殊情况,可以延长至()个月。
A.6,12B.5,8C.4,9D.3,6答案:C6、单选某进出口企业进口一批“已配剂量头孢菌素制剂”(同时列入《进口药品目录》和《进口兽药管理目录》),用于治疗畜禽疾病,该企业向海关申报时应提交()。
A.进口药品通关单B.进口兽药通关单C.进口药品通关单和进口兽药通关单D.进口药品通关单或进口兽药通关单答案:B7、判断题病毒的生理小种称作株系。
答案:对8、判断题任何单位以任何方式进出口列入《麻醉药品管制品种目录》的药品,不论何种用途,均须取得国家食品药品监督管理局核发的《麻醉药品进出口准许证》,《麻醉药品进出口准许证》实行“非一批一证”制度。
()答案:错9、单选反补贴.反倾销针对()不公平贸易而采取的措施。
A.进口产品激增的情况B.价格歧视C.国别歧视D.数量答案:B10、单选进口许可证有效期为(),特殊情况需要跨年度使用的,有效期最长不得超过次年()。
兽药进口管理办法

兽药进口管理办法《兽药进口管理办法》(农业部令第2号)来源:农业部作者:日期: 06月08日第一章总则第一条为了加强进口兽药的监督管理,规范兽药进口行为,保证进口兽药质量,根据《中华人民共和国海关法》和《兽药管理条例》,制定本办法。
第二条在中华人民共和国境内从事兽药进口、进口兽药的经营和监督管理,应当遵守本办法。
进口兽药实行目录管理。
《进口兽药管理目录》由农业部会同海关总署制定、调整并公布。
第三条农业部负责全国进口兽药的监督管理工作。
县级以上地方人民政府兽医行政管理部门负责本行政区域内进口兽药的监督管理工作。
第四条兽药应当从具备检验能力的兽药检验机构所在地口岸进口(以下简称兽药进口口岸)。
兽药检验机构名单由农业部确定并公布。
第二章兽药进口申请第五条兽药进口应当办理《进口兽药通关单》。
《进口兽药通关单》由中国境内代理商向兽药进口口岸所在地省级人民政府兽医行政管理部门申请。
申请时,应当提交下列材料(普通兽药进口《进口兽药通关单》申请应提交的材料):(一)兽药进口申请表;(二)代理合同(授权书)和购货合同复印件;(三)《兽药经营许可证》、工商营业执照复印件;兽药生产企业申请进口本企业生产所需原料药的,提交《兽药生产许可证》、工商营业执照及其所生产产品的批准文号证明文件复印件;(四)《进口兽药注册证书》复印件;生产企业为港、澳、台企业的,提交《兽药注册证书》复印件;(五)产品出厂检验报告;(六)装箱单、提运单和货运发票复印件;(七)产品中文标签、说明书式样。
申请兽用生物制品《进口兽药通关单》的,还应当向兽药进口口岸所在地省级人民政府兽医行政管理部门提交下列材料(兽用生物制品《进口兽药通关单》的申请):(一)农业部依据本办法第七条核发的兽用生物制品进口许可证复印件;(二)生产企业所在国家(地区)兽药管理部门出具的批签发证明。
第六条兽药进口口岸所在地省级人民政府兽医行政管理部门应当自收到申请之日起2个工作日内完成审查。
中华人民共和国农业农村部公告第97号——关于兽药严重违法行为从重处罚情形的公告

中华人民共和国农业农村部公告第97号——关于兽药严重违法行为从重处罚情形的公告文章属性•【制定机关】农业农村部•【公布日期】2018.12.04•【文号】中华人民共和国农业农村部公告第97号•【施行日期】2018.12.04•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】畜牧业正文中华人民共和国农业农村部公告第97号为加强兽药管理,严厉打击兽药违法行为,保障动物产品质量安全,根据《兽药管理条例》有关规定,现就兽药严重违法行为从重处罚情形,公告如下。
一、无兽药生产许可证生产兽药,有下列情形之一的,按照《兽药管理条例》第五十六条“情节严重的”规定处理,按上限罚款,并没收生产设备:(一)生产的兽药添加国家禁止使用的药品和其他化合物,或添加人用药品等农业农村部未批准使用的其他成分的;(二)生产的兽药累计2批次以上或货值金额2万元以上的;(三)生产兽用疫苗的;(四)其他情节严重的情形。
二、持有兽药生产、经营许可证的兽药生产、经营者有下列情形之一的,按照《兽药管理条例》第五十六条“情节严重的”规定处理,按上限罚款,并吊销兽药生产、经营许可证:(一)生产的兽药添加国家禁止使用的药品和其他化合物,或添加人用药品等农业农村部未批准使用的其他成分的;(二)生产的兽药擅自改变组方添加其他兽药成分累计2批次以上的;(三)生产未取得兽药产品批准文号兽用疫苗的,或生产未取得兽药产品批准文号的其他兽药产品累计2批次以上的;(四)生产兽用疫苗擅自更换菌(毒、虫)种,或者非法添加其他菌(毒、虫)种的;(五)生产主要成分含量在国家标准上限150%以上或下限50%以下的劣兽药累计3个品种以上或5批次以上的;(六)生产的兽用疫苗未经批签发或批签发不合格即销售累计2批次以上的;(七)生产假兽药货值金额5万元以上的;(八)兽药经营者未审核并保存兽药批准证明文件材料以及购买凭证,经营假、劣兽药货值金额2万元以上的。
三、持有兽药生产、经营许可证的兽药生产、经营者有下列情形之一的,按照《兽药管理条例》第五十九条“情节严重的”规定处理,吊销兽药生产、经营许可证:(一)兽药生产者未在批准的兽药GMP车间生产兽药累计2批次以上的;(二)未在批准的生产线生产兽药累计2批次以上的;(三)兽药出厂前未按规定进行质量检验,或检验不合格即出厂销售累计5批次以上的;(四)无兽药生产、检验记录或编造、伪造生产、检验记录累计3批次以上的;(五)编造、伪造兽用疫苗批签发材料累计3批次以上的;(六)监督检查和飞行检查发现兽药生产者有2个以上关键项不符合兽药GMP要求的。
进口药品通关单申请事项办理

进口药品通关单申请事项办理1、申请条件(1)从相应海关所辖口岸进口(2)报验单位的资格:报验单位应当是持有《药品经营许可证》的独立法人;药品生产企业进口本企业所需原料药和制剂中间体(包括境内分包装用制剂),应当持有《药品生产许可证》。
(3)进口药品不属于《药品进口管理办法》第十条规定情形的药品2、申请材料办理药品进口备案时应提交的材料:办理进口备案的单位,应当填写《进口药品报验单》,持《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)原件,进口麻醉药品、精神药品还应当持麻醉药品、精神药品《进口准许证》原件,向所在地口岸药品监督管理局报送所进口品种的有关资料一式两份:(一)《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)复印件;(二)报验单位的《药品经营许可证》和《企业法人营业执照》复印件;药品生产企业自行进口本企业生产所需原料药和制剂中间体的进口备案时应提交《药品生产许可证》和《企业法人营业执照》复印件。
(三)原产地证明复印件;(四)购货合同复印件;(五)装箱单、提运单和货运发票复印件;(六)出厂检验报告书复印件;(七)药品说明书及包装、标签的式样(原料药和制剂中间体除外);(八)国家食品药品监督管理局规定批签发的生物制品,需要提供生产检定记录摘要及生产国或者地区药品管理机构出具的批签发证明原件;(九)《药品进口管理办法》第十条规定情形以外的药品,应当提交最近一次《进口药品检验报告书》和《进口药品通关单》复印件。
经其他国家或者地区转口的进口药品,需要同时提交从原产地到各转口地的全部购货合同、装箱单、提运单和货运发票等。
上述各类复印件应当加盖进口单位公章。
3、有关材料的要求根据《药品进口管理办法》和国家有关文件的精神,各企业申请办理《进口药品通关单》时提交的材料应符合如下要求:(一)《药品进口报验单》填写《药品进口报验单》时,请使用《药品进口报验系统》,将磁盘和打印出来的文件一起送口岸药监局。
监管证件代码表2010年

监管证件代码表2010年监管证件名称代码表说明一、定义监管证件名称代码是海关依据我国外贸法律、法规及规章,为便于实施计算机系统管理和便捷通关需求,对实行进出口许可证件管理的货物在海关管理环节须验核的各种进出口许可证件的分类标识。
其总和称为监管证件名称代码表。
二、《监管证件名称代码表》结构《监管证件名称代码表》由两部分组成,即监管证件代码和监管证件名称。
例如:代码“1”,为进口许可证,如果某一商品编号后注有监管证件“1”,则说明在一般贸易项下进口该种商品需申领进口许可证。
三、监管证件名称代码说明(一)代码“1”--进口许可证:指商务部配额许可证事务局或其授权机关签发的进口许可证。
(二)代码“2”---两用物项和技术进口许可证:指列入《两用物项和技术进口许可证管理目录》的商品,进口时由商务部签发的《两用物项和技术进口许可证》。
(三)代码“3”--两用物项和技术出口许可证:根据商务部会同海关总署联合发布《敏感物项和技术出口许可证暂行管理办法》及《敏感物项和技术出口许可证管理目录》,凭商务部签发的敏感物项和技术出口批复到商务部授权的发证机构领取敏感物项和技术出口许可证。
(四)代码“4”--出口许可证:指商务部配额许可证事务局或其授权机关签发的出口许可证。
(五)代码“6”--旧机电产品禁止进口:商品编码后面有此代码的商品, 其旧品禁止进口。
(六)代码“7”--自动进口许可证或重要工业品证明:指进口商品实行自动进口许可管理,由商务部和国家经贸委及其授权机构按职责分工签发自动进口许可证或重要工业品自动进口许可证明。
(七)代码“8”--禁止出口商品:指国务院授权商务部门会同有关部门,依照《中华人民共和国对外贸易法》等有关法律法规,制定、调整并公布的禁止出口货物目录所列商品。
商品编码后有此代码的商品禁止出口。
(八)代码“9”--禁止进口商品:指国务院授权商务部门会同有关部门,依照《中华人民共和国对外贸易法》等有关法律法规,制定、调整并公布的禁止进口货物目录所列商品。
兽药管理条例及实施细则

兽药管理条例(全文)中华人民共和国国务院令第404号《兽药管理条例》已经2004年3月24日国务院第45次常务会议通过,现予公布,自2004年11月1日起施行。
总理温家宝二00四年四月九日兽药管理条例(全文)第一章总则第一条为了加强兽药管理,保证兽药质量,防治动物疾病,促进养殖业的发展,维护人体健康,制定本条例。
第二条在中华人民共和国境内从事兽药的研制、生产、经营、进出口、使用和监督管理,应当遵守本条例。
第三条国务院兽医行政管理部门负责全国的兽药监督管理工作。
县级以上地方人民政府兽医行政管理部门负责本行政区域内的兽药监督管理工作。
第四条国家实行兽用处方药和非处方药分类管理制度。
兽用处方药和非处方药分类管理的办法和具体实施步骤,由国务院兽医行政管理部门规定。
第五条国家实行兽药储备制度。
发生重大动物疫情、灾情或者其他突发事件时,国务院兽医行政管理部门可以紧急调用国家储备的兽药;必要时,也可以调用国家储备以外的兽药。
第二章新兽药研制第六条国家鼓励研制新兽药,依法保护研制者的合法权益。
第七条研制新兽药,应当具有与研制相适应的场所、仪器设备、专业技术人员、安全管理规范和措施。
研制新兽药,应当进行安全性评价。
从事兽药安全性评价的单位,应当经国务院兽医行政管理部门认定,并遵守兽药非临床研究质量管理规范和兽药临床试验质量管理规范。
第八条研制新兽药,应当在临床试验前向省、自治区、直辖市人民政府兽医行政管理部门提出申请,并附具该新兽药实验室阶段安全性评价报告及其他临床前研究资料;省、自治区、直辖市人民政府兽医行政管理部门应当自收到申请之日起60个工作日内将审查结果书面通知申请人。
研制的新兽药属于生物制品的,应当在临床试验前向国务院兽医行政管理部门提出申请,国务院兽医行政管理部门应当自收到申请之日起60个工作日内将审查结果书面通知申请人。
研制新兽药需要使用一类病原微生物的,还应当具备国务院兽医行政管理部门规定的条件,并在实验室阶段前报国务院兽医行政管理部门批准。
兽药采购管理文件

兽药购进的管理程序一、目的:制定进货程序,确保购进的兽药符合质量要求。
二、适用范围:适用于兽药购进的全过程。
三、责任人:经营部负责人、质检负责人四、正文:1、质检负责人对供货企业的法定资格、质量信誉以及供货单位销售人员的合法身份进行调查审核。
GSP要求企业购进兽药时必须严把质量关,审核供货单位的合法性和购入兽药的合法性,并确保按照兽购进质量管理的规定组织采购活动。
同时,要对和本企业进行业务联系的供货单位销售人员,进行合法资格的验证。
索取并审核供货企业的合法证照,审核时应对供货方《兽药经营许可证》和《营业执照》核准的经营方式、经营范围严格把关,确保购进进行为和购进兽药的合法性。
同时,质检负责人负责向购货单位索取供货单位销售员的有关证明资料,并进行合法性资格审核,对供货方销售人员应建立相应的档案,并对其经营行为及身份的合法性实行动态的监督审核,对不再具备合法资格的销售人员应及时采取有效措施,停止业务往来。
质检负责人将审核结果报告经营部领导,最后确定。
审核资料的主要内容;①供货企业证照复印件。
审核《兽药经营(生产)许可证》和“营业执照”核准的经营方式与经营范围与销售员的经营行为是否相符;②兽药销售员身份证;供货企业法定代表人授权委托书,授权委托书应加盖供货企业原印章,其法定代表人应加盖印章或签字,并明确授权经营活动范围或经营品种,标明有效期限。
2、质检人员要对所购入兽药的合法性和质量可靠性进行严格审核,并对与本经营部有业务联系的供货单位销售人员合法身份进行验证。
购进的兽药应符合以下基本条件,以确保其合法性:⑴、合法企业所生产或经营的兽药;⑵、具有法定的质量标准,即国家兽药标准;⑶、应有法定的批准文号和生产批号;⑷、进口兽药应有符合规定的、加盖了供货单位质量管理机构原印章的《进兽药注册证》和《进口兽药检验报告》或《进口兽药通关单》的复印件;3、经营部销售人员要对首营兽药品种,填写“首次经营兽药审批表”,并经经营部领导审核批准;4、经双方协商一致后,经营部领导要与购货单位签订有明确质量条款的购销合同。
进口兽药管理目录

30043900.40
包括零售包装
38
兽用已配剂量的烯丙孕素制剂
3004.3900
30043900.40
包括零售包装
39
兽用已配剂量的吡虫啉制剂
3004.4900
30044900.80
包括零售包装
40
兽用已配剂量的磺胺嘧啶制剂
3004.9010
30049010.10
包括零售包装
41
30049090.84
包括零售包装
64
兽用已配剂量的盐酸替来他明制剂
3004.9090
30049090.84
包括零售包装
65
兽用已配剂量的盐酸阿替美唑制剂
3004.9090
30049090.84
包括零售包装
66
兽用已配剂量的枸橼酸马罗匹坦制剂
3004.9090
30049090.84
包括零售包装
67
兽用已配剂量的西米考昔制剂
3004.2090
30042090.20
包括零售包装
16
兽用已配剂量的泰拉霉素制剂
3004.2090
30042090.20
包括零售包装
17
兽用已配剂量的替米考星制剂
3004.2090
30042090.20
包括零售包装
18
兽用已配剂量的泰乐菌素制剂
3004.2090
30042090.20
包括零售包装
19
3004.2090
30042090.20
包括零售包装
27
兽用已配剂量的拉沙洛西钠制剂
3004.2090
30042090.20
包括零售包装
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
申 请 单 位(盖章):
申 请 日 期:年月日
受 理 日 期:年月日
中华人民共和国农业部制
填 表 说 明
1. 本表须用黑色钢笔、签字笔填写,也可以自制,用A4纸打印,一式二份。字迹不清、项目填写不全者不予受理。
2. 本表1~5栏由申请单位填写、提供资料。
3. 6~8栏由农业部填写。
4. 本表签章复印件无效。
申请编号:
1.申请单位资料
名联系电话
2.进口性质
3.进口日期
4.进口口岸
5.进口兽药资料
兽药名称
(中英文)
规格
单位
数量
生产厂(公司)(中英文)
进口兽药注册证书号
6.行政审批意见
审核: 审批:
盖章 年 月 日
7.有效期
自 年 月 日至 年 月 日
8.备注
