LZ L 微粒污染检验记录
4、医疗器械微粒污染及纯化水检验

(三)注射用水:是指纯化水经蒸馏法或超滤法制备 的同等要求的水。 (四)灭菌注射用水主要用于药品生产企业,医疗器 械行业不涉及。 蒸馏水:即采用特殊设计的蒸馏器以饮用水为原水用 蒸馏法制备的纯化水。 去离子水:为采用离子交换法、反渗透法、超滤法等 非热处理制备的纯化水。即去离子水是指除去了呈 离子形式杂质后的纯化水。
微粒污染
步骤:取60mL冲洗液,使其在1m 静压头下,经药 液过滤器流入洁净的计数器的样品池中,即得洗脱 液。对样品池内洗脱液中≥5μm 的粒子量(个/mL)报告结果。
微粒污染
YY 0451-2003一次性使用输注泵 标准要求:管路与储液囊内15μm~25μm的 微粒数不应超过1.00个/mL,大于25μm的微 粒数不应超过0.50个/mL。 原理:通过冲洗输注泵内腔液体通道表面, 收集滤膜上的微粒, 并用显微镜进行计数。 可采用与本附录等效的试验方法,如采用微 粒计数仪法代替显微镜法对微粒计数。
纯化水检测
亚硝酸盐:取本品10mL,置纳氏管中,加对氨 基苯磺酰胺的稀盐酸溶液( 1→100 ) 1mL 与盐 酸萘乙二胺溶液( 0.1→100 ) 1mL ,产生的粉 红色,与标准亚硝酸盐溶液[取亚硝酸钠 0.750g(按干燥品计算),加水溶解,稀释至 100mL , 摇 匀 , 精 密 量 取 1mL , 加 水 稀 释 成 100mL ,摇匀,再精密量取 1mL ,加水稀释成 50mL , 摇 匀 , 即 得 ( 每 1mL 相 当 于 1μgNO2 ) ]0.2mL ,加无亚硝酸盐的水 9.8mL , 用同一方法处理后的颜色比较,不得更深 (0.000 002%)。
工艺用水定义: 在医疗器械生产过程中,根据不同的工序及 质量要求,所用的不同要求的水的总称。依据 《中华人民共和国药典》规定,工艺用水包括 饮用水、纯化水、注射用水和灭菌注射用水。
尘埃粒子检测记录
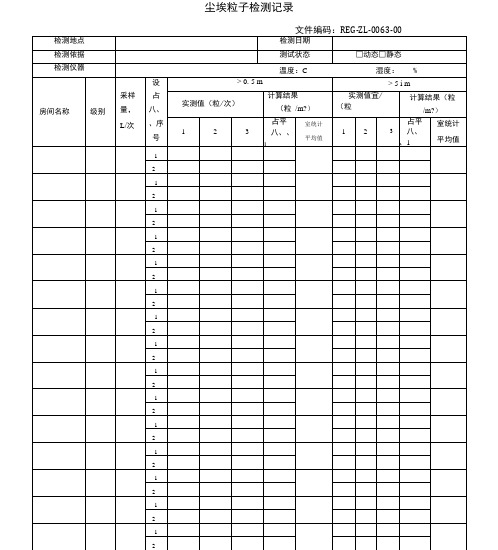
尘埃粒子检测记录
文件编码:REG-ZL-0063-00
检测地点
检测日期
检测依据
测试状态
□动态□静态
检测仪器
温度:C湿度: %
房间名称
级别ቤተ መጻሕፍቲ ባይዱ
釆样 量,
L/次
设
占
八、
、序
号
>0.5m
> 5i m
实测值(粒/次)
计算结果
(粒/m?)
实测值宜/
(粒
计算结果(粒
/m?)
1
2
3
占平
八、、
1
室统计
平均值
1
2
3
占平 八、
、1
室统计
平均值
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
1
2
续表:
1
2
1
2
1
2
1
2
1
2
1
2
计算公式:
C
C
C
1•点平均值:A1
2
1,式中,
Cl一一某一釆样点的粒子浓度(1=1 , 2……,N),粒/ml N—
—某一釆样点上
N
的采样次数,次
A
A
A
2.室统计平均值:UCL二M+tX
Se,式中,M
悬浮粒子测试记录2

上海庆宇药业潢川有限公司洁净区悬浮粒子检测记录编号:SOP09-134(a)-00 取样一更室(C级)尘埃粒子测定取样位置、测试结果:房间面积:1.9 m2 取样点数:2 采样量:升 /次测试依据:GB/T 16292—2010温度:相对湿度:测试日期:报告日期:测试状态:□静态a:空气净化系统开启正常运 min(要求:30 min)后开始测试。
□静态b:生产操作人员撤离现场并经过 min(要求:20 min)自净后开始测试。
□动态:生产开始的时间,测试时间。
测试方法与步骤:按房间面积,本室采样点个,将仪器(名称:激光尘埃粒子计数器;型号:Y09-310;编号:)放置采样点处,采样管口朝向气流方向,采样管口离地面米处高度的水平面上,开机预热稳定后,开始采样。
采样点布局如下:北·1 ·2东测定值警戒值纠偏值标准≥0.5µm (个/m3)≥5.0µm (个/m3)结论:本洁净室按照GB/T 16292—2010 要求测试,悬浮粒子测试结果规定。
复核人员:测试人员:洁净区悬浮粒子检测记录编号:SOP09-134(a)-00取样二更室(C级)尘埃粒子测定取样位置、测试结果:房间面积:1.3m2 取样点数:2 采样量:升 /次测试依据:GB/T 16292—2010温度:相对湿度:测试日期:报告日期:测试状态:□静态a:空气净化系统开启正常运 min(要求:30 min)后开始测试。
□静态b:生产操作人员撤离现场并经过 min(要求:20 min)自净后开始测试。
□动态:生产开始的时间,测试时间。
测试方法与步骤:按房间面积,本室采样点个,将仪器(名称:激光尘埃粒子计数器;型号:Y09-310;编号:)放置采样点处,采样管口朝向气流方向,采样管口离地面米处高度的水平面上,开机预热稳定后,开始采样。
采样点布局如下:北·1 ·2东测定值警戒值纠偏值标准≥0.5µm (个/m3)≥5.0µm (个/m3)结论:本洁净室按照GB/T 16292—2010 要求测试,悬浮粒子测试结果规定。
车间悬浮粒子检测记录

2
C1
C2
L (总采样点)
车间悬浮粒子检测记录
生产开始时间
粒径: 仪器有效期至 ≥5.0μ
粒径:≥0.5μm
均值 (A)
均值的均值 (M)
UCL (粒/m3)
监测频 次洁净度 级别
均值 (A)
1次/季 三十万级
QMR-080-00 测试状态 检测依据 YY0033-2000
粒径:≥5.0μm
均值的均值 (M)
UCL (粒/m3)
结论
C3 C4 C5 C6 C7 C8 C9 C10 C11 C12
C13
M(粒 /m3)
结论
A-某 采样
(粒
Mt-9-平5%
置 UC信L-
平均
复核人
/日
ANGGU
嘉兴康谷医用材料有限公司
检测日期 技术指检标测: 仪器 粒径:≥
检测地点
洗衣间
室内人 数
洗周转箱间
洗手间
更衣室
洁具间
检测地点 室内人数 粒径μm
全自动口 罩机车间
结果计算:
UCL=M + t×
≥0.5 ≥5.0 A1+A2+ M=
检测人/ 日期:
检测时间 仪器型号
采样点
1
2
1
2
1
2
1
2
1
尘埃粒子检测记录[整理版]
![尘埃粒子检测记录[整理版]](https://img.taocdn.com/s3/m/f889a819bb1aa8114431b90d6c85ec3a87c28b23.png)
尘埃粒子检测记录00JL-ZL-08-00000测试部门:测试日期:静压差:相对湿度:温度:000测试状态:检验依据:000房间名称净化级别面积(m2)采样点粒径(um)记录器数据(采样点A,粒/2.83L)记录器数据(采样点B,粒/2.83L)平均值的均值粒/2.83L粒子浓度(粒/m3)UCL标准(粒/m3)1 2 3平均值1 2 3平均值女一更室 D级<10 2≥0.5 ≤3520000≥5 ≤29000女二更室 D级<10 2≥0.5 ≤3520000≥5 ≤29000男更室 D级<10 2 ≥0.5 ≤3520000 ≥5 ≤29000男一更室 D级<10 2≥0.5 ≤3520000≥5 ≤29000男二室 D级<10 2 ≥0.5 ≤3520000 ≥5 ≤29000气闸室 D级<10 2 ≥0.5 ≤3520000 ≥5 ≤29000中控室 D级<10 2 ≥0.5 ≤3520000≥5≤29000灌装室 D级<40 2 ≥0.5 ≤3520000 ≥5≤29000洗烘室 D级<1002≥0.5 ≤3520000≥5≤29000配液室 D级<40 2 ≥0.5 ≤3520000 ≥5≤29000容器存放间 D级<10 2≥0.5 ≤3520000≥5≤29000容器清洗间 D级<10 2≥0.5 ≤3520000≥5≤29000称量间 D级<10 2 ≥0.5 ≤3520000 ≥5≤29000活性炭称量间 D级<10 2≥0.5 ≤3520000≥5≤29000活性炭暂存 D级<10 2≥0.5 ≤3520000≥5≤29000原辅料暂存 D级<40 2≥0.5 ≤3520000≥5≤29000缓冲装盘 D级<10 2≥0.5 ≤3520000≥5≤29000洁具存放间 D级<10 2≥0.5 ≤3520000≥5≤29000洁具清洗间 D级<10 2≥0.5 ≤3520000≥5≤29000消毒液配制室 D级<10 2≥0.5 ≤3520000≥5≤29000废弃物出口 D级<102 ≥0.5 ≤3520000≥5≤29000洁净走廊 D级<1002 ≥0.5 ≤3520000 ≥5≤29000结果判断____________________________________________ 检查人:复核人:000尘埃粒子检测记录00JL-ZL-08-00000测试部门:测试日期:静压差:相对湿度:温度:000测试状态:检验依据:000房间名称净化级别面积(m2)采样点粒径(um)记录器数据(采样点A,粒/2.83L)记录器数据(采样点B,粒/2.83L)平均值的均值粒/2.83L粒子浓度(粒/m3)UCL标准(粒/m3)1 2 3平均值1 2 3平均值微生物限度室 C级<10 2≥0.5 ≤352000≥5 ≤2900无菌检验室 C级<10 2≥0.5 ≤352000≥5 ≤2900阳性菌室C级<10 2 ≥0.5 ≤352000 ≥5 ≤2900阳性菌室超净工作台 A级<10 2≥0.5 ≤3520≥5 ≤20微生物限度室超净工作台A级<10 2≥0.5 ≤3520≥5 ≤20结果判断____________________________________________ 检查人:复核人:000。
检测记录(参数寻找阶段)

产品名称
清洗参数
检测标准
检测结果
显影环
75%乙醇超声清洗10min
电导率≤2.1us/cm
75%乙醇超声清洗15min
75%乙醇超声清洗20min
检验人/日期:审核人/日期:
擦拭试验检测记录
验证目的:确认清洗后产品的擦拭试验能够达到标准要求。
验证要求:应无可见污渍
验证依据:《医疗器械清洗过程确认检查要点指南》2016版
验证方法:在300lx~700lx照度下目测。
检测记录如下:
产品名称
清洗参数
检测标准
检测结果
接头、应变套管、盘管
纯化水超声清洗10min
应当无明显油脂、焊剂、焊渣、热处理或热成型氧化皮、灰尘、垃圾、金属或磨料颗粒和废屑,无明显损伤。
纯化水超声清洗15min
纯化水超声清洗20min
检验人/日期:审核人/日期:
验证(操作)人员姓名:陈浩、陶忠、李昭、梁曦、许平
验证方法:详见《产品初始污染菌检验作业指导书》。
检测记录如下:
产品名称
清洗参数
检测标准
检测结果
显影环
75%乙醇超声清洗10min
≤10cfu/件次
75%乙醇超声清洗15min
75%乙醇超声清洗20min
空白
检验人/日期:审核人/日期:
pH值检验记录
验证目的:确认清洗后显影环的pH值能够达到标准要求。
外观检验记录
验证目的:确认清洗后保护套管的外观能够达到标准要求。
验证要求:应当无明显油脂、焊剂、焊渣、热处理或热成型氧化皮、灰尘、垃圾、金属或磨料颗粒和废屑,无明显损伤。
验证依据:《医疗器械清洗过程确认检查要点指南》2016版;
洁净室悬浮粒子测试记录,输入数目,自动换算平均值,偏差。QA必备
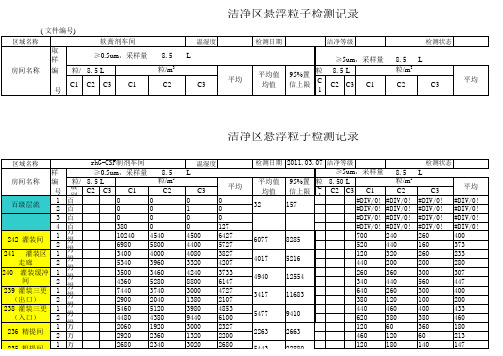
9160 5156 4146 13536 7146 2578 2143 3241 2631 1435 3691 43575
280 140 220 120 80 300 320 260 160 220 180 280 380 320 240 300 80 260 120 220 60 180 340
180 200 60 160 280 860 60 380 100 360 60 60 40 160 120 60 0 100 0 210 147 160 150 80 100 127 346
718 193 350 1177 946 483 286 297 374 310 674 807
13:24:00 10:24:00 10:33:00 10:43:00 10:52:00 11:04:00 11:12:00 11:21:00 11:31:00 11:40:00 11:50:00 10:03:00
万级 十万级 十万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级 万级
5660 2220 1220 1360 1960 4920 3100 3240 2140 1980 1760 2520 2360 2580 2120 2320 820 2100 2160 2140 920 29400 36340
8.5 3 粒/m C2 0 0 0 0 4540 5800 4000 3960 3460 5280 3740 2040 5120 4380 1920 2360 2340 5860 3420
L C3 0 1 0 0 4500 4400 4080 3320 4240 8800 3000 1380 3980 9440 3000 1320 3020 14440 5360 平均 0 0 0 127 6427 5727 3827 4207 3733 6147 4727 2107 4853 6100 2327 2200 2680 8207 4433
悬浮粒子记录表1

XXXX有限公司悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤3500000/m3 , ≥5.0um粒子数≤20000/m3测试单位:塑瓶输液车间、仓库洁净度级别:十万级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:XXXX有限公司悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:1)≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3(万级)2)≥0.5um粒子数≤3500/m3 , ≥5.0um粒子数0 (局部百级)测试单位:塑瓶输液车间洁净度级别:万级(局部百级)测试状态:静态测试日期:报告日期:检验人:复核人:室主任:XXXX有限公司悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:1)≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3(万级)2)≥0.5um粒子数≤3500/m3 , ≥5.0um粒子数0(局部百级)测试单位:中心化验室洁净度级别:万级(局部百级)测试状态:静态测试日期:报告日期:检验人:复核人:室主任:悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤3500/m3 , ≥5.0um粒子数≤0/m3测试单位:软袋二车间洁净度级别:百级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3测试单位:软袋二车间洁净度级别:万级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3测试单位:软袋二车间洁净度级别:万级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3测试单位:软袋二车间洁净度级别:万级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:XXXX有限公司悬浮粒子检验记录测试依据:《中华人民共和国国家标准》(GB/T16292~16294-1996)评定标准:≥0.5um粒子数≤350000/m3 , ≥5.0um粒子数≤2000/m3测试单位:软袋二车间洁净度级别:万级测试状态:静态测试日期:报告日期:检验人:复核人:室主任:。
空气污染检测记录

空气污染检测记录空气污染是当今社会普遍存在的环境问题之一,严重影响人类健康和生活质量。
为了有效监测和掌握空气质量状况,不少地区和国家开展了空气污染检测工作。
以下是一份空气污染检测记录。
日期:2024年5月1日地点:城市市中心天气状况:晴朗,无风检测仪器:空气质量监测站记录如下:8:00 am:空气温度:22°C相对湿度:68%二氧化硫(SO2)浓度:10μg/m³二氧化氮(NO2)浓度:20μg/m³可吸入颗粒物(PM10)浓度:50μg/m³可入肺颗粒物(PM2.5)浓度:30μg/m³臭氧(O3)浓度:50μg/m³11:00 am:空气温度:25°C相对湿度:60%二氧化硫(SO2)浓度:12μg/m³二氧化氮(NO2)浓度:25μg/m³可吸入颗粒物(PM10)浓度:55μg/m³可入肺颗粒物(PM2.5)浓度:35μg/m³臭氧(O3)浓度:45μg/m³2:00 pm:空气温度:28°C相对湿度:55%二氧化硫(SO2)浓度:15μg/m³二氧化氮(NO2)浓度:30μg/m³可吸入颗粒物(PM10)浓度:60μg/m³可入肺颗粒物(PM2.5)浓度:40μg/m³臭氧(O3)浓度:40μg/m³5:00 pm:空气温度:26°C相对湿度:65%二氧化硫(SO2)浓度:14μg/m³二氧化氮(NO2)浓度:28μg/m³可吸入颗粒物(PM10)浓度:52μg/m³可入肺颗粒物(PM2.5)浓度:38μg/m³臭氧(O3)浓度:48μg/m³8:00 pm:空气温度:23°C相对湿度:70%二氧化硫(SO2)浓度:13μg/m³二氧化氮(NO2)浓度:26μg/m³可吸入颗粒物(PM10)浓度:48μg/m³可入肺颗粒物(PM2.5)浓度:36μg/m³臭氧(O3)浓度:55μg/m³根据以上记录,可以看出该城市5月1日的空气质量相对较好。
微粒测试检验报告模板

微粒测试检验报告模板
1. 背景介绍
这个部分提供对测试的背景和目的的简要介绍。
2. 测试目标
明确测试的目标,例如,检验样品中的微粒浓度是否符合标准要求。
3. 测试方法
描述测试所采用的方法和步骤。
3.1 样品采集
详细说明样品的采集方法、时间和地点。
3.2 实验设备
列出实验所使用的设备和仪器。
3.3 测试步骤
按照以下步骤进行测试:
- 步骤1:准备样品和实验设备。
- 步骤2:校准设备,确保其准确性。
- 步骤3:按照标准测试方法进行测试。
- 步骤4:记录测试数据。
4. 运行结果
提供测试的详细结果,包括数值数据和图表。
4.1 数据分析
对测试数据进行分析和描述,并与标准规定的要求进行对比。
4.2 结果图表
将测试结果以图表的形式展示,使其更加直观和易于理解。
5. 结论
对测试的结果进行总结和评估。
6. 建议与改进
提出对于测试方法的建议和改进措施。
7. 参考资料
列出测试中使用到的参考资料。
8. 附录
提供测试中使用到的相关文档、标准和数据表格等。
以上是一份微粒测试检验报告的模板,根据具体情况进行调整和填写。
希望对你的工作有所帮助!。
产品微粒污染检测规程

医疗器材有限公司企业标准QB REV产品微粒污染检测规程编制审核批准签字日期分发部门发布实施产品微粒污染检测规程1.目的控制产品中的微粒数量,保证产品的质量。
2.范围生物部生产的生物产品。
3.职责3.1生产部负责检测样品的制备3.2质检部负责样品检测及报告的填写。
4.依据GB 8368-2005《一次性使用输液器重力输液式》。
《中华人民共和国药典》2015版通则0903《不溶性微粒检查法》。
5.程序5.1试验前准备6mol/L的盐酸、6mol/L氢氧化钠、纯化水、无粉手套。
5.2环境万级环境下的百级工作台上进行。
5.3设备GWJ-5S微粒检测仪。
5.4空白对照液制备5.4.1将接触检测液的器具用纯化水清洁3遍,备用。
5.4.2量取37ml的分析纯盐酸置量筒中,加纯化水至200ml,即得6mol/L的盐酸。
5.4.3称取48g的氢氧化钠置量筒中,加纯化水至200ml,即得6mol/L的氢氧化钠。
5.4.4量取150ml的6mol/L的盐酸置磨口的三角烧瓶中,加6mol/L的氢氧化钠调节至PH7.0左右,再加纯化水至520ml,作为空白对照液,备用。
5.4.5将520ml空白对照液沿壁缓慢倒入检测杯中,避免产生气泡。
5.4.6将检测杯放在检测平台上,静止1-2min,目测溶液没有气泡为止,按《GWJ-5S微粒检测仪标准操作规程》检测。
5.4.7制取2份平行的空白对照液,检测结果取平均值。
5.4.8空白对照液检测数值都应不超过9,否则试验无效。
5.5供试液的制备5.5.1取11块90mm×110mm的生物产品,剪开包装,用镊子夹起生物产品放入500ml的磨口三角烧瓶中。
5.5.4 加入200ml的纯化水,每隔20分钟充分振荡一次,浸提1小时,用镊子将生物产品取出后,量取37ml分析纯盐酸至三角烧瓶中。
5.5.3将磨口三角烧瓶置于105℃的环境下,持续24小时。
5.5.4取出三角烧瓶,目测溶液应无异物,然后加入6mol/L的氢氧化钠溶液调节PH值至7.0左右,加纯化水至500ml。
微生物初始化污染检测记录

微生物初始化污染检测记录一次性使用输液器(内腔、外表面)1.试品的抽取抽样地点:抽样批次:抽样数量:抽样人:抽样时间:2.浸提介质无菌生理盐水3.试验前准备3.1营养琼脂培养基的配制:成份:NaCl 5g;胨 10g;琼脂 15-20g制法:取牛肉膏3g,加水1000ml,配制成肉浸液,将胨、NaCl、琼脂加入肉浸液内,微温溶解后,调节PH值,为弱碱性煮沸,滤清,调节PH值使灭菌后为7.2±0.2。
3.2与供试液接触的所有器具及制备好的营养琼脂培养基一并放入高压蒸汽灭菌器115℃持续30min,待灭菌器冷却后连同抽取的供试品一并放入无菌室内,启动工作台风机,开紫外线灯30min.4.供试液制备及接种4.1内腔供试液制备:输液(血)器:在无菌条件下向每套输液器的内腔注入浸提介质各20ml,作为供试液,反复荡洗5次,然后将每套输液器内腔内的供试液汇集到一无菌具塞试剂瓶内,待混匀后在从瓶内各抽取1ml供试液分别加入10个无菌的空平皿内,最后在将灭了菌凉至45℃的熔化营养琼脂培养基倾注于已加入供试液的平皿中,每平皿中加入培养基量为15-20ml。
作为1:1的供试液。
注射器:每支注射器抽取灭菌生理盐水至公称容量,振摇5次,汇集到一无菌具塞试剂瓶内,待混匀后在从瓶内各抽取1ml供试液分别加入10个无菌的空平皿内,最后在将灭了菌凉至45℃的熔化营养琼脂培养基倾注于已加入供试液的平皿中,每平皿中加入培养基量为15-20ml。
作为1:1的供试液。
4.2外部供试液制备:按产品外表面积每10cm2用1mL的灭菌生理盐水冲洗,作为1:1的供试液。
用棉拭子在输液器表面往返涂抹10次后,将棉试子放入10ml灭菌生理盐水的试管中,将试管震打80次混匀作为供试液,然后再分别取1ml供试液放入2个无菌的空平皿内,最后在将灭了菌凉至45℃的熔化营养琼脂培养基倾注于已加入供试液的平皿中,每平皿中加入培养基量为15-20ml.将所取10套供试品分别按上述方法进行供试液制备及接种。
洁净室区尘埃粒子数测试记录

平均值的均值
M=(A1+A2)/L
标准误差
SE
置信上限UCL=M +t×SE
结果
评定
1
μm
μm
5μm
2
μm
5
μm
5μm
1
μm
μm
5μm
2
μm
5
μm
5μm
1
μm
μm
5μm
2
μm
5
μm
5μm
1
μm
μm
5μm
2
μm
5
μm
5μm
评定标准:
注:(1)A1,A2--某一采样点的平均粒子浓度; UCL--平均值均值95%置信上限; ·SE=
洁净室区尘埃粒子数测试记录
XXXXX公司
洁净室(区)尘埃粒子数测试记录
文件编号:XXX
检测编号:
被测单位
洁净级别
气流形式
测试状态
检测日期
测试依据
报告日期
测试仪器厂家及编号:
记录μm、5μm粒子数:采样流量为min;采样周期为1min;(单位:粒/m3)
洁净室/区
采
样
点
粒子直径C1 NhomakorabeaC2C3
平均值A=C1+C2+C3
文件编号:XXX
检测编号:检测日期:
检测者: 复核者:共页第页
标准误差
SE
置信上限UCL=M +t×SE
结果
评定
1
μm
μm
5μm
2
μm
5
μm
5μm
1
μm
μm
5μm
