化工原理第六章第四节讲稿
合集下载
化工原理讲稿7(第六章)(天大版).

对于接近理想物系的溶液,可用芬斯克方程计算;
③计算出 (R-Rmin)/(R+1),查吉利兰图得: (N-Nmin)/(N+1) ,求得所需的 N;
④确定加料板位置;
⑤由N~R图,求得所需的 R; 由准确操作线求得准确的N;
• 注意:N、Nmin不包括再沸器;
例6-4 用一精馏塔分离甲醇-水混合液,已知: xF=0.628(摩尔分率,下同), xD=0.965, xW=0.03, 泡点进料,回流比R=1.95。 试: 按逐板计算法确定理论塔板数。并近似用 图解法表示第二块板下降液体组成和上升蒸 汽组成。
例6-5 在常压连续精馏塔中分离苯-甲苯混合液, 已知xF=0.4(摩尔分率、下同),xD=0.97, xw=0.04 相对挥发度α=2.47。 试分别求以下三 种进料方式下的最小回流比和全回流下的最小
理论板数。
(1)冷液进料q=1.387(2)泡点进料(3)饱 和蒸汽进料
练习题 用一连续操作的精馏塔分离丙烯-丙烷混合液,进料 含丙烯0.8(摩尔分数,下同),常压操作,泡点进 料,要使塔顶产品含丙烯0.95,塔釜产品含丙烷0.05, 物系的相对挥发度为1.16; 试计算:(1)最小回流比?
Rmin
xD yq
yq xq
截距法: xD Rmin 1
A
Rmin
解析法:
由于
yq
xq 1 ( 1)xq
Rmin
xD yq
yq xq
1
1
xD xq
(1
xD
)
1 xq
当q
1、xq
xF
Rmin
1
1
xD xF
(1 xD 1 xF
)
当q
③计算出 (R-Rmin)/(R+1),查吉利兰图得: (N-Nmin)/(N+1) ,求得所需的 N;
④确定加料板位置;
⑤由N~R图,求得所需的 R; 由准确操作线求得准确的N;
• 注意:N、Nmin不包括再沸器;
例6-4 用一精馏塔分离甲醇-水混合液,已知: xF=0.628(摩尔分率,下同), xD=0.965, xW=0.03, 泡点进料,回流比R=1.95。 试: 按逐板计算法确定理论塔板数。并近似用 图解法表示第二块板下降液体组成和上升蒸 汽组成。
例6-5 在常压连续精馏塔中分离苯-甲苯混合液, 已知xF=0.4(摩尔分率、下同),xD=0.97, xw=0.04 相对挥发度α=2.47。 试分别求以下三 种进料方式下的最小回流比和全回流下的最小
理论板数。
(1)冷液进料q=1.387(2)泡点进料(3)饱 和蒸汽进料
练习题 用一连续操作的精馏塔分离丙烯-丙烷混合液,进料 含丙烯0.8(摩尔分数,下同),常压操作,泡点进 料,要使塔顶产品含丙烯0.95,塔釜产品含丙烷0.05, 物系的相对挥发度为1.16; 试计算:(1)最小回流比?
Rmin
xD yq
yq xq
截距法: xD Rmin 1
A
Rmin
解析法:
由于
yq
xq 1 ( 1)xq
Rmin
xD yq
yq xq
1
1
xD xq
(1
xD
)
1 xq
当q
1、xq
xF
Rmin
1
1
xD xF
(1 xD 1 xF
)
当q
化工原理第六章解析

第六章 蒸发
学习目的 与要求
通过本章学习,掌握蒸发操作的特点、蒸发 器的类型、蒸发过程计算,能够根据生产工艺要 求和物料特性,合理选择蒸发器类型并确定适宜 操作流程和条件。
1
第六章 蒸发
6.1 概述
2
一.蒸发的目的
蒸发 将含有不挥发溶质的溶液加热至沸腾,使
部分挥发性溶剂汽化并移除,从而获得浓缩溶 液或回收溶剂的操作。 蒸发操作的基本要点
18
第六章 蒸发
6.2 蒸发设备 6.2.1 循环型蒸发器 6.2.2 单程型蒸发器
19
一.升膜式蒸发器
图6-8 升膜式蒸发器 1―蒸发器;2―分离室;
20
二.降膜式蒸发器
图6-9 降膜式蒸发器 1― 蒸 发 器 ; 2― 分 离 室 ; 3―布膜器
21
三.升—降膜式蒸发器
图6-11 升―降膜蒸发器 1― 预 热 器 ; 2― 升 膜加 热室;3―降膜加热室; 4―分离室
蒸发器的热负荷
Q D(H hc ) WH ' (F W )h1 Fh0 QL
蒸发器的
热损失
35
二.热量衡算
1.溶液稀释热较大的情况 某些盐、碱的水溶液,在稀释时其放热效
应非常显著。 蒸发是稀释的逆过程。 需通过实验测定焓值随组成和温度的变化。
36
二.热量衡算
图6-15 氢氧化钠的焓浓图
30
蒸发器的选型原则
① 对物料的工艺特性有良好的适应性, 其中对黏度在蒸发过程中的增加程度及结垢情 况应给予特别注意。
② 满足生产工艺对完成液质和量的要求。 ③ 结构简单,操作可靠,造价和操作费 用低廉,经济合理,维修方便。
31
第六章 蒸发
6.2 蒸发设备 6.2.1 循环型蒸发器 6.2.2 单程型蒸发器 6.2.3 蒸发设备和蒸发技术的发展 6.2.4 蒸发器的选型 6.2.5 蒸发器的辅助设备(自学)
学习目的 与要求
通过本章学习,掌握蒸发操作的特点、蒸发 器的类型、蒸发过程计算,能够根据生产工艺要 求和物料特性,合理选择蒸发器类型并确定适宜 操作流程和条件。
1
第六章 蒸发
6.1 概述
2
一.蒸发的目的
蒸发 将含有不挥发溶质的溶液加热至沸腾,使
部分挥发性溶剂汽化并移除,从而获得浓缩溶 液或回收溶剂的操作。 蒸发操作的基本要点
18
第六章 蒸发
6.2 蒸发设备 6.2.1 循环型蒸发器 6.2.2 单程型蒸发器
19
一.升膜式蒸发器
图6-8 升膜式蒸发器 1―蒸发器;2―分离室;
20
二.降膜式蒸发器
图6-9 降膜式蒸发器 1― 蒸 发 器 ; 2― 分 离 室 ; 3―布膜器
21
三.升—降膜式蒸发器
图6-11 升―降膜蒸发器 1― 预 热 器 ; 2― 升 膜加 热室;3―降膜加热室; 4―分离室
蒸发器的热负荷
Q D(H hc ) WH ' (F W )h1 Fh0 QL
蒸发器的
热损失
35
二.热量衡算
1.溶液稀释热较大的情况 某些盐、碱的水溶液,在稀释时其放热效
应非常显著。 蒸发是稀释的逆过程。 需通过实验测定焓值随组成和温度的变化。
36
二.热量衡算
图6-15 氢氧化钠的焓浓图
30
蒸发器的选型原则
① 对物料的工艺特性有良好的适应性, 其中对黏度在蒸发过程中的增加程度及结垢情 况应给予特别注意。
② 满足生产工艺对完成液质和量的要求。 ③ 结构简单,操作可靠,造价和操作费 用低廉,经济合理,维修方便。
31
第六章 蒸发
6.2 蒸发设备 6.2.1 循环型蒸发器 6.2.2 单程型蒸发器 6.2.3 蒸发设备和蒸发技术的发展 6.2.4 蒸发器的选型 6.2.5 蒸发器的辅助设备(自学)
化工原理:第六章蒸馏小结(教案).docx

蒸憾小结
一、定义:利用液体混合物各组分沸点(或挥发度)的不同,经过多次部分汽化与部分冷凝,将液体混合物分离与提纯的过程,称为精馅操作。
二精馅装置及流程
1)塔顶:产品(易挥发性组分)D及回流液L
2)塔底:难挥发性产品W及上升蒸汽W
3)塔内:始终有一股至下而上的蒸汽V及一股
至上而下的液体L ,且两者在每块塔板上进行传质
和传热,结果:上升蒸汽中易挥发组分不断增
加,即y…>y* 下降液体中易挥发组分不断减少, 即x n
塔设备
V X n_i
4)进料位置:塔的中部某处
三、相平衡关系
t-x-y相图(由实验得
出)
1•相图电刊相图(来自“.y相图,常用)
表示方法
(含相对挥)
2.相对挥姬儿l + (a-l)x
4
理论板的概念和恒摩尔流的假设
四
、
理论板的定义:离开该板时气液两相互为平衡。
2.恒摩尔流:
o n Q
(盂)S I
龜棊b)
w <長
£
+a x a H
工XH
Ai+aHH
迂 0 ・
Q
?
M W
.M ng K 纂
((圧邂)M )
M(z
〜
I I) n i
'X I —
I
E E
M
—
p x H - 親耀s 蛋垢回co w 撫養蛊泰^W S B 暫F x 训:竄
(益漿)兀―垢回轴*<
5.
6 •板式塔。
化工原理(第二版)第六章-

管道阻力引起的温度差损失 ,其值一般取为1℃。
第三节 多效蒸发
一、多效蒸发的操作原理
由蒸发器的热量恒算可知,在单效蒸发器中每蒸发1㎏的水需要 消耗1㎏多的生蒸汽。在大规模的工业生产中,水分蒸发量很大,需 要消耗大量的生蒸汽。如果能将二次蒸汽用作另一蒸发器的加热蒸汽, 则可减少生蒸汽消耗量。由于二次蒸汽的压力和温度低于生蒸汽的压 力和温度,因此,二次蒸汽作为加热蒸汽的条件是:该蒸发器的操作 压力和溶液沸点应低于前一蒸发器。采用抽真空的方法可以很方便地 降低蒸发器的操作压力和溶液的沸点。每一个蒸发器称为一效,这样, 在第一效蒸发器中通入生蒸汽,产生的二次蒸汽引入第二效蒸发器, 第 二效的二次蒸汽再引入第三效蒸发器,以此类推,末效蒸发器的二 次 蒸汽通入冷凝器冷凝,冷凝器后接真空装置对系统抽真空。于是, 从第 一效到最末效,蒸发器的操作压力和溶液的沸点依次降低,因此 可以 引入前效的二次蒸汽作为后效的加热介质,即后效的加热室成为 前效 二次蒸汽的冷凝器,仅第一效需要消耗生蒸汽,这就是多效蒸发
降。
3
真空蒸发系统要求有造成减压的装置,使系统的
投资费和操作费提高。
第二节 单效蒸发
F,w0,t0,h0
D, T, H
W, T’, H’
蒸发室
加 热 室
(F-W),w1, t1, h1
D, T, hw
图6-2 单效蒸发示意图
第二节 单效蒸发
二、单效蒸发的计算
单效蒸发计算的主要内容有:水分蒸发量;加热蒸气 消耗量;蒸发器的传热面积。 计算的依据是:物料衡算、热量衡算和传热速率方程。
(6-2)
第二节 单效蒸发
式中
Q——蒸发器的热负荷或传热量,kJ/h ; D——加热蒸气消耗量,kg/h; Cp0——原料液比热容,kJ/(㎏·℃); t0——原料液的温度,℃;
第三节 多效蒸发
一、多效蒸发的操作原理
由蒸发器的热量恒算可知,在单效蒸发器中每蒸发1㎏的水需要 消耗1㎏多的生蒸汽。在大规模的工业生产中,水分蒸发量很大,需 要消耗大量的生蒸汽。如果能将二次蒸汽用作另一蒸发器的加热蒸汽, 则可减少生蒸汽消耗量。由于二次蒸汽的压力和温度低于生蒸汽的压 力和温度,因此,二次蒸汽作为加热蒸汽的条件是:该蒸发器的操作 压力和溶液沸点应低于前一蒸发器。采用抽真空的方法可以很方便地 降低蒸发器的操作压力和溶液的沸点。每一个蒸发器称为一效,这样, 在第一效蒸发器中通入生蒸汽,产生的二次蒸汽引入第二效蒸发器, 第 二效的二次蒸汽再引入第三效蒸发器,以此类推,末效蒸发器的二 次 蒸汽通入冷凝器冷凝,冷凝器后接真空装置对系统抽真空。于是, 从第 一效到最末效,蒸发器的操作压力和溶液的沸点依次降低,因此 可以 引入前效的二次蒸汽作为后效的加热介质,即后效的加热室成为 前效 二次蒸汽的冷凝器,仅第一效需要消耗生蒸汽,这就是多效蒸发
降。
3
真空蒸发系统要求有造成减压的装置,使系统的
投资费和操作费提高。
第二节 单效蒸发
F,w0,t0,h0
D, T, H
W, T’, H’
蒸发室
加 热 室
(F-W),w1, t1, h1
D, T, hw
图6-2 单效蒸发示意图
第二节 单效蒸发
二、单效蒸发的计算
单效蒸发计算的主要内容有:水分蒸发量;加热蒸气 消耗量;蒸发器的传热面积。 计算的依据是:物料衡算、热量衡算和传热速率方程。
(6-2)
第二节 单效蒸发
式中
Q——蒸发器的热负荷或传热量,kJ/h ; D——加热蒸气消耗量,kg/h; Cp0——原料液比热容,kJ/(㎏·℃); t0——原料液的温度,℃;
化工原理课件(十一五)课件第六章第四节物料衡算和操作线方程
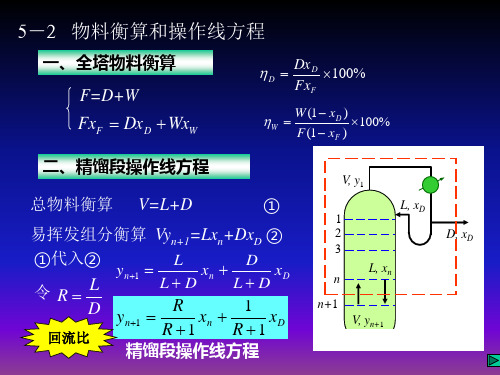
(5)过热蒸气进料
q Cm' p (Ts tF ) < 0 rm
总物料衡算
液相分率 q L' L
F
V ’ =L’-W
L’=V’+W ①
L' L
q
②
F
L,=L+qF
V'=V+(q-1)F
提馏段物料衡算
q的引入,使提馏段上升蒸汽及下降液体流量的计算容易了。
联想恒摩尔流假设中V与V’,L与L’不 一定相等,那么什么情况下相等?
IL≈IL'
代入②式并 与①联立
V,IV
L,IL
V’, IV’ L’, IL’
(V-V') IV =F IF-(L'-L) IL
IV I F L' L
IV IL
F
=q
q L' L F
液相分率
热状况
q
IV IV
IF IL
将1kmol原料变成饱和蒸汽所需热量 1kmol原料的汽化潜热
参数
三、q 线方程(进料方程)
Vy=Lx+DxD ① V'y=L'x-WxW ②
进料板连接着精馏段与提 馏段,因此组成相同,下 标省略!
① - ②:
1.0
(V'-V)y=(L'-L)x-(DxD+WxW)
q=1 q>1
a
0<q<1
(q-1)F y=q F x-F xF
y q x xF q 1 q 1 ——q线方程
W V'
xW
y
1.0
因为 L’=V’+W
而L’、 V’受进料温度状 况的影响,所以在学习 下面内容之前,无法分
化工原理讲稿8(第六章)(天大版).

九、塔高与塔径的计算 (一)塔板效率
指反映实际塔板的气液两相传质的完善程度; 表示方法有总板效率、单板效率等; 1.总板效率(又称全塔效率)ET 指达到指定分离效果所需理论板层数与实际塔板 层数的比值;
ET
NT Np
100%
理论板数 实际板数
Np
NT ET
NT:不包括塔釜再沸器,再沸器相当一块理论板;
问: (1)此时产品组成将有何变化? (2)若维持xD不变,可采用哪些 措施,并比较这些方法的优缺点?
十二、特殊精馏 1.恒沸精馏
原理:在混合液中加入第三组分(称为挟带剂) 形成新的最低恒沸物;
2.萃取精馏 原理:向混合液中加入溶剂(又称萃取剂),萃取剂
不与原料液中任何组分形成恒沸物;
P73页 习题15、16;
xF 对xD, xW 的影响
b. 加料板位置上移
结论:xD , xW
加料板位置对xD, xW 的影响
c. R 结论:xD , xW
R 对xD, xW 的影响
d. q , R 不变, D不变, V’ 结论:xD , xW
q 对xD, xW 的影响
十一、 精馏装置的热量恒算
xn1 xn xn1 f '( yn )
xn1 xn
xn1 f '( xn1 )
习题16
1.y1 xD
F L'
2.
D
V
'
L
'
x1
V
'
yW
WxW
3.yW
1
xW ( 1)xW
指反映实际塔板的气液两相传质的完善程度; 表示方法有总板效率、单板效率等; 1.总板效率(又称全塔效率)ET 指达到指定分离效果所需理论板层数与实际塔板 层数的比值;
ET
NT Np
100%
理论板数 实际板数
Np
NT ET
NT:不包括塔釜再沸器,再沸器相当一块理论板;
问: (1)此时产品组成将有何变化? (2)若维持xD不变,可采用哪些 措施,并比较这些方法的优缺点?
十二、特殊精馏 1.恒沸精馏
原理:在混合液中加入第三组分(称为挟带剂) 形成新的最低恒沸物;
2.萃取精馏 原理:向混合液中加入溶剂(又称萃取剂),萃取剂
不与原料液中任何组分形成恒沸物;
P73页 习题15、16;
xF 对xD, xW 的影响
b. 加料板位置上移
结论:xD , xW
加料板位置对xD, xW 的影响
c. R 结论:xD , xW
R 对xD, xW 的影响
d. q , R 不变, D不变, V’ 结论:xD , xW
q 对xD, xW 的影响
十一、 精馏装置的热量恒算
xn1 xn xn1 f '( yn )
xn1 xn
xn1 f '( xn1 )
习题16
1.y1 xD
F L'
2.
D
V
'
L
'
x1
V
'
yW
WxW
3.yW
1
xW ( 1)xW
化工原理-6章蒸馏

1 yA 1 xA
y x 1 ( 1)x
——相平衡方程
当 α为已知时,可用相对挥发度表示了气液相平衡关系。
当 1 当 1
y=x, 即相平衡时气相的组成与液相的组成相同, 不能用蒸馏方法分离。
则y>x,α愈大,y比x大的愈多,组分A和B愈易分离。
三、双组分理想溶液的气液平衡相图
双组分理想溶液的汽液平衡关系用相图表示比较直观、 清晰,而且影响蒸馏的因素可在相图上直接反映出来。蒸馏 中常用的相图为恒压下的温度-组成( t-x-y )图和气相-液 相组成( x-y )图。
当生产任务要求将一定数量和组成的原料分离成指定组成 的产品时,精馏塔计算的内容有:出液和塔釜残液的流量、塔 板数、进料口位置、塔高、塔径等。
6.4.1 全塔物料衡算
1.全塔物料衡算
单位时间为基准
总物料衡算: qn,F=qn,D+qn,W 易挥发组分物料衡算:
qn,FxF=qn,DxD+qn,WxW qn,F、qn,D、qn,W——流量,kmol/h
二、蒸馏的分类
1、按蒸馏方法:简单蒸馏、平衡蒸馏(闪蒸)、精馏、特殊精馏。 2、按操作压力:常压;减压;加压。 3、按原料液组分数:双组分蒸馏和多组分蒸馏 4、按操作方式:间歇蒸馏和连续蒸馏。
三、蒸馏操作的特点
优点:* 适用面广,液体混合物和气体混合物均可 * 操作流程较简单,无需其他外加介质
缺点:* 能耗大
一、利用饱和蒸气压计算气液平衡关系
法国物理学家拉乌尔在1887年研究含有非挥发性溶质的 稀溶液的行为时发现的,可表述为:“在某一温度下,稀溶 液的蒸气压等于纯溶剂的蒸气压乘以溶剂的摩尔分数”。
PA PA0 xA ——拉乌尔定律
pA0——纯组分A在溶液温度下的饱和蒸气压,Pa; xA——溶液中组分A的摩尔分数;
y x 1 ( 1)x
——相平衡方程
当 α为已知时,可用相对挥发度表示了气液相平衡关系。
当 1 当 1
y=x, 即相平衡时气相的组成与液相的组成相同, 不能用蒸馏方法分离。
则y>x,α愈大,y比x大的愈多,组分A和B愈易分离。
三、双组分理想溶液的气液平衡相图
双组分理想溶液的汽液平衡关系用相图表示比较直观、 清晰,而且影响蒸馏的因素可在相图上直接反映出来。蒸馏 中常用的相图为恒压下的温度-组成( t-x-y )图和气相-液 相组成( x-y )图。
当生产任务要求将一定数量和组成的原料分离成指定组成 的产品时,精馏塔计算的内容有:出液和塔釜残液的流量、塔 板数、进料口位置、塔高、塔径等。
6.4.1 全塔物料衡算
1.全塔物料衡算
单位时间为基准
总物料衡算: qn,F=qn,D+qn,W 易挥发组分物料衡算:
qn,FxF=qn,DxD+qn,WxW qn,F、qn,D、qn,W——流量,kmol/h
二、蒸馏的分类
1、按蒸馏方法:简单蒸馏、平衡蒸馏(闪蒸)、精馏、特殊精馏。 2、按操作压力:常压;减压;加压。 3、按原料液组分数:双组分蒸馏和多组分蒸馏 4、按操作方式:间歇蒸馏和连续蒸馏。
三、蒸馏操作的特点
优点:* 适用面广,液体混合物和气体混合物均可 * 操作流程较简单,无需其他外加介质
缺点:* 能耗大
一、利用饱和蒸气压计算气液平衡关系
法国物理学家拉乌尔在1887年研究含有非挥发性溶质的 稀溶液的行为时发现的,可表述为:“在某一温度下,稀溶 液的蒸气压等于纯溶剂的蒸气压乘以溶剂的摩尔分数”。
PA PA0 xA ——拉乌尔定律
pA0——纯组分A在溶液温度下的饱和蒸气压,Pa; xA——溶液中组分A的摩尔分数;
化工原理讲稿8(第六章)(天大版)

对 全 回 流 操 作 : y n +1 = x n、 y n = x n −1 y n − y n +1 x n −1 − x n E mV = y * − y = f ( x ) − x n n +1 n n 则: x n −1 − x n E = x n −1 − x n = x n −1 − x n = mL x n −1 − x n * x n −1 − f '( y n ) x n −1 − f '( x n −1 )
习题16 习题
1. y1 = xD F = L ' ⇒ L ' x1 = V ' yW + WxW 2. D = V ' α xW 3. yW = 1 + (α − 1) xW 4.EmV y1 − yW = y1 * − yW
设: F = 1kmol / h Dx D x F − xW x D 0.2 − xW 0.28 η D = 0.8 = = = ⇒ xW = 0.0857 Fx F x D − xW x F 0.28 − xW 0.2 D = 0.57 kmol / h、 W = 0.43kmol / h F = L ' F W ⇒ L ' x1 = V ' y W + Wx W ⇒ y W = x1 − xW D D D = V ' 1 0.43 ⇒ 0.206 = x1 − × 0.094 ⇒ x1 = 0.158 0.57 0.57 y1 = x D = 0.28 y1 − y W α xW 2.5 × 0.094 = = 0.206 由于: E mV = 其中: yW = y1 * − y W 1 + (α − 1) xW 1 + 1.5 × 0.094 α x1 2.5 × 0.158 = = 0.319 y1 * = 1 + (α − 1) x1 1 + 1.5 × 0.158 0.28 − 0.206 E mV = = 0655 0.319 − 0.206
化工原理课件第六章 蒸馏2

LV
F
F
L V
LV L V
LV F
L V
2020/7/16
13
二、 进料热状况参数
对加料板虚线范围进行物料衡算,得 qn,F qn,V 'qn,L qn,V qn,L ' (1)
qn,V qn,V ' qn,F qn,L qn,L ' (2) 对加料板虚线范围进行热量衡算,得
F, IF
4
(2)填料塔
填料精馏塔如图(b)所示。塔内装有大比表面和高空隙率的 填料,不同填料具有不同的比表面积和空隙率,为此,在传质 过程中具有不同的性能。填料具有各种不同类型,装填方式分 散装和整装两种。视分离混合物的特性及操作条件,选择不同 的填料。
当回流液或料液进入时,将填料表面润湿,液体在填料表 面展为液膜,流下时又汇成液滴,当流到另一填料时,又重展 成新的液膜。当气相从塔底进入时,在填料孔隙内沿塔高上升, 与展在填料上的液沫连续接触,进行传质,使气、液两相发生 连续的变化,故称填料塔为微分接触设备。
进料的汽化潜热
则
表明进料热状况的参qn,L q qn,F (3)
三、提馏段操作方程的一般形式 将(3)式代入前面的提馏段操作方程,即得P212式5-91
四、q线方程(进料方程) 略去精馏段操作线方程
qn,V yn1 qn,L xn qn,D xD
和提馏段操作线方程 qn,V ' yn1 qn,L ' xn qn,W xW
液两相通道。塔板具
有多种不同型式,分
别称之为不同的板式
塔,在生产中得到广
泛的应用。
(a)
(b)
混合物的气、液两相在塔内逆向流动,气相从下至上流动, 液相依靠重力自上向下流动,在塔板上接触进行传质。两相 在塔内各板逐级接触中,使两相的组成发生阶跃式的变化, 故称板式塔为逐级接触设备。
陈敏恒_化工原理_第六章(全)

A’=1.35m2
4.1 沸腾给热 1. 大容积饱和沸腾 过程特点:汽液两相共存
有利:气泡搅动液体,液体冲刷表面 不利:有可能气泡连成气膜,将液体与加热面隔开 2.沸腾条件 ①过热度(t-tS) —气泡存在之必须
2.α的影响因素 ①物性:ρ, μ, Cp, λ ②设备因素(定性尺寸):l ③流动因素:强制对流:u 自然对流: βgΔt α=f (ρ, μ, λ, l, u, βgΔt, Cp) 基本量纲4个(M,L,T,θ),变量8个, 无量纲准数=8-4=4,即 3 2 l lu Cp gtl f( , , ) 2 Nu=f(Re, Pr, Gr) 强制对流Nu=f(Re, Pr); 自然对流Nu=f(Gr, Pr)
自然对流的冷源、热源应放在恰当的位置
2.强制对流 在外力或Δp作用下引起流动
3.3 对流给热过程的数学描述 1.牛顿冷却定律 q (T TW ) 其中:TW: 壁温;T: 流体主体温度; α:给热系数 W/m2℃ 工程处理方法—分离变量法 ① 便于分解组合传热系数K
T TW TW tW tW t q 1 / 1 / 1/2
第六章 传热
1 概述 1.1 传热目的 ①加热、冷却物料 ②回收热量或冷量 设法促进传热 ③保温,减少热量或冷量损失 设法阻止传热 传热还用于其它单元操作 如蒸发,精馏
1.2传热机理 ①传导—分子热运动(自由电子迁移) ②对流—流体宏观迁移引起载热 ③辐射—电磁波 热水瓶为什么能保温? 1.3冷热流体接触方式 ①蓄热式
2.4 球壳导热
dt Q 4r dr r2 dr t2 Q 2 4 dt r1 r t1 4 ( t1 t 2 ) 4r1r2 ( t1 t 2 ) Q 1 1 r2 r1 r1 r2
讲稿6(第六化工原理章)(天大版)

y x = α − (α − 1 ) y W xW L + qF y = x − L + qF − W L + qF − W
y0
分凝器
全凝器
• 分凝器相当于一块理论板, 分凝器相当于一块理论板, 可以x 可以 0、y0计,y0=xD、 x0 =f′(y0),其他相同; ,其他相同;
W xW F xF D xD
•提馏段操作线方程: 提馏段操作线方程: 提馏段操作线方程 已知: 已知:xF、F、xW、η 、 泡点进料 L’=F, V’=D
∴ ym + 1 F W xW = xm − D D
解(1)间接蒸汽加热时操作线方程 ) 精馏段操作线方程为: 精馏段操作线方程为:
xD R 2 0.9 y= x+ = x+ = 0.667x + 0.3 R +1 R +1 2 +1 2 +1
提馏段操作线方程为: 提馏段操作线方程为:
L + qF W y′ = x′ − xw L + qF −W L + qF −W RD/ F + q W/F ′− x xw = RD/ F + q −W / F RD/ F + q −W / F
= 0.043
y′ = 2×0.3+1.2 0.7 ′− x ×0.043 2×0.3+1.2 − 0.7 2×0.3+1.2 − 0.7 =1.636x′ − 0.0274
(2) 直接蒸汽加热时操作线方程 ) 精馏段操作线方程与( ) 精馏段操作线方程与(1)同; 提馏段操作线方程为: 提馏段操作线方程为:
V0 y0 F xF
D
W xW
y0
分凝器
全凝器
• 分凝器相当于一块理论板, 分凝器相当于一块理论板, 可以x 可以 0、y0计,y0=xD、 x0 =f′(y0),其他相同; ,其他相同;
W xW F xF D xD
•提馏段操作线方程: 提馏段操作线方程: 提馏段操作线方程 已知: 已知:xF、F、xW、η 、 泡点进料 L’=F, V’=D
∴ ym + 1 F W xW = xm − D D
解(1)间接蒸汽加热时操作线方程 ) 精馏段操作线方程为: 精馏段操作线方程为:
xD R 2 0.9 y= x+ = x+ = 0.667x + 0.3 R +1 R +1 2 +1 2 +1
提馏段操作线方程为: 提馏段操作线方程为:
L + qF W y′ = x′ − xw L + qF −W L + qF −W RD/ F + q W/F ′− x xw = RD/ F + q −W / F RD/ F + q −W / F
= 0.043
y′ = 2×0.3+1.2 0.7 ′− x ×0.043 2×0.3+1.2 − 0.7 2×0.3+1.2 − 0.7 =1.636x′ − 0.0274
(2) 直接蒸汽加热时操作线方程 ) 精馏段操作线方程与( ) 精馏段操作线方程与(1)同; 提馏段操作线方程为: 提馏段操作线方程为:
V0 y0 F xF
D
W xW
(化工原理)第四节 传热计算

平均温度差法-2
一、恒温传热时的平均温度差
换热器的间壁两侧流体均有相变化时,就是 恒温传热。
Q =KS(T-t)=KSΔt
二、变温传热下的平均温度差
1.逆流和并流时的平均温度差
逆流 与 并流
平均温度差法-3
平均温度差法-4
由换热器的热量衡算微分式知:
根据前述的假定
(1)传热为稳定操作过程; (2)两流体的比热为常量(可取进、出口的平均值);
逆流另一优点是换热器面积相同时,可节省加热介质的用量。 这是因为逆流时,热流体的出口温度T2可降至的接近冷流体的 进口温度t1 ;而采用并流操作时,只能降到接近冷流体的出口 温度t2,即逆流时热流体的温降较并流时为大,因此逆流加热 介质用量较少。同理逆流时冷流体的温升较并流时大,故冷却 介质的用量可少些
换热器的热量衡算和传热速率方程的微 分式为:
对于热流体,上式可改写为:
传热单元数法-5
上式的积分式称为基于热流体的传热单 元数,用NTU表示,即 :
对于冷流体,换热器的传热单元数 (NTU)c为:
传热单元数法-7
三、传热效率和传热单元数的关系
总传热速率方程为 Q=KSΔtm
若冷流体为最小值流体
平均温度差法-5
如果将Q对T或t作图,由上式可知 Q-T和 Q-t是 直线关系,可分别表示为:
T=mQ+k 及 t=m’Q+k’
上两式相减,得:
T -t =Δt=(m-m’)Q +(k-k’) 式中m、k、m’、k’分别为Q-T和Q-t直线的斜
率和截距。
平均温度差法-6
Q-Δt的直线的斜率为
一、传热效率ε
换热器的传热效率的ε定义为:
传热单元数法-2
化工原理第六章第四节讲稿duo.

2018/10/6
求每小时送入塔内的水量。 溶液浓度(gNH3/100gH2O) 分压Pa 分析: 2 1600 2.5 2000 3 2427
求水量
解:
已知qnL/(qnL)min 吸收剂用量qnL 求(qnL)min
平衡常数
1)平衡关系
* 3 * y 1 . 6 10 p 0.01604 Y* * * 3 3 1 y P p 101.33 10 1.6 10
2018/10/6
Y1
dY qnG Y m[ (Y Y2 ) X 2 ] b qnL
Y2
dY Y2 mqnG mqnG (1 )Y [ Y2 ( mX 2 b)] qnL qnL mqnG m S 令 qnL qnL qnG
Y1
N OG
Y1 Y2
dY
qnG
qnL
qnG(Y1 Y2 ) qnL( X 1 X 2 ) qnL qnL Y1 X 1 Y2 X2 qnG qnG
吸收率 A 混合气中溶质A 被吸收的百分率
qnGY1 qnGY2 Y1 Y2 被吸收的溶质量 A 进塔气体的溶质量 qnGY1 Y1 Y2 Y1 (1 A )
(1 S )Y1 (1 S )Y2 * S (Y2 Y2 * ) 1 ln[ ] * 1 S Y2 Y2
NOG
1 Y1 Y2 ln[( 1 S ) S] * 1 S Y2 Y2
*
mqnG S ——脱吸因数。平衡线斜率和操作线斜率的比值 qnL
无因次。S愈大,脱吸愈易进行。
2)塔的工艺尺寸,塔径和填料层高度
2018/10/6
一、吸收塔的物料衡算与操作线方程
求每小时送入塔内的水量。 溶液浓度(gNH3/100gH2O) 分压Pa 分析: 2 1600 2.5 2000 3 2427
求水量
解:
已知qnL/(qnL)min 吸收剂用量qnL 求(qnL)min
平衡常数
1)平衡关系
* 3 * y 1 . 6 10 p 0.01604 Y* * * 3 3 1 y P p 101.33 10 1.6 10
2018/10/6
Y1
dY qnG Y m[ (Y Y2 ) X 2 ] b qnL
Y2
dY Y2 mqnG mqnG (1 )Y [ Y2 ( mX 2 b)] qnL qnL mqnG m S 令 qnL qnL qnG
Y1
N OG
Y1 Y2
dY
qnG
qnL
qnG(Y1 Y2 ) qnL( X 1 X 2 ) qnL qnL Y1 X 1 Y2 X2 qnG qnG
吸收率 A 混合气中溶质A 被吸收的百分率
qnGY1 qnGY2 Y1 Y2 被吸收的溶质量 A 进塔气体的溶质量 qnGY1 Y1 Y2 Y1 (1 A )
(1 S )Y1 (1 S )Y2 * S (Y2 Y2 * ) 1 ln[ ] * 1 S Y2 Y2
NOG
1 Y1 Y2 ln[( 1 S ) S] * 1 S Y2 Y2
*
mqnG S ——脱吸因数。平衡线斜率和操作线斜率的比值 qnL
无因次。S愈大,脱吸愈易进行。
2)塔的工艺尺寸,塔径和填料层高度
2018/10/6
一、吸收塔的物料衡算与操作线方程
化工原理第六章4资料

2017/10/10
2017/10/10
为实现分离操作,需要: • • 若干层塔板的精馏塔; 塔底-再沸器(精馏釜)-上升蒸 汽;
• 塔顶-冷凝器-下降的液流(回 流);
• 原料液从塔内合适位置加入塔内, 并与塔内气液混合。
连续精馏操作流程
精馏段:进料板上的塔板,物系的
易挥发组成含量比进料的含量高。 精馏段的作用:使气相浓度不断 变高,即不断增浓,以得到合格 的塔顶产品;
连续精馏中物相组成的变化
Xn-1
溢流 管 y
n
(n+1)层上升蒸汽通过 n层板 上的小孔上升,
塔 板
yn+1 xn
(n-1)层液体通过溢流管下 降到n层板上,在该塔板上横 向流动进入下一层塔板。
气相组成yn+1(部分冷凝) ⇔ 液相组成xn-1(部分汽化)
塔板上的液层,
填料湿表面
热量和质量交换的场所
xF <y1<y2<y3→yA→1
可使液相多次部分气化
xF>x1>x2>x3→xA→0 精馏可使混合液得到几乎完全的分离;
3. 精馏是多次部分汽化与多次部分冷凝的联合操作
由图可知, X1 <XF <Y1 , X1 <X2 <Y1 , X2 与XF 比较接近, X3 与Y1 比较接近,若将 第二级产生的中间产品 X2 于第一级的原 料XF 混合,X3 与Y1 混合这样消除了中间 产品。由于温度较高的蒸汽与温度低的 X3 确接触,使液体部分气化,蒸汽自身被冷 凝,省去了中间加热器与冷凝器。
实现组分高纯度分离的关键技术是回流,这也是精馏
与其它蒸馏过程的本质区别。
2017/10/10
塔顶上升蒸汽被冷凝器冷凝后的液体,一部分引回到塔 内的第一块塔板,此液体称为回流液,另一部分作为产品 采出。
2017/10/10
为实现分离操作,需要: • • 若干层塔板的精馏塔; 塔底-再沸器(精馏釜)-上升蒸 汽;
• 塔顶-冷凝器-下降的液流(回 流);
• 原料液从塔内合适位置加入塔内, 并与塔内气液混合。
连续精馏操作流程
精馏段:进料板上的塔板,物系的
易挥发组成含量比进料的含量高。 精馏段的作用:使气相浓度不断 变高,即不断增浓,以得到合格 的塔顶产品;
连续精馏中物相组成的变化
Xn-1
溢流 管 y
n
(n+1)层上升蒸汽通过 n层板 上的小孔上升,
塔 板
yn+1 xn
(n-1)层液体通过溢流管下 降到n层板上,在该塔板上横 向流动进入下一层塔板。
气相组成yn+1(部分冷凝) ⇔ 液相组成xn-1(部分汽化)
塔板上的液层,
填料湿表面
热量和质量交换的场所
xF <y1<y2<y3→yA→1
可使液相多次部分气化
xF>x1>x2>x3→xA→0 精馏可使混合液得到几乎完全的分离;
3. 精馏是多次部分汽化与多次部分冷凝的联合操作
由图可知, X1 <XF <Y1 , X1 <X2 <Y1 , X2 与XF 比较接近, X3 与Y1 比较接近,若将 第二级产生的中间产品 X2 于第一级的原 料XF 混合,X3 与Y1 混合这样消除了中间 产品。由于温度较高的蒸汽与温度低的 X3 确接触,使液体部分气化,蒸汽自身被冷 凝,省去了中间加热器与冷凝器。
实现组分高纯度分离的关键技术是回流,这也是精馏
与其它蒸馏过程的本质区别。
2017/10/10
塔顶上升蒸汽被冷凝器冷凝后的液体,一部分引回到塔 内的第一块塔板,此液体称为回流液,另一部分作为产品 采出。
优秀工程类本科课件《化工原理》第6章 蒸馏

10
拉乌尔定律: pA=pAo xA pB= pBo xB= pBo(1- xA)
pA , pB — 溶液上方A和B两组分的平衡分压,Pa pao , pBo — 同温度下,纯组分A和B的饱和蒸汽压,Pa; xA , xB — 分别为混合液组分A和B的摩尔分率
11
二、 理想溶液气液相平衡
(一)理想溶液 t ~ y ~ x 关系式
组分的挥发度: 是该物质挥发难易程度的标志,表示。
纯组分的挥发度: = pAo
混合液某组分挥发度:
A
pA xA
,
理想溶液:
A
pA xA
pAo xA xA
pAo
B
pB xB
B
pB xB
pBo xB xB
pBo
15
2. 相对挥发度(以α表示)
一般物系:
pA
A xA
B
pB xB
理想气体: 或:
46
确定最佳进料位置
• 图解法求最佳进料板:跨越两操作线交点的梯级。 • 以此为进料板时NT最少。 例 6-9
47
(二)理论板数的逐板计算法 塔顶全凝器 泡点回流 泡点进料 塔釜间接蒸汽加热
精馏段:
x1
F, xF x2
xn
xm-1
y1 1 y2 2
n ym-1
m-1
yW
D, xD W, xW
y1=xD 平 衡 关 系 x1 操 作 关 系 y2 平 衡 关 系 x2 • • • xn xF
q线方位
L与L’
V与V’
L' L F L' L F
V V' V V'
L' L
V V'
拉乌尔定律: pA=pAo xA pB= pBo xB= pBo(1- xA)
pA , pB — 溶液上方A和B两组分的平衡分压,Pa pao , pBo — 同温度下,纯组分A和B的饱和蒸汽压,Pa; xA , xB — 分别为混合液组分A和B的摩尔分率
11
二、 理想溶液气液相平衡
(一)理想溶液 t ~ y ~ x 关系式
组分的挥发度: 是该物质挥发难易程度的标志,表示。
纯组分的挥发度: = pAo
混合液某组分挥发度:
A
pA xA
,
理想溶液:
A
pA xA
pAo xA xA
pAo
B
pB xB
B
pB xB
pBo xB xB
pBo
15
2. 相对挥发度(以α表示)
一般物系:
pA
A xA
B
pB xB
理想气体: 或:
46
确定最佳进料位置
• 图解法求最佳进料板:跨越两操作线交点的梯级。 • 以此为进料板时NT最少。 例 6-9
47
(二)理论板数的逐板计算法 塔顶全凝器 泡点回流 泡点进料 塔釜间接蒸汽加热
精馏段:
x1
F, xF x2
xn
xm-1
y1 1 y2 2
n ym-1
m-1
yW
D, xD W, xW
y1=xD 平 衡 关 系 x1 操 作 关 系 y2 平 衡 关 系 x2 • • • xn xF
q线方位
L与L’
V与V’
L' L F L' L F
V V' V V'
L' L
V V'
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
q
qnL qnL qnF
iV i F iV i L
将1kmol进料变为饱和蒸汽所需热量 原料液的kmol汽化潜热
(1)对于泡点进料
iF iL
2012-12-15
q
iV iF iV iL
1
qnL
qnF qnL'
qnV
qnF qnV qnL
qnV
qnL
qnV
qnV
100.0 qnD qnW
100.0 0.4504 qnD 0.9787 qnW 0.0212
qnD 44.3kmol / h qnW 55.7kmol / h
(2)上升蒸汽量及回流量 精馏段:qnL Rq nD 3 44.8 134.5kmol / h
NT=Nmin •R↑ qnD、qnW不变qnL、qnV↑
2012-12-15
xD/R+1
R↓
xD/R+1↑ N↑
ab上移 a y N=∞ b c xW xF x xD f d
ab、q线与平衡线交于d
R=Rmin
Rmin< R <R∞
2012-12-15
xD/R+1
d点夹紧点
e
2、全回流及最少理论板层数
100%
2012-12-15
2、精馏段操作线方程
对总物料:
qnV
qnL
qnD
qnV qnL qnD
对易挥发组分:
qnF
qnV y n 1 qnL xn qnD x D
2012-12-15
y n 1
qnL qnL qnD
xn
qnD qnL qnD
xD
R R 1
qnD x D qnW x w qnF x F
qnV qnV ( q 1)qnF
qnL qnL qqnF
y
q q 1
x
xF q 1
——q线方程或进料方程
2012-12-15
d)进料热状况对q线及操作线的影响
•过冷液体: q>1, •饱和液体: q=1,
qnD x D qnF x F
qnF x F qnD
•塔顶产品的组成应满足 x D
2012-12-15
塔顶易挥发组分回收率:易挥发组分从塔顶采出的量占全部
进料量中轻组分的百分数。
D
qnD x D qnF x F
100%
塔底难挥发组分回收率:
W
qnW (1 xW ) qnF (1 x F )
qnV qnL qnD 134.5 44.83 179.3kmol / h
2012-12-15
(3)47℃进料时 qnV 、qnL
将料液由47℃升温到93℃所需的热量为:
iL iF 158.2 (93 47) 7277.2KJ / Kmol
q
iV i F iV i L
1
xA x B D
第一层板和第二层板之间的操作关系为:yA2=xA1 ,yB2=xB2 即
组成也可视为均匀的。
2、操作关系
yn+1与xn之间的关系
3、恒摩尔汽化
qnV qnV 2 ...... qnV qnV qnV1 qnV ......qnV qnV
1 n
2 m
2012-12-15
4、恒摩尔溢流
qnL qnL ...... qnL qnL
平衡关系
x1
操作关系
y2 R R 1 x1 xD R 1
qnF
y2
2012-12-15
平衡关系
x2
操作关系
y3
……
xn xF
精馏段
泡点进料 n-1层
2)提馏段 提馏段操作线
x1 xn(已知)
y2 qnL qqnF qnL qqnF qnW x1 qnW qnL qqnF qnW xW
q q 1 0
,ef1 ( )
q q 1
,ef2 (↑)
q 0 ,ef3 (
•汽液混合物 :0<q<1,
•饱和蒸汽:q=0, •过热蒸汽:q<0,
2012-12-15
q 1
)
q q 1 q q 1
0 ,ef4 (←) 0 ,ef ( 5
)
f2 f4 f5 f3
f1
2012-12-15
全回流时,qnD=0, qnF=0,qnW=0 ;达到给定分离程度
所需的理论板层数最少为Nmin。
1)Nmin的求法 a)图解法
xW
2012-12-15
xD
b)解析法——芬斯克(Fenske)方程式 全回流时操作线方程式为:yn+1=xn
∴(yA)n+1=(xA)n,(yB)n+1=(xB)n
离开任一层板的汽液组成间的关系为:
qnL
qnF
qnL'
qnV qnL
qnL'
qnV
qnV
qnF
qnF qnL' qnV qnL' qnV
2012-12-15
qnL qnF qnL
(2)对于饱和蒸汽进料
qnV qnV
iF iV
qnL qnL
q
iV iF iV iL
0
qnV qnV qnF
q qnL qnL qnF
qnL qnL qqnF
qnF qnV qnL qnV qnL
qnV qnV ( q 1)qnF
提馏段操作线方程为:
y m 1
qnL qqnF qnL qqnF qnW
xm
qnW qnL qqnF qnW
xw
2012-12-15
例:用一连续精馏装置在常压下,分离含苯41%(质 量%,下同)的苯-甲苯溶液。要求塔顶产品中含苯不低于 97.5%,塔底产品中含甲苯不低于98.2%,每小时处理的原
料量为8570kg。操作回流比为3,试计算:
(1)塔顶及塔底的产品量;
(2)精馏段上升蒸汽量及回流液量;
(3)当原料于47℃进塔和饱和蒸汽进塔时,提馏段上升 蒸汽量及回流液量 。
qnV '
qnD
qnF qnD qnW
对于易挥发组分:
qnF x F qnD x D qnW xW
qnL' qnW
2012-12-15
qnD qnF
x F xW x D xW
qnW qnF
1
qnD qnF
•当塔顶、塔底产品组成xD、xW及产品质量已规定,产品的 采出率qnD/qnF和qnW/qnF也随之确定,不能再自由选择; •当规定塔顶产品的产率和质量xD,则塔底产品的质量xW及 产率也随之确定而不能自由选择; •在规定分离要求时,应使
qnL qqnF qnL qqnF qnW
'
xW
x xW
y xW
y x
2012-12-15
a
y b c xW xF x xD
f
d
e
2012-12-15
c)q线方程
qnV y qnL x qnD x D- qnV y qnL x qnW x w
( qnV qnV ) y ( qnL qnL ) x ( qnD x D qnW xw )
xn
1 R 1
xD
——精馏段操作线方程
R
qnL qnD
——回流比
2012-12-15
3、提馏段操作线方程
对总物料:
qnF
qnL' qnV '
qnL qnV qnW
对易挥发组分:
qnL xm qnV ym1 qnW x w
qnw
提馏段操作线方程:
qnL qnL qnW xm qnW qnL qnW xw
2)图解方法 2 1 1‘ a
3
4 5 b 6 d e
f
c xW xF xD
2012-12-15
3、最宜的进料位置
2012-12-15
四、回流比的影响及其选择
1、回流比对精馏操作的影响
•R↑ xD/R+1↓ ab 下移 y b c xW xF x xD f d e a
NT↓ R=∞ ab与ac重合
2012-12-15
(已知:原料液泡点温度为93℃,混合液体的平均摩尔比热容 为158.2 kJ/(kmol.K),饱和液体变为饱和蒸汽所需的摩尔汽化热 为33118 kJ/kmol)。
分析: 求qnW、qnD 全塔物料衡算 求xF、xW、xD
求qnV、qnL 求qnV 、qnL
已知R
精馏段物料衡算 求q
qnL qnL qqnF
qnV qnV ( q 1)qnF
2012-12-15
解: (1)产品量
xF 41 / 78 41 / 78 59 / 92
0.4504
xD
97.5 / 78 97.5 / 78 2.5 / 92
1.8 / 78 1.8 / 78 98.2 / 92
饱和蒸汽进料时 q
qnV qnV qnF
iV i F iV i L
0 qnL qnL 134.5kmol / h
179.3 100
79.3kmol / h
