原子物理学第四章碱金属原子PPT课件
合集下载
碱金属元素PPT课件4 人教课标版

1.与非金属反应
• 4Li + O2 • 2Na + O2 • K + O2
点燃 点燃
2Li2O Na2O2
点燃
•铷和铯遇到空气就会立即燃烧。钾、铷等碱金属与O2反 应,生成比过氧化物更复杂的氧化物。 •除与氧气反应外,碱金属还能与氯气等大多数非金属起 反应,表现出很强的金属性,且Li—C成课后的习题。
• • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • •
41、从现在开始,不要未语泪先流。 42、造物之前,必先造人。 43、富人靠资本赚钱,穷人靠知识致富。 44、顾客后还有顾客,服务的开始才是销售的开始。 45、生活犹如万花筒,喜怒哀乐,酸甜苦辣,相依相随,无须过于在意,人生如梦看淡一切,看淡曾经的伤痛,好好珍惜自己、善待自己。 46、有志者自有千计万计,无志者只感千难万难。 47、苟利国家生死以,岂因祸福避趋之。 48、不要等待机会,而要创造机会。 49、如梦醒来,暮色已降,豁然开朗,欣然归家。痴幻也好,感悟也罢,在这青春的飞扬的年华,亦是一份收获。犹思“花开不是为了花落,而是为了更加灿烂。 50、人活着要呼吸。呼者,出一口气;吸者,争一口气。 51、如果我不坚强,那就等着别人来嘲笑。 52、若不给自己设限,则人生中就没有限制你发挥的藩篱。 53、希望是厄运的忠实的姐妹。 54、辛勤的蜜蜂永没有时间悲哀。 55、领导的速度决定团队的效率。 56、成功与不成功之间有时距离很短只要后者再向前几步。 57、任何的限制,都是从自己的内心开始的。 58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。 59、不要说你不会做!你是个人你就会做! 60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。 61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。 62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。 63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。 64、每一个发奋努力的背后,必有加倍的赏赐。 65、再冷的石头,坐上三年也会暖。 66、淡了,散了,累了,原来的那个你呢? 67、我们的目的是什么?是胜利!不惜一切代价争取胜利! 68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。 69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。 70、平凡的脚步也可以走完伟大的行程。 71、胜利,是属于最坚韧的人。 72、因害怕失败而不敢放手一搏,永远不会成功。 73、只要路是对的,就不怕路远。 74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。 75、自己选择的路,跪着也要走完。 76、当你的希望一个个落空,你也要坚定,要沉着! 77、蚁穴虽小,溃之千里。 78、我成功因为我志在成功! 79、凡真心尝试助人者,没有不帮到自己的。 80、相信自己,你能作茧自缚,就能破茧成蝶。 81、偶尔,只需要一个鼓励的微笑,就可以说服自己继续坚强下去。 82、年轻是本钱,但不努力就不值钱。 83、一时的忍耐是为了更广阔的自由,一时的纪律约束是为了更大的成功。 84、在你不害怕的时间去斗牛,这不算什么;在你害怕时不去斗牛,也没有什么了不起;只有在你害怕时还去斗牛才是真正了不起。 85、能把在面前行走的机会抓住的人,十有八九都会成功。 86、天赐我一双翅膀,就应该展翅翱翔,满天乌云又能怎样,穿越过就是阳光。 87、活鱼会逆流而上,死鱼才会随波逐流。 88、钕人总是把男人的谎言当作誓言去信守。 89、任何业绩的质变都来自于量变的积累。 90、要战胜恐惧,而不是退缩。
原子物理学 课件-第四章 碱金属原子和电子自旋

价电子轨道分为两部分: i、在原子实外运动,受原子实库仑场作用,有效电荷
光谱项: 能级因极化下降不太多 ii、价电子进入原子实内:
原子物理学
iii、 都很大,价电子轨道离原子实很远,极化, 贯穿不再发生,碱金属原子能级与氢原子能级差别小。
原子物理学
§4.3 碱金属原子光谱精细结构 一、精细结构
用高分辩本领的光谱仪观察碱金属光谱,每条谱 线又由更精细的两条或三条谱线组成。 例:钠,主线系第一谱线,
二、价电子运动:决定光谱、化学性质 (1)价电子远离原子实: 大, 大, 能级接近氢原子
(2)价电子靠近原子实: 小, 小,两种情况: 原子实极化,轨道贯穿。
原子物理学
1、原子实极化: 没有价电子作用时,原子实内部正、负 电荷中心重合。
价电子靠近原子实,正、负电荷中心不再重合,原 子实被极化形成电偶极子,偶极子电场反作用于电 子,产生附加吸引力,引起能量降低。
Ⅰ:
Ⅱ:
柏:
元素 234567
原子物理学
§4.2 碱金属光谱解释 原子实极化 轨道贯穿
一. 碱金属原子实模型
括号内电子排布 形成稳定完整结 构
原子物理学
原子实:碱金属原子中,除价电子以外的其余部 分,是一稳定结构,带单位正电荷。
原子实=核+2个电子. 占据 轨道
原子实=核+10个电子,占据 轨道,以下类推。
用极化概念解释同一 的能级分裂:
同一
小,轨道偏心率大, 价电子靠近原子实,极 化很强,能级下降多;
大,轨道偏心率小, 价电子远离原子实,极 化很弱,能级下降少
引起同一 . 由于 不同 的能级分裂
原子物理学
2、转道贯穿 当价电子处于 小,偏心率大的轨道上运动时,其 轨道可能贯入原子实内部,引起能级降低的 现象。
光谱项: 能级因极化下降不太多 ii、价电子进入原子实内:
原子物理学
iii、 都很大,价电子轨道离原子实很远,极化, 贯穿不再发生,碱金属原子能级与氢原子能级差别小。
原子物理学
§4.3 碱金属原子光谱精细结构 一、精细结构
用高分辩本领的光谱仪观察碱金属光谱,每条谱 线又由更精细的两条或三条谱线组成。 例:钠,主线系第一谱线,
二、价电子运动:决定光谱、化学性质 (1)价电子远离原子实: 大, 大, 能级接近氢原子
(2)价电子靠近原子实: 小, 小,两种情况: 原子实极化,轨道贯穿。
原子物理学
1、原子实极化: 没有价电子作用时,原子实内部正、负 电荷中心重合。
价电子靠近原子实,正、负电荷中心不再重合,原 子实被极化形成电偶极子,偶极子电场反作用于电 子,产生附加吸引力,引起能量降低。
Ⅰ:
Ⅱ:
柏:
元素 234567
原子物理学
§4.2 碱金属光谱解释 原子实极化 轨道贯穿
一. 碱金属原子实模型
括号内电子排布 形成稳定完整结 构
原子物理学
原子实:碱金属原子中,除价电子以外的其余部 分,是一稳定结构,带单位正电荷。
原子实=核+2个电子. 占据 轨道
原子实=核+10个电子,占据 轨道,以下类推。
用极化概念解释同一 的能级分裂:
同一
小,轨道偏心率大, 价电子靠近原子实,极 化很强,能级下降多;
大,轨道偏心率小, 价电子远离原子实,极 化很弱,能级下降少
引起同一 . 由于 不同 的能级分裂
原子物理学
2、转道贯穿 当价电子处于 小,偏心率大的轨道上运动时,其 轨道可能贯入原子实内部,引起能级降低的 现象。
八年级物理《碱金属》课件

实验步骤详解
1. 准备试剂与仪器
与酸反应实验
火焰颜色实验
3. 安全注意事项
与水反应实验
观察碱金属单质的外观和物理性质
准备好所需碱金属元素(如锂、钠、钾等)的单质或其化合物,以及相应的试剂(如酸、碱等)和实验仪器(如试管、烧杯、滴管、电子天平等)。
记录各碱金属单质的颜色、光泽、硬度等物理性质。
分别取少量碱金属单质,加入盛有水的试管中,观察并记录反应现象(如剧烈程度、颜色变化等)。
利用还原剂在高温下将碱金属离子还原为单质,如用金属钙还原氯化钾可得到金属钾。
利用某些有机溶剂对碱金属的选择性溶解作用,将碱金属从混合物中分离出来。
电解法
热还原法
溶剂萃取法
演示电解熔融氯化钠的实验,展示电解过程中产生的现象和产物。
01
演示电解熔融氯化钠的实验,展示Байду номын сангаас解过程中产生的现象和产物。
02
演示电解熔融氯化钠的实验,展示电解过程中产生的现象和产物。
THANK YOU
感谢聆听
演讲人姓名
202X.00.00
碱金属的碳酸盐易溶于水,且稳定性随金属活泼性增强而降低。例如,碳酸钠(Na2CO3)和碳酸钾(K2CO3)是常见的碱金属碳酸盐。
配合物及其性质
配合物的形成
碱金属离子可以与某些阴离子或分子形成配合物。例如,钠离子可以与氯离子形成氯化钠配合物(Na[Cl])。
配合物的性质
配合物通常具有与简单离子不同的物理和化学性质。例如,配合物的颜色、溶解度和稳定性等可能与相应的简单离子有所不同。此外,配合物在化学反应中可能表现出特殊的反应活性。
碱金属在自然界中存在形态及提取方法
第四章
存在形态
第四章碱金属原子和电子自旋PPT课件
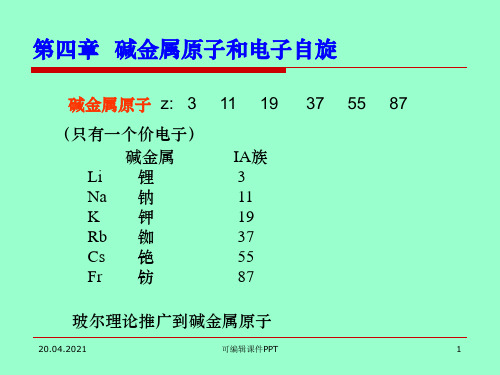
柏格曼系:
vfn
(3Rd)2
R (nf
)2
n=4.5.6...
nf 3d
20.04.2021
可编辑课件PPT
16
特点规律(以锂为例)
主线系: np 2s 第二辅线系: ns 2p 第一辅线系: nd 2p 柏格曼系: nf 3d
n=2.3.4… n=3.4.5…. n=3.4.5….. n=4.5.6...
线 系 限 : n , vv(m R l)2
20.04.2021
可编辑课件PPT
13
2、线系公式
锂的四个线系
主线系:
vpn
R (2s)2
R (np)2
R
R
第二辅线系: vsn (2p)2 (ns)2
n=2.3.4… np 2s n=3.4.5…. ns 2p
第一辅线系:
vdn
R (2p)2
20.04.2021
可编辑课件PPT
9
子价 电
电子态 原子态
l 0 4s, 4S
n
4,
l l
1 4 p, 2 4d,
4P 4D
l 3 4 f , 4F
依次类推
得到如下能级图
20.04.2021
可编辑课件PPT
10
0 5s
10000 4s
3s 20000
30000
40000 2s
cm-1
3s 3p 3d n =4 l =0 l =1 l =2 l =3
4s 4p 4d 4f
有没有 2d, 3f, 4g? 为什么? l=0,1,2,….,n-1
原子态(用大写字母): S P D F G H I K nL 表示原子态
第四章碱金属PPT优选课件

3
三.钠的化学性质
1.与氧气反应:
2. 常温: +1 -2 3. 4Na+O=2=2Na2O (白色)
氧化钠
点2N燃a:+O点2=燃=N+1a2O-(12 淡黄色)
2020/10/18
过氧化钠
沙头角中学 梁洪明
4
2. 与氯气、硫的反应
点燃
2 Na + Cl2 == 2 NaCl
研磨
2Na + S == Na2S
2020/10/18
沙头角中学 梁洪明
11
[练习]
1.钠在空气中长时间放置最终
将转化为_N__a_2C__O__3_.
有关化学方程式为:
(1)4Na+O2==2Na2O
(2)Na2O+CO2==Na2CO3
(3)2Na+2H2O==2NaOH+H2
(4)2NaOH+CO2==Na2CO3+H2O
2020/10/18
沙头角中学Байду номын сангаас梁洪明
12
2. 将一小块金属钠投入氯化铁 溶液中的化学方程式为:
6N—a+—6—H—2O—+—2—Fe—C—l3—=+—2_6F_—Ne_—(a_OC—_Hl_—+_)3—3_H—_2_— 离子方程式为:
6Na+6H2O+2Fe3+=2Fe(OH)3 ———————————+6—N—a—++—3—H—2 —
2020/10/18
沙头角中学 梁洪明
13
3. 将Na、Zn、Fe和Al四种金属
各0.2mol,分别投入100mL
§4.1 碱金属原子的光谱(PPT-YBY)

说明:以上给出的光谱线系图,是发射光谱。若观察吸收光谱 则只能观察到与主线系相对应的吸收光谱。这是因为,只有主 线系与原子的基态相联系,而产生吸收光谱的物质一般都处于 基态。 2、光谱项的表达式 里德伯碱金属原子光谱的公式 (1) (2) (3)
RA RA 1 vn T v (固) T( 动) 2 2 n n n 2
图1.3 氢原子和碱金属原子(锂)能级及跃迁示意图
图1.3 氢原子和 碱金属原子(锂、 钠)能级及跃迁 示意图
二、光谱的特征 1、碱金属原子光谱的四组谱线分类:(以锂Li原子为例) (1)主线系 np 2s 系限:(229.97nm) 紫外到可见
(2)锐线系,又称第二辅线系:ns 2p 系限:(349.9nm) 第一条红外,其余可见
第04章 原子的精细结构:电子的自旋
§4.1 碱金属原子的光谱
1 1 2 2 n n
里德伯公式 RH
系限 第一项是固定项,是跃迁末态 第二项是动项,是跃迁初态
一、碱金属原子光谱的特征 1、氢原子结构及能级
mz 2 e4 hcz 2 R En 2 2 2 2 (4 0 ) 2 n n
三、碱金属原子光谱的精细结构: 1、精细结构及特征: (1)主线系和锐线系(第二辅线系)分裂为两条线。
主线系: p : p (n)
p
: ( n ) 锐线系(第二辅线系: s s
s
(2)第一辅线系(漫)和柏格曼线系(基)分裂为三条。
d13
s
: (n) d12 d
能级只于量子数n有关 2、碱金属原子的结构、光谱及能级 (1)碱金属原子的结构: 原子实和一个价电子构成,见图1.1
原子结构与元素的性质(碱金属) 课件(共13张PPT)高中化学人教版(2019)必修 第一册

②、金属性强弱有哪些判断依据?
金属单质与水反应越容易
金属性越强
最高价氧化物对应水化物的碱性越强
金属性越强
碱性:KOH >NaOH
金属性:K > Na
碱金属性质 · 总结
碱金属性质特点:与Na相似
碱金属化学性质 · 总结
与O2反应
反
Li2O
应
更
Na2O、Na2O2
剧
烈
K2O、K2O2、KO2
、
产
更复杂
碱金属性质
结构
性质
相 似 性
易失e-
最外层电子数=1
元素:金属性 单质:还原性
递
电子层数增多
变
性
原子半径增大
失电子更容易
元素:金属性增强 单质:还原性增强
碱金属性质 · 应用 任务1
预测K的化学性质
①、与O2反应
4Na+O2 == 2Na2O 2Na+O2 == Na2O2
最外层电子数相等 性质相似
物 更
复
更更复杂 LiOH
略微缓慢
更
剧 NaOH
剧烈
烈
、 KOH 更剧烈、轻微爆炸
产
物 RbOH 遇水即燃、爆炸 碱
更 强
CsOH 遇水即燃、剧烈爆炸
碱金属物理性质 · 总结
Li
Na
K
Rb
锂是最轻的金属,保存在石蜡里,Na、K保存在煤油中
碱金属单质 Li Na K Rb Cs
颜色和状态 银白色,柔软 银白色,柔软 银白色,柔软 银白色,柔软 略带金属光泽,柔软
更复杂
②、与H2O反应
2Na+2H2O == 2NaOH+H2↑
更剧烈
第四章碱金属原子和电子自旋优秀课件

极化而成的电偶极子的电场又作用于价电子, 使它感受到除库仑场以外的另加的吸引力,有 效电荷不再为一个单位的正电荷,这就引起能 量的降低。
back
next 目录 结束
对于同一 n 值,L 值较小的轨道是
偏心率较大的椭圆轨道,当电子运 动到一部分轨道上时,由于离原子 实很近,所以引起较强的极化,对 能量的影响大;
R n2
(ZnR*)2
nR*2
n*
n Z*
T
R n*2
R n2
EhcnR*2 hcnR2
<n
小 贯穿几率大 能量低
E n sE n pE n dE n f E n
综上,原子实 极化和价电子 的轨道贯穿两 种效应,使得 碱金属原子能 级分裂,且都 使得能量下降; 值小的能级, 下降较明显。
4.量子力学定量处理
2. 原子实极化
原子实是一个 球形对称的结构, 它里边的原子核
带有Ze正电荷和 (Z-1)e负电荷,
在原子最外层运 动的价电子好象 是处在一个单位 正电荷的库仑场 中,当价电子运 动到靠近原子实 时,
back
next 目录 结束
由于价电子的电场作用,原子实中带正电 的原子核与带负电的电子的中心会发生微小 的偏移,于是负电的中心不再在原子核上, 形成一个电偶极子。这就是原子实的极化。
碱金属原子:带一个正电荷的原子实 + 一个价电子
( H原子:带一个正电荷的原子核+一个电子 )
价电子如被激发到能量高状态上,则从能量高状态向下跃迁 时将发射光谱。
非贯穿轨道贯穿轨道 Nhomakorabea价电子的轨道运动
• 由于原子实的存在,价电子轨道运动有两 种情况是氢原子中所没有的,这就是
back
next 目录 结束
对于同一 n 值,L 值较小的轨道是
偏心率较大的椭圆轨道,当电子运 动到一部分轨道上时,由于离原子 实很近,所以引起较强的极化,对 能量的影响大;
R n2
(ZnR*)2
nR*2
n*
n Z*
T
R n*2
R n2
EhcnR*2 hcnR2
<n
小 贯穿几率大 能量低
E n sE n pE n dE n f E n
综上,原子实 极化和价电子 的轨道贯穿两 种效应,使得 碱金属原子能 级分裂,且都 使得能量下降; 值小的能级, 下降较明显。
4.量子力学定量处理
2. 原子实极化
原子实是一个 球形对称的结构, 它里边的原子核
带有Ze正电荷和 (Z-1)e负电荷,
在原子最外层运 动的价电子好象 是处在一个单位 正电荷的库仑场 中,当价电子运 动到靠近原子实 时,
back
next 目录 结束
由于价电子的电场作用,原子实中带正电 的原子核与带负电的电子的中心会发生微小 的偏移,于是负电的中心不再在原子核上, 形成一个电偶极子。这就是原子实的极化。
碱金属原子:带一个正电荷的原子实 + 一个价电子
( H原子:带一个正电荷的原子核+一个电子 )
价电子如被激发到能量高状态上,则从能量高状态向下跃迁 时将发射光谱。
非贯穿轨道贯穿轨道 Nhomakorabea价电子的轨道运动
• 由于原子实的存在,价电子轨道运动有两 种情况是氢原子中所没有的,这就是
原子物理学 课件-第四章 碱金属原子和电子自旋

原子物理学
证:设是机械自旋 电子半径: 电荷: 磁矩:
安束2(焦/特)
(超过光速)
因此,电子自旋不是机械自旋
(电子自旋,其实一点也没有“自旋”的意义。最好称呼它 为“内禀角动量”,它是微观粒子内部属性,与运动状态毫 无关系。它的性质与角动量类似,但不能用任何经典语言 描述。在经典物理中,找不到对立物)。
原子物理学
二、由光谱精细结构推断碱金属原子能级(以锂为例)
1、二辅系: 的跃迁,由于双线间隔相 等,设想 能级不分裂,单层,p能级分裂,双层。 末态p能级:各能级共 同有关,双线间隔为 2p能级分裂间隔。
2、主线系: 的跃迁,双线间隔随 增 大而减小,p能级分裂间隔随 增大而逐渐减小
原子物理学
原子物理学
(2)自旋取向的意义:
原子实坐标
电子坐标 一个顺着磁场 一个逆着磁场
电子自旋取向:
原子物理学
二、从轨道,自旋角动量的耦合 看能级双分裂
角动量耦合:已知
求:总角动量
原子物理学
1、玻尔理论
与
夹角0,
2、量子力学
从上式可看出,
与
不能平行或反平行
原子物理学
三个终端 主 Ⅰ Ⅱ 柏
光谱项: 若测得T, 则可算得
每一线系限波数 恰为另一线系动 项中最大的一个
原子物理学
对于锂, 表4.1给出, (三)两个量子数 仿效氢光谱:
碱光谱:
即碱原子能量与两个量子数
碱金属原子能级图。
有关.
(1)对同一个主量子数 ,有几个能级 (2)能级按 分类, 相同属同一例
1925年,荷兰:两位大学生,库仑贝克,古兹密特 一)电子自旋假设: 1、每个电子都具有固有的自旋角动量
原子物理第四章-PPT课件
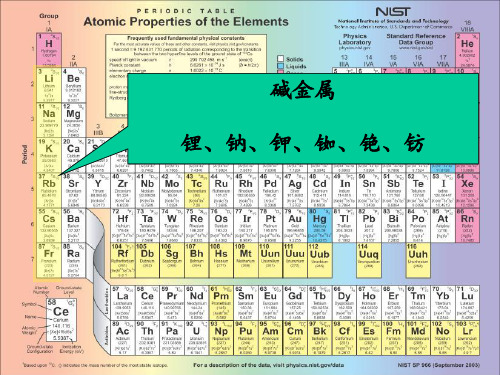
R 所以, T(n) (n)2
辅系最大,主线系、一 辅系、柏格曼线系次之
碱金属原子的光谱线: n
R n*2
~
(n
R )2
.
7
3. 碱金属原子光谱的规律
里德堡发现,碱金属原子的线系之间满足一定的关系:
(1)主线系线系限的波数,恰好等于第二辅线系的第二谱项 值中最大的。
(2)第一辅线系和第二辅线系的线系限的波数相等,其都恰 好等于主线系的第二谱项值中最大的。
结论: (1) n越小,极化效应越显著
(2) 相同的n, l 越小, 轨道贯穿效应越显著, 极化效应也越显著
(3) 在s, p轨道上发生贯穿(能量降低较大)
(4) 在d, f 轨道上,只发生极. 化(能量降低较小)
14
§4-3. 碱金属原子光谱的精细结构
一、光谱的精细结构
对碱金属原子的光谱,用分辨本领足够高的光学仪器 进行观察,会发现每一条光谱线并不是简单的一条线,而 是由两条或三条靠的很近的线组成的,这些线称为光谱的 精细结构(Fine structure)。
.
12
同一n
l大,轨道圆,效应小。 l小,轨道扁,效应大。
同一l
n越大,轨道大,效应小。 n越小,轨道小,效应大。
二.价电子的轨道在原子实中的贯穿效应
当电子与原子实较近(即n小),且轨道又扁平(l小)时接
近原子实的那些轨道会穿过原子实,从而影响了能级。
轨道在原子实外:Z*(有效电荷数) = 1
e
轨道在原子实内:Z*(有效电荷数) > 1
D1=589.0nm, D2=589.6nm.
Na双黄线
.
16
二. 精细结构产生的原因
1. 第二辅线系(ns→xp): 每一条线中二成分间隔相同
《原子物理学》(褚圣麟)第四章-碱金属原子和电子自旋要点58页PPT

《原子物理学》(褚圣麟)第四章-碱金 属原子和电子自旋要点
11、用道德的示范来造就一个人,显然比用法律来约束他更有价值。—— 希腊
12、法律是无私的,对谁都一视同仁。在每件事上,她都不徇私情。—— 托马斯
13、公正的法律限制不了好的自由,因为好人不会去做法律不允许的事 情。——弗劳德
14、法律是为了保护无辜而制定的。——爱略特 15、像房子一样,法
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业,需 要决心 ,能力 ,组织 和责任 感。 ——易 卜 生 54、 唯 书 籍 不 朽。——乔 特
55、 为 中 华 之 崛起而 读书。 ——周 恩来
11、用道德的示范来造就一个人,显然比用法律来约束他更有价值。—— 希腊
12、法律是无私的,对谁都一视同仁。在每件事上,她都不徇私情。—— 托马斯
13、公正的法律限制不了好的自由,因为好人不会去做法律不允许的事 情。——弗劳德
14、法律是为了保护无辜而制定的。——爱略特 15、像房子一样,法
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业,需 要决心 ,能力 ,组织 和责任 感。 ——易 卜 生 54、 唯 书 籍 不 朽。——乔 特
55、 为 中 华 之 崛起而 读书。 ——周 恩来
第四章 碱金属原子和电子自旋PPT22页

谢谢
11、越是没有本领的就越加自命不凡。——邓拓 12、越是无能的人,越喜欢挑剔别人的错儿。——爱尔兰 13、知人者智,自知者明。胜人者有力,自胜者强。——老子 14、意志坚强的人能把世界放在手中像泥块一样任意揉捏。——歌德 15、最具挑战性的挑战莫过于提升自我。——迈克尔·F·斯特利
第四章 碱金属原子和电子自旋
11、获得的成功越大,就越令人高兴 。野心 是使人 勤奋的 原因, 节制使 人枯萎 。 12、不问收获,只问耕耘。如同种树 ,先有 根茎, 再有枝 叶,尔 后花实 ,好好 劳动, 不要想 太多, 那样只 会使人 胆孝懒 惰,因 为不实 践,甚 至不接 触社会 ,难道 你是野 人。(名 言网) 13、不怕,不悔(虽然只有四个字,但 常看常 新。 惜我的 身体, 我用智 慧和知 识充实 我的头 脑。 15、这世上的一切都借希望而完成。 农夫不 会播下 一粒玉 米,如 果他不 曾希望 它长成 种籽; 单身汉 不会娶 妻,如 果他不 曾希望 有小孩 ;商人 或手艺 人不会 工作, 如果他 不曾希 望因此 而有收 益。-- 马钉路 德。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
5 4
3
d =2
5 4
3
f =3
5 4
柏 格 曼 系
2 30000
40000
厘米-1
2
锂原子能级图
H 567 4 3 2
10
§4.2 原子实的极化和轨道贯穿
一、原子实模型 二、原子实极化、轨道贯穿 三、量子力学定量处理
碱金属原子的 价电子模型:
11
一、原子实模型
❖ 内层电子 与原子核结合的较紧密,而价电子 与核结合的很松,可以把内层电子和原子核看 作一个整体称为原子实。价电子绕原子实运动 ,原子的化学性质及光谱都决定于这个价电子 。
4
4s
3 3s
p
d
f
4p
4d
4f
3p
3d
2
特点:
2s Li基态
四系谱线,四个线系;
三个终端:2s,2p,3d; 二个量子数:n, l ;
一条选择定则: l 1
2p
注:除四线系外,高能级到 低能级的跃迁也有,只是强 度小与1/n3成正比.
9
4.能级图 s
0
=0
5 10000 4
3 20000
p =1
主线系:
~(2R s)2(nR p)2 ~2snp
第一辅线系: ~(2R p)2(nR d)2 ~2pnd
第二辅线系:
~ R R ~2pns
(2 p)2 (n s)2
柏格曼系:
~(3R d)2(nR f)2 ~3dnf
碱金属原子光谱项:
T
R n*2
R
n2
8
li 原子跃迁图: Li原子 s
主线系(Principle series): 红光, 紫外E>3.0, E<1.6
第一辅线系(Diffuse series):可见光, 由轮廓弥散的谱 线组成. (漫线系)
第二辅线系(Sharp series):红外, 可见光,由轮廓细锐的 谱线组成.(锐线系)
基线系(Bergmann series): 红外,与氢线系类似, E<1.6
R
(nΔ
)2
402 2(e2p 1)
18
与氢原子的差别
(1)能量由(n, )两个量子数决定,主量子数 相同,角量子数不同的能级不相同。各能级均低 于氢原子相应能级。 (2)对同一n值,不同值的能级,值较大的能级 与氢原子的差别较小;对同一值,不同n值的能级, n值较大的能级与氢原子的差别较小。 (3)n很大时,能级与氢的很接近,少数光谱线 的波数几乎与氢的相同。
❖ 3.光谱项为:
T
RZ 2 n2
R
R
改写后:
T
(
n Z
)2
所 以n2n*<n
15
a 非贯穿轨道
b 贯穿轨道
价电子的轨道运动
16
17
三、量子力学定量处理
远离原子实运动
V(r) Z*e2 4πε0r
靠近原子实运动 V(r)Z*e2 ep
能量和光谱项
40r 40r2
En
hcR (n Δ )2
T(n,)
第四章 碱金属原子和电子自旋
❖ [教学内容] ❖ §4.1 碱金属原子的光谱. ❖ §4.2 原子实的极化和轨道的贯穿. ❖ §4.3 碱金属原子光谱的精细结构. ❖ §4.4 电子自旋同轨道运动的相互作用. ❖ §4.5 单电子辐射跃迁的选择定则. ❖ §4.6 氢原子光谱的精细结构及兰姆移动.
❖ [教学重点] ❖ 碱金属原子光谱;电子自旋;单电子角动量的合成 ❖ 单电子跃迁选择定则 ❖ 原子光谱的精细结构 ❖ [教学难点] ❖ 电子自旋与轨道运动的相互作用 ❖ 碱金属原子光谱精细结构分析
❖ 锂原子的价电子的轨道:n* ≥ 2 ❖ 钠原子的价电子的轨道:n* ≥ 3 ❖ 原子实的有效电荷数 :Z*=Z-(Z-1)
=1
12
价电子远离原子实运动
相当于价电子在n 很大的轨道上运动, 价电子与原子实间的作用很弱,原子实电 荷对称分布,正负电荷中心重合在一起。 有效电荷为+e,价电子好象处在一个单位 正电荷的库仑场中运动,与氢原子模型完 全相似,所以光谱和能级与氢原子相同。
1
整体概述
概况一
点击此处输入相关文本内容 点击此处输入相关文本内容
概况二
点击此处输入相关文本内容 点击此处输入相关文本内容
概况三
点击此处输入相关文本内容 点击此处输入相关文本内容
2
4.1 碱金属原子光谱
引入: 碱金属光谱→能级→结构
中心: 碱金属原子光谱规律:四系; 三端; 两数; 一定则.
一. 碱金属原子光谱------结构相近, 明显分线系
限 条条
条
条
~1 ~; ~,~ 0; ~只有一个
~常;数 ~ 两个
~ 1 辅最 大 ~ 2 辅 ~ 主最大
~1 ~;
~,~;
~只有两个
22
二. 推理解释
4 3
Li原子
s
p
4s
4p
3p 3s
2 2p
2s
Li基态
d
f
4d 4f
3d
23
s
p
d
f
4
4s
4p
4d
4f
3
3p
3d
3s
2 主线系: 二辅:
3
图4.1 锂的光谱线系
4
Δ 几个光谱名词
一个线系的线系限:同一线系中最大的波数,或波数
公式中的第一个光谱项(不动的光谱项)。
原子的共振线:该原子从基态到第一激发态吸收的谱
线。一个原子共振线只有一条。
一个线系的主线:该线系的第一条谱线或该线系的波
数最小的谱线。
5
二、线系公式
❖ H原子光谱:~T(m )T(n)R(m 12n 12)
13
-e
价电子远离原子实
14
二、原子实极化、轨道贯穿
❖ 1.原子实极化(形成电偶极子),使电子又受到电 偶极子的电场的作用,能量降低,同一n值,越小
,极化越强。
❖ 2.轨道贯穿(电子云的弥散),对于那些偏心率很 大的轨道, 接近原子实的那部分还可能穿入原子实 发生轨道贯穿,这时Z*>1,从而使能量降低。
19
204.3 碱金属原子Fra bibliotek谱的精细结构1. 引入: 用高分辨率的仪器观察谱线,发现一条→二/三条
2.本节中心: 谱线精细结构→能级分裂
一.实验事实
~ 增加
主线 系:
二 辅
一
辅
线系 第4 第3 第2 第1
限 条条
条
条
21
主线 系:
二 辅
~ 增加
一 辅
主线系: 二辅: 一辅:
线系 第4 第3 第2 第1
❖ 当 n 时 , ~~T(m 系)限.mR2
1 1
R
n T m * T n * R ( m * 2 n * 2 ) n * 2
1.有效量子数
氢原子:主量子数n 是整数
碱金属原子 n *m * 不是整数有效量子数
2.量子数亏损 l nn* n * R T
6
3.光谱项
7
锂原子的四个线系,可用下列公式表示:
2p
2s
Li基态
~1 ~; ~,~0; ~只有一个
n 增加,ΔE下降
~常;数 ~ 两个 24
d
一辅:
左右两成分间隔取决于P能级双层,与二辅线同.
3
d =2
5 4
3
f =3
5 4
柏 格 曼 系
2 30000
40000
厘米-1
2
锂原子能级图
H 567 4 3 2
10
§4.2 原子实的极化和轨道贯穿
一、原子实模型 二、原子实极化、轨道贯穿 三、量子力学定量处理
碱金属原子的 价电子模型:
11
一、原子实模型
❖ 内层电子 与原子核结合的较紧密,而价电子 与核结合的很松,可以把内层电子和原子核看 作一个整体称为原子实。价电子绕原子实运动 ,原子的化学性质及光谱都决定于这个价电子 。
4
4s
3 3s
p
d
f
4p
4d
4f
3p
3d
2
特点:
2s Li基态
四系谱线,四个线系;
三个终端:2s,2p,3d; 二个量子数:n, l ;
一条选择定则: l 1
2p
注:除四线系外,高能级到 低能级的跃迁也有,只是强 度小与1/n3成正比.
9
4.能级图 s
0
=0
5 10000 4
3 20000
p =1
主线系:
~(2R s)2(nR p)2 ~2snp
第一辅线系: ~(2R p)2(nR d)2 ~2pnd
第二辅线系:
~ R R ~2pns
(2 p)2 (n s)2
柏格曼系:
~(3R d)2(nR f)2 ~3dnf
碱金属原子光谱项:
T
R n*2
R
n2
8
li 原子跃迁图: Li原子 s
主线系(Principle series): 红光, 紫外E>3.0, E<1.6
第一辅线系(Diffuse series):可见光, 由轮廓弥散的谱 线组成. (漫线系)
第二辅线系(Sharp series):红外, 可见光,由轮廓细锐的 谱线组成.(锐线系)
基线系(Bergmann series): 红外,与氢线系类似, E<1.6
R
(nΔ
)2
402 2(e2p 1)
18
与氢原子的差别
(1)能量由(n, )两个量子数决定,主量子数 相同,角量子数不同的能级不相同。各能级均低 于氢原子相应能级。 (2)对同一n值,不同值的能级,值较大的能级 与氢原子的差别较小;对同一值,不同n值的能级, n值较大的能级与氢原子的差别较小。 (3)n很大时,能级与氢的很接近,少数光谱线 的波数几乎与氢的相同。
❖ 3.光谱项为:
T
RZ 2 n2
R
R
改写后:
T
(
n Z
)2
所 以n2n*<n
15
a 非贯穿轨道
b 贯穿轨道
价电子的轨道运动
16
17
三、量子力学定量处理
远离原子实运动
V(r) Z*e2 4πε0r
靠近原子实运动 V(r)Z*e2 ep
能量和光谱项
40r 40r2
En
hcR (n Δ )2
T(n,)
第四章 碱金属原子和电子自旋
❖ [教学内容] ❖ §4.1 碱金属原子的光谱. ❖ §4.2 原子实的极化和轨道的贯穿. ❖ §4.3 碱金属原子光谱的精细结构. ❖ §4.4 电子自旋同轨道运动的相互作用. ❖ §4.5 单电子辐射跃迁的选择定则. ❖ §4.6 氢原子光谱的精细结构及兰姆移动.
❖ [教学重点] ❖ 碱金属原子光谱;电子自旋;单电子角动量的合成 ❖ 单电子跃迁选择定则 ❖ 原子光谱的精细结构 ❖ [教学难点] ❖ 电子自旋与轨道运动的相互作用 ❖ 碱金属原子光谱精细结构分析
❖ 锂原子的价电子的轨道:n* ≥ 2 ❖ 钠原子的价电子的轨道:n* ≥ 3 ❖ 原子实的有效电荷数 :Z*=Z-(Z-1)
=1
12
价电子远离原子实运动
相当于价电子在n 很大的轨道上运动, 价电子与原子实间的作用很弱,原子实电 荷对称分布,正负电荷中心重合在一起。 有效电荷为+e,价电子好象处在一个单位 正电荷的库仑场中运动,与氢原子模型完 全相似,所以光谱和能级与氢原子相同。
1
整体概述
概况一
点击此处输入相关文本内容 点击此处输入相关文本内容
概况二
点击此处输入相关文本内容 点击此处输入相关文本内容
概况三
点击此处输入相关文本内容 点击此处输入相关文本内容
2
4.1 碱金属原子光谱
引入: 碱金属光谱→能级→结构
中心: 碱金属原子光谱规律:四系; 三端; 两数; 一定则.
一. 碱金属原子光谱------结构相近, 明显分线系
限 条条
条
条
~1 ~; ~,~ 0; ~只有一个
~常;数 ~ 两个
~ 1 辅最 大 ~ 2 辅 ~ 主最大
~1 ~;
~,~;
~只有两个
22
二. 推理解释
4 3
Li原子
s
p
4s
4p
3p 3s
2 2p
2s
Li基态
d
f
4d 4f
3d
23
s
p
d
f
4
4s
4p
4d
4f
3
3p
3d
3s
2 主线系: 二辅:
3
图4.1 锂的光谱线系
4
Δ 几个光谱名词
一个线系的线系限:同一线系中最大的波数,或波数
公式中的第一个光谱项(不动的光谱项)。
原子的共振线:该原子从基态到第一激发态吸收的谱
线。一个原子共振线只有一条。
一个线系的主线:该线系的第一条谱线或该线系的波
数最小的谱线。
5
二、线系公式
❖ H原子光谱:~T(m )T(n)R(m 12n 12)
13
-e
价电子远离原子实
14
二、原子实极化、轨道贯穿
❖ 1.原子实极化(形成电偶极子),使电子又受到电 偶极子的电场的作用,能量降低,同一n值,越小
,极化越强。
❖ 2.轨道贯穿(电子云的弥散),对于那些偏心率很 大的轨道, 接近原子实的那部分还可能穿入原子实 发生轨道贯穿,这时Z*>1,从而使能量降低。
19
204.3 碱金属原子Fra bibliotek谱的精细结构1. 引入: 用高分辨率的仪器观察谱线,发现一条→二/三条
2.本节中心: 谱线精细结构→能级分裂
一.实验事实
~ 增加
主线 系:
二 辅
一
辅
线系 第4 第3 第2 第1
限 条条
条
条
21
主线 系:
二 辅
~ 增加
一 辅
主线系: 二辅: 一辅:
线系 第4 第3 第2 第1
❖ 当 n 时 , ~~T(m 系)限.mR2
1 1
R
n T m * T n * R ( m * 2 n * 2 ) n * 2
1.有效量子数
氢原子:主量子数n 是整数
碱金属原子 n *m * 不是整数有效量子数
2.量子数亏损 l nn* n * R T
6
3.光谱项
7
锂原子的四个线系,可用下列公式表示:
2p
2s
Li基态
~1 ~; ~,~0; ~只有一个
n 增加,ΔE下降
~常;数 ~ 两个 24
d
一辅:
左右两成分间隔取决于P能级双层,与二辅线同.
