特殊方法判断有机反应类型论文
有机化学反应特征

有机化学反应特征一、反应缓慢。
由于有机化合物的反应是在分子间进行的,通常需要加热或应用催化剂以促进反应的进行。
如烷烃和卤素单质的取代反应(光照);乙烯和氢气、卤化氢、水等的加成反应;乙醇的催化氧化反应(Cu、加热)和消去反应(浓硫酸、加热);酯化反应(浓硫酸、加热);苯的卤代(漠化铁)和硝化(浓硫酸、加热)。
二、反应复杂。
副反应多,副产物多。
因此书写有机反应时生成物与反应物之间要用“-”而不能用“=”连接。
醇CH3CH=CHCH3 + NaCl + 明C^CH^HC% + NaOH—△«► ,ClCH3CH2CH=CH2 + NaCl + H2OCH3-CH=CH2+HCl —► CH3CH(Cl)CH3或CH3CH2CH2Cl三、反应条件的选择性反应物相同,但因温度、催化剂或溶剂不同,产物可能不同。
A.温度不同产物不同:b.反应溶剂不同产物不同:C.催化剂不同产物不同:Oy~ CH3 +日益----- -- -- ► CH3 ~— Br—K (O)-CH3Br +HBr四. 反应部位的选择性有机反应看起来有多种断键形式,但与不同类型的物质反应有专一的选择性。
如:甲苯的硝化、苯酚与浓漠水的取代都是在苯环的邻、对位上进行。
羧酸与醇发生酯化反应一般是醇分子羟基上脱氢、羧酸中羧基脱羟基;酯水解一般是酯中碳氧单键断裂。
五. 相邻结构的限制性:有些有机反应能否发生还要受到分子中官能团相邻碳原子的结构的限制。
如:醇氧化成醛就必须是羟基连在端位碳原子上的醇。
CHCH(OH)CH就不能氧化成醛。
醇类或卤代烃发生消去反应时,与羟基或卤素原子相莲碳原子南相邻碳原子上就要有氢原子。
如CH3OH、(CH3)3CCH2OH就不能发生消去反应。
六. 官能团、基团的相互影响性:当有机物中有几种官能团直接相连时往往会相互影响。
导致其化学性质有所变化。
如:苯不能与Br水、酸性高锰酸钾溶液反应;而甲苯因甲基与苯环直接相连,甲基活性增强,就与酸性高锰酸钾溶液反应。
有机反应类型的总结

有机反应类型的总结1、取代反应(1)能发生取代反应的官能团有:醇羟基(-OH)、卤原子(-X)、羧基(-COOH)、酯基(-COO-)、肽键(-CONH-)等。
(2)能发生取代反应的有机物种类如下图所示:2、加成反应1.能发生加成反应的官能团:双键、三键、苯环、羰基(醛、酮)等。
2.加成反应有两个特点:①反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原子与其它原子或原子团以共价键结合。
②加成反应后生成物只有一种(不同于取代反应)。
说明:1.羧基和酯基中的碳氧双键不能发生加成反应。
2.醛、酮的羰基只能与H2发生加成反应。
3.共轭二烯有两种不同的加成形式。
3、消去反应(1)能发生消去反应的物质:醇、卤代烃;能发生消去反应的官能团有:醇羟基、卤素原子。
(2)反应机理:相邻消去发生消去反应,必须是与羟基或卤素原子直接相连的碳原子的邻位碳上必须有氢原子,否则不能发生消去反应。
如CH3OH,没有邻位碳原子,不能发生消去反应。
4、聚合反应(1)加聚反应:烯烃加聚的基本规律:(2)缩聚反应:(1)二元羧酸和二元醇的缩聚,如合成聚酯纤维:(2)醇酸的酯化缩聚:此类反应若单体为一种,则通式为:若有两种或两种以上的单体,则通式为:(3)氨基与羧基的缩聚(1)氨基酸的缩聚,如合成聚酰胺6:(2)二元羧酸和二元胺的缩聚:5、氧化反应与还原反应1.氧化反应就是有机物分子里“加氧”或“去氢”的反应。
能发生氧化反应的物质和官能团:烯(碳碳双键)、醇、酚、苯的同系物、含醛基的物质等。
烯(碳碳双键)、炔(碳碳叁键)、苯的同系物的氧化反应都主要指的是它们能够使酸性高锰酸钾溶液褪色,被酸性高锰酸钾溶液所氧化。
含醛基的物质(包括醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)的氧化反应,指银镜反应及这些物质与新制氢氧化铜悬浊液的反应。
要注意把握这类反应中官能团的变化及化学方程式的基本形式。
2.还原反应是有机物分子里“加氢”或“去氧”的反应,其中加氢反应又属加成反应。
有机物的鉴别方法

有机物的鉴别方法用于有机化合物的鉴别的方法多是指利用含有特征官能团的化合物具有特征性化学反应的性质来区分不同的化合物。
这类特征性反应必须具备以下条件:必须是针对各化合物所含官能团的化学反应,不能将一类化合物转变为另一类化合物再鉴别;必须有明显的、易观察的反应现象,如生成沉淀或气体,有颜色变化等现象;反应有一定的专一性。
因此鉴别方法多是根据各类化合物的特殊性质产生的。
一、烯烃1.利用溴与双键的加成反应,反应现象是溴褪色。
能与溴反应的化合物如苯酚、苯胺等都有干扰。
2.利用高锰酸钾对烯烃的氧化反应,反应现象是高锰酸钾褪色。
常用试剂是高锰酸钾的稀硫酸溶液,中性或碱性高锰酸钾水溶液也能用于烯烃鉴别。
能被高锰酸钾氧化的化合物如炔烃、醇、酚、醛、甲酸、乙二酸、苯胺等都有干扰。
二、炔烃1.溴的四氯化碳溶液或高锰酸钾水溶液也用于鉴别炔烃,因此用此法鉴别炔烃时烯烃有干扰;同样用此法鉴别烯烃时炔烃有干扰。
2.叁键在链端上的炔烃(端基炔),与银氨溶液或亚铜-氨配合物溶液反应得到炔化银(灰白色沉淀物)或炔化亚铜(砖红色沉淀物),可用于端基炔的鉴别。
三、卤代烃卤原子连接在饱和碳原子上的卤代烃与硝酸银作用,生成的卤化银是沉淀物。
常用试剂是硝酸银的乙醇溶液。
不同的卤代烃有不同的反应速率,表现反应条件和出现沉淀的快慢不同,可用于不同卤代烃的区别:3o卤代烃、烯丙式卤代烃和苄基卤代烃与硝酸银-乙醇溶液作用立即出现沉淀,2o卤代烃缓慢出现沉淀,1o卤代烃只在加热时才能与硝酸银反应生成沉淀。
四、醇1.高锰酸钾和重铬酸钾都可用于鉴别醇,酸性介质中高锰酸钾与醇作用的现象是褪色(很浅的Mn2+颜色不易看出),在其它介质中现象是高锰酸钾褪色,并有黑色沉淀(MnO2);重铬酸钾与醇作用的现象是橙红色转变为绿色。
用这个反应鉴别醇时,烯烃、炔烃、酚、醛等有干扰。
2.含氯化锌的浓盐酸溶液(卢卡斯试剂)用于区别六个碳原子及六个以下碳原子不同的醇:叔醇与卢卡斯试剂作用立即出现混浊-反应生成的卤代烷不溶于卢卡斯试剂,仲醇与卢卡斯试剂作用缓慢出现混浊(数分钟),伯醇与卢卡斯试剂需经加热才能出现混浊。
化学论文:《有机化学反应类型小结》

有机专题---有机反应类型小结山东省济阳第一中学(251400)王志刚1. 取代反应:定义:有机化合物中的某些原子(或原子团)被其它原子(或原子团)所替代的反应。
特征:两种物质互相交换原子或原子团常见取代反应有:(1)烷烃卤代;如:CH4+Cl2CH3Cl+HCl(2)苯及其同系物(卤代、硝化、磺化);如:+HNO3+H2O(3)卤代烃的水解反应;如:CH3Cl +H2O CH3OH+HCl(4)醇(与HX 、分子间脱水成醚);如:C2H5OH+HBr C2H5Br+H2O2CH3CH2OH C2H5OC2H5+H2O(5)苯酚与浓溴水;如:+Br2+HBr(6)醇与酸的酯化反应;CH3CH2OH+CH3COOH CH3COOC2H5+H2O(7)酯的水解反应(皂化反应);如:CH3COOC2H5+H2O CH3COOH+C2H5OH2. 加成反应:定义:有机物分子中不饱和碳原子跟其它原子(或原子团)直接结合成新物质的反应。
特征:①物质“多变一”②化合物不饱和程度降低(或消失)。
常见加成反应:(1)烯、炔、苯及不饱和烃的衍生物与氢气、卤素、卤化氢、水等反应;如:R-CH=CH2 +H2R- CH2-CH3再如:R-C≡CH+HCl R-CH=CHCl(2)醛和酮、葡萄糖与氢气的反应等;如:CH3CHO+H2CH3CH2OH3. 消去反应:定义:有机物分子中脱去小分子(H2O 、HX等)生成不饱和化合物的反应。
特征:①化合物“一变多”②化合物不饱和程度增大。
常见消去反应:(1)醇分子内脱水制烯;如:C 2H5OH CH2=CH2↑+H2O(2)卤代烃分子内脱卤化氢生成烯;如:C2H5Cl+NaOH CH2=CH2↑+H2O+NaCl4. 氧化反应:定义:有机分子中加氧或去氢的反应。
常见氧化反应:(1)有机化合物的燃烧反应;(2)强氧化剂(如KMnO4)同烯、炔及其衍生物、苯的同系物反应;如:R-CH=CH2 RCOOH+CO2(3)加氧氧化(如:由醛生成酸);如:2CH3CHO+O22CH3COOH(4)去氢氧化(如:醇生成醛);如:2CH3CH2OH+O22CH3CHO+2H2O5. 还原反应:定义:有机物分子中加氢或去氧的反应常见还原反应:(1)加氢还原;如:烯、炔及其衍生物加氢;苯环加氢还原;醛加氢还原成醇;如:CH3CHO+H2CH3CH2OH(2)去氧还原;如:CH3COOH CH3CH2OH ;再如:(注意,该反应不是取代反应)6. 酯化反应(本质是取代反应):定义:酸与醇作用生成酯和水的反应。
有机反应的环化与开环反应

有机反应的环化与开环反应有机反应是研究有机物分子之间的相互作用和转化的领域。
其中,环化反应和开环反应是有机反应中常见的两种重要类型。
本文将从环化反应和开环反应的定义、机理以及应用方面进行论述。
一、环化反应环化反应是指在有机分子中形成环状结构的化学反应。
它是有机化学中重要的构建环状骨架的方法之一,具有广泛的应用价值。
常见的环化反应包括环加成反应、环化脱水反应、环化氧化反应等。
下面以环加成反应为例进行介绍。
环加成反应是一种有机化学中常见的环化反应。
它指的是将一个分子中的两个官能团连接起来形成环状结构。
环加成反应可分为亲电环加成和双位竞争环加成两种机制。
在亲电环加成中,一个亲电试剂攻击另一个亲核位点,生成环状产物。
而在双位竞争环加成中,多个亲电位点同时与亲核试剂反应,形成竞争生成多个环状产物。
环加成反应在药物合成、天然产物合成以及有机分子的构建等方面具有重要应用。
例如,环化反应在合成多环芳烃和天然产物的过程中发挥了关键作用,为有机化学领域的研究提供了有力手段。
二、开环反应开环反应与环化反应相反,是指将一个环状结构的有机分子打开,恢复成直链分子或者生成新的链状结构。
开环反应也是有机化学中常见的反应类型,通过破坏环状结构,可以引入新的官能团或者进行构建骨架的转换。
常见的开环反应包括开环加成、开环氧化、开环酯化等。
以开环加成为例进行介绍。
开环加成是一种将环状有机化合物断开的反应,由于环状有机化合物的特殊性,使得其反应较为独特。
开环加成反应可以通过热力学和动力学两种机制进行,通常需要适当的反应条件和催化剂的存在。
该反应可用于降解环状有机化合物、合成直链化合物以及构建新的官能团等。
开环反应在有机合成中具有重要地位,可以实现对环状结构的改变和控制,为有机合成中的构建和修饰提供了便捷的方法。
三、环化与开环反应的应用环化与开环反应在有机化学领域具有广泛的应用。
它们在药物合成、天然产物的结构修饰和合成,材料科学等方面都扮演着重要的角色。
有机化学论文六篇

有机化学论文六篇有机化学论文范文1备课时需针对不同的专业要求,确定讲课内容和重点。
例如,在给生物制药专业本科生讲授有机化学时,需向同学阐述有机化学在制药领域中的应用,在药物合成过程中所用到的有机反应类型和机理,特殊是引入绿色化学的概念,以削减在制药过程中产生的环境污染,达到资源最大化利用。
在讲到乙烯聚合这一部分内容时,可向同学介绍聚合物在生活中的详细应用。
比如说,生活中塑料制品的主要成分大多是聚乙烯,常用药物纯化分别、污水治理领域的膜分别技术,其核心部件膜组件也大多是高分子聚合物,比如聚醚砜超滤膜、聚偏氟乙烯超滤膜、聚氯乙烯微滤膜等。
而在膜技术领域,膜污染问题是制约膜技术进展的瓶颈,可以通过对膜表面进行化学改性的方法提高膜的抗污染性能,这些都要用到有机化学相关学问。
通过这些事例,进行专业引导,可以提高同学对本门课程的学习热忱。
二、充分利用多媒体,丰富教学形式有机化学中涉及到大量化学方程式、电子结构、分子构型等抽象概念,而多媒体课件则可以对其进行有效的补充。
在讲解相关反应机理时,对于化学反应过程最好做成动画演示,关心同学理解并且加深印象。
例如,在讲解碳原子杂化轨道形成过程中,电子跃迁,轨道的杂化过程可通过flas 演示,老师应结合每一步动画讲解相应的机理,从而让同学对抽象的过程有宏观的熟悉。
同时,在采纳多媒体教学过程中,需留意板书与多媒体课件有机地结合,对于一些反应过程必需利用板书进行具体的讲解,过分依靠课件有可能造成细节讲解不透彻。
在教学过程中,要留意引入生活中的案例,使枯燥的理论生活化。
例如,在讲授蛋白质化学这一章内容时,可先布置一个有关蛋白质的小课题,让同学课后查阅相关资料,并在课中进行讲解。
例如,在生活中,假如误服了含有大量重金属的食物,如何采纳急救措施,其解毒原理又是什么?儿童重金属中毒会对其生长发育有什么影响?同学通过对这些问题的查阅,搞清晰相关问题的原理,同时又增加了生活常识,从而达到学以致用。
有关高考理综化学有机推断论文

有关高考理综化学有机推断的思考【摘要】有机框图综合推断题已成了高考试题中一类保留题型,几乎每份高考化学试卷、理科综合试卷中都会有一道有机框图综合推断类型的大题。
着力考查阅读有机合成方案、利用题设信息、解决实际问题的能力,也考查了学生对信息接受和处理的敏锐程度、思维的整体性和对有机合成的综合分析能力,对学生的信息获取和加工能力提出较高要求。
【关键词】综合推断信息获取加工能力【中图分类号】g427 【文献标识码】a【文章编号】1.对近三年理综试卷有机试题分析后的一些思考1.1有机常考题型,从有机试题的结构特点和考查的内容看,题型、比例和分值都相对比较稳定,每年都有一个有机推断题,所占分值占整个化学试题的20%左右。
⑴考查有机基础知识。
如:判断有机物的类型、用有机化学知识分析生活中常见问题、考查跟有机化学有关的基本技能、判断同分异构体和书写同分异构体的结构简式、高分子化合物与单体的相互判断、有机物质模型的识别,已知物质结构,推断物质性质;⑵考查有机反应类型的定性判断和定量计算。
如:书写有机化学方程式、判断有机反应类型、基本有机计算等。
⑶考查有机物知识的综合分析和应用能力1.2从考查的要求看,以理解层次为最多。
试题特别强调能力和素质的考查,注重考查考生对基础知识的理解以及运用这些基础知识分析、解决问题的能力,体现了学以致用、理论联系实际的思想。
1.3从命题的着眼点看,无论是结构简式、化学方程式的书写,还是有机反应类型的判断,高考试题均根植于教材之中,但考题往往依托社会生活热点问题和科技新成果进行有机物各方面知识的考查,因此只要我们在平时教学中根据《教学大纲》扎扎实实地做好化学基础知识的落实工作,应该说绝大部分学生在面对这种难度的试题时是不会有太大障碍的。
1.4从学生的答题情况看,常见的主要错误有:(1)审题不仔细,没按题目要求准确作答;(2)结构简式的书写不规范:如①. 多写或少写h原子;②.将苯环写成环己烷;③.官能团之间的连接线没有对准所连接的原子;④.有些官能团往左书写时没注意(如:ho-、ohc-、hooc-、o2n-、h2n-等的书写);⑤.书写时未把官能团的结构特征表达出来等;(3)书写方程式时未用结构简式表达,丢产物(如水等小分子),忘了配平或注明反应条件等;(4)化学用语书写错误:如烯、苯、醛、酸、脂和酯等书写错误;(5)对一些复杂同分异构体的书写则很难完整写出。
有机推断之特殊结构、反应类型

d. 在 B中滴加 AgNO3 溶液不会产生淡黄色沉淀
(3)①J 有 多种同分 异构体 ,满 足以下条 件 J 的同
分异构体的个数是
;
a. 遇 FeCl3 溶液呈紫色 b. 能发生银镜反应
c. 1 mol J 能与最多 3 mol NaOH反应 ②生产中 为提高产品质量,将粗品 J溶 于热水、过
滤、
只有一种结构,且能使溴水褪色。
解析 观察 流程图可知 ,A 为(C4H6 O2)n 的单体,分
子式为 C4 H6O2 ,A 分子中 含有碳 碳双键,且 在稀 H2SO4
及 加热 条 件下 反 应 生成 C、D。 C 分 子 含有 醛 基 ;与
Cu(OH)2 反应 后生 成 D,表明 C、D 含 有相 等的 碳原 子
一、常见有机反应类型 取代反应——能发生取代反应的官能团有:醇羟基 (—OH)、卤原子(—X)、羧基(—COOH)、酯基(—COO—)、
O 肽键(—C—NH—)等。
加成 反应—— 能发生 加成反 应的 官能团 :双键、 三键、苯环、羰基(醛、酮)等不饱和官能团。
消去反应——能 发生消去反应的 官能团有:醇羟 基、卤素原子。
,获得 J 的精品。
答案
CH 3
(1)①
CH 3
取代反应
②羧基
n HOOC —
—COOH+nHOCH2 CH2OH→HO—OC—
—
COOCH2CH2
O— H+(2n n
-
1)H2
O
(2)b
(3)①13 ②冷却结晶
点 拨 此题 难度 不 大,是特 别经 典 的有 机 推断
题。 只要大家掌握有机化 学中重要的特征反应 ,再结
以烯烃为原料,合成某些高聚物的路线如下:
化学反应物质变化的判断依据及反应类型的分类与实验结果的分析

化学反应物质变化的判断依据及反应类型的分类与实验结果的分析化学反应是物质之间发生的一系列变化过程。
通过观察反应物质的变化以及分析实验结果,我们可以判断化学反应发生的类型和确定物质的变化。
首先,判断化学反应物质变化的依据主要包括实验观察和理论分析两方面。
一、实验观察在化学实验中,我们通过观察物质的变化来判断化学反应的发生。
以下是常见的实验观察现象和对应的反应类型:1.气体的产生:如果反应中产生了气体,例如氢气、氧气、二氧化碳等,那么可以判断这是气体生成反应。
2.溶液的颜色变化:某些化学反应会导致溶液的颜色发生变化,比如出现浑浊、颜色变深或变浅等,这可能是颜色改变反应。
3.产生光、热或声音:有些反应会伴随着光、热或声音的产生,例如放烟花、爆炸等,可以判断这是放热反应或爆炸反应。
4.沉淀的生成:某些反应会产生沉淀,即固体颗粒悬浮在溶液中,这是沉淀生成反应。
二、理论分析在实验观察的基础上,理论分析可以进一步确定化学反应的类型。
以下是常见的化学反应类型:1.氧化还原反应:氧化还原反应是指电子在反应中的转移。
如果反应中有物质失去电子(被氧化),同时有物质获得电子(被还原),那么这是氧化还原反应。
2.酸碱反应:酸碱反应是指酸和碱在反应中发生中和反应,产生盐和水。
常见的酸碱反应有氢氧化钠与盐酸的中和反应。
3.沉淀反应:沉淀反应是指两种溶液混合后,产生固体沉淀。
比如在氯化钡溶液中加入硫酸钠溶液,会产生白色的硫酸钡沉淀。
4.配位反应:配位反应是指配体与中心金属离子形成配合物的反应。
比如在溴化物离子中加入氯离子,会形成溴氯配合物。
然后,针对实验结果的分析可以进一步确定反应类型和物质变化。
1.物质的质量变化:可以通过质量的增减来判断反应是否发生。
对于闭合系统而言,质量守恒,即反应前后物质的质量之和保持不变。
2.化学方程式的平衡:根据化学方程式的平衡情况来分析反应类型。
如果反应满足动力学平衡,可以通过化学方程式中系数之间的比例确定反应类型。
有机化学反应的主要类型

热消除反应
反应机理
热消除反应是一种通过加热引发 的消除反应,其中有机化合物在 加热条件下断裂碳-碳键或碳-氢
键并消除小分子。
反应条件
通常需要高温条件,不需要额外 的催化剂。
产物特点
生成的产物通常具有不饱和键, 如烯烃或炔烃,比原料化合物少
两个氢原子。
05
重排反应
氢重排反应
氢迁移
在有机化学反应中,氢原子从一 个原子或基团迁移到另一个原子 或基团的过程。
氧化还原偶联反应
氢转移偶联
01
涉及氢原子从一个有机物分子转移到另一个有机物分子的反应
,如醇与醛的氢转移反应生成醚。
电子转移偶联
02
涉及电子从一个有机物分子转移到另一个有机物分子的反应,
如烯烃与卤素的电子转移反应生成卤代烃。
自由基偶联
03
涉及自由基的生成和转移的反应,如烷烃的自由基卤化反应生
成卤代烃和烷基自由基。
有机化学反应的主要类型
汇报人:XX
• 绪论 • 取代反应 • 加成反应 • 消除反应 • 重排反应 • 氧化还原反应
01
绪论
有机化学反应定义与特点
定义
有机化学反应是指涉及有机化合物分子中化学键的断裂和形成的过程,通常伴 随着能量的变化。
特点
有机化学反应具有多样性、复杂性和选择性等特点。多样性表现为反应类型和 反应机理的多样性;复杂性表现为反应条件和反应产物的复杂性;选择性表现 为不同反应条件和反应物结构对反应选择性的影响。
THANKS
感谢观看
氮重排反应
涉及含氮化合物的重排反应, 如霍夫曼重排、柯提斯重排等
。
氧重排反应
涉及含氧化合物的重排反应, 如贝克曼重排、频哪醇重排等 。
有机推断中的反应类型判断的常用方法归纳

有机推断中的反应类型判断的常用方法归纳
(1)由官能团转化推测反应类型。
从断键、成键的角度掌握各反应类型的特点,如取代反应的特点是有上有下或断一下一上一;加成反应的特点是只上不下或断一加二;消去反应的特点是只下不上。
(2)由反应条件推测反应类型。
有机反应的重要条件总结如下:
①NaOH水溶液作条件的反应:卤代烃的水解;酯的碱性水解;NaOH醇溶液与卤代烃发生的是消去反应。
②以浓H2SO4作条件的反应:醇的消去;醇变醚;苯的硝化;酯化反应。
③以稀H2SO4作条件的反应:酯的水解;糖类的水解;蛋白质的水解。
④Fe:苯环的卤代。
光照:烷烃的卤代。
⑤当反应条件为光照且与X2反应时,通常是X2与烷烃或苯环侧链烃基上的氢原子发生取代反应,而当反应条件为催化剂且与X2反应时,通常为苯环上的氢原子直接被取代。
⑥当反应条件为催化剂并有氧气时,通常是醇氧化为醛或醛氧化为酸。
(3)卤代、硝化、磺化、酯化、水解、皂化、分子间脱水等反应,本质上属于取代反应。
(4)有机物的加氢、脱氧属还原反应,脱氢、加氧属于氧化反应。
研究有机反应机理的方法

O H3C CH CN
O H3C CH CN
Several possible reactions might take place at this point. Perhaps the most obvious, however, is the addition of a cyanide ion to the carbonyl group. Now, an acid-base reaction would yield the specified product and regenerate the cyanide ion: Let’s try our procedure for proposing mechanisms on another base catalyzed reaction.
Cl NO2 CH3OH OCH3 NO2
NO2
NO2
活性顺序:I<Br<Cl<F
亲核取代反应
⑶醇的羟基被取代的反应。
OH + HI I
⑷羧酸衍生物的生成反应。
COCl + C2H5OH COOC2H5 + H2O
⑸芳香烃硝基、磺酸基被取代的反应。
NO2 NaHSO3 NO2
NO2
SO3Na
亲电取代反应
EWG X XH
R3N
R R R
EWG
+
R
X=O, NCOOP, NTs, NSO2Ph EWG= electron withdrawing group
Tetrahedron Letters 40(1999)1539-1542 The Baylis-Hillman reaction, the coupling of ,-13-unsaturated carbonyl compounds with aldehydes, is one of the most important carbon-carbon bond-forming processes in organic synthesis. While the original protocol used a tertiary amine, prolonged reaction time was needed even when a stoichiometric amount of a rather strong basic amine such as 1,4diazabicyclo[2,2,2]octane (DABCO) was used.
有机化学鉴别反应

有机化学鉴别反应1.溴的四氯化碳溶液检验烯烃和炔烃烯烃分子中含C=C双键,炔烃分子中含C≡C叁键。
二者均能与溴发生加成反应,使溴的红棕色消失,因此可以来鉴别烯烃或炔烃。
2.高锰酸钾溶液检验烯烃和炔烃烯烃分子中含C=C双键,炔烃分子中含C≡C叁键。
当二者被高锰酸钾溶液氧化时,不饱和键被破坏,同时紫色高锰酸钾溶液褪色生成褐色的二氧化锰沉淀。
根据上述实验现象可以来鉴别烯烃或炔烃。
3.硝酸银氨溶液鉴别末端炔烃末端炔烃含有活泼氢,可与硝酸银氨溶液反应生成炔化银沉淀。
借此可鉴别末端炔烃类化合物。
4.铜氨溶液鉴别末端炔烃末端炔烃含有活泼氢,可与铜氨溶液反应生成炔化铜沉淀。
借此可鉴别末端炔烃类化合物。
5.硝酸银-乙醇溶液检验卤代烃的相对活性硝酸银-乙醇溶液与卤代烃反应时,如果烃基相同,不同卤素作为离去基团的反应性为:RI>RBr>RCl>RF如果卤原子相同而烃基不同,则受电子效应和空间效应的影响,卤代烃的相对反应性为:苯甲型、烯丙型>三级>二级>一级>苯型、乙烯型两个和两个以上卤原子同连在一个碳原子上的卤代烃,如氯仿等,不与硝酸银溶液反应。
由此可以推测卤代烷的可能结构。
6.苯甲酰氯检验醇苯甲酰氯与醇反应生成有香味的酯,以此可鉴别醇类化合物。
7.卢卡斯试剂检验一、二、三级醇氯化锌-盐酸溶液称卢卡斯试剂。
一级醇、二级醇、三级醇与卢卡斯试剂反应的速率不同。
三级醇最快,二级醇次之,一级醇极慢。
六个碳原子以下的各级醇均溶于卢卡斯试剂,反应后生成的氯代烷不溶于该试剂,故反应发生后体系会出现混浊或分层。
根据实验现象可判别反应速率的快慢,以次区别一、二、三8.土伦试剂鉴别醛和酮*土伦试剂是银氨离子(硝酸银的氢氧化铵溶液),它与醛反应时,醛被氧化成酸,银离子被还原成银,附着在试管壁上形成银镜,由此称该反应为银镜反应。
土伦试剂与酮不发生上述反应,所以此实验可区别醛和酮。
9. 2,4-二硝基苯肼检验醛和酮2,4-二硝基苯肼能与醛、酮的羰基发生亲核加成反应并生成黄色、橙色或红色沉淀。
特殊方法判断有机反应类型

特殊方法判断有机反应类型作者:杨碧莹来源:《读写算》2011年第43期有机反应类型的判断在历年高考题中都有所体现,有些时候还是有机推断的题眼。
有机反应类型的推断方法很多,下面就高考中有机反应类型的判断,介绍几种特殊方法。
一、由有机物断键方式判断常见的有机反应断键方式如下:1、烃的卤代反应:烃断C-H键2、烯、炔烃的加成反应,烯烃断C=C键、炔烃断C≡C键3、醛、酮的加成反应:醛(酮)断C=O键4、醇分子间脱水反应:一醇断C-O键,另一醇断O-H键5、卤代烃水解反应:卤代烃断C-X6、酯化反应:羧酸断C-OH键,醇断O-H键7、酯水解反应:断酯基中的C-O键8、醇的卤代反应:断羟基中的C-OH键9、肽的水解反应:断肽键中的C-N键二、由试剂和反应条件确定反应类型常见试剂、条件与反应类型关系如下:1、与(卤素单质)/光照的反应,为烷烃或苯环侧链烃基上的取代反应2、与(卤素单质)/催化剂的反应,为芳香烃苯环上的取代反应3、与Br2(液溴)/CCl4的反应,为碳碳双键(烯)、碳碳三键(炔)的加成反应4、与溴水反应,为烯、炔加成;酚取代;醛及含-CHO物质的氧化5、与H2/催化剂的反应,为烯、炔、芳香烃、醛(酮)等加成反应(还原反应)6、与O2/催化剂的反应,为醇氧化成醛(酮)或醛氧化成酸的反应7、与酸性高锰酸钾溶液反应,为烯、炔、醇、醛及含-CHO物质、苯的同系物等氧化8、与浓在加热条件下反应,为醇脱水生成醚或不饱和烃的反应;醇与酸的酯化反应9、与稀在加热条件下的反应,为酯或淀粉的水解反应10、与浓HNO3/浓的反应,为苯(芳香烃)的硝化反应11、与NaOH的水溶液反应,为羧酸、酚、氨基酸的中和;若加热则为卤代烃、酯水解反应12、与NaOH的醇溶液在加热条件下反应,通常为卤代烃的消去反应13、与银氨溶液反应,为醛类、还原性糖、甲酸盐、HCOOH、HCOOR等氧化反应14、与新制Cu(OH)2(悬浊液)反应,在加热条件下为醛类、还原性糖、HCOOH、HCOOR等氧化反应;常温为低碳羧酸的中和反应例1.(2010安徽高考)F是新型降压药替米沙坦的中间体,可由下列路线合成:则A→B 的反应类型是________;D→E的反应类型是_________;E→F的反应类型是_________________。
浅析化学反应类型的判别方法
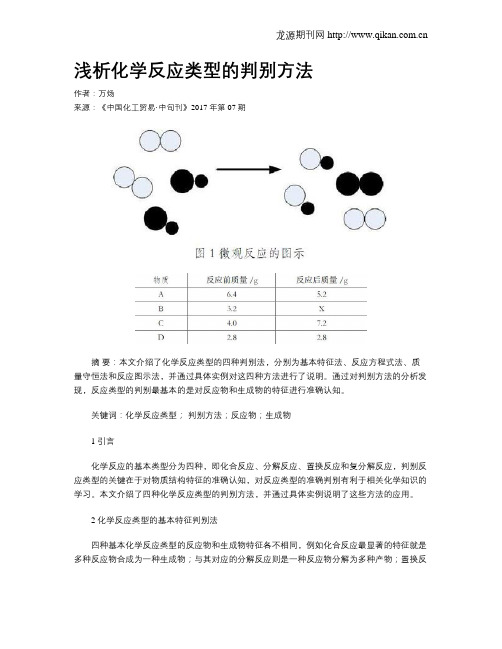
浅析化学反应类型的判别方法作者:万炀来源:《中国化工贸易·中旬刊》2017年第07期摘要:本文介绍了化学反应类型的四种判别法,分别为基本特征法、反应方程式法、质量守恒法和反应图示法,并通过具体实例对这四种方法进行了说明。
通过对判别方法的分析发现,反应类型的判别最基本的是对反应物和生成物的特征进行准确认知。
关键词:化学反应类型;判别方法;反应物;生成物1 引言化学反应的基本类型分为四种,即化合反应、分解反应、置换反应和复分解反应,判别反应类型的关键在于对物质结构特征的准确认知,对反应类型的准确判别有利于相关化学知识的学习。
本文介绍了四种化学反应类型的判别方法,并通过具体实例说明了这些方法的应用。
2 化学反应类型的基本特征判别法四种基本化学反应类型的反应物和生成物特征各不相同,例如化合反应最显著的特征就是多种反应物合成为一种生成物;与其对应的分解反应则是一种反应物分解为多种产物;置换反应是单质和化合物反应生成另一种单质和另一种化合物;复分解反应则是两种化合物的组分互换,生成不同的两种化合物。
以实例说明化学反应类型的基本特征判别法。
现有如下几种物质,分别为CO2、KNO3溶液、Ag、CuSO4溶液、稀硫酸、NaOH溶液、Fe以及NaCl溶液,分别以1#-8#编号。
根据四种类型的基本特征,选出可以发生置换反应和复分解反应的物质编号。
置换反应的基本特征是反应物为单质和化合物,发生置换反应后形成新的单质和化合物,在上述物质中满足这一基本特征的只有4#7#以及5#7#两组。
复分解反应的基本特征是遵循组分交换且化合价不发生改变,满足这一特征的物质为4#6#和5#6#两组。
3 化学反应类型的反应方程式判别法通过反应方程式可以直观的判断出化学反应的类型,如式1所示的反应:HCl+NaOH=NaCl+H2O (1)式1所示的反应中是两种化合物(HCl和NaOH)的组分发生了互换,最终生成了新的化合物(NaCl和H2O),因此属于复分解反应。
分析有机反应的方法和有机反应类型

六、显色反应 酚 淀粉 蛋白质
5.分子间脱水 5.分子间脱水 除了酯化和硝化外 醇与醇 氨基酸 羧酸与羧酸
二、加成反应
1.加H2 1.加 烯烃 炔烃 芳香烃 酚 醛 酮
2.加X2 2.加 烯烃 炔烃 芳香烃 3.加HX 3.加 烯烃 炔烃 4.加H2O 4.加 烯烃 炔烃
三、消去反应
1.消去水分子 1.消去水分子 醇 2.消去卤化氢 2.消去卤化氢 卤代烃
小结有机反应类型
定义 发生反应的有机物类别 有机物官能团变化 反应试剂和条件 举例 具有代表性的反应,规范书写方程式
一、取代反应 1.卤代 1.卤代 烷烃 芳香烃 酚 醇 2.硝化 2.硝化 芳香烃 酚
3.酯化 3.酯化 醇与羧酸 醇与硝酸 4.水解 4.水解 卤代烃 酯 蛋白质、肽 二糖、多糖
3.分析有机反应的方法和有机反应类型 3.分析有机反应的方法和有机反应类型
分析有机反应的方法: 参加反应Байду номын сангаас机物 反应条件
反应试剂
反应产物
有机物
无机物
反应试剂和反应条件 有机物分子组成和结构的变化 官能团变化、碳骨架变化 反应类型 化学键的断裂与形成
有机化学方程式书写注意: 正确、规范书写有机物的结构简式 正确表示无机反应试剂和无机产物的化学式 准确的反应条件和连接符号 配平
四、氧化反应、还原反应 1.氧化反应 1.氧化反应 完全氧化生成CO 完全氧化生成CO2和H2O 部分氧化 烯烃和炔烃 芳香烃 酚 醇 醛
2.还原反应 2.还原反应 醛 酮 烯烃和炔烃
五、聚合反应 1.加聚反应(加成反应) 1.加聚反应(加成反应) 一种单体 两种单体 2.缩聚反应(取代反应) 2.缩聚反应(取代反应) 二元酸与二元醇 二元酸与二胺 羟基酸 氨基酸 酚与醛
特殊方法判断有机反应类型论文

特殊方法判断有机反应类型有机反应类型的判断在历年高考题中都有所体现,有些时候还是有机推断的题眼。
有机反应类型的推断方法很多,下面就高考中有机反应类型的判断,介绍几种特殊方法。
一、由有机物断键方式判断常见的有机反应断键方式如下:1、烃的卤代反应:烃断c-h键2、烯、炔烃的加成反应,烯烃断c=c键、炔烃断c≡c键3、醛、酮的加成反应:醛(酮)断c=o键4、醇分子间脱水反应:一醇断c-o键,另一醇断o-h键5、卤代烃水解反应:卤代烃断c-x6、酯化反应:羧酸断c-oh键,醇断o-h键7、酯水解反应:断酯基中的c-o键8、醇的卤代反应:断羟基中的c-oh键9、肽的水解反应:断肽键中的c-n键二、由试剂和反应条件确定反应类型常见试剂、条件与反应类型关系如下:1、与(卤素单质)/光照的反应,为烷烃或苯环侧链烃基上的取代反应2、与(卤素单质)/催化剂的反应,为芳香烃苯环上的取代反应3、与br2(液溴)/ccl4的反应,为碳碳双键(烯)、碳碳三键(炔)的加成反应4、与溴水反应,为烯、炔加成;酚取代;醛及含-cho物质的氧化5、与h2/催化剂的反应,为烯、炔、芳香烃、醛(酮)等加成反应(还原反应)6、与o2/催化剂的反应,为醇氧化成醛(酮)或醛氧化成酸的反应7、与酸性高锰酸钾溶液反应,为烯、炔、醇、醛及含-cho物质、苯的同系物等氧化8、与浓在加热条件下反应,为醇脱水生成醚或不饱和烃的反应;醇与酸的酯化反应9、与稀在加热条件下的反应,为酯或淀粉的水解反应10、与浓hno3/浓的反应,为苯(芳香烃)的硝化反应11、与naoh的水溶液反应,为羧酸、酚、氨基酸的中和;若加热则为卤代烃、酯水解反应12、与naoh的醇溶液在加热条件下反应,通常为卤代烃的消去反应13、与银氨溶液反应,为醛类、还原性糖、甲酸盐、hcooh、hcoor 等氧化反应14、与新制cu(oh)2(悬浊液)反应,在加热条件下为醛类、还原性糖、hcooh、hcoor等氧化反应;常温为低碳羧酸的中和反应例1.(2010安徽高考)f是新型降压药替米沙坦的中间体,可由下列路线合成:则a→b的反应类型是________;d→e的反应类型是_________;e→f的反应类型是_________________。
例谈高考中有机反应类型判断的方法与技巧

例谈高考中有机反应类型判断的方法与技巧
王睿婷
【期刊名称】《数理化解题研究》
【年(卷),期】2024()13
【摘要】本文通过根据有机物中官能团的衍变、反应的条件、参与反应的有机物等重要信息判断有机反应类型,同时对相关必备知识整合归类,以期能提高复习的针对性,高效备考.
【总页数】3页(P140-142)
【作者】王睿婷
【作者单位】内蒙古赤峰市宁城县高级中学
【正文语种】中文
【中图分类】G632
【相关文献】
1.例谈高考化学图表信息题的解题技巧——以2014年福建高考理科综合试卷化学试题为例
2.例谈有机化合物同分异构体数目的判断方法
3.例谈高考地理试题数据分析的方法和技巧
4.例谈高考漫画题的解题方法与技巧——2005年江苏高考政治试卷的一点启示
5.例谈高考中的几种解题方法与技巧
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
特殊方法判断有机反应类型
有机反应类型的判断在历年高考题中都有所体现,有些时候还是有机推断的题眼。
有机反应类型的推断方法很多,下面就高考中有机反应类型的判断,介绍几种特殊方法。
一、由有机物断键方式判断
常见的有机反应断键方式如下:
1、烃的卤代反应:烃断c-h键
2、烯、炔烃的加成反应,烯烃断c=c键、炔烃断c≡c键
3、醛、酮的加成反应:醛(酮)断c=o键
4、醇分子间脱水反应:一醇断c-o键,另一醇断o-h键
5、卤代烃水解反应:卤代烃断c-x
6、酯化反应:羧酸断c-oh键,醇断o-h键
7、酯水解反应:断酯基中的c-o键
8、醇的卤代反应:断羟基中的c-oh键
9、肽的水解反应:断肽键中的c-n键
二、由试剂和反应条件确定反应类型
常见试剂、条件与反应类型关系如下:
1、与(卤素单质)/光照的反应,为烷烃或苯环侧链烃基上的取代反应
2、与(卤素单质)/催化剂的反应,为芳香烃苯环上的取代反应
3、与br2(液溴)/ccl4的反应,为碳碳双键(烯)、碳碳三键(炔)的加成反应
4、与溴水反应,为烯、炔加成;酚取代;醛及含-cho物质的氧化
5、与h2/催化剂的反应,为烯、炔、芳香烃、醛(酮)等加成反应(还原反应)
6、与o2/催化剂的反应,为醇氧化成醛(酮)或醛氧化成酸的反应
7、与酸性高锰酸钾溶液反应,为烯、炔、醇、醛及含-cho物质、苯的同系物等氧化
8、与浓在加热条件下反应,为醇脱水生成醚或不饱和烃的反应;醇与酸的酯化反应
9、与稀在加热条件下的反应,为酯或淀粉的水解反应
10、与浓hno3/浓的反应,为苯(芳香烃)的硝化反应
11、与naoh的水溶液反应,为羧酸、酚、氨基酸的中和;若加热则为卤代烃、酯水解反应
12、与naoh的醇溶液在加热条件下反应,通常为卤代烃的消去反应
13、与银氨溶液反应,为醛类、还原性糖、甲酸盐、hcooh、hcoor 等氧化反应
14、与新制cu(oh)2(悬浊液)反应,在加热条件下为醛类、还原性糖、hcooh、hcoor等氧化反应;常温为低碳羧酸的中和反应
例1.(2010安徽高考)f是新型降压药替米沙坦的中间体,可由下列路线合成:则a→b的反应类型是________;d→e的反应类型
是_________;e→f的反应类型是_________________。
解析:a→b的反应条件为空气(o2)/催化剂,由此可知是间二甲苯的氧化反应;d→e的反应条件是h2/催化剂,应是还原反应,e→f的反应类型要从断键方式上判断,e中-nh2中的一个n-h键断裂,h原子被-occh2ch2ch3原子团代替,因此是取代反应。
答案:a→b:氧化;d→e:还原;e→f:取代
三、由反应物和生成物的化学式推断
对照反应物和产物化学式 (分子式),确定发生反应类型
例2.(2011上海高考)化合物m是一种治疗心脏病药物的中间体,以a为原料的工业合成路线如下图所示。
已知:rona+ rx → ror + nax根据题意完成下列填空:(1)写出反应类型。
反应①
____________反应②____________
解析:由合成路线中反应①,不难写出产物的化学式为c7h8o2,与a的化学式c6h6o相差ch2o,而ch2o刚好是一个分子hcho,因此反应①的类型应是a与hcho发生加成反应;b的化学式为c7h6o2,与c7h8o2相比,少了h2,所以反应②应为氧化反应。
答案:①加成反应;②氧化反应
四、由反应物或生成物中的结构(官能团)推测反应类型
根据反应物或产物的结构 (官能团),或对照反应物和产物的结构式、结构简式或官能团,确定发生反应类型。
例3.下列是某有机物合成反应的流程图:已知甲溶液遇石蕊溶液变红。
反应①、④的反应类型分别是:___________、___________。
解析:甲溶液遇石蕊溶液变红说明甲中含羧基(-cooh),①的反应物中并无羧基,所以羧基应是醛基(-cho)氧化后生成的,即反应①的反应类型应为氧化反应;反应④的生成物中含酯基,则应是-cooh和-oh的酯化反应(取代)
答案:氧化、酯化(取代)反应
五、借助信息判断
借助题目中所给的已知反应,分析判断反应类型。
例4.(2011天津高考)已知:①:rch2cooh ;②:+rcl+nacli.冠心平f是降血脂、降胆固醇的药物,它的一条合成路线如下:c+ef 的反应类型为_______________。
解析:ab的反应类型与反应①的类型相同,c+ef的反应类型与反应的②类型相同。
由题中所给的两个反应断键情况可知,两个反应均是取代反应,所以c+ef的反应类型是应取代反应
答案:取代反应
跟踪练习
1、(2011安徽高考)室安卡因(g)是一种抗心率天常药物,可由下列路线合成;f→g的反应类型是___________。
2、(2011浙江高考)白黎芦醇(结构简式:)属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用。
某课题组提出了如下合成路线:
已知::。
根据以上信息回答下列问题:
c→d的反应类型是____________;e→f的反应类型是
____________。
3、(2011海南高考)pct是一种新型聚酯材料,下图是某研究小组合成pct的路线。
请回答下列问题:(1)由b生成c的反应类型是________________;(2)由e生成f的反应类型为
________________;
答案:1.取代2.取代;消去3.酯化(取代);加成。
