重组蛋白纯化基本策略
重组蛋白[Recombinant Protein]纯化的基本策略
![重组蛋白[Recombinant Protein]纯化的基本策略](https://img.taocdn.com/s3/m/634720d9d05abe23482fb4daa58da0116c171f98.png)
重组蛋白[Recombinant Protein]纯化的基本策略一、融合表达蛋白的纯化:融合表达蛋白可以在原目标分子之外带有GST肽段或(His)6肽段,从而使得可以分别用Glutathione Sepharose凝胶或Chelating Sepharos e凝胶进行亲和色谱分子,一步可以达到~90%的纯度,经过特异蛋白酶切后,再进行离子交换及高分辨凝胶过滤一般便可以达到所需的纯度(95~99%)。
二、包含体表达蛋白的纯化:在E.coli系统表达重组蛋白,表达量高时,常形成包含体,包含体易于与细胞其他组分分离,但需要注意的是蛋白复性的步骤。
一般采用盐酸胍溶解包含体蛋白后,用稀释的办法进行复性,也可以利用凝胶过滤色谱进行复性(已有多种凝胶可以促进蛋白质的复性的报道)。
以下以rhGM-CSF(重组人粒细胞 -巨噬细胞集落刺激因子)的下游纯化工艺为例:E.coli细胞,超声破碎,离心收集包含体,用7mol/L盐酸胍溶解包含体蛋白,作1:70稀释使蛋白复性,加硫酸铵至一定浓度后,上样于 P henyl-Sepharose 6 FF(high sub)色谱柱,活性组分再上Q-Sepharo se FF进行离子交换,最后上Superdex 75 prep grade凝胶进行凝胶过滤色谱,最终获得了纯度较高的rhGM-CSF,同时,DNA及内毒素去除率均很高。
如下表所示:步骤体积(ml)蛋白(mg)内毒素(EU/ml)DNA(pg/ml)起始(复性样品)4344 490 421 180HIC疏水柱 880 220 243 0.46AIEX阴离子交换 620 88 251 0.14GF凝胶过滤 1045 62 9 0.08三、周质表达的蛋白的纯化:可用渗透压休克方法,使周质释放,然后利用扩张床技术将含有菌体的悬液直接上柱(STREAmlINE系列凝胶),菌体穿过而表达的蛋白上柱。
重组蛋白质的表达与纯化

重组蛋白质的表达与纯化重组蛋白质是指通过基因工程技术将目标蛋白的基因导入到宿主细胞中,使其在宿主中表达并纯化得到的蛋白质。
这项技术应用广泛,被广泛用于生物制药、医学研究以及工业生产等领域。
下面将详细介绍重组蛋白质的表达与纯化过程。
一、重组蛋白质表达过程1. 选择表达宿主重组蛋白质表达宿主的选择十分重要。
常用的表达宿主包括大肠杆菌(E. coli)、酵母(yeast)、哺乳动物细胞等。
不同的表达宿主具有不同的特点和适用范围。
例如,大肠杆菌是最常用的表达宿主之一,具有高表达水平、易操作、成本低等特点。
2.构建表达载体表达载体是将目标基因导入宿主细胞的载体。
常用的表达载体有质粒、病毒载体等。
质粒是最常用的表达载体,它可轻松被细菌胞内扩增,并在细胞内产生大量目标蛋白。
3.转染和表达将构建好的表达载体导入到宿主细胞中,实现转染。
转染有多种方法,如电穿孔法、化学法、微粒子轰击法等。
转染后,宿主细胞会开始表达目标基因,合成目标蛋白。
4.优化表达条件为了提高重组蛋白质的产量和纯度,需要对表达条件进行优化。
常见的优化方法包括调节培养基成分、改变培养条件、优化诱导剂浓度等。
二、重组蛋白质的纯化过程1.细胞破碎与分离表达宿主中产生的重组蛋白质往往与其他细胞组分混合在一起,需要通过细胞破碎与分离来获取目标蛋白。
细胞破碎方法包括机械法、超声法、高压法等。
分离方法包括离心、电泳、柱层析等。
2.柱层析柱层析是常用的蛋白质纯化方法之一,它基于蛋白质在柱中不同吸附剂上的亲和力差异来实现分离纯化。
常用的柱层析方法有离子交换层析、亲和层析、凝胶过滤层析等。
3.其他纯化方法除了柱层析外,还有许多其他的纯化方法可供选择。
例如,凝胶电泳、过滤、冷冻干燥等。
这些方法通常用于进一步提纯和去除杂质,以获得纯度更高的重组蛋白质。
三、重组蛋白质应用与挑战重组蛋白质的应用广泛,涉及到生物制药、医学研究、农业等领域。
例如,通过重组蛋白质技术,可以生产用于治疗疾病的药物,如人胰岛素、白介素等。
重组蛋白的概述

重组蛋白的概述1.概述分离纯化组成了基因工程的下游处理(downstream processing)阶段,这一过程又和上游过程紧密相联系,上游过程的诸方面影响到下游的分离纯化,所以在进行目标蛋白质表达纯化时要统一考虑和整体设计,并充分考虑上游因素对下游的影响,如是否带有亲和标签,是否进行分泌表达。
目前应用最广泛的表达系统有三大类,分别是大肠杆菌表达系统、酵母表达系统和CHO细胞表达系统,不同的表达系统和培养方法显著影响下游的处理过程,目标蛋白表达是否形成包涵体,目标蛋白表达的定位(胞内、细胞内膜、周质空间和胞外),蛋白表达的量都依赖于所选择的表达系统。
选择将所表达的蛋白分泌到细胞外或周质空间可以避免破碎细胞的步骤,并且由于蛋白质种类少,目标蛋白容易纯化;而在细胞质内表达蛋白,可能是可溶性表达,可能形成包涵体,可溶性的蛋白往往需要复杂的纯化步骤,而包涵体易于分离,纯度较高,但回收具有生物活性的蛋白却变的相当困难,需要对聚集的蛋白进行变复性,通常活性蛋白的得率比较低,表1列出了不同策略对表达、纯化的影响,对于其中的有些缺点可以通过一定的方法进行克服和避免,如利用DNA重组技术给外源蛋白加上一个亲和纯化的标签,有助于可溶性外源蛋白的选择性纯化,并能保护目标蛋白不被降解(96)。
表 1 重组蛋白不同表达策略的优点和缺点表达策略优点缺点分泌表达至细胞外增强正确二硫键的形成降低蛋白酶对表达蛋白的降解可获得确定的N末端显著减少杂蛋白水平,简化纯化不需要细胞破碎表达水平低多数蛋白不能进行分泌表达表达蛋白需要进行浓缩细胞周质空间表达增强正确二硫键的形成可获得确定的N末端显著减少杂蛋白水平,简化纯化好些蛋白不能分泌进入周质空间没有大规模选择性的释放周质空间蛋白的技术周质蛋白酶可引起重组蛋白酶解胞内包涵体表达包涵体易于分离保护蛋白质不被降解蛋白质不具有活性对宿主细胞生长没有大的影响,通常可获得高的表达水平需要体外的折叠和溶解,得率较低具有不确定N末端胞内可溶性蛋白表达不需要体外溶解和折叠一般具有正确的结构和功能高水平的表达常难以得到需要复杂的纯化可发生蛋白质的酶解具有不确定的N末端在细胞的提取物中,除了目标蛋白外,还含有其它各种性质的蛋白、核酸、多糖等。
重组蛋白质的分离纯化 (1)

重组蛋白质的分离纯化摘要:90年代以来基因重组技术得到很大的发展,基因工程产品的分离纯化的成本约占其全部成本的60%~80%,因此重组蛋白的分离纯化技术越来越重要。
本文主要介绍了沉淀、液液萃取、层析等常用分离重组蛋白方法的原理及应用,旨在为开展蛋白质的制备及其应用研究提供理论依据。
关键词:重组蛋白质;分离;纯化;沉淀;液液萃取;层析;包涵体随着基因重组技术的发展,出现了很多基因工程产品,而作为基因工程技术的下游工程中的基因重组蛋白的分离纯化技术越来越显示其重要性。
据有人统计,基因工程产品的分离纯化成本约占到其全部成本的60%~80%[1]。
由此可见产品的分离纯化是获得目的产物的关键一步,也是比较困难的一步,它标志着生物产业的高低。
纯化重组蛋白质和普通蛋白质的不同就在于要选择合适的表达系统,因为表达系统决定了细胞培养过程中产物的性质以及可能产生的杂蛋白,而纯化重组蛋白质的主要目的是去除杂蛋白质,通常对一种重组蛋白质的纯化会采用多个系统[2]。
但是重组蛋白有几种不同的表达形式,如细胞外的分泌表达;细胞内可溶性表达以及包涵体形式的存在,因此对于重组蛋白的纯化要依据其表达形式的不同,采取不同的纯化工艺。
与传统方式相似,重组蛋白的分离纯化也是利用其物理和化学性质的差异,即以分子的大小、形状、溶解度、等电点、亲疏水性以及与其它分子的亲和性等性质建立起来的。
目前主要的纯化方法有浓缩沉淀法,层析和电泳技术。
重组蛋白质在分离纯化的过程中,必须维持一定的浓度和生物活性形式,以及防止被降解。
因此从生物体中有效分离纯化重组蛋白质一直是个难题。
90 年代以来,国内外许多科学工作者在蛋白质分离纯化技术和工艺上进行了大量的研制和开发,将原有的纯化技术水平提高到一个新的高度。
本文将简单介绍一些传统的分离纯化方法,并介绍近10 年来重组蛋白分离纯化中的新进展和一些新出现的技术。
1 沉淀分离技术1.1 盐析法其原理是蛋白质在高浓度盐溶液中,随着盐浓度的逐渐增加,由于蛋白质水化膜被破坏、溶解度下降而从溶液中沉淀出来。
重组胶原蛋白纯化内容介绍

重组胶原蛋白纯化内容介绍
重组胶原蛋白的纯化主要包括以下步骤:
1. 发酵:通过基因工程技术将编码所需胶原蛋白的基因克隆进入适当的宿主细胞中,在培养基中进行发酵。
2. 细胞破碎:发酵完成后,对细胞进行破碎,使细胞壁破裂,释放出细胞内的胶原蛋白。
3. 初步分离:将破碎后的细胞和培养基中的其他成分进行初步分离,常用的方法有离心、过滤等。
4. 纯化:采用各种纯化技术,如凝胶过滤、离子交换、亲和色谱等,将胶原蛋白与其他杂质进行分离。
5. 浓缩:对纯化后的胶原蛋白进行浓缩,使其浓度更高。
6. 干燥:采用真空干燥或冷冻干燥等方法,将胶原蛋白从液态变为固态,便于保存和运输。
在纯化过程中,需要注意保持胶原蛋白的生物活性和天然结构,避免对其造成破坏。
同时,还需要对胶原蛋白进行质量检测,确保其纯度和稳定性符合要求。
重组蛋白质的表达纯化和结构鉴定

重组蛋白质的表达纯化和结构鉴定在生物医学领域中,重组蛋白质凭借其广泛的应用前景成为了研究热点。
然而,要想获得高纯度的重组蛋白质,并对其结构进行准确的鉴定,需要经历一系列复杂而细致的实验步骤。
本文将从表达、纯化和结构鉴定三个方面介绍重组蛋白质的研究过程。
一、表达重组蛋白质的表达是研究重组蛋白质最初的关键步骤之一。
通常采用大肠杆菌(Escherichia coli)作为表达宿主。
首先,需要将目标基因克隆至表达载体中,确保其与启动子、转录因子等相互配合,并携带一定的标签,如His 标签、GST 标签等。
接着,将修饰好的表达载体转化至大肠杆菌中,采用选择性培养基筛选出目标菌株。
最后,将筛选得到的菌株进行大规模培养,促使目标基因在细胞内表达。
二、纯化获得表达目标蛋白的菌株后,需要将蛋白从细胞中纯化出来。
首先,采用超声波或高压颠破细胞壁,释放出蛋白质。
接着,通过离心等手段将蛋白质与其他细胞组分分离。
此时,可以利用目标蛋白质特异性的亲和层析柱,如镍柱、葡聚糖柱等,吸附目标蛋白质,并通过逆向洗脱等方法,得到高纯度的目标蛋白质。
三、结构鉴定获得纯度较高的重组蛋白质后,需要对其结构进行进一步的鉴定。
常用的结构鉴定方法包括X射线晶体学、核磁共振(NMR)、电子显微镜等。
X射线晶体学是目前应用最广泛的方法,通过将蛋白质结晶并进行X射线衍射实验,得到蛋白质的高分辨率结构。
NMR则通过测量蛋白质中核自旋的相对位置和相互作用关系,获取蛋白质的三维结构信息。
电子显微镜是一种能够获得蛋白质高分辨率结构的技术,主要应用于研究大分子复合物和纤维形态的蛋白质。
除了上述常用技术外,近年来还涌现出一些新的结构鉴定方法,如质谱联用技术、光学显微镜成像、负染电镜等。
这些方法的出现,为蛋白质结构鉴定提供了更多的选择和便利。
由于篇幅所限,本文仅对重组蛋白质的表达、纯化和结构鉴定进行了简要介绍。
事实上,研究重组蛋白质的过程还包括目标基因的设计与合成、蛋白质的功能分析等环节。
重组蛋白质的表达与纯化技术

重组蛋白质的表达与纯化技术蛋白质是生命体活动的重要组成部分,对于生命体的生长、繁殖和免疫功能起着至关重要的作用。
而重组蛋白质则是利用基因工程技术,将人工合成的外源基因导入到特定的宿主细胞中,通过细胞表达和纯化技术得到的转录翻译产物。
这种技术不仅可以生产天然蛋白质,还可以生产人工合成的新型蛋白质,对于疾病的治疗和新药的研发有着重要的意义。
一、蛋白质表达技术蛋白质表达是获得大量重组蛋白质的重要方法。
选择适当的宿主细胞和表达载体是获得高水平表达的关键。
常用的宿主细胞包括大肠杆菌、酵母菌、昆虫细胞、哺乳动物细胞等。
1.大肠杆菌表达系统大肠杆菌表达系统具有生长快、表达量高等优点,广泛应用于重组蛋白质的表达和纯化。
其表达载体主要有pET和pBAD两种,pET系统一般用于产生可以形成包涵体的重组蛋白,pBAD系统用于在分泌表达中产生滞留蛋白。
2.昆虫细胞表达系统昆虫细胞表达系统包括SF9、Sf21、HighFive等细胞系,常用的表达载体为pIB/V5-His、pFastBac等。
昆虫细胞表达系统通常用于表达大分子蛋白质,如糖蛋白、膜蛋白等。
3.哺乳动物细胞表达系统哺乳动物细胞表达系统是目前表达规模最大、表达产物最接近人体蛋白质的一种表达系统。
其表达载体主要有pCDNA3.1、pCI 等,常用于表达与人体有关的蛋白质,如抗体、生长因子等。
二、蛋白质纯化技术蛋白纯化是重组蛋白质生产的重要环节,其目的是得到高质量的、纯度较高的蛋白质样品。
常见的纯化方法包括亲和层析法、离子交换层析法、凝胶过滤层析法、逆流式层析法等。
1.亲和层析法亲和层析法是指因与载体中固定的亲和剂相互结合而纯化目标蛋白质的一种方法。
亲和剂通常是与目标蛋白质有特异性结合作用的化合物,如亲和标签、酶底物、抗体等。
常见的亲和层析方法有亲和柱层析、亲和膜层析等。
2.离子交换层析法离子交换层析法是根据蛋白质带有正或负电荷的差异性进行分离的一种方法。
离子交换层析的柱填充物常为离子交换树脂,其一般分为阴离子交换树脂和阳离子交换树脂两种。
重组蛋白纯化基本策略

重组蛋白纯化基本策略捕获阶段:目标是澄清、浓缩和稳定目标蛋白。
中度纯化阶段:目标是除去大多数大量杂质,如其它蛋白、核酸、内毒素和病毒等。
精制阶段:除去残余的痕量杂质和必须去除的杂质。
分离方法的选择根据蛋白质的特殊性质采用不同的分离方法:蛋白质的性质方法电荷(等电点)离子交换(IEX)分子量凝胶过滤(GF)疏水性疏水(HIC)反相(RPC)特异性结合亲和(AC)每一种方法都有分辨率、处理量、速度和回收率之间的平衡。
分辨率:由选择的方法和层析介质生成窄峰的能力来实现。
总的来说,当杂质和目标蛋白性质相似时,在纯化的最后阶段分辨率是重要因素。
处理量:一般指在纯化过程中目标蛋白的上样量。
如上样体积、浓度等。
速度:在初纯化中是重要因素,此时杂质如蛋白酶必须尽快除去。
回收率:随着纯化的进行渐趋重要,因为纯化产物的价值在增加。
在三阶段纯化策略中每一种方法的适用性见下表:技术主要特点捕获中度纯化精制样品起始状态样品最终状态IEX高分辨率高容量高速度低离子强度样品体积不限高离子强度或pH改变。
样品浓缩HIC分辨率好容量好高速度高离子强度样品体积不限低离子强度样品浓缩AC高分辨率高容量高速度结合条件特殊样品体积不限洗脱条件特殊样品浓缩GF高分辨率(使用Supedex)样品体积(<总柱体积的5%)和流速范围有限制缓冲液更换(如果需要)样品稀释RPC高分辨率需要有机溶剂在有机溶剂中,有损失生物活性的风险提示:1、通过组和各种方法使纯化步骤之间的样品处理减至最少,以避免需要调节样品。
第一个步骤的产物的洗脱条件应适宜于下一个步骤的起始条件。
2、硫酸铵沉淀是常用的样品澄清和浓缩方法,所以HIC是捕获阶段的理想方法。
3、 GF很适宜在由浓缩效应的方法(IEX、 HIC、 AC)后使用,凝胶过滤对上样体积有限制,但不受缓冲液条件的影响。
4、在捕获阶段选择对目标蛋白具有最高选择性或/和处理量的方法5、如果对目标蛋白的性质了解甚少的情况下,可采用IEX-HIC-GF的方法组合作为标准方案。
重组蛋白分离纯化的方法策略及案例介绍

肽配体结合为基础。同时,带有 GST 的蛋白与配体结合是可逆的,能够在温和,非变性的条件下通过加入还原型 谷胱甘肽被洗脱下来。
材料 BL21 感受态细胞 PGEX 表达载体 LB 培养基 Amp(氨苄青霉素) IPTG 蛋白酶抑制剂 缓冲液 1(100mmol/L Tris,PH 8.5,500mmol/L NaCl) 缓冲液 2(100mmol/L NaAc,PH 4.5,500mmol/L NaCl) PBS 缓冲液(100mmol/L NaCl,2.7mmol/L KCl,10mmol/L Na2HPO4,1.8mmol/L KH2PO4) 洗脱缓冲液(50mmol/L Tris,PH 8.0,10mmol/L GSH) 微量紫外分光光度计 超声波破碎仪 高速冷冻离心机 GST 柱
由上表可知选择将所表达的蛋白分泌到细胞外或周质空间可避免破碎细胞的步骤,而且细胞外和周质空间内的 蛋白种类较少,目的蛋白易纯化;而在细胞质内表达重组蛋白时,重组蛋白通常是可溶性表达,但也易形成包涵体。 可溶性蛋白往往需要复杂的纯化步骤,而包涵体易于分离且纯度较高,但回收具有生物活性的蛋白质却变得相当困 难,通常需要对聚集的蛋白进行变,复性,而通常情况下活性蛋白的得率比较低。德泰生物凭借多年的蛋白表达服 务操作经验和相关的技术,可以提供可溶性重组蛋白保证型服务和更高纯度的上清蛋白。
分离纯化原则总结: 1 应尽可能利用蛋白质不同物理特性选择所用的分离纯化技术,而不是利用相同技术多次纯化; 2 不同的蛋白在性质上有很大区别,每一步纯化步骤都应当充分利用目的蛋白和杂质成分物理性质差异; 3 在纯化早期阶段要尽量减少处理体积,方便后续纯化; 4 在纯化后期阶段,再使用造价高的纯化方法,有利于纯化材料的重复使用,减少再生复杂性。
重组猪瘟E2蛋白纯化工艺策略
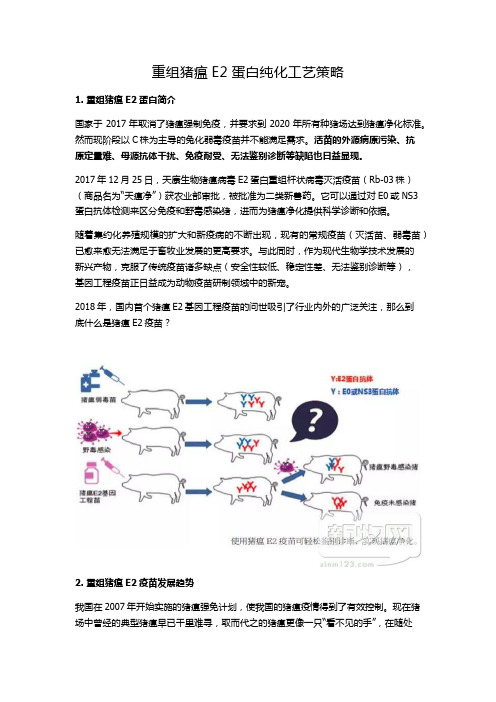
重组猪瘟E2蛋白纯化工艺策略1. 重组猪瘟E2蛋白简介国家于2017年取消了猪瘟强制免疫,并要求到2020年所有种猪场达到猪瘟净化标准。
然而现阶段以C株为主导的兔化弱毒疫苗并不能满足需求。
活苗的外源病原污染、抗原定量难、母源抗体干扰、免疫耐受、无法鉴别诊断等缺陷也日益显现。
2017年12月25日,天康生物猪瘟病毒E2蛋白重组杆状病毒灭活疫苗(Rb-03株)(商品名为“天瘟净”)获农业部审批,被批准为二类新兽药。
它可以通过对E0或NS3蛋白抗体检测来区分免疫和野毒感染猪,进而为猪瘟净化提供科学诊断和依据。
随着集约化养殖规模的扩大和新疫病的不断出现,现有的常规疫苗(灭活苗、弱毒苗)已愈来愈无法满足于畜牧业发展的更高要求。
与此同时,作为现代生物学技术发展的新兴产物,克服了传统疫苗诸多缺点(安全性较低、稳定性差、无法鉴别诊断等),基因工程疫苗正日益成为动物疫苗研制领域中的新宠。
2018年,国内首个猪瘟E2基因工程疫苗的问世吸引了行业内外的广泛关注,那么到底什么是猪瘟E2疫苗?2. 重组猪瘟E2疫苗发展趋势我国在2007年开始实施的猪瘟强免计划,使我国的猪瘟疫情得到了有效控制。
现在猪场中曾经的典型猪瘟早已千里难寻,取而代之的猪瘟更像一只“看不见的手”,在随处撩拨着猪瘟防控的现有规则。
此外,国家于2017年取消了猪瘟强制免疫,并要求到2020年,所有种猪场要达到猪瘟净化标准。
这一举措不但全面激活了猪瘟疫苗市场,也宣示着政府整合市场及自身资源,努力推进我国猪瘟疫病净化的决心。
如今,在“净化”的大旗下,便于鉴别诊断的标记疫苗成为了市场亟需产品。
然而现阶段以C株为主导的兔化弱毒疫苗并不能满足需求。
C株兔化弱毒苗自研制后广泛应用长达60多年,被业界惯称为“安全、高效”的疫苗典范。
但完美的C株也并非“神苗”,随着人们对猪瘟防控和根除的需求更替,活苗外源病原污染、抗原定量难、母源抗体干扰、免疫耐受、无法鉴别诊断等缺陷和不足也日益显现。
重组蛋白质表达和纯化的新策略

重组蛋白质表达和纯化的新策略一、引言在生物医学研究和工业生产中,蛋白质的表达和纯化是非常重要的步骤。
传统的蛋白质表达和纯化方法存在许多问题,例如低表达水平、纯化困难、失活等。
为了突破这些限制,科学家们不断探索新的策略和技术。
本文将介绍一些新的重组蛋白质表达和纯化策略,以期提高表达水平和纯化效率。
二、全细胞重组表达系统为了提高蛋白质的表达水平,许多研究人员采用了全细胞重组表达系统。
这种系统将目标蛋白的基因导入宿主细胞中,并利用宿主细胞的生物合成机制进行表达。
与传统的胞外表达系统相比,全细胞重组表达系统具有优势,例如高表达水平、一次性纯化等。
其中,大肠杆菌是最常用的宿主细胞之一。
此外,酵母菌、昆虫细胞和哺乳动物细胞也被广泛应用于全细胞重组表达系统中。
三、亲和纯化技术亲和纯化技术是纯化重组蛋白质的关键步骤之一。
常见的亲和纯化技术包括金属螯合层析、抗体亲和层析和亲和标签纯化等。
金属螯合层析是利用金属离子与亲和标签结合,实现目标蛋白的纯化。
抗体亲和层析则是利用抗体与目标蛋白结合,通过柱子进行分离纯化。
亲和标签纯化是在目标蛋白的C或N端添加亲和标签,利用标签与亲和介质结合,从而实现纯化。
这些亲和纯化技术在重组蛋白质表达和纯化中发挥了重要作用,提高了纯化效率和纯度。
四、纳米技术在蛋白质纯化中的应用纳米技术是当前研究的热点之一,其在蛋白质纯化中的应用也受到了广泛关注。
例如,纳米颗粒可以作为纯化材料的载体,具有较大的比表面积,从而提高了纯化效率。
此外,纳米技术还可以用于改善蛋白质的稳定性和抗失活能力。
例如,通过纳米包裹技术,可以使蛋白质受到保护,从而提高其稳定性和生物活性。
五、衍生技术的应用除了上述策略和技术外,还有一些衍生技术被应用于重组蛋白质表达和纯化中。
例如,基因工程技术可以通过修改目标蛋白质的氨基酸序列,提高其表达水平和稳定性。
此外,蛋白质工程技术可以通过改变蛋白质的结构和功能,进一步提高纯化效率和生物活性。
蛋白质浓缩与纯化技术

★ ★★★ 需要有机溶剂 中,有损失生
物活性的风险
宁馨阁
提示: 1、 通过组和各种方法使纯化步骤之间的样品处理减至最少,以避免需要调节样品。第一
个步骤的产物的洗脱条件应适宜于下一个步骤的起始条件。 2、 硫酸铵沉淀是常用的样品澄清和浓缩方法,所以 HIC 是捕获阶段的理想方法。 3、 GF 很适宜在由浓缩效应的方法(IEX、 HIC、 AC)后使用,凝胶过滤对上样体积有限
宁馨阁
前者进行反应时,配体(类似底物)是固相存在;后者进行反应时,底物呈液相存在。实质 上亲和层析是把具有识别能力的配体 L(对酶的配体可以是类似底物、抑制剂或辅基等)以 共价键的方式固化到含有活化基团的基质 M(如活化琼脂糖等)上,制成亲和吸附剂 M-L, 或者叫做固相载体。而固化后的配体仍保持束缚特异物质的能力。因此,当把围相载体装人 小层析柱(几毫升到几十毫升床体积)后,让欲分离的样品液通过该柱。这时样品中对配体 有亲和力的物质 S 就可借助静电引力、范德瓦尔力,以及结构互补效应等作用吸附到固相 载体上,而无亲和力或非特异吸附的物质则被起始缓冲液洗涤出来,并形成了第一个层析峰。 然后,恰当地改变起始缓冲 液的 PH 值、或增加离子强度、或加人抑③剂等因子,即可把 物质 S 从固相载体上解离下来,并形成了第 M 个层析峰(见图 6-2)。显然,通过这一操 作程序就可把有效成分与杂质满意地分离开。如果样品液中存在两个以上的物质与固相载体 具有亲和力(其大小有差异)时,采用选择性缓冲液进行洗脱,也可以将它们分离开。用过 的固相载体经再生处理后,可以重复使用。
宁馨阁
二.重组蛋白纯化的基本策略
来源: 生物谷 >> 实 验 >> 蛋白实验 >> 蛋白纯化 >>
重组蛋白的表达与分离纯化

基因工程重组蛋白的表达与分离纯化实验目的:1.了解基因工程重组表达载体的构建和筛选方法;2.掌握重组蛋白诱导表达的机理;3.掌握蛋白的分离纯化方法,并学会使用SDS-蛋白质凝胶电泳;实验原理:将外源基因克隆在含有lac启动子的pET-30表达载体中,让其在E.coli中表达。
先让宿主菌生长,lacI产生的阻遏蛋白与lacI操纵基因结合,从而不能进行外源基因的转录与表达,此时宿主菌正常生长。
然后向培养基中加入lac操纵子的诱导物IPTG,阻遏蛋白不能与操纵基因结合,则DNA外源基因大量转录并高效表达。
表达蛋白可经SDS-PAGE检测。
实验器材:1.仪器:高速冷冻离心机、恒温培养箱、高压灭菌锅、SDS-凝胶电泳仪、水浴锅、抽滤装置、AKTA液相色谱仪等;2.材料:LB培养基、溶菌酶、缓冲液A和B、氨苄青霉素、IPTG诱导剂、10%SDS等;实验内容:1.灭菌:①配置LB培养基20 ml*2 +100 ml*6(配方:酵母粉 0.5%,NaCl 1%,胰蛋白胨1%);②黄、蓝枪头各一盒;2.菌体活化及扩培:①每瓶20 ml LB培养基中加入20 ul Amp后,再加入30~40 ul DH5α菌液,置于37℃恒温箱内,培养12~16 h;②活化后,在六瓶100 ml LB培养基中分别加入100 ul Amp后,再从20 ml活化后的菌液中取2 ml,置于37℃恒温箱内扩大培养,至少培养2.5 h以后加入IPTG 200ul,37℃,培养14~16h;3.细胞破碎及蛋白分离:①将菌液用大离心管收集,配平后,4000r/min,离心15 min,收集菌体;②用20 ml BufferA重悬菌体,4000r/min,再离心15 min,收集菌体;③用4 ml BufferA重悬菌体,加入溶菌酶40 ul混匀,静置15min;④再加入4 ml BufferB,混匀,75℃水浴保温1 h;⑤用高速冷冻离心机在4℃的条件下,8000r/min,离心20 min,收集上清液;⑥将上清液分装入几个浓缩管中,4℃,3000r/min浓缩一段时间至终体积为5-10ml,做好标记,备用;⑦实验过程中,配置五种AKTA液相色谱仪所需液体,并抽滤2遍;4.AKTA液相色谱分析及SDS凝胶电泳:①首先学习AKTA仪器的相关使用方法和注意事项,对仪器进行排气,平衡缓冲液冲洗等操作(该部分由老师操作演示);②取5 ml浓缩后的液体过滤后上样,观察屏幕上紫外吸收曲线的变化,适时用离心管收集每个峰的样品,做好标号,备用。
以包含体形式表达的基因重组蛋白的纯化策略

以包含体形式表达的基因重组蛋白的纯化策略点击:112 添加时间: 2007-7-27 9:29:25 分离纯化以包含体形式表达的基因重组蛋白的步骤为:细胞破碎→包含体洗涤→包含体变性→蛋白复性→层析纯化。
一、包含体的洗涤:纯化以包含体形式表达的基因重组蛋白,包含体的洗涤至关重要,实验室最常用的破碎细胞的方法是超声破碎,超声处理时,DNA被切断无需再加DNA酶I,超声时产生大量的热,需在冰水浴中间断进行,一般选择超声强度和次数与包含体表达状况有关,表达量高,包含体致密的可以反复多次超声,和多次用超声缓冲液吹洗,8000-10000 rpm/min 10min弃上清,留取沉淀;对于表达量低,包含体不够致密的,在洗涤时就应注意,超声条件要温和,离心速度要提高12000-15000rpm/min 10-15min,必要时可以加入1-5%的TritonX-100和1-4M尿素浸泡过夜,或进行磁力搅拌以增加洗涤强度和净度。
二、包含体的变性常用的变性剂有8M尿素、6M盐酸胍、SDS。
尿素因价格低廉、呈电中性,变性条件温和,稀释复性后可以直接过离子交换剂进行纯化,常作为包含体变性剂的首选。
盐酸胍是强变性剂,复性时易出现沉淀,影响回收,且复性液中必须透析除净盐酸胍后,方可进行离子交换层析分离,不作首选;SDS与蛋白形成带负电的阴离子复合物,并与阴离子交换剂有强吸附,与阳离子交换剂不结合,更致命的弱点是常常会影响蛋白质的生物学活性,不常使用。
变性条件的选择,包含体变性完全与否直接影响进一步的复性,因此包含体的变性一定要完全。
对于易变性的包含体,室温放置或37℃1-3hr,甚至过夜变性,不易变性的包含体,可选择60℃3hr变性。
对于含有二硫键的蛋白质,为了变性完全,使二硫键完全打开,还应加入还原剂ß-ME和DTT。
三、蛋白质的复性蛋白质复性的最大问题,是在复性过程中形成中间体和多聚体,中间体阻碍作用大的使蛋白质正确折叠困难,复性就困难;阻碍小或无阻碍的容易复性。
带有His标签重组蛋白的纯化步骤

带有His标签重组蛋白的纯化步骤一、实验试剂Bind Buffer、Elution Buffer(500mM咪唑洗脱液)、20mM咪唑洗液、250mM咪唑洗脱液(目的蛋白洗脱液)、待纯化样品(含Vc蛋白)二、实验设备和材料填料(Ni SepharoseTM6Fast Flow)、纯化柱(带有滤膜)、可调节流速的塞子、500mL塑料瓶(正面经剪裁,配备20ml注射器管)、1L移液枪及相应枪头、100µL移液枪及相应枪头、10mL EP管或50mL离心管及相应板架、2mLEP管和1.5mL EP管及相应板架、冰盒;三、操作步骤(一)样品准备:(1)重组表达菌加IPTG后经低温(16˚C,摇速150rpm~180rpm)诱导表达8~16h,10000rpm离心5min,弃去上清(Amp+LB);(2)用PBS或Bind Buffer洗一次(重悬后在离心),加PBS或Bind Buffer (1/10的原上清体积量)重悬;(3)然后在冰水混合合物中超生破碎(工作时间5s,间隙时间5s,1个循环99次,一般6mL菌液1个~1.5个循环即可)(4)超声破碎后12000rpm(或10000g)4˚C离心10min,用5mL注射器小心吸取上清经0.45µm滤器过滤到干净的10mL EP管内(每管7mL)备用(如无需立即纯化,可暂存于-80˚C冰箱保存,使用时提前取出放冰上解冻)。
(二)装柱取填料2mL加入纯化柱中(可以先加2mL超纯水,用Marker笔标出位置),用超纯水洗5~7次(此步骤不需控制流速),除去储存液中的酒精,每次7mL。
(三)结合(1)用Bind Buffer洗3次(过柱时,用可调节流速的塞子将流速调至5s左右滴一滴的速度,下同),每次7mL,平衡柱子;(2)堵住下口,吸取7mL样品(使用用0.45µm滤器过滤;同时取100µL样品备用,SDS-PAGE鉴定时使用,下同)加入柱中,堵住上口,旋转柱子,使填料(镍柱)与样品充分混匀,4˚C垂直静置20~30min后(此时填料已沉到底部),打开上、下柱口,控制流速,回收滤液(滤液可取样100µL作对照),然后用4mL Bind buffer洗一次;(3)重复上一步骤2~3次;(4)打开上、下柱口,控制流速,收集滤液并取100µL样品取样备用;(5)用Bind buffer洗5次,每次4mL。
常见重组蛋白纯化方法

常见重组蛋白的纯化韦新桂(Chromatography) 北京韦氏博慧色谱科技有限公司,,weixingui@前言:近年来随着生物技术的进步,特别是基因工程的迅猛发展,表达蛋白已经变得很容易,相对而言,纯化却是一个非常繁杂的工作,所以越来越多的研究者把需要表达的目标蛋白和亲和纯化用的标签融合表达,这样纯化相对得比较容易,即使如此,由于蛋白的多样性,纯化依然是比较复杂而专业的工作,尤其对于不熟悉纯化的研究者而言,它成为一个项目的瓶颈,本手册就是把一些相关的材料汇集,希望对纯化重组蛋白有所帮助。
1.1常见纯化的标签理想的标签需要有以下的几个特点,1最好能一步纯化得到纯品;2对目标蛋白的结构和活性没有影响;3方便切除标签;4 应用范围广,可适用各种表达系统或目标蛋白。
但是没有哪个标签是完美的,只能根据实际需要去自己筛选,下表是部分的标签以及纯化的方案:标签纯化用的填料或配基洗脱方法多聚组氨酸(6XHis)螯合镍、铜、钴离子的填料咪唑或降低pH谷胱甘肽硫转酶(GST)键合谷胱甘肽的亲和填料 10-20mM还原谷胱甘肽麦芽糖结合蛋白(MBP)淀粉琼脂糖凝胶麦芽糖金黄色葡萄球菌蛋白A IgG琼脂糖凝胶低pHFlag peptide 抗Flag抗体 ,M1,M2 低pH或EDTA多聚精氨酸(Poly-Arg) SP琼脂糖凝胶高盐多聚半胱氨酸(Poly-Cys)活化巯基琼脂糖凝胶 DTT多聚苯丙氨酸(Poly-Phe)苯基琼脂糖凝胶乙二醇钙调蛋白结合肽钙调蛋白 EGTA 纤维素结合域纤维素盐酸胍或脲几丁质结合域几丁质巯基乙醇,半胱氨酸由于篇幅有限,手册只只写多聚组氨酸标签、GST融合蛋白。
2.组氨酸标签蛋白的纯化His-Tag融合蛋白是目前最常见的表达方式,而且很成熟,它的优点是表达方便而且基本不影响蛋白的活性,无论是表达的蛋白是可溶性的或者包涵体都可以用固定金属离子亲和色谱去(IMAC)纯化。
2.1 IMAC(Immobilized Metal-ion affinity chromatography)是Porath et al.1975年用固定IDA作为配基的填料螯合过渡金属铜、镍、钴或锌离子,可以吸附纯化表面带组氨酸、色氨酸或半胱氨酸残基的蛋白,1987年Smith et al. 发现带有几个组氨酸或色氨酸小肽和螯合金属离子的IDA-sephadex G-25作用力更强,此前在1986年他和他的合作者用Ni2+-IDA-sephadex G-25亲和纯化在氨基端带组氨酸和色氨酸的胰岛素原。
基因工程的下游技术重组蛋白的表达、纯化和分析

2. 亲和层析柱的安装 把层析柱固定在铁支架上,柱下端出 口封闭。加入少量的无离子水,排去下端 的空气泡。取出20%乙醇浸泡的螯合凝胶 4mL到烧杯中,加入少量的无离子水制成 糊状,沿着贴紧柱内壁的玻璃棒把糊状凝 胶倒进柱内,打开下端的排水口,让亲和 凝胶剂随水流自然沉下。亲和层析剂为 45mL。
3. 1#:接50μL空载工程菌(含pUC18)过夜培 养物,25-28℃培养10 h-12h; 2# :接 50μL 重组菌(含 pGFPuv )过夜培养 物,25-28℃培养10 h-12h; 3#:接50μL重组菌(含pGFPuv )过夜培养 物, 37℃培养至 O.D600 约为 0.5 (约 3h-4h) , 然后加入20%葡萄糖50μL至终浓度为0.2%, 及100mM IPTG 5μL至终浓度为0.1mM,2528℃培养8h-10h或过夜; 6#:接500μL重组菌(含pGFPuv)过夜培养 物, 37℃培养至 O.D600 约为 0.5 (约 3h-4h) , 然后只加入 100mM IPTG 50μL 至终浓度为 0.1 mM,25-28℃培养8h-10h或过夜。
一.实验目的 了解和掌握IPTG诱导表达的原理。 了解降解物阻遏的现象及其机理。
二.实验原理
操纵子是基因表达的协调单位。通常由2 个以上功能相关的结构基因以及一些调节 序列(如启动子序列、操纵序列等)组成。
乳糖操纵子由三个结构基因 Z 、 Y 、 A 和 操纵序列、启动子、 CAP 结合位点等调 节序列组成。
四.实验仪器
超净工作台、 恒温摇床、离心机等。
五.操作步骤 1. 挑取含pUC18质粒工程菌及含pGFPuv质 粒工程菌单菌落,分别接种于含氨苄青霉 (终浓度为100μg/mL,以下同)的5mL的 LB培养基中,于37℃、250rpm过夜培养 12h-14h至对数生长期。 2. 取 3 支已灭菌的大试管,分别加入 5mL 含 有氨苄青霉素的 LB 培养液,编号为 1# , 2#,3#,另取一个250mL的灭菌三角瓶, 编号为6#,加入50mL含氨苄青霉素的 LB 培养液。
重组蛋白纯化工艺建立

重组蛋白纯化工艺建立
重组蛋白纯化工艺的建立是一个涉及多个步骤的复杂过程。
以下是一个基本的步骤概述:
1. 设计和构建表达载体:首先,需要设计和构建一个包含目标基因的表达载体。
这个载体通常包括一个启动子、目标基因和一个终止子。
启动子和终止子用于控制目标基因的表达,而目标基因则编码所需的重组蛋白。
2. 转化和筛选宿主细胞:将构建好的表达载体转化到适当的宿主细胞中,并进行筛选,以获得能够高效表达目标蛋白的细胞株。
3. 蛋白表达和纯化:在选定的宿主细胞中诱导目标蛋白的表达,并通过离心、过滤等步骤收集细胞或上清液。
然后,利用适当的纯化方法,如亲和层析、离子交换层析、凝胶过滤等,去除杂质,获得纯度较高的重组蛋白。
4. 纯化工艺优化:对纯化工艺进行优化,以提高目标蛋白的纯度、产量和稳定性。
这可能涉及改变纯化步骤的顺序、调整纯化条件(如pH值、离子强度等)或使用不同的纯化方法等。
5. 质量控制:对纯化后的重组蛋白进行质量控制,以确保其符合预期的纯度、活性和稳定性等要求。
这可能包括使用SDS-PAGE、Western blot等方法检测蛋白的纯度和大小,以及使用生物活性测定等方法检测蛋白的活性。
需要注意的是,具体的纯化工艺会因目标蛋白的性质、宿主细胞的选择以及下游应用的需求而有所不同。
因此,在实际操作中,需要根据具体情况进行灵活调整和优化。
重组蛋白的分离纯化

疫苗: 大肠杆菌, 酵母, 大多数沿用细胞培养产物进行灭毒
单抗生产: 杂交瘤细胞 工业酶生产: 各种微生物
重组蛋白分离纯化方法选择的基因原则
针对不同的产物表达形式采取不同的策略 针对不同性质的重组蛋白选择不同的层析类型 多种分离纯化技术的联合运用 合适分离纯化介质的选择
1、重组载体的构建
特导引物设计,以pBV220-ALR质粒为模板扩增目的条带 构建酵母表达重组质粒,转化毕赤酵母GS115 重组蛋白的表达及鉴定 rhALR的纯化
菌液上清经低盐透析后,超过DEAESepharose FF柱的饱和吸附量上样,洗脱组 分脱盐后再上DEAE-Sepharose FF 柱,然后 再用Sephades G-75 柱进一步纯化。
这个末端突出通常由大约20个氨基酸组成, 并且在内质网中从成熟蛋白上剪切下来。
人们已经利用含有合适重组质粒的酵母细 胞分泌了大量的非酵母多肽,而且绝大多 数情况下都用到了a-因子信号序列。
外源基因的表达产物,通过运输或分泌的方式穿过细胞 的外膜进入培养基中,即为分泌型外源蛋白。
外源蛋白以分泌型蛋白表达时,须在N端加入15~30个 氨基酸组成的信号肽(signal peptides)序列。信号肽N端的 最初几个氨基酸为极性氨基酸,中间和后部为疏水氨基酸, 它们对蛋白质分泌到细胞膜外起决定性作用。当蛋白质分泌 到位于大肠杆菌细胞内膜与外膜之间的外周质时,信号肽被 信号肽酶所切割。
• Moreover , gel filtration is more generic, can be performed in any buffer condition, and can be used to resolve the oligomerization state of the target protein.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
捕获阶段:目标是澄清、浓缩和稳定目标蛋白。
中度纯化阶段:目标是除去大多数大量杂质,如其它蛋白、核酸、内毒素和病毒等。
精制阶段:除去残余的痕量杂质和必须去除的杂质。
分离方法的选择根据蛋白质的特殊性质采用不同的分离方法:蛋白质的性质方法电荷(等电点)离子交换(IEX)分子量凝胶过滤(GF)疏水性疏水(HIC)反相(RPC)特异性结合亲和(AC)每一种方法都有分辨率、处理量、速度和回收率之间的平衡。
分辨率:由选择的方法和层析介质生成窄峰的能力来实现。
总的来说,当杂质和目标蛋白性质相似时,在纯化的最后阶段分辨率是重要因素。
处理量:一般指在纯化过程中目标蛋白的上样量。
如上样体积、浓度等。
速度:在初纯化中是重要因素,此时杂质如蛋白酶必须尽快除去。
回收率:随着纯化的进行渐趋重要,因为纯化产物的价值在增加。
在三阶段纯化策略中每一种方法的适用性见下表:技术主要特点捕获中度纯化精制样品起始状态样品最终状态IEX高分辨率高容量高速度低离子强度样品体积不限高离子强度或pH改变。
样品浓缩HIC 分辨率好容量好高速度高离子强度样品体积不限低离子强度样品浓缩AC高分辨率高容量高速度结合条件特殊样品体积不限洗脱条件特殊样品浓缩GF高分辨率(使用Supedex)样品体积(<总柱体积的5%)和流速范围有限制缓冲液更换(如果需要)样品稀释RPC高分辨率需要有机溶剂在有机溶剂中,有损失生物活性的风险提示:1、通过组和各种方法使纯化步骤之间的样品处理减至最少,以避免需要调节样品。
第一个步骤的产物的洗脱条件应适宜于下一个步骤的起始条件。
2、硫酸铵沉淀是常用的样品澄清和浓缩方法,所以HIC是捕获阶段的理想方法。
3、 GF很适宜在由浓缩效应的方法(IEX、 HIC、 AC)后使用,凝胶过滤对上样体积有限制,但不受缓冲液条件的影响。
4、在捕获阶段选择对目标蛋白具有最高选择性或/和处理量的方法5、如果对目标蛋白的性质了解甚少的情况下,可采用IEX-HIC-GF的方法组合作为标准方案。
6、只要目标蛋白耐受的情况下,可以考虑采用RPC 方法用于精制阶段。
注:应该指出,三阶段纯化策略不是说所有的策略都必须是三个纯化步骤。
所用的步骤数目取决于纯度要求和蛋白的最终用途。
蛋白质的蛋白质特性与分离纯化技术的选择摘要:蛋白质的一级、二级、三级和四级结构决定了它的物理、化学、生物化学、物理化学和生物学性质,综述了不同蛋白质之间的性质存在差异或者改变条件是使之具有差异,利用一种同时多种性质差异,在兼顾收率和纯度的情况下,选择蛋白质提纯的方法。
关键词:蛋白质分离纯化前言:蛋白质在组织或细胞中一般都是以复杂的混合物形式存在,每种类型的细胞都含有成千种不同的蛋白质。
蛋白质的分离和提纯工作是一项艰巨而繁重的任务,到目前为止,还没有一个单独的或一套现成的方法能把任何一种蛋白质从复杂的混合物中提取出来,但对任何一种蛋白质都有可能选择一套适当的分离提纯程序来获取高纯度的制品。
蛋白质提纯的总目标是设法增加制品纯度或比活性,对纯化的要求是以合理的效率、速度、收率和纯度,将需要蛋白质从细胞的全部其他成分特别是不想要的杂蛋白中分离出来,同时仍保留有这种多肽的生物学活性和化学完整性。
能从成千上万种蛋白质混合物中纯化出一种蛋白质的原因,是不同的蛋白质在它们的许多物理、化学、物理化学和生物学性质有着极大的不同,这些性质是由于蛋白质的氨基酸的序列和数目不同造成的,连接在多肽主链上氨基酸残基可是荷正电的、荷负电的、极性的或非极性的、亲水的或疏水的,此外多肽可折叠成非常确定的二级结构(α螺旋、β折叠和各种转角)、三级结构和四级结构,形成独特的大小、形状和残基在蛋白质表面的分布状况,利用待分离的蛋白质与其它蛋白质之间在性质的差异,即能设计出一组合理的分级分离步骤。
可依据蛋白质不同性质与之相对应的方法将蛋白质混合物分离:1.分子大小不同种类的蛋白质在分子大小方面有一定的差别,可用一些简便的方法,使蛋白质混合物得到初步分离。
1.1透析和超滤透析在纯化中极为常用,可除去盐类(脱盐及置换缓冲液)、有机溶剂、低分子量的抑制剂等。
透析膜的截留分子量为5000左右,如分子量小于10000的酶液就有泄露的危险,在纯化中极为常用,可除去盐类、有机溶剂、低分子量的抑制剂等。
超滤一般用于浓缩和脱色1.2离心分离置换缓冲液许多酶富集于某一细胞器内,匀浆后离心得得到某一亚细胞成分,使酶富集10~20倍,再对特定的酶进行纯化。
差速离心,分辨率较低,仅适用于粗提或浓缩。
速率区带法,如离心时间太长所有的物质都会沉淀下来,故需选择最佳分离时间,可得到相当纯的亚细胞成分用于进一步纯化,避免了差速离心中大小组分一起沉淀的问题,但容量较小,只能用于少量制备。
等密度梯度离心常用的离主介质有蔗糖、聚蔗糖、氯化铯、溴化钾、碘化钠等等1.3凝胶过滤这是根据分子大小分离蛋白质混合物最有效的方法之一,注意使要离的蛋白质分子量落在凝胶的工作范围内。
选择不同的分子量凝胶可用于脱盐、置换缓冲液及利用分子量的差异除去热源。
2.形状蛋白质在离心通过溶液运动时,或通过膜、凝胶过滤填料颗粒或电泳凝胶中的小孔运动时,都会受到形状的影响:对两种相同质量的蛋白质而言,球状蛋白质具有较小的有效半径(斯托克半径),通过溶液沉降时遇到的摩擦力小,沉降较快而显得比其它形状的蛋白质大;反之,在体积排阻色谱时,斯托克半径较小的球状蛋白质更容易扩散进入凝胶过滤填料颗粒内部,较迟洗脱出来,因而显得比其它形状的蛋白质要小。
3.溶解度利用蛋白质的溶解度的差别来分别各种蛋白质常用的方法。
影响蛋白质溶解度的外界因素很多,其中主要有:溶液的pH、离子强度、介电常数和温度,但在同一的特定外界条件下,不同的蛋白质具有不同的溶解度。
适当改变外界条件,控制蛋白质混合物中某一成分的溶解度3.1pH控制和等电点沉淀蛋白质在其等电点一般较不易溶解。
3.2蛋白质的盐溶和盐析3.3有机溶剂分级法蛋白质在不同的溶剂中的溶解度有很大不同,从基本不溶(<10μg/ml)直至极易溶解(>300mg/ml)不等。
影响蛋白质溶解度的可变因素包括温度、pH、溶剂的极性、离子性质和离子强度。
引起蛋白质沉淀的有机溶剂的浓度不同,故控制有机溶剂的浓度可分离蛋白质。
水溶性非离子聚合物如聚乙二醇也能引起蛋白质的沉淀。
3.4温度不同的蛋白质在不同的温度具有不同的溶解度和活性。
大多数蛋白质在低温下比较稳定,故分离操作一般在0℃或更低温度下进行。
4.1电泳不仅是分离蛋白质混合物和鉴定蛋白质纯度的重要手段,而且也是研究蛋白质性质很有用的方法。
等电聚焦分辨率很高,pI有的差异就能分开。
2D-PAGE分离蛋白质分辨率已经发展到100000个蛋白点。
4.2离子交换层析改变蛋白质混合物溶液中的盐离子强度、pH和(阴、阳)离子交换填料,不同蛋白质对不同的离子交换填料的吸附容量不同,蛋白质因吸附容量不同或不被吸附而分离。
洗脱可采用保持洗脱剂成分一直不变,也可采用改变洗脱剂的盐度或pH的方法洗脱,后一种可分分段洗脱和梯度洗脱。
梯度洗脱一般效果好,分辨率高,特别是使用交换容量小,对盐浓度敏感的离子交换剂,多用梯度洗脱。
控制洗脱剂的体积(与柱床体体积相比)、盐浓度和pH,样品组分能从离子交换柱上分别洗脱下来。
蛋白分子暴露在外表面的侧链基团的种类和数量不同,故在一定的PH值和离子强度的缓冲液的所带的电荷不同5.电荷分布电荷的氨基酸残基可均匀地分布于蛋白质的表面,既可以适当的强度与阳离子交换柱结合也能以适当强度与阴离子结合,因多数蛋白质都有不能在单一的溶剂条件下同时与两种类型的离子交换柱结合,故可得用此性质纯化;电荷的氨基酸残基亦可成簇分布,使某一区域带强正电荷而另一区域带强负电荷,呈强酸性或强碱性,只能在极端pH与阳离子交换树脂或阴离子交换树脂结合,如钙调蛋白只能在pH2时与阳离子交换树脂结合。
6.疏水性多数疏水性的氨基酸残基藏在蛋白质的内部,但也有一些在表面。
蛋白质表面的疏水性氨基酸残基的数目和空间分布决定了该蛋白质是否具有与疏水柱填料结合从而利用它来进行分离的能力。
因其廉价和纯化后的蛋白质具有生物活性,是一种通用性的分离和纯化蛋白质的工具。
高浓度盐水溶液中蛋白质在柱上保留,在低盐或水溶液中蛋白质从柱上被洗脱,故特别适用于浓硫酸铵溶液沉淀分离后的母液以及该沉淀用盐溶解后的含有目标产品的溶液直接进样到柱上,当然也适用7mol/盐酸胍或8mol/L脲的大肠杆菌的治疗蛋白质提取液直接进样到柱上,在分离的同时也进行了复性。
7.密度多数蛋白质的密度在~cm3之间,分级分离蛋白质时一般不常用此性质,不过对含有大量磷酸盐或脂质的蛋白质与一般蛋白质在密度上明显不同,可用密度梯度法离心与大部分蛋白质分离。
8.基因工程构建的纯化标记通过改变 cDNA在被表达的蛋白的氨基端或羧基端加入少许几个额外氨基酸,这个加入的标记可用来作为一个有效的纯化依据。
8.1GST融合载体使要表达的蛋白质和谷胱甘肽S转移酶一起表达,然后利用Glutathione Sepharose 4B作亲和纯化,再利用凝血酶或因子Xa切开。
8.2蛋白A融合载体使要表达的蛋白和蛋白A的IgG结合部位融合在一起表达,以IgG Sepharose纯化。
8.3含组氨酸标记(Histidine-tagged)Chelating Sepharose最通行的标记之一,是在蛋白质的氨基端加上6~10个组氨酸,在一般或变性条件(如8M 尿素)下借助它能与Ni2+螯合柱紧紧结合的能力,用咪唑洗脱,或将pH降至使组氨酸充分质子化,不再与结合Ni2+使之得以纯化。
重组蛋白在设计、构建时已融入纯化构想。
样品多夹杂了破碎细胞或可溶产物,扩张床吸附技术STREAMLINE适合做粗分离9.亲和能力结合效率高,分离速度快的特点。
配基可是酶的底物、抑制剂、辅因子、特异性的抗体、吸附后可改变缓冲液的离子强度和PH的方法,洗脱下来,也可用更高浓度的同一配体溶液或亲和力更强的配体溶液洗脱亲和层析固定相的配基与生物分子之间的特殊的生物大分子亲和能力不同来进行相互分离的,依亲和选择性的高低分为:基团性亲和层析,固定相上的配基对一类基团的极强的亲和力。
如含有糖基的一类蛋白质或糖蛋白对三嗪染料显示特别强的吸附能力;高选择性(专一性)亲和层析,配基仅对某一种蛋白质有特别强的亲和性。
如单克隆抗体对抗原的特异性的吸附。
亲和层析除特异性的吸附外,仍然会因分子的错误认别和分子间非选择性的作用力而吸附一些杂蛋白质,另洗脱过程中的配体不可避免的脱落进入分离体系。
与超滤结合起来,将两者优点集中形成超滤亲和纯化,具有高分离效率和大规模工业化的优点,适用于初分离。
按配基的不同可分为:(1)金属螯合介质过渡金属离子Cu2+、Zn2+和Ni 2+等以亚胺络合物的形式键合到因定相上,由于这些金属离子与色氨酸、组氨酸和半胱氨酸之间形成了配价键,从而形成了亚胺金属—蛋白螯合物,使含有这些氨基酸的蛋白被这种金属螯合亲和色谱的固定相吸附。
