溶液 溶解度专题复习(word)
最新溶液 溶解度知识点总结及经典习题(含答案)(word)1

最新溶液 溶解度知识点总结及经典习题(含答案)(word )1一、溶液选择题1.30℃时,取甲、乙、丙中的两种固体各1g 分别放进盛有10g 水的两支试管中,充分振荡后的溶解情况如图。
下列说法正确的是A .甲物质的溶解度比乙物质的溶解度大B .加入试管1的固体是丙C .向烧杯中加入NH 4NO 3固体后,试管2中一定有晶体析出D .将30℃时甲、乙、丙三种物质的饱和溶液降温至 20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙【答案】B【解析】A .比较物质的溶解度大小须确定温度,故A 错误;B .30℃时三种物质只有丙的溶解度小于10g ,即100g 水中溶解溶质的质量小于10g ,则10g 水中溶解溶质的质量小于1g ,所以30℃时,取其中两种固体各1g 分别放进盛有10g 水的两支试管中,充分振荡后有剩余固体的是丙,即试管1,故B 正确;C .向烧杯中加入NH 4NO 3固体后,温度降低,若降到20℃以下,才有晶体析出,高于此温度,则无晶体析出;所以向烧杯中加入NH 4NO 3固体后,试管2中不一定有晶体析出,故C 错误;D .将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,甲乙溶解度减小,均析出晶体,溶质的质量减小,溶质的质量分数减小,丙溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数与降温前相等;饱和溶液中溶质质量分数=100g溶解度溶解度×100%,即溶解度越大质量分数也就越大,20℃时乙的溶解度大于甲的溶解度大于30℃时丙的溶解度,故所得溶液中溶质的质量分数的大小关系是乙>甲>丙,故D 错误;故选B 。
2.盐场晒盐后得到的卤水中含有MgCl 2、KCl 和MgSO 4等物质,它们的溶解度曲线如下图所示。
下列说法正确的是A.MgSO4的溶解度始终随温度的升高而减小B.t1℃时,KCl和MgSO4两溶液所含溶质质量一定相等C.t2℃时,100gMgCl2的饱和溶液中含有agMgCl2D.将t1℃时的KCl饱和溶液升温到t2℃,溶液由饱和变为不饱和【答案】D【解析】【分析】【详解】A、由溶解度曲线可知,MgSO4的溶解度不是始终随温度的升高而减小,故A错误;B、t1℃时,氯化钾和硫酸镁的溶解度相等,如果两种溶液是饱和溶液,并且溶液质量相等,则溶质质量一定相等,但题目未告知两溶液质量是否相等,故B错误;C、t2℃时,溶解度的含义是100g水中最多能溶解ag氯化镁,因此100gMgCl2的饱和溶液中含有氯化镁的质量小于ag,故C错误;D、氯化钾的溶解度随着温度的升高而增大,将t1℃时的KCl饱和溶液升温到t2℃,溶液由饱和溶液变成不饱和溶液,故D正确。
最新溶液 溶解度知识点总结及经典习题(含答案)(word)

最新溶液溶解度知识点总结及经典习题(含答案)(word)一、溶液选择题1.下图为两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )A.40℃恒温蒸发甲、乙两物质的饱和溶液,析出的乙比甲多B.20℃~40℃时,乙中含有少量甲,可用升温的方法提纯乙C.35℃,等质量的甲、乙溶液中,溶质的质量分数相等D.50℃向 100g25%的甲溶液中加入12.5g甲,溶液刚好饱和【答案】D【解析】A、甲、乙两物质的饱和溶液的质量不确定,错误;B、由溶解度曲线可知,20℃~40℃时,甲、乙的溶解度都随温度的升高而增大,且乙受温度的影响变化较大,故20℃~40℃时,乙中含有少量甲,可用降温的方法提纯乙,错误;C、由溶解度曲线可知,35℃时,甲、乙的溶解度相等,故35℃,等质量的甲、乙饱和溶液中,溶质的质量分数相等,错误;D、由溶解度曲线可知,50℃时,甲的溶解度为50g,即100g水中最多溶解50g甲物质,那么75g水中最多溶解37.5g甲物质。
100g25%的甲溶液中溶质的质量为100g×25%=25g,溶剂的质量为75g。
故50℃向100g25%的甲溶液中加入12.5g甲,溶液刚好饱和,正确。
故选D。
点睛:重点是抓住溶解度的实质结合溶解度曲线进行分析即可解决。
2.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( )①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①② B.①③ C.②④ D.③④【答案】A【解析】①称量的氯化钠固体中含有不溶性杂质,导致氯化钠质量偏小,从而导致配制的氯化钠溶液溶质质量分数偏小,正确;②用量筒量取水时仰视读数,导致读数偏小,而量筒中水的体积偏大,最终导致配制的氯化钠溶液溶质质量分数偏小,正确;③往烧杯中加水时有水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,错误;④溶液具有均一性,将配制好的溶液往试剂瓶中转移时有少量溅出,溶质质量分数不变,错误。
【化学】溶液 溶解度知识点总结及经典习题(含答案)(word)1

【化学】溶液 溶解度知识点总结及经典习题(含答案)(word )1一、溶液选择题1.甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是A .t 3℃时,甲的饱和溶液溶质与溶液的质量比为1:2B .t 1℃时,甲的溶解度大于乙的溶解度C .t 2℃时,甲、乙溶液的溶质质量分数都为30%D .t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量【答案】D【解析】A 、t 3℃时,甲物质的溶解度是50g ,所以甲的饱和溶液溶质与溶液的质量比为1:3,故A 错误;B 、通过分析溶解度曲线可知,t 1℃时,甲的溶解度小于乙的溶解度,故B 错误;C 、t 2℃时,甲、乙物质的溶解度是30g ,所以甲、乙饱和溶液的溶质质量分数都为30130g g×100%=23.1%,故C 错误; D 、t 3℃时,甲物质的溶解度大于乙物质的溶解度,所以t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量,故D 正确。
点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
2.甲、乙两种固体物质的溶解度曲线如图所示。
下列有关叙述中错误的是A .t 2℃时甲的溶解度比乙的大B .将甲、乙的饱和溶液从t 2℃降到t 1℃,析出甲的质量大C .升高温度可将甲的饱和溶液变成不饱和溶液D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等【答案】B【解析】【分析】由甲、乙两种固体物质的溶解度曲线图可知,甲的溶解度受温度的影响较大,乙的溶解度受温度的影响较小。
【详解】A、由甲、乙两种固体物质的溶解度曲线图可知,t2℃时甲的溶解度比乙的大,故A正确;B、将等质量甲、乙的饱和溶液从t2降到t1,析出甲的质量大,故B不正确;C、甲的溶解度随温度升高而增大,升高温度可以将甲的饱和溶液变成不饱和溶液,故C正确;D、t1℃时,两种物质的溶解度相等,甲和乙的饱和溶液各100g,其溶质的质量一定相等,故D正确。
溶液 溶解度知识点总结(word)1

溶液 溶解度知识点总结(word )1一、溶液选择题1.30℃时,取甲、乙、丙中的两种固体各1g 分别放进盛有10g 水的两支试管中,充分振荡后的溶解情况如图。
下列说法正确的是A .甲物质的溶解度比乙物质的溶解度大B .加入试管1的固体是丙C .向烧杯中加入NH 4NO 3固体后,试管2中一定有晶体析出D .将30℃时甲、乙、丙三种物质的饱和溶液降温至 20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙 【答案】B【解析】A .比较物质的溶解度大小须确定温度,故A 错误;B .30℃时三种物质只有丙的溶解度小于10g ,即100g 水中溶解溶质的质量小于10g ,则10g 水中溶解溶质的质量小于1g ,所以30℃时,取其中两种固体各1g 分别放进盛有10g 水的两支试管中,充分振荡后有剩余固体的是丙,即试管1,故B 正确;C .向烧杯中加入NH 4NO 3固体后,温度降低,若降到20℃以下,才有晶体析出,高于此温度,则无晶体析出;所以向烧杯中加入NH 4NO 3固体后,试管2中不一定有晶体析出,故C 错误;D .将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,甲乙溶解度减小,均析出晶体,溶质的质量减小,溶质的质量分数减小,丙溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数与降温前相等;饱和溶液中溶质质量分数=100g溶解度溶解度×100%,即溶解度越大质量分数也就越大,20℃时乙的溶解度大于甲的溶解度大于30℃时丙的溶解度,故所得溶液中溶质的质量分数的大小关系是乙>甲>丙,故D 错误;故选B 。
2.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( ) ①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数; ③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A .①② B .①③ C .②④ D .③④ 【答案】A【解析】①称量的氯化钠固体中含有不溶性杂质,导致氯化钠质量偏小,从而导致配制的氯化钠溶液溶质质量分数偏小,正确;②用量筒量取水时仰视读数,导致读数偏小,而量筒中水的体积偏大,最终导致配制的氯化钠溶液溶质质量分数偏小,正确;③往烧杯中加水时有水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,错误;④溶液具有均一性,将配制好的溶液往试剂瓶中转移时有少量溅出,溶质质量分数不变,错误。
(完整word版)初中九年级溶液、溶解度知识点总结和专题练习[含答案解析],推荐文档
![(完整word版)初中九年级溶液、溶解度知识点总结和专题练习[含答案解析],推荐文档](https://img.taocdn.com/s3/m/fa87576c51e79b89690226e2.png)
饱和溶液,不饱和溶液饱和溶液和不饱和溶液的概念:①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液饱和溶液与不饱和溶液的相互转化方法:(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大;七GD升温②培和溶剤饱和溶液不饱和溶液(2)对于Ca(0H)2:在一定量的水中溶解的最大量随温度升高而减少| :匕①降谧丄迦增加落训t饱和石灰水卩温不饱和石灰水概念的理解:(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。
因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。
如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:|呕①饱和溶液不饱和溶液(或不饱和溶液饱和溶液。
不发生结晶的前提下)溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液饱和溶液溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
ihL' J jb .乱■ >i|③不饱和溶液饱和溶液(不发生结晶的前提下)溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液不饱和溶液溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小判断溶液是否饱和的方法:①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。
溶液 溶解度知识点总结和题型总结(word)

溶液溶解度知识点总结和题型总结(word)一、溶液选择题1.下列四个图象分别对应四种操作过程,其中正确的是()A.将一定质量分数的硫酸溶液加水稀释B.向硫酸铜的溶液中加入氢氧化钠溶液直至过量C.常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应D.将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直到有晶体析出【答案】C【解析】【分析】稀释酸性溶液,溶液酸性减弱, 硫酸铜和氢氧化钠反应生成蓝色沉淀氢氧化铜和硫酸钠, 稀硫酸和锌反应生成硫酸锌和氢气,和铁反应生成硫酸亚铁和氢气, 饱和溶液和不饱和溶液之间可以相互转化。
【详解】A、将一定质量分数的硫酸溶液加水稀释,溶液酸性减弱,pH升高,但是不能升高到7,更不能大于7,故A不正确;B、向硫酸铜的溶液中加入氢氧化钠溶液,硫酸铜和氢氧化钠反应生成蓝色沉淀氢氧化铜和硫酸钠,立即产生沉淀,故B不正确;C、常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应,锌比铁活泼,反应速率快,反应需要时间短,最终铁和稀硫酸反应生成的氢气多,故C正确;D、一定质量的硝酸钾不饱和溶液溶质质量分数不能是0,故D不正确。
故选C。
2.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A.10℃时,甲、乙两种物质的饱和溶液浓度相同B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【答案】D【解析】【分析】【详解】A、根据溶解度曲线,10℃时,甲、乙的溶解度都是20g,故甲、乙两种物质的饱和溶液浓度相同,选项A正确;B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,选项B正确;C、根据溶解度曲线,30℃时,甲物质的溶解度为60g,故将40g甲物质加入到50g水中并充分搅拌,只能溶解30g,故充分溶解后溶液的质量为80g,选项C正确;D、根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故10℃时,将两种饱和溶液升温至30℃,都成为30℃时的不饱和溶液,但溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,选项D错误。
最新溶液 溶解度中考题集锦(word)
最新溶液溶解度中考题集锦(word)一、溶液选择题1.配制一定质量分数的氯化钠溶液,下列操作正确的是A.称量固体时,左盘放砝码,右盘放氯化钠B.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签C.量取液体时,手持量筒,视线与液体的凹液面的最低处保持水平D.称量固体时,发现指针向左偏,应该用镊子将游码向右移动直至天平平衡【答案】B【解析】A、称量固体药品的质量时要注意“左物右码”,错误;B、溶于配制好后需要标明溶液的名称和溶质的质量分数,正确;C、量取液体体积时,量筒应放在水平桌面上,错误;D、定量称量固体质量时,指针向左偏,说明左盘重了,应该减少药品的质量直至天平平衡,错误。
故选B。
2.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( )①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①② B.①③ C.②④ D.③④【答案】A【解析】①称量的氯化钠固体中含有不溶性杂质,导致氯化钠质量偏小,从而导致配制的氯化钠溶液溶质质量分数偏小,正确;②用量筒量取水时仰视读数,导致读数偏小,而量筒中水的体积偏大,最终导致配制的氯化钠溶液溶质质量分数偏小,正确;③往烧杯中加水时有水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,错误;④溶液具有均一性,将配制好的溶液往试剂瓶中转移时有少量溅出,溶质质量分数不变,错误。
故选A。
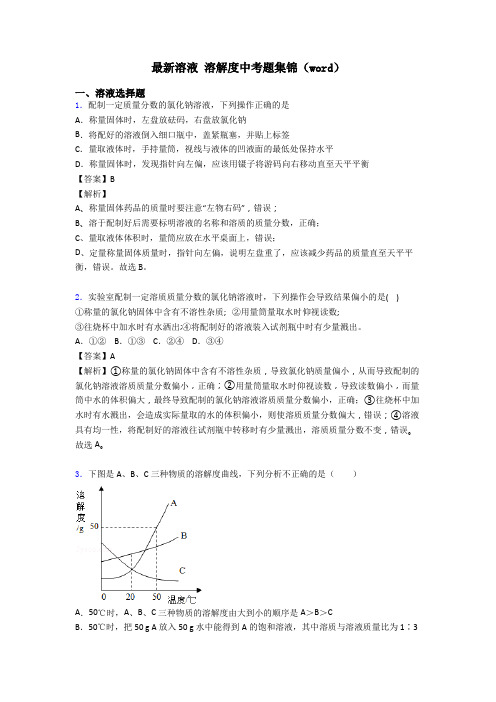
3.下图是A、B、C三种物质的溶解度曲线,下列分析不正确的是()A.50℃时,A、B、C三种物质的溶解度由大到小的顺序是A>B>CB.50℃时,把50 g A放入50 g水中能得到A的饱和溶液,其中溶质与溶液质量比为1∶3C.将50℃时,A、B、C三种物质的饱和溶液降温度20℃时,这三种溶液的溶质质量分数的大小关系是B>C=AD.将C的饱和溶液变为不饱和溶液,可采用降温的方法【答案】C【解析】【分析】【详解】A、由A、B、C三种固体物质的溶解度曲线可知,在50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C,选项A正确;B、由A物质的溶解度曲线可知,在50℃时,A物质的溶解度是50g,把50g A放入50g水中能得到A的饱和溶液,只能溶解25gA物质,其中溶质与溶液质量比为25g∶(25g+50g)=1∶3,选项B正确;C、将50℃时A、B、C三种物质的饱和溶液降温至20℃时,由于A、B的溶解度随温度的降低而减小,形成的是20℃时饱和溶液,此时溶质质量分数B>A;由于C的溶解度随温度的降低而增大,溶液中溶质的质量分数仍是原来50℃时饱和溶液溶质的质量分数,因此从图中可以判断,降温至20℃时三种溶液的溶质质量分数的大小关系是:B>A>C,选项C错误;D、由C物质的溶解度曲线可知,C物质的溶解度随温度降低而增大,所以将C的饱和溶液变为不饱和溶液,可采用降温的方法,选项D正确。
【化学】溶液 溶解度知识点总结及经典习题(含答案)(word)

【化学】溶液溶解度知识点总结及经典习题(含答案)(word)一、溶液选择题1.甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是()A.a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液B.甲和乙的溶解度相等C.a2℃时,在 100 g 水中加入 60 g 甲,形成 160 g 溶液D.a1℃时,甲和乙各 30 g 分别加入 100 g 水中,均形成饱和溶液【答案】D【解析】A、由图象可知,甲、乙的溶解度随着温度的升高而增大,因此a1℃时甲和乙的饱和溶液,升温到a2℃时变为不饱和溶液,错误;B、物质的溶解度与温度有关,a1℃时,甲和乙的溶解度相等,不是a1℃时,甲和乙的溶解度不等,错误;C、a2℃时,甲的溶解度为50g,在100g水中加入60g甲,形成饱和溶液,并有10g甲溶解不了,错误;D、a1℃时,甲和乙的溶解度均为30g,所以甲和乙各30g分别加入100g水中,均形成饱和溶液,正确。
故选D。
2.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( )①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①② B.①③ C.②④ D.③④【答案】A【解析】①称量的氯化钠固体中含有不溶性杂质,导致氯化钠质量偏小,从而导致配制的氯化钠溶液溶质质量分数偏小,正确;②用量筒量取水时仰视读数,导致读数偏小,而量筒中水的体积偏大,最终导致配制的氯化钠溶液溶质质量分数偏小,正确;③往烧杯中加水时有水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,错误;④溶液具有均一性,将配制好的溶液往试剂瓶中转移时有少量溅出,溶质质量分数不变,错误。
故选A。
3.如图是KNO3、MgSO4、NaCl三种物质的溶解度曲线。
下列说法正确的是()A.t2℃时,把40g KNO3放入50g水中能得到KNO3饱和溶液,其中溶质和溶液的质量比为4:9B.t3℃时,图中三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数大小关系为NaCl>MgSO4>KNO3C.t4℃时,其他条件不变,把MgSO4饱和溶液升温到t5℃,在此操作过程中溶液里无明显现象D.KNO3中含有少量的NaCl杂质,采用蒸发结晶法提纯【答案】B【解析】【详解】A、t2℃时,硝酸钾的溶解度是40g,所以把40g KNO3放入50g水中能得到KNO3饱和溶液,其中溶质和溶液的质量比为20g:70g=2:7,故A错误;B、t1℃时,氯化钠的溶解度最大,硝酸钾的溶解度最小,所以t3℃时,图中三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数大小关系为NaCl>MgSO4>KNO3,故B正确;C、t4℃时,其他条件不变,把MgSO4饱和溶液升温到t5℃,溶解度减小,在此操作过程中溶液里会析出晶体,故C错误;D、硝酸钾的溶解度受温度变化影响较大,所以KNO3中含有少量的NaCl杂质,采用降温结晶法提纯,故D错误。
溶液 溶解度总复习经典例题、习题(word)

A.t1℃时将等质量的乙、丙溶于水中,分别配成饱和溶液,所得溶液质量:乙=丙 B.将 t1℃时甲、丙的饱和溶液升温到 t2℃,两种溶液中溶质的质量分数相等 C.要将接近饱和的丙溶液变为饱和溶液,可以采用降温或蒸发的方法 D.t3℃时,将三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量顺序:甲>丙>乙 【答案】A 【解析】A、t1℃时,乙的溶解度等于甲,将等质量的甲、乙分别配成饱和溶液,所需要的 水的质量相等,故所得溶液质量甲=乙,故正确; B、将 t1℃时甲、丙的饱和溶液升温到 t2℃,甲的溶解度随温度的升高而增大,故溶液组成 不变,而丙的溶解度随温度的升高而减小,会析出晶体,溶质质量分数会减小,但 t2℃是 丙的溶解度大于 t1℃时甲的溶解度,故两种溶液中溶质的质量分数丙大于甲,故错误; C、由溶解度曲线可知,丙的溶解度随着温度的降低而增大,因此要将接近饱和的丙溶液 变为饱和溶液,可以采用升温或蒸发的方法,故正确; D、t3℃时三种物质的溶解度关系为甲>乙>丙,将 t3℃时三种物质的饱和溶液恒温蒸发等 量水后,析出溶质的质量甲>乙>丙,故错误。 点睛: 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解 性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的 大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶 的方法达到提纯物质的目的。
溶液中溶质质量分数= 溶解度 ×100%,即溶解度越大质量分数也就越大,20℃时 溶解度 100g
乙的溶解度大于甲的溶解度大于 30℃时丙的溶解度,故所得溶液中溶质的质量分数的大小 关系是乙>甲>丙,故 D 错误;故选 B。
最新溶液溶解度知识点梳理及经典练习(超详细).docx

D.可采用降低温度的方法使乙的饱和溶液变为不饱和溶液
【答案】B
【解析】试题分析:温度小于t1℃时甲的溶解度随温度变化比乙小;t2℃时甲的饱和溶液
的溶质质量分数=30克/130克×100%,小于30%;t1℃时,甲、乙饱和溶液的溶质质量分
数相等;可采用升高温度的方法使乙的饱和溶液变为不饱和溶液。故选B.
氢氧化钠、碳酸钠分别在水、酒精中的溶解度
氢氧化钠碳酸钠
20℃9g
21.8g
49g
酒精17.3g40g不溶不溶
A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观
B.由表格数据可知,物质的溶解度只受温度影响
C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液
【解析】
【分析】
【详解】
A、t℃时K2CO3和KNO3的溶解度相同,由表格中的数据可知,在60℃到
都包括126-139间的数值,所以t℃在60℃到80℃之间,故A正确;
80℃之间溶解度
B、t℃时,两种物质只有是饱和溶液时,溶质质量分数一定相等
相等,故B正确 ;
,则 溶质质量分数不一定
C、等质量的两种饱和液从80℃降温到20℃,析出晶体(不含结晶水)的质量硝酸钾比碳酸
们的关系是:N<M<P=Q,故D正确;答案为B。
点睛:准确理解图像并获取信息是解题关键,此图象是
t℃时物质的溶解情况,不能验证
不同温度下溶解度大小的关系,图中四点的含义分别是
N点100g
水中溶解20g
溶质的不
饱和溶液;M点80g水中溶解20g溶质的不饱和溶液;
P点100g水中溶解40g溶质的饱和
最新溶液 溶解度知识点总结和题型总结(word)1

最新溶液溶解度知识点总结和题型总结(word)1一、溶液选择题1.如图为甲、乙两种物质的溶解度曲线,下列说法正确的是A.20℃时,12 g的乙物质能完全溶于50 g的水中B.30℃时,甲物质的溶解度大于乙物质的溶解度C.将甲溶液从50℃降温到30℃时,一定有晶体析出D.将接近饱和的乙溶液变为饱和溶液,可以升高温度【答案】B【解析】A.根据20℃时,乙物质的溶解度分析;B.根据30℃时,甲、乙两物质的溶解度分析;C.根据溶液是否饱和分析;D.根据乙的溶解度随温度的升高而增大分析。
解:A. 由图可知,20℃时,乙物质的溶解度为20g。
因此20℃时,12 g的乙物质不能完全溶于50 g的水中,故错误;B. 由图可知,30℃时,甲物质的溶解度大于乙物质的溶解度,正确;C. 将甲溶液从50℃降温到30℃时,不一定有晶体析出,因为此时溶液不一定饱和,故错误;D. 由图可知,乙物质的溶解度随温度的升高而增大。
因此将接近饱和的乙溶液变为饱和溶液,可以升高温度是错误的。
点睛:饱和溶液与溶解度。
2.一定温度下,向盛有100g蔗糖溶液的烧杯中再加入5克蔗糖,充分搅拌后一定不变的是A.溶质的质量B.溶液的质量C.溶质的质量分数D.蔗糖的溶解度【答案】D【解析】【分析】溶液由溶质和溶剂组成,溶液的质量等于溶质和溶剂的质量和,被溶解的物质叫溶质。
【详解】在一定温度下,向盛有100克蔗糖溶液的烧杯中再加入5克蔗糖,不确定蔗糖是否溶解,溶质、溶液、溶质的质量分数不能确定是否改变,影响固体物质溶解度的因素是温度,温度没有改变,溶解度一定不改变,故选D。
3.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A.10℃时,甲、乙两种物质的饱和溶液浓度相同B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【答案】D【解析】【分析】【详解】A、根据溶解度曲线,10℃时,甲、乙的溶解度都是20g,故甲、乙两种物质的饱和溶液浓度相同,选项A正确;B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,选项B正确;C、根据溶解度曲线,30℃时,甲物质的溶解度为60g,故将40g甲物质加入到50g水中并充分搅拌,只能溶解30g,故充分溶解后溶液的质量为80g,选项C正确;D、根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故10℃时,将两种饱和溶液升温至30℃,都成为30℃时的不饱和溶液,但溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,选项D错误。
最新溶液 溶解度知识点(大全)(word)1

最新溶液溶解度知识点(大全)(word)1一、溶液选择题1.如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是A.t1℃时三种物质溶解度的大小为b>a=cB.将t2℃时a的饱和溶液150g降温到t1℃时,析出溶质30gC.要从含有少量c的a溶液中得到较多的a晶体,通常采用降温结晶的方法D.t2℃时,将1ga物质加入到2g水中不断搅拌,能形成3g不饱和深【答案】D【解析】A.由溶解度曲线可知t1℃时三种物质溶解度的大小为b>a=c,故A正确;B.将t2℃时a的溶解度是50g,饱和溶液150g中含溶质50g,当降温到t1℃时,因t1℃时a物质的溶解度为20g,因此会析出溶质30g,故B正确;C.a的溶解度随温度升高增大且影响较大,而c物质的溶解度随温度升高而减小,因此要从含有少量c的a溶液中得到较多的a晶体,通常采用降温结晶的方法,故C正确;D.从图象中可以看出t2℃时,a物质的溶解度为50g,即50g固体a在100g水中溶解达到饱和状态,形成150g溶液,比值为1:2:3,故t2℃时,将1g a物质加入到2g水中不断搅拌,能形成应是3g饱和溶液,故D 不正确;故选D。
2.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是()A.t2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的升高而增大C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%【答案】D【解析】A、根据题中溶解度曲线图可知t2℃时,甲乙两种物质的溶解度相等,故正确.B、根据题中溶解度曲线图可知, 甲的溶解度随温度的升高而增大,故正确C、t2℃时,甲、乙、丙三种物质的饱和溶液溶质质量分数由大到小的顺序为:甲乙丙;当降温到t1℃,甲乙仍为饱和溶液,丙为不饱和溶液,在t1℃乙的饱和溶液的溶质质量分数大于甲饱和溶液的溶质质量分数;故降温至t1℃,所得溶液中溶质的质量分数的大小顺序为乙>甲>丙D、 t1℃时,丙的饱和溶液中溶质的质量分数为40/140100%=28.6%,故错误故选D3.如图是甲乙两种物质的溶解度曲线,下列说法正确的是()A.甲的溶解度大于乙的溶解度B.t℃时,甲乙饱和溶液中溶质的质量分数相等C.升高温度能使接近饱和的甲溶液变为饱和溶液D.10℃时,分别用100g水配制甲乙的饱和溶液,所需甲的质量大于乙的质量【答案】B【解析】【分析】【详解】A、由两种物质的溶解度曲线可以看出,当0~t℃时,乙的溶解度大于甲的溶解度,选项A 错误;B、t℃时,二者的溶解度相等,饱和溶液中溶质的质量分数也相等,选项B正确;C、由甲物质的溶解度曲线可以看出,甲物质的溶解度随着温度的升高而增大,所以升高温度不能使接近饱和的甲溶液变为饱和溶液,选项C错误;D、过10℃作一条垂直于横坐标的垂线,看垂线与曲线的交点高低,从图象可以看出,此时乙的溶解度大于甲的溶解度,选项D错误。
【化学】中考考点_溶液 溶解度知识点汇总(全)(word)1

【化学】中考考点_溶液溶解度知识点汇总(全)(word)1一、溶液选择题1.NaCl、KNO3两种固体物质的溶解度曲线如图所示。
下列说法正确的是A.20℃时,NaCl的溶解度为31.6 gB.将10℃时两物质饱和溶液升温至30℃,溶液中溶质的质量分数都增大C.为了除去NaCl固体中混有的少量KNO3,可加热将其完全溶解后,再通过降温结晶、过滤来除之D.50℃时,将50g KNO3加入50g水中,充分溶解后溶液的质量为92.75g【答案】D【解析】A. 在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。
20℃时,NaCl的溶解度为31.6 g;B. 将10℃时两物质饱和溶液升温至30℃,;两种物质的溶解度变大,溶质的质量不变,溶液中溶质的质量分数都不变;C. 为了除去NaCl固体中混有的少量KNO3,可加热将其完全溶解后,再通过降温结晶、过滤来除之;因为硝酸钾的溶解度随温度的降低而迅速减小,而氯化钠的溶解受温度的影响很小,所以降温析出晶体几乎全是硝酸钾。
过滤得硝酸钾固体。
D. 50℃时,将50g KNO3加入50g水中,溶解硝酸钾42.75g,充分溶解后溶液的质量为92.75g;选D2.下表是KCl与KNO3在不同温度的溶解度。
下列说法不正确...的是()温20304050度/℃KCl34.0g37.0g40.0g42.6gKNO331.6g45.8g63.9g85.5gA.20℃时,KC1的溶解度大于KNO3的溶解度B.两物质溶解度相等的温度在20~30℃之间C.40℃时,5gKCl中加10g水可得33.3%溶液D.50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出【答案】C【解析】试题分析:由两种物质的溶解度可知20℃时,KNO3溶解度小于KC1的溶解度,A正确;由表格数据可知温度在20~30℃时,两物质的溶解度有相同的部分,即两物质溶解度相等的温度在20~30℃之间,B正确;40℃时,KCl的溶解度为40g,即该温度下40g氯化钾溶解在100g水中恰好形成饱和溶液,那么10g水中最多溶解4g氯化钾,形成的溶液的溶质质量分数=4g/14g ×100%=28.6%,C错误;30℃时硝酸钾的溶解度为45.8g,即该温度下45.8g硝酸钾溶解在100g水中恰好形成饱和溶液,那么20g水中最多溶解硝酸钾9.16g,即50℃时,10g KNO3中加20g水,充分溶解,再降温到30℃,有KNO3固体析出,D正确。
【化学】溶液 溶解度知识点总结(word)1

【化学】溶液溶解度知识点总结(word)1一、溶液选择题1.A、B、C三种物质的溶解度曲线如图所示。
下列分析正确的是()A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量相等B.t2℃时,把30g甲放入50g水中能得到80g甲的饱和溶液C.将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是甲=乙D.将t2℃时的乙溶液降温到t1℃时,一定有晶体乙析出【答案】C【解析】【分析】甲、乙两种物质的溶解度随温度增加而增大,交点表示两种物质的溶解度相同。
【详解】A、t1℃时,甲、乙两种物质的溶解度相等,如果甲、乙两物质的饱和溶液的溶液质量相等,则所含的溶质质量相等,但是如果溶液质量不等,则溶质质量不等,故A不正确;B、t2℃时,甲的溶解度为50g,把30g甲放入50g水中能溶解的质量为100g,把30g甲放入50g水中能得到50g+25g=75g甲的饱和溶液,故B不正50g=25g50g确;C、将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃,溶液仍是饱和溶液,甲、乙的溶解度相同,所得溶液的溶质质量分数的大小关系是甲=乙,故C正确;D、t2℃时的乙溶液可能是饱和溶液,也可能不是饱和溶液,如果是饱和溶液,降温到t1℃时,才有晶体乙析出,故D不正确。
故选C。
【点睛】固体物质的溶解度是指在一定的温度下,100g溶剂中溶解溶质达到饱和状态时溶解的溶质的质量,故分析有无晶体析出,要看溶液是否饱和。
2.下图是不含结晶水的甲、乙两种固体物质的溶解度曲线,下列叙述正确的是A.t1℃时,100g甲的饱和溶液中含有50g甲B.t1℃时,配制甲乙两种物质的饱和溶液,需要相同体积的水C.t1℃时,将等质量的甲、乙的饱和溶液升温至t2℃,溶液质量仍然相等D.要从含少量乙的甲中提纯甲,通常可采用蒸发结晶的方法【答案】C【解析】A.由图知t1℃时,甲物质的溶解度是50g,即100g水中最多能溶解甲物质50g,故A错误;B. t1℃时,甲、乙两物质的溶解度都是50g,但是不知道所配甲乙两种物质的饱和溶液的质量是否相等,故需要的水的体积也不一定相等,故此选项错误;C. 因两物质的溶解度都是随温度的升高而增大,故当t1℃时,将等质量的甲、乙的饱和溶液升温至t2℃,两溶液都变为不饱和溶液,故溶液质量仍然相等,此选项正确。
溶液 溶解度专题复习(word)

溶液溶解度专题复习(word)一、溶液选择题1.甲、乙两种物质的溶解度曲线如图所示。
下列叙述正确的是A.甲的溶解度比乙的大B.将t2℃时甲、乙饱和溶液降温到t1℃,析出甲的质量大C.t2℃时,等质量甲和乙的饱和溶液中所含溶剂的质量甲>乙D.将t1℃时甲、乙饱和溶液升温的t2℃,溶液的溶质质量分数相等【答案】D【解析】A、在比较物质的溶解度时,需要指明温度,故错误;B、将甲、乙的饱和溶液的质量不确定,所以从t 2℃降到t1℃,析出晶体的质量也不确定,故错误;C、t2℃时,甲物质的溶解度>乙物质的溶解度,即100g溶剂中甲物质的质量>乙物质的质量,等质量甲和乙的饱和溶液中所含溶剂的质量甲<乙,故错误;D、由于在t1℃时甲、乙两物质的溶解度相同,溶液中溶质的质量分时也相同。
甲、乙的溶解度都温度的升高而增大,所以,将t1℃甲、乙两物质的饱和溶液升温至t2℃,都变成了不饱和溶液,由于溶液中溶质的质量、溶剂的质量都不变,所得甲溶液溶质质量分数=乙溶液溶质质量分数,故正确。
点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
2.如图是甲乙两种物质的溶解度曲线,下列说法正确的是()A.甲的溶解度大于乙的溶解度B.t℃时,甲乙饱和溶液中溶质的质量分数相等C.升高温度能使接近饱和的甲溶液变为饱和溶液D.10℃时,分别用100g水配制甲乙的饱和溶液,所需甲的质量大于乙的质量【答案】B【解析】【分析】【详解】A、由两种物质的溶解度曲线可以看出,当0~t℃时,乙的溶解度大于甲的溶解度,选项A 错误;B、t℃时,二者的溶解度相等,饱和溶液中溶质的质量分数也相等,选项B正确;C、由甲物质的溶解度曲线可以看出,甲物质的溶解度随着温度的升高而增大,所以升高温度不能使接近饱和的甲溶液变为饱和溶液,选项C错误;D、过10℃作一条垂直于横坐标的垂线,看垂线与曲线的交点高低,从图象可以看出,此时乙的溶解度大于甲的溶解度,选项D错误。
中考考点_溶液 溶解度知识点汇总(全)(word)1

中考考点_溶液溶解度知识点汇总(全)(word)1一、溶液选择题1.下图中,图甲为四种物质的溶解度曲线,在图乙中分别向两支试管内滴加一定量的水后,X和Y的饱和溶液均变浑浊,则下列说法错误的是A.10℃时,物质溶解度大小关系为:①>③>②>④B.X为Ce2(SO4)3,Y不一定是NH4H2PO4C.若NH4H2PO4中混有少量的NaCl 杂质,可以降温结晶的方法提纯D.20℃时,将40gNaCl 加入到100g水中,所得溶液中溶质和溶剂的质量比是2∶5【答案】D【解析】【详解】A、由溶解度曲线可知,10℃时,物质溶解度大小关系为:①>③>②>④,故A选项正确,不符合题意;B、氢氧化钠固体中加入水,放热,X溶液变浑浊,说明X的溶解度随温度的升高而降低,故X是Ce2(SO4)3,硝酸铵固体中加入水温度降低,Y饱和溶液变浑浊,故Y可能是NH4H2PO4,故B选项正确,不符合题意;C、NH4H2PO4、NaCl的溶解度都随温度的升高而升高,NH4H2PO4的溶解度随温度的变化较大,NaCl的溶解度随温度的变化较小,故NH4H2PO4中混有少量的NaCl 杂质,可以降温结晶的方法提纯,故C选项正确,不符合题意;D、由图可知,20℃时,氯化钠的溶解度为35g左右,故将40g氯化钠加入100g的水中,氯化钠不能完全溶解,故所得溶液中溶质和溶剂的质量比小于2∶5,故D选项错误,符合题意。
故选D。
2.下列关于溶液的说法错误的是()A.固体、液体、气体都可以做溶质B.NH4NO3溶解过程中吸热,溶液温度降低C.欲使100克KNO3溶液的质量分数由5%变成10%,可向其中加入5克KNO3固体D.25℃时,将某KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a 与b的质量不一定相等【答案】C【解析】试题分析:A 、溶质可以是固体、液体、气体,故A 说法正确;B 、NH 4NO 3溶解过程中吸热,溶液温度降低,故B 说法正确;C 、溶质质量分数:,故C 错;D 、如果硝酸钾溶液蒸发溶剂前,是饱和溶液,蒸发10克水析出a 克晶体,再蒸发10克水析出b 克晶体,a 与b 的质量一定相等,如果硝酸钾溶液蒸发溶剂前,是不饱和溶液,蒸发10克水析出a 克晶体,再蒸发10克水析出b 克晶体,a 与b 的质量一定不相等,故D 说法正确。
2020-2021年复习专题——溶液 溶解度知识点归纳(word)

2020-2021年复习专题——溶液 溶解度知识点归纳(word )一、溶液选择题1.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )A .将等量甲、乙的饱和溶液从t3℃降到t2℃,析出甲的质量大大B .t2℃时,甲和乙的饱和溶液各100 g ,其溶质的质量一定相等C .分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D .t1℃时,丙的饱和溶液中溶质的质量分数为40%【答案】D【解析】A 、将相同质量甲、乙的饱和溶液从t 3℃降到t 2℃,可通过比较甲、乙两物质在t 2℃和t 3℃时溶解度的差的大小作出判断,差值大析出晶体多。
由溶解度曲线可知,t 2℃时两物质的溶解度相等,而t 3℃时甲物质的溶解度大于乙,故析出甲的质量大,正确;B 、据溶解度曲线知,t 2℃时,甲和乙两种溶液的溶解度相同,故t 2℃时,甲和乙的饱和溶液各100g ,其溶质的质量一定相等,正确;C 、甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度的升高而减小,t 3℃时甲、乙、丙的溶解度大小关系是甲>乙>丙,由于饱和溶液中饱和时质量分数的计算式: =?100%+100溶解度溶质的质量分数溶解度,即溶解度越大质量分数也就越大,故t 3℃时甲、乙、丙的溶质质量分数大小关系是甲>乙>丙;降温至t 1℃,甲、乙析出晶体,依然是饱和溶液,此时溶解度大小关系是乙>甲,丙降温后变为不饱和溶液,溶质的质量分数与t 3℃时相等,而t 3℃时丙的溶解度小于t 1℃时甲的溶解度,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙,正确;D 、饱和溶液中=?100%+100溶解度溶质的质量分数溶解度知。
t 1℃时,丙的饱和溶液中40g =?100%40g+100g溶质的质量分数<40%,错误。
故选D 。
2.下表是KCl 与KNO 3在不同温度的溶解度。
下列说法不正确...的是( ) 温度/℃20 30 40 50KCl 34.0g 37.0g 40.0g 42.6gKNO331.6g45.8g63.9g85.5gA.20℃时,KC1的溶解度大于KNO3的溶解度B.两物质溶解度相等的温度在20~30℃之间C.40℃时,5gKCl中加10g水可得33.3%溶液D.50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出【答案】C【解析】试题分析:由两种物质的溶解度可知20℃时,KNO3溶解度小于KC1的溶解度,A正确;由表格数据可知温度在20~30℃时,两物质的溶解度有相同的部分,即两物质溶解度相等的温度在20~30℃之间,B正确;40℃时,KCl的溶解度为40g,即该温度下40g氯化钾溶解在100g水中恰好形成饱和溶液,那么10g水中最多溶解4g氯化钾,形成的溶液的溶质质量分数=4g/14g ×100%=28.6%,C错误;30℃时硝酸钾的溶解度为45.8g,即该温度下45.8g硝酸钾溶解在100g水中恰好形成饱和溶液,那么20g水中最多溶解硝酸钾9.16g,即50℃时,10g KNO3中加20g水,充分溶解,再降温到30℃,有KNO3固体析出,D正确。
溶液 溶解度知识点总结(word)1

溶液 溶解度知识点总结(word )1一、溶液选择题1.甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是A .t 3℃时,甲的饱和溶液溶质与溶液的质量比为1:2B .t 1℃时,甲的溶解度大于乙的溶解度C .t 2℃时,甲、乙溶液的溶质质量分数都为30%D .t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量【答案】D【解析】A 、t 3℃时,甲物质的溶解度是50g ,所以甲的饱和溶液溶质与溶液的质量比为1:3,故A 错误;B 、通过分析溶解度曲线可知,t 1℃时,甲的溶解度小于乙的溶解度,故B 错误;C 、t 2℃时,甲、乙物质的溶解度是30g ,所以甲、乙饱和溶液的溶质质量分数都为30130g g×100%=23.1%,故C 错误; D 、t 3℃时,甲物质的溶解度大于乙物质的溶解度,所以t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量,故D 正确。
点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
2.20℃时,往100g 硝酸钾溶液中加入20g 硝酸钾,充分搅拌,硝酸钾部分溶解。
下列说法正确的是A .硝酸钾的溶解度变大B .溶质的质量分数保持不变C .所得溶液是饱和溶液D .所的溶液的质量为120g【答案】C【解析】【分析】【详解】A 、硝酸钾的溶解度只受温度一个外界因素的影响,温度不变,溶解度不变,故A 不正确;B、硝酸钾部分溶解,溶质的质量分数变大,故B不正确;C、硝酸钾部分溶解,则溶液为饱和溶液,故C正确;D、20g的硝酸钾部分溶解,溶液的质量小于120g,故D不正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A.将 ℃时 b 的饱和溶液加水可变为不饱和溶液 B.将 ℃时 a 的饱和溶液降温至 ℃,溶液质量不变 C. ℃时,两种物质的饱和溶液中溶质质量分数 a b D.将 ℃时 a、b 的饱和溶液分别降温至 ℃,两溶液的溶质质量分数相等 【答案】B 【解析】 试题分析:A、任何物质的饱和溶液加水都可变为不饱和溶液,故将 t1℃时 b 的饱和溶液加 水可变为不饱和溶液,正确,B、根据溶解度曲线,物质 a 的溶解度随温度的升高而增大, 故将 t2℃时 a 的饱和溶液降温至 t1℃,有晶体析出,故溶液质量变小,错误,C、根据溶解 度曲线,t2℃时,物质 a 的溶解度比物质 b 的溶解度要更大,故两种物质的饱和溶液中溶 质质量分数 a>b,正确,D,根据溶解度曲线,t1℃时, a、b 种物质的溶解度大小关系是: a=b,将 t2℃时 a、b 的饱和溶液分别降温至 t1℃,两溶液的溶质质量分数相等,正确,故 选B 考点:溶解度曲线的意义
【答案】C 【解析】A、根据溶解度的变化来判断是否饱和; B、根据溶解度曲线中溶解度与温度的关系考虑; C、根据降温后溶质的变化考虑; D、根据饱和溶液溶质质量分数的计算考虑。 解:A、将 100 克甲、乙饱和溶液从 t2℃降到 t1℃,甲物质溶解度减小析出晶体,还是饱和 溶液,但乙物质溶解度变大,变为不饱和溶液,故 A 错; B、因为从 t2℃降到 t1℃时,甲和乙两物质溶解度相等,故 B 错; C、将 100 克甲、乙饱和溶液从 t2℃降到 t1℃时,由于甲物质析出晶体,所以溶液质量减 少。乙物质降温后变为不饱和,溶液质量不变,还是 100g,所以甲<乙,故 C 正确;
溶液 溶解度专题复习(word)
一、溶液选择题
1.K2CO3 和 KNO3 在不同温度时的溶解度及其溶解度曲线如下。下列说法错误的是
A.t℃在 60℃到 80℃之间 B.t℃时,两种溶液的溶质质量分数不一定相等 C.两种饱和液从 80℃降温到 20℃,析出晶体的质量(不含结晶水)无法比较 D.把 60℃时的 105g KNO3 饱和液降温至 20℃,能析出晶体 73.4g 【答案】D 【解析】 【分析】 【详解】 A、t℃时 K2CO3 和 KNO3 的溶解度相同,由表格中的数据可知,在 60℃到 80℃之间溶解度 都包括 126-139 间的数值,所以 t℃在 60℃到 80℃之间,故A 正确; B、t℃时,两种物质只有是饱和溶液时,溶质质量分数一定相等,则溶质质量分数不一定 相等,故 B 正确; C、等质量的两种饱和液从 80℃降温到 20℃,析出晶体(不含结晶水)的质量硝酸钾比碳酸 钾多,如质量不等,则无法比较,故C 正确; D、把 60℃时硝酸钾的溶解度为 110g,则 105g KNO3 饱和液中溶剂是 50g,溶质是 55g, 20℃,硝酸钾的溶解度为 31.6g,50g 水中最多能溶 15.8g,所以降温后能析出晶体 39.2g,故 D 不正确。故选 D。
态,再根据一定温度下饱和溶液的溶质分数= s 100% ,判定溶液溶质质量分数的 100g+s
大小。
5.如图是甲、乙两种固体物质的溶解度曲线。若分别将 100g 甲、乙饱和溶液的温度从 t2℃降至 t1℃,对所得溶液的叙述正确的是( )
A.两溶液都仍为饱和溶液 B.两物质的溶解度:甲>乙 C.两溶液的质量:甲﹤乙 D.两溶液溶质的质量分数:甲﹤乙
故选 C。
点睛:本题容易出错的地方是降温后溶质质量分数的比较,要利用好饱和溶液溶质质量分
数的计算公式。
6.实验室有碳酸钾和碳酸钙的固体混合物 75g,使之与 500g 质量分数为 14.6%的盐酸充分 反应,将反应后的溶液蒸干得到 82.7g 固体。则原混合物中金属元素的质量分数为 A.44% B.50% C.55% D.68% 【答案】A 【解析】碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为 CaCO3+2HCl═CaCl2+H2O+CO2↑ 、 K2CO3+2HCl═2KCl+H2O+CO2↑ , 由 上 述 化 学 方 程 式 可 知 , 碳 酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相 对原子质量的和是 71,碳酸根的相对原子质量的和是 60,差是 11,即完全反应后质量增 加了 11 份质量.实际反应后固体质量增加了 82.7g-75g=7.7g,设原混合物中含碳酸根的 质量为 x,则 60:11=x:7.7g,x=42g;则所含金属元素质量为 75g-42g=33g,原混合物中
7.NaCl、KNO3 两种固体物质的溶解度曲线如图所示。下列说法正确的是
A.20℃时,NaCl 的溶解度为 31.6 g B.将 10℃时两物质饱和溶液升温至 30℃,溶液中溶质的质量分数都增大 C.为了除去 NaCl 固体中混有的少量 KNO3,可加热将其完全溶解后,再通过降温结晶、过 滤来除之 D.50℃时,将 50g KNO3 加入 50g 水中,充分溶解后溶液的质量为 92.75g 【答案】D 【解析】A. 在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。20℃时,NaCl 的溶解度 为 31.6 g; B. 将 10℃时两物质饱和溶液升温至 30℃,;两种物质的溶解度变大,溶质的质量不变, 溶液中溶质的质量分数都不变;C. 为了除去 NaCl 固体中混有的少量 KNO3,可加热将其完 全溶解后,再通过降温结晶、过滤来除之;因为硝酸钾的溶解度随温度的降低而迅速减 小,而氯化钠的溶解受温度的影响很小,所以降温析出晶体几乎全是硝酸钾。过滤得硝酸 钾固体。D. 50℃时,将 50g KNO3 加入 50g 水中,溶解硝酸钾 42.75g,充分溶解后溶液的 质量为 92.75g;选 D
30g ×100%=23.1%,故 C 错误; 130g
D、t3℃时,甲物质的溶解度大于乙物质的溶解度,所以 t2℃时,质量相同的甲、乙饱和溶 液分别升温至 t3℃,为达饱和状态,需加入甲的质量大于乙的质量,故 D 正确。 点睛: 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解 性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的 大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶 的方法达到提纯物质的目的。
有晶体析出,质量分数不变,一定温度下饱和溶液的溶质分数= s 100% ,溶解度 100g+s
越大,质量分数越大,t1℃时乙的溶解度大于甲的溶解度大于 t3℃时丙的溶解度,所以 t1℃ 时三种物质的溶质质量分数由大到小的顺序是乙>甲>丙,故 B 正确; C、t2℃时,甲、丙溶液的状态没有确定,溶液中溶质的质量分数也不能确定,故 C 错误; D、t3℃时,将甲、乙两物质的饱和溶液降温到 t2℃,饱和溶液的质量没有确定,析出晶体 质量也不能确定,故 D 错误。故选 B。 【点睛】 在分析饱和溶液温度改变后溶质质量分数的变化时,首先根据溶解度曲线判定溶液的状
到饱和状态,饱和溶液的质量分数= 30g 100% 23.1% ,不能得到 30%的甲溶 30g+100g
液,故 A 错误; B、将 t3℃时 A、B、C 三种物质的饱和溶液降温到 t1℃时,甲、乙的溶解度减小,丙的溶 解度随温度的降低而增大,甲、乙有晶体析出,质量分数变小,溶液仍为饱和溶液,丙没
D、饱和溶液的质量分数:
×100%,甲物质降温后析出晶体,仍然饱和,质量分
数用 t1℃时溶解度计算即可;乙物质降温后变为不饱和,所以溶质质量分数不变,所以乙
物质的质量分数按照 t2℃时乙物质的溶解度计算,所以只要比较出 t1℃时甲物质溶解度与
t2℃时乙物质的溶解度的大小即可,通过图象可知甲>乙,故 D 错。
2.下表是 KCl 与 KNO3 在不同温度的溶解度。下列说法不.正.确.的是( )
温
度 20
30
40
50
/℃
KCl 34.0g 37.8g 63.9g 85.5g
A.20℃时,KC1 的溶解度大于 KNO3 的溶解度 B.两物质溶解度相等的温度在 20~30℃之间 C.40℃时,5gKCl 中加 10g 水可得 33.3%溶液 D.50℃时,10g KNO3 中加 20g 水,充分溶解后再降温到 30℃,有 KNO3 固体析出 【答案】C 【解析】 试题分析:由两种物质的溶解度可知 20℃时,KNO3 溶解度小于 KC1 的溶解度,A 正确;由 表格数据可知温度在 20~30℃时,两物质的溶解度有相同的部分,即两物质溶解度相等的 温度在 20~30℃之间,B 正确;40℃时,KCl 的溶解度为 40g,即该温度下 40g 氯化钾溶解 在 100g 水中恰好形成饱和溶液,那么 10g 水中最多溶解 4g 氯化钾,形成的溶液的溶质质 量分数=4g/14g ×100%=28.6%,C 错误;30℃时硝酸钾的溶解度为 45.8g,即该温度下 45.8g 硝酸钾溶解在 100g 水中恰好形成饱和溶液,那么 20g 水中最多溶解硝酸钾 9.16g,即 50℃时,10g KNO3 中加 20g 水,充分溶解,再降温到 30℃,有 KNO3 固体析出,D 正确。 故选 C。 考点:溶解度
3.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( ) ①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数; ③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。 A.①② B.①③ C.②④ D.③④ 【答案】A 【解析】①称量的氯化钠固体中含有不溶性杂质,导致氯化钠质量偏小,从而导致配制的 氯化钠溶液溶质质量分数偏小,正确;②用量筒量取水时仰视读数,导致读数偏小,而量 筒中水的体积偏大,最终导致配制的氯化钠溶液溶质质量分数偏小,正确;③往烧杯中加 水时有水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,错误;④溶液 具有均一性,将配制好的溶液往试剂瓶中转移时有少量溅出,溶质质量分数不变,错误。 故选 A。
