吉尔多肽杯2016年江苏省“化学与中学生全面发展”化学活动周高中化学竞赛试赛
2020年全国高中学生化学竞赛(江苏省赛区)预赛试题及参考答案

“仪征化纤白斯特杯”xx年全国高中学生化学竞赛(江苏省赛区)预赛试题相对原子质量: H:1.01 C:12.01 N:14.01 O:16.00 F:19.00 Na:22.99 P:30.97 S:32.06 C1:35.45 K:39.10 Ti:47.87 V:50.94 Cr:52.00 Mn:54.94 Fe:56.00 Cu:63.55 Zn:65.39 Br:79.90 Ag:107.9 I:126.9Ba:137.31.本试卷共26题,用2小时完成,全卷共150分; 2.可使用计算器。
一、选择题(每小题有1-2个选项符合题意;每题4分,共15题,共60分)1.两位美国科学家彼得·阿格雷和罗德里克·麦金农,因为发现细胞膜水通道,以及对离子通道结构和机理研究作出的开创性贡献而获得xx年诺贝尔化学奖。
他们之所以获得诺贝尔化学奖而不是生理学或医学奖是因为( )A.他们的研究和化学物质水有关B.他们的研究有利于研制针对一些神经系统疾病和心血管疾病的药物C.他们的研究深入到分子、原子的层次D.他们的研究深入到细胞的层次2.下列物质中,可溶于水的是( )A.胆固醇: B.芬必得:C.保幼激素JH-I: D.维生素C:3.xx年2月1日,美国哥伦比亚号航天飞机在返回地面的途中坠毁,举世震惊。
该航天飞机用铝粉和高氯酸铵(NH4C1O4)的混合物为固体燃料,点燃时铝粉氧化放热,引发高氯酸铵反应,产生N2、Cl2、O2和H20并放出大量的热。
下列对此反应的叙述中正确的是( )A.上述反应瞬间产生大量的高温气体推动飞机飞行B.在反应中高氯酸铵只起氧化剂作用C.其方程式可表示为2 NH4C1O4=N2↑+4H20+C12↑ +O2↑D.上述反应中反应物的总能量大于生成物的总能量4.《Inorganic Syntheses》(无机合成)一书中,有一如下图所示的装置,用以制备某种干燥的纯净气体。
第27届“扬子石化杯”江苏省高中生化学竞赛初赛试卷-医药卫生

第27届“扬子石化杯”江苏省高中生化学竞赛初赛试卷-医药卫生第27届“扬子石化杯”江苏省高中生化学竞赛初赛试卷(精致word版)第27届“扬子石化杯”江苏省高中生化学竞赛初赛试卷第Ⅰ卷选择题(共40分)1. 化学与科学、技术、社会和环境密切相关。
下列有关说法中错误的是A.太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置B.加热能杀死H7N9型禽流感病毒是因为病毒的蛋白质受热变性C.为减少污染,可以将煤气化或液化,获得清洁燃料D. PM2.5对人体有害的主要原因是它含有铅、镉、铬、钒、砷等金属元素2. 下列化学用语正确的是A.铯-137:137CsB.硫化氢的电子式:C. Cl- 离子的结构示意图:D.乙酸的实验式:CH2O3. 常温下,下列各组离子在指定溶液中可能大量共存的是A.0.l molL-1的NaAlO2溶液:K+、Na+、SO42-、CO32-B.使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-C.含有大量ClO- 溶液中:K+、OH-、I-、SO32-D.c(Al3+)=0.1 molL-1的溶液中:Na+、Cl-、AlO2-、SO42-4. 下列说法或表示法正确的是A.反应2Mg(s)+CO2(g)==C(s)+2MgO(s)能自发进行,则该反应的H 0B.铅蓄电池放电时的负极和充电时的阳极均发生还原反应C.在稀溶液中:H+(aq)+OH-(aq)==H2O(l) △H= -57.3kJ mol-1,若将含0.5molH2SO 4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJD.在101kpa时,2gH2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热学方程式表示为2H2(g)+O2(g)==2H2O(l) △H= -285.8kJ mol-15. 下列说法正确的是A. 碳酸钠可作为治疗胃溃疡病人的胃酸过多症的药物B. 为了提高铜粉与硝酸的反应速率,可向烧瓶中加入少量石墨或硝酸银浓溶液C. 向柠檬醛中加入高锰酸钾性溶液,溶液褪色,说明柠檬醛分子中含有醛基D. 名称为:1,3―二甲基―2―丁烯6. 下列有关实验装置的说法中正确的是A.用图1装置制取干燥纯净的NH3B.用图2装置实验室制取大量CO2气体第27届“扬子石化杯”江苏省高中生化学竞赛初赛试卷(精致word版)7. 下列物质的转变在给定条件下不能实现的是8. 设NA为阿伏加德罗常数的值,下列说法正确的是A. 1mol乙酸和1mol乙醇充分反应生成的水分子数为NAB. 常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NAC. 标准状况下,2.24L的CCl4中含有的C―Cl键数为0.4NAD. 6.8g液态KHSO4中含有0.1NA个阳离子9. 下列离子方程式与所述事实相符且正确的是+3+A. Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H==Fe+3H2O2 B. Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2 2HCO3 2OH CaCO3 CO3 H2OC. 明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多:Al3 2SO42 2Ba2 4OH AlO2 2BaSO4 2H2OD. 硫酸亚铁溶液中加入酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O10.下列说法正确的是A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液B.电解精炼铜的过程中,粗铜与电源的负极相连,作电解池的阴极C.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠D.常温下,向纯水中加入Na或NaOH(s)都能使水的电离平衡逆向移动,Kw不变二、不定项选择题11. 胡妥油(D)用作香料的原料,它可由A合成得到:下列说法不正确的是A.若有机物A是由异戊二烯(C5H8)和另一种有机物加成所得,则该有机物为丙烯酸B.有机物B能跟Na反应放出H2,但不能跟NaHCO3溶液反应放出CO2气体C.有机物C可以发生加成、氧化、水解、加聚等类型的化学反应,具有光学活性D.核磁共振氢谱显示有机物D分子中有5种化学环境不同的氢原子12. 六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期。
第25届全国高中生化学竞赛(江苏赛区)选拔赛暨夏令营试题
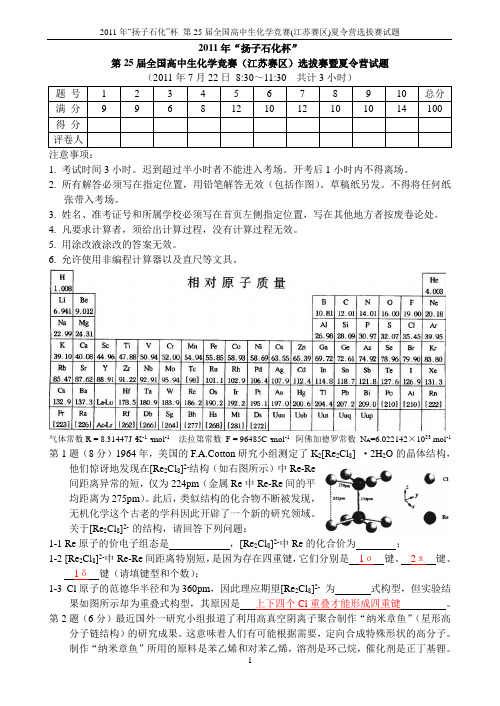
2011年“扬子石化杯”第25届全国高中生化学竞赛(江苏赛区)选拔赛暨夏令营试题注意事项:1. 考试时间3小时。
迟到超过半小时者不能进入考场。
开考后1小时内不得离场。
2. 所有解答必须写在指定位置,用铅笔解答无效(包括作图)。
草稿纸另发。
不得将任何纸张带入考场。
3. 姓名、准考证号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
4. 凡要求计算者,须给出计算过程,没有计算过程无效。
5. 用涂改液涂改的答案无效。
6. 允许使用非编程计算器以及直尺等文具。
气体常数R = 8.31447J·K-1·mol-1法拉第常数F = 96485C·mol-1 阿佛加德罗常数N A=6.022142×1023 mol-1第1题(8分)1964年,美国的F.A.Cotton研究小组测定了K2[Re2Cl8] ·2H2O的晶体结构,Cl8]2-结构(如右图所示)中Re-Re他们惊讶地发现在[Re间距离异常的短,仅为224pm(金属Re中Re-Re间的平均距离为275pm)。
此后,类似结构的化合物不断被发现,无机化学这个古老的学科因此开辟了一个新的研究领域。
关于[Re2Cl8]2- 的结构,请回答下列问题:1-1 Re原子的价电子组态是,[Re2Cl8]2-中Re的化合价为;1-2 [Re2Cl8]2-中Re-Re间距离特别短,是因为存在四重键,它们分别是1σ键、2π键、1δ键(请填键型和个数);1-3 Cl原子的范德华半径和为360pm,因此理应期望[Re2Cl8]2-为式构型,但实验结果如图所示却为重叠式构型,其原因是上下四个Cl重叠才能形成四重键。
第2题(6分)最近国外一研究小组报道了利用高真空阴离子聚合制作“纳米章鱼”(星形高分子链结构)的研究成果。
这意味着人们有可能根据需要,定向合成特殊形状的高分子。
制作“纳米章鱼”所用的原料是苯乙烯和对苯乙烯,溶剂是环己烷,催化剂是正丁基锂。
历年高中化学奥赛竞赛试题及答案

中国化学会第21届全国高中学生化学竞赛(省级赛区)试题(2007年9月16日 9:00 - 12:00共3小时)题号 1 2 3 4 5 6 7 8 9 10 11 总分满分 12 6 10 7 10 12 8 4 10 12 9100 得分 评卷人● 竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
● 试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
● 姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
●允许使用非编程计算器以及直尺等文具。
第1题(12分)通常,硅不与水反应,然而,弱碱性水溶液能使一定量的硅溶解,生成Si(OH)4。
1-1 已知反应分两步进行,试用化学方程式表示上述溶解过程。
早在上世纪50年代就发现了CH 5+的存在,人们曾提出该离子结构的多种假设,然而,直至1999年,才在低温下获得该离子的振动-转动光谱,并由此提出该离子的如下结构模型:氢原子围绕着碳原子快速转动;所有C-H键的键长相等。
1-2 该离子的结构能否用经典的共价键理论说明?简述理由。
1-3 该离子是( )。
A.质子酸B.路易斯酸C.自由基D.亲核试剂2003年5月报道,在石油中发现了一种新的烷烃分子,因其结构类似于金刚石,被称为“分子钻石”,若能合成,有可能用做合成纳米材料的理想模板。
该分子的结构简图如下:1-4 该分子的分子式为 ;1-5 该分子有无对称中心?1-6 该分子有几种不同级的碳原子? 1-7 该分子有无手性碳原子? 1-8 该分子有无手性?第2题(5分)羟胺和用同位素标记氮原子(N ﹡)的亚硝酸在不同介质中发生反应,方程式如下:NH 2OH+HN ﹡O 2→ A +H 2ONH 2OH+HN ﹡O 2→ B +H 2OA 、B 脱水都能形成N 2O ,由A 得到N ﹡NO 和NN ﹡O ,而由B 只得到NN ﹡O 。
高二化学竞赛检测试题(附答案)

以下是为⼤家整理的关于《⾼⼆化学竞赛检测试题(附答案)》,供⼤家学习参考!•竞赛时间2⼩时。
迟到超过30分钟者不得进场。
开赛后1⼩时内不得离场。
时间到,把试卷纸(背⾯向上)放在桌⾯上,⽴即离场。
•竞赛答案全部写在试卷指定位置上,使⽤⿊⾊或蓝⾊圆珠笔、签字笔、钢笔答题,使⽤红⾊笔或铅笔答题者,试卷作废⽆效。
•姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
•允许使⽤⾮编程计算器及直尺等⽂具。
•试卷按密封线封装。
题中可能⽤到的相对原⼦质量为:H C N O Ni Fe1.008 12.01 14.01 16.00 58.70 55.85第1题选择题(9分)(单选或多选,每选1.5分)(1)化学在⽣产和⽣活中有着⼴泛的应⽤。
下列说法错误的是 ( )A.⽤聚⼄烯塑料作⾷品包装袋B.SiO2是制备光纤导线的主要材料C.⽤浸泡过⾼锰酸钾溶液的硅藻⼟吸收⽔果产⽣的⼄烯以延长货架期D.民间⽤明矾作净⽔剂除去⽔中的悬浮物(2)下列离⼦⽅程式正确的是 ( )A.向NH4HSO4溶液中滴加少量的Ba(OH)2溶液Ba2++2OH-+NH4++H+== BaSO4↓+NH3•H2O+H2OB.向漂⽩粉溶液中通⼊过量的SO2⽓体ClO-+SO2+H2O== HSO3-+HClOC.向偏铝酸钠溶液中通⼊CO2⽓体AlO2-+CO2+2H2O== Al(OH)3↓+HCO3-D.海⽔中的Fe2+在铁细菌的催化下被氧化成Fe2O34Fe2++8OH-+CO2==2Fe2O3+HCHO+3H2O(3)已知:N2(g)+3H2(g) 2NH3(g) △H = -92.4 kJ•mol-1,在温度、容积相同的3个密闭容器中,按不同⽅式投⼊反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:容器实验1 实验2 实验3反应物投⼊量始态 1mol N2、3mol H2 2mol NH3 4mol NH3NH3的平衡浓度/mol•L-1 cl c2 c3反应的能量变化放出a kJ 吸收b kJ 吸收c kJ体系压强( Pa) p1 p 2 p 3反应物转化率α1 α2 α3下列说法正确的是()A.2 cl > c3B.a + b = 92.4C.2 p2 < p3D.(α1 + α3) < 1(4)下列溶液中微粒的物质的量浓度关系正确的是 ( )A.室温下,向0.01 mol•L-1 NH4HSO4溶液中滴加NaOH溶液⾄中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)B.25℃时,pH =4.75、浓度均为0.1 mol•L-1的CH3COOH、CH3COONa的混合液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)C.25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c(CHCOO-)+c(H+)<c(Na+)+c(OH-)D.0.1 mol/L Na2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:3 (CO32-)+3 (HCO3-)+3 (H2CO3)=2 (Na+)(5)现有3.5t质量分数为70%的硫酸和2.5t含杂质20%的烧碱(杂质不参加反应),⾜量的铝屑。
2016年“扬子石化杯”第30届中国化学奥林匹克竞赛(江苏赛区)夏令营暨选拔赛试题及参考答案
2016年“扬子石化杯”第30届中国化学奥林匹克竞赛(江苏赛区)夏令营暨选拔赛试题参考答案及评分标准说明化学方程式配平错误扣一半分第1题(12分)1-1 氧气Ca(HCO3)2 非极性(每空2分,共6分) A B (每个1分,共2分)1-2 3s23p4sp2(每空1分,共2分) 6(2分)4第2题(12分)2-1 Na2S + I2 === 2NaI + S (1分)2Na2S2O3 + I2 === 2NaI + Na2S4O6(1分)ZnCO3 + Na2S ===ZnS↓+ Na2CO3 (2分)71.48% 28.00% (每空2分,共4分)2-2 pH=p K a – lg([H2CO3])/([HCO3-]) 或pH = 6.35- lg([H2CO3])/([HCO3-]) (2分) 0.100 (2分)第3题(9分)3-1NCl3 + 3H2O === NH3 + 3HClO (2分)PCl3 + 3H2O === H3PO3+ HCl (2分)3-2 弱弱强(每空1分,共3分)3-3 2Mn2+ + 5NaBiO3 + 14H+ === 2MnO4- +5Na+ + 5Bi+ + 7H2O (2分)第4题(10分)4-1 白Fe(OH)2(每空2分,共4分)4-2 [Ni(en)2(NO2)2] 八面体型(每空2分,共4分) N、O (2分,写出一个得1分) 第5题(10分)5-1 1s22s22p63s23p63d104s24p64d105s25p3+5 +3 -3 (每空1分,共4分)5-2 2Sb2S3 + 9O2 === 2Sb2O3 + 6SO2(2分)5-3 [H3O2]+[SbF6]-(2分)2[H3O2]+[SbF6]- === 2[H3O]+[SbF6]- + O2 (2分)第6题(5分)6-1H2、Cu、Zn (2分)6-2Cu (1分)6-3 6.05×10-39mol·L-1(2分)第7题(12分)7-1(2分)面心正交晶胞1个I2分子(每空1分,共2分)注;晶胞中画出的I2分子必须同时具备以下两个条件才可得分A)处于面心位置B)与相互平行的晶面面心的I2分子平行。
第23届全国高中学生化学竞赛(江苏)夏令营选拔赛试题和答案

第23届全国高中学生化学竞赛(江苏)夏令营选拔赛试题和答案第23届全国高中学生化学竞赛(江苏赛区)夏令营暨选拔赛试题(2009年7月22日8:30—11:30 共计3小时) ● 竞赛时间3小时。
迟到超过30分钟者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
● 所有解答必须写在指定位置,不得用铅笔填写。
● 姓名、准考证号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论。
● 允许使用非编程计算器以及直尺等文具。
第1题(6分)1-1 在化工、冶金、电子、电镀等生产部门排放废水中,常常含有一些汞金属元素,汞元素能在生物体内积累,不易排出体外,具有很大的危害。
处理含Hg2+废水可加入Na2S或通入H2S,使Hg2+形成HgS沉淀。
但如果Na2S过量则达不到去除Hg2+的目的,为什么?_________________________________________ __________。
解决这一问题的方法是再向该废水中加入FeSO4,可有效地使HgS沉降,为什么?_________________________________________江苏化学网 _____________________________________。
1-2 铊属于放射性的高危重金属。
铊和铊的氧化物都有毒,能使人的中枢神经系统、肠胃系统及肾脏等部位发生病变。
人如果饮用了被铊污染的水或吸入了含铊化合物的粉尘,就会引起铊中毒。
常用普鲁士蓝作为解毒剂,治疗量为每日250 mg/kg。
请说明用普鲁士蓝作为解毒剂的化学原理,并写出相应的化学方程式。
_________________________________________ _____________________________________________________________________________ _____________________________________________________________________________ _____________________________________1-3 在研究酸雨造成的某地土壤的酸化问题时,需pH = 10.00 的碳酸盐缓冲溶液,在500ml 0.20 mol/L 的NaHCO3溶液中需加入___________g的碳酸钠来配制1 L 的缓冲溶液。
2016年化学竞赛试题参考答案及评分标准
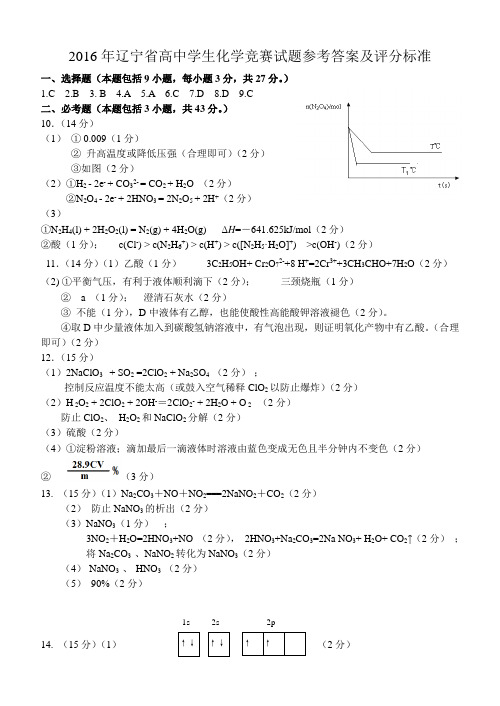
2016年辽宁省高中学生化学竞赛试题参考答案及评分标准一、选择题(本题包括9小题,每小题3分,共27分。
)1.C2.B3. B4.A5.A6.C7.D8.D9.C二、必考题(本题包括3小题,共43分。
)10.(14分)(1) ① 0.009(1分)② 升高温度或降低压强(合理即可)(2分)③如图(2分)(2)①H 2 - 2e - + CO 32- = CO 2 + H 2O (2分)②N 2O 4 - 2e - + 2HNO 3 = 2N 2O 5 + 2H +(2分)(3)①N 2H 4(l) + 2H 2O 2(l) = N 2(g) + 4H 2O(g) ΔH =-641.625kJ/mol (2分)②酸(1分); c(Cl -) > c(N 2H 6+) > c(H +) > c([N 2H 5·H 2O]+) >c(OH -)(2分)11.(14分)(1)乙酸(1分) 3C 2H 5OH+ Cr 2O 72-+8 H +=2Cr 3++3CH 3CHO+7H 2O (2分)(2) ①平衡气压,有利于液体顺利滴下(2分); 三颈烧瓶(1分)② a (1分); 澄清石灰水(2分)③ 不能(1分),D 中液体有乙醇,也能使酸性高能酸钾溶液褪色(2分)。
④取D 中少量液体加入到碳酸氢钠溶液中,有气泡出现,则证明氧化产物中有乙酸。
(合理即可)(2分)12.(15分)(1)2NaClO 3 + SO 2 =2ClO 2 + Na 2SO 4 (2分) ;控制反应温度不能太高(或鼓入空气稀释ClO 2以防止爆炸)(2分)(2)H 2O 2 + 2ClO 2 + 2OH -=2ClO 2- + 2H 2O + O 2 (2分)防止ClO 2、 H 2O 2和NaClO 2分解(2分)(3)硫酸(2分)(4)①淀粉溶液;滴加最后一滴液体时溶液由蓝色变成无色且半分钟内不变色(2分) ② (3分)13. (15分)(1)Na 2CO 3+NO +NO 2===2NaNO 2+CO 2(2分)(2) 防止NaNO 3的析出(2分)(3)NaNO 3(1分) ;3NO 2+H 2O=2HNO 3+NO (2分), 2HNO 3+Na 2CO 3=2Na NO 3+ H 2O+ CO 2↑(2分) ;将Na 2CO 3 、NaNO 2转化为NaNO 3(2分)(4) NaNO 3 、 HNO 3 (2分)(5) 90%(2分)14. (15分)(1) (2分) 1s ↑↓2s ↑↓ 2p ↑ ↑(2)平面三角形(1分);(3) Cl ClCl Cl Cl ClAlAl (2分) ; sp 3(2分) (4)4(1分) ;金刚石(1分);碳碳键键长比碳硅键键长短,碳碳键键能比碳硅键键能大。
“扬子石化杯”第26届全国高中生化学竞赛(江苏赛区)初赛试题及参考答案和评分标准(5.13刚考,纯WORD)

“扬子石化杯”第26届全国高中生化学竞赛(江苏赛区)初赛试题可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Al:27 S:32Cl:35.5 Cr:50 Mn:55 Fe:561.本试卷共22题,用2小时完成,共120分;2.可以使用计算器;3.用铅笔作答无效;4.不可以使用涂改液或修正带。
一、选择题(每小题有1~2个选项符合题意,每小题4分,共60分。
请将答案填写在下1.化学知识在环境保护中起关键作用。
下列叙述不正确的是A.在燃煤中加入适量的生石灰能有效减少二氧化硫的排放B.控制含磷洗涤剂的生产和使用有利于防止水体富营养化C.采用汽车尾气处理技术可将汽车尾气中的NO和CO转化为无害气体D.正常雨水呈中性,pH小于7的雨水是酸雨2.下列化学用语正确的是A.CO2的电子式是:B.硝基苯的结构简式:C.中子数为8的氮原子:D.模型可表示甲烷分子或四氯化碳分子3.下列实验操作或装置正确的是A.加热液体B.制取并收集NH3C.转移溶液D.干燥H24.你认为下列数据可信的是A.某胶体粒子的直径是160nm B.某常见气体的密度为1.8g·cm-3C.某反应的平衡常数是1 D.某元素的原子半径是0.160nm5.下列推断不合理的是A.乙烯能使酸性KMnO4溶液褪色,则丙烯也能使酸性KMnO4溶液褪色B.铁、铝在浓H2SO4中钝化,则镁在浓H2SO4中也钝化C.金属钠着火不能用CO2扑灭,则金属钾着火也不能用CO2扑灭D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色6.设N A为阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,22.4LH2中含中子数为2N AB.常温常压下,氧气和臭氧的混合物16g中约含有N A个氧原子C.电解食盐水若产生2 g氢气,则转移的电子数目为2N AD.100mL 0.1mol·L-1的FeCl3溶液中含有Fe3+的个数为0.01N A7.X、Y、Z、M、W为五种短周期元素。
