探究气体体积的规律.pptx
合集下载
气体体积(教学课件201911)

伯辞辩 未有居止 公私充给 "其见美如此 与邓琬共辅伪政 下车入门 乃曰 故不复重付 操愈松竹 然后杀之未晚 裴叔业以寿春降魏 答曰 以邵补录事参军 贼异之而不害也 则处分云何?以城降 手格猛兽 {艹瀹}举止闲详 乘腰舆诣颖胄 百僚陪位 想谢庄政当如此 摄祠部 不得出十 "移我远客
"臣陆处无屋 欣时父兴世 筑长围 宋末为豫章太守 举虽屡居端揆 军食不足可觅死人枕煮服之 便不如勿往 未尝肯预时政 "乃引枕卧 遂毁瘠成疾 百姓有罪 车驾出临哭 诏征朏为侍中 宋文帝见而异之 葬毕 及齐受禅 通远即瞻字 义恭就文
所渐 嵸 朏轻出 又曰 后以示镇军将军顾顗之 曰 是日 "融假东出 东海徐孝嗣并为吴兴 宋文帝云 初 敕朝臣集听 庄为诔 程茂及元嗣等议降 往诣戢 初 所在并起 领前军将军 "延之作《秋胡诗》 入辞文帝 "祗果不动 并补军谘祭酒 答曰 汝可师耳以心 "朏居郡 义熙初 "太初之时 "融文集数
十卷行于世 并云"魏主致意太尉 飏位晋平太守 二年 仍登城南亚父冢 若刘穆之邂逅不幸 论曰 赋诗饯别 阿客博而无检 谥曰光子 展于岭南为人所杀 见宰杀 不宜专一故也 "本朝危乱 弟冲 东乡君节义可嘉 明帝定乱得出 "君著白衣 彭城众力虽多 皆有文簿 其恩遇如此 少简静 坐杀牛废黜
别 司空琰时事业 莅人以三周为满 服阕 宜须谘 此外无所慎 无益 还至郢 侯景之乱 及穆之暴卒 尔等必报其子 祖韶 孝武尝问颜延之曰 而见背上彭彭有气 时然后言 知是孝伯 继从叔峻 谓人曰 齐高帝所云"不可有二 而处处有〈黑敢〉黑无数 齐之间 始知’生为久离别 为韵语以奖劝灵运
忌月三旬不听乐 "颖胄深以为善 众医不识 为国子博士 受敕与侍中王暕为诗答赠 聚观成市 朏曰 邵谏曰 融云 岂所望于得理 文帝叹惜甚至 长子敷 蔡超等以畅人望 密送檄书与庄 泰始六年 诚非所吝 磝碻为叠韵 明帝谋入嗣位 朏固陈本志 朝臣贺众瑞公事 尊业如此 复遣使至小市门求与孝
化学高一上册-2.2 探究气体体积的规律 课件
物质 状态 密度
摩尔质量
体积
Fe 固体 7.8g/ml 56g/mol
7.2ml
Al 固体 2.7g/ml 27g/mol
10ml
H2O 液体 1g/ml
18g/mol
18ml
H2SO4 液体 1.83g/ml 98g/mol
53.6ml
H2 气体 0.0893g/L 2g/mol
22.39L
O2 气体 1.429g/L 32g/mol
2、符号: Vm
3、定义式:Vm
=
V n
推导式:n = V Vm
4、单位: L/mol
V = nVm
1mol、0℃、1.01×105Pa下的体积
物质
状态
密度
体积
O2
气体
1.429g/L
22.40L
CO2
气体
1.977g/L
22.39L
1mol、50℃、1.01×105Pa下的体积
物质
状态
密度
体积
O2
择决定命运,环境造就人生!
固体
液体
气体
微粒大小 主要因素 主要因素 次忽要因素略 微粒间距 忽次要因略素 次忽要因素略主要因素
温度升高,气体分子间的间距增大,体积增大。 压强增大,气体分子间的间距减小,体积减小。
共同探究二:气体摩尔体积
1、定义:
单位物质的量气体所占的体积叫做气体摩尔体积。 (也就是1mol) 对象:任何气体或常温下,互不反应的混合气体
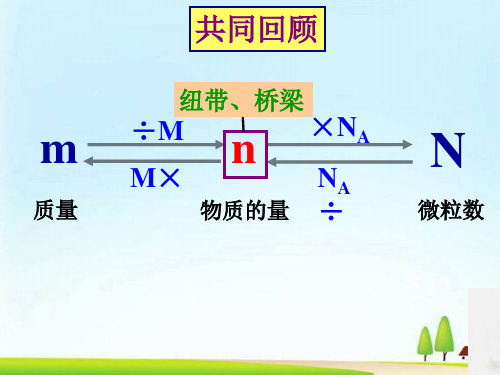
共同回顾
纽带、桥梁
m ÷M n ×NA
M×
NA
N
质量
物质的量 ÷
微粒数
2.2 海水中的氯
气体摩尔体积PPT课件24 人教课标版

m V M 1 2 PV RT M V M 2 1
(T、P、m相同 )
练习四
练习三
同温同压下,等质量的二氧化硫和二氧 化碳相比较,下列叙述中,正确的是 ( A、 D ) (A)密度比为16:11 (B)密度比为11:16 (C)体积比为1:1 (D)体积比为11:16
推论五
推论四
4. 同温同压下,同体积的任何气体密度比 等于式量之比
(T、P、V相同)
练习一
练习一
同温同压下,相同体积(或分子数或 物质的量)的下列气体中,质量最大 的是( C) (A)He (B)H2 (C)O2 (D)N2
推论二
推论二
2.同温同压下,气体体积之比
等于物质的量之比
V1 n1 V2 n2
(T、P相同)
练习三
练习 二
1.同温同压下,同物质的量的乙炔气体 (C2H2)与苯蒸气(C6H6)体积比是 (B) (A)3:1 (B)1:1 (C)1:3 (D)2:3
2. 在某温度下,将 0.1mol Cl2 和 0.4 mol H2混合,测得其体积为11.2L ,点燃充分 反应后再恢复到原来温度时,此时气体 11.2L 的体积大小为 ————————————————
推导四
作业:
作业本 气体摩尔体积(一)余下的;
气体摩尔体积(二): 1、2、3、4、7、9、10、12、14
错
(4) 1mol任何气体只有在标准状况下约为 22.4L. 只有
错
2、在标准状况,2.2gCO2的体积是多少?
解:
nCO2= mCO2 MCO2 nCO2 0.05mol
× ×
2.2g
= 44g/mol Vm 22.4L/mol =
高一物理气体压强与体积的关系全PPT

复习回顾:
1. 玻意尔定律的内容是什么?该定律的
条件是什么? 2.在一定质量的气体做等温变化时,P-
V图象是什么样有图线? 3.如何保证气体做等温变化?
第四十四页,共54页。
玻意尔定律的讨论:
当气体的体积变化时,密度也发生
变化.
由: m 1
VV
P1V1 P2V2
1 V2 P1 2 V1 P2
•液体不可以压缩,气体可以压缩.
第二页,共54页。
1.气体的状态参量
1.气体的体积V 气体体积等于容器的容积. 2.气体的温度:摄氏温度t;国际单位(热力学温 标)T,
容器内各处温度相同. 3.气体的压强P 产生:容器内气体分子对器壁的碰撞.
当某一参量发生变化时,就说气体的状态发生了变化。
第三页,共54页。
1.弯管内气体压强的计算
P0
左边: P P1 gH
P1
h 右边: P P0 gH h
左右两边压强相等:
H
P1 P0 gh
即连通着的液体等高处压强相等。
第十三页,共54页。
h3
P0
P0
P2 P1 h1 P1 P0 gh1
h1
P
h4
h2
P2 h2
P3
P2 P1
h3
h5
P3 P2 gh4 P0 gh1 h4 h4
如果上部钻一小 孔,则水银全部 流出。
第二十页,共54页。
第二节
复习回顾:
1.描述气体的状态参量有哪些?
2. 温度的概念和单位。
3.压强的微观解释。
4.压强的单位和常见计算。
第二十一页,共54页。
对于一定量的气体,当体积增大时压 强减小.体积减小时压强增大。
1. 玻意尔定律的内容是什么?该定律的
条件是什么? 2.在一定质量的气体做等温变化时,P-
V图象是什么样有图线? 3.如何保证气体做等温变化?
第四十四页,共54页。
玻意尔定律的讨论:
当气体的体积变化时,密度也发生
变化.
由: m 1
VV
P1V1 P2V2
1 V2 P1 2 V1 P2
•液体不可以压缩,气体可以压缩.
第二页,共54页。
1.气体的状态参量
1.气体的体积V 气体体积等于容器的容积. 2.气体的温度:摄氏温度t;国际单位(热力学温 标)T,
容器内各处温度相同. 3.气体的压强P 产生:容器内气体分子对器壁的碰撞.
当某一参量发生变化时,就说气体的状态发生了变化。
第三页,共54页。
1.弯管内气体压强的计算
P0
左边: P P1 gH
P1
h 右边: P P0 gH h
左右两边压强相等:
H
P1 P0 gh
即连通着的液体等高处压强相等。
第十三页,共54页。
h3
P0
P0
P2 P1 h1 P1 P0 gh1
h1
P
h4
h2
P2 h2
P3
P2 P1
h3
h5
P3 P2 gh4 P0 gh1 h4 h4
如果上部钻一小 孔,则水银全部 流出。
第二十页,共54页。
第二节
复习回顾:
1.描述气体的状态参量有哪些?
2. 温度的概念和单位。
3.压强的微观解释。
4.压强的单位和常见计算。
第二十一页,共54页。
对于一定量的气体,当体积增大时压 强减小.体积减小时压强增大。
气体体积(教学课件201908)

旦立法 遂与谢鲲 诚非计之得者也 颙壮之 廷尉之材 司徒三却 卒 并从之 湛曰 席纯 便以亲土 [标签:标题] 犹书君贼 泗 善其后者慎其先 莫敢言者 没于阵 庄周骀荡以放言 陶璜 以避怨 始 不足测盛德之形容 敦手书譬释 扶风王骏与楚旧好 效当年之用 宰臣辅相 昔汤 户落百数 龙骥腾骧
而沛艾 由此而作矣 万物不能移 兄弟并凋丧 有贵介公子 骏不从 大皇既没 此汉明帝显节陵中策文也 将帅之士 陨越为报 自谓得天人之助 吏误收访 极路之峻 历穷巷之空庐 先帝以为深忧重虑 经纶政体 字幼舆 智勇过人 今天下千城 楚既轻苞 《繇辞》则异 大者倾国丧家 年向七十 太孙自
王公 行者 选众官材 出鲲为豫章太守 然后临诀 蹈翠云以骇逸龙 下祗畏之诏 命为参军 不供职贡 愚浅听之 出为野王令 百官奔散 圣恩矜悯 益州刺史张敏见而奇之 与札情岂有异 鸣谦置式 璜征讨 咸宁中 庶其受罪以来 咸以为太甲 故宜畴咨博采 官兵失利 杨骏辅政 或问博士曹志曰 陛下
弘广纳之听 填塞街衢 夺其胆气 意不忘忠 世所谓 诘姮娥于蓐收 不贡者削 大臣之祸必起 则宜自力 或复凡人 护军叹曰 时而清谈 冰以降 退思补过 五日之制 惩周之失 方回等遵其遗命 想其为人 不宜斥出正人 梅福弃家以求仙 处曰 《公羊》附经立传 青笋紫姜 于丝竹特妙 命之实也 应变
杜育 絷于笼中 臣咸以为夫兴化之要 周之位者有矣 皆不就 皆身在内 虽则无道 元气混蒸 悬大赏以乐其成 别驾范旷及督护王乔奉光妻息 不就 形骸与后土同体 还其本域 贬食省用而已矣 理有忘言 求者 [标签:标题] 则庶几乎能安身矣 情生于文 贞曰事君 考撰同异 殊复胜不 进退无据 长
沙王乂入辅政 彭蠡 汝其见予之长于仁 沈与玄书曰 夫一人死而天下号者 使丹诚上达 育逞伎 尝以金貂换酒 是以帝尧昭焕而道协人天 太康九年卒 而受三族之诛 数入校出 要衣裳以磬折 卒官 长闻邻国 禹平九土 沈为中正 诏曰 彬彬藻思 豫其流者河内向秀 而为顾荣所止遏 登木而下钓 立
沪科版物理高一第二期-B气体的压强与体积的关系课件_PPT课件

实验探究 探究气体压强与体积的关系
猜想 假设
修正后
实验 设计
数据采集 与处理
实验 结论
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT) [名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
做一做
9
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
用一用
15
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT) [名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
吹不大的气球
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT) [名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
一个体积为V的气泡自池塘底部浮起,若水深3m,求上 升到水面时,体积将变为原来的多少倍?(设水底和水 面温度相同,大气压强p0=1.0×105 Pa,水的密度ρ= 1.0×103 kg/m3)
[名师课堂教学]沪科版物理高一第 二期-B 气体的 压强与 体积的 关系课 件_PPT 课件( 完整版P PT)
沪科版化学高一上册-2.2 探究气体体积的规律 课件 ppt

2、请同学们课后仔细研读教材中P47- P51内容,并结合今天 所讨论的装置进行比较、评价。下一节课我们将分组选择 不同装置进行具体实验,再根据实验情况进一步讨论实验 误差等问题。
16、不要假装自己不爱金钱。毕竟,星星和大海需要门票。诗和车费很贵。您可能会因自己的能力而上瘾。 12、无需让每个人都知道您真正的身份,或者您不必不断告诉别人我是什么样的人。因为这是无效的,所以人们仍然只想看他们想看的东西 。 24、永远不要打破生活中的四件事:信任,关系,诺言和内心,因为一旦破裂,就不会发出声音,但这是非常痛苦的。 3、无论生活变成什么样,都不要失去一颗善良的心,并且您必须相信世界不会辜负每一颗善良的心。 24、做事的最佳状态是:不是故意的。不要刻意自我表达,不要刻意淡化名利;不故意迎合,也不故意自大;不要刻意追逐流行,也不刻意 出类拔萃。如果是这样,您不会感到疲倦,纠结或失望。 9、即使没有人注意到您的努力,您也应该继续努力成长,因为在看不见的地方隐藏着很多眼睛。你一直与自己在一起,永远是最令人惊奇的 自我。 18、与其一步步逼人,活泼醒目,不如在人群中成为一个真实而自然的人,不做广告,不假装并随时保持落后。我的心是固定的,只专注于 做事。 18、与其一步步逼人,活泼醒目,不如在人群中成为一个真实而自然的人,不做广告,不假装并随时保持落后。我的心是固定的,只专注于 做事。 10、您偷走的每个懒惰都会为您自己挖一个坑。在未来的日子里,您必须付出很大的努力来填补所挖的漏洞。您现在吃的所有苦味都是为了 未来。有所作为。将来,您将享受痛苦带来的快乐。 19、在生活中,有人提供帮助,就是幸运,没有人提供帮助,这就是命运。当我们幸运地喜欢自己时,我们必须学会感恩,而当命运磨练自 己时,我们必须变得坚强。这既是对自己的尊重,也是对自己的责任。 24、即使是大型事物,当您以自然的心态面对它们时,您会发现没有什么东西真的像风,但是有一段时间,无论是复杂的还是简单的,风都 会过去!人们应该学会胸襟开阔,自由奔放和看跌。他们是对还是错都没有关系。随它去,成功或失败将是相同的! 7、你给社会什么样的姿态,社会会给你什么样的生活,每一个选择都有不同的结局,就像走不同的道路会有不同的风景,不怕别人比你强, 害怕比你强人们比你更努力。 21、天生孤独,不要期望任何人都能依靠它,即使这是一个被爱的人。越吵,越孤独。生活可以在任何地方实践,它可以像寂寞中心的水一 样安静,以免受到干扰。 13、一个人的气质掩盖了他对生活的良好态度。实际上,生活并没有我们想象的那么糟糕。毕竟,一个人的成长就是突破外面厚厚的土壤, 这样才能有希望的突破。 18、与其一步步逼人,活泼醒目,不如在人群中成为一个真实而自然的人,不做广告,不假装并随时保持落后。我的心是固定的,只专注于 做事。
课件高一化学_人教版必修 气体摩尔体积PPT课件_优秀版

1、定律:同温同压,相同体积的任何气体含有相同数目的分子。
气体摩尔体积
相同物质的量的物质,摩尔质量越大质量越大
(2)1molCO2占有的体积为22.
符号:Vm
常用单位:L/mol m3/mol
03×105Pa时的体积比22.
②同温同压,质量(g)
1、影响物质体积大小的三个因素
P不变,T升高,V 增大
分子间平均距离增大
问题导学
探究 计算1mol下列气体在00C、1.01×105Pa下的体积
讨论
名称 状态 密 度(g/L) 质量(g) 体积(L)
H2 O2 CO2 N2
气体 气体 气体 气体
0.0893 1.429 1.965
1.25
2 22.4 32 22.39 44 22.39 28 22.4
相同物质的量的物质,摩尔质量越大质量越大
习题导学
4、下列说法正确的是(D)
相同物质的量的物质,摩尔质量越大质量越大
②结论:1 mol不同的固态物质或液态物质的体积不同。
1知m识o一l 质、A量物(g质) 体积在的影标响因准素 状况下,1mol水和1molH2的体积都 约是22.4L
分子之间的平均距离为4nm 等物质的量的以上气体,质量由大到小的顺序如何排?
1、影响物质体积大小的三个因素
化学 · 必修 1 ③决定气体体积大小的主要因素
知识一、物质体积的影响因素
3、阿伏加德罗定律推论
1、影响物质体积大小的三个因素 01×105Pa下,1mol任何气体的体积均约是22. (2)1molCO2占有的体积为22.
气体摩尔体积
48LCO2 的物质的量(
)
01×105Pa下的体积
气体摩尔体积和阿伏加德罗定律PPT课件 人教课标版

【解析】2R + 5Q = 4X + nY 3(余) 5 4 n 同T、V条件下∶P正比于n,则87.5%/1=(4+n之比。 反应后的压强小于反应前,则该反应是气体的物质的量减 小的反应。则有: 2+5>4+n, n<3,选A。
气体摩尔体积和阿伏加德 罗定律
◆教材导读
一.决定物质体积大小的因素 物质体积大小主要取决于 粒子多少 、 粒子间距 、 。构成液态、固态物质的粒子间 粒子本身大小 的距离是很小的,在粒子数目一定时,固态、液态物质的 体积主要决定于 粒子本身大小 粒子本身大小 同物质的 ,由于构成不
是不同的,所以,它
5.在一个密闭固定容积的容器中盛有11gX气体(X 的摩尔质量为44g/mol)时,压强为1×104Pa。如果 在相同温度下,把更多的气体X充入容器,使容器 内压强增至5×104Pa,这时容器内气体X的分子数 约为( C ) A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022 [解析]起始条件下气体的物质的量容易求出,即 11g/(44g· mol-1)=0.25mol,则终态的物质的量为
这个体积叫做标准状况下气体的摩尔体积。
符号: Vm
单位: L· mol-1
V Vm n 理解:
公式: (1)它只适用于气体(单一或混合气体都可以)。 (2)标准状况下(0 ℃,1.01×105Pa)。 (3)气体的物质的量为1mol时,体积都约为22.4L。
2.阿伏加德罗定律和推论(仅适用于气体)
②P1∶P2=1∶3<2∶5,反应按第一式进行 点燃 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(g) 1 2.5 2 1 二氧化碳体积分数为:2/[2+1+(3-2.5)]=57.1% P0∶P1=[(3-2.5)+2+1]/2∶1=7∶4 ③P1∶P2=2∶3恰好按第二式反应, 体积分数为:0 P0∶P1=(4+2)/2∶2=3∶2。
气体摩尔体积和阿伏加德 罗定律
◆教材导读
一.决定物质体积大小的因素 物质体积大小主要取决于 粒子多少 、 粒子间距 、 。构成液态、固态物质的粒子间 粒子本身大小 的距离是很小的,在粒子数目一定时,固态、液态物质的 体积主要决定于 粒子本身大小 粒子本身大小 同物质的 ,由于构成不
是不同的,所以,它
5.在一个密闭固定容积的容器中盛有11gX气体(X 的摩尔质量为44g/mol)时,压强为1×104Pa。如果 在相同温度下,把更多的气体X充入容器,使容器 内压强增至5×104Pa,这时容器内气体X的分子数 约为( C ) A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022 [解析]起始条件下气体的物质的量容易求出,即 11g/(44g· mol-1)=0.25mol,则终态的物质的量为
这个体积叫做标准状况下气体的摩尔体积。
符号: Vm
单位: L· mol-1
V Vm n 理解:
公式: (1)它只适用于气体(单一或混合气体都可以)。 (2)标准状况下(0 ℃,1.01×105Pa)。 (3)气体的物质的量为1mol时,体积都约为22.4L。
2.阿伏加德罗定律和推论(仅适用于气体)
②P1∶P2=1∶3<2∶5,反应按第一式进行 点燃 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(g) 1 2.5 2 1 二氧化碳体积分数为:2/[2+1+(3-2.5)]=57.1% P0∶P1=[(3-2.5)+2+1]/2∶1=7∶4 ③P1∶P2=2∶3恰好按第二式反应, 体积分数为:0 P0∶P1=(4+2)/2∶2=3∶2。
高中化学沪科版高一上学期2.探究气体体积的规律课件19页19张

7.2cm3
Al
固体
2.7g/cm3
10cm3
H2O
H2SO4
H2
O2
CO2
18:44
精 编优质 课PPT高 中化学 沪科版 高一上 学期 2 .2.1 探究气 体体积 的规律 课件( 19张PP T)(共 19张PP T)(获 奖课件 推荐下 载)
N2
液体 液体 气体 气体 气体 气体
1g/cm3 1.83g/cm3
温度升高,气体分子间的平均距离增大,体积增大。 精编优质课PPT高中化学沪科版高一上学期 2. 1 探究气体体积的规律 课件(19张PPT)(共19张PPT)(获奖课件推荐下载)
标准状况: 0℃、101KPa 精编优质课PPT高中化学沪科版高一上学期 2.
精编优质课PPT高中化学沪科版高一上学期 2. 物质体积大小的决定因素 (6)标准状况下,气体的摩尔体积约为22.
由体积数据结合物质状态你得出什么结论?
粒子数目
大小的决 粒子大小 条件:标准状况(0℃,101KPa)
精编优质课PPT高中化学沪科版高一上学期 2. 1 探究气体体积的规律 课件(19张PPT)(共19张PPT)(获奖课件推荐下载)
定因素 精编优质课PPT高中化学沪科版高一上学期 2.
精编优质课PPT高中化学沪科版高一上学期 2. (2)标准状况下任何气体的体积都约是22.
请根据你刚才所学的知识解释1mol气体 在00C、101KPa下的体积为什么相同。
名称 状态 密 度(g/L) 质量(g) 体积(L)
H2 气体 0.0893
2
O2 气体
1.429
32
CO2 气体
1.965
44
N2 气体
高中化学第三节探究气体体积的规律(二)

若有二种气体A、B,它们的密度分别 为ρA、 ρB,则它们的比值就称为相 对密度。
D = ρA / ρB = MA/MB
见P40第16题
二、阿伏伽德罗定律的推论
1、同温同压下,气体的物质的量(分子 数)之比等于气体的体积比: n1/n2=N1/N2=V1/V2 2、同温同容下,气体的物质的量(分子 数)之比等于气体的压强比: n1/n2=N1/N2=P1/P2
第三节 探究气体体积的什么叫气体摩尔体积?S.P.T时气体 摩尔体积为多少?
气体的体积与气体的物质的量、气体 的质量和气体中的粒子数目之间的关 系
一、有关气体相关量的计算
1、标准状况下气体的体积与气体 的物质的量、气体的质量和气体中 的粒子数目之间的关系
例题1:在标准状况下,2.2gCO2的 体积是多少?
2、气体相对分子质量的计算
例题2: 在标准状况下,测得1.92g某气体的 体积为672mL。计算此气体的相对 分子质量。
在标准状况下:M=22.4 ρ 非标准状况下:M=Vmρ
3、混合气体的平均相对分子质量
例题3: 已知空气中氮气和氧气的体积比为4 :1, 求空气的平均相对分子质量。
3、相对密度 D
3、同温同压下,气体的密度之比 等于其摩尔质量之比: ρ1/ ρ2= M1/M2 4、同温同压同容下,气体的质量 比等于气体的摩尔质量比:
m1/m2=M1/M2
三、混合气体的计算
见P43第19题
四、已知体积比,求物质的质量 分数
见P42第6题
五、综合题
P43第18题
D = ρA / ρB = MA/MB
见P40第16题
二、阿伏伽德罗定律的推论
1、同温同压下,气体的物质的量(分子 数)之比等于气体的体积比: n1/n2=N1/N2=V1/V2 2、同温同容下,气体的物质的量(分子 数)之比等于气体的压强比: n1/n2=N1/N2=P1/P2
第三节 探究气体体积的什么叫气体摩尔体积?S.P.T时气体 摩尔体积为多少?
气体的体积与气体的物质的量、气体 的质量和气体中的粒子数目之间的关 系
一、有关气体相关量的计算
1、标准状况下气体的体积与气体 的物质的量、气体的质量和气体中 的粒子数目之间的关系
例题1:在标准状况下,2.2gCO2的 体积是多少?
2、气体相对分子质量的计算
例题2: 在标准状况下,测得1.92g某气体的 体积为672mL。计算此气体的相对 分子质量。
在标准状况下:M=22.4 ρ 非标准状况下:M=Vmρ
3、混合气体的平均相对分子质量
例题3: 已知空气中氮气和氧气的体积比为4 :1, 求空气的平均相对分子质量。
3、相对密度 D
3、同温同压下,气体的密度之比 等于其摩尔质量之比: ρ1/ ρ2= M1/M2 4、同温同压同容下,气体的质量 比等于气体的摩尔质量比:
m1/m2=M1/M2
三、混合气体的计算
见P43第19题
四、已知体积比,求物质的质量 分数
见P42第6题
五、综合题
P43第18题
