化工原理课件第11章:萃取
合集下载
萃取-课件

乳化现象
有机相 水相
乳化层
水包油(O/W)型 油包水(W/O)型
乳浊液的破坏措施
物理法:离心、加热,吸附,稀释 化学法:加电解质、其他表面活性剂 * 转型法 加入一种乳化剂,条件: ① 形成的乳浊液类型与原来的相反,使原乳浊液转型 ② 在转型的过程中,乳浊液破坏,控制条件不允许形成 相反的乳浊液, * 顶替法 加入一种乳化剂,将原先的乳化剂从界面顶替出来: ① 形成的乳浊液类型与原来的一致 ② 它本身的表面活性 > 原来的表面活性 ③ 不能形成坚固的保护膜。
1 你能叙述一下四氯化碳萃取碘水的过程吗?
我们把四氯化碳称为萃取剂,碘水中的水 2 称为原溶剂,你能归纳出选择萃取剂的原
则吗?
3 请你给萃取下一个定义
b. pH值
c. 相比 影响分配系数,影响物质解离情况
d. 盐分
溶媒比=溶媒体积/萃取体积
溶媒比↑萃取效果↑溶媒回收费用↑
e. 乳化程度
盐分影响分配系数
尽量破坏乳浊液,如轻度乳化,要加热过滤离心(热 敏物质不用热);重度乳化,加SDS、溴化十五烷基 吡啶等去乳化剂。
pH的影响
pH对表观分配系数的影响(pH ~ K) pH低有利于酸性物质分配在有机相,碱性 物质分配在水相。 对弱酸随pH ↓K ↑, 当pH << pK 时, K→K0
当含有生化物质的溶液与互不相溶的第二相接触时生化物质倾向于在两相之间进行分配当条件选择得恰当时所需提取的生化物质就会有选择性地发生转移集中到一相中而原来溶液中所混有的其它杂质如中间代谢产物杂蛋白等分配在另一相中这样就能达到某种程度的提纯和浓缩
本章主要内容
1.萃取概念及基本原理 2.萃取的操作过程 3. 萃取过程的影响因素
化工原理 液液萃取

第十一章 液液萃取(抽提) Liquid Extraction
11.1 概述
液-液萃取(抽提):在液体混合物中加入一种 与其不溶或部分互溶的液体溶剂,经过充分混合, 分相,利用混合液中各组分在溶剂中溶解度的差 异而实现分离的一种单元操作。又称溶剂萃取。
目的: 分离液-液混合物。 操作依据: 利用混合物中各组分在某一溶剂中 的溶解度之间的差异。
两相接触方式
微 分 接 触
级 式 接 触
11.2 液-液相平衡关系
11.2.1 三角形坐标及杠杆定律
11.2.1.1 三角形坐标 三元混合液的表示方法:
三角形坐标
等边三角形 直角三角形(等腰直角三角形和不等腰直角三角形)
① 表示方法 习惯表示法: ▲ 各顶点表示纯组分; ▲ 每条边上的点为两组分混合物; ▲ 三角形内的各点代表不同组成的三元混合物。
液液萃取的应用
1、在石油化工中的应用 随着石油化工的发展,液液萃取已广泛应用于分离各种
有机物质。轻油裂解和铂重整产生的芳烃混合物的分离是重 要的一例。该混合物中各组分的沸点非常接近,用一般的分 离方法很不经济。工业上采用Udex、Shell、Formex等萃取 流程,分别用环丁砜、四甘醇、N-甲基吡咯烷酮为溶剂,从 裂解汽油的重整油中萃取芳烃。对于难分离的乙苯体系,组 分之间的相对挥发度接近于1,用精馏方法不仅回流比大, 塔板还高达300多块,操作费用极大。可采用萃取操作以HFBF3作萃取剂,从C8馏分中分离二甲苯及其同分异构体。
A
mE RM mR ME
点P组成按上述长度为
A:30% B:50% S:20%
A
80
20
UF
60 Q Z 40
40 E 20
S%
11.1 概述
液-液萃取(抽提):在液体混合物中加入一种 与其不溶或部分互溶的液体溶剂,经过充分混合, 分相,利用混合液中各组分在溶剂中溶解度的差 异而实现分离的一种单元操作。又称溶剂萃取。
目的: 分离液-液混合物。 操作依据: 利用混合物中各组分在某一溶剂中 的溶解度之间的差异。
两相接触方式
微 分 接 触
级 式 接 触
11.2 液-液相平衡关系
11.2.1 三角形坐标及杠杆定律
11.2.1.1 三角形坐标 三元混合液的表示方法:
三角形坐标
等边三角形 直角三角形(等腰直角三角形和不等腰直角三角形)
① 表示方法 习惯表示法: ▲ 各顶点表示纯组分; ▲ 每条边上的点为两组分混合物; ▲ 三角形内的各点代表不同组成的三元混合物。
液液萃取的应用
1、在石油化工中的应用 随着石油化工的发展,液液萃取已广泛应用于分离各种
有机物质。轻油裂解和铂重整产生的芳烃混合物的分离是重 要的一例。该混合物中各组分的沸点非常接近,用一般的分 离方法很不经济。工业上采用Udex、Shell、Formex等萃取 流程,分别用环丁砜、四甘醇、N-甲基吡咯烷酮为溶剂,从 裂解汽油的重整油中萃取芳烃。对于难分离的乙苯体系,组 分之间的相对挥发度接近于1,用精馏方法不仅回流比大, 塔板还高达300多块,操作费用极大。可采用萃取操作以HFBF3作萃取剂,从C8馏分中分离二甲苯及其同分异构体。
A
mE RM mR ME
点P组成按上述长度为
A:30% B:50% S:20%
A
80
20
UF
60 Q Z 40
40 E 20
S%
萃取(化工原理)..31页PPT

25、学习是劳动,是充满思想的劳动。——乌申斯基
谢谢!
。— —爱献 生
21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈
23、一切节省,归根到底都归结为时间的节省。——马克思 24、意志命运往往背道而驰,决心到最后会全部推倒。——莎士比亚
萃取(化工原理)..
36、如果我们国家的法律中只有某种 神灵, 而不是 殚精竭 虑将神 灵揉进 宪法, 总体上 来说, 法律就 会更好 。—— 马克·吐 温 37、纲纪废弃之日,便是暴政兴起之 时。— —威·皮 物特
38、若是没有公众舆论的支持,法律 是丝毫 没有力 量的。 ——菲 力普斯 39、一个判例造出另一个判例,它们 迅速累 聚,进 而变成 法律。 ——朱 尼厄斯
谢谢!
。— —爱献 生
21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈
23、一切节省,归根到底都归结为时间的节省。——马克思 24、意志命运往往背道而驰,决心到最后会全部推倒。——莎士比亚
萃取(化工原理)..
36、如果我们国家的法律中只有某种 神灵, 而不是 殚精竭 虑将神 灵揉进 宪法, 总体上 来说, 法律就 会更好 。—— 马克·吐 温 37、纲纪废弃之日,便是暴政兴起之 时。— —威·皮 物特
38、若是没有公众舆论的支持,法律 是丝毫 没有力 量的。 ——菲 力普斯 39、一个判例造出另一个判例,它们 迅速累 聚,进 而变成 法律。 ——朱 尼厄斯
萃取ppt课件

11
萃取剂S 原料F
萃取相E
萃 取
萃
设 备
取 剂 回
萃取物E′
收
回 收 萃 取 剂
S’
设
备
萃余相R
萃
设 备
取 剂 回
收
萃余物R′
萃取过程
12
一、中药材中的成分 分为有效成分,辅助成分,无效
成分和组织物。在提取中,前两者应 尽量提取完全,后两者尽量除去。
二、中药提取的类型 分为单体成分提取、单味药提取
变动范围大
15~75 6~45 3~6 3~60 4~95
75%~95%
he=3~6m he=1.5~6m 对HT=100~300mm时 微30% 3.4~12.5级
润滑油工艺,核燃料加 工
用氨水从NaOH中萃取
NaC1 回收苯酚 糠醛处理润滑油工艺 废水中脱酚
萃取设备的类型很多。按萃取设备的构造特点大体上 可以分为三类:一是单件组合式;二是塔式;三式离心6式。
油、挥发油、蜡),用于脱脂。易燃。
19
常用提取辅助剂: 主要是酸、碱和表面活性剂。
五、提取方法
1、煎煮法
用水作溶剂,将药材饮片或粗粉加热煮 沸一定的时间,以浸出有效成分的方法。
适用于有效成分能溶解于水且对湿、热
稳定的药材。
20
2、浸渍法
用定量溶剂,在一定的温度下将药材饮 片或颗粒浸泡一定时间,以浸出有效成分的 方法。
优点:提取液浓度和提取率较高,适 用于大批量生产;缺点:热敏性药材不适合, 占地面积大。
36
37
10、连续逆流提取 采用浸渍法或重渗漉法动态连续式提取, 药材的总体运动方向和溶液的总体流动方向 相反,药材连续不断地进入提取器的同时药 渣和提取液连续不断地排出。提取率高,适 合大规模提取。
萃取剂S 原料F
萃取相E
萃 取
萃
设 备
取 剂 回
萃取物E′
收
回 收 萃 取 剂
S’
设
备
萃余相R
萃
设 备
取 剂 回
收
萃余物R′
萃取过程
12
一、中药材中的成分 分为有效成分,辅助成分,无效
成分和组织物。在提取中,前两者应 尽量提取完全,后两者尽量除去。
二、中药提取的类型 分为单体成分提取、单味药提取
变动范围大
15~75 6~45 3~6 3~60 4~95
75%~95%
he=3~6m he=1.5~6m 对HT=100~300mm时 微30% 3.4~12.5级
润滑油工艺,核燃料加 工
用氨水从NaOH中萃取
NaC1 回收苯酚 糠醛处理润滑油工艺 废水中脱酚
萃取设备的类型很多。按萃取设备的构造特点大体上 可以分为三类:一是单件组合式;二是塔式;三式离心6式。
油、挥发油、蜡),用于脱脂。易燃。
19
常用提取辅助剂: 主要是酸、碱和表面活性剂。
五、提取方法
1、煎煮法
用水作溶剂,将药材饮片或粗粉加热煮 沸一定的时间,以浸出有效成分的方法。
适用于有效成分能溶解于水且对湿、热
稳定的药材。
20
2、浸渍法
用定量溶剂,在一定的温度下将药材饮 片或颗粒浸泡一定时间,以浸出有效成分的 方法。
优点:提取液浓度和提取率较高,适 用于大批量生产;缺点:热敏性药材不适合, 占地面积大。
36
37
10、连续逆流提取 采用浸渍法或重渗漉法动态连续式提取, 药材的总体运动方向和溶液的总体流动方向 相反,药材连续不断地进入提取器的同时药 渣和提取液连续不断地排出。提取率高,适 合大规模提取。
化工原理第十一章液液萃取和固液萃取

E R
kA yA
xA
y
0 A
x
0 A
y
0 A
x
0 A
B
kB
yB xB
y
0 B
x
0 B
1
y
0 A
1
x
0 A
M
S
要求:1,
kA 越大越好,kB 越小越好。
原料液
萃取剂 S
S
A+B
xF
yA
萃取相 E
y0
萃取液 E A
A(大量),B(少量)
S+A+B 萃余相 R
x B+A+S A
S
x0
萃余液 R A B (大量),A(少量)
R R
B
第十一章 液液萃取和固液萃取
S
R,xR E,yE
R,xR E,yE
S
E M
S0
S
16/19
2.解析法
总: F S R E
溶质 A:FxA,F SyA,S RxA,R EyA,E
萃取剂 S:0 SyS,S RxS,R EyS,E
相平衡:k A
y A, E x A,R
kB
yB,E xB,R
幻灯片1目录
§11.1 概述 §11.2 液液相平衡关系及相图
浙江大学本科生课程 化工原理
第十一章 液液萃取和固液萃取
1/12
第十一章 液液萃取和固液萃取
§11.1 概述
1.什么是液液萃取?
利用液体混合物中各组分在外加溶剂中溶解度 的差异而分离该混合物的操作,称为~。外加 溶剂称为萃取剂。
浙江大学本科生课程 化工原理
FxF S 0 MxM
第十一章 萃取

y ' 1 x' 1 y ' x'
K A y A / xA
K B yB / xB
2.3 萃取剂的选择
2、萃取剂与稀释剂的互溶度 互溶度越小,萃取操作范围越大,萃取液最大组成越高, 并且互溶度小的系统β越大,分离效果越好。
2.3 萃取剂的选择 3、萃取剂的其他物性 溶解度大,所用萃取剂量少; 要有较大的密度差,便于相分离; 界面张力要适中(相分散和相分离); 溶剂比热小便于回收; 粘度小便于相分散; 化学稳定性好,无腐蚀,无毒,不易燃、易爆,价廉易 得。
第一节 第二节 第三节 第四节 概述
液-液萃取
萃取的基本原理 萃取过程计算 萃取设备
第三节 萃取过程的理论计算
3.1
3.2 3.3 3.4
单级萃取
多级错流萃取 多级逆流萃取 连续逆流萃取
234
3.1 单级萃取过程
M F S ER
S FM xF xM F MS xM y0
2.3 萃取剂的选择
4. 天生的一对矛盾:混合与澄清(相分散与相分离) 搅拌 混合液 萃取剂
A+B
(溶剂S)
萃取相
(S+A+B)
萃余相
(B+A+S)
2.4 温度对萃取过程的影响
T ↓,S与B互溶度↓,两相区面积↑,对萃取有利;但是T ↓ , 液体μ ↑ ,D ↓ ,不利传质,所以应综合考虑。
第十一章
2.1.1 三角形相图法
3. 三角相图中的相平衡关系
溶解度曲线
混溶点 两相区和单相区 共轭相
平衡联结线
临界混溶点: 辅助线:(两种方法)
大学课件-化工原理下册-萃取2.2
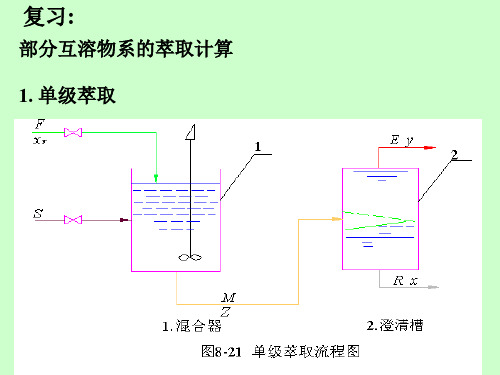
(qms/qmF)
操作线斜率, 趋于分配曲线的斜率
(qmS/qmF) (qms/qmF)min-- 最小溶剂比
P点(夹紧点)所对应的两相联结线和级联线重合, yi=yi+1
夹紧点附近各级无分离能力,N
p
(2) 最小溶剂比的求法
Dmin的位置,既和平衡关系有关,又和分离要求有关。
R2 M2
R'3 R3
M3
B
S
8.3.3多级逆流萃取 一.流程:
二.特点
连续逆流操作,分离程度较高
三.计算
设计型问题:已知S的组成,qmF、xF,
规定 qmS/qmF (溶剂比)和分离要求RN',求N。
解法:每级内平衡
R i-1 i
Ei
Ri E i+1
Ei和Ri平衡,若能确定Ri组成xi和Ei+1组成yi+1之间的关系, 即可求得理论级数(逐级计算) 。
D''
qmS/qmF 较大
MS, D是E1和F的差点, 净物流向左流动, D点必在三角形相图右侧。
qms/qmF
MF, E1升高,D点远离S点。
qms/qmF
qmD=0, D点移到无穷远时, 级联线互相平行。
qms/qmF F为E1和D的和点, D点落在三角形相图左侧, 净物流向右流动。
3.逐级图解 (1)相图:Ri 和Ei互成平衡
已知F、S可确定M,由M、RN可确定E1 由 qmE1 qmF qmS qmRN qmD 可确定 D 点。
A
F
E1
R'N RN
M
D
B
S
由E1通过平衡关系确定R1,R1和D连线确定E2 , 如此交替 直至xi<xN, 则N为理论级数。
化工原理下册萃取本科图文PPT学习教案

方法二:
A
分别从E1、E2、E3、E4点 引 AB 平 行 线 , 与 分 别 从
R1、R2、R3、R4点引出的 AS 平 行 线 相 交 , 连 结 各
交点即得辅助曲线;
P
E4
E3
辅助曲线延长线与溶解度
R4
E2
曲线的交点即为临界混溶 点P;
R3 R2 R1 B
E1 S
借助辅助曲线可求出任何
一对共轭相的对应点,即
萃取设备的分类萃取设备的分类产生分散相的动力产生分散相的动力微分接触式微分接触式逐级接触式逐级接触式重力差重力差喷啉塔填料塔填料塔筛板塔筛板塔流动混合器流动混合器机械搅拌机械搅拌转盘萃取塔转盘萃取塔搅拌萃搅拌萃取塔振动筛板塔振动筛板塔混合澄清器混合澄清器脉冲脉冲脉冲填料塔脉冲填料塔脉冲筛脉冲筛脉冲混合澄清器脉冲混合澄清器离心力作用离心力作用连续式离心萃取器连续式离心萃取器逐级式离心萃取器逐级式离心萃取器第82页共106页常见工业萃取设备常见工业萃取设备逐级接触式萃取设备
(1)萃取剂的选择
萃取剂应不易水解和热解,耐酸、碱、盐、氧化剂或还原剂,腐 蚀性小。在原子能工业中,还应具有较高的抗辐射能力。
物理性质
(a) 溶解度:萃取剂在料液相中的溶解度要小。 (b) 密度:密度差大,有利于分层,不易产生第三相和乳化现象
,两液相可采用较高的相对速度逆流。
(c) 界面张力:界面张力大,有利于液滴的聚结和两相的分离; 另一方面,两相难以分散混合,需要更多外加能量。由于液 滴的聚结更重要,故一般选用使界面张力较大的萃取剂。
B xSD xSM xSC
S
(2) 分量与合量的质量与直线上相应线段的长度成比例,即:
C DM C DM D CM
第11章:萃取
化工原理——萃取
④E、R脱除溶剂得E0、R0
F E 0 R0
E0
E0 FR 0 F R0 E 0
d
R0 R
E
C
化工原理——萃取
⑤
y0 max A
E
0
FC S x 0 min A F max SC
y0 max ⑥过S做切线Se得 A
e
d
x Amin
R0 R 0
化工原理——萃取
11.2 萃取过程的平衡关系
2.2 平衡相图——溶解度曲线
根据萃取操作中各组分的互溶性,将混合
液分成两类:
பைடு நூலகம்
① A完全溶于B及S,B与S不互溶
B与S部分互溶 ② A完全溶于B,A与S部分互溶 B与S部分互溶
Ⅰ类物系
√
Ⅱ类物系
化工原理——萃取
1.溶解度曲线与平衡连接线
均相区 临界混溶点(P): 两共轭相的组成无限趋近 而变为一相,表示这一组 成的点。 P 溶解度 曲线 联结线 两相区
S / F 较小
S / F 为某数值 化工原理——萃取
11.4 萃取设备
4.1 萃取设备的基本要求
两相充分的接触并伴有较高程度的湍动。
有利于液体的分散与流动。
有利于两相液体的分层。
化工原理——萃取
4.2 萃取设备的分类
项目 逐级接触式 微分接触式
无外加能量
脉冲
筛板塔
脉冲混合-澄清器 混合澄清器 夏贝尔塔
化工原理——萃取
第1级: F E2 R1 E1 即:
A
F E1 R1 E2
第2级:R1 E2 R2 E3 第N级: RN 1 E N RN S
化工原理课件12萃取(LiquidExtraction)

05
萃取过程的优化与改进
提高萃取效率的途径
选择合适的萃取剂
根据待分离物质的特点和分离要 求,选择具有高选择性、高溶解
度、低能耗的萃取剂。
优化萃取工艺参数
通过调整温度、压力、浓度等工 艺参数,提高萃取效率和分离效
果。
强化传质过程
采用多级萃取、逆流萃取等工艺, 增加萃取剂与待分离物质接触机
会,提高传质效率。
3
萃取技术的优化
根据不同天然产物的性质和目标成分,选择合适 的萃取剂和工艺条件,提高萃取效率和纯度。
THANKS
感谢观看
它由多个塔板组成,液体在塔 内逐板下降,同时与上升的气 体或液体逆流接触,实现传质 与分离。
塔式萃取器的优点是处理能力 大、分离效果好,但结构复杂、 造价高、操作维护困难。
离心萃取器
离心萃取器利用离心力的作用使两液 相实现分离。
离心萃取器的优点是处理能力大、分 离效果好、结构简单、操作方便,但 制造成本较高。
04
萃取过程的设备
混合-澄清槽
混合-澄清槽是一种简单的萃取 设备,适用于两相接触后能迅速
分离的情况。
它由一个混合室和一个澄清室组 成,混合室用于使不相溶的两液 相混合,澄清室则用于分离两液
相。
混合-澄清槽结构简单,操作方 便,但处理能力较小,且分离效
果不够理想。
塔式萃取器
塔式萃取器是一种常见的萃取 设备,适用于处理大量物料。
双水相萃取技术
利用两种水相间物质分配的差异,实现高效分离和纯化。
06
萃取过程的实例分析
工业废水处理中的萃取应用
工业废水中的有害物质
01
工业废水可能含有重金属、有机污染物等有害物质,对环境和
化工原理第十一章 液液萃取和固液萃取

yA yA
同样,对稀释剂B有
kB
B在E相中得浓度= B在R相中得浓度
yB yB
萃取剂的选择性,用选择性系数 表示
kA yA / xA yA / yB (A / B)E kB yB / xB xA / xB ( A / B)R
要注意以下几方面:
1、 选择性 2、 萃取相与萃余相的分离 3、 萃取剂得回收
C2 ( b)
C1
图11-3 相平衡图
2024/3/26
5
三、杠杆规则
如图11-4所示,混合物M分成任意两个 相E和R,或由任意两个相E和R混合成一 个相M,或任意两个组分E和R混合成一个 混合物M(E、、R、M可以为同一相)。 则在三角形相图中表示其组成得点M、E 和R必在以直线上,且符合以下比例关系
除此之外,萃取剂还应满足一般得工业要求。
2024/3/26
7
11.1.4单级萃取
S F
S
E 3
萃 取 液E'
M
S
2
1
R
4
图 11- 5 单 击 萃 取 流 程
萃 余 液 R‘
1- 混 合 器 ; 2- 分 层 器 ; 3- 萃 取 相 分 离 设 备 ; 4- 萃 余 相 分 离 设 备
2024/3/26
8
一、利用三角形相图的图解计算
如图11—6所示,单级萃取得计算步骤
如下:
A
E'
1、 根据已知得平衡数据在直角三角形
相图中作出溶解度曲线及辅助曲线。
辅助曲线
2、由已知原料液组成xF在边AB上定点
F,连接点S和F。有
F
S FM
F MS
3、点M利用辅助曲线作联结线。有
相关主题
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工原理——萃取
3.3 多级萃取
1. 多级错流萃取 B与 S部分互溶物系的计算
已知:原料量 F 、原料组成 xF
各级萃取剂用量 Si 规定:最终萃余相组成 xn 计算:萃取级数 n
化工原理——萃取
F
xF
M1
E1
R1
E2
M2
R2
E3
R3
M3
x x n计算 ≤ n规定
n=3
化工原理——萃取
多级错流萃 取三角形相 图图解计算
均相区
溶解度
P
曲线
联结线
两相区
化工原理——萃取
化工原理——萃取
2.平衡连接线的内插
化工原理——萃取
3.分配系数和分配曲线
(1)分配系数
• 随体系的温度、浓度而变化,其数值需通过实验测定; • kA↑,萃取效果↑,需S量↓。
化工原理——萃取
3.分配系数和分配曲线
(2)分配曲线
化工原理——萃取
4.温度对溶解度曲线的影响
化工原理——萃取
第1级:F E2 R1 E1
即: F E1 R1 E2
A
第2级:R1 E2 R2 E3
E0
第N级:RN1 EN RN S
F
R1
R2
M E1 E2
R0
B
S
化工原理——萃取
化工原理——萃取
溶剂比的影响
S / F 较大
S / F 较小
(2) 用纯S萃取含A20%的AB原料,F=100kg/h,单级萃取时的 Smin为多少?此时E的量及组成?
(3) 单级萃取,萃取液可能达到的最大浓度为多少?当进料分 别为含A30%和10%时,是否都能使E0的浓度达到最大值? 所得萃取液浓度最大时S的用量?
化工原理——萃取
温度 ~ 互溶度 ~ 两相区 不利于萃取过程
T1 T2
T1<T2
化工原理——萃取
2.3 相平衡与萃取操作的关系
化工原理——萃取
2.3 相平衡与萃取操作的关系
① 在F中加入S,和点M由杠杆规则定。
F SM M F S S FM
② S用量应使M在 d 与 c 之间 ③ E和R的位置由辅助曲线试差得到
卢威离心萃取机
微分接触式 喷洒塔 填料塔
脉冲填料塔 液体脉冲筛板塔
转盘塔(RDC) 偏心转盘塔(ARDC)
库尼塔 往复筛板塔 POD离心萃取机
化工原理——萃取
(1) 有含A50%的AB原料液30kg及S15kg,将它们混合在一起, 问①混合液是否分层?若不分层,用什么方法使其分层? 若分层,用什么方法使其不分层?定量算出结果。
3. 两相的接触方式
化工原理——萃取
11.2 萃取过程的平衡关系 2.1 三角形相图
1. 溶液组成的表示方法
化工原理——萃取
2. 物料衡算与杠杆定律 化工原理——萃取
2.1 三角形相图
3. 混合物的和点与差点
化工原理——萃取
2.1 三角形相图
3. 混合物的和点与差点
化工原理——萃取
11.2 萃取过程的平衡关系
S1 S2 S3
3.3 多级萃取
2. 多级逆流萃取
化工原理——萃取
A
E0
F
M E1
R0
B
总物衡:F S E1 RN M
可求S、E1、RN 流量(杠杆规则)
S
化工原理——萃取
2. 多级逆流萃取
第1级:F E2 R1 E1 即: F E1 R1 E2 第2级:R1 E2 R2 E3 第N级:RN1 EN RN S
e
E
C
化工原理——萃取
化工原理——萃取
化工原理——萃取
2.4 萃取剂的选择性系数
E0
d R0 R
E
C
化工原理——萃取
E0
R0 R
β>1,能萃取分离,且愈大分离愈容易 β=1,不能萃取分离 β→∞,B与S不互溶
与分配系数 的区别 E
化工原理——萃取
2.5互溶度的影响 化工原理——萃取
11.3 萃取过程的计算
3.1 理论级和级效率
E, yA
F, xF
M, xM ∞
m
S, zA
R, xA
理论级:离开的R与E达到平衡
级效率:实际萃取级和理论级分离能力的差异。
化工原理——萃取
11.3 萃取过程的计算
3.2 单级萃取的计算
1.
2.
化工原理——萃取
3.3 多级萃取
1. 多级错流萃取
多级错流萃取的总溶剂用量为各级溶剂用量之和,原 则上,各级溶剂用量可以相等也可以不等。当各级溶剂用 量相等时,达到一定的分离程度所需的总溶剂用量最少。
11 液液萃取
11.1 萃取过程概述
1. 萃取过程的原理
液体混合物 (A + B)
引入另一液相 (萃取剂S)
各组分在萃取剂 中溶解度不同
液相E(萃取相) S + A(B)
液相R(萃余相) B +(A,S)
化工原理——萃取
S+A(B) B+(A,S)
化工原理——萃取
11.1 萃取过程概述
2. 萃取过程的经济性 萃取操作应用场合:
化工原理——萃取
S / F 为某数值
11.4 萃取设备
4.1 萃取设备的基本要求 两相充分的接触并伴有较高程度的湍动。 有利于液体的分散与流动。 有利于两相液体的分层。
化工原理——萃取
4.2 萃取设备的分类
项目 无外加能量
脉冲
外加能量 旋转搅拌 往复搅拌 离心力
逐级接触式 筛板塔
脉冲混合-澄清器 混合澄清器 夏贝尔塔
2.2 平衡相图——溶解度曲线
根据萃取操作中各组分的互溶性,将混合
液分成两类:
① A完全溶于B及S,B与S不互溶
Ⅰ类物系
B与S部分互溶
√
ቤተ መጻሕፍቲ ባይዱ
② A完全溶于B,A与S部分互溶 B与S部分互溶
Ⅱ类物系
化工原理——萃取
1.溶解度曲线与平衡连接线
临界混溶点(P):
两共轭相的组成无限趋近 而变为一相,表示这一组 成的点。
d
E RM
E
RME
R
M RE
C
化工原理——萃取
E0
d R0 R
④E、R脱除溶剂得E0、R0
F E0 R0
E 0 FR0
F R0E0
E
C
化工原理——萃取
y0 A max E0
d
x
0R0
A min
R
⑤
S F
max
FC SC
x0 Amin
⑥过S做切线Se得
y0 A max
相对挥发度α 接近 1或形成恒沸物的分离 产品浓度很低,且为难挥发组分物系的分离 热敏性物系的分离
化工原理——萃取
2. 萃取过程的经济性 化工原理——萃取
3. 两相的接触方式 (1)微分接触
喷洒萃取塔
化工原理——萃取
3. 两相的接触方式
(2)级式接触 单级连续萃取
单级混合沉降槽 化工原理——萃取
3.3 多级萃取
1. 多级错流萃取 B与 S部分互溶物系的计算
已知:原料量 F 、原料组成 xF
各级萃取剂用量 Si 规定:最终萃余相组成 xn 计算:萃取级数 n
化工原理——萃取
F
xF
M1
E1
R1
E2
M2
R2
E3
R3
M3
x x n计算 ≤ n规定
n=3
化工原理——萃取
多级错流萃 取三角形相 图图解计算
均相区
溶解度
P
曲线
联结线
两相区
化工原理——萃取
化工原理——萃取
2.平衡连接线的内插
化工原理——萃取
3.分配系数和分配曲线
(1)分配系数
• 随体系的温度、浓度而变化,其数值需通过实验测定; • kA↑,萃取效果↑,需S量↓。
化工原理——萃取
3.分配系数和分配曲线
(2)分配曲线
化工原理——萃取
4.温度对溶解度曲线的影响
化工原理——萃取
第1级:F E2 R1 E1
即: F E1 R1 E2
A
第2级:R1 E2 R2 E3
E0
第N级:RN1 EN RN S
F
R1
R2
M E1 E2
R0
B
S
化工原理——萃取
化工原理——萃取
溶剂比的影响
S / F 较大
S / F 较小
(2) 用纯S萃取含A20%的AB原料,F=100kg/h,单级萃取时的 Smin为多少?此时E的量及组成?
(3) 单级萃取,萃取液可能达到的最大浓度为多少?当进料分 别为含A30%和10%时,是否都能使E0的浓度达到最大值? 所得萃取液浓度最大时S的用量?
化工原理——萃取
温度 ~ 互溶度 ~ 两相区 不利于萃取过程
T1 T2
T1<T2
化工原理——萃取
2.3 相平衡与萃取操作的关系
化工原理——萃取
2.3 相平衡与萃取操作的关系
① 在F中加入S,和点M由杠杆规则定。
F SM M F S S FM
② S用量应使M在 d 与 c 之间 ③ E和R的位置由辅助曲线试差得到
卢威离心萃取机
微分接触式 喷洒塔 填料塔
脉冲填料塔 液体脉冲筛板塔
转盘塔(RDC) 偏心转盘塔(ARDC)
库尼塔 往复筛板塔 POD离心萃取机
化工原理——萃取
(1) 有含A50%的AB原料液30kg及S15kg,将它们混合在一起, 问①混合液是否分层?若不分层,用什么方法使其分层? 若分层,用什么方法使其不分层?定量算出结果。
3. 两相的接触方式
化工原理——萃取
11.2 萃取过程的平衡关系 2.1 三角形相图
1. 溶液组成的表示方法
化工原理——萃取
2. 物料衡算与杠杆定律 化工原理——萃取
2.1 三角形相图
3. 混合物的和点与差点
化工原理——萃取
2.1 三角形相图
3. 混合物的和点与差点
化工原理——萃取
11.2 萃取过程的平衡关系
S1 S2 S3
3.3 多级萃取
2. 多级逆流萃取
化工原理——萃取
A
E0
F
M E1
R0
B
总物衡:F S E1 RN M
可求S、E1、RN 流量(杠杆规则)
S
化工原理——萃取
2. 多级逆流萃取
第1级:F E2 R1 E1 即: F E1 R1 E2 第2级:R1 E2 R2 E3 第N级:RN1 EN RN S
e
E
C
化工原理——萃取
化工原理——萃取
化工原理——萃取
2.4 萃取剂的选择性系数
E0
d R0 R
E
C
化工原理——萃取
E0
R0 R
β>1,能萃取分离,且愈大分离愈容易 β=1,不能萃取分离 β→∞,B与S不互溶
与分配系数 的区别 E
化工原理——萃取
2.5互溶度的影响 化工原理——萃取
11.3 萃取过程的计算
3.1 理论级和级效率
E, yA
F, xF
M, xM ∞
m
S, zA
R, xA
理论级:离开的R与E达到平衡
级效率:实际萃取级和理论级分离能力的差异。
化工原理——萃取
11.3 萃取过程的计算
3.2 单级萃取的计算
1.
2.
化工原理——萃取
3.3 多级萃取
1. 多级错流萃取
多级错流萃取的总溶剂用量为各级溶剂用量之和,原 则上,各级溶剂用量可以相等也可以不等。当各级溶剂用 量相等时,达到一定的分离程度所需的总溶剂用量最少。
11 液液萃取
11.1 萃取过程概述
1. 萃取过程的原理
液体混合物 (A + B)
引入另一液相 (萃取剂S)
各组分在萃取剂 中溶解度不同
液相E(萃取相) S + A(B)
液相R(萃余相) B +(A,S)
化工原理——萃取
S+A(B) B+(A,S)
化工原理——萃取
11.1 萃取过程概述
2. 萃取过程的经济性 萃取操作应用场合:
化工原理——萃取
S / F 为某数值
11.4 萃取设备
4.1 萃取设备的基本要求 两相充分的接触并伴有较高程度的湍动。 有利于液体的分散与流动。 有利于两相液体的分层。
化工原理——萃取
4.2 萃取设备的分类
项目 无外加能量
脉冲
外加能量 旋转搅拌 往复搅拌 离心力
逐级接触式 筛板塔
脉冲混合-澄清器 混合澄清器 夏贝尔塔
2.2 平衡相图——溶解度曲线
根据萃取操作中各组分的互溶性,将混合
液分成两类:
① A完全溶于B及S,B与S不互溶
Ⅰ类物系
B与S部分互溶
√
ቤተ መጻሕፍቲ ባይዱ
② A完全溶于B,A与S部分互溶 B与S部分互溶
Ⅱ类物系
化工原理——萃取
1.溶解度曲线与平衡连接线
临界混溶点(P):
两共轭相的组成无限趋近 而变为一相,表示这一组 成的点。
d
E RM
E
RME
R
M RE
C
化工原理——萃取
E0
d R0 R
④E、R脱除溶剂得E0、R0
F E0 R0
E 0 FR0
F R0E0
E
C
化工原理——萃取
y0 A max E0
d
x
0R0
A min
R
⑤
S F
max
FC SC
x0 Amin
⑥过S做切线Se得
y0 A max
相对挥发度α 接近 1或形成恒沸物的分离 产品浓度很低,且为难挥发组分物系的分离 热敏性物系的分离
化工原理——萃取
2. 萃取过程的经济性 化工原理——萃取
3. 两相的接触方式 (1)微分接触
喷洒萃取塔
化工原理——萃取
3. 两相的接触方式
(2)级式接触 单级连续萃取
单级混合沉降槽 化工原理——萃取
