超细碳酸钙的制备实验报告.
多种形状超细碳酸钙的制备

制备多种形状的超细碳酸钙可以通过多种方法。
其中,化学沉淀法是一种常用的方法,包括直接沉淀法、碳化法、溶胶-凝胶法等。
此外,物理法也可以用来制备超细碳酸钙,如喷雾干燥法、机械研磨法、热解法等。
在这些方法中,碳化法是一种常用的制备超细碳酸钙的方法。
通过控制反应条件,如温度、压力、搅拌速度等,可以制备出不同形状的超细碳酸钙。
同时,通过添加表面活性剂或控制晶型控制剂的浓度和加入速度,可以进一步控制碳酸钙的形貌和粒径。
除了碳化法,其他方法也可以用来制备不同形状的超细碳酸钙。
例如,通过控制溶胶-凝胶法制备过程中的条件,可以制备出球形或立方体形状的超细碳酸钙。
机械研磨法可以将大颗粒的碳酸钙研磨成小颗粒,同时也可以改变其形貌和晶型。
热解法可以用来制备出空心或实心球形碳酸钙。
综上所述,制备不同形状的超细碳酸钙需要选择合适的方法,并控制反应条件和添加物,以获得所需的形貌和粒径。
多孔性超细碳酸钙粉体制备研究_郁平

图 1 CaCl2 溶液碳化法工艺流程示意图
首先在两个溶解槽中用 NH4 Cl 母液分别溶解 CaCl2 和 NH4 HCO3 ,配制成 1 molΠL 的 CaCl2 溶液和 2 molΠL 的 NH4 HCO3 溶液 ,并且在 NH4 HCO3 溶液中加
Preparation of Ultra2fine Calcium Carbonate with Porosity
YU Ping1 ,2 , YU Wen2liang1 , FANG Ding2ye
( 1. Department of Chemical Engineering , Shanghai Institute of Technology , Shanghai 200235 , China ; 2. School of Chemical Engineering , ECUST , Shanghai 200237 , China)
撞击流反应能使反应物在反应器中的停留时间
图 6 NH4 Cl 结晶颗粒显微照片
从图 6 可知 :在 NH4 Cl 结晶过程中 ,控制结晶体 系冷却速度在 0. 6 ℃Πmin ,连续冷却 25 min 可以获得 颗粒直径约为 0. 5 mm 的 NH4 Cl 结晶颗粒 ,此结晶易 于与水分离 ,干燥时间短 ,制得的 NH4 Cl 样品不潮 解。
在nh4ci结晶过程中控制结晶体系冷却速度在06min连续冷却25min可以获得颗粒直径约为05into的nh4ca结晶颗粒此结晶易于与水分离干燥时问短制得的nh4ci样品不潮在nh4ci结晶过程中控制过饱和度在结晶过程的介稳区内能使nh4ci结晶成长速度大于晶核生成速度使nh4ci结晶沉积在已有的晶核上使生成的nh4ci结晶大而均匀
超细碳酸钙的制备

2.2 实验步骤
(1)取6.36克的碳酸钠溶于200ml的蒸馏水中制成溶液。
取1.1克氯化钙溶于200ml蒸馏水中并且加入指定的添加剂放置在水浴锅中加热至指定温度。
(2)将已经配置好的碳酸钠溶液加入滴定漏斗中,打开并且调整活塞
使滴定液滴入待滴定溶液中,同时进行匀速搅拌,滴定完成后,继续搅
拌20min之后静置。
(3)倒掉上层清夜,用玻璃棒蘸取少量的余下部分做成切片,在生物显微
镜下观察晶形,并做好实验记录。
将余下部分过滤,待滤液过滤完成后,得
到白色沉淀。
(4)将(3)中沉淀置于设定温度为60℃的数显式电热培养箱内,直至干燥。
然后将烘干的沉淀物研细装入洗净的小试剂瓶中,并贴好标签,做好标记。
(5)通过做对比试验,得出最佳反应条件。
3.1实验数据记录。
超细碳酸钙粉末的制备研究

超细碳酸钙粉末的制备研究作者:余俊杰来源:《西部论丛》2019年第26期摘要:综述了超细碳酸钙粉末的生产工艺,着重结合了物理制备方法与化学制备方法进行比对,以此完善其生产工艺。
关键词:超细碳酸钙;生产工艺;物理方法;化学方法碳酸钙是一种重要的无机化工产品,由于无毒性、成本低、易获取,被广泛用作塑料工业、涂料工业、橡胶工业、医用、日用化工等各个行业。
而粒径在0.01~0.08μm之间的超细碳酸钙,由于其分散性、透明性、增韧补强性、流平性和稳定性等各方面性能与常规粉体材料相比都表现出较明显的优良性能,因此研究相对优良的生产工艺,已成为我国无机化工产业的重要工作。
一、物理方法制备超细碳酸钙(一)机械粉碎法机械粉碎法是利用外力使物體之间相互冲击、剪切、压缩、研磨,先通过破碎的方法将大块物料处理成小块物料,在利用粉磨的方法变成微小的颗粒,从而达到粉碎和磨细的目的,也可称之为研磨法。
工业生产中,常将石灰石、方解石、白垩石等碳酸钙含量较高的矿石,通过粉碎研磨得到重质CaCO3的产品。
由于其设备简单、运行稳定、适应能力较强、生产能力较大,可以满足工业化大生产,因此作为工业上的主要生产方式,但由于其效率低、能耗大、设备笨重、噪声污染严重,因此寻求更好的方法已成为工业发展的重大任务。
二、化学方法制备超细碳酸钙(一)复分解法复分解法一般是使用含Ca2+的水溶性钙盐(一般为氯化钙)和含有CO32-的水溶性碳酸盐(一般为碳酸铵),在一定条件下通过复分解反应制成油包水型碳酸钠乳状液[3],再通过一定条件分离,在真空中的条件下进行干燥之后,即可得到超细碳酸钙。
由于方法较为简单,步骤较少,操作性较高,但原材料成本高,且生产的产量较少,不适合在工业中使用。
(二)碳化法制备超细碳酸钙1多级喷雾碳化法多级喷雾碳化法是生产能力较大的一种方法,在喷雾碳化塔中,将Ca(OH) 2浆液由上而下以喷雾形式喷出,再将CO2气体自下而上吹入,使得增大二者原料之间的有效接触面积。
纳米级超细碳酸钙的制备

碳酸钙粒径,通过添加形状控制剂可得到纺锤形、 片状、 球 形、 立方形、 链状等形状各异 的颗粒 日本在超细碳酸钙 的研制、 生产、 应用方面处于 国际领 先地位, 白石工业公司 1 1 年, 9 4 发明了“ 碳化法” 生产轻质碳 酸钙。12 9 7年发 明了“ 细微活性碳酸钙” 的制法。13 9 3年研 制 出了用硬脂酸进行表面化的产品。15 9 2年生产出了粒径 在 O0 1 的碳酸钙。在 1 6 . ̄ 4m 9 5年发展到粒径细至 00 1n . a, 2 以后又陆续 开发了各种形貌 各种 粒径 的产品和表面改性 剂 , 目前为止 , 到 具有纺锤形、 立方形、 针形、 球形、 链锁型及 无定型等形态及表面改性的品种达 5 O余种。 美国着重于超 细碳酸钙在造纸和涂料上的应用,英 国则主要从事填料专 用超细碳酸钙 的研制, 2 年来英国在汽车专用塑料用碳 近 O 酸钙中占垄断地位。我国从 8 O年代开始进行超细碳酸钙的 研究, 上海碳酸钙厂等单位已研制、 生产 出了几种不 同型号 的超细碳酸钙产品,但品种少 、 产量低、生产工艺及设备落 后, 高档产 品主要依靠进 口。加强研制和开发新的高档纳米 级超细碳酸钙产品的生产工艺及设备 ,是我国碳酸钙 工业 发展的重要 目标 。 间歇鼓泡碳化法工艺流程如下: 石灰、 水一化灰池一熟 浆池一碳化塔一浆池一脱水一千燥 一过筛一成品 生产纳米级碳酸钙是在生产轻质碳酸钙的基础上,改 变碳化工艺 ( 加入结晶控制剂) 控制形和粒径, 经沉淀 ( 加沉 淀剂) 再经分离、 干燥、 粉碎、 包装制得不同晶形, 大小均匀 的 纳米级超细碳酸钙。 连续喷雾多段碳化法与间歇鼓泡碳化法相 比,连续喷 雾多段碳化法适应于连续大规模生产, 生产能力大, 且生产 效率高 , 碳化时间短、 产品晶形、 粒度易控制, 可制得优质稳 定的纳米级超细碳酸钙 。 连续喷雾多段碳化法是气液反应, 制备方法大致如下: 6 数字 化整正的优点和特点 () 1 数据化整正可以真正做到有的放矢, 克服支柱整正 的盲目性, 能够提前判 定支柱位置的适用性 : () 2 消除了线坠测量整正法对天气的依赖和影响; ( )避 免了线坠测量经验不足和水平差异对支柱整正 3 标准的影响, 利于标准化施工 ; ( )提 高了整正效率,避免了整正后限界不达标 的返 4 工, 可做到一次成优; () 5 较经纬仪测量更方便 、 经济、 劳动强度小 7 工程实测 此方法 目前 已在京广线和武襄线推广使用 。整正结果 满足验标要求 , 整正效果标准 、 统一、 美观 。整正过程高效、 可控 , 便于量化管理, 受到 了建设、 监理等单位 的一致好评 。
化学法制备超细碳酸钙

化学法制备超细碳酸钙钱海燕万永敏石防震张少明CaCO3是一种重要的无机化工产品。
由于价格低、原料广、无毒性,广泛地用作橡胶、塑料、纸张、涂料、牙膏等的填料。
全世界每年在纸张中CaCO3的用量约1100万t,占填料总量的60%以上,用于塑料的约150万t以上。
普通CaCO3用作填料仅起增容、降低成本的作用,而超细CaCO3(粒径小于0.1um)除了起到上述作用外,还具有补强作用。
粒径小于0.02um的碳酸钙产品,其补强作用可与白碳黑相比。
粒径小于0.08um且粗径分布很窄的碳酸钙,可用作汽车底盘防石击的涂料。
因此,超细碳酸钙的研制、开发受到国内外的关注。
粒径如此小的碳酸钙用机械粉碎法很难达到,一般采用化学合成法制得。
日本在超细碳酸钙的研制、生产、应用方面处于国际领先地位,现已有纺锤型、立方型、针型、球型、链锁型及无定型等形态及表面改性的品种达50余种。
美国着重于超细碳酸钙在造纸和涂料上的应用,英国则主要从事填料专用超细碳酸钙的研制,近20年来英国在汽车专用塑料用碳酸钙中占垄断地位。
我国从80年代开始进行超细碳酸钙的研究,上海碳酸钙厂等单位已研制、生产出了几种不同型号的超细碳酸钙产品,但品种少、产量低、生产工艺及设备落后,高档产品主要依靠进口。
加强研制和开发新的高档超细碳酸钙产品的生产工艺及设备,是橡胶、塑料制品、造纸等工业的迫切要求,也是我国碳酸钙工业发展的重要目标[1-2.5]化学法制备超细碳酸钙主要利用Ca(OH)2连续碳化法和间歇碳化法。
本文主要研究间歇碳化法制备超细碳酸钙。
1.实验部分化学法制备碳酸钙的反应式为Ca(OH)2+CO2→CaCO3↓+H2O在实验过程中,可控制的条件有:①氢氧化钙的浓度;③二氧化碳的质量分数;③添加剂的种类、数量和添加时间。
从化学反应速率和碳酸钙成核机理角度考虑,又存在两个可控因素:④搅拌速率;⑤反应温度。
从以上可控因素入手,选择①、②、③、④共4个控制因素进行对比实验。
超细碳酸钙的制备方法

近年来,随着碳酸钙的生产技术不断发展,从而提升其应用价值。
由于一些技术被国外垄断,我国也在不断改进生产工艺,就目前主要的一些制备方法给您举例说明一下。
我国对于超细碳酸钙的制备和生产方法大体可分为以下几种:(1)间歇鼓泡碳化法目前国内在多数厂家采用此法来生产轻质碳酸钙,根据碳化塔中是否有搅拌装置,该法又可分为普通间歇鼓泡碳化法和搅拌式间歇鼓泡碳化法。
该法是在锥底圆柱体碳化塔中加入精制氢氧化钙悬浊液和适当的添加剂,然后从塔底通入二氧化碳碳化之终点,得到所要求的碳酸钙产品。
在反应过程中需要严格控制反应条件,如碳化温度、二氧化碳流量、石灰乳浓度及搅拌速度,并加入适当的添加剂。
该法投资少、操作简单,但生产不连续,自动化程度低,产品质量不稳定,主要表现在产品晶形不易控制、粒度分布不均、不同批次产品的重现性差。
(2)连续鼓泡碳化法国内有些碳酸钙生产厂家可以根据用户的需求,通过严格控制石灰乳浓度、碳化温度、添加剂的类型和配比等来生产所需晶形和粒径的产品。
连续鼓泡碳化法一般采用两级或三级串联碳化工艺,即精制石灰乳经第一级碳化塔进行部分碳化或得到反应混合液,在浆液槽中加入适当的添加剂后进入第二级碳化塔碳化制得最终产品。
该法由于碳化过程分步进行,采用级间进行表面活性处理,可通过制冷来控制碳化温度,因此对晶形的成核、生长过程和表面处理分段控制,从而可得到较好的晶形、较小的粒径和粒径分布。
(3)连续喷雾碳化法连续喷雾碳化法一般采用三级串联碳化工艺。
精制石灰乳从第一级碳化塔顶部喷雾成0.01-0.1mm的液滴加入,二氧化碳从塔底通入,二者逆流接触发生碳化反应。
反应混合液从塔底流出,进入浆液槽,添加适当的分散剂处理后,喷雾进入第二级碳化塔继续碳化,然后再经表面活性处理、喷雾进入三级碳化塔碳化制得最终产品。
其产品粒径可达40-80nm。
(4)超重力反应结晶法该技术的特征是以强化气液传质过程为基本出发点,其核心在于碳化反应是在超重力离心反应器(旋转螺旋或填充床反应器)中进行,利用填充床高速旋转产生的几十到几百倍重力加速度,可获得超重力场环境,并通过CO2和Ca(OH)2悬浊液在超重力专用设备中逆流接触,使相间传质和微观混合得到极大强化,为CaCO3均匀快速成核创造了理想环境。
一种从蚝壳中制备超细碳酸钙的方法

一种从蚝壳中制备超细碳酸钙的方法
将蚝壳经过一系列的处理步骤可以制备超细碳酸钙。
以下是一种常见的蚝壳制备超细碳酸钙的方法:
1. 收集蚝壳:从海洋或水产加工工厂获得新鲜的蚝壳。
确保蚝壳没有杂质或污染物。
2. 清洗蚝壳:将蚝壳放入清水中浸泡数小时,用刷子或手套清洗,去除蚝壳表面的污垢。
3. 烘干蚝壳:将清洗干净的蚝壳排放在烘干机中,以适当的温度和时间进行烘干。
确保蚝壳完全干燥。
4. 研磨蚝壳:将烘干后的蚝壳放入研磨机中进行研磨,直到获得所需的细碎度。
可以使用不同尺寸的研磨球来控制粒径。
5. 筛选:通过筛网将研磨后的蚝壳颗粒进行筛选,分离出所需尺寸的颗粒。
6. 分散:将筛选后的蚝壳颗粒放入分散器或搅拌器中,加入适量的溶剂(如水或有机溶剂),搅拌分散,使其成为均匀的浆液。
7. 沉淀:将分散的蚝壳浆液放置一段时间让其静置,使碳酸钙颗粒逐渐沉淀到底部。
8. 离心分离:将静置后的蚝壳浆液进行离心分离,分离出上清
液和沉淀物。
9. 干燥沉淀物:将沉淀物取出并进行烘干,以去除多余的溶剂。
10. 碾磨:将烘干后的沉淀物进行碾磨,以获得更细的超细碳
酸钙粉末。
11. 过筛:将碾磨后的碳酸钙粉末通过筛网进行过筛,去除较
大的颗粒。
12. 包装储存:将超细碳酸钙粉末装入密封容器中,储存使用。
注意:制备超细碳酸钙的过程中需要注意防止污染物的引入,同时要注意操作安全,如佩戴适当的防护设备。
超细碳酸钙的制备

一.超细碳酸钙的制备来源:世界化工网全文请访问:/睡过站了超细碳酸钙是白色粉末,粒径小(0.02~0.08μm),粒径大小均匀,比表面积大.制备超细碳酸钙的方法很多,可以以天然产出的石灰岩,大理石等为原料,通过机械粉碎,物理分离等方法制造;也可以通过化学反应合成碳酸钙产品.当然,天然产出的碳酸噶中常含有镁,铁等杂质,但其成本低;合成碳酸钙的纯度高,粒径控制好,虽其成本高,但质量可以得到保证.下面讨论超细碳酸钙的合成制备.1.合成方法将一定量的经粉碎至60目的生石灰加入到温度为80~90℃的水中,保温搅拌一定时间后,室温陈化若干小时,加入稀释到所需体积,过120目筛,加入结晶控制剂,充分搅拌,即得到一定浓度的氢氧化钙乳液(俗称石灰料浆).将此料浆转移都反应器中,控制所需温度(15~30℃),通过一定压力的二氧化碳和空气的混合体,搅拌,待反应达到终点时(pH=7.0),放出熟浆(必要是进行改性处理),过滤,烘干,即得白度较高的超细碳酸钙.2.合成条件的选择(1)温度在氢氧化钙乳液浓度,二氧化碳气流量及总气量保持不变时,反应达到终点的时间(t)与温度(T)的关系图如图所示,随着1/T增大(T减小)反应时间越长.对于该反应,升高温度,反应速率加快,到达终点的时间缩短.超细碳酸钙的粒径也与反应温度有关,随着反应温度的升高,合成超细碳酸钙的粒径增大.在温度为15~30℃时得到的碳酸钙粒径范围在0.02~0.1μm之间.(2)氢氧化钙乳液浓度当温度和二氧化碳总气体流量保持不变时,反应到达终点所需时间与氢氧化钙乳液的浓度成直线关系.石灰料浆的浓度越大,反应到达终点所需的时间越长.(3)二氧化碳气体流量当温度与CaO量保持不变时,随着二氧化碳在总气体流量中的百分含量减少,反应到达终点所需的时间增加.3.合成工艺过程分析合成超细碳酸钙反应时比较容易控制的,合成产品的质量与温度,浓度,气量及操作都有关系.实验表明:①在一定量的结晶控制条件下,合成差西碳酸钙反应到达终点的时间,随碳化温度的升高而缩短,随氢氧化钙乳液浓度的增加而增加;随二氧化碳气体占总气体流量百分比的增加而呈减少趋势.②碳化温度在15~30℃,氢氧化钙乳液自4~6°Bé之间,二氧化碳占总气体流量百分比为18%~30%之间,合成制得的碳酸钙可以达到超细碳酸钙的标准.生石灰原料质量必须稳定.它的质量好坏对超。
超细碳酸钙的制备实验报告

班 级: 化 工 122 班 姓 名: XXX 学 号: 201200601047 组 员: XXX 、XXX 、XXX 指导教师: 乐 志 文 成绩评定:超细碳钙的制备实验一、实验目的1、了解轻质碳酸钙的用途及工业制备方法。
2、熟悉板框过滤机的结构和操作方法。
3、熟悉常压洞道式(厢式)干燥器的构造和操作。
4、测定恒压下干燥曲线。
5、测定恒压过滤操作时的过滤常数。
6、掌握过滤问题的简化工程处理方法。
二、实验原理1、轻质碳酸钙(CaCO3)是一种重要的无机粉体材料。
具有价格低、原料广、无毒无害等优点,被广泛应用于塑料、橡胶、造纸、涂料、油墨、化妆品等行业作为填料,起到增加体积、降低成本的作用。
研究表明,不同晶型、不同粒度碳酸钙具有不同性质,纳米级超细碳酸钙由于具有较大比表面,因而具有较好的补强特性。
轻质碳酸钙的生产方法有多种,有碳化法、纯碱(Na2CO3)氯化钙法、苛化碱法、联钙法、苏尔维(Solvay)法。
本实验采用碳化法,以生石灰CaO为原料,经消化、碳化、过滤、干燥、粉碎等步骤而成,涉及的主要反应为:用水消化氧化钙生成石灰乳:CaO+H2O=Ca(OH)2用二氧化碳碳化石灰乳生成碳酸钙沉淀和水:Ca(OH)+ CO2= CaCO3↓+H2O2待反应完成后用泵将完成液送至板框过滤机进行过滤,将所得的滤饼在洞道干燥机中干燥即可得到轻质碳酸钙成品。
2、成品的检测主要有以下两个方面内容:①重容:重是指其物体体积中所占有的重量,即用克/立方厘米表示。
重量与密度相关,密度大容重也大,密度小容重也小。
测定方法:准确称取n克干燥过的样品尽量碾碎,转移到量筒中,静置,观测其所占的体积。
②沉降体积:轻质碳酸钙沉降体积值含义:以定量水为连续相,定量碳酸钙为分散相,分散均匀后,一定时间内每克沉降物样品所占有的容积即为碳酸钙沉降体积值。
测定方法:准确称取n克干燥过的样品于烧杯中,加入适量去离子水,并搅拌均匀,转移到10mL或20mL的量筒中,静置,记录不同时刻沉降物所占体积。
振动磨超细粉碎碳酸钙的试验研究

制作碳酸钙的实习报告

实习单位:XX化工有限公司实习岗位:生产实习实习时间:2023年X月X日至2023年X月X日实习内容:碳酸钙生产工艺一、实习背景碳酸钙是一种重要的无机化工原料,广泛应用于建筑材料、橡胶、塑料、造纸、涂料、医药等领域。
为了更好地了解碳酸钙的生产工艺,提高自身的实践能力,我于2023年X月X日至2023年X月X日在XX化工有限公司进行了为期两周的生产实习。
二、实习过程1. 实习初期,我了解了碳酸钙的基本性质、应用领域以及生产过程中的注意事项。
通过与生产师傅的交流,我对碳酸钙的生产工艺有了初步的认识。
2. 实习中期,我参与了碳酸钙的生产过程。
具体如下:(1)原料准备:将石灰石破碎成小颗粒,经过筛选、烘干等工序,得到符合要求的原料。
(2)煅烧:将烘干后的原料送入高温炉中进行煅烧,使其分解成氧化钙和二氧化碳。
(3)磨粉:将煅烧后的氧化钙送入磨粉机进行磨粉,得到一定细度的碳酸钙粉。
(4)洗涤:将磨粉后的碳酸钙粉送入洗涤设备,去除其中的杂质。
(5)干燥:将洗涤后的碳酸钙粉送入干燥设备进行干燥,得到干燥的碳酸钙。
(6)筛选:将干燥后的碳酸钙粉送入筛选设备进行筛选,得到符合规格的碳酸钙。
3. 实习后期,我参与了生产过程中的质量控制工作。
在生产过程中,我对原料、设备、工艺参数等方面进行了严格把控,确保了产品质量。
三、实习收获1. 通过实习,我对碳酸钙的生产工艺有了全面的认识,了解了生产过程中的各个环节。
2. 在实习过程中,我学会了如何使用生产设备,掌握了生产过程中的操作技巧。
3. 实习过程中,我锻炼了自己的团队协作能力和沟通能力,提高了自己的实践能力。
4. 通过实习,我认识到理论知识与实际操作相结合的重要性,为今后的工作打下了坚实的基础。
四、实习总结本次实习让我受益匪浅,不仅提高了我的实践能力,还让我对碳酸钙的生产有了更深入的了解。
在今后的学习和工作中,我会将所学知识运用到实际生产中,为我国化工事业贡献自己的力量。
超细碳酸钙制备2015年指导书
超细轻质碳酸钙的制备【实验目的】1、综合了解超细碳酸钙生产原理、方法、工艺流程、参数控制、相关设备、原料和产品性能测定,培养学生动手能力、提高学生的综合素质和创新意识;2、掌握电导率仪、pH 仪、白度仪等的使用;3、了解碳化过程的特性及pH 值和电导率随时间的变化规律;4、掌握粉体材料密度、粒度、沉降体积等的测定;5、掌握石灰乳比重和浓度测定方法。
【实验原理】纳米超细粉体材料是目前研究开发的热点,本实验选择超细碳酸钙粉体材料制备为对象采用生石灰CaO 为原料,经消化、碳化、过滤、干燥、粉碎等过程制备超细碳酸钙,涉及的主要反应为:消化: CaO + H 2O → Ca(OH)2碳化: Ca(OH)2 + CO 2 → CaCO 3↓ +2H 2O +Q反应为放热反应,为控制产品粒径,需控制温度在<20℃。
【仪器试剂】1. 仪器pHS-3C 精密pH 计,DDS-Ⅱ电导率仪,WSD-Ⅲ固定探头式白度仪,WKB —1空气泵。
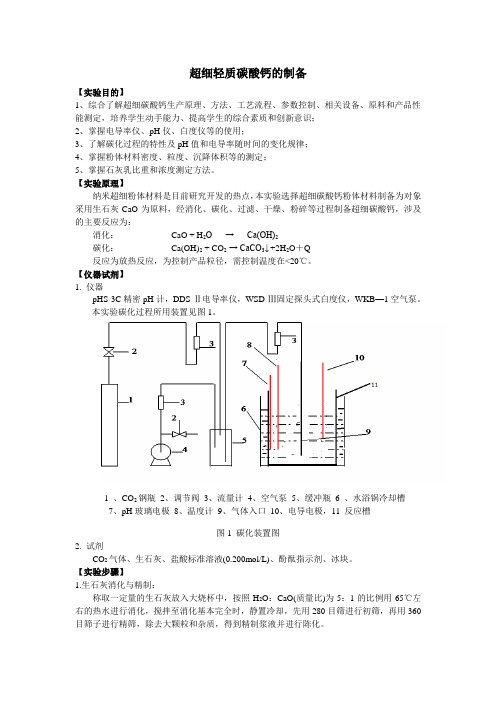
本实验碳化过程所用装置见图1。
图1 碳化装置图2. 试剂CO 2气体、生石灰、盐酸标准溶液(0.200mol/L)、酚酞指示剂、冰块。
【实验步骤】1.生石灰消化与精制:称取一定量的生石灰放入大烧杯中,按照H 2O :CaO(质量比)为5:1的比例用65℃左右的热水进行消化,搅拌至消化基本完全时,静置冷却,先用280目筛进行初筛,再用360目筛子进行精筛,除去大颗粒和杂质,得到精制浆液并进行陈化。
1 、CO 2钢瓶 2、调节阀 3、流量计 4、空气泵 5、缓冲瓶 6 、水浴锅冷却槽7、pH 玻璃电极 8、温度计 9、气体入口 10、电导电极,11 反应槽2.石灰乳测定(1)比重:将浆料搅匀后,移取25mL 石灰乳于25mL 容量瓶(质量已称)中,用天平称其质量w(g),计算其密度ρ(g/mL):25w ρ= (2)浓度:取5mL 石灰乳于250mL 锥形瓶中,加入2滴酚酞,用0.200moL/L 盐酸标准溶液滴至红色消失:+2+22Ca(OH)+2H H O+Ca =由消耗的盐酸量v (mL)计算石灰乳中 Ca(OH)2含量c (g/mL ):v 0.20074/25.00c ⨯⨯= 3.碳化将配制定量浓度(wB 为3%~10%)的Ca(OH)2悬浮液先进行预冷至20℃,加入到碳化反应器中,加入冰袋控制温度为20-25℃。
超细碳酸钙粉体的制备

超细碳酸钙粉体的制备任丽英;张群;李倩倩【摘要】以 CaCl2和(NH4)2 CO3为原料,采用气相扩散法合成碳酸钙晶体。
通过添加合适的晶形控制剂,选择适当的用量,合成了花生状碳酸钙晶体。
用发射扫描电子显微镜(FESEM)和 X 射线衍射仪(XRD)进行了表征,结果表明,当控制剂柠檬酸钠用量在10 mmol/ L 时,生成的花生状碳酸钙粒子粒度分布均匀,在700 nm 左右,且粒子分散性良好。
并对花生状碳酸钙粒子的形成机理进行了探讨。
%The CaCO3 particles were prepared using calcium chloride and ammonium carbonate by vapor diffusion method. Through adding right crystalline controlling modifiers and selecting right amount,the Ca-CO3 particles with peanut-like were synthesized. The particles were characterized by FESEM and XRD. The results indicated that when the amount of crystalline controlling modifiers( sodium citrate)was 10 mmol/ L,the calcium carbonate particles with peanut-like which size was uniform and about 700 nm were obtained,the particles decentralize was better. And the synthesis mechanism of CaCO3 particles with peanut-like was discussed.【期刊名称】《应用化工》【年(卷),期】2014(000)005【总页数】3页(P850-852)【关键词】晶形控制;合成;晶体生长;形貌【作者】任丽英;张群;李倩倩【作者单位】安庆医药高等专科学校药学系,安徽安庆 241052;安庆师范学院化学化工学院功能配合物安徽省重点实验室,安徽安庆 246003;安庆飞凯高分子材料有限公司,安徽安庆 246005【正文语种】中文【中图分类】TQ132.3+2生物体内存在各种各样的生物矿化材料。
超细碳酸钙的合成及结晶过程_诸葛兰剑

第27卷第2期硅酸盐学报Vol.27,No.2 1999年4月JOURNAL OF THE CHINESE CERAMIC SOCIETY April,1999超细碳酸钙的合成及结晶过程诸葛兰剑张士成韩跃新蒋军华(苏州大学分析测试中心)(东北大学资源与环境系)(苏州非金属矿产设计研究院)摘要首先在不加添加剂的条件下,对超细碳酸钙CaCO3的结晶过程进行了研究.结果表明,CaCO3的结晶过程是先形成线束状物,随着碳化反应的继续,线束状物断裂,最后得到粒径为40~70nm的立方颗粒.通过加入添加剂,分别合成了短链状和棒状CaCO3,并对它们的形成机理进行了分析.关键词碳酸钙,超细粒子,形状,合成中图法分类号O611不同行业对超细CaCO3的晶形有不同的要求.如油墨生产,需立方或球形;而橡胶行业,需针形或链状CaCO3.为了充分利用我国丰产的石灰石矿源,提高经济效益,对结晶过程及工艺条件对超细CaCO3晶形的影响进行研究,具有着实用价值.1实验方法用自来水将CaO(化学纯)消化,配成一定浓度的石灰乳.通入CO2气体(工业纯钢瓶气体),进行碳化反应,在搅拌反应器中进行.用DDS-11A数显电导率仪跟踪反应过程.根据电导率的变化在反应过程的不同阶段取样,取样点见图1的a,b,c,d,e点.以H-600透射电镜观察反应过程中不同阶段a,b,c,d,e点产物的形貌,研究CaCO3的结晶过程.同时以D/MAX-3C型X射线衍射仪检测反应进行的程度.最后在反应过程中加入添加剂A和B,见表1,研究添加剂对CaCO3形貌的影响.在通CO2气体30min后取样.2结果和讨论2.1C aCO3的结晶过程从图2所示的XRD图中可以清楚地看到,随着反应的进行,Ca(OH)2逐渐减少,CaCO3逐渐增多,到取样点d后,Ca(OH)2消失,只存在CaCO3.根据XRD分析,生成的CaCO3是方解石型.但从图1看,d点到e点,电导率略有上升的趋势,这可能是在d点反应完毕后(见XRD1998年4月6日收到.通讯联系人:诸葛兰剑,男,31岁,硕士,工程师,苏州大学分析测试中心,江苏省苏州市215006.图),产品全部是CaCO 3,继续通CO 2气体,有可能使少量CaCO 3转变为Ca(OH)2,使电导率略为上升,由于生成的Ca(OH )2数量较少,在XRD 图上没有反映出来.图1 电导率随反应时间的变化Fig.1 Variation of conductiv ity w ith r eactive time 图2 不同反应阶段的XRD 谱F ig.2 XRD patterns w ith var ious stag es of r eaction 从图3反应过程各个阶段的照片可看到,反应前,此时只存在Ca(OH)2,它是形状不规则的颗粒,见图3上标有/反应前0的分图.通入CO 2气体后,开始了CaCO 3的结晶过程.通入CO 2气体10m in 后,即达到取样点a,形成较多的线束状物,见图3a.随着反应继续进行,Ca(OH)2逐渐减少和CaCO 3逐渐增多,线束状物逐渐断裂、减少,见图3b 和图3c.通入CO 2气体25min 和30min 后即分别达到取样点d 和e.从图2知,此时只存在CaCO 3,相应从图3d 和图3e 的T EM 照片得知,线束状物消失,最后得到的是粒径40~70nm 的CaCO 3超细颗粒.从以上结果可得出,在反应前阶段,此时只存在Ca(OH)2,呈不规则形状,无线束状物,反应到d 点后,此时只有CaCO 3,是立方超细颗粒,也无线束状物.线束状物是在Ca(OH)2和CaCO 3共同存在的阶段出现的,这表明线束状物是由Ca(OH)2颗粒和CaCO 3颗粒所组成.在乳液中通入CO 2气体,产生的CO 2-3与Ca(OH )2颗粒表面的Ca 2+形成CaCO 3晶核,然后生长成微小颗粒.由于小颗粒是存在极性的晶体[1],它的表面活性较大,定向吸附溶液中存在的Ca(OH )2小颗粒,这样,交互定向吸附,就形成了线状物,而数条线状物吸附在一起,就形成了线束状物.随着反应的进行,Ca(OH)2逐渐减少,线束状物也随之断裂、减少.当Ca(OH )2完全消失,线束状物也完全消失,形成CaCO 3小颗粒,见图3d 和图3e.由于立方CaCO 3表面能最低,在自然界中最稳定[2].所以,在无外界干扰的情况下,最后得到的是立方CaCO 3超细颗粒.2.2 添加剂对CaC O 3晶形的影响添加剂分A,B 二种,其中A 为络合剂,B 为金属离子添加剂.由于添加剂需在晶体形核#160# 硅 酸 盐 学 报 1999年图3不同反应阶段的T EM照片Fig.3T EM photog raphs wit h various stages of reactio n或生长阶段加入或之前加入才能发挥作用,因此,设计了2个方案.试验1,A和B都在反应前(即通入CO2气体前)加入;试验2,A在反应前加,B在通CO2气体15min时(b点)加入.结果分别在通CO2气体30min后,得到棒状CaCO3和短链状CaCO3,见表1.表1添加剂对C aCO3形貌的影响Table1Inf luence of additive on CaCO3with various shapesNo.Additive A Additive B Shape Size/nm(b@l)T EM observati on(flowinggas CO2for30min)-1AddingbeforereactionAddi ngbeforereactionChai n_like40@150Fig.42AddingbeforereactionAdding at/b0pointBar_like20@150Fig.4#161#第27卷第2期诸葛兰剑等:超细碳酸钙的合成及结晶过程试验1:它们先络合反应成络离子BA.通入CO 2气体后,形成CaCO 3晶核,络离子BA 吸附在晶核某一晶面上,抑制了该晶面生长[3],在晶核生长过程中,使其沿某些方向择优生长,形成棒状CaCO 3超细颗粒,见图4a,颗粒的尺寸约40nm @150nm.图4 不同形貌CaCO 3的T EM 照片F ig.4 T EM photographs of CaCO 3with various shapes试验2:首先在反应前加入添加剂A 到Ca(OH )2乳液中,A 与乳液中的Ca 2+发生络合反应,使部分Ca(OH )2固体颗粒溶解,使乳液中Ca 2+浓度增加,通入CO 2气体一段时间后,会形成较多CaCO 3的晶核,同时,由于添加剂A 在CaCO 3晶核表面的吸附,降低晶核形成的能垒,从而得到更多的、粒径较小的稳定晶核.在通CO 2气体15min 后(即b 点)再加入金属离子添加剂B,B 与A 形成络离子亦被Ca -CO 3吸附.吸附了BA 络离子的晶面,其生长受到抑制,使其它晶面沿择优方向生长,形成链状CaCO 3,见图4b,尺寸约为20nm @150nm.3 结 论(1)石灰乳即Ca(OH )2乳液为形状不规则的颗粒,当通入CO 2气体25m in 后,产品中全部为半径约为40~70nm 的超细CaCO 3颗粒.存在由CaCO 3颗粒和Ca(OH )2颗粒粘附而成的形状为线束状的中间结晶过程.(2)在反应前加入络合剂A 和金属离子添加剂B 到Ca(OH )2乳液中,在通入CO 2气体30min 后,得到棒状CaCO 3颗粒,尺寸是40nm @150nm.(3)在反应前和通入CO 2气体15m in 后,分别加入络合剂A 和金属离子添加剂B 到Ca(OH)2的乳液中,则在通CO 2气体30min 后,得到短链状CaCO 3,尺寸约为20nm @150nm.苏州非金属矿产设计研究院对本工作提供了许多帮助,谨此致谢.#162# 硅 酸 盐 学 报 1999年参 考 文 献1 Yamada H,Hara N.T ransformation of amorphous CaCO 3in the s ystem of Ca(OH)2-H 2O-CO 2.Gypsum and Lime,1986,20(3):2212 Cui Aili,W ang Zi chen,Luo Yu,et al.Synthesis of ultrafine calcium carbonate with various shapes.c 96China-Japan Sympo -sium on Particuology,Bei jing,1996:164-1673 Reeder R J.Interaction of divalent cobalt,cadmium,and bari um w ith the calcite surface during layer grow th.Geoch emical et Cosmochimica Acta,1996,60(9):1543SYNTHESIS OF ULTRAFINE CALCIUM CARBONATEAND ITS C RYSTALLIZATIONZhuge Lanj ian(T esting and Analysis Center ,Suzhou U niversity)Zhang Shichen H an Yuex inJiang Junhua (Nort heaster n U niversit y)(Suzhou Designing and Resear ch Instituteof Nonmetallic M inerals Industr y)ABSTRAC T A t first,t he crystallizat ion of ultrafine calcium carbonate w ithout additiv e is investig ated.T he results show that CaCO 3crystals initially formed is in the shape of bundles.Such crystals can be broken with the progress of carbonation,and the cubic CaCO 3with the size of 40~70nm is finally obtained.T he chain_like CaCO 3and bar_like CaCO 3can be sy nthesized by adding addit ive.T he mechanism of synthesis is discussed.KEY WORDS calcium carbonate,ultrafine par ticle,shapes,synthesis.Received:April 6,1998.Correspon dent:Zhuge Lanjian,Testing and Analysi s Center,Suzhou University,Suzhou City of Ji angs u Province 215006.#163# 第27卷第2期 诸葛兰剑等:超细碳酸钙的合成及结晶过程。
超细纳米碳酸钙生产制备工艺方法及装置

超细纳米碳酸钙生产制备工艺方法及装置超细纳米碳酸钙(Ultrafine Nanometer Calcium Carbonate)是一种重要的无机功能材料,具有广泛的应用前景。
本文将介绍一种超细纳米碳酸钙的生产制备工艺方法及装置。
一、工艺方法超细纳米碳酸钙的制备方法主要包括化学合成法和物理法两种。
1. 化学合成法化学合成法是通过化学反应将溶液中的钙离子和碳酸根离子反应生成碳酸钙沉淀,再经过后处理过程得到超细纳米碳酸钙产品。
该方法具有反应速度快、操作简单、产量高等优点。
化学合成法的具体步骤如下:(1)将含有钙离子的溶液与含有碳酸根离子的溶液缓慢混合;(2)调节溶液的pH值,使之适合碳酸钙的形核和生长;(3)控制反应温度和时间,促进碳酸钙的沉淀和成长;(4)将沉淀物进行过滤、洗涤、干燥等后处理步骤。
2. 物理法物理法是通过机械研磨或超声波处理等物理力作用将粗颗粒的碳酸钙颗粒分散、破碎,最终得到超细纳米碳酸钙产品。
该方法具有工艺简单、设备投资少等优点。
物理法的具体步骤如下:(1)将粗颗粒的碳酸钙颗粒置于研磨机或超声波设备中;(2)通过机械作用或超声波作用,将碳酸钙颗粒逐渐破碎、分散;(3)控制研磨时间和超声波处理时间,使得颗粒尺寸逐渐减小;(4)对处理后的样品进行过滤、洗涤、干燥等后处理步骤。
二、装置介绍超细纳米碳酸钙的生产制备装置主要包括反应槽、控制系统、过滤系统、洗涤系统、干燥系统等组成部分。
1. 反应槽反应槽是实施化学合成法时的关键设备,用于混合含有钙离子和碳酸根离子的溶液,并通过调节pH值、温度等参数控制反应过程。
2. 控制系统控制系统用于监测和控制反应过程中的温度、pH值、搅拌速度等参数,保证反应条件的稳定性和一致性。
3. 过滤系统过滤系统用于从反应溶液中分离出碳酸钙沉淀,常用的过滤设备有压滤机、离心机等。
4. 洗涤系统洗涤系统用于对过滤后的碳酸钙沉淀进行洗涤,去除杂质和未反应的溶液。
5. 干燥系统干燥系统用于将洗涤后的碳酸钙沉淀进行干燥处理,得到最终的超细纳米碳酸钙产品。
超细轻质碳酸钙的制备及其测试表征_张珍一

第35卷第1期非金属矿Vol.35 No.1 2012年1月 Non-Metallic Mines January, 2012超细轻质碳酸钙是指原生粒子粒径在0.1~2 μm 之间的碳酸钙[1],由于其价格低廉、无毒性、白度高、补强性能优良,广泛用于橡胶、塑料、造纸、涂料等行业。
近年来,粉体技术取得了长足进展,尤其在粒径超细、晶体多样化等方面加快了研究开发[2]。
长期以来我国超细轻质碳酸钙主要依赖进口。
片状结构的超细轻质碳酸钙应用于塑料等行业,既能发挥碳酸钙原有性能,又能保持材料的力学性能。
因此,超细轻质碳酸钙制备技术的研究具有重要意义。
本实验对超细轻质碳酸钙制备技术中各工艺参数作了详细研究,确定出制备片状超细轻质碳酸钙的工艺。
1 实验部分1.1 原料、试剂及主要仪器氧化钙,山东淄博,工业级;六偏磷酸钠,潍坊华博化工有限公司,分析纯;草酸,博山昆山化工有限公司,分析纯;硫酸钠、硫酸锌,上海绿源化工,分析纯;二氧化碳、氮气,淄博压力容器厂,工业级;蒸馏水,自制。
DHG-9055A型电热恒温鼓风干燥箱,上海-恒科技有限公司;JSM-5900LV 型扫描电子显微镜(SEM);SC-80型全自动测色色差仪,北京康光仪器有限公司;Winner2066激光粒度分析仪,济南微纳仪器有限公司。
1.2 超细轻质碳酸钙的制备间歇鼓泡法制备轻质碳酸钙是在带有搅拌装置的碳化反应器中进行,通过搅拌来改善反应体系的传质、传热效果,同时在反应器外用循环冷却水进行冷却,以保证碳化反应在较低温度下进行[3],严格控制反应温度、搅拌速度、气体流量、灰乳浓度、添加剂的加入量和加入时间等工艺条件,可以制得平均粒径较小的轻质碳酸钙产品[4],通常反应温度控制在室温条件下,搅拌速度为300 r/min。
1.2.1 石灰的消化和石灰乳的精制:选择水灰质量比为(4.5~6)∶1,在70 ℃的水中消化40 min左右后,除杂、封口陈化1 h。
1.2.2 碳化过程:分A、B、C 3组进行碳化,A组不加任何添加剂,分别将波美度调成8~13,二氧化碳体积分数为20%~50%进行碳化;B组采取和A组相同的工艺流程,不同之处在于B组分别加入1.5%~3%的六偏磷酸钠、草酸、硫酸锌,加入时间分别在反应刚开始、反应进行到30 min (pH值为12.4)和反应后期(pH值为8.5),进行3次实验;C组同样分别以1.5%~3%的六偏磷酸钠、草酸、硫酸钠为添加剂进行3次实验。
化学法制备超细碳酸钙粉体的方法和工艺

化学法制备超细碳酸钙粉体的方法和工艺我呀,对这个化学法制备超细碳酸钙粉体这事儿可感兴趣嘞。
你知道碳酸钙不?就像那些石头啊,贝壳啊,里面都有这东西。
可这超细碳酸钙粉体,那可就不一样嘞。
我就去看那些个制备的方法和工艺。
那化学法啊,就像一个神秘的魔法世界。
我看到那些做实验的人,戴着眼镜,眼睛里透着一种专注劲儿,那眉毛有时候皱着,好像在跟那些化学试剂较劲儿似的。
周围的环境呢,实验室里摆满了瓶瓶罐罐,各种颜色的试剂在玻璃瓶里闪着光,有点像小时候看到的彩色糖豆,可我知道这玩意可不能吃。
这制备方法里啊,首先得选原料嘞。
有的原料看起来白白净净的,就像冬天的雪一样,可这时候还不是碳酸钙粉体嘞。
然后就是加各种化学试剂进去,这时候就开始发生神奇的反应嘞。
我看着那些溶液在容器里咕噜咕噜冒泡,就像水烧开了一样,可这泡泡里都是化学变化的奥秘。
那些个气泡一个一个往上冒,就像小鱼吐的泡泡,只不过这些泡泡带着未来碳酸钙粉体的希望。
我就问旁边一个看起来经验很丰富的老师傅,我说:“师傅,这反应要多久才能成嘞?”老师傅慢悠悠地说:“这可急不得,就像炖肉,火候不到,肉就不烂。
这化学反应啊,时间不到,碳酸钙粉体就制备不好。
”我听了觉得挺有道理。
这工艺里还有温度的讲究呢。
就像人穿衣服,不同的温度得穿不同的衣服。
这反应在不同的温度下,出来的碳酸钙粉体那也是不一样的。
有时候温度高一点,反应就像发疯了似的,变得特别快;温度低一点呢,就慢悠悠的,像个懒汉。
还有搅拌这个环节。
那搅拌的速度也是个大学问。
我看到那个搅拌器在容器里呼呼转着,那些溶液就跟着一起转,就像一群小朋友在围着圈跳舞。
如果搅拌得太快,溶液都要溅出来了;要是太慢呢,里面的东西又混合不均匀。
这化学法制备超细碳酸钙粉体啊,每一个步骤都像是一个关卡,每个细节都得注意到。
我在那看了半天,觉得这就像是一场精心编排的戏,每个演员(化学试剂、温度、搅拌等)都得在正确的时间做正确的事情,才能最后得到那超细碳酸钙粉体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
班级: 姓名: 学号: 组员:指导教师: 成绩评定:超细碳钙的制备实验化工122班XXX 201200601047 XXX XXX XXX 乐志文一、实验目的1、了解轻质碳酸钙的用途及工业制备方法。
2、熟悉板框过滤机的结构和操作方法。
3、熟悉常压洞道式(厢式)干燥器的构造和操作。
4、测定恒压下干燥曲线。
5、测定恒压过滤操作时的过滤常数。
6掌握过滤问题的简化工程处理方法。
二、实验原理1、轻质碳酸钙(CaC03)是一种重要的无机粉体材料。
具有价格低、原料广、无毒无害等优点,被广泛应用于塑料、橡胶、造纸、涂料、油墨、化妆品等行业作为填料,起到增加体积、降低成本的作用。
研究表明,不同晶型、不同粒度碳酸钙具有不同性质,纳米级超细碳酸钙由于具有较大比表面,因而具有较好的补强特性。
轻质碳酸钙的生产方法有多种,有碳化法、纯碱(Na2CO3 )氯化钙法、苛化碱法、联钙法、苏尔维(Solvay)法。
本实验采用碳化法,以生石灰CaO为原料,经消化、碳化、过滤、干燥、粉碎等步骤而成,涉及的主要反应为:用水消化氧化钙生成石灰乳:CaO+H 2O=Ca(OH)用二氧化碳碳化石灰乳生成碳酸钙沉淀和水:Ca(OH)+ CO2= CaCO 3 J +H2O 待反应完成后用泵将完成液送至板框过滤机进行过滤,将所得的滤饼在洞道干燥机中干燥即可得到轻质碳酸钙成品。
2、成品的检测主要有以下两个方面内容:①重容:重是指其物体体积中所占有的重量,即用克/立方厘米表示。
重量与密度相关,密度大容重也大,密度小容重也小。
测定方法:准确称取n克干燥过的样品尽量碾碎,转移到量筒中,静置,观测其所占的体积。
②沉降体积:轻质碳酸钙沉降体积值含义:以定量水为连续相,定量碳酸钙为分散相,分散均匀后,一定时间内每克沉降物样品所占有的容积即为碳酸钙沉降体积值。
测定方法:准确称取n克干燥过的样品于烧杯中,加入适量去离子水,并搅拌均匀,转移到10mL或20mL的量筒中,静置,记录不同时刻沉降物所占体积。
按下式计算沉降体积x:x (mL/g)=V/n工艺流程生石茨3.板式过滤的原理:过滤是利用能让液体通过而截留固体颗粒的多孔介质(滤布和滤渣),使悬浮液中固体、液体得到分离的单元操作。
过滤操作本质上是流体通过固体颗粒床层的流动,所不同的是,该固体颗粒床层的厚度随着过滤过程的进行不断增加。
过滤操作分为恒压过滤和恒速过滤。
当恒压操作时,过滤介质两侧的压差维持不变,单位时间通过过滤介质的滤液量不断下降;当恒速操作时,即保持过滤速度不变。
恒压过滤方程q2 2qqe = Kr (1)式中:q=V单位过滤面积获得的滤液体积(斥/卅);V――滤液体积(m3)AA――过滤面积(m2);q e――单位过滤面积上的虚拟滤液体积(m / m)二——实际过滤时间(s); K ——过滤常数(m2 / s)由式⑴得:計R令............................ ⑵式(2)表明,恒压过滤时二/q与q之间为线性关系。
实验中记录下不同过滤时间9内的单位面积滤液量q,将9 /q对q作图,可得一直线,其斜率为1/K,而截距为2q e /K。
I-園迢匕2—檢忘4-悔梅6—机按了一懵劝粗头板8—固至H丄版4. 洞道式干燥的原理:干燥是利用热量去湿的一种方法,它不仅涉及到气、固两相间的传热与传质, 而且涉及到湿分以气态或液态的形式自物料内部向表面传质的机理。
由于物料的含水性质和物料形状的差异,水分传递速率的大小差别很大,概括起来,它受到 物料及其含水性质,干燥介质的性质、流速,干燥介质与湿物料接触方式等各种 因素的影响。
按干燥过程中空气状态参数是否变化, 可将干燥过程分为恒定干燥 条件操作和非恒定干燥条件操作两大类。
本次实验采用恒定干燥条件操作。
干燥速率的定义为单位干燥面积(提供湿分汽化的面积)、单位时间内所除去式中:U --- 干燥速率,又称干燥通量,kg/(m 2s );A ――干燥表面积,吊; W ――汽化的湿分量,kg ;T --- 干燥时间,s ; G C 绝干物料的质量,kg ;X ――物料湿含量,kg 湿分/kg 干物料,负号表示X 随干燥时间的增加而减少。
干燥速率的测定方法:将湿物料试样置于恒定空气流中进行干燥实验,随着干 燥时间的延长,水分不断汽化,湿物料质量减少。
若记录物料不同时间下质量G, 直到物料质量不变为止,也就是物料在该条件下达到干燥极限为止, 此时留在物 料中的水分就是平衡水分X 。
再将物料烘干后称重得到绝干物料重 G C ,则物料中 瞬间含水率X 为:G -G c G c计算出每一时刻的瞬间含水率X,然后将X 对干燥时间T 作图,即为干燥曲线。
由已测得的干燥曲线求出不同X 下的斜率,再由式(3)计算得到干燥速 d i 率U,将UM X 作图,就是干燥速率曲线。
三、 实验仪器和药品主要药品:CQ 生石灰(CaO )、1.0%酚酞酒精指示剂、干空气主要仪器:消化池、泵、碳化塔、三级筛、旋液分离器、全数字板框过滤机、数字型洞道干燥机、波美度计、量筒、带磨口塞的刻度量筒等。
四、 实验步骤1、 生石灰消化称取一定量的生石灰放入消化池中,按照H 2O : CaO (质量比)为5: 1的比例用80C 左右的热水在消化池进行消化,搅拌至消化基本完全时,静置冷却 60mi n ,再搅拌10min 后就可以放出石灰乳。
2、 石灰乳的精制用冷水将粗灰乳的浓度调和到约13Be 后,用泵将粗灰乳送入三级筛过筛,然 后再送入旋液分离器再次进行分离,得到精制石灰乳并进行陈化。
的湿分质量即:UdW AdG C dX Ad .(3)(4)3、碳化将配制定量浓度12Be的Ca(0H)2悬浮液先进行预冷或加热至某温度(10〜40C),加入到碳化塔中,前期控制温度(如加入冰袋控制至30-40 C)。
然后通入CO2和空气的混合气体(其中CO2气体为100ml/h,空气为250ml/h左右),在反应后期温度控制在50-60C。
从碳化塔底部的采样口先放掉沉积在管口内的悬浮液后,再放出约100ml 的悬浮液与500ml的烧杯中,静置约一分钟后向悬浮液中滴入2滴1.0%酚酞酒精指示剂并振摇,若呈红色则碳化未完全,若无色则到达终点,应该测两次。
然后再碳化10min后停止。
4、过滤(板框过滤机)过滤温度应在50E以上,在配浆糟中加入CaCO3和一定量的水配制成CaCO3 含量为8%〜10%质量)的滤液。
按板框的编号顺序排列过滤机的板与框。
装滤布时,须把滤布用水浸透,再将湿滤布盖在滤框的两侧,滤布孔要对准过滤机的孔道,表面要平整不起皱纹,然后压紧螺杆和板与框。
调节贮浆罐前后各阀门开启状态。
用将滤浆送入浆罐,当滤浆高度达到浆罐的3/4左右时,关闭送料阀,然后停进料泵。
在压力调节阀开启的状态下,启动空压机,开启压缩空气进气阀,向系统输送压缩空气。
检查有关调节阀的开启状态,用容器接滤出口处的滤液,打开滤液出口阀,开启滤液进口阀,开始过滤。
滤速渐慢呈滴状流出时,停止过滤操作。
洗涤,开启进水阀向洗水罐加一定量的水,进行洗涤操作。
涤完毕后,关闭有关的阀门,旋开压紧螺杆并将板滤拉开,卸出滤饼,清洗滤布,整理滤板。
实验结束,立即用压缩空气将贮料罐内的剩余悬浮液压回配浆灌及其液位计等清洗干净。
5、干燥(洞道式干燥器)调节好各项参数,检查天平是否正常。
待空气状态稳定后,打开干燥室门将湿产品放入。
观察天平,记录下质量每减少0.1g时所用的时间,当质量稳定时,即30min后质量不再减少时,停止干燥。
干燥结束后,将样品取出,后再放入干燥室称重,记录秤盘的重量。
实验结束后,先关闭加热器再关风机。
6、沉降体积测量测定方法:确称取10.0克干燥过的样品于烧杯中,加入适量去离子水,并搅拌均匀,转移到10ml或20ml的量筒中,静置,记录不同时刻沉降物所占体积。
按下式计算沉降体积x:X (mL/g)=V/10. 0 (mL/g)7、容重测量测定方法:确称取10.0克干燥过的样品尽量碾碎,转移到量筒中,静置,观测其所占的体积。
X 唔(g/cm3) 本实验流程如下所示: 五、实验数据记录1、超细碳酸钙的过滤实验数据记录测量知压滤板板框边长为11.7cm,宽为6.8cm ,则圆的半径r 为表1滤液量随时间的变化情况表序号滤液量(ml时间 1 1000 0 '10〃 81 2 2000 0 '29〃 53 3 2500 0 '43〃 23 4 3000 0 '59〃 5 5 3500 1'19〃 932、轻质碳酸钙的干燥实验数据记录物料盘直径D=8.40cm 空盘质量:69.0g ,湿物料+空盘质量:79.0g表2轻质碳酸钙的干燥数据记录序号物料质量(包括托盘)G/g时间T /S序号物料质量(包括托盘)G/g时间T /S1 79.0 0' 00〃 00 21 77.0 13' 15〃 82 78.9 0' 49〃 9 22 76.9 13' 58〃 23 78.8 1' 13〃 1 23 76.8 14' 31〃 54 78.7 1' 49〃 6 24 76.7 15' 21〃 45 78.6 2' 56〃 0 25 76.6 15' 43〃 2 6 78.5 3' 18〃 1 26 76.5 16' 30〃 27 78.4 3' 51〃 2 27 76.4 17' 03〃 58 78.3 4' 30〃 8 28 76.3 18' 07〃 39 78.2 4' 55〃 5 29 76.2 19' 16〃 3 10 78.1 5' 35〃 0 30 76.1 20' 19〃 7 11 78.0 6' 30〃 9 31 76.0 20' 40〃 5 12 77.9 7' 01〃 1 32 75.9 22' 13〃 8 13 77.8 7' 41〃 8 33 75.8 23' 28〃 7 14 77.7 9' 00〃 8 34 75.7 24' 26〃 2 15 77.6 9' 24〃 4 35 75.6 29' 00〃 6 16 77.5 9' 55〃 3 36 75.5 34' 57〃 2 17 77.4 10' 45〃 33775.443' 35〃 318 77.3 11 ' 26〃91977.2 11 ' 50〃2077.112'30〃111. 7 - 6.8=2. 45cm实验到2615.3s 后,物料质量保持75.4g 在10min 之内不变,可认为达到干 燥极限,停止干燥。
