课题3溶液的浓度ppt课件
合集下载
溶液的浓度ppt课件

3. 量取:用量筒量取所需的水(水的密度近似看做1g/cm3),倒入盛有 氯化钠的烧杯中。
4. 溶解:用玻璃棒搅拌,使氯化钠溶解。 5. 装瓶,贴签(质量分数和溶液名称)。
3 配制一定溶质质量分数的溶液
实验1:用氯化钠配制配制50g溶质质量分数为6%的氯化钠溶液
计算:溶质 和溶剂的量
称量:溶质质量 量取:溶剂体积 溶解
Ⅱ 有关溶质质量分数的计算
2 有关溶质质量分数的计算
用固体药品配制溶液的计算
例1:在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。 现要配制150 kg的这种溶液,需要氯化钠和水的质量各是多少?
解:溶质质量=溶液质量×溶质的质量分数 =150 kg×16% =24 kg
溶剂质量=溶液质量-溶质质量 = 150 kg-24 kg = 126 kg
充分溶解后,所得溶液的溶质质量分数是多少?
溶解度
溶质的质量分数= 100g+溶解度
×100%
100g水 ~ 0.17g Ca(OH)2 200g水 ~ ? Ca(OH)2
0.34g
= 0.17g 100g+0.17g
= 0.17%
×100%
该温度下200g水中只能溶解0.34g Ca(OH)2固体,溶液即饱和。
3 配制一定溶质质量分数的溶液
实验2:用6%氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液
v mρ 1. 计算: 6%氯化钠溶液 =
6%氯化钠溶液 = 25g
≈ 24ml
6%氯化钠溶液
1.04g/cm3
v m 水 = 加入水 = 50-25g = 25ml
ρ水
1g/cm3
2. 量取:用量筒量取所需的6%氯化钠溶液和水,倒入烧杯中。
课题3溶液的浓度ppt

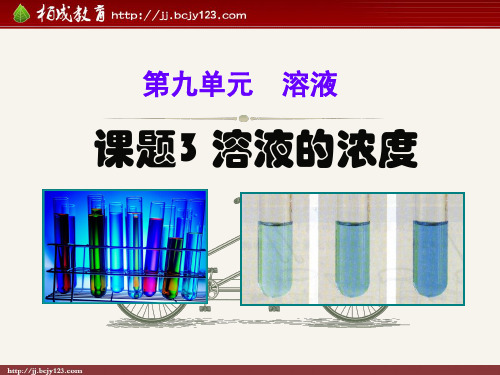
[2011]4蔗糖是生活中常用的调味品, 其溶解度曲线如下图。 下列说法正确的是【 B 】 A、蔗糖在热水中的溶解度比 在冷水中的小 B、将蔗糖饱和溶液蒸发溶剂后 恢复至原温度,有结晶现象 C、温度升高,溶液中蔗糖的质 量分数一定增大 D、t1℃和t2℃时的两份蔗糖溶液, 所含溶质的质量不可能相等
[2010]3KCl是一种常用钾肥,其溶解度如下表。下列说 法正确的是( D ) 0 20 40 60 温度/℃ 34.0 40.0 45.5] 溶解度/g 27.6 A.KCI饱和溶液中不能再溶解其他物质 B.20℃时,100 g KCl饱和溶液中含KCI 34.0 g C.40℃时,KCl饱和溶液的质量分数为40.0% D.60℃的KCl饱和溶液降温至20℃,有晶体析出
稀硫酸中硫酸的质量分数 =
9 .8 g 100%=9.8% 100 g
答:生成氢气0.2g,稀硫酸中溶质的质量分数为9.8%。
4:40g10%NaOH溶液跟多少克10%盐酸完全反应? (NaOH + HCl = NaCl + H2O) 解:设稀盐酸的质量为X
NaOH + HCl = NaCl + H2O 40 36.5 40g10% X . 10%
练习:3(课本P45)某温度时,蒸干35g氯化钾溶液, 得到7g氯化钾,求该溶液中溶质的质量分数。
溶质质量 【解】 溶质的质量分数= ×100% 溶液质量 7g 溶质的质量分数 = × 100% = 20% 35g 答:该溶液中溶质的质量分数为20%
练习:4(课本P45)配制500mL质量分数为10%的氢氧化钠溶液 (密度为1.1g/cm3),需要氢氧化钠和水的质量各是多少?
浅 较深 深
20g 20g
0.1g 0.5g
人教版九年级化学下册第9单元《溶液-溶液的浓度》课件
再把该溶液分为四等份,每一等份分别进行 如下操作,求所得溶液中溶质质量分数。
1.加入10g水
2.加入10g硝酸钾且全部溶解
3.蒸发10g水且无晶体析出
4.加入100g10%的硝酸钾溶液
2、有关体积的计算
练习1:配制500g 20%的稀盐酸,需要38%的浓盐酸和水各多少克? 换算成体积,各多少毫升?(38%的浓盐酸的密度1.19g/cm3)
一、溶质的质量分数
1、定义:溶质质量与溶液质量之比 2、公式: 单位要 统一
溶质质量 ×100% 溶质的质量分数 = 溶液质量 溶质质量 = ×100 % 溶质质量 + 溶剂质量
溶质质量 = 溶液质量× 溶质的质量分数
溶液的质量 = 溶质的质量/ 溶质的质量分数
溶液的“浓”和“稀”与质量分数的关系——溶液越 浓, 溶质质量分数越大。
第九单元
溶液
课题3 溶液的浓度
正确理解“浓”和“稀”溶液
试管编 号 溶液颜色 比较 溶剂质量 /g 溶质质量/g 溶液质量/g
1 2 3
浅蓝色 蓝色 深蓝色
20
20 20
0.1
0.5 2
20.1 20.5 22
归纳:对有色溶液来说,根据颜色深浅可以区分溶液是浓还 是稀。
1.溶液是否饱和与浓稀没有必然联系,即浓溶液 不一定是饱和溶液,稀溶液也不一定是不饱和溶 液。 2.相同温度下,同种物质的溶液,饱和的比不饱 和的溶液浓。 3.用浓稀溶液不能准确的表示一定量的溶液里含 溶质的多少。实际应用时,通常需要准确知道一 定量的溶液里含溶质的量——即溶液组成的确切 表示。 4. 溶液组成的表示方法很多,通常用溶液中溶质 的质量分数来表示溶液的组成。
《溶液的浓度》PPT课件

×100 %
溶质质量 =
×100 %
溶质质量 + 溶剂质量
思考与交流 “5%的NaCl溶液”的含义
食盐的质量占整 个溶液质量的5%
100g食盐溶液中 含有食盐5g
每5g食盐溶于95g 水形成的溶液
m食盐:m水:m食盐溶液 =5:95:100
练一练
在实验9 – 7 中三种硫酸铜溶液的溶质的质量分数各是多少?把 计算结果填在表中。
Ag×a% = Bg×b% (稀释前) (稀释后)
课堂小结
溶质的质 量分数
概念 公式
溶质质量与溶液质量之比
溶质质量
溶质的质量分数=
×100% 溶液质量
简单计算
溶质质量分数的简单计算 溶液的稀释
随堂训练
1.下列几种硝酸钾溶液中溶质的质量分数最大的是( D )
A.150g水溶解30g硝酸钾 B.15g硝酸钾溶解在85g水中 C.85g硝酸钾溶液中含有15g硝酸钾 D.一定量的硝酸钾溶于80g水中制成100g硝酸钾溶液
烧杯编号
溶液颜色 比较
溶剂质量 /g
溶质质量 /g
溶液质量 /g
溶质的质 量分数
1
浅
20
0.1
20.1
0.05%
2
较深
20
0.5
20.5
2.44%
3
深
20
2
22
9.09%
实验 9 – 8 配制两种质量分数不 同的氯化钠溶液
溶质 质量/g
10
溶剂(水) 质量/g
90
现象
氯化钠 溶解
溶液中溶质 的质量ห้องสมุดไป่ตู้数
4.某食品加工厂生产的酱油中氯化钠的质量分数为15%~18%, 该厂日产酱油15 t。试计算该厂每月(按30天计)消耗氯化钠的 质量。
溶液的浓度课件(1、2课时)
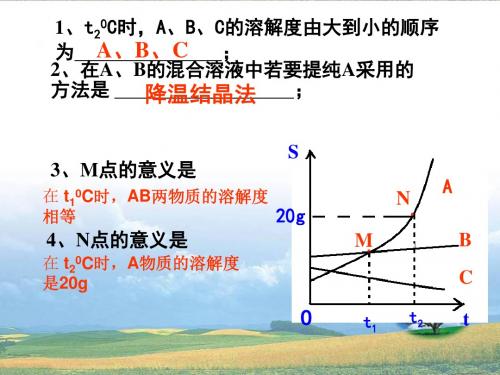
=
= =
在溶质的质量分数计算中要注意哪些 问题呢?
烧杯编号 1 2 3
溶液颜色比较
溶剂质量/g
溶质质量/g
溶液质量/g
溶质的质量分数
浅蓝 蓝色
20
0.1 0.5
20.1 20.5
0.4% 2.4%
20 20
深蓝
2
22
9%
氯化钠 的质量
水的质量
氯化钠溶 液的质量
0克
1、计算 2、量取 3、混匀 4、装瓶贴标签 课本47页: 用已配好的质量分数为6%的氯 化钠溶液(密度约为1.04g/ml),配制50g质 量分数为3%的氯化钠溶液? 计算: 需5%的食盐溶液的体积为:
50 g× 3% / (1.04g/ml × 6% )=24.0ml 需水: ( 50 g–24.0ml × 1.04g/ml )/ 1g/ml = 25.0ml
量取: 用量筒分别量24.0 ml 6%的食盐溶液和25.0ml水 混匀: 将24.0 ml 6%的食盐溶液倒入烧杯中,加入 25.0 ml 水,玻璃棒搅拌均匀。 装瓶贴标签:
实验仪器:量筒、 胶头滴管、烧杯、玻璃棒
当 堂 检 测 第九单元
溶液
小刚同学在做一定溶质质量分数的氯化钠溶液的配
制实验时,其配制过程如图S5-3所示。
答:略
三、跟化学方程式有关的溶质 质量分数的计算
溶液中发生的反应,实质上溶质之间 的反应,因此,代人化学方程式的是 溶质的质量
下面哪种解法正确? 实验室用100g稀硫酸和多少g锌恰好完全 反应可制得0.8g氢气。
A解:设所需锌的质量为 X B解:设所需锌的质量为 X
H2SO4 + Zn = ZnSO4 + H2 98 65 100g X
人教版九年级第九单元课题3 溶液的浓度(34张)

溶解度
固体的溶解度表示在一定温度下, 某固态物质在100 g溶剂里达到饱 和状态时所溶解的质量。
溶质质量 S= 溶剂质量 100g (溶质的质量和溶剂的质量指的是 饱和溶液中溶质和溶剂的质量)
必须指明
溶质的质量分数
溶质的质量分数 是溶质质量与溶 液质量之比。
溶质质量
a%= 溶液质量 100%
可以不指明
体积分数
氧 气(O2) (21%)
稀有气体 (0.94%)
(0.03%) 二氧化碳
(CO2)
其他气体
杂质
(0.03%)
【补充例题1】100g某硫酸溶液恰好与13g锌完全反应。试计算:
①这种硫酸溶液中溶质的质量分数。②反应后所得的溶液中溶质
的质量分数是多少?
方法一
【解】设:这种硫酸溶液中溶质的质量为x,生成ZnS04的质 量为y,生成H2的质量为z。
课前热身
课前加油站 ——神奇的海
同学们,你们听说过死海吗?请看几幅在死海中游泳的图片:
为什么人可以漂浮在水面上? 盐份多,浓度大。
我们都有这样的生活经验:在两 杯等量的水中分别加入1勺糖和2勺糖, 完全溶解后两杯糖水的甜度是不同的, 通俗地说就是这两杯水的浓、稀不同。 那么,在化学中如何定量地表示溶液 的浓、稀呢?
44
x
x8.8g
通常指温度为0℃和压强 为1标准大气压的情况。
这些二氧化碳在标准状况下的体积是:8.8g÷1.977g/L=4.45L
答:生成二氧化碳的质量是8.8g,这些二氧化碳在标准状况 下的体积是4.45L。
(经典教学PPT)人教版九年级第九单 元课题 3 溶液的浓度(共34张PPT)-导学课件( 示范)
说:“20 ℃时氯化钠饱和溶液中溶质的质量分 数为36%。”这种说法对吗?为什么?
第九单元 课题3 溶液的浓度 课件九年级化学人教版下册(共19张PPT)

解:设参加反应的稀硫酸中溶质质量为x 。
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g x
注意点:溶液是混合物,溶液的 质量不能直接代入化学方程式中
65 98
13xg
计算,必须换算成溶质的质量。
参加反应的稀硫酸的质量分数为:1190.06gg 100% 19.6%
答:参加反应的稀硫酸的质量分数为19.6%
答:略
(2)用稀溶液稀释:
例2:用溶质质量分数为60%的NaCl溶液和25%的NaCl溶液混合配制 45%的NaCl溶液1400g,问各取多少克?
解:取质量分数为60%的NaCl溶液质量为x,
25%的NaCl溶液质量为y.
60%x + 25%y = 1400 x 45%
x + y = 1400
解得: x= 800g y= 600g
二、配制一定溶质质量分数的溶液
配制50g质量分数为6%的氯化钠溶液。
烧杯,玻璃棒
药匙
托盘天平
量筒,胶头滴管
(1) 计算: (2)称量: (3)量取:
需氯化钠 3 g;水 47 mL;
用天平称量所需氯化钠的质量; 用量筒量取所需水的体积;
(4)溶解:
将氯化钠和水放入烧杯中,用玻璃棒搅拌
(5)装瓶贴标签:
课题3 溶液的浓度
一、溶质的质量分数 二、配制一定溶质质量分数的溶液
生活中有哪些表示溶液浓度的方法?
每100ml溶液中含溶质体积 如:某白酒的酒精度为 38%
每100 ml溶液中含溶质的质量 如:生理盐水浓度为0.9%
每100g溶液中含溶质的质量 如:某氢氧化钠溶液浓度10%
溶液的浓度 =
第九单元 课题3 溶液的浓度-2020年秋人教版九年级下册化学作业课件 (共17张PPT)

___不__变_______。
课时2 根据化学方程式进行溶质质量分数 相关的计算(拓展)
夯实基础 1. 实验室利用某过氧化氢溶液制取氧气,向 100 g 过氧化氢溶液中加入5 g 的二氧化锰, 充分反应后,过滤,得到滤液97.2 g,则原过氧 化氢溶液中氢元素的质量分数是( A )
A. 10.8%
____5_0_%______。
能力提升 3. 某化学小组同学为了测定实验室一瓶稀盐酸 中溶质的质量分数。他们用石灰石和此稀盐酸完 成了如图K9-3-2所示的实验。
(1)恰好完全反应时生成二氧化碳的质量是 __4_._4_____g。 (2)计算该瓶稀盐酸中溶质的质量分数。
解:设该瓶稀盐酸中溶质的质量为x。
CaCO3+2HCl==CaCl2+H2O+CO2↑
73
44
x
4.4 g
x=7.3 g
该瓶稀盐酸中溶质的质量分数为 ×100%=7.3% 答:该瓶稀盐酸中溶质的质量分数为7.3%。
4. 取50 g炉渣(含24%CaSO3)逐滴加入20%的盐 酸,请在图K9-3-3坐标中画出相应的曲线图。横 坐标为盐酸的质量,纵坐标请设定具体物质;并 标出曲线中必要的数据(写出计算过程)。
【已知】①设炉渣已不含石灰石,炉渣其他成分 不与盐酸反应;②CaSO3和盐酸反应类似于CaCO3。
解:设反应消耗盐酸中溶质的质量为x。 CaSO3 + 2HCl==CaCl2+SO2↑+H2O 120 73
50g×24% x
x=7.3 g
反应消耗盐酸溶液的质量为
=36.5 g
恰好完全反应时剩余固体的质量为
(2)一定温度下,向NaCl的饱和溶液中加入 NaCl固体,NaCl溶液的溶质质量分数___不_变____; 若采用升温蒸发溶剂的方法析出晶体后剩余溶液 的溶质质量分数____增__大______。
课时2 根据化学方程式进行溶质质量分数 相关的计算(拓展)
夯实基础 1. 实验室利用某过氧化氢溶液制取氧气,向 100 g 过氧化氢溶液中加入5 g 的二氧化锰, 充分反应后,过滤,得到滤液97.2 g,则原过氧 化氢溶液中氢元素的质量分数是( A )
A. 10.8%
____5_0_%______。
能力提升 3. 某化学小组同学为了测定实验室一瓶稀盐酸 中溶质的质量分数。他们用石灰石和此稀盐酸完 成了如图K9-3-2所示的实验。
(1)恰好完全反应时生成二氧化碳的质量是 __4_._4_____g。 (2)计算该瓶稀盐酸中溶质的质量分数。
解:设该瓶稀盐酸中溶质的质量为x。
CaCO3+2HCl==CaCl2+H2O+CO2↑
73
44
x
4.4 g
x=7.3 g
该瓶稀盐酸中溶质的质量分数为 ×100%=7.3% 答:该瓶稀盐酸中溶质的质量分数为7.3%。
4. 取50 g炉渣(含24%CaSO3)逐滴加入20%的盐 酸,请在图K9-3-3坐标中画出相应的曲线图。横 坐标为盐酸的质量,纵坐标请设定具体物质;并 标出曲线中必要的数据(写出计算过程)。
【已知】①设炉渣已不含石灰石,炉渣其他成分 不与盐酸反应;②CaSO3和盐酸反应类似于CaCO3。
解:设反应消耗盐酸中溶质的质量为x。 CaSO3 + 2HCl==CaCl2+SO2↑+H2O 120 73
50g×24% x
x=7.3 g
反应消耗盐酸溶液的质量为
=36.5 g
恰好完全反应时剩余固体的质量为
(2)一定温度下,向NaCl的饱和溶液中加入 NaCl固体,NaCl溶液的溶质质量分数___不_变____; 若采用升温蒸发溶剂的方法析出晶体后剩余溶液 的溶质质量分数____增__大______。
人教版 溶液的浓度 精品PPT课件3

2.对于反应后所得溶液的质量有两种求法:
(1) 溶液质量=反应物质量总和 - 生成气体的质量(或-生成沉 (2) 溶液的质量=溶质质量+溶剂(水)质量。
练 习 1.已知 6.5g 锌与 100g 稀硫酸,恰好完全反应。
求(1)稀硫酸中溶质的质量分数是多少?(2)反应后溶液的质量是
解:设 H2SO4 的质量为 x,H2 的质量为 y。 H2SO4+Zn=ZnSO4+H2↑ 98 x 65 6.5g y x=9.8g y=0.2g 2
2NaOH+H2SO4=Na2SO4+2H2Ox 98
80 40g = y 142
x=49g
y=71g
硫 酸 溶 质 质 量 分 数 = 49g/200g× 100% = 24 . 5% 71g/300g×100%≈23.7%
硫酸
答:硫酸钠的质量是 71g,硫酸的溶质质量分数是 24.5%,生 分数约等于 23.7%。
答:稀硫酸的溶质质量分数约等于 15.4%,反应后溶液质量为
提
升
训
练
4.100 克 40%的氢氧化钠溶液恰好与 200 克硫酸溶液完全反应,生 (1)生成硫酸钠多少克? (2)硫酸溶液中溶质质量分数? (3)生成物溶液中溶质质量分数? 解:设 H2SO4 的质量为 x, Na2SO4 的质量为 y,
73 x = 65 3.25g
盐酸溶质质量分数=3.65g/100g×100%=3.65% 答:稀盐酸的溶质质量分数是 3.65%。
练
习 3.将一定质量的金属锌投入到 63.7g 稀硫酸中,恰好完全
质量与反应时间的关系如图所示。请你据此分析计算:(1)稀硫酸 是多少?(2)反应后溶液的质量是多少?
由图可知氢气质量为 0.2g。 解:设 H2SO4 的质量为 x,Zn 的质量为 y, H2SO4+Zn=ZnSO4+H2↑ 98 x 65 y 2 0.2g
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶质质量分数
溶解度
意义
温度 溶剂量
表示溶液中溶质 质量的多少
不一定 不一定
表示物质 溶解性的强弱
一定 100克
是否饱和
不一定
必须饱和
单位
是一个比值
质量单位(克)
关系式
溶质的质量分数
溶质质量 溶液质量
100%
溶解度
溶质质量 溶剂质量
100克
二:溶质质量分数计算
[题型一] :有关溶质、溶剂和溶液之间的换算
课题3 溶液的浓度
主讲人:
课题3 溶液的浓度
温故而知新
1、饱和溶液 在一定温度下、一定量的溶剂中, 溶质不能继续溶解的溶液。
2、饱和溶液和不饱和溶液之间的相互转化方法Leabharlann 蒸发溶剂 增加溶质 降低温度
不饱和溶液
增加溶剂 升高温度 饱和溶液
3、固体溶解度
在一定温度下,某固态物质在100克溶剂里达
到饱和状态时所溶解的质量,
=9.1%
加盐:20g X10%+2g 20g +2g
=18.2%
练习2、20g 10%的盐水中倒出一半,求: 剩余溶液的溶质的质量分数。
剩余溶液的溶质质量分数不变,仍是 10 %
[题型二] :有关溶液稀释或浓缩的计算
计算的依据 :
稀释前溶质质量 = 稀释后溶质质量 浓缩前溶质质量 = 浓缩后溶质质量
的解质:量方分法数一增大增到加10溶%质,可以采取的方法是?
设应加入氯化钠固体的质量为x 40gX5%+x= (40g+x)X10%) 解得 X=2.22g
方法二 蒸发水分
设应蒸发掉水的质量为y 40gX5%= (40g—y)X10%
解得 y=20g
答:加入2.22g氯化钠,或蒸发掉20g水。
溶质质量分数与溶解度的比较
计算的依据 :
溶质质量分数=
溶质质量 溶液质量 100%
溶液质量 = 溶质质量 + 溶剂质量
【例题1】在农业生产中,常需要用质量分数为16%的氯
化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各是多少?
【解】溶质的质量分数 溶质质量 溶液质量
100%
溶质质量 溶液质量×溶质的质量分数
据《扬子晚报》报道:
2009年7月20日,河南一果农,因用 自己全部家当种植的果树离奇死亡而 伤心过度,菜农自尽而死,据其家人 介绍,他本人不大识字,7月18日晚 买来了250千克的液体肥料,他掺入 了1000千克的水后进行喷洒两天后,
所有果树离奇死亡。
经警方调查,结果显示该农民所配肥料 浓度过大,导致叶片大面积死亡。
5 : 95 : 100
讨论:
已知20℃时,氯化钠的溶解度是36g。有人 说:“20℃时氯化钠饱和溶液中溶质的质
量
分数为36%。”这种说法对吗?为什么?
分析:
溶解度 氯化钠(溶质) 水(溶剂)饱和溶液 溶质的质量分数
36g 36g 100g
136g
26.5%
结论:
溶解度
饱和溶液的溶质质量分数= 100g+溶解度
④不要忘记X100%,最后得到百分数。
⑤物质的质量分数要在不超过其最大溶解 量的范围时才有意义。
练一练:
在实验9-7中,三种硫酸铜溶液中溶质的质量分 数各是多少?把计算结果填写在下表中。
试管 溶液颜 溶 剂 溶 质 溶 液 溶质质 编号 色比较 质量/g 质量/g 质量/g 量分数
1 浅 20g 0.1g 20.1g 0.5% 2 较深 20g 0.5g 20.5g 2.4% 3 深 20g 2g 22g 9.1%
[实验9-8]
两杯溶液都是无色透明,
怎样比较溶液的稀浓?
溶质质量/g 溶剂(水)质 现象
量/g
10
90
20
80
固体溶解 固体溶解
溶液中溶质 的质量分数
10%
20%
结论:溶液中溶质的质量 分数越大,溶液浓度越大
溶质质量分数的含义:
溶质质量
溶液质量
5 % 的食盐溶液 ①.5g食盐溶于95g水形成的溶液。 ②.食盐的质量占整个食盐溶液的5%。 ③.将100g食盐溶液蒸干可以得到食盐5g。 ④.组成:M(食盐):M(水):M(食盐溶液) =
实验9-7 药品:水10mL 硫酸铜
仪器:试管 滴管
颜色: 淡蓝 蓝色 深蓝
填写实验记录
试管 溶液颜 溶 剂 溶 质 溶 液 溶 液 编号 色比较 质量/g 质量/g 质量/g 的浓稀
1 浅 20g 0.1g 20.1g
2 较深 20g 0.5g 20.5g
3 深 20g 2g
22g
分析实验结论
一:溶质质量分数
1、定义:是溶质质量和溶液质量之比 。 2、公式:
溶质质量 溶质质量分数= 溶液质量 100%
溶质的质量 =溶液质量 ×溶质质量分数
注意:
①溶质的质量:形成溶液的那部分溶质, 无溶入溶液的不计。
②溶液的质量 = 溶质的质量 + 溶剂的质 量。
(必须分清溶质、溶剂与溶液)。
③计算时上下质量单位要统一。
150kg 16% 24kg 溶剂质量 溶液质量 — 溶质质量
150kg 24kg 126kg
答: 配制150kg质量分数为16%的氯化钠溶液 需24 kg氯化钠和126 kg水。
练习1、20g 10%的盐水中放入 2g水或2g 食盐,求:所得溶液的溶质质量分数。
解: 加水: 20g X10%
20g +2g
叫做这种物质在这种溶剂里的溶解度。
4、气体溶解度 指该气体的压强为101KPa和一定温度时,在1体 积水里溶解达到饱和状态时的气体体积。
安徽 巢湖 谢玉荣
你知道下面瓶中标签是什么 意思吗?
化学纯
500mL
浓盐酸(HCl)
含HCl 37 % 密度为1.18 g/cm3
下面我们就来学习溶液 组成的表示方法。
溶质的质量分数36% 是指:100g溶液中含有36g溶质。 溶质T0C时溶解度36g是指:
①对于有色溶液,我们可以根据颜色深浅来判断溶液是 浓还是浅;但是这种分法比较粗略,不能准确地表明一定 量溶液里究竟含有多少溶质。
②在实际应用中,常常要准确知道一定量溶液里含有多 少溶质,即溶液的浓度(浓稀程度)
喷洒药水
飞机喷洒农药
药液太稀不能杀死害虫和病菌,但 药液太浓又会毒害农作物或树木.
农夫自杀 只因果树离奇死亡
练习:1(课本P44)把50g质量分数为98%的浓硫酸 稀释成20%的稀硫酸,需要水的质量是多少?
【解】设:稀释后溶液的质量为X。
50g × 98% = X × 20% X = 245g
需要水的质量 = 245g - 50g = 195g 答:需要水的质量为195g。
2有40g溶质质量分数为5%的氯化钠溶液,若将其溶质
