食品微生物检验原始记录(三级抽样检验)
微生物检验原始记录范本.pdf

微生物检验原始记录范本样品名称:生产日期:样品规格:产品批号:抽样数量:检测依据:□GB 4789.2-2010 □GB 4789.3-2010 □GB 4789.15-2010 使用仪器:天平□电热恒温培养箱□水浴箱□环境条件:室温℃实验地点:无菌室检测日期:20 年月日~ 月日检测项目:□菌落总数、□大肠杆菌、□霉菌计数、□酵母计数、□霉菌和酵母计数样品处理:1. □以无菌操作将检样25 注入225ml灭菌□磷酸盐缓冲液或□生理盐水或□蒸馏水中均质或混匀,□用灭菌吸管吸取检样1ml 注入9ml灭菌稀释液中充分振摇,做成1:10的均匀稀释样; 2. □用灭菌吸管吸取1:10稀释样1ml注入9ml灭菌稀释液中,混匀做成1:100稀释样;3. □同样方法做成10倍递增稀释样。
1.菌落总数2.大肠杆菌接种2~3个稀释度各2的平皿,每皿1ml检样或稀释样,注入46℃平板计数琼脂约15ml,凝固,℃培养h(时分~ 时分)。
选择接种3个稀释度10x1x0.1x0.01x0.001x稀释度10-10-所选稀释度平均值空白对照稀释液对照乳糖胆盐发酵管经36℃h(时分~ 时分)后产气管数菌落数转种在伊红美蓝琼脂平板上36℃h,革兰氏蓝色发酵管经36℃h(时分~ 时分)后产气管数计算方法所选稀释度的平均菌落数()X稀释倍数()=根据证实为大肠菌群阳性的管数,查大肠菌群(MPN)检索表,MPN值为=3.霉菌和酵母计数选择接种3个稀释度,平行接种2个平皿,每皿1ml检样或稀释样;注入46℃孟加拉红琼脂约15ml,凝固,26℃培养= d(/ : ~ / : );空白对照菌数灭菌水对照菌数=稀释度10-10-所选稀释度平均值□霉菌菌落数计算方法所选稀释度平均菌落数()X稀释倍数()=□霉菌菌落数计算方法所选稀释度平均菌落数()X稀释倍数()=检验菌落总数大肠菌群霉菌酵母结果:cfu/ MPN/100 计数cfu/ 计数cfu/检测者:审核者:。
微生物检验原始记录
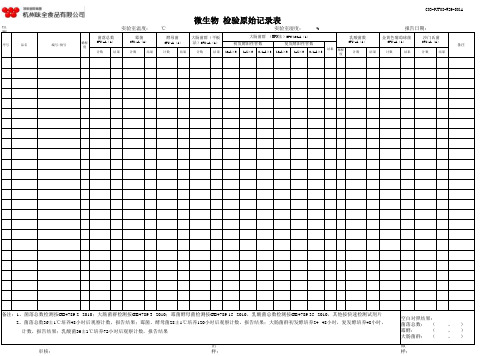
审核:出样:
做样:
编号/批号
稀释度
乳酸菌数
CFU/mL(g)
计数
结果
计数
结果
0.1ml×3
金黄色葡萄球菌
CFU/mL(g)沙门氏菌
CFU/mL(g)菌落总数
CFU/mL(g)结果
初发酵阳性管数
10ml×3
1ml×3
霉菌
CFU/mL(g)酵母菌
CFU/mL(g)
大肠菌群(平板法)CFU/mL(g)
0.1ml×3
10ml×3
1ml×3
结果
大肠菌群 (MPN法)MPN/100mL(g)
计数
空白对照结果:
菌落总数: ( , )霉酵: ( , )大肠菌群: ( , ) 2、菌落总数36±1℃培养48小时后观察计数,报告结果;霉菌、酵母菌28±1℃培养120小时后观察计数,报告结果;大肠菌群初发酵培养24--48小时,复发酵培养48小时,备注:1、菌落总数检测按GB4789.2--2010;大肠菌群检测按GB4789.3--2010;霉菌酵母菌检测按GB4789.15--2010,乳酸菌总数检测按GB4789.35--2010,其他按快速检测试剂片 计数,报告结果;乳酸菌36±1℃培养72小时后观察计数,报告结果
结果
计数
结果
计数
稀释度
C03-PJF08-W29-S01A
微生物 检验原始记录表
序号
复发酵阳性管数
备注
结果
计数
品名
计数
结果。
微生物检验原始记录
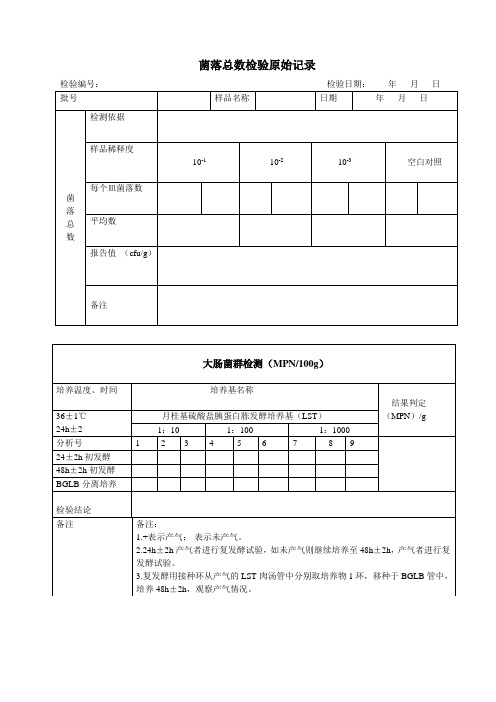
1:100
1:1000
分析号
1
2
3
4
5678源自924±2h初发酵
48h±2h初发酵
BGLB分离培养
检验结论
备注
备注:
1.+表示产气;-表示未产气。
2.24h±2h产气者进行复发酵试验,如未产气则继续培养至48h±2h,产气者进行复发酵试验。
3.复发酵用接种环从产气的LST肉汤管中分别取培养物1环,移种于BGLB管中,培养48h±2h,观察产气情况。
菌落总数检验原始记录
检验编号:检验日期:年月日
批号
样品名称
日期
年月日
菌
落
总
数
检测依据
样品稀释度
10-1
10-2
10-3
空白对照
每个皿菌落数
平均数
报告值(cfu/g)
备注
大肠菌群检测(MPN/100g)
培养温度、时间
培养基名称
结果判定
(MPN)/g
36±1℃
24h±2
月桂基硫酸盐胰蛋白胨发酵培养基(LST)
微生物检测原始记录
创作编号:BG7531400019813488897SX
创作者:别如克*
XXXX检测有限公司
菌落总数与大肠菌群检验原始记录
共页第
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
共页第
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第
主检: 年 月 日 校核: 年
月 日
XXXX 检测有限公司 乳酸菌与大肠菌群检测记录
共 页第
主检: 年 月 日 校核:
年 月 日
XXXX 检测有限公司 致病菌检验原始记录
共 页第
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共页第
培养温度:28±1℃培养时间:年月日时--- 年月日时:
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:
创作编号:BG7531400019813488897SX
创作者:别如克*。
微 生 物 检 验 原 始 记 录
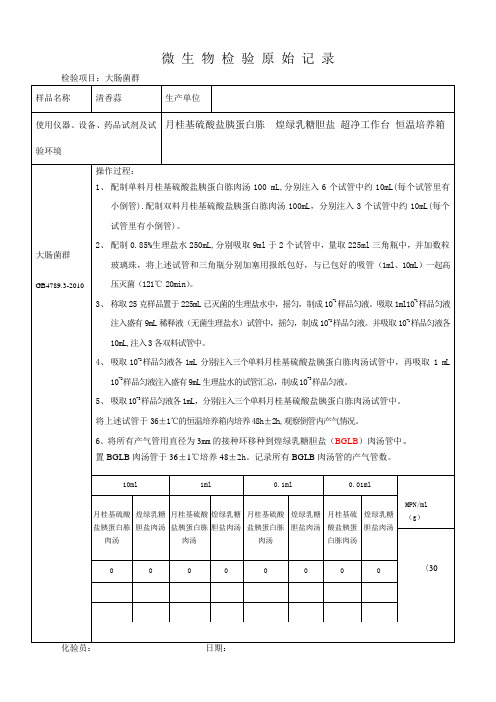
微生物检验原始记录检验项目:大肠菌群样品名称清香蒜生产单位使用仪器、设备、药品试剂及试验环境月桂基硫酸盐胰蛋白胨煌绿乳糖胆盐超净工作台恒温培养箱大肠菌群GB4789.3-2010操作过程:1、配制单料月桂基硫酸盐胰蛋白胨肉汤100 mL,分别注入6个试管中约10mL(每个试管里有小倒管).配制双料月桂基硫酸盐胰蛋白胨肉汤100mL,分别注入3个试管中约10mL(每个试管里有小倒管)。
2、配制0.85%生理盐水250mL,分别吸取9ml于2个试管中,量取225ml三角瓶中,并加数粒玻璃珠,将上述试管和三角瓶分别加塞用报纸包好,与已包好的吸管(1ml、10mL)一起高压灭菌(121℃ 20min)。
3、称取25克样品置于225mL已灭菌的生理盐水中,摇匀,制成10-1样品匀液。
吸取1ml10-1样品匀液注入盛有9mL稀释液(无菌生理盐水)试管中,摇匀,制成10-2样品匀液。
并吸取10-1样品匀液各10mL,注入3各双料试管中。
4、吸取10-2样品匀液各1mL分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中,再吸取1 mL10-2样品匀液注入盛有9mL生理盐水的试管汇总,制成10-3样品匀液。
5、吸取10-3样品匀液各1mL,分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中。
将上述试管于36±1℃的恒温培养箱内培养48h±2h,观察倒管内产气情况。
6、将所有产气管用直径为3mm的接种环移种到煌绿乳糖胆盐(BGLB)肉汤管中。
置BGLB肉汤管于36±1℃培养48±2h。
记录所有BGLB肉汤管的产气管数。
10ml 1ml 0.1ml 0.01ml月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤MPN/ml(g)〈300 0 0 0 0 0 0 0化验员:日期:。
微生物检验原始记录表
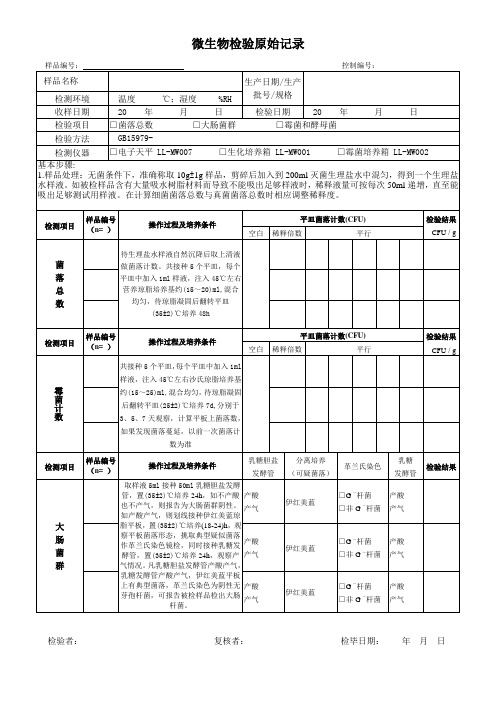
生产日期/生产批号/规格
检测环境
温度 ℃;湿度 %RH
收样日期
20 年 月 日
检验日期
20 年 月 日
检验项目
□菌落总数 □大肠菌群 □霉菌和酵母菌
检验方法
GB15979-
检测仪器
□电子天平LL-MW007□生化培养箱LL-MW001□霉菌培养箱LL-MW002
基本步骤:
1.样品处理:无菌条件下,准确称取10g±1g样品,剪碎后加入到200ml灭菌生理盐水中混匀,得到一个生理盐水样液。如被检样品含有大量吸水树脂材料而导致不能吸出足够样液时,稀释液量可按每次50ml递增,直至能吸出足够测试用样液。在计算细菌菌落总数与真菌菌落总数时相应调整稀释度。
检测项目
样品编号(n=)
操作过程及培养条件乳Fra bibliotek胆盐发酵管
分离培养
(可疑菌落)
革兰氏染色
乳糖
发酵管
检验结果
大
肠
菌
群
取样液5ml接种50ml乳糖胆盐发酵管,置(35±2)℃培养24h,如不产酸也不产气,则报告为大肠菌群阴性。如产酸产气,则划线接种伊红美蓝琼脂平板,置(35±2)℃培养(18-24)h,观察平板菌落形态,挑取典型疑似菌落作革兰氏染色镜检,同时接种乳糖发酵管,置(35±2)℃培养24h,观察产气情况。凡乳糖胆盐发酵管产酸产气,乳糖发酵管产酸产气,伊红美蓝平板上有典型菌落,革兰氏染色为阴性无芽孢杆菌,可报告被检样品检出大肠杆菌。
样品编号(n=)
操作过程及培养条件
平皿菌落计数(CFU)
检验结果
CFU/g
空白
稀释倍数
平行
霉菌计数
共接种5个平皿,每个平皿中加入1ml样液,注入45℃左右沙氏琼脂培养基约(15~25)ml,混合均匀,待琼脂凝固后翻转平皿(25±2)℃培养7d,分别于3、5、7天观察,计算平板上菌落数,如果发现菌落蔓延,以前一次菌落计数为准
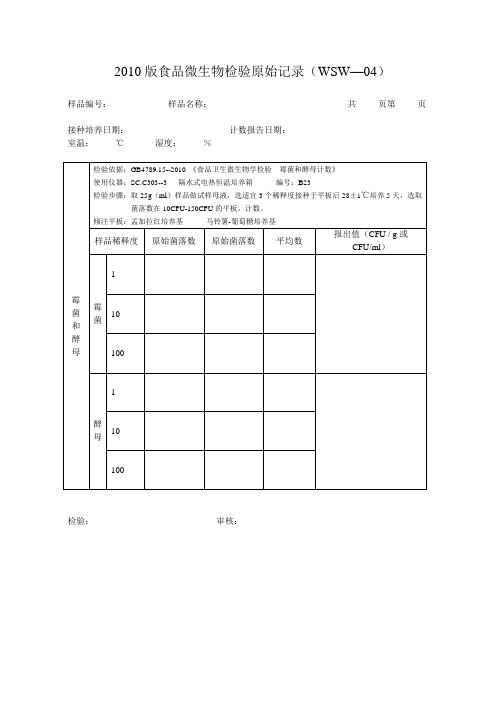
2010版食品微生物检验霉菌酵母原始记录(WSW
1
10
100
酵母
1
10
100
检验:审核:
使用仪器:SC.C303--3隔水式电热恒温培养箱编号:B23
检验步骤:取25g(ml)样品做试样母液,选适宜3个稀释度接种于平板后28±1℃培养5天,选取菌落数在10CFU-150CFU的平板,计数。
倾注平板:孟加拉红培养基马铃薯-葡萄糖培养基
样品稀释度
原始菌落数
原始菌落数
平均数பைடு நூலகம்
报出值(CFU / g或CFU/ml)
孟加拉红培养基马铃薯葡萄糖培养基样品稀释度原始菌落数原始菌落数平均数报出值cfug或cfuml霉菌110100酵母110100检验
2010版食品微生物检验原始记录(WSW—04)
样品编号:样品名称:共页第页
接种培养日期:计数报告日期:
室温:℃湿度:%
霉菌和酵母
检验依据:GB4789.15--2010《食品卫生微生物学检验霉菌和酵母计数》
乳制品微生物检测原始记录模板

产商品质量监督检验所原始记录
样品编号方法依据GB 4789 —2010 温度℃湿度(RH) %
样品类别乳制品检测项目微生物指标培养时间
一、乳酸菌总数: cfu/mL
稀释度及菌落数
CK(空白) 1:1000(第一稀释度)1:10000(第二稀释度)1:100000(第三稀释度)
二、菌落总数:(GB 4789.2—2010) cfu/mL
稀释度及菌落数
CK(空白) 1:1(第一稀释度)1:10(第二稀释度)1:100(第三稀释度)
三、大肠菌群:(GB/T4789.3—2010) MPN/100mL cfu/mL
第一法稀释度及菌落数
1 g ×3 0.1 g ×3 0.01g ×3
第二法稀释度及菌落数
CK(空白) 1:1(第一稀释度)1:10(第二稀释度)1:100(第三稀释度)
四、霉菌(GB4789.15—2010) cfu/mL
稀释度及菌落数
CK(空白) 1:1(第一稀释度)1:10(第二稀释度)1:100(第三稀释度)
五、酵母菌(GB4789.15—2010) cfu/mL
稀释度及菌落数
CK(空白) 1:1(第一稀释度)1:10(第二稀释度)1:100(第三稀释度)
六、致病菌:
【□沙门氏菌(GB4789.4—2010)□金黄色葡萄菌(GB4789.10—2010)□志贺氏菌(GB4789.5—2012)】样品经(前)增菌处理,分离培养,在固态选择性培养基上均无可疑特征菌落出现,视为未检出。
核对:检验员:。
微生物检验原始记录

⑴菌落总数(平板计数琼脂36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑵霉菌、酵母菌计数(孟加拉虎红27±1℃5d)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
微生物检验原始记录
NO:
品名:包装规格:
批号:数量:
生产车间:检品数量:
检验人员:复核人员:
检验依据:检验目的:
检验日期:报告日期:
检验记录与结果:
1.取样:
(1)原液取样
(2)无菌称取样品25g或者25ml,置225ml灭菌的0.85%的生理盐水中,充分混匀,制成1:10稀释液。取1:10稀释液1ml置9ml灭菌的0.9%生理盐水中,制成1:100稀释液。
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑶大肠杆菌(月桂基磺酸盐胰蛋白胨【LST】肉汤,36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:10稀释液(10ml)双料
1:100稀释液(1ml)
阴性对照
阳性对照
结果:MPN/mL
1
均值:
2
微生物检测原始记录文本

菌落总数与大肠菌群检验原始记录
共页第页
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
培养温度:28±1℃培养时间:年月日时 --- 年月日时:
菌落计数:
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
微生物检验原始记录表格式
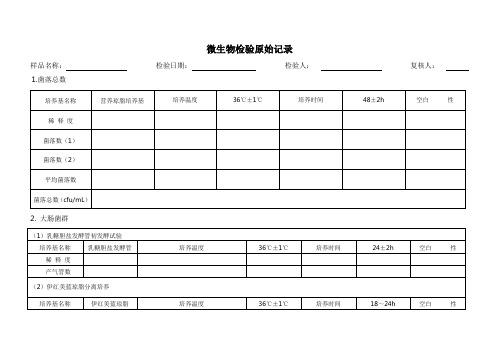
稀释度
产气管数
(2)伊红美蓝琼脂分离培养
培养基名称
伊红美蓝琼脂
培养温度
36℃±1℃
培养时间
18~24h
空白性
(3)证实试验(凡乳糖发酵管产气、革兰氏染色为阴性的无芽孢杆菌,即可报告为大肠菌阳性)
培养基名称
乳糖发酵管
培养温度
36℃±1℃
培养时间
248±2h
空白性
阳性管数
大肠菌群(MPN/ mL)
微生物检验原始记录
样品名称:检验日期:检验人:复核人:
1.菌落总数
培养基名称
营养琼脂培养基
培养温度
36℃±1℃
培养时间
48±2h
空白性
稀释度
菌落数(1)
菌落数(2)
平均菌落数
菌落总数(cfu/mL)
2.大肠菌群
(1)乳糖胆盐发酵管初发酵试验
培养基名称
乳糖胆盐发酵管பைடு நூலகம்
培养温度
36℃±1℃
培养时间
24±2h
微生物检验原始记录
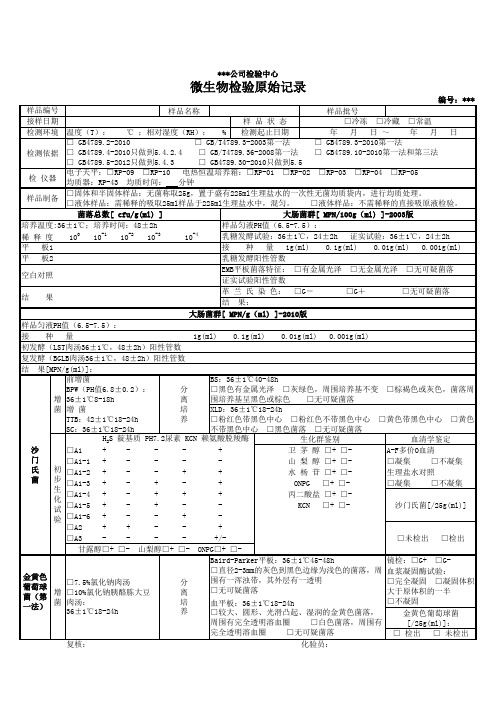
志 贺 氏 菌
分离培养 XLD琼脂平板:36±1℃20-48h □粉红色至无色、半透明、光滑、湿润、圆 形、边缘整齐或不齐的菌落 □无可疑菌落
MAC琼脂平板:36±1℃20-48h □无色至浅粉红色、半透明、光滑、湿润、 赖氨酸脱羧酶: □+ □圆形、边缘整齐或不齐的菌落 □无可疑菌落 鸟氨酸脱羧酶: □+ □水杨苷: □+ □七叶苷: □+ □增菌 初筛 LB1增菌液:30±1℃24h 木 糖:□+ □LB2增菌液:30±1℃18-24h 分离培养 鼠李糖:□+ □PALCAM琼脂平板:36±1℃24-48h 鉴定 □ 较小的圆形灰绿色菌落,周围有棕黑色水 解圈 染色镜检:□G+□G□ 较小的圆形灰绿色菌落,周围有棕黑色水 解圈,菌落有黑色凹陷 动力试验:□+ □□ 无典型或可疑菌落 显色培养基:36±1℃24-48h 增菌 初步生化试验 mEC+n肉汤:36±1℃18-24h TSI:36±1℃18-24h 分离培养 □斜面与底层均黄色,产气或不产气, □其他反应现象 CT-SMAC平板:36±1℃18-24h 不产H2S □圆形、光滑、较小的无色菌 MUG-LST:36±1℃18-24h 大肠埃 落,呈现较暗的灰褐色中心 □有荧光 □无荧光 希氏菌 □红色菌落 □无可疑菌落 血清学鉴定 O157: □凝集 □不凝集 改良CHROMagarO157显色琼脂 O157血清: H7 平板:36±1℃18-24h H7因子血清: □凝集 □不凝集 □圆形、较小的菌落,中心呈 生理盐水对照: □凝集 □不凝集 淡紫色-紫红色,边缘无色或 浅灰色 单 核 细 胞 增 生 李 斯 特 氏 菌 □无典型或可疑菌落 接种和培养 金黄色 葡萄球 菌(第 三法) 10%氯化钠胰酪胨大豆肉汤 36±1℃ 45-48h 复核: 典型菌落确认+增菌 BHI肉汤 36±1℃ 18-24h
微生物限度检查原始记录表格

稀释倍数
10-1
10-2
-3
阴性对照
1
2
平均
结果
标准规定:
霉菌(28℃±1℃,120h±2h)
开始培养时间月 日 时结束培养时间月 日 时
稀释倍数
10-1
10-2
10-3
阴性对照
1
2
平均
结果
标准规定:
酵母菌(28℃±1℃,120h±2h)
开始培养时间月 日 时结束培养时间月 日 时
稀释倍数
10-1
10-2
10-3
阴性对照
1
2
平均
结果
标准规定:
大肠菌群测定
开始培养时间月 日 时结束培养时间月 日 时
初发酵(36℃±1℃,24h±2 h)
查(MPN)检
索表结果
大肠菌群总数(MPN/100g)
稀释倍数
10-1
10-2
10-3
阴性对照
1
2
3
结论:□符合规定□不符合规定
检验人: 复核人:
微 生 物 限 度 检 查 原 始 记 录
[编号]:
检品名称:批号:
检验编码:请检单位:固体车间软胶囊车间
请检日期:年 月 日检验日期:年 月 日
供试液制备:□1常规法 供试品 g (ml) 0.9%氯化钠溶液 ml
□2非水溶性供试品 供试品g(ml)加乳化剂 g(ml )
菌落总数(36℃±1℃,48h±2 h)
微生物检测原始记录

X X X X检测有限公司
菌落总数与大肠菌群检验原始记录
共
页第页
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共
页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共
页第页
主检:年月日校核:年月日
XXXX检测有限公司
致病菌检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共
页第页
培养温度:28±1℃培养时间:年月日时 --- 年月日时:
菌落计数:
培养温度:28±1℃培养时间:年月日时 --- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共
页第页
主检:日期:校核:日期:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
计数:培养温度℃,培养时间h
证实:培养温度℃,培养时间h
10010-110-210-3
空白
结果
10010-110-210-3
证实
试验
空白
结果
样1
样2
样3
样4
样5
注
计数时平行结果以A / B的方式记录
检验员/日期:审核/日期:
食品微生物检验原始记录
样品名称
样品编号
抽样地点
样品批号
检测环境
温度(T):℃;相对湿度(RH):%
接样日期
年月日
检测地点
化验室、无菌室
检测起止日期
年月日~月日
检测依据
□GB4789.2-2016□GB4789.3-2016第一法□GB4789.3-2016第二法□GB4789.4-2010
□GB/T4789.5-2003□GB4789.10-2010□GB/T4789.11-2003□GB4789.15-2010
检测仪器
□电子天平(型号:SC6010)编号00-2□霉菌培养箱(型号:WJP-150)25~28℃编号04-16
□电热恒温培养箱(型号:DNP-9272)36±1℃编号□04-15□04-24□05-11
□均质器(型号:BJ-IV)编号08-J3转速8000r/min时间□1分钟□2分钟□3分钟
培养基
□平板计数琼脂ML□LST肉汤ML□BGLB肉汤ML□VRBA琼脂ML
□BPWMI□TTBML□SCML□BS平板ML
□XLD平板ML□GNML□SS平板ML□EMB平板ML
□7.5%氯化钠肉汤ML□Baird-Parker平板ML□血平板ML□兔血浆ML
□葡萄糖肉浸液肉汤ML□EMB平板ML□虎红琼脂ML
□API20E生化鉴定试剂盒RR□其他
样品备
□固体和半固体样品:无菌称取25g,置于盛有225ml生理盐水的无菌灭菌杯内,进行均质处理。
□液体样品:吸取25ml样品于225ml生理盐水中,混匀。□液体样品:直接吸原液检验。
□pH测定及调节:样品原pH为,□无需调节用□1mol/LNaOH/□1mol/LHCl调节至。
样品
菌落总数[ CFU/mLg]
大肠菌群MPN计数法[ MPN/100mLg]
培养温度℃,培养时间h
初发酵温度℃,时间h
复发酵温度℃,时间h
10010-110-210-3
空白
结果
10×31×30.1×3 0.01×3
分离鉴定
结果
样1
样2
样3
样4
样5
样品
□霉菌□及酵母菌[ CFU/□mL□g]
大肠菌群平板计数法[ CFU/□mL□g]
