明胶成品检验原始记录
胶囊用明胶原始检验记录(2020版药典)

胶囊用明胶原始检验记录文件编号:第1 页共4页名称胶囊用明胶规格批号包装生产单位供应单位检验项目检验依据检验仪器【性状】本品为(应为微黄色至黄色、透明或半透明、微带光泽的薄片或粉粒;)取本品5g置100ml烧杯中,加水25~50ml,观察本品,因吸水而(应膨胀变软)。
取本品1g,加入盛有9ml热水(70~80℃)的烧杯中,能全部溶解;取本品1g,在29ml醋酸或甘油与水的热混合液中(溶解);取本品0.01g,加入盛有100ml乙醇的量瓶中,每隔5分钟强力震摇30秒钟,在30分钟内(不溶解)。
项目结论:【鉴别】(1)取本品约0.5g,加水50ml,加热使溶解后,取溶液5ml,加重铬酸钾试液-稀盐酸(4:1)数滴,(应即生成橘黄色絮状沉淀)。
项目结论:(2)取鉴别(1)项下剩余的溶液1ml,加水100ml,摇匀后,加鞣酸试液数滴,(应即发生浑浊)项目结论:(3)取本品,加钠石灰后,加热,(应即发生氨臭)项目结论:【检查】酸碱度取本品1.0g,加入热水100ml中,充分振摇使溶解,放冷至350C,依法测定(通则0631),pH值为(应为4.0~7.2)项目结论:检验者:年月日复核者:年月日产品名称:胶囊用明胶批号:规格:第2 页共4页透光率取本品7.5g,精密称定,加水105g,加盖,放置1-4小时,在65℃±2℃的水浴加热15分钟,充分搅拌使供试品溶散均匀,制成6.67%的溶液,冷却至45℃,照紫外可见分光度法(通则0401)分别在450nm与620nm的波长处测定透光率,分别不得低于50%和70%。
样品在450nm波长处的透光率为T1T2T3平均值:样品在620nm波长处的透光率为:T1T2T3平均值:项目结论:电导率取本品1.0g,加不超过60℃的水溶解并制成1.0%的溶液,作为供试品溶液;另取水100ml作为空白溶液。
将供试品溶液与空白溶液置30±1℃的水浴中保温1小时后,用电导率仪测定,以箔黑电极作为测定电极,先用空白溶液冲洗电极3次后,测定空白溶液的电导率,其电导率为(应不得过5.0µS/cm)。
明胶空心胶囊检验操作记录

检品编号:第1页共5页检验记录:【性状】本品呈。
本品为空囊。
﹙﹚【鉴别】﹙1﹚取本品g,加水50ml,加热使溶化,放冷,取溶液5 ml,加重铬酸钾试液-稀盐酸﹙4:1﹚的混合液滴,即生成。
﹙﹚﹙2﹚取鉴别﹙1﹚项下剩余的溶液 1 ml,加水50 ml,摇匀,加鞣酸试液滴,即。
﹙﹚﹙3﹚取本品约g,置试管中,加钠石灰少许,加热,产生的气体能使湿润的红色石蕊试纸。
﹙﹚【检查】1、松紧度:取本品10粒,用拇指和食指轻捏胶囊两端,旋转拔开,粘结、变形、或破裂,然后装满滑石粉,将帽体套合,逐粒在1 m的高度处直坠于厚度为2cm的木板上,。
﹙漏粉不得过1粒﹚﹙﹚2、脆碎度:取本品50粒,置表面皿中,移入盛有硝酸镁饱和溶液的干燥器内,置25℃恒温24小时,取出,立即分别逐粒放入直立在木板﹙厚度为2cm﹚上的玻璃管内﹙内径为24mm,长为200 mm﹚,将圆柱形砝码﹙材质为聚四氟乙烯,直径为22 mm、重20 g±0.1 g﹚从玻璃管口处自由落下,。
﹙不得超过5粒﹚﹙﹚3、崩解时限:取本品6粒,装满滑石粉,照崩解时限检查法﹙附录ⅩA﹚温度:℃湿度:%仪器:ZB-1D 智能崩解仪介质:水测温:℃内全部溶化崩解﹙应在10分钟内全部溶化崩解﹚﹙﹚4、黏度:温度:℃湿度:%取本品g,置100 ml具塞锥形瓶中,加水使胶液总重量达到下列计算公式的重量﹙含干燥品15.0%﹚,密塞,置60℃水浴中不时振摇使溶化。
移至40℃±0.1℃水浴中,,约10分钟后,移至平氏粘度计内,照黏度测定法﹙附录ⅥG第一法,毛细管内径为2.0 mm﹚,于40℃±0.1℃水浴中测定。
﹙1-干燥失重﹚×4.50×100胶液总重量﹙g﹚= ———————————————————=15.0仪器:BS124S电子天平单位:g 初读数为:。
电子秒表分度0.1s 50℃温度计分度0.1℃检品编号:第2页共5页粘度计编号:粘度计K值:流出时间t﹙s﹚﹙1﹚﹙2﹚﹙3﹚t﹙s﹚平均值运动黏度﹙mm2/s﹚N=Kt平均值﹙不得低于60mm2/s﹚﹙﹚5、亚硫酸盐:﹙以SO2计﹚:取本品g,置长颈圆底烧瓶中,加热水100 ml使溶化,加磷酸ml与碳酸氢钠g,即时连接冷凝管,加热蒸馏,以0.05mol/l碘溶液15ml为接收液,收集馏出液50ml,用水稀释至100ml,摇匀,量取50ml,置水浴上蒸发,随时补充水适量,蒸至溶液几乎无色,用水稀释至40ml,照硫酸盐检查法﹙ⅧB﹚检查,如显浑浊,与标准硫酸钾溶液3.75ml制成的对照液比较:对照管制备:精密量取标准硫酸钾溶液3.75ml,加水使成约40ml,加稀盐酸2ml;样品管制备:加入蒸至几乎无色的馏出液,加水使成约40ml,加稀盐酸2ml;两管同时加25%氯化钡溶液5ml,加水稀释至50ml,振摇,同置黑色背景上,由管口向下观察;比较结果:。
08微生物限度检查记录(平皿法)-明胶
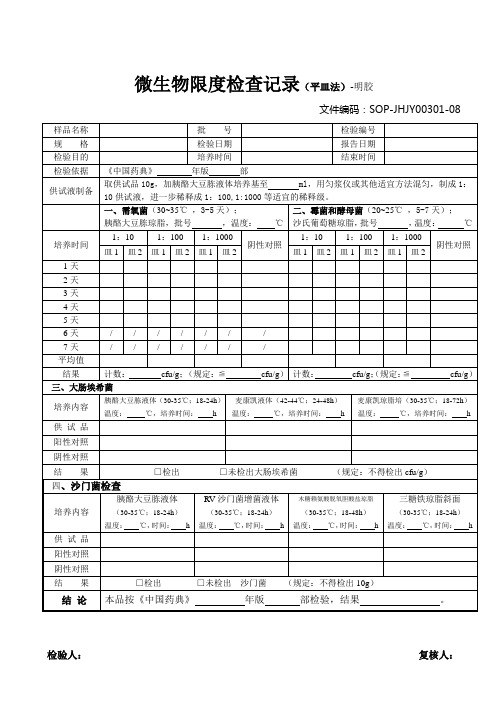
微生物限度检查记录(平皿法)-明胶文件编码:SOP-JHJY00301-08样品名称批号检验编号规格检验日期报告日期检验目的培养时间结束时间检验依据《中国药典》年版部供试液制备取供试品10g,加胰酪大豆胨液体培养基至 ml,用匀浆仪或其他适宜方法混匀,制成1:10供试液,进一步稀释成1:100,1:1000等适宜的稀释级。
一、需氧菌(30~35℃,3-5天);胰酪大豆胨琼脂,批号,温度:℃二、霉菌和酵母菌(20~25℃,5-7天);沙氏葡萄糖琼脂,批号,温度:℃培养时间1:10 1:100 1:1000阴性对照1:10 1:100 1:1000阴性对照皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿21天2天3天4天5天6天/ / / / / / /7天/ / / / / / /平均值结果计数: cfu/g;(规定:≦cfu/g)计数: cfu/g;(规定:≦cfu/g)三、大肠埃希菌培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,培养时间:h麦康凯液体(42-44℃;24-48h)温度:℃,培养时间:h麦康凯琼脂培(30-35℃;18-72h)温度:℃,培养时间:h供试品阳性对照阴性对照结果□检出□未检出大肠埃希菌(规定:不得检出cfu/g)四、沙门菌检查培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,时间:hRV沙门菌增菌液体(30-35℃;18-24h)温度:℃,时间:h木糖赖氨酸脱氧胆酸盐琼脂(30-35℃;18-48h)温度:℃,时间:h三糖铁琼脂斜面(30-35℃;18-24h)温度:℃,时间:h供试品阳性对照阴性对照结果□检出□未检出沙门菌(规定:不得检出10g)结论本品按《中国药典》年版部检验,结果。
检验人:复核人:。
明胶质量标准与检验规程

2.范围:适用于明胶的检验。
3.责任人:QA、QC人员。
4.内容:4.1.性状4.1.1.本品为淡黄色至黄色细粒,应保持干燥、洁净、均匀,无夹杂物;均应通过孔径4mm标准筛网;2.5%的明胶溶液无不适气味。
4.1.2.凝冻强度4.1.2.1.质量指标:≥180 Bloom g。
4.1.2.2.检验方法步骤4.1.2.2.1.胶冻的制备:在三角烧瓶中配制6.67%(以商品胶计)胶液150ml,将120ml测定溶液放入冻力瓶内,加盖,在10±0.1℃低温恒温水槽内冷却16~18h。
4.1.2.2.2.测定胶冻强度:将冻力瓶从恒温水槽中取出,外面擦干,拿掉塞子,迅速放在冻力仪圆台上进行凝冻强度测定。
4.1.2.2.3.直接从冻力仪中读出试验胶的凝冻强度,单位以Bloom g表示(注:低温恒温水槽内及冻力仪要校正水平)。
4.1.3.勃氏粘度4.1.3.1.质量指标:≥3.5mPa•s。
4.1.3.2.检验方法步骤4.1.3.2.1.在三角烧瓶中配制6.67%胶液,一次测定量需要100ml,将胶液冷却至60±0.1℃时,将胶液水平调节到上刻线。
4.1.3.2.2.将手指移开毛细管末端时按下秒表。
胶液水平达到下刻线时停下秒表,记下时间,准确到0.1s。
4.1.3.2.3.结果表示和计算n=1.005At —1.005B/t式中:n ——胶液粘度,mPa•s;t ——流过时间,s;A,B ——粘度计常数,通过校正测定。
4.2.检查4.2.1.水分4.2.1.1.指标要求:≤14.0%。
4.2.1.2.试验方法步骤4.2.1.2.1.在已知恒重的平底铝制或不锈钢小盒中称入胶样0.9~1.1g,准确至0.001g。
4.2.1.2.2.在盒中加蒸馏水10ml,膨胀30min。
4.2.1.2.3.将小盒去盖放在红外灯下加热,温度调节到105~110℃,将胶样溶解,然后蒸至基本干燥;小盒移至烘箱中,在105±2℃下烘至恒重;取出置于干燥器内,冷却至室温;计算水分。
验证原始记录(模板).总结

炮制工艺验证原始记录ZK-DXYP-YZ- )平凉市铸康中药饮片有限责任公司年月日1. 验证内容1.1. 单元项目:净制1.1.1 •概述:净制对药效和药物的质量的影响也较大,如药物中的杂质,泥沙,灰屑 等,因此我们在中药的净制处理过程和结果进行审计。
1.1.2. 执行文件:《炮制工艺规程》(ZK-DXYP-SOP-PS- -01 );《中华人民共和国药典》2010年版;毒性中药饮片生产记录。
1.1.3 .净制:在净制前、净制后各随机取样三次,检查净制前和净制后川乌原药材 中的泥沙、其它异物杂质、净制效果进行判定。
1.1.4.净制方法: 拣口 筛口簸口 刮口 风选口 机选口 1.2. 验证结果:操作人: _______________________ Q A _______ 风险分析:结论:操作人:_______________________ Q A _______ : 风险分析:结论:3.设备拆装操作:4.清洁4.1. 清洁内容:42清洁方法:4.3. 取样:表面直接取样法;漂洗液样品44检测方式:4.4.1. 目测检查4.4.2. 接受限度:设备在清洁后,无可见的物质残留在设备表面;4.4.3. 取最后冲洗水样,与纯化水比色,冲洗水样与纯化水色度一致呈无色状态最终淋洗水PH值应符合饮用水标准(6.5 ----8.5 );4.4.4. 残留物检测:4.4.4.1. 仪器:三用紫外仪4.4.4.2. 测定过程:用滤纸擦拭清洗后的设备取样,样纸静置晾干,置于三用紫外仪(365nn)下观察。
4.4.4.3. 结果判断:若滤纸上显示有所产毒性饮片相对应的荧光斑点,则设备清洗不干净;若滤纸上无明显的荧光斑点,则设备清洗干净。
4.4.5. 风险分析由于上以产品对下一产品的污染并不是均匀分布在整个设备的接触面上,因此清洁验证的残留成分抽样计划的确定必须进行风险分析,且在风险分析中确定清洁验证的关键部位。
4.4.6. 结论测试结果不得大于计算出的检测限。
产品检验原始记录与检验报告(表格)

产品检验原始记录(糕点)检验员: 审核员: 日期:产品检验报告(糕点)佛山市金城速冻食品有限公司产品检验原始记录(面包)检验员: 审核员: 日期:产品检验报告(面包)产品检验原始记录(裱花蛋糕)检验员: 审核员: 日期:产品检验报告(裱花蛋糕)产品检验原始记录(冰皮月饼)检验员: 审核员: 日期:产品检验报告(冰皮月饼)产品检验原始记录(月饼)检验员: 审核员: 日期:产品检验报告(月饼)不合格品处置:()返工()报废()改作他用()其它:负责人:日期:产品检验原始记录(月饼)检验员: 审核员: 日期:产品检验报告(馅料)()返工()报废()改作他用()其它:日期:负责人:()佛山市金城速冻食品有限公司()佛山市金城速冻食品有限公司南海分公司(以“V”标识生产公司)审核人: 复核人: 日期:理化检验原始记录(一)判定标准 __________________________________________________________________________1水分:检测方法:GB/T 5009 32003 □称量瓶质量(g ): 1 #2 #3 #样品+称量瓶质量(g ): 1 # 2 # 3 #烘后恒重:1 #2 #3 #样品中水分含量(%):1# 2 #3#平均 标准要求:w%检验人:2、馅含量:检测方法: SN/T 0801.19-1999 □样品总质量(g ): 1 #2 #3 #馅料质量m (g ): 1 # 2 #3 #馅料含量(% :1# 2#3#平均 标准要求:》%检验人3、总糖:样品质量(g ): 1检测方法:GB/T 5009.7、8-2008 □#2 #3#斐林氏系数(A ):试样消耗的体积( ml ): 1# 2 # 3 #试样的总糖(以 计)(%):1#2 #3#平均: 标准要求:w%检验人:理化检验原始记录()佛山市金城速冻食品有限公司()佛山市金城速冻食品有限公司南海分公司(以“V”标识生产公司)判定标准 __________________________________________________________________________1灰分: 检测方法:GB/T 5009.4-2003□坩埚的质量(g): 1#2#样品+坩埚质量(g): 1#2#坩埚和灰分的质量(g): 1#2#样品中灰分含量(glOO/g): 1#2#平均标准要求:w g/lOOg检验人2、酸价:检测方法:GB/T 5009.37-2003 □样品质量(g): 1# 2#氢氧化钾标准溶液浓度(mol/L):试样消耗标准溶液的体积(ml ): 1 # 2#试样的酸价(以KOH计)(mg/g): 1 # 2# 平均标准要求:w mg/g检验人3、过氧化值:检测方法:GB/T 5009.37-2003 □样品质量(g): 1# 2#硫代硫酸钠标准溶液浓度(mol/L ):试剂空白消耗标准溶液的体积(ml):试样消耗标准溶液的体积(ml): 1# 2#试样的过氧化值:1# 2# 平均标准要求:w g/100g检验人审核人: 复核人: 日期:产品检验报告()佛山市金城速冻食品有限公司()佛山市金城速冻食品有限公司南海分公司(以“V”标识生产公司)判定标准___________________________________________________________________________检验员审核员日期。
食品检验原始记录模板
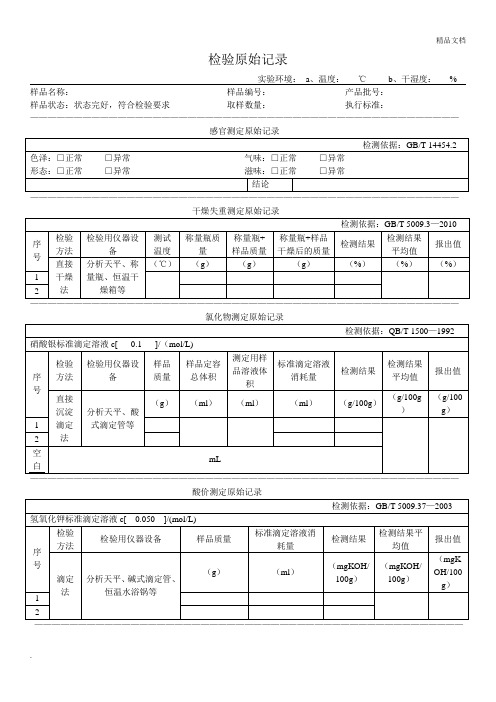
48小时培养(36℃±1℃)水对空对平均菌落数
结果报出值(cfu/g)
营养琼脂法
蒸汽灭菌锅、恒温水浴锅、超净工作台、培养箱、培养皿等
1:10
1:100
1:1000
—————————————————————————————————————————————————
大肠菌群检测原始记录
报出值
直接干燥法
分析天平、称量瓶、恒温干燥箱等
(℃)
(g)
(g)
(g)
(%)
(%)
(%)
1
2
—————————————————————————————————————————————————
氯化物测定原始记录
检测依据:QB/T 1500—1992
硝酸银标准滴定溶液c[0.1]/(mol/L)
序号
检验方法
滴定法法
分析天平、酸式滴定管、恒温水浴锅等
(g)
(ml)
(g/100g)
(g/100g)
(g/100g)
1
2
空白
mL
—————————————————————————————————————————————————
菌落总数测定原始记录
检测依据:GB/T4789.2—2010
检验方法
检验用仪器设备
稀释度
检验用仪器设备
样品质量
样品定容总体积
测定用样品溶液体积
标准滴定溶液消耗量
检测结果
检测结果平均值
报出值
直接沉淀滴定法
分析天平、酸式滴定管等
(g)
(ml)
(ml)
(ml)
(g/100g)
产品检验原始记录与检验报告(最新表格)

乌鲁木齐市沃德爱里食品有限公司产品检验原始记录(糕点)产品名称规格型号生产批号生产日期20 年月日样品数量检验日期20 年月日样品状态一、感官1.形态:□(烘烤类糕点)外形整齐,底部平整,无霉变,无变性,具有该品种应有的形态特征。
□(冷加工糕点)具有该品种应有的形态特征。
2.色泽:□(烘烤类糕点)表面色泽均匀,具有该品种应有的色泽特征。
□(冷加工糕点)具有该品种应有的色泽特征。
3.组织:□(烘烤类糕点)无不规则大空洞。
无糖粒,无粉块。
带馅类饼皮厚薄均匀,皮馅比例适当,馅料分布均匀,馅料细腻,具有该品种应有的组织特征。
□(冷加工糕点)具有该品种应有的组织特征4.滋味口感:□味纯正,无异味,具有该品种应有的风味和口感特征。
5.杂质:□无可见杂质。
二、干燥失重序号试样的质量和称量瓶的质量m1(g)称量瓶及干燥后样品的质量m2(g)称量瓶的质量m3(g)干燥失重(%)平均值(%)报出值(%)12计算:X=(m1-m2)/ (m1-m3)×100乌鲁木齐市沃德爱里食品有限公司产品出厂检验报告(糕点)产品名称规格型号生产日期20 年月日生产批号取样日期20 年月日样品数量检验日期20 年月日检验依据序号检验项目质量要求检验结果1 糕点形态□(烘烤类糕点)外形整齐,底部平整,无霉变,无变性,具有该品种应有的形态特征。
□(冷加工糕点)具有该品种应有的形态特征。
色泽□(烘烤类糕点)表面色泽均匀,具有该品种应有的色泽特征。
□(冷加工糕点)具有该品种应有的色泽的特征组织□(烘烤类糕点)无不规则大空洞。
无糖粒,无粉块。
带馅类饼皮厚薄均匀,皮馅比例适当,馅料分布均匀,馅料细腻,具有该品种应有的组织特征。
□(冷加工糕点)具有该品种应有的组织特征滋味与口感味纯正,无异味,具有该品种应有的风味和口感特征杂质正常视力无可见杂质2 净含量(g)□ 0g~50g 允许短缺量:9% □ 50g~100g 允许短缺量:4.5g □ 100g~200g 允许短缺量:4.5% □ 200g~300g 允许短缺量:9g □300g~400g 允许短缺量:3%3 干燥失重(%)≤424 菌落总数(cfu/g)□热加工≤1500 □冷加工≤100005 大肠菌群(MPN/100g)□热加工≤30 □冷加工≤3007 标签符合GB 7718和GB 13432的规定检验结论:()合格,准予放行。
药品检验原始记录书写范例

2.1.3 相对密度:记录采用的方法(比重瓶法或韦氏比重秤法),测定时的温度,测定值或各项称量数据,计算式与结果。
例:
相对密度:检验日期:2014.07.05 t:25℃
2.1.8 酸值(皂化值、羟值或碘值)
2.2【鉴别】
2.2.1 中药材的经验鉴别
2.2.2 显微鉴别
2.2.3 显色反应或沉淀反应
2.2.4 薄层色谱(或纸色谱)
2.2.5 气(液)相色谱
2.2.6 紫外-可见吸收光谱
2.2.7 红外吸收光谱
2.3【检查】
2.3.1含氟量
2.3.2含氮量
2.3.3pH值
供试品重量
供试品的相对密度=
水重量
称量:
比重瓶105℃干燥1小时后放冷称重:12.0356g
装满供试品置20℃水浴放置20分钟后取出称重:44.0276g
装满新沸过蒸镏水置20℃水浴放置20分钟后称重:37.0293g
计算:
44.0276-12.0356
相对密度= = 1.28
37.0293-12.0356
1.3检验记录中,应先写明检验的依据。凡按《中国药典》、《局(部)颁药品标准》、《地方药品标准》或国外药典检验者,应列出标准名称、版本和页数;凡按送检者所附检验资料或有关文献检验者,应先检查其是否符合要求,并将前述有关资料的影印件附于检验记录之后,或标明归档编码。
1.4检验过程中,可按检验顺序依次记录各检验项目。内容包括:项目名称,检验日期,操作方法(如系完全按1.3检验依据中所载方法,可简略扼要叙述;但如稍有修改,则应将改变部分全部记录),实验条件(如实验温度、仪器名称型号和校正情况等),观察到的现象(不要照抄标准,而应简要记录检验过程中观察到的真实情况;遇有反常的现象,则应详细记录并鲜明标出,以便进一步研究),实验数据,计算(注意有效数字和数值的修约及其运算,详见《中国药品检验标准操作规范2014年版》)和结果判断等;均应及时、完整地记录,严禁事后补记或转抄。如发现记录有误,可用单线划去并保持原有的字迹可辨,不得擦抹涂改,并应在修改处签名或盖章,以示负责。检验或试验结果,无论成败(包括必要的复试),均应详细记录和保存。对废弃的数据或失败的实验,应及时分析其可能的原因,并在原始检验记录上注明。
品保成品检测原始记录模板
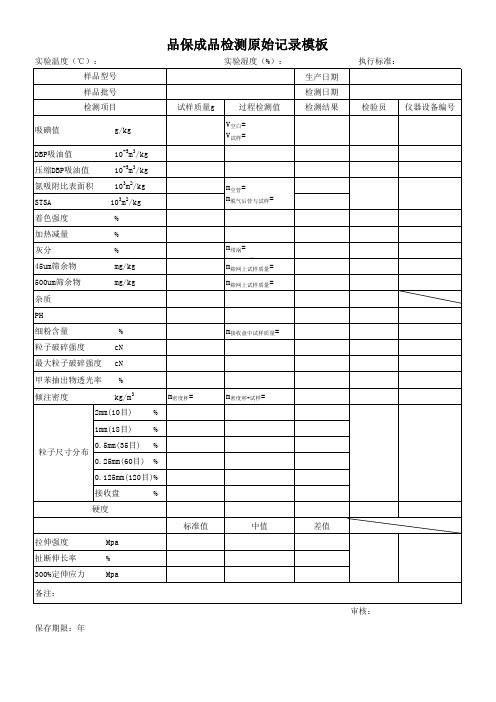
实验温度(℃): 样品型号 样品批号 检测项目
实验湿度(%):
试样质量g
过程检测值
生产日期 检测日期 检测结果
吸碘值
g/kg
DBP吸油值 压缩DBP吸油值 氮吸附比表面积 STSA 着色强度
10-5m3/kg 10-5m3/kg 103m2/kg 103m2/kg %
V空白= V试样=
m空管= m脱气后管与试样=
加热减量 灰分 45um筛余物 500um筛余物 杂质
% % mg/kg mg/kg
m坩埚= mm坩 筛埚网+上灰试=样质量=
m筛网上试样质量=
PH
细粉含量
%
粒子破碎强度
cN
m接收盘中试样质量=
最大粒子破碎强度 cN
甲苯抽出物透光率 %
倾注密度
kg/m3 2mm(10目)
m密度杯= %
m密度杯+试样=
1mm(18目) %
0.5mm(35目) % 粒子尺寸分布
0.25mm(60目) %
0.125mm(120目)%
接收盘
%
硬度
标准值
中值
差值%
300%定伸应力 Mpa
执行标准: 检验员 仪器设备编号
备注:
保存期限:年
审核:
食品出厂检验原始记录文本表格模板

编号:样品名称:生产日期:
样品数量:检验日期:
批量:规格:
1.感官
3.菌落总数
4.大肠菌群
优质参考资料
编号:样品名称:生产日期:
样品数量:检验日期:
批量:规格:
1.水分
2.食盐
优质参考资料
1.亚硝酸盐
2.可溶性无盐固形物
优质参考资料
编号:样品名称:生产日期:
样品数量:检验日期:
批量:规格:
1.氨基酸态氮
2.全氮
优质参考资料
检验员:复核
编号:样品名称:生产日期:
样品数量:检验日期:
批量:规格:
1.铵盐
2.总酸
优质参考资料
检验员:复核
编号:样品名称:生产日期:
样品数量:检验日期:
批量:规格:
1.总酸
2.不挥发酸
优质参考资料。
实验原始记录模板(检查)

实验原始记录模板(检查)预览说明:预览图片所展示的格式为文档的源格式展示,下载源文件没有水印,内容可编辑和复制实验原始记录模板(检查)温度:湿度:三、检查1. 水分标准:取本品内容物,照水分测定法(药典2005二部附录ⅧM 第一法A),以为溶剂,水分不得过%。
仪器:水分测定仪:结果:标定值: mg/ml RSD= % (附水分报告)2.干燥失重标准:照干燥失重法测定,于℃干燥至恒重,减失重量不得过%。
仪器:烘箱:恒温减压干燥箱:真空泵:电子天平:(感量0.1mg)方法:烘箱干燥法、恒温减压法、干燥器干燥法(分常压、减压两种)干燥剂:硅胶(显蓝色)、五氧化二磷(粉未状)、无水氯化钙(块状)结果:批号:单位:g公式:干燥失重(%)=(W0+W1-W3)/ W1×100% 结论:符合规定温度:湿度:3.(重量)装量差异标准:取本品20片(5瓶),按药典二部附录方法检查,限度为±%。
仪器:电子天平:感量0.1mg(适用于平均片重0.30g以下的片剂)感量1mg(适用于平均片重0.30g或0.30g以上的片剂)结果:重量差异(片剂)单位:g装量差异(粉针)单位:g公式:(重量)装量差异(%)=(W供- w平均)/ w平均×100%装量差异= - ~+ % 结论:符合规定4.酸度(碱度)标准:取供试品加水制成每1ml中含mg 的溶液,依法测定。
pH 值应为~。
仪器:酸度计:电子天平:供试液:g ―→ml结果:结论:温度:湿度:5. 溶液的澄清度与颜色、pH值标准:仪器:澄明度检测仪:酸度计:方法:取供试品5瓶, 分别按标示量加水制成每1ml 中含mg的溶液,与浊度标准液及标准比色液比较后,测定pH值。
供试液:每瓶加水ml结果:6. 不溶性微粒(例如)标准:每1.0g样品中含10μm以上的微粒不得过6000粒,含25μm以上的微粒不得过600粒方法:取本品3份,加微粒检查用水制成每1ml中含50mg的溶液,依法检查(中国药典2010年版二部附录IX C)仪器:微粒分析仪GWF-8JC温度:湿度:7. 可见异物仪器:澄明度检测仪:方法:灯检法、光散射法(深色透明容器或大于7号颜色)结果判定:5份供试品在静置一定时间后轻轻旋转时均不得检出烟雾状微粒柱,且不得检出金属屑、玻璃屑、长度或最大粒径超过2mm 纤维和块状物等明显可见异物。
明胶空心胶检验报告
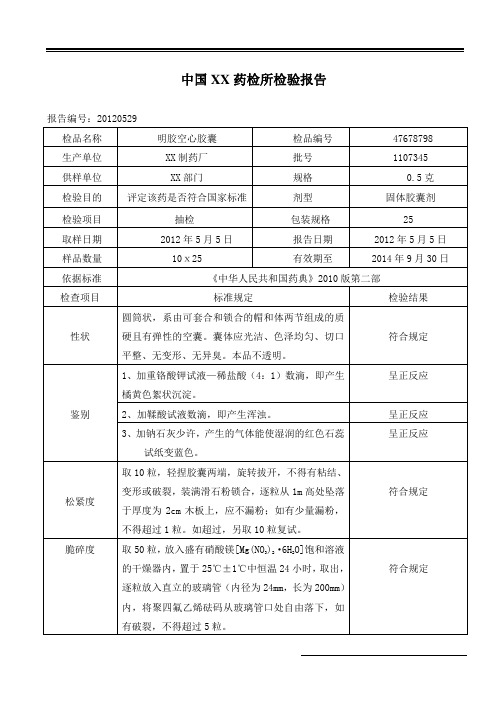
中国XX药检所检验报告报告编号:20120529检品名称明胶空心胶囊检品编号 47678798 生产单位XX制药厂批号1107345 供样单位XX部门规格0.5克检验目的评定该药是否符合国家标准剂型固体胶囊剂检验项目抽检包装规格25取样日期2012年5月5日报告日期2012年5月5日样品数量10ⅹ25 有效期至2014年9月30日依据标准《中华人民共和国药典》2010版第二部检查项目标准规定检验结果性状圆筒状,系由可套合和锁合的帽和体两节组成的质硬且有弹性的空囊。
囊体应光洁、色泽均匀、切口平整、无变形、无异臭。
本品不透明。
符合规定鉴别1、加重铬酸钾试液—稀盐酸(4:1)数滴,即产生橘黄色絮状沉淀。
呈正反应2、加鞣酸试液数滴,即产生浑浊。
呈正反应3、加钠石灰少许,产生的气体能使湿润的红色石蕊试纸变蓝色。
呈正反应松紧度取10粒,轻捏胶囊两端,旋转拔开,不得有粘结、变形或破裂,装满滑石粉锁合,逐粒从1m高处坠落于厚度为2cm木板上,应不漏粉;如有少量漏粉,不得超过1粒。
如超过,另取10粒复试。
符合规定脆碎度取50粒,放入盛有硝酸镁[Mg(NO3)2·6H2O]饱和溶液的干燥器内,置于25℃±1℃中恒温24小时,取出,逐粒放入直立的玻璃管(内径为24mm,长为200mm)内,将聚四氟乙烯砝码从玻璃管口处自由落下,如有破裂,不得超过5粒。
符合规定崩解时限取6粒,装满滑石粉,加挡板检查,应在10分钟内全部溶化或崩解。
符合规定黏度运动黏度不得低于60mm2/s。
符合规定亚硫酸盐(以SO2计)如显浑浊,与标准硫酸钾溶液3.75ml制成的对照液比较,不得更浓(0.01%)符合规定干燥失重12.5%~17.5%。
符合规定炽灼残渣不得过5.0%。
符合规定铬含铬不得过百万分之二。
符合规定重金属含重金属不得过百万分之四十。
符合规定细菌数法定标准为每1g不得过1000cfu。
符合规定霉菌和酵母菌数法定标准为每1g不得过100cfu。
化妆品企业微生物检验原始记录(国标法)

所用培养基及批号:□Baird Parker培养基□甘露醇发酵培养基
镜检
甘露醇发酵试验
血浆凝固酶试验
结果:□未检出(符合规定)
□检出(不符合规定)
结论:□检验合格□检验不合格
4、被检样品经增菌分离培养后,经证实为革兰氏阴性杆菌,氧化酶及绿脓菌素试验皆为阳性者,即可报告被检样品中检出铜绿假单胞菌;如绿脓菌素试验阴性而液化明胶、硝酸盐还原产气和42℃生长试验三者皆为阳性时,仍可报告被检样品中检出铜绿假单胞菌。
所用培养基及批号:□SCDLP液体培养基
□十六烷三甲基溴化铵琼脂培养基
2、如产酸产气,划线接种到伊红美蓝琼脂平板上,置36℃±1℃培养18h-24h。同时取该培养液1-2滴接种到蛋白胨水中,置44.5℃±0.5℃培养24h±2h。经培养后,在上述平板上观察有无典型菌落生长。平板上无菌落生长,可作出未检出耐热大肠菌群。耐热大肠菌群在伊红美蓝琼脂培养基上的典型菌落呈深紫黑色,圆形,边缘整齐,表面光滑湿润,常具有金属光泽。也有的呈紫黑色,不带或略带金属光泽,或粉紫色,中心较深菌落。挑取上述可疑菌落,涂片作革兰氏染色镜检。在蛋白胨水培养液中,加入靛基质试剂约0.5mL,观察靛基质反应。阳性者液面呈玫瑰红色,阴性反应液面呈试剂本色。根据发酵乳糖产酸产气,平板上有典型菌落,并经证实为革兰氏阴性短杆菌,靛基质试验阳性,则报告被检样品中检出耐热大肠菌群。
微生物检验记录
产品名称
产品批号
检验日期
年月日
检验类别
原料半成品成品
报告日期
年月日
供试液制备:取供试品□10g□10mL,加到90mL灭菌生理盐水中,混匀制成1:10供试液,下一级稀释采用10倍递增稀释法。
明胶成品检验原始记录

明胶成品检验原始记录1、水分测定:取本品①②,放置已知恒重①恒重:②恒重的铝制小盒中,加入蒸馏水10ml,膨胀30分钟,将小盒去盖放在红外灯下加热,将胶样溶解,然后蒸至基本干燥,然后放入105℃的干燥箱烘2小时,称重:①恒重:②恒重:。
计算:结果:。
(应≦14% )2、凝冻强度测定:取本品 g,加入 g纯化水配置成6.67%胶液,放置在10±0.1℃低温横槽内冷却16-18小时,直接用冻力仪测定读数:①。
②。
结果:。
()3、粘度测定:取本品 g,加蒸馏水 g膨胀2小时,放置60℃的水浴锅中加热15分钟振摇使其溶解,再在40℃的水中平衡10分钟,用粘度计吸取后再在40℃的水中平衡15分钟,然后用秒表测定读数:①。
②。
计算:结果:。
()4、透明度测定:取本品 g,配置成5%的胶液 ml,在40℃时倒入玻璃圆筒内,测定读数:。
5、灰分测定:取本品①②,放置已知恒重的瓷坩埚中①恒重:②恒重: ,用电炉子烤至完全炭化,放置600±50℃马弗炉中至完全灰化,称重:①恒重:②恒重:。
计算:结果:。
(应≦ 2.0% )6、二氧化硫测定:在500ml烧瓶内放入75ml蒸馏水和 g胶样溶胀后加入25ml(1+4)的硫酸溶液,连接冷凝管,在接收器内放入20ml(1+9)的过氧化氢,并中和至指示剂终点(在过氧化氢内加入2滴甲基红亚-甲基蓝指示剂,颜色呈浅紫色,用氢氧化钠中和至终点时,颜色呈草绿色),将冷凝管接管导入过氧化氢底部,加热煮沸三角烧瓶中的蒸馏水,收集80ml的馏出液,使接收器内总体积为100ml,补加甲基红亚-甲基蓝指示计1滴,用0.025mol/l 的氢氧化钠滴定液滴定至颜色为草绿色为终点。
计算:结果:。
(应≦150mg/kg )7、PH值测定:取本品 g,加蒸馏水 g配置成1%的胶液,在35℃时测PH值结果为:。
( 应在5.5—7.0 ) 8、水不溶物测定:取本品 g,加蒸馏水 g使之成500g胶液,将胶液通过已知恒重的玻璃坩埚:恒重:用真空抽滤泵抽滤,然后将坩埚置105-110℃的烘箱烘干称重:恒重:。
食品添加剂明胶生产企业卫生规范

山东省卫生厅卫生监督所 王桂春
主要内容(七部分) 主要内容(七部分)
总则
选址、 选址、设计与设施卫生要求 生产过程卫生要求
卫生质量检验要求
贮存与运输卫生要求 从业人员卫生要求 附则
第一章 总则
为加强食品添加剂明胶(以下简称" 第一条 为加强食品添加剂明胶(以下简称"明 生产企业的卫生监督管理, 胶")生产企业的卫生监督管理,保证产品的卫生 安全,依据《中华人民共和国食品卫生法》 安全,依据《中华人民共和国食品卫生法》和 食品添加剂卫生管理办法》的有关规定, 《食品添加剂卫生管理办法》的有关规定,制定 本卫生规范。 本卫生规范。 本规范规定了明胶生产企业的选址、 第二条 本规范规定了明胶生产企业的选址、 设计与设施、原料采购、生产过程、质量检验、 设计与设施、原料采购、生产过程、质量检验、 贮存与运输和从业人员的基本卫生要求和管理原 则。 从事明胶生产的企业都必须遵守本规范。 第三条 从事明胶生产的企业都必须遵守本规范。 明胶生产企业负责人是产品卫生安全的责任人, 明胶生产企业负责人是产品卫生安全的责任人, 应当承担确保产品卫生安全的责任。 应当承担确保产品卫生安全的责任。 第四条 各级人民政府卫生行政部门监督本规范 的实施。 的实施。
选址、设计与设施卫生要求(ቤተ መጻሕፍቲ ባይዱ选址、设计与设施卫生要求(续)
产品混配、 第十九条 产品混配、包装场所应具备空气 消毒和净化设施。采用紫外线消毒者应按30 消毒和净化设施。采用紫外线消毒者应按30 /10—15平方米设置,高于地面2米吊装。 15平方米设置 瓦/10 15平方米设置,高于地面2米吊装。 采用空气净化装置的生产车间, 采用空气净化装置的生产车间,其空气进风 口应远离排风口,距地面2.0米以上, 2.0米以上 口应远离排风口,距地面2.0米以上,附近 不得有污染源。 不得有污染源。 生产设施、电线管、水管、 第二十条 生产设施、电线管、水管、汽 管的安装,要防止水滴和冷凝物污染产品、 管的安装,要防止水滴和冷凝物污染产品、 容器。提倡自动化、管道化、封闭化生产。 容器。提倡自动化、管道化、封闭化生产。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
明胶成品检验原始记录
1、水分测定:取本品①②,放置已知恒重①恒
重:②恒重的铝制小盒中,加入蒸馏水10ml,膨胀30分钟,将小盒去盖放在红外灯下加热,将胶样溶解,然后蒸至基本干燥,然后放入105℃的干燥箱烘2小时,称重:①恒重:
②恒重:。
计算:
结果:。
(应≦14% )
2、凝冻强度测定:取本品 g,加入 g纯化水配置成6.67%胶液,放
置在10±0.1℃低温横槽内冷却16-18小时,直接用冻力仪测定读数:
①。
②。
结果:。
()3、粘度测定:取本品 g,加蒸馏水 g膨胀2小时,放置60℃的水浴
锅中加热15分钟振摇使其溶解,再在40℃的水中平衡10分钟,用粘度计吸取后再在40℃的水中平衡15分钟,然后用秒表测定读数:
①。
②。
计算:
结果:。
()4、透明度测定:取本品 g,配置成5%的胶液 ml,在40℃时
倒入玻璃圆筒内,测定读数:。
5、灰分测定:取本品①②,放置已知恒重的瓷坩埚中
①恒重:②恒重: ,用电炉子烤至完全
炭化,放置600±50℃马弗炉中至完全灰化,称重:①恒重:
②恒重:。
计算:
结果:。
(应≦ 2.0% )6、二氧化硫测定:在500ml烧瓶内放入75ml蒸馏水和 g胶样溶胀后加入
25ml(1+4)的硫酸溶液,连接冷凝管,在接收器内放入20ml(1+9)的过氧化氢,并中和至指示剂终点(在过氧化氢内加入2滴甲基红亚-甲基蓝指示剂,颜色呈浅紫色,用氢氧化钠中和至终点时,颜色呈草绿色),将冷凝管接管导入过氧化氢底部,加热煮沸三角烧瓶中的蒸馏水,收集80ml的馏出液,使接收器内总体积为100ml,补加甲基红亚-甲基蓝指示计1滴,用0.025mol/l 的氢氧化钠滴定液滴定至颜色为草绿色为终点。
计算:
结果:。
(应≦150mg/kg )7、PH值测定:取本品 g,加蒸馏水 g配置成1%的胶液,在35℃
时测PH值结果为:。
( 应在5.5—7.0 ) 8、水不溶物测定:取本品 g,加蒸馏水 g使之成500g胶液,将
胶液通过已知恒重的玻璃坩埚:恒重:用真空抽滤泵抽滤,然后将坩埚置105-110℃的烘箱烘干称重:恒重:。
计算:
结果:。
(应≦0.2% )9、铬的测定:取本品 g于坩埚中,精确至1.000g,使之加热炭化,放
冷,加浓硝酸数滴,慢慢加热,气体停止逸出时,移入马弗炉中600℃下加热之黑色颗粒全部消失,取出放冷,加入1mol/l硫酸10 ml和蒸馏水20ml,加热煮沸,滴加0.5%高锰酸钾溶液煮沸,如此反复直至紫红色不退色为止,
放冷,加10%尿素溶液10ml,剧烈振摇下滴加10%亚硝酸钠溶液,直至过量的高锰酸钾完全消除,溶液呈无色。
如二氧化锰明显存在则过滤。
把溶液移入50ml容量瓶中,加入0.5%焦磷酸钠溶液2ml,二苯碳酰二肼溶液0.5ml,摇匀,加纯水至刻度。
放置30分钟。
取上述溶液,在540nm波长处测定吸光度:
计算:
结果:。
(应≦2.0% )10、砷盐:样品砷斑制备:取本品 g,加淀粉 g与氧化钙 g
加水少量,搅拌均匀,干燥后,先用小火炽灼使炭化,再在600℃炽灼成灰白色,放冷,加盐酸8ml和水20ml溶解后置A反应瓶中。
标准砷斑制备:精密量取标准砷溶液2ml,置B反应瓶中,加盐酸5ml和水21ml.
A、B两瓶中分别加入碘化钾试液5ml与酸性氯化亚锡试液5滴,在室温放置
10分钟,加锌粒1.5g,立即将装妥的导气管密赛于反应瓶上,置25-40℃水浴中反应60分钟,取出溴化汞试纸比较:
结果:。
(应≦1mg/kg )11、重金属(以铅计):
取5项下炽灼残渣(500-600℃),加盐酸2ml和硝酸0.5ml,置水浴上蒸干,加水5ml再蒸干,加稀乙酸5ml与水20ml,温热数分钟加水适量使成50ml,,吸取25ml依法检查。
取50ml纳氏比色管两支,甲管中加入 ml标准铅溶液与稀乙酸2ml,加蒸馏水至25ml;乙管中加上述溶液25ml。
再在甲乙两管中加入硫化氢液各10ml,摇匀,在暗处放置10分钟,同置白纸上,自上而下透视,比较两管中的颜色。
结果:。
(应≦50mg/kg )
结论:
检验人:复核人:。
