甘草苷质量标准
甘草CHP、USP、BP、JP质量标准比较
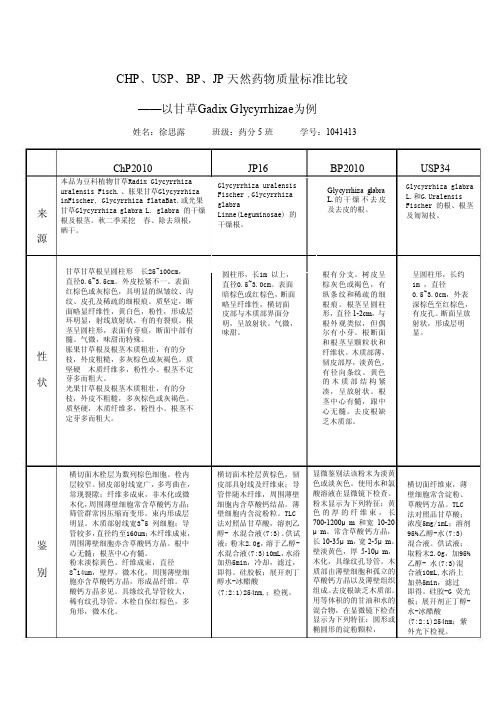
别鉴 状性 甘草甘草根呈圆柱形 25~100cm , 直径0.6~3.5cm 。
外皮松紧不一。
表面 红棕色或灰棕色,具明显的纵皱纹、沟 纹、皮孔及稀疏的细根痕。
质坚定,断 面略显纤维性,黄白色,粉性,形成层 环明显,射线放射状,有的有裂痕。
根 茎呈圆柱形,表面有芽痕,断面中部有 髓。
气微,味甜而特殊。
胀果甘草根及根茎木质粗壮,有的分 枝,外皮粗糙,多灰棕色或灰褐色。
质 坚硬 质纤维多,粉性小。
根茎不定 芽多而粗大。
光果甘草根及根茎木质粗壮,有的分 枝,外皮不粗糙,多灰棕色或灰褐色。
质坚硬,木质纤维多,粉性小。
根茎不 定芽多而粗大。
源来 Glycyrrhiza glabra L.和G.Uralensis Fischer 的根、根茎 及匍匐枝。
USP34BP2010本品为豆科植物甘草Radix Glycyrrhizauralensis Fisch.、胀果甘草Glycyrrhiza inFischer, Glycyrrhiza flataBat.或光果甘草Glycyrrhiza glabra L. glabra 的干燥根及根茎。
秋二季采挖 、除去须根, 晒干。
JP16ChP2010——以甘草Gadix Glycyrrhizae 为例显微鉴别法该粉末为淡黄色或淡灰色。
使用水和氯酸溶液在显微镜下检查。
粉末显示为下列特征:黄色的厚的纤维束,长700-1200μm 和宽10-20μm 。
常含草酸钙方晶,长10-35μm ,宽2-5μm 。
壁淡黄色,厚5-10μm ,木化,具缘纹孔导管。
木质部由薄壁细胞和孤立的草酸钙方晶以及薄壁组织组成。
去皮根缺乏木质部。
用等体积的的甘油和水的混合物,在显微镜下检查显示为下列特征:圆形或椭圆形的淀粉颗粒,Glycyrrhiza uralensis Fischer ,Glycyrrhiza glabraLinne(Leguminosae) 的 干燥根。
圆柱形,长1m 以上,直径0.5~3.0cm 。
甘草炮制方法与标准

甘草炮制方法与标准【药材来源】甘草为豆科植物甘草、胀果甘草或光果甘草的干燥根及根茎。
春、秋二季采挖,除去须根,晒干。
【古代炮制方法】汉代有炙焦为末(《玉函》)、微炒(《金匮》)的方法。
南北朝刘宋时代有“火炮令内外赤黄”、及用酒浸蒸后炙酥尽为度(《雷公》)的方法。
唐代有炙制(《千金方》)、蜜煎(《千金翼》)法。
宋代增加了炒存性(《博济》)、纸裹醋浸煨(《苏沈》)、淡浆水炙(《证类》)、盐水浸炙、猪胆汁浸炙、油浸炙(《总录》)、爁制(《局方》)、炮、黄泥裹煨(《朱氏》)等方法。
明、清时代又增加了炮再麸炒(《普济方》)、蜜炙(《医学》)、酥制(《纲目》)、涂麻油炙、姜汁炒、酒炒(《必读》)、长流水浸透,炭火炙(《大成》)、粳米拌炒(《得配》)、乌药煎汁吸入,去乌药(《从众录》)等炮制方法。
【现代炮制方法】1.甘草:取原药材,除去杂质,洗净,润透,带皮或刮去皮,切厚片,干燥。
筛去碎屑。
带皮者为甘草片,不带皮者为粉甘草片。
2.甘草梢:取净甘草,用刀剁下甘草的尾部(即细小部分),用水浸泡,切小段。
干燥,筛去碎屑。
3.蜜甘草:带皮者称炙甘草或炙草,不带皮者为炙粉草,或蜜粉草。
取炼蜜,加适量开水稀释后,淋入净甘草片或粉甘草片中拌匀,闷润,置炒制容器内,用文火加热,炒至老黄色,不粘手时,取出,晾凉。
甘草片每100kg用炼蜜25kg。
【饮片性状】甘草为类圆形或椭圆形厚片,或斜片。
表面黄白色,略显纤维性,中间有一较明显的棕色形成层环纹及放射状纹理,有裂隙,传统称为“菊花心”。
周边棕红色、棕色或灰棕色,粗糙,具纵皱纹。
质坚,有粉性。
气微,味甜而特殊。
甘草梢为类圆柱形小段,表面、断面、质地、气味均同甘草片。
蜜炙甘草表面老黄色,微有光泽,略带黏性,气焦香,味甜。
粉甘草表面淡黄色,显菊花纹,周边光洁,淡黄色,有刀削痕迹,质坚实、有粉性、气味同甘草。
【质量标准】甘草按干燥品计算,甘草水分不得过12.0%,总灰分不得过7.0%,酸不溶性灰分不得过2.0%,铅不得过百万分之五,镉不得过千万分之三,砷不得过百万分之二,汞不得过千万分之二,铜不得过百万分之二十。
028-甘草原料质量标准

文件名称甘草原料质量标准文件编码STP-ZL-YL-028-01制定人制定日期年月日复制日期年月日审核人审核日期年月日生效日期年月日批准人批准日期年月日复制份数颁发部门质量部分发部门质量部、生产设备部、物料部、普通饮片车间编订依据《中国药典》2015年版一部目的:制定甘草原料质量标准,规定检验项目及限度要求。
范围:适用于甘草原料。
职责:质量部、生产设备部、物料部、普通饮片车间。
内容:1、品名:甘草原料2、代码:Y01-0113、来源:本品为豆科植物甘草Glycyrrhiza uralensis Fisch.、胀果甘草Glycyrrhiza inflata Bat.或光果甘草Glycyrrhiza glabra L.的干燥根和根茎。
4、质量指标:4.1、性状甘草根呈圆柱形,长25~100cm,直径0.6~3.5cm。
外皮松紧不一。
表面红棕色或灰棕色,具显著的纵皱纹、沟纹、皮孔及稀疏的细根痕。
质坚实,断面略显纤维性,黄白色,粉性,形成层环明显,射线放射状,有的有裂隙。
根茎呈圆柱形,表面有芽痕,断面中部有髓。
气微,味甜而特殊。
胀果甘草根和根茎木质粗壮,有的分枝,外皮粗糙,多灰棕色或灰褐色。
质坚硬,木质纤维多,粉性小。
根茎不定芽多而粗大。
光果甘草根和根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
4.2、鉴别4.2.1显微鉴别照《显微鉴别法标准操作规程》(S0P-ZL-TY-003-01)测定。
本品横切面:木栓层为数列棕色细胞。
栓内层较窄。
韧皮部射线宽广,多弯曲,常现裂隙;纤维多成束,非木化或微木化,周围薄壁细胞常含草酸钙方晶;筛管群常因压缩而变形。
束内形成层明显。
木质部射线宽3〜5列细胞;导管较多,直径约至160μm,木纤维成束,周围薄壁细胞亦含草酸钙方晶。
根中心无髓;根茎中心有髓。
粉末淡棕黄色。
纤维成束,直径8〜14μm,壁厚,微木化,周围薄壁细胞含草酸钙方晶,形成晶纤维。
草酸钙方晶多见。
甘草数字质量标准的研究

甘草为豆科(Leguminosae)甘草属(Glycyrrihiza L.)多年生草本植物,根和根状供药用[1]。
世界甘草属植物有29种6变种,我国有17~18种3变种[2]。
《中国药典》2015版国家药典收摘甘草基原植物为甘草(Gly-cyrrhia uralensis Fisch),胀果甘草(Glycyrrhia.inflata Bat.)和光果甘草(Glycyrrhia.glabra L.)[3]。
其中甘草(Glyc-yrrhia uralensis Fisch)是我国资源分布最广,同时甘草酸含量最高的种[4]。
甘草属我国传统大宗药材,作为药物使用首载于西汉《五十二病方》,始载于东汉《神农本草经》[5]。
随着对甘草的不断开发,甘草在药理作用方面不断有新的发现,同时,甘草提取物被广泛地用于化工业、食品工业、化妆品等行业。
由于近20年来对野生甘草过度拆挖,甘草野生资源濒临枯竭,为满足市场的需要,国内各原甘草产区开始大量种植甘草,为进一步揭示甘草的内在质量,尽可能控制其内在质量特性,本研究依据甘草色谱特征,在生长过程中体内化学成分的变化,在符合《中国药典》2015版质量要求的基础上分析各类成分的代谢与积累,通过特异性外标物的确定,经对测试结果的统计学聚类分析,建立了数字图谱,以全信息控制甘草质量为目的,建立了甘草数字控制标准,补充了甘草质量全信息控制方法,为甘草及药材质量控制提供了新的方法。
1仪器与试药Waters1200液相色谱仪;岛津LC-2010A高效液相色谱仪;岛津SPD-M10Avp二极管阵列测器。
超声波清洗器(天津AUTOSCIENCE公司);sartorius225D 电子天平。
甘草酸单铵盐对照品(批号110731-201720),甘草苷(批号11610-201607)购自中国药品生物制品检定研究院;乙腈为色谱纯,磷酸为分析纯,水为二级反渗透实验用水,色谱柱:Hypersil C18(5μm,4.6mm×250mm);保护柱:Hypersil C18(5μm,4mm×40mm);甘草为Glycyrrhiza uralensis Fisch.将样品切头取1cm以下至0.3cm部分,样品产自甘肃省各主产区地区及宁夏、内蒙古等地。
甘草质量标准

甘草质量标准制疋人:日期:审核人:日期:批准人:批准日期:生效日期:________甘草GancaoRADIX GLYCYRRHIZAE本品为豆科植物甘草Glycyrrhiza uralensis Fisch. 、胀果甘草Glycyrrhiza inflata Bat. 或光果甘草Glycyrrhiza glabra L. 的干燥根及根茎。
春、秋二季采挖,除去须根,晒干。
[性状]甘草根呈圆柱形,长25〜100cm直径0.6〜3.5cm。
外皮松紧不一。
表面红棕色或灰棕色,具显著的纵皱纹,沟纹、皮孔及稀疏的细根痕。
质坚实,断面略显纤维性,黄白色,粉性,形成层环明显,射线放射状,有的有裂隙。
根茎呈圆柱形,表面有芽痕,断面中部有髓。
气微,味甜而特殊。
胀果甘草根及根茎木质粗壮, 有的分枝, 外皮粗糙, 多灰棕色或灰褐色。
质坚硬,木质纤维多,粉性小。
根茎不定芽多而粗大。
光果甘草根及根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
[鉴别](1)本品横切面:木栓层为数列棕色细胞。
栓内层较窄。
韧皮部射线宽广,多弯曲,常现裂隙;纤维多成束,非木化或微木化,周围薄壁细胞常含草酸钙方晶;筛管群常因压缩而变形。
束内形成层明显。
木质部射线宽3〜5列细胞;导管较多,直径约至160 口木纤维成束,周围薄壁细胞亦含草酸钙方晶。
根中心无髓;根茎中心有髓。
粉末淡棕黄色。
纤维成束,直径8〜14卩m壁厚,微木化,周围薄壁细胞含草酸钙方晶,形成晶纤维。
草酸钙方晶多见。
具缘纹孔导管较大,稀有网纹导管。
木栓细胞红棕色,多角形,微木化。
(2)取本品粉末1g,加乙醚40ml,加热回流1小时,滤过,药渣加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加水40ml使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,蒸干,残渣加甲醇5ml 使溶解,作为供试品溶液。
另取甘草对照药材1g,同法制成对照药材溶液。
再取甘草酸铵对照品,加甲醇制成每1ml含2mg的溶液,作为对照品溶液。
甘草检验操作规程

甘草检验操作规程目的:建立甘草的检验操作规程范围:适用于甘草的检验职责: QC主任及检验员执行标准:《中国药典》2020年版一部规程:1【性状】1.1 甘草:根呈圆柱形,长25~100cm,直径0.6~3.5cm。
外皮松紧不一。
表面红棕色或灰棕色,具显著的纵皱纹、沟纹、皮孔及稀疏的细根痕。
质坚实,断面略显纤维性,黄白色,粉性,形成环明显,射线放射状,有的有裂隙。
根茎呈圆柱形,表面有芽痕,断面中部有髓。
气微,味甜而特殊。
1.2 胀果甘草:根及根茎木质粗状,有的分枝,外皮粗糙,多灰棕色或灰褐色。
质坚硬,木质纤维多,粉性小。
根茎不定芽多而粗大。
1.3 光果甘草:根及根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
2【鉴别】2.1 鉴别(1)2.1.1 仪器与用具:显微镜、玻片。
2.1.2 操作步骤按药材(饮片)及成方制剂显微鉴别法标准操作规程操作。
本品横切面:木栓层为数列棕色细胞。
皮层较窄。
韧皮部射线宽广,多弯曲,常现裂隙;纤维多成束,非木化或微木化,周围薄壁细胞常含有草酸钙方晶;筛管群常因压缩而变形。
束内形成明显。
木质部射线宽3~5列细胞;导管较多,直径约至160µm;木纤维成束,周围薄壁细胞亦含有草酸钙方晶。
根中心无髓;根茎中心有髓。
粉末淡棕黄色。
纤维成束,直径8~14µm,壁厚,微木化,周围薄壁细胞含草酸钙方晶,形成晶纤维。
草酸钙方晶多见。
具缘纹孔导管较大,稀有网纹导管。
木栓细胞红棕色,多角形,微木化。
2.2 鉴别(2)2.2.1 试剂:乙醚、甲醇、正丁醇、甘草对照药材、甘草酸铵对照品、1%氢氧化钠、醋酸乙酯、甲酸、冰醋酸、1%硫酸乙醇。
2.2.2 仪器与用具:回流装置、量瓶(5ml、25ml、50ml)、锥形瓶、硅胶G薄板、展开缸、点样管、试管、三用紫外分析仪、电热恒温干燥箱、电子天平(1/10000)。
2.2.3 操作步骤:取本品粉末1g,加乙醚40ml,加热回流一小时,滤过,药渣加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加水40ml使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。
六味甘草丸中甘草苷的鉴别和含量测定

5 m) 分 析 柱 , 动 相 为 乙腈 一 . mo. 。 酸 , 速 l . n , 温 : 温 , 测 波 长 为 流 0 5 1L 醋 流 mL mi 柱 室 检
味甘 草丸 中甘草 苷的含 量 。
苷 对照 色谱位 置未 检 出相 同颜 色荧 光斑 点 。
2 2 甘 草 苷 的含 量 测 定 2 2 1 分 析 条 . . . 件 _ 色 谱 柱 : p riC 1 2 Hy es — 一 8柱 ( 5 mm × 4 6 l 20 . mm,
利思 ) 紫外可 见分光 光度 计 ( , TU一 8 0 北京 普析 通用 11 ,
仪 器 有 限 责 任 公 司 ) 甘 草 苷 ( 0 2 3 / 0 5 2 , 国 , 10 81 200 中
药品生 物制 品检验 鉴定 所含 量测 定用 ) 乙腈 (河 北赛 ,
瑞 科技 有 限公 司 ) 样 品 六 味 甘 草 丸 ( 院制 剂 室 自 , 本
2 2 2 实 验 方法 : 密 称 取 置 五氧 化 二 磷 干燥 . . 精 中干燥 1 h的甘 草苷 对 照 品适 量 , 流动 相 制 成 4 . 2 加 O 2 g mL 溶 液作 为对照 品 。 密称 取样 品 2 3 g・ 精 g置锥 形 瓶 中, 精密 加入 流 动相 乙腈一 . mo ・ 。 0 5 l L 醋酸 1 0 0 mL, 精密称 定 , 超声 3mi 放冷 , 0 n, 称定 重 量 , 流 动相补 足 用
甘草片、炙甘草质量标准及检验操作规程

XXXXXXXXXX成品质量标准及检验操作规程1 品名:1.1中文名:甘草片炙甘草1.2 汉语拼音:Gancaopian Zhigancao2 代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7净药材质量标准:8 检验操作规程:8.1 试药试剂:乙醚、甲醇、正丁醇、甘草对照药材、甘草酸铵对照品、1%氢氧化钠溶液、乙酸乙酯、甲酸、冰醋酸、10%硫酸乙醇溶液、0.2mol/L 醋酸铵溶液、甘草酸单铵盐对照品、乙腈、70%乙醇溶液、甘草苷对照品。
8.2 仪器设备:游标卡尺、显微镜、电子天平、回流装置、水浴锅、硅胶G薄层板、紫外灯、烘箱、原子吸收仪、马弗炉、超声波清洗器、高效液相色谱仪。
8.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
8.4 鉴别:8.4.1甘草片取本品制片置10×10显微镜下做显微观察。
8.4.2甘草片、炙甘草取本品粉末1g,加乙醚40ml,加热回流1小时,滤过,药渣加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加水40ml 使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,弃去水液,正丁醇液蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。
另取甘草对照药材1g,同法制成对照药材溶液。
再取甘草酸单铵盐对照品,加甲醇制成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1~2µl,分别点于同一用1%氢氧化钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15:1:1:2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点;在与对照品色谱相应的位置上,显相同的橙黄色荧光斑点。
8.5 检查:甘草片8.5.1水分:不得过11.0%(附录15第二法)。
凉茶产品中部分中药原料标准

凉茶产品中部分中药原料的质量标准一.金银花1.来源:本品为忍冬科植物忍冬Lonicera japonica Thunb.的干燥花蕾或带初开的花。
夏初花开前采收、干燥。
2.质量要求:2.1性状:本品呈棒状,上粗下细,略弯曲,长2~3cm,上部直径约3mm,下部直径约1.5mm。
表面黄白色或绿白色(贮久色渐深),密被短柔毛。
偶见叶状苞片。
花萼绿色,先端5裂,裂片有毛,长约2mm。
开放者花冠筒状,先端二唇形;雄蕊5个,附于筒壁,黄色;雌蕊1个,子房无毛。
气清香,味淡、微苦。
2.2鉴别:2.2.1薄层鉴别:取本品粉末0.2g,加甲醇5ml,放置12小时,滤过,滤液作为供试品溶液。
另取绿原酸对照品,加甲醇制成每1ml含1mg的溶液,作为对照品溶液,照薄层色谱法试验,吸取供试品溶液10~20μl,对照品溶液10μl,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶H薄层板上,以醋酸丁酯-甲酸-水(7:2.5:2.5)的上层溶液为展开剂,展开,取出,晾干,置紫光灯(365nm)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。
2.3检查:2.3.1水分:应为不得过12.0%。
2.3.2总灰分:应为不得过10.0%。
2.3.3酸不溶性灰分:应为不得过3.0%。
2.3.4重金属及有害元素:铅:不得过百万分之五;镉:不得过千万分之三;砷:不得过百万分之二;汞:不得过千万分之二;铜:不得过百万分之二十;2.4含量测定:本品按干燥品计算,含绿原酸(C16H18Ο9)不得少于1.5%。
本品按干燥品计算,含木犀草苷(C21H20Ο11)不得少于0.05%。
3.分布: 金银花分布于山东、河南、河北、湖南等地。
4.年产量: 约20000吨,其中目前饮料需求量约6000吨,其它为中成药和中药饮片使用。
当前贵公司选用的是烘干和晒干,且无硫磺薰的金银花。
二.甘草1.来源: 本品为豆科植物Glycyrrhiza uralensis Fisch.、胀果甘草Glycyrrhiza inflata Bat.或光果甘草Glycyrrhiza glabra L.的干燥根及根茎。
甘草原料检验操作规程

制药GMP管理文件一.目的:为规范甘草的检验标准和生产要求,特制定此标准。
二.适用范围:适用于中药材甘草的质量检验。
三.责任者:质量检验员四.正文:检品名称:甘草检验依据:《甘草内控质量标准》检验仪器:显微镜三用紫外分析仪干燥箱马弗炉高效液相色谱仪操作内容:【性状】甘草根呈圆柱形,长25~100cm,直径0.6~3.5cm。
外皮松紧不一。
表面红棕色或灰棕色,具显著的纵皱纹,沟纹、皮孔及稀疏的细根痕。
质坚实,断面略显纤维性,黄白色,粉性,形成层环明显,射线放射状,有的有裂隙。
根茎呈圆柱形.表面有芽痕,断面中部有髓。
气微,味甜而特殊。
━サ胀果甘草н根及根茎木质粗壮,有的分枝,外皮粗糙,多灰棕色或灰褐色。
质坚硬,术质纤维多,粉性小。
根茎不定芽多而粗大。
光果甘草∧根及根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
【鉴别】(1)本品横切面:木栓层为数列棕色细胞。
皮层较窄。
韧皮部射线宽广,多弯曲,常现裂隙;纤维多成束,非木化或微木化,周围薄壁细胞常含草酸钙方晶;筛管群常因压缩而变形。
束内形成层明显。
木质部射线宽3~5列细胞;导管较多,直径约至160μm;木纤维成束,周围薄壁细胞亦含草酸钙方晶。
根中心无髓;根茎中心有髓。
粉末淡棕黄色。
纤维成束,直径8~14μm,壁厚,微木化,周围薄壁细胞吉草酸钙方晶,形成晶纤维。
草酸钙方晶多见。
具缘纹孔导管较大,稀有网纹导管。
木栓细胞红棕色,多角形,微木化。
加热回流1小时,滤过,滤液蒸干,残渣加水40ml使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。
另取甘草对照药材1g,同法制成对照药材溶液。
再取甘草酸铵对照品,加甲醇制成每lml含2mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述三种溶液各1~2μl,分别点于同一用1%氢氧化钠溶液制备的硅胶G薄层板上,以醋酸乙酯-甲酸-冰醋酸-水(15:1:1:2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365nm)下检视。
甘草提取物指标

甘草提取物指标甘草提取物是从甘草根部提取的一种天然草药成分,具有广泛的药用价值。
甘草提取物的质量可以通过一系列指标来评估,以下是一些常见的甘草提取物指标。
一、甘草酸含量甘草酸是甘草提取物中最重要的有效成分之一,具有抗炎、抗氧化、抗菌等作用。
甘草酸含量是评估甘草提取物质量的重要指标之一。
一般来说,甘草酸含量越高,说明甘草提取物的质量越好。
二、甘草素含量甘草素是甘草提取物中的另一种重要成分,具有抗炎、抗氧化、抗菌等作用。
甘草素含量也是评估甘草提取物质量的重要指标之一。
与甘草酸不同的是,甘草素含量越低,说明甘草提取物的质量越好。
三、甘草甜素含量甘草甜素是甘草提取物中的一种甜味成分,具有增加甜味、增强口感的作用。
甘草甜素含量是评估甘草提取物质量的重要指标之一。
一般来说,甘草甜素含量越高,说明甘草提取物的甜味越强。
四、重金属含量重金属是指相对密度较高的金属元素,如铅、汞、镉等。
重金属的含量过高会对人体健康产生不良影响。
因此,评估甘草提取物质量的一个重要指标就是重金属含量。
一般来说,重金属含量越低,说明甘草提取物的质量越好。
五、微生物限度微生物限度是评估甘草提取物是否符合卫生标准的重要指标之一。
微生物限度包括总菌落数、霉菌和酵母菌的数量。
过高的微生物限度可能导致甘草提取物发生变质,造成质量问题。
六、水分含量水分含量是评估甘草提取物质量的重要指标之一。
水分含量过高可能导致甘草提取物受潮变质,影响其药效和保质期。
七、酸度和碱度酸度和碱度是评估甘草提取物酸碱性的重要指标之一。
酸度和碱度的平衡有利于甘草提取物的稳定性和药效。
甘草提取物指标涉及甘草酸含量、甘草素含量、甘草甜素含量、重金属含量、微生物限度、水分含量以及酸度和碱度等。
这些指标能够全面评估甘草提取物的质量,确保其安全有效地应用于医药、保健品等领域。
对于生产商和消费者而言,了解这些指标对于选择和使用甘草提取物具有重要意义。
成品药材甘草质量标准

杂质、灰屑检查不得过3.0%。
二氧化硫残留量不得过150mg/kg。
总灰分不得过7.0%(附录Ⅸ K)。
酸不溶性灰分不得过2.0%(附录Ⅸ K)。
重金属及有害元素照铅、镉、砷、汞、铜测定法(附录Ⅸ B原子吸收分光光度法或电感耦合等离子体质谱法)测定,铅不得过百万分之五,镉不得过千万分之三,砷不得过百万分之二,汞不得过千万分之二,铜不得过百万分之二十。
本品按干燥品计算,含甘草苷(C21H22O9)不得少于0.50%;甘草酸(C42H62O16)不得少于2.0%。
【性味与归经】甘,平。归心、肺、脾、胃经 。
【功能与主治】补脾益气,清热解毒,祛痰止咳,缓急止痛,调和诸药。用于脾胃虚弱,倦怠乏力,心悸气短,咳嗽痰多,脘腹、四肢挛急疼痛,痈肿疮毒,缓解药物毒性、烈性。
粉末淡棕黄色。纤维成束,直径8~14µm,壁厚,微木化,周围薄壁细胞含草酸钙方晶,形成晶纤维。草酸钙方晶多见。具缘纹孔导管较大,稀有网纹导管。木栓细胞红棕色,多角形,微木化。
(2)取本品粉末1g,加乙醚40ml,加热回流1小时,滤过,弃去醚液,药渣加甲醇30ml,加热加流1小时,滤过,滤液蒸干,残渣加水40ml使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,弃去水液,正丁醇液蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。另取甘草对照药材1g,同法制成对照药材溶液。再取甘草酸单铵盐对照品,加甲醇制成每1ml含2mg的溶液,作为对照品溶液。照薄层色谱法(附录Ⅵ B)试验,吸取上述三种溶液各1~2µl,分别点于同一用1%氢氧化钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15:1:1:2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点;在与对照品色谱相应的位置上,显相同的橙黄色荧光斑点。
甘草质量标准及检验操作规程
XXXXXX有限公司原料质量标准及检验操作规程1 品名:1.1 中文名:甘草1.2 汉语拼音:Gan cao2 代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7 检验操作规程:7.1 试药与试剂:乙醚、甲醇、水、正丁醇、甘草对照药材、甘草酸单铵盐对照品、甘草苷对照品、甘草酸铵对照品、氢氧化钠、乙酸乙酯、甲酸、冰醋酸、乙腈、磷酸、硫酸、乙醇。
7.2 仪器与用具:显微镜、电子天平、硅胶G薄层板、水浴锅、三用紫外分析仪、恒温鼓风干燥箱、马福炉、原子吸收仪、气相色谱仪、高效液相色谱仪、超声波清洗器。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:7.4.1 取本品制片置10×10显微镜下做显微观察。
7.4.2取本品粉末1g,加乙醚40ml,加热回流1小时,滤过,弃去醚液,药渣加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加水40ml使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,弃去水液,正丁醇液蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。
另取甘草对照药材1g,同法制成对照药材溶液。
再取甘草酸单铵盐对照品,加甲醇制成每1ml 含2mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1~2µl,分别点于同一用1%氢氧化钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15 : 1 : 1 : 2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点;在与对照品色谱相应的位置上,显相同的橙黄色荧光斑点。
7.5 检查:7.5.1水分:不得过12.0%(附录15第二法)7.5.2总灰分:不得过7.0%(附录17)7.5.3酸不溶性灰分:不得过2.0%(附录17)7.5.4二氧化硫残留量:照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
甘草药材标准检验操作规程

甘草药材标准检验操作规程本品为豆科植物甘草Glycyrrhiza uralensis Fisch.、胀果甘草Glycyrrhiza inflata Bat.或光果甘草Glycyrrhiza glabra L.的干燥根和根茎。
春、秋二季采挖,除去须根,晒干。
【性状】甘草根呈圆柱形,长25~100cm,直径0.6~3.5cm。
外皮松紧不一。
表面红棕色或灰棕色,具显著的纵皱纹、沟纹、皮孔及稀疏的细根痕。
质坚实,断面略显纤维性,黄白色,粉性,形成层环明显,射线放射状,有的有裂隙。
根茎呈圆柱形,表面有芽痕,断面中部有髓。
气微,味甜而特殊。
胀果甘草根和根茎木质粗壮,有的分枝,外皮粗糙,多灰棕色或灰褐色。
质坚硬,木质纤维多,粉性小。
根茎不定芽多而粗大。
光果甘草根和根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
【鉴别】(1)本品横切面:木栓层为数列棕色细胞。
栓内层较窄。
韧皮部射线宽广,多弯曲,常现裂隙;纤维多成束,非木化或微木化,周围薄壁细胞常含草酸钙方晶;筛管群常因压缩而变形。
束内形成层明显。
木质部射线宽3~5列细胞;导管较多,直径约至160μm;木纤维成束,周围薄壁细胞亦含草酸钙方晶。
根中心无髓;根茎中心有髓。
粉末淡棕黄色。
纤维成束,直径8~14μm,壁厚,微木化,周围薄壁细胞含草酸钙方晶,形成晶纤维。
草酸钙方晶多见。
具缘纹孔导管较大,稀有网纹导管。
木栓细胞红棕色,多角形,微木化。
(2)取本品粉末1g,加乙醚40ml,加热回流1小时,滤过,弃去醚液,药渣加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加水40ml 使溶解,用正丁醇提取3次,每次20ml,合并正丁醇液,用水洗涤3次,弃去水液,正丁醇液蒸干,残渣加甲醇5ml使溶解,作为供试品溶液。
另取甘草对照药材1g,同法制成对照药材溶液。
再取甘草酸单铵盐对照品,加甲醇制成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法(通则0502)试验,吸取上述三种溶液各1~2μl,分别点于同一用1%氢氧化钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15:1:1:2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365nm)下检视。
2008甘草质量标准
1、品名:甘草Radixet RhizomaGlycyrrhizae
2、药用部位:豆科植物甘草Glycyrrhiza uralensis Fisch.、胀果甘草Glycyrrhiza inflata Bat.或光果甘草Glycyrrhiza.的干燥根及根茎。
3、规格标准
项目名称Βιβλιοθήκη 单位合格品标准内控标准
检验依据
性状
甘草:根呈圆柱形,长25-100cm,直径0.6 –3.5cm。外皮松紧不一。表面红棕色或灰棕色,具显著的纵皱纹、沟纹、皮孔及稀疏的细根痕。质坚实,断面略显纤维性,黄白色,粉性,形成层环明显,射线放射状,有的有裂隙。根径呈圆柱形,表面有芽痕,断面中部有髓。气微,味甜而特殊。
胀果甘草:根及根茎木质粗壮,有的分枝,外皮粗糙,多灰棕色或灰褐色。质坚硬,木质纤维多,粉性小。根茎不定芽多而粗大。
8、复验周期:六个月。
光果甘草:根及根茎质地较坚实,有的分枝,外皮不粗糙,多灰棕色,皮孔细而不明显。
同合格品
《中国药典》2005版一部P59.
鉴别
(1)特征明显(2)呈正反应
同合格品
水分
%
≤12.0
≤10.0
总灰分
%
≤7.0
≤6.0
酸不溶性灰分
%
≤2.0
≤1.8
重金属及有害元素
%
铅≤5ppm;镉≤0.3ppm;砷≤2ppm;汞≤0.2ppm;
铜≤20ppm;
同合格品
有机氯农药残留量
PPm
六六六≤0.2ppm;DDT≤0.2ppm;PCNB≤0.1ppm;
同合格品
4、采收及加工标准:每年春、秋二季采挖,除去须根,晒干。
5、炮制标准:取甘草,除去杂质,洗净,润透,切厚片,干燥。
炮制辅料甘草汁的质量标准研究

31218样品的含量测定取10家饮片厂生产的10个批号甘草饮片制备甘草汁按3121212法制备供试品溶液甘草汁相关项目测定结果厂家产地批次ph值相对密度总固体甘草苷浓度甘草酸浓度甘草次酸浓度安徽神州山西8071188551411107271011424016802113863012511安国市祁瑞山西09030551561106531010726019463116668013856vol厂家产地批次ph值相对密度总固体甘草苷浓度甘草酸浓度甘草次酸浓度安徽海鑫山西08111051841108191012295016857113553012774安徽省万生内蒙09060151491107431011577017485115146014382安国市金康迪内蒙2008030151471107791011916017513115282013905安国市神禾甘肃2009020151431106781010965016817113974013004亳州市京皖内蒙2009040151701107521011661017074114643013624山西浑源万生山西08120351781107921012038017251114527013538河北康派山西09050851651106611010799016855113772012822安国市京兴甘肃2008051351751108091012196016761113841012966平均值51611107411011560017288114527013338甘草汁为甘草饮片加水煎煮去渣浓缩至甘草115倍量的黄棕色至深棕色液体其ph值在5141517510107261012295范围其平均值分别为5161110741和1011560
甘草中甘草素的质量检测研究.

HPLC法测定不同产地甘草中甘草苷的含量方法一:建立甘草中甘草苷含量测定的HPLC法,测定不同产地甘草中甘草苷的含量,以控制其质量。
[方法]HPLC色谱条件为分析柱为Kromasil C18柱(4.6 mm×25 cm,5μm);流动相为乙腈-0.5%醋酸溶液(V/V,1∶4);流速为1.0 ml/min;柱温为25℃;紫外检测波长为270 nm;采用外标法定量测定。
[结果]甘草苷在0.1~1.2μg范围内呈良好的线形关系(r=0.999 9),其平均加样回收率和RSD值分别为97.86%和2.04%(n=6)。
[结论]该方法操作简单、准确、快速、重现性好,可作为甘草苷的定量分析方法。
色谱条件的确定。
HPLC色谱条件为:分析柱为Kro-masil C18柱(4.6 mm×25 cm,5μm);流动相为乙腈-0.5%醋酸溶液(V/V,1∶4);流速为1.0 ml/min;柱温为25℃;紫外检测波长为270 nm;采用外标法定量测定。
1.2.2对照品溶液的制备。
取适量甘草苷对照品,溶于甲醇制成0.15 mg/ml的对照品溶液。
1.2.3供试品溶液的制备。
取供试样品0.25 g,置于50 ml量瓶中,加40 ml 70%甲醇,超声处理45 min,放冷,滤过,加70%甲醇定容置刻度,摇匀,静置,即得。
HPLC法测定甘草酸和甘草苷的含量*:方法二:建立以HPLC法同时测定甘草中甘草酸和甘草苷含量的方法。
方法:采用C18柱(4.6mm×15cm,5μm)为分析柱;以乙腈—1%醋酸溶液为流动相;流速为0.6 ml·min-1;柱温25℃;采用外表法定量测定。
结果表明甘草酸在4.16-28.0μg/ml范围内,回归方程为Y=10562.8X+30963(r=0.9999);甘草苷在13.0-23.4μg/ml范围内,回归方程为Y=12857.4X+16437(r=0.9997),平均加样回收率均大于96.08%,日内、日间的RSD值分别小于1.41%和1.85%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
甘草苷质量标准
1仪器与试药
LC??20A高效液相色谱仪,可变紫外检测器(日本岛津)。
111610??200503);止嗽丸为实验室样品;甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2方法与结果
2.1色谱条件
色谱柱:HypersilC18柱(5μm;4.0mm×250mm):流动相:乙腈??0.5%冰醋酸(体积比20∶80);流速1.1mL/min;检测波长276nm;柱温30℃;进样量:10μL。
取甘草苷对比品适量,加体积分数70%乙醇制成每1mL含20μg的溶液,即得。
2.3供试品溶液的制备
取本品粉末约1g,置具塞锥形瓶中,周密加入体积分数70%乙醇
100mL,称定重量,超声处理30min,取出,再称定重量,用体积分数70%乙醇补足减失的重量,滤过,即得。
2.4方法的专属性考察
在上述的色谱条件下,将甘草苷对比品溶液、供试品溶液、甘草阴性
对比溶液注入液相色谱仪中,得HPLC图(见图1),结果显示阴性对
比无干扰。
A.甘草苷对比品;
B.止嗽丸样品;
C.甘草阴性对比
图1HPLC图谱(略)
Figure1HPLCchromatograms
2.5线性关系的考察
周密称取甘草苷对比品适量,加流动相制成每1mL分别含甘草苷
2.001、4.002、10.00、20.01、40.02、200.1μg的溶液,分别吸取10μL进样测定峰面积。
以峰面积为纵坐标,对比品的质量浓度为横坐标,绘制标准曲线,计算得回归方程:y=29543x+144.52,r=1.000。
表明甘草苷进样量在0.020~2.001μg范围内与峰面积呈良好的线形关系。
论文百事通
2.6周密度试验
分别取对比品溶液10μL,连续进样5次,测定峰面积,计算得甘草苷的峰面积RSD分别为0.4%。
2.7重复性试验
周密称取同一批号样品,按供试品溶液制备方法平行制备5份,依法测定,计算甘草苷含量RSD值为0.6%。
2.8稳定性试验
取同一供试品溶液,于0、2、3、4、6、8、11、24h进样测定,计算得甘草苷的峰面积的RSD为1.0%,表明样品溶液在24h内稳定。
2.9加样回收率试验
分别周密称取已知含量(含量为1.312mg/g)的本品适量6份,分别周密加入甘草苷对比品溶液(0.2001mg/mL)各3mL,按”2.3”项下方法制得供试品溶液。
分别吸取上述供试品溶液各10μL,注入液相色谱仪,测定其中甘草苷的总量,与止嗽丸中应含有的甘草苷总量实行比较,计算回收率,结果见表1。
表1甘草苷回收率试验测定结果(略)
br1Resultsofrecoverytest
2.10样品测定
分别周密称取不同批号的止嗽丸适量,按“2.3”项下方法制备溶液,按“2.1”项下色谱条件实行HPLC分析,结果3个批号的样品所测得
的平均含量为1.312、1.323、1.298mg/g。
3讨论
甘草中的黄酮类成分具有抗氧化、抗病毒、抗炎、抗溃疡作用[1]。
甘草苷是甘草的黄酮类成分之一,也是止嗽丸治疗疾病的活性成分,
故选择甘草苷作为该制剂的定量指标。
通过参考文献[2-5]并实行实验,选用乙腈??0.5%醋酸(体积比
1∶4)为流动相,能很好地将甘草样品中的甘草苷分离出来。
甘草苷可溶于乙醇、甲醇和水等溶剂,但因溶剂极性的不同,其溶解
度也不同,参考《中国药典》2005年版一部甘草项下甘草苷的提取方法,选用体积分数70%乙醇作为提取溶剂[2],提取效率高。
另外,对比品及阴性对比的制备同样采纳体积分数70%乙醇为溶剂,确保与
供试品平行一致,且该溶剂低毒环保。
新晨范文网
本法简便、快速、专属性强、重现性好,可作为止咳丸的质量操纵方法。
【参考文献】
[1]贾国惠,贾世山.甘草中黄酮的药理作用研究进展[J].中国
药学杂志,1998,33(9):513-514.
[2]国家药典委员会.中华人民共和国药典:2005年版一部[M].北京:化学工业出版社,2005:60.
[3]李仁秋.高效液相色谱法测定新止咳合剂中甘草苷的含量[J].
云南中医中药杂志,2008,29(2):35-36.
[4]闫永红,王文全,杨娜.HPLC测定栽培甘草中甘草苷的含量[J].中国中药杂志,2006,31(11):926-927.
[5]伍蔚萍,阎宏涛,孙文基.HPLC法测定甘草中甘草苷的含量[J].药物分析杂志,2004,24(4):425-427
甘草苷质量标准。
