初中化学1思维导图全册
初中化学思维导图

第一单元走进化学世界思维导图
编辑版word
第二单元我们周围的空气思维导图
编辑版word
第三单元物质构成的奥秘思维导图
编辑版word
编辑版word
第四单元自然界的水思维导图
编辑版word
第五单元化学方程式思维导图
编辑版word
第六单元碳与碳的氧化物思维导图
编辑版word
第七单元燃料及其利用思维导图
编辑版word
第八单元金属和金属材料思维导图
编辑版word
第九单元溶液思维导图
编辑版word
编辑版word
第十单元酸和碱思维导图
编辑版word
第十一单元盐化肥思维导图
编辑版word
编辑版word
第十二单元化学与生活思维导图
编辑版word
编辑版word
编辑版word
1、征服畏惧、建立自信的最快最确实的方法,就是去做你害怕的事,直到你获得成功的经验。
2、忍别人所不能忍的痛,吃别人所别人所不能吃的苦,是为了收获得不到的收获。
就像驴子面前吊着个萝卜就会往前走。
正因为有那个目标,你才有劲儿往前走。
编辑版word
编辑版word
(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,供参考,感谢您的配合和支持)
编辑版word。
(人教版)初中化学全册思维导图(知识点版)+初中化学知识点总结
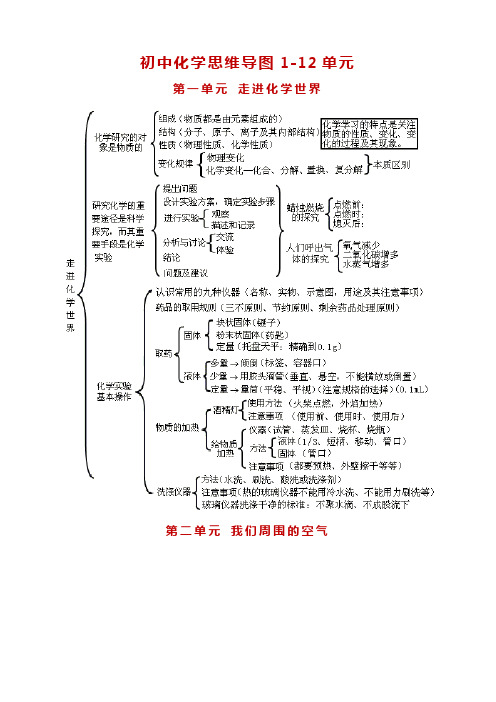
初中化学思维导图1-12单元第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料第九单元溶液第十单元酸碱第十一单元盐化肥第十二单元化学与生活初中化学知识点总结1、单质:非惰性气体一般由两个原子组成:F2,O2,H2,Cl22、惰性气体:一般由一个原子组成:He,Ne,Ar,Kr,Xe3、化合物:氢化物居多:H2S,HCl,H3P,HF,HBr,HI(一)、固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁(二)、液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢等气体。
(一)质量增加的1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸;2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜;3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙;(二)质量减少的1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水;2、由于风化而减少的:碳酸钠晶体。
(一)、气体的检验1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.4、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气.5、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气.(二)、离子的检验.。
初中化学-思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第一单元走进化学世界思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第二单元我们周围的空气思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第三单元物质构成的奥秘思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第四单元自然界的水思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第五单元化学方程式思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第六单元碳与碳的氧化物思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第七单元燃料及其利用思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第八单元金属和金属材料思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第九单元溶液思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第十单元酸和碱思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第十一单元盐化肥思维导图
———————欢迎下载,祝您学习进步,成绩提升———————第十二单元化学与生活思维导图。
初中化学思维导图
第一单元走进化学世界思维导图
完美DOC格式整理
第二单元我们周围的空气思维导图
完美DOC格式整理
第三单元物质构成的奥秘思维导图
完美DOC格式整理
完美DOC格式整理
第四单元自然界的水思维导图
完美DOC格式整理
第五单元化学方程式思维导图
完美DOC格式整理
第六单元碳与碳的氧化物思维导图
完美DOC格式整理
第七单元燃料及其利用思维导图
完美DOC格式整理
第八单元金属和金属材料思维导图
完美DOC格式整理
第九单元溶液思维导图
完美DOC格式整理
完美DOC格式整理
完美DOC 格式整理
第十单元 酸和碱 思维导图
第十一单元盐化肥思维导图
完美DOC格式整理
完美DOC格式整理
第十二单元化学与生活思维导图
完美DOC格式整理
完美DOC格式整理。
(完整版)初中化学思维导图(可编辑修改word版)

身边的化学物质形成悬浊液 乱油液溶解性:在某溫度,压强下,一种物质在另一种物质里溶解能力的大小 槪念饱和溶液,不饱和溶液转化槪念:溶质质量与溶液质量之比 公式计算空气的成分(体R 分数> R 气的ft®及用途MW 气体的11®及用i« 空气、氧气 氣't 空,®量LJB 的主赛》«1容(空气污M «'<-= ^VS, 5气《量纽期、空气®量状况> 史气獨量B 緝 丨什乂gn/G 染IHB 的项冃:MM , co 、NOi.珂吸入_輪物,O >««_与非会《««反应・c . s. r. in• i 、与金属_质氏曲1 Fe ・Al. Ca与化学tt 反fib CH4. CUIMIII| niit <支N«ct.供给柙明) 实W 审 W 法I KMnO4 . KCIO3、HlOl物现矜城1无&.无味.不易番;于•水.»度比g 气大 I 收《枝:分興®态空气&初中似性质组成:电解分解净化:静置沉淀、过滤,吸附、蒸® 硬水与软水区分、危害、转化 用途 保护水资源:节约用水,防治水污染氬气物理性质:无色无味,难溶于水,所有气体密度嚴小的气体 性质 化学性质:可燃性(不纯燸炸)、还原性 用途:氢能源、氢气球、冶金 制取溶液:均一、稳定溶质 溶剂水,溶液 溶液 与浓、稀溶液的关系溶解度固体的溶解度气体的溶解度槪念影晌因素 外因:温度内因:溶质溶剂的性质溶解度曲线槪念彩响因索结晶:固体物质从溶液中析出晶体的过程莰发结晶 冷却热饱和溶液溶液的溶质质■分数无色透明正八面体形状固阼金刚石J 天然物质中最硬的物质 L —可作钻头、装饰品、玻璃刀头 (-深灰色磷片状固阼,不透明,石墨质软—作铅笔芯 S-s 滑鼠感—作润滑剤物理性质 导电性—作电极及用途木炭、活性炭:吸附性—作净水剤、防橐面具滤春剤广①一般愔况下不燃烧也不支持燃烧② 不供给呼吸③ 与水反应:H 2CO 3=H 2O+CO 2H 2O+CO2= H2CO3 化学性质J ④与喊反应:Ca (OH )2+CO 2=CaCO 3 \ +H 20⑤光合作用:6CO 、+6HoO_ 光眩 C 6H 12O 6+6O 2叶妹京、⑥氧化性:CO 2+C=^2CO用途:①灭火②干冰用于人工降雨、作致冷剤③碳酸饮料 ④温室肥料⑤工业原料制法:①CaCO 3+2HCl=CaCl2+H 2O+CO21 (实验室)② CaCO 3=^=CaO+ C021 (工业制法)温室效应:温室气体包括C02、03、CH4、氣氳代烷等、C02在自然界的循环:即产生和消耗的途径物理性质:无色无味气体,密度比空气略小,难滔于水①可燃性:2CO+O 2=^=2CO 2化学性质4 ②还原性:CO+CuO=^=Cu+CO 2③砉性:极易与血红蛋白r _造矽机怍鈸氧 L 用途:①作燃料②冶炼金厘单质: (金刚石、 Ceo:石墨、 C+O 2=^=CO 2 (充分燃烧) 2C+O 2=^=2CO (不充分'鵬)2CuO+C^=2Cu+CO 2t (现象:黒色粉末变成红色,澄潛石灰水变浑浊)物理性质:无色无味气体,密度比空气大,易溶干水,固阼叫 <干冰易JI 化可作燃料CO 2+C=^=2CO可冶炼金厘物理性质:大部分常溫下固体,具有金厲光潘,电和热的良导体,錄 较好的延展性,密度大,熔沸点较S 用途-性质溉念-•混合物硬度: >纯金展合金合金与纯金属性质差异熔点:〈纯金属 抗腐蚀性: >纯金展 常见的合金(含碳量,生铁〉钢)寻找金風®代品金厲材科金属的化学性质金质与金质材料反应类型:置换反应反应类型:置换反应 反应条件:前換后 窻义应用铁的冶炼(CO 还原Fe203)金厲资源在自然界的存在 单质:金矿石:磁铁矿、赤铁矿 金属资源的利用和保护铁的锈蚀与防护•保护金風资源的措施防止金属生锈回收利用废旧金属 有计划合理开采矿物 与氯气反应活泼金属与黢反应与盐溶液的反应金厲活动性顾序表浓盐酸-挥发性浓硫酸-吸水性、强腐蚀性,强氧化性,稀释 指示剂:紫色石S 变红,无色酚酞不变色 +活泼金属~»益+水♦金風组化物■♦益+水 +減>*盐+水♦某些盐"♦新益♦水指示剂:紫色石蕊变蓝,无色酚酞变红+非金展氣化物■♦益+水 +酸-»盐+水+某些盐-♦新盐+水 弦定义:金属离子/NH3++M 根离子 NaCI. Na2CO3、NaHCO3、CaCOMl 质与用途 定义 氮肥:尿素等 磺肥:矿粉等 钾肥:草木灰等复合使!用途 化学肥料常见化肥酸碱性: 蛇碱度用梅示剂检验槪念:定量表示酸碱性 表示方法:pH測定pH 的方法:用干净的玻璃棒程取被測溶液 并滴在pH 试纸上,半分钟后对比试纸与 标准比色卡的顔色 改变溶液pH 的方法通性格动的拥子益及化学肥科通性:阴离子:0H-金風离子/NH3++0H-溶液的黢碱性与酸碱度相0H 性质、俗称,用途 Sa (OH) 2性质、俗秣、 MUH2O混合物纯净物单质化合物分子离子分子是保持物质化学性质的最小粒子性质:质量体积小,不断运动,有间隔,可分割表示方法原子是化学变化中最小的粒子性质:质ft体积小,不断运动,有间隔,可分割表示方法:元紊符号结构带电的原子或原子团分类:阴阳离子表示方法离子与原子的相互转化具有相同核电荷数即核内电子数的一类原子的总数元素的存在形式:单质、化合物元素的表示方法元素与原子的关系:总体和个体元素周期表:7周期16族化学式化合价元素符号和数字组成表示物质组成的式子一种元素一定数目的原子跟其他元素一定数目相化合的性质. 叫做这种元素的化合价表示方法物理变化槪念參加反应的各种物质的质量总和=反应后的各物质的质量总和五个不变物质的变化化学变化物质的变化和性质物质的性质燃烧与灭火遇守质量守恒定律两个一定变两个可能变宏观:反应物.生成物的总量不变;元承的种类不变、微观:原子的种类、数目,质■不变宏观:物质的种决一定变做现:构成物痪的分子种类一定变分子的总数可能变物质的状态可能变化学方程式:写.配,注反应现象:题色的变化,发光,放热,生成气体薄化合反应分解反应置换反应复分解反应有眾参加的反应:ft化还原反应一般反应条件为高湿的反应基本类型相据能量变化吸热反应放热反应物理变化与化学变化的区别和联系判断:在变化中是否有某他物质生成物理性质化学性质物质不W要发生化学变化就表现出来的性质熔点,密度,硬度,气味,状S,賴色等物质在化学变化中表现出来的性珉可燃性,还厍《,S化性,薄性,般味性等物理性班与化学性质的区别和联系燃烧定义:发光,发热的斟烈的氰化反应条件:可燃物,讯气/空气、溫度达到着火点灭火内因:可燃物的性质外囚:与《气榜触的®积灭火原理:破坏燃烧的条件泡沬灭火H党见的灭火器干粉灭火器二氣化砖灭火器缓慢氣化、自燃燸炸J4-W66含杂质的质量应換成纯物质的质量 _时位祕成観密度•体积质■单位代入化学方程式咬囂胃 统一化学方程式中物胰质■单位应统一 比例法 关系式法守恒法差量法平均值法暮本的实tt 技期化学仪a 的识别与《用«■的连罎发生装震幻收集装霣的达择M 学S 究气》的»IB. f?JSK2与净化气<«的Uft 气镡”质的Kii 气体的净化化华球合实tt«««»的分®«质的検嗆与榷醣來兕化学物拓的袷的«质格K 的方法 分A.曲浼的K 本願n相夜的分离与提鲭,物理方法:过»,结«.费»权方法,化气法,济3法,冒换5 ?皆>:川秘.时法"V-/ '.’化««興 化聿与V 康石浪天K 气元素在人体内的ft 在形武0, C 、H, N 、C«、P 、*,5,如,CI, «« M ■光扇 Fe * 加,加,Cr ' 如,r * *• W ■元章 鴻汴薷 太曲廉元薫与人停tt 康&•费富物质 破瀵 化石燃对坏凌的彩_化史,衣灼利环》的影_水汽染2气污» 土®污史环磔?itt 及W 沿 白色穴染化擎与蛘壤 化学与W®*«会食金羼M 愈S合tom 僉成濬K着合鉍科 •精不冏功®和灼鼸的多裨F.戶iXIMtfc **•柃相对®子质最的计算W 念:以一个味-12原子届■的1/12为标准, 其他原子的屏酱跟它的比值化学计算有关化学式的计算 溶液的相关计算相对分子质■ 化学式中各®子的相对傑子的总和 物质组成的元累质量比各元子个败与相对原子质■的番R 之比 物质中某种元素的质■分数该元素的质■与组成物质的各元素总旗■之比 概念溶质质■分数计算公式溶质质■分数与溶解度的换算溶液与化学方程式的综合计算依据一质■守恒定律步现及格式设,写、列、解‘答纯物质的质不纯物质的质量*纯度根据化学方程式的计算方法技巧相时质子ft®。
