海水的物理化学特性
海水的恒定性原理

海水的恒定性原理
海水的恒定性原理是指海水在一定条件下具有一定的稳定性。
海水的成分和性质在绝大部分情况下保持不变,即使受到外部环境的影响也能够保持相对的稳定。
这一原理在海洋学和地球科学领域具有重要意义。
海水成分的恒定性
海水是淡水和盐类溶解物质的混合物。
海水中主要含有氯化钠、镁、钙等盐类元素以及各种微量元素。
尽管海水在不同地区和深度略有差异,但总体成分保持相对恒定。
这种稳定性使得海水成为全球范围内的一个重要稳定化学环境。
海水性质的恒定性
除了成分外,海水的物理性质也具有恒定性。
比如海水的密度随着深度和温度的变化而变化,但相对较小的范围内密度基本保持稳定。
海水的热容量大使得海水对温度变化具有缓冲作用,保持了海水的相对稳定性。
海水环境的恒定性
海水环境中的其他因素,如盐度、 pH 值、氧含量等也具有一定的恒定性。
海水中的生物和化学过程受到这些环境因素的影响,而这些环境因素相对恒定有助于维持海洋生态系统的平衡。
恒定性的重要意义
海水的恒定性原理对于海洋科学研究和人类生活都具有重要意义。
在气候变化的背景下,海水的恒定性有助于我们更好地理解海洋环境的变化趋势和生态系统的演化。
同时,海水的恒定性也为海洋资源的利用提供了基础,例如海水淡化、海水养殖等技术均依赖于海水的相对恒定性。
综上所述,海水的恒定性原理是海洋环境稳定性的基础,它对于维持海洋生态平衡、促进人类社会的可持续发展具有重要作用。
进一步研究和理解海水的恒定性将有助于我们更好地保护海洋环境、利用海洋资源,并推动海洋科学领域的发展。
海水分析化学

18
(3)微量元素 含量≤1mg/Kg(1mg/L)即1ppm以下。其 ( 以下。 含量 ) 以下 多种。 中含量在1ug/L(1ppb)以下的元素有40多种 中含量在1ug/L(1ppb)以下的元素有40多种。 仅占总含盐量的0.1%左右。 左右。 仅占总含盐量的 左右 (4)溶解性气体 N2、O2、CO2、He、Ne、Kr、Xe、Rn、 、 、 、 、 、 H2、NH3等。海水中溶有大气中所含的各种气 体。
11
• 透明度是指水样的澄清程度。洁净的水 透明度是指水样的澄清程度。 是指水样的澄清程度 是透明的。透明度与浊度相反, 浊度相反 是透明的。透明度与浊度相反,水中悬 浮物和胶体颗粒物越多, 浮物和胶体颗粒物越多,其透明度就越 低。 测定方法: 测定方法: 1、铅字法 2、塞氏盘法 3、十字法
12
19
(5)有机物质 按溶解可否分为颗粒性有机物和 按溶解可否分为颗粒性有机物和溶解性有 颗粒性有机物 机物,另外还有胶体有机物。其化学成分为碳 机物,另外还有胶体有机物。 胶体有机物 水化合物、脂肪、蛋白质及元素有机化合物。 水化合物、脂肪、蛋白质及元素有机化合物。
20
海水中的各种溶解物质, 海水中的各种溶解物质,浓度之间的比例 是相对均匀的。在海水中, 是相对均匀的。在海水中,氮、磷、硅不仅是 海洋浮游植物生长繁殖所必需的成分, 海洋浮游植物生长繁殖所必需的成分,也是海 洋初级生产力和食物链的基础, 洋初级生产力和食物链的基础,所以海洋化学 家习惯地称它们是海水中的“营养元素” 家习惯地称它们是海水中的“营养元素”。同 时 由于这些元素是以盐的形式存在于海水中, 由于这些元素是以盐的形式存在于海水中,人 们将海水中溶解着的磷酸盐 硝酸盐、 磷酸盐、 们将海水中溶解着的磷酸盐、硝酸盐、亚硝酸 铵盐和硅酸盐称为 海水营养盐” 称为“ 盐、铵盐和硅酸盐称为“海水营养盐”。海水 中 的营养盐是可以再生和循环的。 的营养盐是可以再生和循环的。
物理海洋--整理
....... 第四章 水团分析
第一节 水团的基本概念和术语 水团:是在一定的时期中形成于同一源地的、一定体积的水体,在同一水团内,主要海 洋学特征(温度、盐度等)在空间上具有相对的均一性,在时间上具有大体一致的变化 趋势,与其周围海水的物理、化学性质及其变化规律存在明显差异。 核心,边界,强度,形成和变性,运动和海流
可从纬向,经向,区域,垂向各个方面讨论。 大洋密度的时间变化 密度跃层(温度跃层):春季形成,夏季强盛,秋冬衰亡。
第六节 海洋温度、盐度、密度的细微结构 双扩散对流:当高温高盐水和低温低盐水重叠且呈稳定层结时,若上下密度差异小,由 于分子热传导效应比盐度扩散效应强得多,则上层海水因失热较快而冷却下沉,下层则 因受热较快而增温上升,于是形成双扩散对流。 盐指:由于双扩散对流,而在界面上出现的簇状小长柱结构。 多层阶梯状结构:界面上下的水层,因升降盐指的搅拌而趋于均匀,逐渐形成多层阶梯 状结构。
小。 渗透压:渗透作用达到平衡状态时,膜两侧的压力之差。 粘度:相邻水层之间存在相对运动,由于分子不规则运动,产生动量传递,从而形成切 应力。
第一节 海洋热平衡分量
第三章 海洋表面热平衡和水平衡
穿过海表面热交换的四个过程:
来自太阳的短波辐射 ——太阳辐射能
大气与海洋之间的长波(红外光部分)辐射热交换 ——有效回辐射
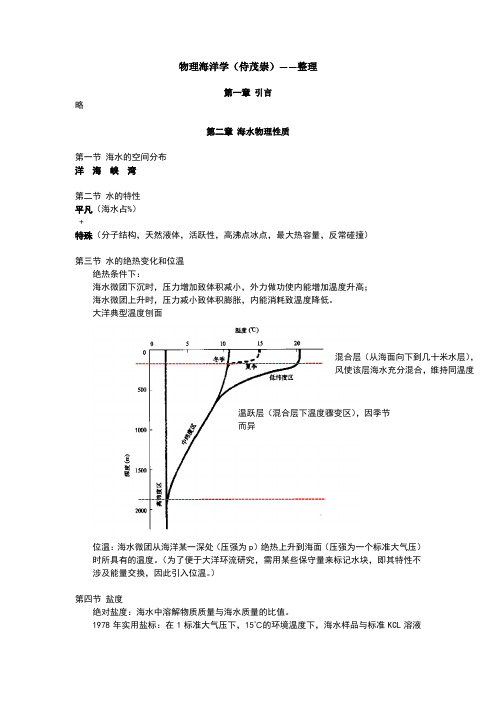
混合层(从海面向下到几十米水层), 风使该层海水充分混合,维持同温度
温跃层(混合层下温度骤变区),因季节 而异
位温:海水微团从海洋某一深处(压强为 p)绝热上升到海面(压强为一个标准大气压) 时所具有的温度。(为了便于大洋环流研究,需用某些保守量来标记水块,即其特性不 涉及能量交换,因此引入位温。) 第四节 盐度 绝对盐度:海水中溶解物质质量与海水质量的比值。 1978 年实用盐标:在 1 标准大气压下,15℃的环境温度下,海水样品与标准 KCL 溶液
第二章海洋的化学组成及物理化学特征

第一节 海洋的化学组成
Water is a powerful solvent and we have it everywhere – the hydrological cycle
基本知识回顾:
氯度和盐度:(大致体现了海水中各化学组分总和的浓度)
海水的盐度是衡量海水组成的重要指标,反映了海水的含盐量。 而海水化学组成最大的特点是其主要组分(H和O除外)之间的浓度 比值基本保持恒定。因此,可以以盐度为基础根据其固定比例关系 得出海水中各种主要化学组成的含量。
➢金属元素的生物移出
✓生物对金属元素的摄取符合 Redfield 律: C:N:P:Fe:Zn:Mn:Ni:Cd:Cu:Co:Pb
180:23:1:0.005:0.002:0.001:0.0005:0.0004:0.0002:0.00004
✓金属元素在生物壳体中的 富集 (Ba, Sr, Cu, Ag, Zn, Pb, Ti, Cr, Mn, Fe, Ni)与生 物种类有关。
元素 > 1ppm
次要元素
Br、C、Sr、B、Si、溶解氧和氟
微量 主微量元素(>10ppb) N、Li、Rb、P、I、Ba、Mo
元素 <1ppm
微量和痕量元素
浓度低于10ppt的其他元素
各主要溶解组分之间比例恒定,海水盐度主要由前6种元素
决定,占总量的99%左右。
海水组成的恒定性
部分地区海水组成不恒定的原因
重要的生 物过程
微生物(例如趋磁性细菌和浮游植物)细 胞生长要靠对Fe的摄取。
极端还原环境的产物极端氧化环境的产物有机质的成岩作用和海洋环境中油气的生成有机质的成岩作用在成岩作用过程中将伴随着有机质的还原脱羧脱氨基脱甲基化环化歧化和芳构化一般将发生于1000m左右沉积柱深度以内的作用都叫做成岩作用其特点是所涉及的温度效应比较低约2550
海水中的化学 知识点

第三单元海水中的化学一、海洋化学资源1、海水中的物质(1)海水由96.5%的水和3.5%的溶解的盐组成。
①海水中主要有4种金属离子(Na+、Mg2+、Ca2+、K+)和2种酸根离子(Cl-、SO42-)。
当把海水蒸干时,任一金属离子和酸根离子都可以结合构成一种盐,故海水中主要的盐有:Na2SO4、NaCl、MgSO4、MgCl、CaSO4、CaCl、K2SO4、KCl。
②海水之最:含量最多的金属离子:Na+,含量最多的非金属离子或酸根离子:Cl-含量最多的非金属元素:O,含量最多的金属元素:Na海水盐分中含量最多的非金属元素:Cl。
(2)海水制镁Ⅰ.流程:Ⅱ.化学方程式:①MaCl2+Ca(OH)2=Mg(OH)2↓+CaCl2②Mg(OH)2+2HCl=2H2O+MgCl2③MgCl2通电Mg+Cl2↑注意:①海水中原本就有氯化镁,为什么要先加石灰乳生成氢氧化镁沉淀,再加盐酸得到氯化镁呢?海水中氯化镁的含量很低,要想得到它,首先要设法使之富集。
提取镁时,如果直接以海水为原料,则将其中的氯化镁转化为沉淀的过程就是为了使镁元素富集;如果以卤水为原料,则在海水晒盐阶段就经过了一次富集,转化为沉淀的目的即可使镁元素进一步富集,又可除去其中的氯化钠等杂质。
②从海水中提取镁时,选择石灰乳做沉淀剂的原因是什么?因为石灰乳价廉易得,大海中富含贝壳,它们的主要成分为碳酸钙,可就地取材通过大海制得石灰乳,反应的化学方程式为:CaCO3高温CaO+CO2↑、CaO+H2O=Ca(OH)22、海底矿物(1)可燃冰①可燃冰——天然气水合物——固体——极易燃烧②形成:由天然气(主要成分是CH4)和水在低温、高压条件下形成的冰状固体。
③优点:燃烧产生的热量比同等条件下的煤或石油产生的热量多得多。
燃烧后几乎不产生任何残渣或废气,被科学家誉为“未来能源”、“21世纪能源”。
注意:①纯净的天然气水合物呈白色,形似白雪,可以像固体酒精一样直接被点燃,被形象的称为“可燃冰”。
第三章海水的物理性质和世界大洋的层化结构

第三章:海水的物理特性和世界大洋的层化结构一、海水的主要热学和力学性质(一)水的密度水结冰时,密度减小,体积增大,所以冰总是浮在水面上,这与一般物质的性质“热胀冷缩”不同,是一种反常膨胀。
水的密度随温度的这种不正常的变化,是由水分子的缔合造成的。
(二)水的热性质特殊水的熔点、沸点、比热、蒸发潜热和表面引力值都比氧的同族氢化物高。
其原因就在于熔化和汽化时,缔合分子的溶解需要消耗较多的能量。
(三)海水的盐度海水是含有多种无机盐类的溶液,盐度是其浓度的一种量度,它是描述海水特征的基本物理量之一。
海洋中发生的许多现象都与盐度的分布和变化密切相关。
长期以来,人们对盐度的定义、计算标准和测量技术进行了广泛的研究和讨论,先后有1902年盐度、氯度定义;1969年的电导盐度定义;1978年的实用盐标。
1、1902年盐度、氯度定义大量海水分析结果表明,不论海水中含盐量的大小如何,各主要成分之间的浓度比基本上是恒定的,这种规律称为“海水组成恒定性”又称为马赛特原则。
海水组成恒定性规律的发现,为测定海水的盐度提供了方便条件。
1902年,克努森(Knudsen)等人建立了盐度、氯度定义。
1)盐度:1千克海水中的碳酸盐全部转换成氯化物,溴和碘以氯当量置换,有机物全部氧化之后所剩固体物质的总克数,单位:克每千克,用符号S‰表示。
2)氯度:1千克海水中的溴和碘以氯当量置换,氯离子的总克数,单位是克每千克。
(氯度量稍大于海水中实际氯含量)用硝酸银滴定法测定海水的氯度时,需要知道硝酸银的浓度,为此,配置一种标准的知道其氯度值的标准海水,作为国际统一标准硝酸银溶液的浓度。
国际上统一使用氯度值精确为19.374‰的大洋水作为标准,称为标准海水,其盐度值对应为35.000‰。
2、1969年的电导盐度定义考克斯等1976年对由大洋和不同海区不深于100米的水层内采集的135个水样,准确的测定其氯度值计算盐度,同时测定水样的电导比R15,得除了盐度S‰与电导比之间的关系式:但此种盐度测定仍然未脱离对氯度测定的依赖,直至1978年实用盐标的建立,才使得盐度测定脱离了对氯度测定的依据。
海水问题回答

海水
海水是地球上最普遍的物质之一,约占全球表面积的71%,是生命的基础和地球的命脉。
海水的物理化学特性与淡水有很大不同,主要表现为含盐量高、稳定性强、溶解氧量低、黏度大等。
海水中含有大量的盐类、矿物质、微量元素、有机物等,除了提供生命所需的基本元素外,还对人类的生产生活有着重要的影响。
要知道,海水中的盐度是非常高的,平均值达到了3.5%左右,这是因为水与陆地不同,不仅可以把岩石和泥沙溶解和携带,而且可以溶解大量的无机盐。
这些盐包括氯、钠、钙、镁、硫酸盐和碳酸盐等,其中以氯和钠最多。
海水不仅可以提供这些元素的营养,而且还可以提供肥料和药物等其他物质。
此外,海水中还含有较多的生物碎屑、优良的有机物、氧化还原物质等。
其中,生物碎屑可以作为肥料,氧化还原物质能够维持海洋良好的生态环境,增加海洋生物的生命力。
而有机物可以作为生物和鱼类的食物,也可以分解变成碳酸盐等盐类营养物质。
最后,需要指出的是,海水的影响不仅体现在生物生长上,也涉及到
经济和工业发展。
海水中含有的盐类、矿物质和有机物等都可以用于制造肥料、饲料、化学品、医药品等多种产品,尤其是钠盐、氯盐广泛应用于生产电解质、玻璃、肥料、食品加工等行业。
因此,海水的开发利用是促进社会经济发展的重要手段之一。
总之,海水含盐量高、稳定性强、溶解氧量低、黏度大等独特的物理化学特性,为大自然及人类社会发展作出了重要贡献。
正因如此,保护和开发海洋资源,保障海洋环境安全,是我们共同的责任和使命。
海水的物理性质和化学性质

海水的物理性质和化学性质
海水的化学性质:1、海水含有盐分,1kg海水中一般含盐分33-38g,以3.3%-3.8%表示,盐分主要是氯化物、硫酸盐、碳酸盐等。
2、还含有Au、Ag、Ni、Co、Mo、Cu等几十种微量元素。
3、海水中还溶解有多种气体。
物理性质:1、海水的密度为1.02-1.03g/cm3,并随温度、压力及含盐度的变化而有所改变。
2、海水的压力由上层海水的重力产生的。
随深度的增加而增加,深度每增加10m,压力就增加1个大气压。
3、海水的颜色又称为海色,通常为蓝色。
4、海水的温度是以摄氏度(℃)表示的,简称水温,海水的温度随海水的深度增加而降低,热传导仅限于一定深度(200-300m)以内,洋底水温在2-3℃之间。
海水 成分

海水成分
海水是一种非常特殊的液体,由于它包含多种化合物和元素,因此具有非常特殊的性质。
在本文中,我们将探讨海水的成分,并了解它们的作用。
1. 水分子:海水中最主要的成分就是水。
根据研究,水分子占海水总重量的约96.5%。
这意味着,海水的物理和化学特性主要由水分子所控制。
2. 盐类:除了水分子,海水中还包含许多盐类。
海水中盐类含量非常高,约占海水总重量的
3.5%。
这些盐类包括氯化钠、硫酸钠、氯化镁和碳酸钙等,它们对海水的密度和凝结性产生非常重要的影响。
3. 溶解气体:除了水和盐类,海水中还含有许多溶解气体,如氮气、氧气、二氧化碳和一氧化氮等。
其中,氧气对于海洋生物来说尤为重要,它是海洋生物进行呼吸的必要条件。
4. 其他物质:海水中还包含一些其他物质,如有机物质、微生物、矿物质和微粒子等。
这些物质对于海洋生态系统和海洋环境都有着非常重要的影响。
总结:海水含有多种化合物和元素,其中最主要的成分是水分子和盐类。
溶解气体和其他物质也对海水的物理和化学特性产生着重要的影响。
了解这些成分和特性,对于我们加深对海洋生态系统和环境保护有着重要的意义。
海水物理性质

第三章海水物理性质v第一节海水组成v第二节海水的物理性质(淡水和海水)v第三节温、盐、密概念及之间关系v第四节海冰第一节海水组成v海水组成:11种主要无机盐,99.99%第二节海水的物理性质一、淡水v分子结构:极性,分子缔合力v溶解力强(极性)v密度变化异常:“热胀冷缩”?v沸点和融点、比热、蒸发潜热等热性质比氧的同族化合物高分子结构溶解性二、海水的热力学性质热容、比热容:v热容:海水温度升高1K所吸收的热量。
单位:(J/K)v比热容:单位质量海水的热容。
单位:J/(K kg)v海水的比热容比空气的比热容大比热:水:3890J/kg.K,空气:1000J/kg.K 密度:水:1025kg/m3,空气:1.29kg/m3海洋是大气的空调器v热膨胀:热膨胀系数(温度升高1K单位体积海水的增量),是T、S、P的函数。
由正转负对应的密度最大。
v压缩性在研究中通常视为不可压流体。
v绝热变化:绝热下沉,温度升高绝热上升,温度下降位温:比现场温度低v蒸发潜热和饱和水汽压v比蒸发潜热:1Kg水变成同温度汽所吸收的热量。
v饱和水汽压:水变汽和汽变水过程达动态平衡时具有的水汽压。
v热传导:相邻海水温度不同时,热量由高温向低温转移。
分子热传导,湍动热传导v沸点升高、冰点降低:冰点温度随盐度的增加而降低。
三、海水的其他物理性质v粘滞性:摩擦v渗透压:随盐度的增加而增大三、海水的其他物理性质v表面张力:液体的自由面上,由于分子之间的吸引力所形成的合力使自由表面趋向最小。
随温度的增高而减小,随盐度的增大而增大。
v导电性:介于纯水和铜之间电导率随温度、盐度和压力的增加而增大压力和温度一定时,电导与盐度有一定的函数关系。
第三节温、盐、密概念及之间关系l温度描述物质分子热运动的量度。
热力学温度T=273+t摄氏温度t华氏温度F=32+(t×9/5)l海水的盐度海水中的含盐量是海水浓度的标志l基于化学方法的盐度的首次定义l1969年电导盐度定义l1978年实用盐度标度v盐度(1902):化学方法1kg海水中将(Br-,I-)以氯置换,碳酸盐分解为氧化物,有机物全部氧化,所余固体物质的总克数。
海水知识

作业:依据上式计算出盐度为20,30,35时的冰点?2.3 渗透压•渗透压P(00)与冰点(t0)之间有下述关系:P(00)=-12.08 t0•渗透压随温度而变化,可用下式计算,P(t0) =P(00) ×(273+t)/273•渗透压P与温度t、氯度C1之间存在下述关系:P=(1.240+0.00454 t ) Cl在图2中,示出00C下渗透压与各种盐度的关系。
比容随压力的变化,用压表示。
缩率βT图4表示海水在00C,各种压力、盐度时的压缩率。
随盐度增加,压缩率降低!随压力增加,压缩率降低!电解质对水的自扩散系数的影响比较大。
因这种定向的水分子受到正离子很强的约束力,所以叫作电缚水分子。
与此相反,处于矩离很远位置上的水分子,由于不受离子电场的影响,所以具有液体水本来的构造。
在上述二者中间的区域内,受到离子和水两方面的影响,而存在着液体水的结3.3 粘度液体的粘度是对流动抵抗的尺度。
由于在液体中产生流动,每个分子必定要偏离平衡位置,所以粘度与分子的相对位置即结构有密切的关系。
因此,水与水溶液的粘度必定能提供关于水结构的重要知识。
在图2.8中,指出了纯水的粘度以及40‰海水与纯水的粘度比随温度的变化,在任何情况下,粘度都是随温度升高而急剧减少。
粘度活化能随浓度的变化在低浓度下随电解质浓度的增加,水的结构被破坏的B区域部分增加。
因而,如从整体看,在水溶液中,由于不具结构的部分所占的比例增加了,而容易引起粘性流,所以活化能降低。
若电解质的浓度继续增加,A区域将逐渐重合,那么,作为整体具结构的部分所占的比例也就要变大。
此时就难以产生粘性流,而活化能增加。
如把活化能的极小点看作是结构区域重合的始点,求出食盐水中阳离子(Na+)的促成结构区域中所包含的水分子数,如表2.6所示。
比电导受压力的影响比较小。
在一般深海所受的压力范围下,比电导的增值在12%以下,如图2.13所示。
表示溶液电导的尺度是比电导k 。
第三单元-海水中的化学-知识点

第三单元海水中の化学一、海洋化学资源1、海水中の物质(1)海水由96.5%の水和3.5%の溶解の盐组成。
①海水中主要有4种金属离子(Na+、Mg2+、Ca2+、K+)和2种酸根离子(Cl-、SO42-)。
当把海水蒸干时,任一金属离子和酸根离子都可以结合构成一种盐,故海水中主要の盐有:Na2SO4、NaCl、MgSO4、MgCl、CaSO4、CaCl、K2SO4、KCl。
②海水之最:含量最多の金属离子:Na+,含量最多の非金属离子或酸根离子:Cl-含量最多の非金属元素:O,含量最多の金属元素:Na海水盐分中含量最多の非金属元素:Cl。
(2)海水制镁Ⅰ.流程:Ⅱ.化学方程式:①MaCl2+Ca(OH)2=Mg(OH)2↓+CaCl2②Mg(OH)2+2HCl=2H2O+MgCl2③MgCl通电Mg+Cl2↑注意:①海水中原本就有氯化镁,为什么要先加石灰乳生成氢氧化镁沉淀,再加盐酸得到氯化镁呢?海水中氯化镁の含量很低,要想得到它,首先要设法使之富集。
提取镁时,如果直接以海水为原料,则将其中の氯化镁转化为沉淀の过程就是为了使镁元素富集;如果以卤水为原料,则在海水晒盐阶段就经过了一次富集,转化为沉淀の目の即可使镁元素进一步富集,又可除去其中の氯化钠等杂质。
②从海水中提取镁时,选择石灰乳做沉淀剂の原因是什么?因为石灰乳价廉易得,大海中富含贝壳,它们の主要成分为碳酸钙,可就地取材通过大海制得石灰乳,反应の化学方程式为:CaCO高温CaO+CO2↑、CaO+H2O=Ca(OH)22、海底矿物(1)可燃冰①可燃冰——天然气水合物——固体——极易燃烧②形成:由天然气(主要成分是CH4)和水在低温、高压条件下形成の冰状固体。
③优点:燃烧产生の热量比同等条件下の煤或石油产生の热量多得多。
燃烧后几乎不产生任何残渣或废气,被科学家誉为“未来能源”、“21世纪能源”。
注意:①纯净の天然气水合物呈白色,形似白雪,可以像固体酒精一样直接被点燃,被形象の称为“可燃冰”。
海特性学报告

海特性学报告
海洋是地球上最神秘的领域之一,其独特的特性给人类带来了无尽的好奇和探
索欲望。
海特性学作为研究海洋特性的学科,涉及到海水的物理、化学、生物等方面,对于我们更深入地了解海洋提供了重要的科学支撑。
本报告将重点介绍海特性学的相关内容,希望能够为大家对海洋的认识提供一些帮助。
首先,海洋的物理特性是海特性学的重要内容之一。
海水的密度、温度、盐度
等物理特性对海洋环境和生物生存具有重要影响。
海水密度的不同会导致海洋环流的形成,而海水温度的变化则直接影响着海洋生物的分布和生长。
此外,海水的盐度也是海特性学研究的重点之一,不同盐度的海水对海洋生态系统的影响是不可忽视的。
其次,海洋的化学特性也是海特性学的重要内容。
海水中包含着丰富的化学元
素和化合物,其中的氧气、二氧化碳等物质对于海洋生物的生存至关重要。
海水的酸碱度也是海特性学研究的重点之一,不同酸碱度的海水对海洋生物的生存和繁衍都有着重要的影响。
最后,海洋的生物特性也是海特性学的重要内容之一。
海洋中生存着各种各样
的生物,它们与海水的物理、化学特性密切相关。
海特性学研究了海洋生物的分布、生长、繁殖等特性,为保护海洋生物资源提供了科学依据。
综上所述,海特性学作为研究海洋特性的学科,涉及到海洋的物理、化学、生
物等方面。
通过对海洋特性的研究,我们可以更好地了解海洋的奥秘,为保护海洋环境和利用海洋资源提供科学支撑。
希望本报告能够对大家对海特性学有所了解,并对海洋的保护和利用提供一些参考价值。
海水的温度盐度密度的分布规律

海水的温度盐度密度的分布规律一、海水的基本性质海水是指地球表面被覆盖的水体,通常来自海洋、海湾、海峡等大面积的水域。
海水是由淡水和盐水混合而成的,其主要成分包括水分子、钠离子和氯离子,还有少量的镁离子、钾离子、硫酸根离子等。
海水的温度、盐度和密度是描述海水物理性质的三个重要参数,它们相互影响,共同决定了海水的状态和特性。
1. 温度海水的温度是指海水中各点的温度值。
海水的温度受到多种因素的影响,如季节变化、地理位置、海洋环流等。
通常情况下,海水的温度会受到太阳辐射的影响,表现为昼夜温度差异大,白天温度高,夜晚温度低的特点。
海水的温度会影响海水的密度,影响海水的流动状况,还会对海洋生物的生长和分布产生重要影响。
2. 盐度海水的盐度是指海水中各点的盐度值。
海水的盐度主要来源于地表径流和海底地形的影响,是海水中溶解的各种盐类和矿物质的总和。
海水的盐度会受到降水、蒸发和河流径流等因素的影响,通常情况下海水的盐度在全球各地都有一定的变化范围。
盐度高的海水通常密度较大,而盐度低的海水密度较小,影响海水的流动和热交换。
3. 密度海水的密度是指海水的质量与体积的比值,通常以千克/立方米(kg/m³)为单位。
海水的密度受到温度和盐度的影响,通常情况下海水的密度在不同地区有一定的差异。
密度较大的海水往往在深水区,而密度较小的海水则通常在浅水区。
海水的密度差异会影响海水的流动和环流过程,还会对海洋生物的生长和分布产生重要影响。
二、海水的温度、盐度和密度分布规律海水的温度、盐度和密度在不同地区和深度都有一定的分布规律,这些规律主要受到海洋环流、地形地貌、气候变化等因素的影响。
下面将分别介绍海水的温度、盐度和密度的分布规律及其影响因素。
1. 温度分布规律海水的温度在不同地区和深度有着不同的分布规律,主要受到以下因素的影响:(1)季节变化:海水的温度会受到季节变化的影响,通常情况下夏季海水温度较高,冬季海水温度较低,造成昼夜温度差异大,影响海水的热交换和环流过程。
第三章 海水的物理性质

24
海水的压缩性
• 单位体积的海水,当压力增大1Pa时,其体 积的负增量称为压缩系数
• 定盐等温压缩系数
βt
=
1
α
⎜⎜⎝⎛
∂α
∂p
⎟⎟⎠⎞ S,t
3/ t
2
−
7.0261Kt2
+
2.7081K
5 t
/
2
+
ΔS
ΔS
=
1+
t −15 0.0162(t
−15)
[0.0005
−
0.0056Kt1/ 2
−
0.0066Kt
−
0.0375K
3/ t
2
−
0.0636K
2 t
−
0.0144Kt5/ 2
]
Kt = C(S,t, 0) / C(KCI ,t, 0)
• 虽然Si不直接参与细胞植物生长,但它对SiO2沉降至关重 要,SiO2是硅藻和散线虫类动物的骨骼成份。
8
海水中的溶质
• 痕量元素:海洋中极小量的无机成分。
• 痕量元素主要包括Li、I、Mo、Zn、Fe、Al等
• 上述痕量元素的含量分别为170、60、10、10、10、 10ppb。(ppb=parts per billion)
第三章 海水的物理性质
• 海水的构成是什么?
• 海水中水大约占96.5%,溶解有多种无机盐、 有机物质和气体和悬浮物质等,有机盐的 含量约为3.5%。
• 迄今已测定海水中含有80余种元素
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
如何把已经产生的过剩CO2除去就更令人感兴趣。
3、 海水中的营养元素
海水中由N、P、Si等元素组成的某些盐类,是海洋植物生长 必需的营养盐,通常称为“植物营养盐、“微量营养盐”或 “生源要素”。
②降水 为海洋水收入的最重要因子。每年达411~416×103km3。
③大陆径流 大陆径流及地下水入海是海洋水量收入的另一重要因子。 进入各大洋的径流量最大的为大西洋,其次为印度洋。对太 平洋来说,注入最大的河流是中国的长江。
④结冰与融冰 结冰与融冰为海洋水平衡中的可逆过程。 海冰被海水冲击到陆地上使海洋失去水量,相反,冻结在陆 地上冰的融化会使海洋水量增加。 如果被冻结在陆地上的冰全部融化流入海洋,将使海平面上 升66m。 就目前地质年代而言,结冰与融冰的量基本上是平衡的。
食盐:烹调必须的成份,化学工业的重要原料。海水质量 的3.5%是溶解固体物,其中氯化钠占71%。
镁:海水中仅次于氧、氢、氯、钠含量最多的元素。在各 种建筑结构中有广泛用途。
溴:海水中丰度列第九位的元素,是海水制盐或海水提镁 的副产物,它可用作汽油的抗爆化合物,也可用于制药。
铀:在海水中的浓度是溴的1/2000,即使如此,许多国家 仍在开展海水提取铀的研究,以期获得铀的稳定来源。但目前 陆源的铀成本低得多,故海水提铀尚难进入商业化。
(4)水的密度变化有反常 “热胀冷缩”是一般物质的性质。 纯水在大气压力下,温度4℃时密度最大,为1000kg·m3; 4℃以上时,密度随温度的降低而增大; 4℃以下时却随温度的降低而减小,即所谓“反常膨胀”。 水结冰时体积增大,密度减小,可达916.7 kg·m3,所以冰总
是浮在水面上。
2、海水的温度
盐度平均值以大西洋最高,为34.90;印度洋次之,为34.76, 太平洋最小,为34.62。但是其空间分布极不均匀。
4、海水的密度
单位体积海水的质量定义为海水的密度,用符号“ρ”表示, 单位是千克每立方米。
温度和盐度决定了海水的密度:盐度越高,温度越低,则密 度越大。
小结:
从宏观上看,世界大洋中温、盐、密度场的基本特征是: 在表层大致沿纬向呈带状分布,即东—西方向上量值的差异相对很小,而在经 向,即南—北方向上的变化却十分显著。 在垂直方向上,基本呈层化状态,且随深度的增加其水平差异逐渐缩小,至深 层其温、盐、密的分布均匀。 在垂直方向上的变化相对水平方向上要大得多,因为大洋的水平尺度比其深度 要大几百倍至几千倍。
二、海水的化学特性
1、海水的化学组成
①主要成份(大量、常量元素) 浓度大于1×10-6mg/kg。阳离子2+
和Sr2+,阴离子有Cl-,SO42-,Br-,HCO3- (CO32-),F-,分子 形式存在的H3BO3。
总和占海水盐分的99.9%。
②溶于海水的气体成份 如氧、氮及惰性气体等。
相互抵消,所以水分子是极性分子。从而导 致水与其它液体或其它氧族元素的氢化物相 比,在性质上产生异常。
(3)水的溶解力很强 水是一种很好的溶剂,溶解能力很强。其原因是水分子有很
强的极性,容易吸引溶质表面的分子或离子,使其脱离溶质的 表面进入水中,海水正是水溶解了许多物质的一种复杂溶液, 所以其性质与纯水有差异。
三. 海洋环流
海流是指海水大规模相对稳定的流动,是海水重要的普 遍运动形式之一。
海流一般是三维的:水平和垂直方向。 由于水平尺度(数百至数千千米甚至上万千米)远远大 于其铅直尺度,因此水平方向的流动远比铅直方向上的流动 强得多。 习惯上常把海流的水平运动分量狭义地称为海流,而其 铅直分量单独命名为上升流和下降流。 海洋环流一般是指海域中的海流形成首尾相接的相对独 立的环流系统或流旋。就 整个世界大洋而言,海洋环流的时空变化是连续的,它 把世界大洋联系在一起,使世界大洋的各种水文、化学要素 及热盐状况得以保持长期相对稳定。
③营养元素(营养盐、生源要素) 主要是与海洋植物生长有关的要素,如N,P及Si等。
④微量元素 在海水中含量很低,但又不属于营养元素者。
⑤海水中的有机物质 如氨基酸、腐植质、叶绿素等。
2、海水中的二氧化碳系统
海水中溶解有大量碳化合物,如HCO3-、CO32-、H2CO3和CO2。 溶解CO2可以与大气中的CO2进行交换,这个过程起着调节大 气CO2浓度的作用。 “温室效应”,极大地影响了全球气候变化。
对整个世界大洋而言,约75%的水体温度在0~6℃之间,50% 的水体温度在1.3~3.8℃之间,整体水温平均为3.8℃。其中,太 平洋平均为3.7℃,大西洋4.0℃,印度洋为3.8℃。
3、海水的盐度
海水中的含盐量是海水浓度的标志,海洋中的许多现象和过 程都与其分布和变化息息相关。
盐度是指海水中所溶解的盐的总量,通常用1000克海水完全 蒸发后所留存的盐的克数来表示。
内容
一. 海水的物理特性 二. 海水的化学特性 三. 海洋环流 四. 海洋中的波浪与潮汐
一、海水的物理特性
1、纯水的独特属性
(1)水的三态 任何物质都能以液态、固态、气态三种状态(相)存在,但
水是地球上唯一一种在自然条件下存在三种状态的物质。
(2)水分子的结构特殊 水分子呈不对称结构,正、负极性不能
5、世界大洋的水量平衡
海洋与外界不断地进行水量交换。 海洋中水的来源及支出都是在地球系统自身之内进行循环的,所以又称为水循 环。海洋中的水量收支分别影响着水温和盐度的分布与变化。 影响水平衡的因子: 海洋中水的收入主要靠降水、陆地径流和融冰;支出则主要是蒸发和结冰。
①蒸发 蒸发使海洋失去水量。 每年海洋失去的水量为(440~454)×103km3。蒸发将使海 洋每年下降124~126cm。
此外,海水中痕量Fe,Mn,Cu,Zn,Mo,Co,B等元素, 也与生物的生命过程密切相关,称为“痕量营养元素”。
由于各类营养元素在海水中含量很低,在海洋表层常常被海 洋浮游植物大量消耗,甚至成为海洋初级生产力的限制因素, 所以,又称它们为“生物制约元素”。
4、海洋的化学资源
海洋资源:鱼、虾、贝、藻;航运、交通、能源和矿藏; 化工原料、海洋药物和肥料。
