化学键和分子结构(习题及答案)
化学键及分子化合物测试题(附详细答案)

化学键及分子化合物测试题(附详细答案)1. 下列分子中哪一个有离子键:- 氯气 (Cl<sub>2</sub>)- 氧气 (O<sub>2</sub>)- 硝酸 (HNO<sub>3</sub>)- 甲烷 (CH<sub>4</sub>)答案:硝酸 (HNO<sub>3</sub>)2. 下列化合物中哪一个是离子化合物:- 二氧化碳 (CO<sub>2</sub>)- 氯化钠 (NaCl)- 丙烷 (C<sub>3</sub>H<sub>8</sub>)- 甲醇 (CH<sub>3</sub>OH)答案:氯化钠 (NaCl)3. 分子式为C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>的化合物是以下哪一个:- 葡萄糖- 甲烷- 乙炔- 苯答案:葡萄糖4. 哪一种键是由电子共享形成的:- 离子键- 共价键- 隧道键- 金属键答案:共价键5. 下列化合物中,键的极性最小的是:- H<sub>2</sub>O- CO<sub>2</sub>- HCl- NH<sub>3</sub>答案:CO<sub>2</sub>6. 下列哪一种键是由金属原子形成的:- 离子键- 共价键- 隧道键- 金属键答案:金属键7. 分子式为H<sub>2</sub>SO<sub>4</sub>的化合物是以下哪一个:- 硫酸- 硝酸- 氯酸- 醋酸答案:硫酸8. 下列化合物中,含有三个氧原子的是:- 二氧化碳 (CO<sub>2</sub>)- 氯酸 (HClO<sub>3</sub>)- 亚硝酸 (HNO<sub>2</sub>)- 偏磷酸 (H<sub>3</sub>PO<sub>4</sub>)答案:亚硝酸 (HNO<sub>2</sub>)9. 化学键是原子间的相互作用力,下列哪一种化学键是最强的:- 离子键- 隧道键- 金属键- 氢键答案:离子键10. 下列化合物中,键的极性最大的是:- CO<sub>2</sub>- HCl- H<sub>2</sub>O- NH<sub>3</sub> 答案:HCl。
高等有机化学各章习题及答案 (1)
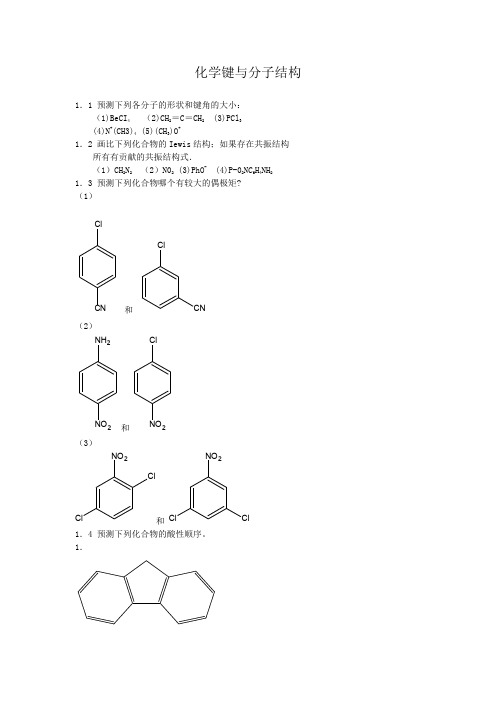
1.1 预测下列各分子的形状和键角的大小: (1)BeCI4 (2)CH2=C=CH2 (3)PCl3 (4)N+(CH3)4 (5)(CH3)O+
1.2 画比下列化合物的 Iewis 结构;如果存在共振结构 所有有贡献的共振结构式. (1)CH2N2 (2)N02 (3)PhO- (4)P-02NC6H4NH2
1.8 (2)和(7)不能形成分子间氢键 (1)HCN┈HCN (3)H2CO┈HOH
(6)H2NCH2CH2OH┈NH2CH2CH2OH
(4)Cl┈HOH
(5) (CH3)2CO┈HOOCC6H4OH
当第一个羧基上的 H+电离后,所形成的负离子是一个强的给电子基,它对第二个羧基所 发生的直接诱导,将使第二个羧基上好的电离趋于困难,这种影响也是顺式大于反式,所以 丁烯二酸的第二电离常数是顺式小于反式。这种诱导影响是通过空间或溶剂间的场效应传递 的。 1.6 (1)无芳香性
分子没有一个闭合的共轭体系,因而无芳香性,然后失去 H-以后生成的 A 为含有六个π 电子的离子,则具有芳香性。
1.8 下列各组化合物能否形成分子间氢键?若有的话,请画出分子间氢键。
(1)HCN 和 HCN (2)HCHO 和 HCHO
(3)HCHO 和 H2O
(4)Cl-和H
和丙酮
(6)HOCH2CH2NH2 和 HOCH2CH2NH2
答案: 1.1 (1)线性 (2)三个碳原子呈线型,氢位于相互垂直的平面上 (3)棱锥型,键角约
105~110°(4)正四面体 (5)棱锥型,键角约 105~110°。
1.2 (1) (2)
(3)
(4)
1.3 (1)Ⅰμ=2.5D Ⅱμ=3.4D (2)Ⅰμ=6.3D Ⅱμ=2.6D (3)Ⅰμ=3.48D Ⅱμ=2.68D
化学键与分子结构练习题(附答案)

)
A
一般来说键键能小于键键能; 原子形成共价键的数目等于基态原子的未成对电子数; 相同原子间的双键键能是单键键能的两倍; 所有不同原子间的键至少具有弱极性.
提交
B
C
D
多选题
1分
下列说法中不正确的是(
)
A B C D E
键的一对成键电子的电子密度分布对键轴方向呈园柱型对称;
键电子云分布是对通过键轴的平面呈镜面对称; 键比键活泼性高,易参与化学反应;
提交
知识点
电子层构型 晶格能大小 共价键:单电子,自选相反,最大重叠 杂化轨道:中心原子杂化类型 几何构型
溶解度大小
熔点和硬度的高低 离子极化理论
直线型、平面正三角、正四面体、三角双锥、 正八面体 晶体类型 分子间作用力
单选题
1分
下列离子属于18电子构型的是 ( )
A
Na+ Ag+ Fe3+ Fe2+
提交
A
B
C
D
多选题
1分
下列说法正确的是(
)
A B C D E
原子形成的共价键数等于游离气态原子中不成对电子数; 同种原子双键的键能为单键键能的两倍; 键长是指成键原子的核间距离; 线性分子如A-B-C是非极性的; 共价键的极性是由成键元素的电负性差造成的.
提交
单选题
1分
关于共价键的说法,下述说法正确的是(
NaF>NaCl>NaBr>NaI NaCl<MgCl2<AlCl3<SiCl4 LiF>NaCl>KBr>CsI Al2O3>MgO>CaO>BaO
提交
B
无机化学化学键与分子结构选择题

(三)化学键与分子结构1.下列分子中,两个相邻共价键的夹角最小的是A、BF3 B、H2S C、NH3D、H2O2.下列分子中,两个相邻共价键的夹角最小的是A、BF3 B、CCl4C、NH3D、H2O3.下列分子和离子中,中心原子成键轨道不是sp2杂化的是A、NO 3-B、HCHOC、BF3D、NH34.NCl3分子中,N原子与三个氯原子成键所采用的轨道是A、两个sp轨道,一个p轨道成键B、三个sp3轨道成键C、P X、P y 、P z 轨道成键D、三个sp2轨道成键5.水分子中氧原子的杂化轨道是A、sp B、sp2C、sp3D、dsp26.下列化合物中,极性最大的是A、CS2B、H2S C、SO3D、SnCl47.下列分子中,偶极矩不等于零的是A、BeCl2B、BF3C、NF3 D、CO28.下列液态物质中只需克服色散力就能使之沸腾的是A、H2O B、CO C、HF D、Xe9.极化能力最强的离子应具有的特性是A、离子电荷高、离子半径大B、离子电荷高、离子半径小C、离子电荷低、离子半径小D、离子电荷低、离子半径大10.下列各组离子中,离子的极化力最强的是A、K+、Li+B、Ca2+、Mg2+C、Fe3+、Ti4+D、Sc3+、Y3+11.比较下列各组物质的熔点,正确的是A、NaCl > NaF B、CCl4> CBr4C、H2S > H2Te D、FeCl3 < FeCl212.下列各分子中,偶极矩不为零的分子为A、BeCl2B、BF3C、NF3D、CH413.下列各组离子化合物的晶格能变化顺序中,正确的是A、MgO> CaO> Al2O3B、LiF> NaCl >KIC、RbBr< CsI <KClD、BaS> BaO> BaCl214.下列物质熔点变化顺序中,不正确的是A、NaF> NaCl > NaBr > NaIB、NaCl< MgCl2< AlCl3<SiCl4C、LiF> NaCl >KBr > CsID、Al2O3>MgO> CaO> BaO15.下列原子轨道的n相同,且各有一个自旋方式相反的不成对电子,则沿X 轴方向可形成π 键的是A、P X-P XB、P X-P yC、P y-P ZD、P z-P z16.下列分子或离子中,键角最大的是A、XeF2B、NCl3C、CO32-D、PCl4+17.下列分子或离子中,具有反磁性的是A、O2B、O2-C、O2+D、O22-18.按分子轨道理论,下列稳定性排列正确的是A、O2 > O2+> O22-B、O2+> O2 > O22-C、O22-> O2 > O2+D、O2+> O22-> O219.下列各组原子轨道中不能叠加成键的是A、P X-P X B、P X-P Y C、S-P X D、S-P Z20.下列分子或离子中,中心原子的价层电子对几何构型为四面体,而分子(离子)的空间构型为V 字形的是A、NH4+B、SO2C、ICl-2D、OF221.几何形状是平面三角形的分子或离子是A、SO3B、SO-23C、CH-3D、PH322.几何形状是平面三角形的分子或离子是A、SO32-B、SnCl3-C、CH3-D、NO3-23.下列分子中偶极矩大于零的是A、SF4B、PF5C、SnF4 D、BF324.下列分子中偶极矩大于零的是A、BF3B、PF3C、SiF4 D、PF525.下列分子中属于非极性分子的是A、PH3B、AsH3C、BCl3 D、CHCl326.下列分子中属于非极性分子的是A、SF4B、PCl5C、PCl3 D、IF527.根据VSEPR理论,BrF3分子的几何构型为A、平面三角形B、三角锥形C、三角双锥形D、T字形28.下列各组物质中,沸点高低次序不正确的是A、HF>NH3B、S2(g)>O2C、NH3>PH3D、SiH4>PH329.下列体系中,溶质和溶剂分子间,三种分子间力和氢键都存在的是A、I2和CCl4溶液B、I2酒精溶液C、酒精的水溶液D、CH3Cl的CCl4溶液30.下列晶体中,熔化时只需克服色散力的是A、K B、H2O C、SiC D、SiF431.下列物质的熔点由高到低的顺序正确的是a、CuCl2b、SiO2c、NH3 d、PH3A、a > b > c > dB、b > a > c > dC、b > a > d > cD、a > b > d > c32.下列分子中,离域π 键类型为П33的是A、O3 B、SO3C、NO2 D、HNO333.根据分子轨道中电子排布,下列分子、离子稳定性顺序正确的是A、O2 >O+2>O-2> O-22B、O-22>O-2>O+2> O2 C、O+2>O-2> O-22> O2D、O+2>O2>O-2> O-2234.若中心原子采用s p3 d2杂化轨道成键的分子,其空间构型可能是A、八面体B、平面正方形C、四方锥形D、以上三种均有可能35.下列氟化物分子中,分子偶极矩不为零的是A、PF5 B、BF3C、IF5D、XeF436.下列化合物中具有氢键的是A、CH3F B、CH3OH C、CH3OCH3 D、C6H637.下列晶格能大小顺序中正确的是A、CaO>KCl> MgO>NaClB、NaCl> KCl> RbCl>SrOC、M g O>RbCl> SrO>BaOD、Mg O>NaCl> KCl> RbCl38.在下列各种含氢化合物中,有氢键的是A、CHF3 B、C2H6 C、C6H6 D、HCOOH E、CH439.HF具有反常的高沸点是由于A、范德华力B、极性共价键C、氢键D、离子键40.在石墨晶体中,层与层之间的结合力是A、金属键B、共价键C、范德华力D、大π键41.关于晶格能,下列说法中正确的是A、晶格能是指气态阳离子与气态阴离子生成1 mol离子晶体所释放的能量B、晶格能是由单质化合成1 mol 离子化合物时所释放的能量C、晶格能是指气态阳离子与气态阴离子生成离子晶体所释放的能量D、晶格能就是组成离子晶体时,离子键的键能42.下列物质中,既有离子键又有共价键的是A、KCl B、CO C、Na2SO4D、NH4+43.下列说法中,正确的是A、离子键和共价键相比,其作用范围更大B、所有高熔点物质都是离子型的C、离子型固体的饱和水溶液都是导电性极其良好D、阴离子总是比阳离子大44.下列原子轨道中各有一个自旋方向相反的不成对电子,则沿x 轴方向可形成 键的是A、2 s-4 d z2B、2 p x-2 p xC、2 p y-2 p yD、3 d xy-3 d xy45.下列说法中,正确的是A、相同原子间的双键键能是单键键能的两倍B、原子形成共价键的数目等于基态原子的未成对电子数C、分子轨道是由同一原子中能量相近、对称性匹配的原子轨道组合而成D、p y 和d xy 的线性组合形成π成键轨道和π反键轨道46.下列关于O22-和O2-的性质的说法中,不正确的是A、两种离子都比O2分子稳定性小B、O22-的键长比O2-键长短C、O22-是反磁性的,而O2-是顺磁性的D、O22-的键能比O2-的键能小47.下列分子和离子中,中心原子杂化轨道类型为s p3 d杂化,且分子(离子) 空间构型呈直线型的是A、ICl2-B、SbF4-C、CO2D、SO248.若中心原子采用sp3d杂化轨道成键的分子,其空间构型可能是A、三角双锥形B、变形四面体C、直线形D、以上三种均有可能49.AB2型的分子或离子,其中心原子可能采取的杂化轨道类型是A、s p B、s p2C、s p3 D、除A、B、C 外,还有s p3d50.下列物质熔点沸点变化顺序中,正确的一组是A、He >Ne >Ar B、HF >HCl >HBr C、CH4 < SiH4 < GeH4D、W >Cs >Ba51.下列物质熔点高低顺序正确的是A、He > Kr B、Na < Rb C、HF < HCl D、MgO > CaO52.下列化学键中,极性最弱的是A、H-F B、H-O C、O-F D、C-F53.下列叙述中正确的是A、F2的键能低于Cl2B、F的电负性低于Cl C、F2的键能大于Cl2D、F的第一电离能低于Cl54.OF2分子的中心原子采取的杂化轨道是A、s p2B、s p3C、s p D、d s p255.CH4分子中,C-H键是属于A、离子键B、p-p键C、s -s p3σ键D、配位共价键56.CO2分子中,碳原子轨道采取的杂化方式是A、s p B、s p2 C、s p3等性杂化D、s p3不等性杂化57.下列分子中属于极性分子的是A、SiCl4( g ) B、SnCl2( g ) C、CO2 D、BF358.下列各组判断中,正确的是A、CH4,CO2是非极性分子B、CHCl3,BCl3,H2S,HCl是极性分子C、CH4,H2S,CO2是非极性分子D、CHCl3,BCl3,HCl是极性分子59.下列各组判断中,不正确的是A、CH4,CO2,BCl3是非极性分子B、CHCl3,HCl,H2S是极性分子C、CH4,CO2,BCl3,H2S,是非极性分子D、CHCl3,HCl是极性分子60.为确定分子式为XY2的共价化合物是直线型还是弯曲型的,最好是测定它的A、与另一个化合物的反应性能B、偶极矩C、键能D、离子性百分数61.在单质碘的四氯化碳溶液中,溶质和溶剂分子之间存在着A、取向力B、诱导力C、色散力D、诱导力和色散力62.下列物质中属于以分子间作用力结合的晶体是A、KBr(s) B、CO2(s) C、CuAl2(s) D、SiC(s)63.下列物质在液态时只需要克服色散力就能使之沸腾的是A、O2B、CO C、HF D、H2O64.下列能形成分子间氢键的物质是A、NH3B、C2H4C、HI D、H2S65.下列氢键中最强的是A、S-H……O B、N-H……N C、F-H……F D、C-H……N66.HCl,HBr,HI三种物质的沸点依次升高的主要原因是A、范德华力减小B、取向力增大C、诱导力增大D、色散力增大67.下列化合物中,不存在氢键的是A、HNO3B、H2S C、H3BO3 D、H3PO368.下列化合物中,存在分子内氢键的是A、H2O B、NH3C、CH3F D、HNO369.SO2分子间存在着A、色散力B、色散力、诱导力C、色散力、取向力D、色散力、诱导力、取向力70.干冰升华时吸收的能量用于克服A、键能B、取向力C、诱导力D、色散力71.晶体溶于水时,其溶解热与下列两种能量的相对值有关的是A、离解能和电离能B、离解能和水合能C、水合能和晶格能D、晶格能和电离能72.电价键占优势的液态化合物的特征是A、凝固点低,导电性弱B、凝固点高,导电性强C、凝固点低,导电性强D、凝固点高,导电性弱73.下列说法中不正确的是A、σ键比π键的键能大B、形成σ键比形成π键电子云重叠多C、在相同原子间形成双键比形成单键的键长要短D、双键和叁键都是重键74.下列分子中C与O之间键长最短的是A、CO B、CO2C、CH3OH D、CH3COOH75.下列分子或离子中,呈反磁性的是A、B2B、O2C、CO D、NO76.下列分子和离子中,中心原子杂化轨道类型为s p3 d杂化,且分子(离子) 空间构型呈直线型的是A、ICl-2B、SbF-4C、IF3D、ICl-477.按分子轨道理论,O-2的键级是A、1 B、2 C、121D、22178.按分子轨道理论,下列稳定性大小顺序正确的是A、N-22>N-2>N2B、N2 >N-2> N-22C、N-2>N-22> N2D、N-2>N2 > N-2279.下列分子或离子中,磁性最强的是A、O2B、O2-C、O2+D、O22-80.在下列物质中,氧原子间化学键最稳定的是A、O22-B、O2-C、O2D、O2+81.下列分子中,中心原子以s p 3 d 2杂化的是A、IF5B、PCl5C、SF4D、XeF282.根据分子轨道理论,下列分子或离子中键级最高的是A、O22+B、O2+C、O2D、O2-83.用分子轨道理论来判断下列说法,不正确的是A、N2+的键能比N2分子的小B、CO+的键级是2.5C、N2-和O2+是等电子体系D、第二周期同核双原子分子中,只有Be2分子不能稳定存在84.按分子轨道理论,下列分子或离子中键级等于2的是A、O2-B、CN-C、Be2D、C285.下列说法中正确的是A、BCl3分子中B-Cl键是非极性的B、BCl3分子和B-Cl键都是极性的C、BCl3分子是极性分子,而B-Cl键是非极性键D、BCl3分子是非极性分子,而B-Cl键是极性键86.ClO3F分子的几何构型属于A、直线形B、平面正方形C、四面体形D、平面三角形87.下列物质中,属于极性分子的是A、PCl5(g) B、BCl3C、NCl3 D、XeF288.用VSEPR判断下列离子或分子几何构型为三角锥形的是A、SO3B、SO32-C、NO3-D、CH3+89.下列各组分子中,均有极性的一组是A、PF3,PF5B、SF4,SF6C、PF3,SF4D、PF5,SF690.下列物质中,含极性键的非极性分子是A、H2O B、HCl C、SO3D、NO291.下列各对物质中,分子间作用力最弱的是A、NH3和PH3B、He和Ne C、N2和O2D、H2O和CO292.下列分子中,分子间作用力最强的是A、CCl4B、CHCl3C、CH2Cl2 D、CH3Cl93.下列说法中正确的是A、色散力仅存在于非极性分子之间B、极性分子之间的作用力称为取向力C、诱导力仅存在于极性分子与非极性分子之间D、分子量小的物质,其熔点、沸点也会高于分子量大的物质94.在NaCl晶体中,Na+(或Cl-)离子的最大配位数是A、2 B、4 C、6 D、895.下列物质熔点变化顺序中,正确的一组是A、MgO>BaO> BN> ZnCl2>CdCl2B、BN>MgO>BaO>CdCl2>ZnCl2C、BN>MgO>BaO> ZnCl2>CdCl2D、BN> BaO>MgO> ZnCl2> CdCl296.ICl-2离子中,其中心原子I的杂化态为A、s p3B、s p2C、d s p3D、s p3 d97.CO-23的几何构型是A、平面三角形B、三角锥形C、T字形D、直线形98.下列分子中,偶极矩为零的是A、CO2B、SO2C、H2O D、NH399.下列化合物中,既存在离子键和共价键,又存在配位键的是A、NH4F B、NaOH C、H2S D、BaCl2100.下列氯化物的热稳定次序正确的是A、NaCl>MgCl2>AlCl3>SiCl4B、NaCl<MgCl2<AlCl3<SiCl4C、NaCl<MgCl2>AlCl3>SiCl4D、NaCl>MgCl2<AlCl3>SiCl4101.石英和金刚石的相似之处在于A、都具有四面体结构B、都是以共价键结合的原子晶体C、都具有非极性共价键D、其硬度和熔点相近102.如果正离子的电子层结构类型相同,在下述情况中极化能力较大的是A、离子的电荷多,半径大B、离子的电荷多,半径小C、离子的电荷少,半径大D、离子的电荷少,半径小103.下列离子中,极化率最大的是A、Na+B、I-C、Rb+D、Cl-104.下列离子中,属于(9~17)电子构型的是A、Li+B、F-C、Fe3+D、Pb2+105.下列离子中,变形性最大的是A、CO-23B、SO-24C、ClO-4D、MnO-4106.下列分子中,偶极矩不为零的是A、CO2B、BF3C、CHCl3 D、PCl5107.下列说法正确的是A、非极性分子内的化学键总是非极性的B、色散力仅存在于非极性分子之间C、取向力仅存在于极性分子之间D、有氢原子的物质分子间就有氢键108.按离子的电子构型分类,Li+属于A、9~17电子型B、2电子型C、8电子型D、18电子型C、B2 109.下列分子或离子中键级等于零的是A、O2B、O+2D、Ne2110.根据VSEPR理论,可判断下列分子中具有直线形结构的是A、CS2B、NO2 C、OF2D、SO2111.下列分子中,偶极矩不为零的是A、CCl4B、PCl5C、PCl3 D、SF6112.下列各组物质中,熔点最高的一组是A、NaI和SiI4B、NaI和SiF4 C、NaF和SiF4D、NaF和SiI4113.下列说法不正确的是A、离子晶体中,离子的电荷数越多,核间距离越大,晶格能越大B、离子晶体在熔融时能导电C、离子晶体的水溶液能导电D、离子晶体中,晶格能越大,通常熔点越高,硬度越大114.关于杂化轨道的下列说法,正确的是A、CH4分子中的s p3杂化轨道是由H原子的1个n s轨道和C原子的3个p轨道混合起来而形成的B、s p3杂化轨道是由同一原子中的1个n s轨道和3个n p轨道混合起来重新组合成的4个新的原子轨道C、凡是中心原子采取s p3杂化轨道成键的分子,其几何构型都是正四面体D、凡AB3型共价化合物,其中心原子A均采用s p3杂化轨道成键115.常态下:F2、Cl2是气态,Br2是液态,I2是固态,这是由于A、聚集状态不同B、电负性不同C、价电子构型不同D、色散力不同116.下列分子中极性最小的是A、H2O B、NH3C、H2S D、CO2117.下列化合物中,熔点最高的是A、CaO B、SrO C、BaO D、MgO118.下列关于共价键说法错误的是A、两个原子间键长越短,键越牢固B、两个原子半径之和约等于所形成的共价键键长C、两个原子间键长越长,键越牢固D、键的强度与键长无关119.下列关于杂化轨道说法错误的有A、所有原子轨道都参与杂化B、同一原子中能量相近的原子轨道参与杂化C、杂化轨道能量集中,有利于牢固成键D、杂化轨道中一定有一个电子120.s轨道和p轨道杂化的类型有A、s p,s p2B、s p,s p2,s p3C、s p,s p3 D、s p,s p2,s p3,s p3不等性121.下列晶体中具有σ键、大π键和分子间力的有A、MgO B、BN C、CO2(s) D、石墨122.下列关于晶体点缺陷说法错误的是A、点缺陷主要是由于升高温度和掺入杂质引起的B、置换固溶体可看做是一种点缺陷C、点缺陷仅限于晶体中的某一点上D、点缺陷可发生在晶体中的某些位置123.根据分子轨道理论解释He 2分子不存在,是因为其电子排布式为A、(σs1)2 (σ*s1)2B、(σs1)2 (σ2 s)2C、(σs1)2 (σ*s1)1 (σ2 s)1 D、(σs1)2(σ2p)2124.下列分子构型中以s p3杂化轨道成键的是A、直线形B、平面三角形C、八面体形D、四面体形125.非整数比化合物的化学式为A、AmBn+δB、AnBm C、AmBn (1+D、A1Bm (1+126.下列分子或离子中键角最小的是A、NH3B、PCl4+C、BF3D、H2O E、ICl2-127.下列叙述中错误的是A、相同原子间双键的键能等于单键键能的两倍B、对双原子分子来说,键能等于键离解能C、对多原子分子来说,原子化能等于各键键能总和D、键级、键能和键离解能都可作为衡量化学键牢固程度的物理量,其数值愈大,表示键愈强128.下列叙述中正确的是A、旋转操作后ψ 数值恢复但符号相反,这种原子轨道属于u对称B、H2O分子的C2旋转轴是通过O原子核并垂直于分子平面的轴C、HF的最高占有轨道是1π反键轨道D、HF分子中对成键有贡献的是进入3σ的电子129.IF5的空间构型是A、三角双锥形B、平面三角形C、四方锥形D、变形四面体130.下列键能大小顺序中正确的是A、O2+<O2<O2-B、NO<NO+C、N2>O2> O2+D、CO<NO<O2131.H2S分子的空间构型、中心原子的杂化方式分别为A、直线形、s p杂化B、V形、s p2杂化C、直线形、s p3 d杂化D、V 形、s p3杂化132.下列叙述中错误的是A、单原子分子的偶极矩等于零B、键矩愈大,分子的偶极矩也愈大C、有对称中心的分子,其偶极矩等于零D、分子的偶极矩是键矩的矢量和133.下列各组物质沸点高低顺序中正确的是A、HI>HBr>HCl>HFB、H2Te>H2Se>H2S>H2OC、NH3>AsH3>PH3D、CH4>GeH4>SiH4134.在金属晶体的面心立方密堆积结构中,金属原子的配位数为A、4 B、6 C、8 D、12135.下列离子中,极化力最大的是A、Cu+B、Rb+C、Ba2+D、Sr 2+136.下列离子半径大小次序中错误的是 A 、Mg 2+<Ca 2+ B 、Fe 2+>Fe 3+ C 、Cs +>Ba 2+ D 、F ->O 2-137.下列分子中至少有两个长度的键的是 A 、CS 2 B 、BF 3 C 、SF 4D 、XeF 4138.下列分子中,其空间构型不是“V”字形的是 A 、NO 2 B 、O 3 C 、SO 2 D 、BeCl 2139.下列分子中,其空间构型不是“V”字形的是 A 、NO 2 B 、O 3 C 、SO 2 D 、XeF 2140.由键级大小推断下列键长大小次序正确的是A 、N 2>N +2和NO>NO +B 、N 2>N +2和NO<NO +C 、N 2<N +2和NO<NO +D 、N 2<N +2和NO>NO +141.按照分子轨道理论,O 2的最高占有轨道是 A 、1πu B 、1πg C 、3σ u D 、3σ g142.下列式子中,X 是以s p 杂化轨道成键的是A 、 A -X -AB 、A =X =AC 、 A =••X -XD 、A -••••X -A 143.下列分子中,具有直线形结构的是 A 、OF 2 B 、NO 2 C 、SO 2D 、CS 2144.下列分子中,具有直线形结构的是 A 、OF 2 B 、NO 2 C 、SO 2D 、XeF 2145.已知H -H 、Cl -Cl 和H -Cl 的键能分别为436、243和431 kJ·mol -1,则下列反应H 2 ( g )+ Cl 2 ( g ) =2 HCl ( g )的焓变kJ·mol -1)为A 、-183B 、183C 、-248D 、248146.在25℃和标态下,已知NH 3的生成焓Δ f H m Θ =-46.2 kJ·mol -1,H -H 和N≡N 的键能分别为436和946 kJ·mol -1,则N -H 键的键能(kJ·mol -1)为A 、1173B 、-1173C 、391D 、-391147.已知C -H 的键能为416 kJ·mol -1,CH 3Cl(g)的原子化热为1574 kJ·mol -1,C -Cl 的键能(kJ·mol -1)为A 、326B 、-326C 、357D 、-357148.下列离子的电子结构中,未成对电子数等于零的是 A 、Cu 2+ B 、Mn 2+C 、Pb 2+D 、Fe 2+149.下列离子的电子结构中,未成对电子数等于零的是 A 、Cu 2+ B 、Mn 2+C 、Cd 2+D 、Fe 2+150.根据VSEPR 理论,可判断XeO 3和ClF 3的分子空间构型是A 、平面三角形和三角锥形B 、三角锥形和T 字形C 、T 字形和平面三角形D 、三角锥形和平面三角形151.原子轨道之所以要发生杂化是因为A 、进行电子重排B 、增加配对的电子数C 、增加成键能力D 、保持共价键的方向性152.在Br -CH =CH -Br 分子中,C -Br 键的轨道重叠方式是 A 、s p -p B 、s p 2-s C 、s p 2-p D 、s p 3-p153.在下列物种中,不具有孤电子对的是A、NCl3B、H2S C、OH -D、NH+4154.HNO3的沸点(86℃)比H2O的沸点(100℃)低得多的原因是A、HNO3的分子量比H2O的分子量大得多B、HNO3形成分子间氢键,H2O形成分子内氢键C、HNO3形成分子内氢键,H2O形成分子间氢键D、HNO3分子中有Π4大3π键,而H2O分子中没有155.PH3分子中P原子采取的杂化类型是A、s p B、s p2C、s p3 D、不等性s p3156.分子间的范德华力是随下列哪一个量值增加而增加?A、分子量B、温度C、电子数D、电离能157.CH3OCH3和HF分子之间存在的作用力有A、取向力、诱导力、色散力、氢键B、取向力、诱导力、色散力C、诱导力、色散力D、色散力158.下列各组物质中,两种分子间存在氢键的一组是A、CH3OH和HF B、HCl 和HBr C、C6H6和H2O D、H2S和H2O159.下列单键键能最大的是A、O-H B、F-H C、F-F D、N-H160.下列说法中正确的是A、非极性分子中没有极性键B、键长不是固定不变的C、四个原子组成的分子一定是四面体D、三个原子组成的分子一定是直线形161.下列分子中键有极性,分子也有极性的是A、PH3 B、SiF4C、BF3 D、CO2162.下列杂化轨道中可能存在的是A、n=1 的sp B、n=2 的sp3d C、n=2 的sp3D、n=3 的sd163.在H-C-H 分子中,四个原子处于同一平面上,C原子采用的杂化轨道是‖OA、spB、sp2C、sp3D、sp3d164.在乙烯(CH2=CH2)分子中,六个原子处于同一平面上,一条π键垂直于该平面,则C原子采用的杂化轨道是A、spB、sp2C、sp3D、sp3d165.乙醇和醋酸易溶于水而碘和二硫化碳难溶于水的根本原因是A、分子量不同B、有无氢键C、分子的极性不同D、分子间力不同166.在N2、O2和F2分子中,键的强度次序为N2 >O2 > F2。
第2章化学键与分子结构

第2章化学键与分子结构第2章化学键与分子结构习题一、思考题1.什么叫共价键的饱和性和方向性?为什么共价键具有饱和性和方向性,而离子键无饱和性和方向性?2.举例说明什么是σ键,什么是π键?它们有哪些不同?3.价键理论和分子轨道理论的基本要点是什么?4.s、p原子轨道主要形成哪几种类型的杂化轨道?中心原子利用上述杂化轨道成键时,其分子构型如何?5.实验测定BF3为平面三角形,而[BF4]-为正四面体形。
试用杂化轨道的概念说明在BF3和[BF4]-中硼的杂化轨道类型有何不同?6.试用分子轨道表示式写出O2+的电子构型。
7.分子间力有几种?各种力产生的原因是什么?试举例说明极性分子之间、极性分子和非极性分子之间以及非极性分子之间的分子间力。
在大多数分子中以哪一种分子间力为主?8.何为极性分子和非极性分子?分子的极性与化学键的极性有何联系?9.分子间力的大小对物质的物理性质有何影响?10.什么叫做氢键?哪些分子间易形成氢键?形成氢键对物质的性质有哪些影响?11.氢键与化学键有何区别?与一般分子间力有何区别?12.下列各化合物中分子间有氢键的有哪几种?C2H6,NH3,C2H5OH,H3BO3,CH4。
13.写出下列物质的晶体类型:SO2,SiC,HF,KCl,MgO。
14.晶体有几种类型?确定晶体类型的主要因素是什么?各种类型晶体的性质有何不同?15.根据下列物质的性质,判断它们是属于何种类型的晶体。
(1)CaCO3晶体的硬度高,在1173K时尚未熔融就已分解。
(2)B的硬度极高,熔点为2573K,导电性很差。
(3)SnCl4熔点为240K,沸点为387K16.要使BaF2,F2,Ba,Si晶体熔融,需分别克服何种作用力?二、是非题(对的在括号内填“√”号,错的填“×”号)1.共价键的重叠类型有σ键π键两种。
()2.NH3和BF3都是4原子分子,所以二者空间构型相同。
()3.He2的分子轨道表示式为(σ1s)2(σ1s*)2。
(完整版)化学键习题及答案

化学键一、离子键1、下列说法正确的是( D )A.含有金属元素的化合物一定是离子化合物B.第IA族和第VIIA族原子化合时,一定生成离子键C.由非金属元素形成的化合物一定不是离子化合物D.活泼金属与非金属化合时,能形成离子键2、与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( AD ) A. Na2S B. CCl4 C. KCl D. KF3、下列说法正确的是:( D )A.离子键就是使阴、阳离子结合成化合物的静电引力B.所有金属与所有非金属原子之间都能形成离子键C.在化合物CaCl2中,两个氯离子之间也存在离子键D.钠原子与氯原子结合成氯化钠后体系能量降低4、下列各数值表示有关元素的原子序数,能形成AB2型离子化合物的是: ( D )A.6与8B.11与13C. 11与16D.12与17二、电子式1.下列电子式有误的是( BC )A.氯原子• Cl∶ B.硫离子∶S∶ C.溴离子 [∶Br∶] D.钙离子Ca2+2.下列用电子式表示化合物的形成过程正确的是:( A )3. 用电子式表示下列离子化合物的形成过程:(1)Na2O (2)MgBr24.下列化合物电子式书写正确的是( BD )A.Ca2+[∶Cl∶]-2B.Na+[∶S∶]2-Na+C. [Mg2+][∶O∶]2-D. Na+[∶F∶]-三、共价键1.下列物质中含有共价键的离子化合物是( AB )A.Ba(OH)2B.CaCl2C.H2OD.H22、下列既含有离子键又含有共价键的化合物是( B )A.HI B.NaOH C.Br2 D.NaCl3.下列电子式书写正确的是( A )A.∶N ∶∶∶N ∶B.H ∶N ∶HC.H +[∶O ∶]2-H +D.Na +[∶Cl ∶]-4.下列说法中正确的是( AD )A.含有离子键的化合物必是离子化合物B.具有共价键的化合物就是共价化合物C.共价化合物可能含离子键D.离子化合物中可能含有共价键四、化学键1.下列物质中,不存在化学键的是( D )A.水B.食盐C.氯气D.氦气2.下列各分子中,化学键类型有差异的是( B )A.H2O 、CO2B.MgF2、H2O2C.NaOH 、Ba(OH)2D.NaCl 、KCl3、下列说法正确的是 ( D )A.含有金属元素的化合物一定是离子化合物B.第ⅠA 族和第ⅦA 族原子化合时,一定生成离子键C.由非金属元素形成的化合物一定不是离子化合物D.活泼金属与非金属化合时,能形成离子键其中A 项AlCl3是共价化合物;B 项HCl 是共价键;C 项如NH4Cl 是离子化合物。
(完整版)第四章分子结构习题及答案

第四章分子结构习题1。
是非判断题1-1化学键是相邻原子与原子(或离子与离子)之间的强烈相互作用。
1—2 50Sn2+是18+2电子构型,50Sn4+是18电子构型。
1-3 Al3+,Ba2+,Si(IV)的电子构型都属于8电子构型.1-4具有未成对电子的两个原子相互接近时可以形成稳定的共价键.1—5原子形成共价键的数目等于基态原子的未成对电子数。
1-6σ键的特点是原子轨道沿键轴方向重叠,重叠部分沿键轴呈圆柱形对称。
1-7一般来说,σ键的键能比π键键能小。
1—8 s电子与s电子配对形成的键一定是σ键,p电子与p电子配对形成的键一定为π键.1—9两个σ键组成一个双键.1-10键的强度与键长无关。
1-11所有非金属元素之间形成的化合物都不是离子化合物。
1—12μ=0的分子,其化学键一定是非极性键.1—13共价键具有饱和性的原因在于每个原子提供一定数目的自旋方向相反的未成对电子。
1—14原子核外有几个未成对电子,就能形成几个共价键。
1-15共价键类型可以分为σ键和π键,π键的键能小于σ键的键能,因此π键的稳定性弱于σ键. 1—16烷烃分子中C-H键的键能为413 KJ·mol -1,因此提供413KJ·mol -1的能量能使甲烷和乙烷分子中C-H键断裂。
1-17沿键轴方向的s轨道和p轨道进行重叠可形成π键。
1-18原子轨道相互重叠应满足最大重叠原理,所以沿键轴以“头碰头”方式才能成键。
1—19原子轨道之所以要发生杂化是因为能增大成键能力。
1—20 sp3杂化是,s轨道的主量子数和p轨道的主量子数可以是不同的,也可以是相同的。
1-21 1个s轨道和3个p轨道,形成1个sp3杂化轨道.1-22在sp,sp2,sp3杂化中,杂化轨道的成键能力随s轨道成分增多而增强。
1-23发生轨道杂化的原子轨道可以具有成对电子。
1-24原子轨道发生杂化,若轨道上有孤对电子存在,这类杂化是不等性的。
1-25 NH3和H2O分子中的中心原子都是发生sp3杂化,但氧原子的2对孤对电子占据2 个杂化轨道而产生更大的斥力,使O—H键键角大于氨分之中N—H键键角。
结构化学课后习题答案

结构化学课后习题答案结构化化学课后习题答案一、化学键与分子结构1. 选择题a) 正确答案:D解析:选择题中,选项D提到了共价键的形成是通过电子的共享,符合共价键的定义。
b) 正确答案:B解析:选择题中,选项B提到了离子键的形成是通过电子的转移,符合离子键的定义。
c) 正确答案:C解析:选择题中,选项C提到了金属键的形成是通过金属原子之间的电子云重叠,符合金属键的定义。
d) 正确答案:A解析:选择题中,选项A提到了氢键的形成是通过氢原子与高电负性原子之间的吸引力,符合氢键的定义。
2. 填空题a) 正确答案:共价键解析:填空题中,根据问题描述,两个非金属原子之间的键称为共价键。
b) 正确答案:离子键解析:填空题中,根据问题描述,一个金属原子将电子转移到一个非金属原子上形成的键称为离子键。
c) 正确答案:金属键解析:填空题中,根据问题描述,金属原子之间的电子云重叠形成的键称为金属键。
d) 正确答案:氢键解析:填空题中,根据问题描述,氢原子与高电负性原子之间的吸引力形成的键称为氢键。
二、有机化学1. 选择题a) 正确答案:C解析:选择题中,选项C提到了烷烃是由碳和氢组成的,符合烷烃的定义。
b) 正确答案:D解析:选择题中,选项D提到了烯烃是由含有一个或多个双键的碳原子组成的,符合烯烃的定义。
c) 正确答案:B解析:选择题中,选项B提到了炔烃是由含有一个或多个三键的碳原子组成的,符合炔烃的定义。
d) 正确答案:A解析:选择题中,选项A提到了芳香烃是由芳香环结构组成的,符合芳香烃的定义。
2. 填空题a) 正确答案:醇解析:填空题中,根据问题描述,含有羟基(-OH)的有机化合物称为醇。
b) 正确答案:醚解析:填空题中,根据问题描述,含有氧原子连接两个碳原子的有机化合物称为醚。
c) 正确答案:酮解析:填空题中,根据问题描述,含有羰基(C=O)的有机化合物称为酮。
d) 正确答案:酯解析:填空题中,根据问题描述,含有羧基(-COO)的有机化合物称为酯。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1
General Chemistry
Chapter 3 Homework
5.下列分子中含有极性键的非极性分子是( A ) A.BeCl2 A.O2B.H2S B.S2C.F2 C.FD.HBr 6.下列物种中,变形性最大的是( B )。 D.Cl7. 下列物质中只需克服色散力即沸腾的是( D ) A.HCl B.Cu C.CH2Cl2 D.CS2
9
8. 下列化合物中存在氢键的是( C )
A.HCl B.C2H5OC2H5 C.HNO3 D.CH3F
形成氢键要具备两个条件: ① 分子中必须有电负性较大而半径较小的元素(X=F、O、 N),并与H形成共价键; ② 分子中还必须有另外一个电负性大而半径小,有孤对电子的 原子(Y=F、O、N) 。
2
General Chemistry
2012-8-2
ionic bond theory
11
General Chemistry
Chapter 3 Molecular Structure
影响离子变形性的因素: ① 离子的半径。半径越大,变Байду номын сангаас性越大。 如:I->Br- >Cl- >F② 离子的电荷。负离子电荷越高,变形性越大,正离子电 荷越高,变形性越小。
如: O2- > F- >Na+ > Mg2+ > Al3+ >Si4+
③ 离子的电子构型。 18电子构型、 9~17电子构型>8电子构型 ④ 复杂离子的变形性通常不大,且复杂离子中心原子氧 化数越高,变形性越小。 如: I->Br- >OH- > NO3- >F- >ClO49
2012-8-2
Supplement(transition of bonding type)
I(g)
EA
4
General Chemistry
Chapter 3 Homework
四、简答题 1.试用杂化轨道理论说明BF3是平面三角形,而NF3却 是三角锥形。 BF3中的B采用等性sp2杂化,形成三条sp2杂化轨道,
分别与三个F的p轨道形成σ键。其分子构型Wie平面三角形。
NF3中的N采用不等性的sp3杂化,形成四条sp3杂化轨 道,其中一条被孤对电子占据,另外的三条分别与F的p轨 道形成σ键。由于孤对电子的存在,使得NF3呈三角锥形。
General Chemistry
Chapter 3 Molecular Structure
离子半径的变化规律 ◆同一元素,r正<r原子<r负,正电荷数增大离子半径减小 如: r(Fe3+)< r(Fe2+) < r(Fe)。 ◆同主族元素,自上而下,具有相同电荷的离子半径依次增大 如:r (Li+)<r (Na+)<r(K+)<r (Rb+)<r (Cs+); r(F-)<r(Cl-)<r(Br-)<r(I-) ◆同一周期中,电子构型相同时,随着离子电荷数增加,正离 子半径减小,负离子半径增大 如:r (Na+) >r(Mg2+) >r (Al3+); r(F-)<r(O2-)<r(N3-) ◆元素周期表中处于相邻的左上方和右下方斜对角线上的正离 子半径近似相等 如: r (Li+)(60pm) ≈ r(Mg2+)(65pm) ; r (Na+)(95pm) ≈ r(Ca2+)(99pm) 8
5. 比较下列各组中两种物质的熔点高低,并简单说明原因。 (提示:分子间作用力,氢键,晶体类型,极化作用都可 能影响物质熔沸点) (1) NH3和PH3 (2) PH3和SbH3 (3) Br2和ICl (4) MgO和Na2O (5) SiO2和SO2 (6) SnCl2和SnCl4
(1) NH3>PH3 (2) PH3<SbH3 (3) Br2<ICl (4) MgO>Na2O (5) SiO2>SO2 (6) SnCl2>SnCl4 前者分子间存在氢键 后者分子量大,分子间作用力强 后者为极性分子 前者阳离子电荷高,半径小,晶格能大 前者为原子晶体,后者为分子晶体 后者阳离子极化能力强,分子共价成分多 7
3
General Chemistry
三、计算题 已知KI的晶格能(U)为-631.9kJ∙mol-1,钾的升华热为 90.0kJ∙mol-1,钾的电离能为418.9 kJ∙mol-1,碘的升华热为62.4 kJ∙mol-1,碘的离解能为151 kJ∙mol-1,碘的电子亲合能为-310.5 kJ∙mol-1,求碘化钾的生成热(△fHm⊙)。 解: K(s) + 1/2I2(s)
Chapter 3 Homework
二、填空题
1.Fe原子的价层电子组态 3d64s2 ,Fe2+的价层组态为 3d6 , Fe3+的价层组态为 3d5 ,二者的半径大小为 r(Fe2+) >r(Fe3+) 。 2.Li—F,Li—H,Li—Li,Li—S按键极性由大到小应排为 Li—F>Li—S>Li—H>Li—Li __________________________________________________。 3.C2H4分子中包含有 5 个σ键, 1 个π键,两个C原子采用 C C 了 sp2 杂化形式,π键在 原子与 原子间形成。 4.AgCl、AgBr、AgI在水中的溶解度依次 减小 ,颜色依 次 加深 ,这是因为 Ag+具较强的极化作用,而Cl-、Br-、I离子的半径依次增大,变形性增强,化合物共价性依次增强。 。 5.H2Te比H2S的沸点高是因为 H2Te的分子量大,分子间 作用力大 ,而H2O比H2S的沸点高则因为 H2O间存在氢键 。
5
General Chemistry
Chapter 3 Homework
2. 将下列化合物按熔点从高到低的顺序排列: NaF SiF4 NaBr SiBr4 NaCl SiCl4 NaI SiI4 NaF >NaCl> NaBr> NaI> SiI4> SiBr4> SiCl4 > SiF4 3. 指出下列各对分子之间存在的分子间作用力的类型(取 向力、诱导力、色散力、氢键): (1) 苯和CCl4 (3) CO2和H2O (2) 甲醇和H2O (4) HBr和HI
(1) 色散力(非极性分子间) (2) 色散力、取向力、诱导力、氢键(极性分子间) (3) 色散力、诱导力、(极性和非极性分子间) (4) 色散力、取向力、诱导力、(极性分子间)
6
General Chemistry
Chapter 3 Homework
4. 下列化合物中哪些化合物能形成氢键? C2H6 H2O2 C2H5OH CH3CHO H3BO3 H2SO4 (CH3)2O H2O 2 C2H5OH H3BO3 H2SO4
△subHm △subHm △fHm⊙
Chapter 3 Homework
KI(s)
U
1/2I2(g)
△disHm
I-(g) + I K(g) K+(g) △fHm⊙= △subHm(K)+I(K)+1/2 △subHm(I2) + 1/2△disHm(I2)+EA(I2)+U = -326.8(kJ· -1) mol
General Chemistry
Chapter 3 Homework
第三章 分子结构
一、选择题:
1.下列离子中具有9~17电子组态的是( B ) A.Na+ B.Ni2+ C.Pb2+ D.Zn2+ 2.下列各组中离子原子半径大小关系不正确的是( B ) A.Na+ < Cs+ B.Cu2+ > Cu+ C.S2- > ClD.F- > F 3.在BrCH=CHBr分子中,C-Br键采用的成键轨道是( C ) A.sp-p B.sp2-s C.sp2-p D.sp3-p 4.下列分子中具有平面三角形几何构型的是( B ) A.ClF3 B.BF3 C.NH3 D.PCl3
