第八章__配位平衡与滴定
无分—配位平衡与配位滴定法

Fe(CO)5
S92-
2. 配位体 ligand
① 配位体 与中心离子直接结合的阴 离子或分子。 配体中配体和多基配体
② 配位原子 合的原子,含孤对电子。
单基(齿)配体(unidentate ligand) NH3 H2O CN- OHSCN- 硫氢根 C2O42en FNCS- 异硫氢根
[Cu(NH3)4]SO4
K3[Fe(CN)6]
二.配合物的组成
配位原子
[Cu(NH3)4]SO4 [Ag(NH3)2]Cl
中心离子 配位体 内界 外界 配合物
配位数
K3[Fe(CN)6]
◆ ◆ ◆ ◆ ◆
1. 中心离子 central cation ——形成体 过渡金属阳离子 Cu2+ 、Ag+ 、 Ni2+ 、Zn2+ 主族阳离子 Al3+ 、 Ca2+ 、 Mg2+ 高价非金属元素 SiF62- 、 BF4金属原子 阴离子 Ni(CO)4 I 3、 、 、 PF6 -
三. 配位化合物的命名
1.内界与外界命名
外界为简单负离子 [ ] X,称某化某 , ] SO4 ,称某酸某 。 ]配离子是负离子,则将 外界为复杂复离子,[ 外界为正离子, K[
配阴离子看成复杂酸根离子,称某酸某
2+ [Cu(NH ) ] 四氨合铜(II) 2、内界的命名顺序 3 4
配位数(一、二、三…) —配体名称 —“合”—中心离子名称—中心离子 电荷数(罗马数字); 3、配体命名顺序 [CoCl(H2O) (en)2]Cl2
b. 中心离子半径越大,配位数越大; c. 配体电荷越少、体积越小时,配位数越大;
d.配体浓度越大,温度越低,配位数越大。
配位平衡与配位滴定法共37页PPT

谢谢!
21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈
23、一切节省,归根到底都归结为时间的节省。——马克思 24、意志命运往往背道而驰,决心到最后会全部推倒。——莎士比亚
配位平衡与配位滴定法
26、机遇对于பைடு நூலகம்准备的头脑有特别的 亲和力 。 27、自信是人格的核心。
28、目标的坚定是性格中最必要的力 量泉源 之一, 也是成 功的利 器之一 。没有 它,天 才也会 在矛盾 无定的 迷径中 ,徒劳 无功。- -查士 德斐尔 爵士。 29、困难就是机遇。--温斯顿.丘吉 尔。 30、我奋斗,所以我快乐。--格林斯 潘。
无机及分析化学第八章答案
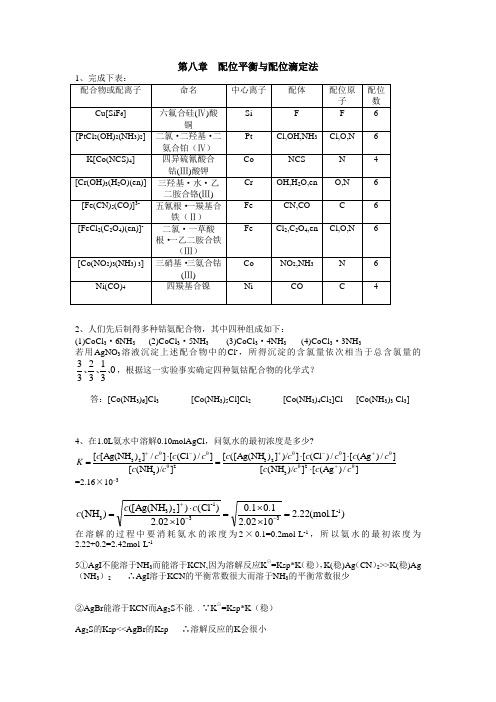
第八章 配位平衡与配位滴定法2、人们先后制得多种钴氨配合物,其中四种组成如下:(1)CoCl 3·6NH 3 (2)CoCl 3·5NH 3 (3)CoCl 3·4NH 3 (4)CoCl 3·3NH 3若用AgNO 3溶液沉淀上述配合物中的Cl -,所得沉淀的含氯量依次相当于总含氯量的0313233、、、,根据这一实验事实确定四种氨钴配合物的化学式?答:[Co(NH 3)6]Cl 3 [Co(NH 3)5Cl]Cl 2 [Co(NH 3)4Cl 2]Cl [Co(NH 3)3 Cl 3]4、在1.0L 氨水中溶解0.10molAgCl ,问氨水的最初浓度是多少?=2.16×10–3)mol.L (22.21002.21.01.01002.2)(Cl )])[Ag(NH ()(NH 1-33-1233=⨯⨯=⨯⋅=--+c c c 在溶解的过程中要消耗氨水的浓度为2×0.1=0.2mol·L -1,所以氨水的最初浓度为 2.22+0.2=2.42mol·L -15①AgI 不能溶于NH 3而能溶于KCN,因为溶解反应K ⊙=Ksp*K (稳),K(稳)Ag (CN )2>>K(稳)Ag (NH 3)2 ∴AgI 溶于KCN 的平衡常数很大而溶于NH 3的平衡常数很少②AgBr 能溶于KCN 而Ag 2S 不能,,∵K ⊙=Ksp*K (稳)Ag 2S 的Ksp<<AgBr 的Ksp ∴溶解反应的K 会很小]/)Ag ([])/(NH []/)Ag ([]/)Cl ([])/])([Ag(NH [])/(NH []/)Cl ([]/])Ag(NH [[θ2θ3θθθ232θ3θθ23c c c c c c c c c c c c c c c c K ++-+-+⋅⋅⋅=⋅=③Fe 与SCN -会生成血红色的配合物 ④略6、0. l0mol ∙L -1的AgNO 3溶液50mL ,加密度为0.932g ∙ mL -1含NH 3 18.24%的氨水30mL ,加水稀释到100mL ,求算这溶液中的Ag +浓度。
第八章 配位

为什么要加入NH3·NH4Cl缓冲液 维持 缓冲液,维持 为什么要加入 缓冲液 pH在10左右 在 左右 1.滴Mg2+允许最低 在10左右 滴 允许最低pH在 左右 2.滴定过程中释放 +,由缓冲溶液控制 滴定过程中释放H 由缓冲溶液控制 滴定过程中释放 pH不变 不变 3.铬黑 指示剂需在 铬黑T指示剂需在 左右,变色敏 铬黑 指示剂需在pH10左右 变色敏 左右 锐
第三节 金属离子指示剂
一.金属指示剂的变色原理 金属指示剂的变色原理 二.指示剂应具备的条件 指示剂应具备的条件 三.指示剂封闭现象与掩蔽作用 指示剂封闭现象与掩蔽作用
一.金属指示剂的变色原理 金属指示剂的变色原理
通常利用一种能与金属离子生成有色络合物的 有机染料来指示滴定过程中金属离子浓度变化 指示剂也是一种配位剂 滴定前加入指示剂(In) 也是一种配位剂,滴定前加入指示剂 指示剂也是一种配位剂 滴定前加入指示剂
常用的金属指示剂
1.铬黑 铬黑T 铬黑
pK2 = 6.3 pK3 = 11.5 2− 3− H 2 In → HIn → In
−
红 蓝 红 <6 7-11 >12 MIn 红色 红色→蓝色,能在pH7-11使用,用于直接 使用, 红色→蓝色,能在 使用 滴定, 滴定,Mg2+,Zn2+,Pb2+,Hg2+,Cd2+
2. 二甲酚橙 pH<6.3 黄 MIn- 红色 3.钙指示剂 钙指示剂 酒红→ 酒红→纯蓝 MIn In
pH>6.3 红色 只适用于pH<6 只适用于 pH 10-13 测Ca2+
第七节 应用与示例
一.直接滴定法 直接滴定法
例1 镁盐测定 Mg2+ + HIn2Mg2+ + H2Y2MgIn- + H2Y2酒红 铬黑T指示剂 铬黑 指示剂 MgIn- + H+ MgY2- + 2H+ MgY2- + H2In纯蓝
《分析化学》第八章-配位滴定法

EDTA各型体分布
2022/3/23
10
各型体浓度与溶液pH关系
❖ pH < 1 强酸性溶液 → H6Y2+ ❖ pH 2.67-6.16 → 主要H2Y2❖ pH > 10.26碱性溶液 → Y4-
2022/3/23
11
三、 EDTA与金属离子形成配 合物的特点
❖ (1)广泛配位性→五元环螯合物→稳定 ❖ (2)具6个配位原子,与金属离子多形成1:1配合物 ❖ (3)配位反应迅速 ❖ (4)大多数配合物可溶于水 ❖ (5)与无色金属离子形成的配合物无色,与有色金属
求出酸效应系数,从表中查出对应的pH, 即是最高酸度
2022/3/23
27
一、 酸度的选择
❖ 练习1
求用EDTA滴定液(0.02000mol/L)滴定 同浓度的Fe3+溶液的最低pH。lg KFeY = 25.10
解 求出酸效应系数
lg aY(H) = lg K FeY -8 = 25.10 -8 =17.10
2022/3/23
33
1.配位掩蔽法
❖ 利用配位反应降低或消除干扰 离子
例:EDTA→Zn2+,Al3+, 加入三乙醇胺掩蔽Al3+
2022/3/23
34
2.沉淀掩蔽法
❖ 加入沉淀,使干扰离子生成沉淀 而被掩蔽,从而消除干扰
例:Ca2+,Mg2+共存溶液,加入NaOH 溶从液而, 消使除pMHg>2+1干2,扰Mg2+→Mg(0H)2 ,
有酸效应
a Y(H)越大,酸效应对主反应的影响越大
aY(H)=1,〔Y〕=〔Y〕 没有酸效应。
配位化合物与配位滴定教案

第八章配位化合物与配位滴定第八章配位化合物与配位滴定第一节配位化合物一、配位化合物的定义配位化合物(简称配合物,也称络合物)是指独立存在的稳定化合物进一步结合而成的复杂化合物。
例:[Cu(NH3)4]SO4是由一个Cu2+和四个NH3分子组成的独立基团。
特点:1.在结构中都包含有中心离子和一定数目的中性分子或阴离子相结合而成的结构单元,此结构单元表现出新的特征。
2.在配位化合物中中心离子或阴离子或中性分子通过形成配位共价键而结成独立的结构单元。
配位化合物的定义:由中心离子(或原子)和一定数目的中性分子或阴离子通过形成配位共价键相结合而成的复杂结构单元称配位单元,凡是由配位单元组成的化合物称配位化合物。
若配位单元带电荷称配离子,如[Ag(CN)2]-,配离子与带相反电荷的离子组成中性配合物。
若配位单元不带电荷,则配位单元本身就是配合物,如Fe(CO)5另外,必须指出有一类叫复盐的化合物,如KCl·MgCl2·6H2O、KAl(SO4)2·12H2O无复杂离子和复杂的配位单元,不是配合物。
二、配合物的组成配合物在组成上一般包括内界和外界两部分。
中心体(离子或原子)内界配合物配体(单齿或多齿配体)外界现以[Cu(NH3)4]SO4为例说明配合物的组成。
内界外界[ Cu (NH3) 4 ]2+ SO42-中配配配外心位位位界离原体数离子子子组成:配合物的组成由外界离子、配体、中心离子(或原子)构成。
1.中心离子(或原子)也叫形成体,它位于配合物的中心,一般是金属离子,以过渡态金属离子最常见,也有中性原子或高氧化态的非金属元素。
如:Fe(CO)5中的Fe为形成体,是原子。
[PF6]-中的P是形成体,非金属元素。
作为中心离子的条件是:必须具有空的价电子轨道,可以接受配体所给予的孤对电子。
周期表中绝大多数元素可作为中心离子,常见的一些过渡元素如铁、铜、银、金、锌、汞、铂等元素的离子或原子,它们具有(n-1)d、ns、np、nd等的空的价电子轨道,都是强的形成体。
无机及分析化学第八章配位滴定法

HOOC—CH2 HOOC—CH2
H+
H+ CH2—COOH N—CH2CH2—N CH2—COOH
在水溶液中EDTA是以H6Y2+ 、 H5Y+ 、 H4Y 、 H3Y、H2Y2- 、 HY3- 、Y4-七种形式存在
17
EDTA与金属离子形成螯合物的特点
1、普遍性,几乎能与所有的金属离子形成稳定的配合物。 优点:应用广泛;缺点:选择性差 2、稳定性,螯合物具有特殊的稳定性。
15
H6Y2+ H5Y+ H4Y H3YH2Y2HY3
H+ + H+ + H+ + H+ + H+ + H+ +
H5Y+ H4Y H3YH2Y2HY3Y4-
各型体浓度取决于溶液pH值
pH < 1 强酸性溶液 → H6Y2+
pH 2.67~6.16 → 主要H2Y2-
pH > 10.26碱性溶液 → Y4-
子。过渡金属的离子最适合做中心离子(ⅢB~ⅡB):
Fe2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Ag+;也有少
数高氧化态的非金属元素离子:Si(Ⅳ)、P(Ⅴ)。
二、配体与配位ቤተ መጻሕፍቲ ባይዱ子:
配离子中,与中心离子紧密结合的中性分子或负离子叫配体。
常见配体:
N H3 、 H 2 O 、Cl 、I 、 SCN 、 S O 、en、EDTA
指示剂的封闭现象:化学计量点时不见指示剂变色 产生原因:
干扰离子: KMIn > KMY →指示剂无法改变颜色
第八章配位平衡和配位滴定法ppt课件

K f
1
(
K
a
)6
Kf越小,即生成的配合物稳定性越小;Ka越小, 即生成 的酸越弱,K就越大。
Fe3+ + 6F3OH-
[FeF6]3+
Fe(OH)3↓
既要考虑配位体的酸效应,又要考虑金属离子的水解效应。
2. 沉淀反应对配位平衡的影响
[Cu(NH3) 4]2+
Cu2+ + 4NH3 +
S2-
CuS↓
y 2.2310-7
二、配位平衡的移动
Mn+ + x L-
水解 氧化还原 沉淀
酸效应
MLx(n-x)
1. 酸度的影响 2.沉淀影响 3.氧化还原的影响
1. 酸度的影响
Fe3+ + 6F+ 6H+
[FeF6]36HF
总反应为:[FeF6]3- +6H+
Fe3+ + 6HF
K
c(Fe3 ) c6 (HF) c(Fe3 ) c6 (HF) • c6 (F- ) c([FeF6 ]3 ) c6 (H ) c([FeF6 ]3 ) c6 (H ) c6 (F- )
2. 配位体和配位原子 有孤电子对
Na[BF4]中[BF4]-是配位体, F为配位原子. a 单基配位体(一个配位体中只有一个配位原子)
含氮配位体 NH3 、 NCS-
含氧配位体 H2O 、 OH-
含卤素配位体 F- 、 CI- 、 Br- 、 I- 含碳配位体 CN- 、 CO
含硫配位体 SCN-
代入稳定常数表达式得:
Kf
c(Ag(NH3 )2 ) c(Ag )c2 (NH3 )
第八章 配位滴定法

第八章 配位滴定法一、内容提要本章讨论了以配位平衡为理论基础的配位滴定法,以及在配位平衡中常见的酸效应和配位效应;重点阐述了配位滴定中常用的指示剂,配位滴定可行性判据和提高配位滴定选择性的措施。
目前应用最多的氨酸配位剂为基础的配位滴定,其中又以乙二胺四乙酸(简称EDTA )应用最广。
EDTA 能与多种金属离子进行配位反应,所形成的配合物的稳定性可用配位反应的平衡常数,即稳定常数K MY 或K 稳来衡量。
M+Y==MY K MY = 不同的金属离子,由于其离子半径、电子层结构及电荷的差异,因而与EDTA 形成的配合物稳定性不同。
在配位反应中,除了M 与Y 之间的主反应外,还存在由H +、缓冲溶液、掩蔽剂、干扰离子等引起的副反应。
M 与Y 的主反应及其副反应的平衡关系如下: ←主反应←副反应羟基配 辅助配体 共存离子效应 酸效应 混合配位效应位效应 配位效应 (或干扰离子效应)其中由H +和其它配位体(L )所引起的副反应称为酸效应和配位效应,相应的酸效应系数和配位效应系数为:6++--L2n2n -]][[][Y M MY 12345623456345645656665432)(][][][][][][1a a a a a a a a a a a a a a a a a a a a a H Y K K K K K K H K K K K K H K K K K H K K K H K K H K H ++++++++++++=α考虑了酸效应和配位效应影响后得到的稳定常数称为条件稳定常数,它与稳定常数的关系为: 在配位滴定中,一般根据lgC M ·'MY K ≥6来判断金属离子能否准确滴定,根据准确滴定时对'MY K 的要求,可以确定滴定的最高允许酸度。
直接滴定时的最低允许酸度主要取决于金属离子的水解酸度。
对于混合金属离子的滴定,可根据具体情况采用控制酸度及加掩蔽剂等方法来达到分别滴定的目的。
配位化合物与配位确定

2019/4/7
第八章 配位化合物与配位滴定
13
8.1.2 配位化合物的命名
配合物的命名同无机化合物:阴离子在前,阳离子在后; 配阳离子 [Co(NH3)6]Br3 三溴化六氨合钴(Ⅲ) [Co(NH3)2(en)2](NO3)3 硝酸二氨· 二(乙二胺)合钴(Ⅲ) 配阴离子 K2[SiF6] 六氟合硅(Ⅳ)酸钾 配体数—配体名称—合—中心离子(罗马数字表示氧化数) 配体数用二、三等中文数字表示;配体间用圆点“·”分 开,也可省略; 配体次序:先阴离子、后中性配体;先无机、后有机配体; 阴离子次序:简单离子-复杂离子-有机酸根离子。 中性分子次序:按配位原子元素符号的英文字母顺序排列。
3.87 4.90 5.92
[Fe(CN)6]3 1.8 1 3d5
[FeF6]3
/B.M
n(未成对电子数) Fe3+的d电子构型 杂化轨道类型 配合物类型
2019/4/7
5.90 5
sp3d2 外轨型
第八章 配位化合物与配位滴定
d2sp3 内轨型
25
自由的Fe2+电子层结构:
n=4,有磁性
5
CuSO4 4NH3 [Cu(NH3 )4 ]SO4
内界配离子 外界离子
[Cu(NH3 ) 4 ]SO 4
配位数 形成体 配位体
2019/4/7
第八章 配位化合物与配位滴定
6
8.1.1 配位化合物的组成
1. 形成体——中心离子或中心原子,为具有能接受孤
电子对空轨道的原子或离子。 绝大多数为金属离子,如:
(EDTA)
11
3. 配位数
配合物 [Cu(NH3)4]2+ [Co (NH3)3Cl3] [Cu(en)2]2+
无机分析化学配位平衡

故:必须控制溶液的酸碱度在适宜的范围之内。
2.沉淀溶解平衡对配位平衡影响 一些沉淀会因形成配离子而溶解,同时有些配离子会因加 入沉淀剂而生成沉淀,这之间的转化主要决于Ksp和Kf的相对大 小,同时与沉淀剂及配位剂的浓度有关。 例如: AgCl +2NH3 = [Ag(NH3)2]+ +Cl- K=Ksp·f K
(2)一个或少数的配体分子就可以满足被滴定金属原子的 配位数。有固定的鳌合比。 其中应用最广泛的一个氨羧配位剂是:乙二胺四乙酸(EDTA)
HOOCH3C NCH2CH2N CH3COOH
HOOCH3C
CH3COOH
一、EDTA的性质
EDTA是一种四元酸,用H4Y表示
结构:在水溶液中,两个羧羟基H转移到氨基N上形成双 偶基离子,当溶液的酸度较大时,两个—COO-还可再接受两 个H,这时的EDTA就相当于一个六元酸H6Y2+。 EDTA因溶解度太小(0.02g/L水)故在配位滴定时常用其 二钠盐Na2H2Y·2H2O,简称EDTA。在酸性溶液中,EDTA存在 六级解离平衡,有H6Y2+,H5Y+,H4Y,H3Y-,H2Y2-,HY3-, Y4 - ,其中只有Y4-可以与金属离子配位。 由分布系数可知,不同的pH总对应一种主要型体,由不 同pH下EDTA的解离可看出pH>10.26以Y4-为主要型体,即pH 升高对配位有利。见下图。
第八章 配位化合物与配位滴定法
【要点】1、掌握配位化合物组成、命名化学式的写法;
2、掌握配位平衡及相关计算; 3、了解EDTA及其金属离子配合物的特点;
4、理解EDTA滴定法的原理,能够利用条件稳定常
数KMY讨论EDTA配位滴定的条件; 5、理解并掌握金属制实际的作用原理和指示剂的 选择原则; 6、理解并灵活使用提高配位滴定选择性的方法;
第八章 配位滴定法(1)

第八章配位滴定法1. 用于配位滴定的配位剂EDTA属于下列哪种配位剂()A “OO型”B “NO型”C “NN型”D “SO型”2. EDTA能与许多种金属离子进行配位反应。
在其多种存在形式中,以何种形式与金属离子形成的配合物最稳定()A H2Y2-B H3Y‾C H4YD Y4-3. 配位滴定法中配制滴定液使用的是()A EDTAB EDTA二钠盐C EDTA六元酸D EDTA负四价离子4. 有关EDTA叙述正确的是()A 在水溶液中EDTA一共有5级电离平衡B EDTA是一个二元有机弱酸C EDTA在溶液中总共有7种形式存在D EDTA不溶于碱性溶液5. 金属离子与EDTA形成稳定配合物的主要原因是()A 不分级配位B 配位比简单C 形成环状螯合物D 配合物的颜色较深6. EDTA与金属离子形成螯合物时,其螯合比一般为()A 1:1B 1:2C 1:4D 1:67. 关于稳定常数的概念错误的是()A 又称绝对稳定常数B 其倒数称为不稳定常数C 稳定常数与温度无关D 稳定常数越大,配合物越稳定8. 影响EDTA配合物稳定性的因素之一是酸效应。
酸效应是指()A 加入酸使溶液酸度增加的现象B 酸能使配位体配位能力降低的现象C 酸能使金属离子配位能力降低的现象D 酸能抑制金屑离子水解的现象9. 在下列叙述EDTA溶液中Y4-的分布系数为δ时,说法正确的是()A δ随pH增大而减小B δ随酸度减小而减小C δ随酸度减小而增大D δ与pH变化无关10. 下列叙述条件稳定常数K’MY的概念中,说法正确的是()A 随酸度减小而减小B K’MY随pH增大而减小C K’MY与pH变化无关D K’MY随酸度减小而增大11. 在EDTA配位滴定中,下列有关酸效应系数的叙述,正确的是()A 酸效应系数越小,越利于滴定B 酸效应系数越大,越利于滴定C pH越大,酸效应系数愈大D 酸度越低,酸效应系数愈大12. 浓度为1.0×10-3mol/L配位剂L滴定1.0×10-3mol/L金属离子M,设配合物ML的稳定常数为K ML=1014.0,在何种pH条件下可以准确滴定?()A pH=2.0,logαL(H)=14.0B pH=8.0,logαL(H)=3.0C pH=6.0,logαL(H)=5.5D pH=4.0,logαL(H)=10.013. EDTA滴定金属离子M时,能使滴定反应的平衡常数增加的效应是()A EDTA酸效应B M的水解反应C MY的副反应D M 的其他配位效应14. 配位滴定法的直接法终点所呈现的颜色是指()A 游离的金属指示剂的颜色B 被测金属离子与EDTA形成配合物的颜色C 游离的金属离子的颜色D 金属指示剂与被测金属离子形成配合物的颜色15. 金属指示剂一般为有机弱酸或弱碱,它具有酸碱指示剂的性质,同时它也是()A 有颜色的金属离子B 无颜色的金属离子C 金属离子的配位剂D 金属离子的氧化剂16. 用EDTA法测定自来水的硬度,已知水中含有少量Fe3+,某同学用NH3-NH4Cl调pH=9.6,选络黑T为指示剂,用EDTA标准溶液滴定,但溶液一直是红色找不到终点,其原因是()A pH太高B Fe3+封闭了指示剂C pH太低D 指示剂失效17. 配位滴定中,使用铬黑T作指示剂,用来调节溶液酸度的缓冲溶液是()A 硝酸B 盐酸C 氨-氯化铵缓冲液D 醋酸-醋酸钠缓冲液18. 用EDTA单独滴定Ca2+时,选用钙指示剂,适宜pH范围是()A pH<6B pH6~12C pH=12D pH=1019. 当溶液中有两种金属离子共存时,若要求滴定误差小于0.1%,则∆(lgcK)应大于()A 7B 4C 6D 520. 采用EDTA滴定法测定Al3+时,宜采用的滴定方式为()A 置换滴定法B 返滴定法C 直接滴定法D 间接滴定法21. EDTA测定水的总硬度时,选择适宜的指示剂为()A 钙指示剂B 铬黑TC PAND 二甲酚橙22. EDTA滴定测定Al3+时,下列金属离子标准溶液中适用于返滴定过量EDTA的是()A Mg2+B Ag2+C Ca2+D Zn2+23. 在Ca2+、Mg2+共存时,可不加掩蔽剂用 EDTA滴定Ca2+的pH条件是()A pH5B pH10C pH12D pH224. 以EDTA为滴定剂,以铬黑T为指示剂,不会出现封闭现象的离子是()A Fe3+B Mg2+C Al3+D Cu2+25. EDTA滴定Ca2+、Mg2+时,可用下列掩蔽剂掩蔽Fe3+是()A KCN或抗坏血酸B 乙酰丙酮或三乙醇胺C 乙酰丙酮或抗坏血酸D 三乙醇胺或KCN参考答案: BDBCC ACBCD ABCAC BCCCB BDCBD。
湖南理工学院2011年无机化学习题及答案第八章 配位化合物与配位滴定

第八章 配位化合物与配位滴定习题1:配位化合物部分1 无水CrCl 3和氨作用能形成两种配合物A 和B ,组成分别为CrCl 3·6NH 3和CrCl 3·5NH 3。
加入AgNO 3,A 溶液中几乎全部氯沉淀为AgCl ,而B 溶液中只有2/3的氯沉淀出来。
加入NaOH 并加热,两种溶液均无氨味。
试写出这两种配合物的化学式并命名。
解:因加入AgNO 3,A 溶液中几乎全部氯沉淀为AgCl ,可知A 中的三个Cl -全部为外界离子,B 溶液中只有2/3的氯沉淀出来,说明B 中有两个Cl -为外界,一个Cl -属内界。
加入NaOH ,两种溶液无氨味,可知氨为内界。
因此A 、B 的化学式和命名应为,A :[Cr(NH 3)6]Cl 3 三氯化六氨合铬(Ⅲ) B :[Cr(NH 3)5Cl]Cl 2 二氯化一氯五氨合铬(Ⅲ)2 指出下列配合物的中心离子、配体、配位数、配离子电荷数和配合物名称。
解:3 试用价键理论说明下列配离子的类型、空间构型和磁性。
解:(1)CoF 63-和Co(CN)63-CoF 63-为外轨型,空间构型为正八面体,顺磁性,磁矩=B μ90.4)24(4=+。
Co(CN)63-为内轨型,空间构型为正八面体,抗磁性,磁矩为零。
(2)Ni(NH 3)42+和Ni(CN)42-Ni(NH 3)42+为外轨型,正四面体型,顺磁性,磁矩=B μ83.2)22(2=+。
Ni(CN)42-为内轨型,平面正方型,抗磁性,磁矩为零。
4 将0.1mol·L -1ZnCl 2溶液与1.0 mol·L -1NH 3溶液等体积混合,求此溶液中Zn(NH 3)42+和Zn 2+的浓度。
解:等体积混合后,ZnCl 2和NH 3各自的浓度减半,生成的Zn(NH 3)42+的浓度为0.05 mol·L -1,剩余的NH 3的浓度为0.3 mol·L -1,设Zn 2+的浓度为x mol·L -1。
酸碱平衡与酸碱滴定法

第一节 酸碱理论的发展及应用
一、Arrhenius 电离理论 酸:在水中电离出H+(水合离子)的物质。 碱:在水中电离出OH-的物质。 酸和碱的一般特征: 1. 酸和碱可以发生中和反应; 2. 酸和碱可以分别使指示剂变色; 3. 酸和碱对许多化学反应有催化作用。 4. 酸碱反应的实质:H++OHH 2O
一元弱酸(碱)溶液
若酸的浓度比较小或酸极弱 Ka 小,水的离解不能忽 略,又[HA]≈CHA,且满足c/Ka≥500条件, cKa<20Kw,简化为近似公式:
[H ] cKa K w
(3)如果同时满足c/Ka≥500和cKa≥20Kw两个条件, 则可进一步简化为
[H ] cKa
这种溶剂称为质子溶剂。( 举例)
二、酸碱质子理论
三、Lewis 酸碱电子理论
酸:凡是接收电子对的物质; 如:H+、Na+、BF3等。 碱:凡是给出电子对的物质。 如:OH-、CN-、NH3、F-等。 酸碱反应不再是H+和OH-的中和,而是碱性物 质提供电子对与酸性物质生成配位共价键的反 应。 BF3 + F- → BF4- Ag+ + Cl- → AgCl
[H+]=cHA,pH=-lgcHA
强酸(碱)溶液
(2) 当c ≤ 1.0×10-8 mol· dm-3时,溶液pH 值主要由水的离解决定:
[H ] Kw
(3)当强酸或强碱的浓度较稀时, ca介于10-6 mol· dm-310-8 mol· dm-3之间时 得精确式: 1 2 [ H ] (ca ca 4 K w ) 2
( 0 ) A
[ A ] [ A ] 1 1 Ka [ H ] [ H ] Ka c [ HA] [ A ] 1 [ HA] 1 [A ] Ka
配位平衡

②多齿配(位)体:
乙二胺 (简写en) (双齿)
乙二胺四乙酸(简写EDTA)( 六齿)
1 配合物的组成
配合物
[Cu(NH3)4]SO4 [Fe(CO)5] [CoCl3(NH3)3]
配体 配位 配 形成体 配位 数 体数 氧化数 原子
NH3 CO NH3、 Clen 4 5 6 4 5 6 +2 0 +3 N C N、Cl
8.4 螯合物
2 常见的螯合剂
乙二胺 草酸
8.4 螯合物
2 常见的螯合剂
邻菲罗啉
磺基水杨酸
EDTA分子
8.4 螯合物
3 螯合物的稳定性:
螯合物的主要特性是具有较高的稳定性 螯合效应:由于螯环的形成而使配离子 稳定性显著增强的作用
8.4 螯合物
4 影响螯合物稳定性的主要因素: 螯环的大小:螯合物以五元环、六元 环最稳定 螯环的数目:中心离子相同时,螯环
0.030-2×0.010
平衡浓度/mol.L-1 c(Ag+)
0.010+2c(Ag+) 0.010-c(Ag+)
Kfo =c([Ag(NH3)2]+)/c(Ag+)· c2(NH3)
=[0.010-c(Ag+)]/c(Ag+)· [0.010+2c(Ag+)]2
2 配位平衡的计算
Ag+ + 2NH3 = [Ag(NH3)2]+ 因为Kfo 较大,说明配离子稳定,解离得到的Ag+浓度 相对较小;又因过量配体—NH3 抑制了配离子的解离,因 此可做近似处理,即平衡时: c (NH3)≈0.010mol.L-1 c([Ag(NH3)2]+)≈0.010mol.L-1
8.配位平衡和配位滴定法

习 题八一、选择题(将正确答案的序号填在括号内) 1.下列配合物中心离子的配位数有错误的是( )a.[Co(NO 2)3(NH 3)3];b.K 2[Fe(CN)5NO];c.[CoCl 2(NH 2)2(en)2];d.[Co(NH 3)4Cl 2]Cl 。
2.关于配合物,下列说法错误的是( )a.配体是一种可以给出孤对电子或π健电子的离子或分子;b.配位数是指直接同中心离子相连的配体总数;c.广义地讲,所有金属离子都可能生成配合物;d.配离子既可以存在于晶体中,也可以存在于溶液中。
3.关于外轨型与内转型配合物的区别,下列说法不正确的是( )a.外轨型配合物中配位原子的电负性比内轨型配合物中配位原子的电负性大;b.中心离子轨道杂化方式在外轨型配合物是ns 、np 、nd 轨道杂化,内轨型配合物是(n-1)d 、ns 、np 轨道杂化;c.一般外轨型配合物比内轨型配合物键能小;d.通常外轨型配合物比内轨型配合物磁矩小。
4.当下列配离子浓度及配体浓度均相等时,体系中Zn 2+离子浓度最小的是( )a.()+243NH Zn ; b.()+22en Zn ;c. ()-24CN Zn d.()-24OH Zn。
5.Fe(Ⅲ)形成配位数为6的外轨型配合物中,Fe 3+离子接受孤对电子的空轨道是( )a.d 2sp 3;b.sp 3d 2;c.p 3d 3d.sd 5 6.下列配离子能在强酸性介质中稳定存在的是( )a.()-3232O S Ag ; b.()+243NH Ni ; c.()-3342O C Fe ; d.-24HgCl 。
7.测得()+363NH Co 的磁矩µ=0.0B· M,可知Co 3+离子采取的杂化类型为( )a.d 2sp 3;b.sp 3d 2;c.sp 3 ;d.dsp 2 8.下列物质具有顺磁性的是( )a.()+23NH Ag ; b.()-46CN Fe ; c.()+243NH Cu ; d.()-24CN Zn9.下列物质中,能作为螯合剂的为( )a.HO-OH ;b.H 2N-NH 2;c.(CH 32)2N-NH 2;d.H 2N-CH 2-CH 2-NH 2。
第八章 配位化合物与配位滴定

26
4.配离子的转化
在配位反应中,一种配离子可以转化成更稳定 的配离子。
如[HgCl4]2-与I-反应生成[HgI4]2-,[Fe(NCS)6]3-
与F-反应生[FeF6]3-,其反应式如下:
[HgCl4]2- +4I-
[HgI4]2- +4Cl-
[Fe(NCS)6]3-+6F- [FeF6]3-+6SCN- 血
红色
无色
原因:Kf([HgI4]2-)> Kf (HgCl42-); Kf ([FeF6]3-)> Kf {[ Fe(NCS)63-]}
*
第八章 配位化合物与配位滴定
27
例8-3 计算反应
[Ag(NH3)2]+ + 2CN-
[Ag(CN)2]- + 2NH3
的平衡常数,并判断配位反应进行的方向。
Fe3+ + I-
Fe2+ + 1/2I2
向该系统中加入F-,Fe3+立即与F-形成了[FeF6]3-, 降低了Fe3+浓度,因而减弱了Fe3+的氧化能力,使上述 氧化还原平衡向左移动。I2又被还原成I-。
总反应: Fe3+ + 1/2I2 + 6F-
[FeF6]3-+ I-
*
第八章 配位化合物与配位滴定
32
配位性质
EDTA 有 6 个配位基
2个氨氮配位原子 4个羧氧配位原子
溶解度
型体
溶解度 (22 ºC)
H4Y
0.2 g / L
Na2H2Y 111 g / L, 0.3 mol /L
*
第八章 配位化合物与配位滴定
(完整word版)第八章配位平衡与配位滴定法.docx

第八章配位平衡与配位滴定法§8-1 配合物教学目的及要求: 1.掌握配合物及其组成。
2.掌握配合物命名。
教学重点:配合物命名。
教学难点:配合物命名。
一、配合物及其组成1.中心离子中心离子绝大多数为金属离子特别是过渡金属离子。
2.配体和配位原子配合物中同中心离子直接结合的阴离子或中性分子叫配体,配体中具有孤电子对并与中心离子形成配位键的原子称为配位原子(单基(齿)配体,多基(齿)配体)3.配位数配合物中直接同中心离子形成配位键的配位原子的总数目称为该中心离子的配位数配位数 =配位体数×齿数4.配离子的电荷数配离子的电荷等于中心离子和配体电荷的代数和。
[Cu (NH3)4 ] SO 4K 3 [Fe(CN) 6 ]↑ ↑↑ ↑↑ ↑ ↑ ↑中配配中配配心心位位离离体数体数子子内界外界外界内界配合物配合物二、配合物的命名配离子按下列序依次命名:阴离子配体→中性分子配体→“合”→中心离子(用数字明氧化数) 。
氧化数无化的中心离子可不注明氧化数。
若有几种阴离子配体,命名序是:离子→ 复离子→ 有机酸根离子;若有几种中性分子配体,命名序是:NH 3→ H 2O→有机分子。
各配体的个数用数字一、二、三⋯⋯写在种配体名称的前面。
整个配合物的命名与一般无机化合物的命名相同,称某化某、某酸某和某某酸等。
由于配离子的成复,有其特定的命名原,搞清楚配离子的名称后,再按一般无机酸、碱和的命名方法写出配合物的名称。
例: K 4[Fe(CN) 6 ]六合 ( Ⅱ) 酸H[AuCl 4]四合金 (Ⅲ )酸[CoCl 2(NH 3)3(H 2O)]Cl化二三氨一水合(Ⅲ)[PtCl(NO 2)(NH 3)4]CO 3碳酸一一硝基四氨合(Ⅳ )[Ni(CO) 4]四基合§8-2配离子的配位离解平衡教学目的及要求:1.理解配位平衡常数。
2.掌握配位平衡的移。
教学重点:1.配位平衡常数的算。
2.配位平衡的移。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章配位平衡与配位滴定法
一、选择题
1. 关于配合物,下列说法错误的是()
A. 配体是一种可以给出孤对电子或π键电子的离子或分子
B .配位数是指直接同中心离子相结合的配体总数
C. 广义地讲,所有金属离子都可能生成配合物
D. 配离子既可以存在于晶体中,也可以存在于溶液中
2. 关于外轨型与内轨型配合物的区别,下列说法不正确的是()
A. 外轨型配合物中配位原子的电负性比内轨型配合物中配位原子的电负性大
B. 中心离子轨道杂化方式在外轨型配合物是ns、np、nd轨道杂化,内轨型配合物是(n-1)d、ns、np轨道杂化
C. 一般外轨型配合物比内轨型配合物键能小
D. 通常外轨型配合物比内轨型配合物磁矩小
3. 当下列配离子浓度及配体浓度均相等时,体系中Zn2+离浓度最小的是()
A.Zn(NH3)42+ B. Zn(en)22+
C. Zn(CN)42-
D. Zn(OH)42-
4. Fe(Ⅲ)形成配位数为6的外轨型配合物中,Fe3+离子接受孤对电子的空轨道是()
A. d2sp3
B. sp3d2
C. p3d3
D. sd5
5.下列配离子能在强酸性介质中稳定存在的是()
A.Ag(S2O3)23-B.Ni(NH3)42+C.Fe(C2O4)33-D.HgCl42-
6. 测得Co(NH3)63+的磁矩μ=0B.M,可知Co3+离子采取的杂化类型为( )
A.d2sp3
B.sp3d2
C.sp3
D. dsp2
7.下列物质具有顺磁性的是()
A.Ag(NH3) +B.Fe(CN)64-C.Cu(NH3)42+D.Zn(CN)42-
8.下列物质中,能作为螯合剂的为( )
A. HO-OH
B. H2N-NH2
C. (CH3)2N-NH2
D. H2N-CH2-CH2-NH2
9. 在[RhBr2(NH3)4]+中,Rh的氧化数和配位数分别是()
A.+2和4
B.+3和6
C. +2和6
D. +3和4
10.Cu(en)22+的稳定性比Cu(NH3)42+大得多,主要原因是前者()
A. 配体比后者大
B.具有螯合效应
C. 配位数比后者小
D. en的相对分子质量比NH3大
11.下列离子中,形成配合物的能力最强的是()
A. Cu2+
B. Ca2+
C. Zn2+
D. Mg2+
12.下列配体中,配合能力最强的是()
A. NH3
B. H2O
C. Cl-
D. CN-
13.下列物质中,难溶于Na2S2O3溶液,而易溶于KCN溶液的是()
A. AgCl
B. AgI
C. AgBr
D. Ag2S
14.向含有Ag(NH3)2+配离子的溶液中分别加入下列物质时,平衡不向Ag(NH3)2 +离解方向移动的是()
A. 稀HNO3
B. NH3·H2O
C. Na2S
D. KI
15.下列各组盐溶液中加入浓氨水产生沉淀不溶解的是()
A. ZnCl2和AgCl
B. CuSO4和CoSO4
C. Mg(NO3)2和FeCl3
D. Ni(NO3)2和AgCl
16. EDTA与金属离子形成螯合物时,其螯合比一般为
A. 1:1
B. 1:2
C. 1:4
D. 1:6
17. EDTA与金属离子配位时,一分子的EDTA可提供的配位原子个数为
A. 2
B. 4
C. 6
D. 8
18. 在非缓冲溶液中用EDTA滴定金属离子时,溶液的pH将
A. 升高
B. 降低
C. 不变
D. 与金属离子价态有关
19. 下列叙述α[Y(H)]正确的是
A. α[Y(H)]随酸度减小而增大
B. α[Y(H)]随pH增大而减小
C. α[Y(H)]随酸度增大而减小
D. α[Y(H)]与pH变化无关
20. 以铬黑T为指示剂,用EDTA溶液滴定Ca2+、Mg2+总量, 可选择的缓冲溶液为
A. KHC8H4O4-HCl
B. KH2PO4-Na2HPO4
C. NH4Cl-NH3·H2O
D. NaAc-HAc
21. 用EDTA直接滴定有色金属离子,终点时所呈现的颜色是
A. 游离指示剂In的颜色
B. MY的颜色
C. MIn的颜色
D. A和B的混合颜色
22. Fe3+、Al3+对铬黑T有
A.僵化作用
B.氧化作用
C.沉淀作用
D.封闭作用
23. 在配位滴定中,用返滴定法测Al 3+时,以某金属离子标准溶液滴定过量的EDTA ,最适合的金属离子标准溶液是 ( )
A. Mg 2+
B. Zn 2+
C. Ag +
D. Bi 3+
24. 某溶液含Ca 2+、Mg 2+及少量Fe 3+、Al 3+,现加入三乙醇胺,调至pH=10,以铬黑T 为指示剂,用EDTA 滴定,此时测定的是 ( )
A. Mg 2+含量
B. Ca 2+含量
C. Ca 2+、Mg 2+总量
D. Ca 2+、Mg 2+、Fe 3+ 、Al 3+总量
25. 在配位滴定中,金属离子与EDTA 形成的配合物越稳定,K(MY)越大,在滴定时允许pH (仅考虑酸效应)
A. 越低
B. 越高
C. 中性
D. 无法确定
26. 在pH=5.0时,下列0.01 mol·L -1金属离子溶液中,可用EDTA 标准溶液直接准确滴定的是 ( )
A. Mg 2+
B. Mn 2+
C. Ca 2+
D. Zn 2+
27. Co(Ⅲ)的八面体配合物CoClm·nNH 3, 若1mol 配合物与AgNO 3作用生成1molAgCl 沉淀, 则m 和n 的值是 ( )
A. m=1, n=5
B. m=3, n=4
C. m=5, n=1
D. m=4, n=5
二、填充题
1.下列几种配离子:Ag(CN)2-、FeF 63-、Fe(CN)64-、Ni(NH 3)42+属于内轨型的是 。
2.在CuSO 4溶液中加入少量氨水,则溶液中有 色沉淀生成,若加入过量氨水,则沉淀溶解,生成 色 配离子。
3.根据下列配合物的名称,写出它们的化学式。
(1)二(硫代硫酸)合银(Ⅰ)酸钠 。
(2)二氯·一草酸根·一(乙二胺)合铁(Ⅲ) 。
(3)四氯合铂(Ⅱ)酸六氨合铂(Ⅱ) 。
(4)四(异硫氰根)·二氨合钴(Ⅲ)酸铵 。
4.根据Kj θ值,判断标态时下列反应进行的方向。
(1) 2--244[HgCl ] + 4I []4j HgI Cl K θ--
+= (2) 22223434()()j
C u N H Z n Z n N H C u K θ++++++=
5. 在无色溶液A中加入NaCl溶液得到白色沉淀B;B沉淀加氨水得溶液C;C 中加入KBr溶液得淡黄色沉淀D;D溶于Na2S2O3溶液得溶液E; D溶于KCN溶
6. [CoCl2(en)2]的名称是,中心离子是,配体是,配位数是。
7. 在含有酒石酸和KCN的氨性溶液中,用EDTA滴定Pb2+、Zn2+混合溶液中的Pb2+,加入KCN的作用是。
8. Ni(NH3)42+具有顺磁性,则它的几何构型为,杂化类型为;Ni(CN)42-具有反磁性,则它的几何构型为,杂化类型为。
