微生物测定原始记录
微生物检测原始记录文本

XXXX检测有限公司
菌落总数与大肠菌群检验原始记录
共页第页主检:
菌落总数和大肠菌群检测原始记录
共页第页
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页主检:
XXXX检测有限公司
致病菌检验原始记录
共页第页
XXXX 检测有限公司 主检:
年 月 日 校核:
主检: 年 月 日 校核: 年 月 日
XXXX 检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
商业无菌检验原始记录
共页第页
XXXX检测有限公司
主检日期校核日期。
微生物原始记录(消毒效果监测)

微生物检验原始记录受理编号:检(20 )号第页/共页检验依据卫生部《消毒技术规范》2002版一、实验器材1.试验菌株:大肠杆菌,菌株号:1022,培养代数代,营养琼脂斜面培养基培养,培养条件:2.试剂及培养基配制、灭菌见《试剂及培养基配制记录C》:第1次;第2次;第3次。
3.恒温培养箱(36±1°C):编号 SCCDC 。
4. 载体:玻片(10mm×10mm).5.样品名称:,批号:。
二、试验方法1.试验步骤:按《消毒技术规范》2002版2.1.5.2红外线消毒碗柜和2.1.5.7臭氧消毒柜消毒效果监测方法进行。
2.培养条件受理编号:检()号第页/共页三、结果阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/片。
对数值:阴性对照:菌生长。
阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/片。
对数值:阴性对照:菌生长。
阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/片。
对数值:阴性对照:菌生长。
受理编号:检()号第页/共页四. 结果处理:三次试验平均结果阳性对照:菌液浓度: cfu/片。
对数值:阴性对照:菌生长。
五.计算公式:(1)接种稀释倍数=V×A×B=5.0×A×1.0=5A式中V为PBS体积(5ml);A为接种前中和管液体稀释倍数;B接种样液体积。
(2)试验组菌片菌数或阳性对照菌片菌数=平皿生长平均菌数×接种稀释倍数(3)杀灭对数值=lg(阳性对照菌片菌数)-lg(试验组菌片菌数)(以下空白)检验者:复核者:。
微生物检验原始记录
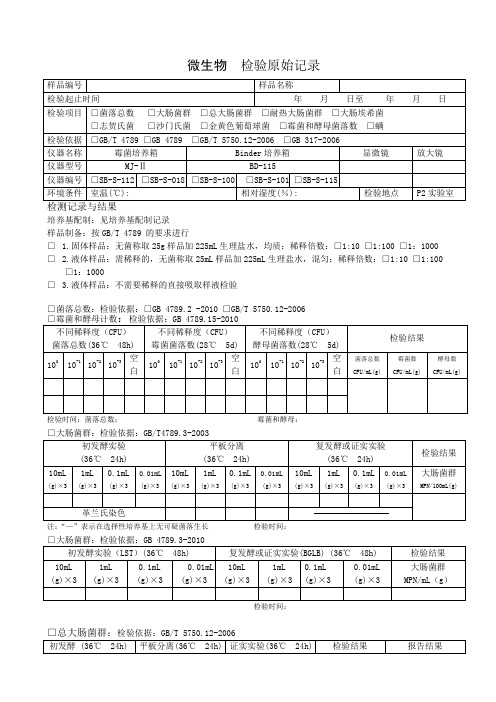
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠菌群:检验依据:GB 4789.3-2010
检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:。
公共场所空气微生物检验原始记录

公共场所空气微生物检验原始记录日期:XXXX年XX月XX日地点:XXXX公共场所(如:商场/学校/医院等)检验目的:本次检验旨在对XXXX公共场所的空气中微生物进行检测,以评估其空气质量和卫生状况。
检验方法:1.采样器选择:使用一次性采样器进行操作,以避免交叉感染和污染。
2.采样时间:每次采样时间为15分钟,分为两个时间段,分别为上午XX时XX分至上午XX时XX分和下午XX时XX分至下午XX时XX分。
3.采样位置:根据公共场所的不同区域,选取代表性的区域进行采样。
包括但不限于入口处、办公区、卫生间、通道等区域。
4. 采样方法:将采样器放置在距离地面1.5米的位置,打开采样器电源并调整合适的流量(通常为1.0L/min),进行采样。
5.采样器编号:每个采样位置的采样器都标有唯一的编号,以避免混淆。
检验结果:上午采样结果:位置1(入口处):XXXCFU/m^3位置2(办公区):XXXCFU/m^3位置3(卫生间):XXXCFU/m^3位置4(通道):XXXCFU/m^3下午采样结果:位置1(入口处):XXXCFU/m^3位置2(办公区):XXXCFU/m^3位置3(卫生间):XXXCFU/m^3位置4(通道):XXXCFU/m^3结论与建议:1.根据检测结果,XXXX公共场所的空气中微生物的总数超出了标准范围,表明空气质量较差。
2.位置X(如:卫生间)的微生物数目明显高于其他位置,建议加强该区域的清洁和消毒工作。
3.建议在公共场所增加通风设施,以提高空气流通和减少微生物滋生的可能性。
4.对于公共场所,尤其是人员流通频繁的区域,定期进行微生物检测,并根据检测结果进行相应的清洁和卫生措施。
注意事项:1.检验前,确保采样器的清洁和消毒,以避免外部污染对结果的影响。
2.检验时,避免对采样器进行过度触摸,以防手部细菌污染采样器。
检验人员签名:____________________。
医疗机构污水微生物检测原始记录表
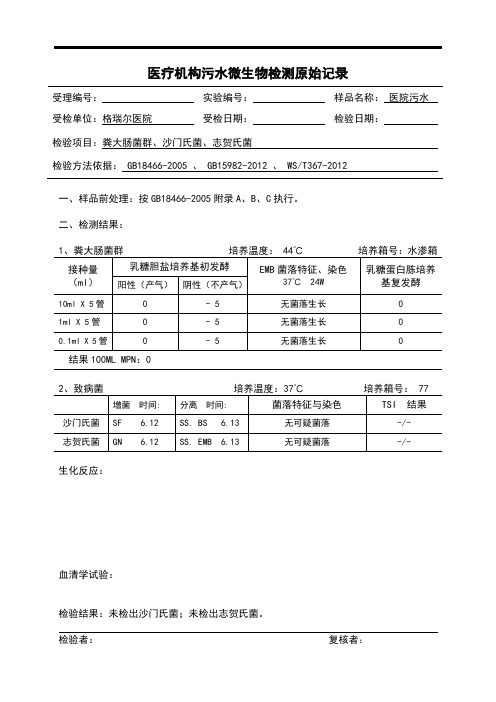
受理编号:
实验编号:
样品名称:医院污水
受检单位:格瑞尔医院
受检日期:
检验日期:
检验项目:粪大肠菌群、沙门氏菌、志贺氏菌
检验方法依据:GB18466-2005 、 GB15982-2012 、 WS/T367-2012
一、样品前处理:按GB18466-2005附录A、B、C执行。
二、检测结果:
1、粪大肠菌群 培养温度: 44℃ 培养箱号:水渗箱Байду номын сангаас
接种量
(ml)
乳糖胆盐培养基初发酵
EMB菌落特征、染色
37℃ 24W
乳糖蛋白胨培养基复发酵
阳性(产气)
阴性(不产气)
10ml X 5管
0
- 5
无菌落生长
0
1ml X 5管
0
- 5
无菌落生长
0
0.1ml X 5管
0
- 5
无菌落生长
0
结果100ML MPN:0
2、致病菌 培养温度:37℃ 培养箱号: 77
增菌 时间:
分离 时间:
菌落特征与染色
TSI 结果
沙门氏菌
SF 6.12
SS. BS 6.13
无可疑菌落
-/-
志贺氏菌
GN 6.12
SS. EMB 6.13
无可疑菌落
-/-
生化反应:
血清学试验:
检验结果:未检出沙门氏菌;未检出志贺氏菌。
检验者: 复核者:
微生物检测原始记录

微生物检测原始记录一、目的本文档旨在规定微生物检测的原始记录格式和内容,以确保检测过程和结果的准确性和可追溯性。
二、记录格式1、记录纸张:使用A4纸,横向排列,页边距至少留有2cm。
2、记录标题:在页面顶部居中书写“微生物检测原始记录”。
3、日期和实验室名称:在页面右下角书写检测日期和实验室名称。
4、检测样品信息:在页面中部或适当位置填写样品信息,包括样品名称、编号、来源、处理方式等。
5、检测项目和指标:在页面中部或适当位置列出检测项目和指标,如菌落总数、大肠杆菌、沙门氏菌等。
6、检测方法和仪器:在页面中部或适当位置描述检测所采用的方法和使用的仪器设备。
7、检测结果记录:在页面中部或适当位置详细记录每个检测项目的实验数据,并确保数据准确、清晰、可追溯。
8、结论和建议:在页面底部或适当位置总结检测结果,并给出相应建议或处理意见。
9、检测人员签名:在页面右下角或适当位置由检测人员签名,以示负责。
10、备注:根据需要添加其他相关信息,如样品异常情况说明、引用标准、注意事项等。
三、记录内容1、样品信息:样品名称、编号、来源(如生产批次、产地等)、处理方式(如取样、前处理等)。
2、检测项目和指标:根据实际需要确定检测项目和指标,如菌落总数、大肠杆菌、沙门氏菌等微生物指标,以及可能的化学指标等。
3、检测方法:描述微生物检测所采用的方法,如国标法、第三方检测方法等。
同时应注明所用方法的版本号和发布机构。
4、仪器设备:列出在检测过程中使用的所有仪器设备的名称、型号、编号和使用状态等信息。
5、实验数据记录:详细记录每个检测项目的实验数据,包括观察结果、计数结果、吸光度值等。
数据应准确、清晰、可追溯,并附上必要的图表和曲线图。
6、结论和建议:根据检测结果给出相应的结论和建议,如是否符合标准要求,是否需要进一步处理或跟进等。
7、其他信息:根据需要添加其他相关信息,如样品异常情况说明、引用标准、注意事项等。
8、检测人员签名:由检测人员签名,以示负责。
微生物检验原始记录

⑴菌落总数(平板计数琼脂36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑵霉菌、酵母菌计数(孟加拉虎红27±1℃5d)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
微生物检验原始记录
NO:
品名:包装规格:
批号:数量:
生产车间:检品数量:
检验人员:复核人员:
检验依据:检验目的:
检验日期:报告日期:
检验记录与结果:
1.取样:
(1)原液取样
(2)无菌称取样品25g或者25ml,置225ml灭菌的0.85%的生理盐水中,充分混匀,制成1:10稀释液。取1:10稀释液1ml置9ml灭菌的0.9%生理盐水中,制成1:100稀释液。
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑶大肠杆菌(月桂基磺酸盐胰蛋白胨【LST】肉汤,36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:10稀释液(10ml)双料
1:100稀释液(1ml)
阴性对照
阳性对照
结果:MPN/mL
1
均值:
2
微生物检验原始记录
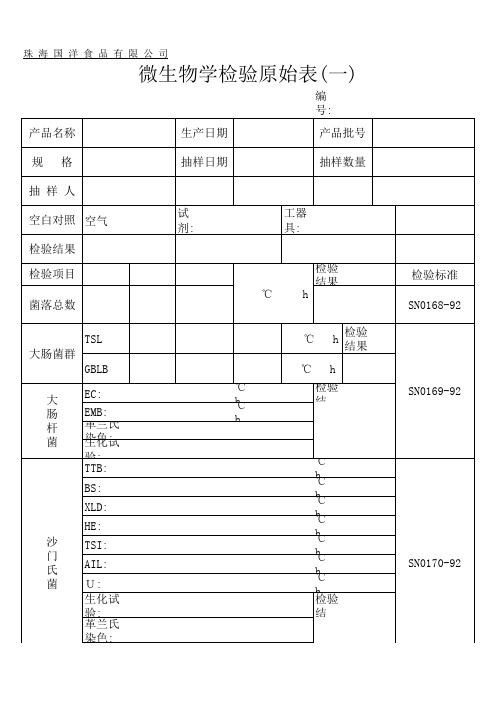
染色:
TCBS: 无盐胰
胨水: 副 30g/L: 溶 NaCl三 性 糖革铁兰琼氏 弧 染色: 菌 70g/L:
100g/L: 生化试
验: TCBS:
T1N1: 氧酶试
验:
霍 TSI:
乱 弧
KIA:
菌 AGS:
T1N0:
T1N3: 生化试 验:
寄生虫
℃ h
℃ h℃ h
粘丝试 验:
℃ h℃ h
编 号: ℃ h ℃ h ℃ h 检验 结
℃ h℃ h℃ h℃ h
检验 结
℃ h℃ h
℃ h℃ h℃ h检验 结
检验 结
SN0172-92 SN0173-92 SNT1022-2001 93/140/EEC
检验日期: 检 验 员:
验讫 日审 核:
报告 日 复 核:
珠海国洋食品有限公司
微生物学检验原始表(一)
编 号:
产品名称
生产日期
产品批号
规格
抽样日期
抽样数量
抽样人 空白对照 空气 检验结果 检验项目 菌落总数
试
工器剂:具:来自检验结果℃
h
TSL 大肠菌群
GBLB
大 EC: 肠 EMB: 杆 革兰氏 菌 染生色化:试
验: TTB:
BS:
XLD:
HE: 沙 TSI: 门 氏 AIL: 菌 U:
生化试 验: 革兰氏 染色:
℃
h
检验 结果
℃h
℃
检验
h℃
结
h
℃ h℃ h℃ h℃ h℃ h℃ h℃ h检验 结
检验标准 SN0168-92 SN0169-92
SN0170-92
血清学 试验:
微生物检测原始记录
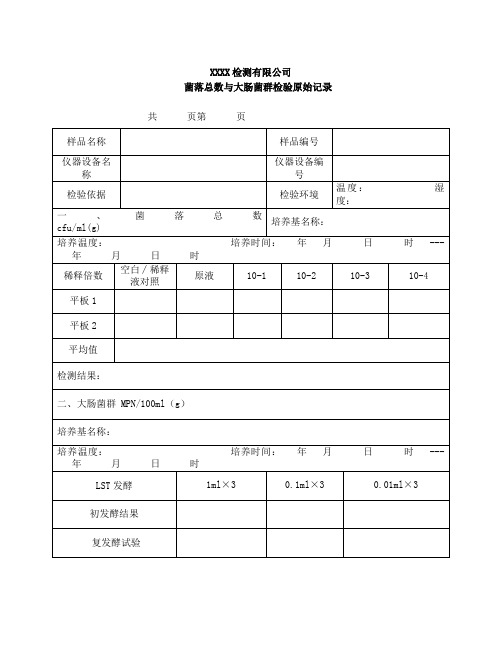
XXXX检测有限公司
菌落总数与大肠菌群检验原始记录共页第页
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
共页
第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
致病菌检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共页第页
培养温度:28±1℃培养时间:年月日时 ---年月日时:
菌落计数:
培养温度:28±1℃培养时间:年月日时 --- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
饲料微生物检验原始记录

饲料微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:检测依据:一、菌落总数、霉菌总数以无菌操作称(量)取样品25g(或10g),加入225ml(或90ml)的无菌生理盐水中,均质后,做成1∶10样品液。
取1∶10稀释液1ml加入到9ml生理盐水中,混匀,做成1∶100样品均液。
以上法制备10倍系列稀释样品均液。
选择2-3个适宜稀释度的样品均液,吸取1ml样品均液于无菌平皿内,每个稀释度做2个平皿。
同时,分别吸取1ml空白稀释液加入两个无菌平皿内作空白对照,及时将15-20ml 冷至46℃的营养琼脂培养基倾注平皿,转动平皿使其混合均匀,凝固后,可在培养基表面倾注冷至46℃的水琼脂培养基4ml, 凝固后翻转平板,置 30±1℃培养小时,计数平板上菌落数(CFU)。
霉菌计算及结果:细菌菌落数(CFU/g,ml):霉菌菌落数(CFU/g,ml):二、大肠菌群测定:按菌落总数测定方法制备lO0、10-1、10-2、10-3、10-4……稀释液。
选择3个适宜的连续稀释度的样品均液,每个稀释度接种3管乳糖胆盐发酵管,每管接种1ml(接种量超过1ml,则用双料乳糖胆盐发酵管),36±1℃培养24±2h,观察倒管内是否有气泡产生,对于24±2h产气者,用接种环从产气的乳糖胆盐发酵管中分别取培养物一环,分别转种到在伊红美蓝琼脂平板上,36±1℃培养18h~24h,观察菌落形态,并做确证实验。
如果所有乳糖胆盐发酵管都不产气,则可报告为大肠菌群阴性。
注:○+产酸产气;+产酸不产气或有可疑菌落;-不产酸不产气或无可疑菌落;G-b革兰氏阴性杆菌;G+b革兰氏阳性杆菌;G+c革兰氏阳性球菌。
结果:根据证实为总大肠菌群阳性的管数,查MPN检索表,得 MPN/100g(mL)。
电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:三、产气荚膜梭菌以无菌操作称取样品25g(ml)加入225ml蛋白胨生理盐水稀释液,均质后,做成1∶10稀释液。
纸尿裤微生物原始记录
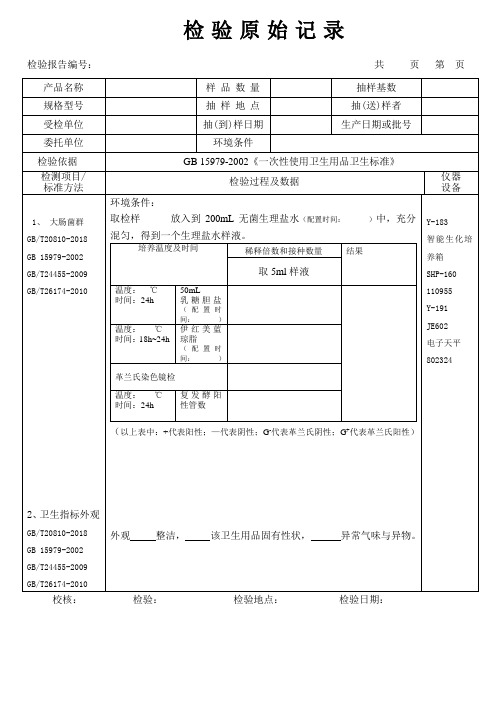
检验报告编号:共页第页
产品名称
样品数量
抽样基数
规格型号
抽样地点
抽(送)样者
受检单位
抽(到)样日期
生产日期或批号
委托单位
环境条件
检验依据
GB 15979-2002《一次性使用卫生用品卫生标准》
检测项目/
标准方法
检验过程及数据
仪器
设备
1、 大肠菌群
GB/T20810-2018
GB 15979-2002
Y-191
JE602
电子天平
802324
Y-183
智能生化培养箱
SHP-160110955
Y-191
JE602
电子天平802324
Y-183
智能生化培养箱
SHP-160110955
Y-191
JE602
电子天平802324
校核:检验:检验地点:检验日期:
检验报告编号:共页第页
检测项目/标准方法
检验过程及检验数据
仪器设备
1、 绿脓杆菌
GB 15979-2002
GB/T26174-2010
2、 真菌菌落总数
GB 15979-2002
GB/T26174-2010
环境条件:
取检样放入到200mL无菌生理盐水(配置时间:)中,充分混匀,得到一个生理盐水样液。
检样5ml +50mlSCDLP培养液(配置时间:)
( ℃ 培养24h)
智能生化培养箱
SHP-160
110955
Y-191
JE602
电子天平
802324
校核:检验:检验地点:检验日期:
检验报告编号:共页第页
微生物检验原始记录范本
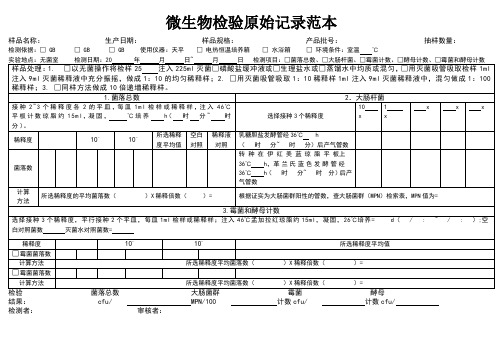
所选稀释度的平均菌落数( )X稀释倍数( )=
根据证实为大肠菌群阳性的管数,查大肠菌群(MPN)检索表,MPN值为=
3.霉菌和酵母计数
选择接种3个稀释度,平行接种2个平皿,每皿1ml检样或稀释样;注入46℃孟加拉红琼脂约15ml,凝固,26℃培养=d( / :~/ : );空白对照菌数灭菌水对照菌数=
微生物检验原始记录范本
样品名称:生产日期:样品规格:产品批号:抽样数量:
检测依据:□ GB□GB□GB使用仪器:天平□ 电热恒温培养箱 □ 水浴箱 □ 环境条件:室温℃
实验地点:无菌室检测日期:20年月日~月日检测项目:□菌落总数、□大肠杆菌、□霉菌计数、□酵母计数、□霉菌和酵母计数
样品处理:1.□以无菌操作将检样25注入225ml灭菌□磷酸盐缓冲液或□生理盐水或□蒸馏水中均质或混匀,□用灭菌吸管吸取检样1ml注入9ml灭菌稀释液中充分振摇,做成1:10的均匀稀释样;2. □用灭菌吸管吸取1:10稀释样1ml注入9ml灭菌稀释液中,混匀做成1:100稀释样;3. □同样方法做成10倍递增稀释样。
1.菌落总数
2.大肠杆菌
接种2~3个稀释度各2的平皿,每皿1ml检样或稀释样,注入46℃平板计数琼脂约15ml,凝固,℃培养h(时分~时分)。
选择接种3个稀释度
10
x
1
x
x
x
x
稀释度
10-
10-
所选稀释度平均值
空白对照
稀释液对照
乳糖胆盐发酵管经36℃h
(时 分~时分)后产气管数
菌落数
转 种 在 伊 红 美 蓝 琼 脂 平 板上36℃h,革兰氏蓝色发酵管经36℃h(时分~时 分)后产气管数
稀释度
10-
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ቤተ መጻሕፍቲ ባይዱ第一次
第二次
备注:将混合均匀的试样迅速研细至颗粒小于2nm,称取2g-10g试样(精确至0.0001g),放入称量瓶中,试样厚度不超过5mm。
检验员:日期:审核:
样品数
菌落总数
大肠菌群
10-1
10-2
10-3
空白
菌落总数(cfu/g)
结果判定
10-1
10-2
10-3
空白
大肠菌群(cfu/g)
结果判定
1
2
3
4
5
大肠菌群复发酵实验
BGLB管
10-1
10-2
10-3
空白
结果
水分:(检验标准:GB5009.3-2010)
称量瓶重g
烘瓶起始时间
烘瓶结束置于干燥器冷却时间
微生物检测原始记录
产品名称:批号:生产日期:检验日期:
检验项目
操作过程
菌落总数(检验标准GB4789.2-2010)
大肠菌群(检验标准GB4789.3-2010)
步骤
培养过程记录
从月日时至月日时,放至36℃±1℃培养箱内培养48h±2h。
从月日时至月日时,放置36℃±1℃培养箱内培养24h±2h
项目
冷却时间
称重g
是否恒重
瓶:
第一次
第二次
备注:烘瓶条件:101-105℃烘箱中,瓶盖斜放于瓶边,加热1h,取出改好,置于干燥器内冷却0.5h,称重,并重复干燥至前后两次,质量差不超过2mg,概为恒重。
称量瓶+样品重g
烘(瓶+样)起始时间
烘(瓶+样)结束置于干燥器冷却时间
冷却时间
称重g
是否恒重
水分含量(%)
