水体中溶解性磷酸盐测定
水中总磷的测定

实验步骤
1、预处理 (1)水样 取适量的进水和出水于50mL具塞比色管+蒸馏水于25mL 50mL具塞比色管 取适量的进水和出水于50mL具塞比色管+蒸馏水于25mL 标线+4mLK2S2O8加塞后管口包一小块双层纱布并用线扎紧, 标线+ 加塞后管口包一小块双层纱布并用线扎紧, 置于高压蒸汽消毒器中消解 (2)标准曲线 取七支50mL具塞比色管,分别加入磷酸盐标准使用液0 50mL具塞比色管 取七支50mL具塞比色管,分别加入磷酸盐标准使用液0、 0.50、1.00、3.00、5.00、10.0、15.0mL,加蒸馏水至25ml 0.50、1.00、3.00、5.00、10.0、15.0mL,加蒸馏水至25ml 加塞捆纱布后, +4mLK2S2O8 ,加塞捆纱布后,同样放在高压蒸汽消毒器中消 解
A
AX
mX
SinoSino-Dutch Demonstration Researcher and Training Centre for Water Treatment
m
数据处理
C(PO43-,mg/L)= mx / V mx— 由校准曲线查得的磷含量(ug) 由校准曲线查得的磷含量(ug) V — 水样体积(mL) 水样体积(mL)
SinoSino-Dutch Demonstration Researcher and Training Centre for Water Treatment
六、思考题
1、过硫酸钾消解的作用? 过硫酸钾消解的作用? 2、用分光光度计测吸光度时,如果比色皿中有气 用分光光度计测吸光度时, 泡对结果有什么影响? 泡对结果有什么影响?
SinoSino-Dutch Demonstration Researcher and Training Centre for Water Treatment
水质总磷的测定

水质总磷的测定水质总磷是水体中一种重要的污染物,也是水体的一种重要的指示物之一。
对总磷的测定对于人们了解水体的质量和特性有重要意义。
总磷是指水体中溶解和悬浮态磷化物总和,其包括聚磷酸酯、磷酸盐、磷酸根离子等。
总磷的测定主要包括分光光度法、比色法和化学发光法等。
分光光度法是一种常用的总磷测定方法,它采用分光光度计和适当的滴定液对水样中的总磷进行测定。
分光光度法是以磷酸根根离子作为检出元,将其配制为色素探针,然后用分光光度计对样品的吸光度进行测定,从而计算出样品中的总磷含量。
比色法也是一种常用的总磷测定方法,它利用比色杯中的比色剂和含有磷酸根根离子的样品对总磷进行测定。
该方法是添加比色剂,当比色剂与样品反应时,比色剂中的磷酸根离子会被磷酸根离子所取代,使样品的吸光度发生变化,从而将吸光度变化与样品中的总磷含量建立起一一对应的关系,从而确定水样中的总磷含量。
化学发光法是一种近年来发展起来的总磷测定方法,它利用激发器对水体中的总磷物质进行激发,从而产生磷光,并将磷光的强度与样品中的总磷含量建立起一一对应的关系。
该方法具有易于操作、灵敏度高、精确度高等优点,可以很好地代替其它总磷测定方法。
自20世纪80年代以来,随着科技发展和环境污染的加剧,对水质中总磷的测定变得更加重要。
目前,总磷测定过程涉及到诸多技术,其操作步骤较为复杂,必须建立准确的技术程序才能得到准确的测定结果,这是不可忽视的,因此,总磷测定的准确性尤为重要。
总磷的测定方法有很多,但各种方法都有一定的局限性,比如,分光光度法时受干扰系数影响,容易产生偏差;比色法灵敏度低,不适合对低浓度的总磷进行测定;化学发光法仪器较贵,检测时间较长。
因此,总磷的测定应根据具体情况,选择最适宜的方法以保证测定结果的准确性。
综上所述,总磷是水体中重要的污染物,对总磷的测定对于人们了解水体的质量和特性有重要意义。
目前,总磷的测定主要采用分光光度法、比色法和化学发光法等,但由于各种方法都存在一定的局限性,因此总磷的测定应根据具体情况,选择最适宜的方法以保证测定结果的准确性。
水中溶解性总固体的检测方法对比研究

水中溶解性总固体的检测方法对比研究关键词:溶解性总固体,对比分析1引言溶解性总固体(Total Dissolved Solids,TDS),又称总矿化度,指溶解在水中的固体的总量,是表征水体矿化程度的重要指标。
水体中溶解的硝酸盐、氯化物、磷酸盐等物质,会对设备产生腐蚀、结垢等影响,因而是生活饮用水及其水源水中最常见也是最重要的检测项目之一[1]。
目前,测定水中溶解性总固体的国标方法是GB/T 5750.4-2006《生活饮用水标准检验方法感官性状和物理指标》中的称量法:将过滤后的水样经水浴蒸汽蒸干后于烘箱中烘一定时长,恒重后根据蒸发皿前后质量差计算水样中溶解性总固体的浓度,该法原理简单,但操作费时、过程繁琐,在水浴过程中,水样长期暴露于空气中,易吸附空气中的灰尘等杂质[2],并且水浴锅孔有限,不适用大批量样品分析。
另外,电导率法也可以直接测定生活饮用水中的溶解性总固体,其原理是利用水样中的阴、阳离子在电场作用下产生的电流来测定溶解性总固体的含量,此方法无需任何前处理、测量速度快、成本低,适合大批量样品分析,但因水样中各离子成分比较复杂,不同离子的导电性能存在差异,导致测量结果存在误差[3]。
国标法规定了105℃和180℃均可测定溶解性总固体,考虑到不同水体的复杂程度各不相同,本实验采用蒸汽法(国标法)、直接水浴法、直接烘干法和电热板法对四种水(自来水、市售商品水、包装饮用水、企业中水)中的溶解性总固体于180℃条件下进行分析,将测定结果与国标法进行对比,并对其测量结果的相对标准偏差、实验用时进行统计分析。
2 实验材料与方法步骤2.1 实验材料电子天平(德国塞多利斯CP225D);电热鼓风干燥箱(北京科伟永兴仪器有限公司G2-06);电热恒温水浴锅(北京科伟永兴仪器有限公司);可调式电热板(北京科伟永兴仪器有限公司180514G9754);100mL蒸发皿;干燥器;碳酸钠(分析纯)2.2实验方法2.2.1 蒸汽法(国标法)将洁净的蒸发皿于烘箱中180℃烘30min,取出,于干燥器内冷却30min后,于分析天平上称量,再次烘烤、称量,直至恒定质量(两次称量相差不超过0.0004g)。
水质中磷酸盐测定的误差分析

水质中磷酸盐测定的误差分析摘要:在自然水体及污水中,磷主要是以磷酸盐的形态存在与于水质中,主要包括正磷酸盐、缩合磷酸盐以及有机结合磷酸盐。
在自然水体中,磷酸盐的含量并不高。
化肥和化学工业产生的工业废水和生活污水中含有大量的磷。
若水中磷的含量过高,则会引起藻类的过度繁殖,若浓度达到一定程度,则形成富氧化,会引起湖泊、河流、海水的透明度下降,水质恶化,对海洋环境造成破坏。
在水质环境质量评价中,磷是一项非常重要的指标。
总磷含量的测定在锅炉用水、冷却水和污水的运行和排放监控中起着非常重要的作用。
关键字:总磷;磷酸盐;标准曲线;水处理锅炉水、冷却水中的磷,一般根据磷的赋存状态,主要是测定总磷、溶解全磷、溶解正磷。
总磷是通过消化(一般采用过硫酸钾消化方法)转变为正磷酸盐的水样品;可溶性全磷是将水样品经0.45微米滤膜过滤后,经消化后转变成正态全磷的结果;可溶磷酸根是通过滤膜直接过滤后得到的可溶磷酸根。
可以看出,无论测定何种形态的磷,正磷酸盐的测定都是磷测定的最后指标,其测定方法主要是离子色谱法和钼酸铵分光光度法。
1磷酸盐测定的误差来源在各种测量方法中,误差是不可避免的,一般可分为系统性误差、偶发误差和错误误差。
通常情况下,由于仪器的不稳定,测试环境的改变,以及操作者的习惯等原因而引起的系统误差,可以通过对仪器进行修正,对环境条件进行控制,并纠正不良的习惯来加以消除。
随机误差通常是一种不确定的、不易控制的误差。
但是,如果使用相同精度的仪器,在相同的情况下,如果测量的次数达到一定的数量,就会发现,偶然误差是符合统计学的,它的算术平均值会逐步趋近于零。
因此,从理论上来说,可以采用多个测量的平均法来降低偶然性的误差。
另一种错误是过失错误,它完全是由人的原因引起的,例如,工作态度粗心,操作马马虎虎,过度疲劳等不良状态因素引起的。
克服错误错误的措施包括:增强操作人员的责任心、完善操作规程、强化数据审计等。
为确保分析结果的准确、准确,使分析结果的误差降到最低,已成为分析工作的首要任务。
总磷的测定(钼锑抗分光光度法)解读

六、思考题
1、过硫酸钾消解的作用? 2、用分光光度计测吸光度时,如果比色皿中有气 泡对结果有什么影响?
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
总磷的测定
(钼锑抗分光光度法 )
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
实验目的
1、了解磷(总磷、溶解性正磷酸盐和溶解性总磷) 的测定方法
2、掌握分光光度计的使用、标准曲线的绘制及计 算方法
A
AX
mX
m
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
数据处理
C(PO43-,mg/L)= mx / V mx— 由校准曲线查得的磷含量(ug) V — 水样体积(mL)
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
蓝色络合物(磷钼蓝)
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
1、预处理
实验步骤
(1)水样
取适量的进水和出水于50mL具塞比色管+蒸馏水于25mL 标线+4mLK2S2O8加塞后管口包一小块双层纱布并用线扎紧, 置于高压蒸汽消毒器中消解
Sino-Dutch Demonstration Researcher and Training Centre for Water Treatment
城市污水中磷(总磷、溶解性磷酸盐和溶解性总磷)的测定方法

量过高(如0.2mg/L超过),可造成藻类的过度繁殖,甚至数量上达到有害的程
度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。磷是评价水质的
重要指标。
1、方法选择
水中磷的测定Leabharlann 通常按其存在形式而分别测定总磷、溶解性正磷酸盐和总
城市污水中磷(总磷、溶解性磷酸盐和溶解性总磷)的测定方法
城市污水中磷(总磷、溶解性磷酸盐和溶解性总磷)
测定方法
在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,他们分为正磷酸
盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷(如磷脂
等),它们存在于溶液中,腐殖质粒子中或者水生生物中。
普通天然水中磷酸盐含量不高。化肥、冶炼、合成洗涤剂等行业的工业废
溶解性磷,如图所示。
正磷酸盐的测定可采用离子色谱法、钼锑抗光度法、氧化亚锡还原钼蓝法
(灵敏度较低,干扰较多),而孔雀绿–磷钼杂多酸法灵敏度较高,且容易普及
的方法。罗丹明6G荧光分光光度法灵敏度最高。
2、样品的采集与保存
总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。溶解性正磷酸盐
的测定,不加任何保存剂,于2~50C冷处保存,在24h内进行分析。
(一)水样的预处理
采集的水样即将经0.45µm微孔滤膜过滤,其滤液供可溶性正磷酸盐的测定。
磷(总磷、溶解性磷酸盐和溶解性总磷)

七、磷(总磷、溶解性磷酸盐和溶解性总磷)在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,它们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷(如磷脂等),它们存在与溶液中,腐殖质粒子中或水生生物中。
一般天然水中磷酸盐含量不高。
化肥、冶炼、合成洗涤剂等行业的工业废水及生活污水中常含有较大量磷。
磷是生物生长必需的元素之一。
但水体中磷含量过高(如超过0.2mg/L),可造成藻类的过度繁殖,直至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
磷是评价水质的重要指标。
1.方法选择水中磷的测定,通常按其存在的形式而分别测定总磷、溶解性磷酸盐和总溶解性磷,如图3-3-5所示。
正磷酸盐的测定可采用离子色谱法、钼锑抗光度法、氯化亚锡还原钼蓝法(灵敏度较低,干扰也较多),而孔雀绿-磷钼杂多酸法是灵敏度较高,且容易普及的方法。
罗丹明6G(Rh6G)荧光分光光度法灵敏度最高。
2.样品的采集与保存总磷的测定,于水样采集后,加硫酸酸化至pH≤1保存。
溶解性正磷酸盐的测定,不加任何保存剂,与2~5℃冷处保存,在24h内进行分析。
(一)水样的预处理采集的水样立即经0.45μm微孔滤膜过滤,其滤液供可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测得可溶性总磷。
混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
过硫酸钾消解法1.仪器①医用手提式高压蒸汽消毒器或一般民用压力锅,1~1.5kg/cm2。
②电炉2kW。
③调压器,2kV A,0~220V。
④50ml(磨口)具塞刻度管。
2.试剂5%过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100ml。
3.步骤①吸取25.0ml混匀水样(必要时,酌情少取水样,并加水至25ml,使含磷量不超过30μg)于50ml具塞刻度管中,加过硫酸钾溶液4ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
实验七、活性磷的测定

实验七、活性磷的测定
研究性试验 以SnCl2还原法测定活性磷时,钼蓝化合物的颜 色强度受盐度的影响较大,以至于用纯水制作的工 作曲线计算结果时,形成一定的误差。 若用纯水和浓度为25%的NaCl溶液进行盐度调 节、以自然海水和淡水的含盐量(或离子含量)作 为盐度调节考虑的上、下限,请设计不同的盐度剃 度,利用SnCl2还原测定法,求出不同盐度下相应的 盐误差校正系数。
实验八、水中铁的测定
原理
亚铁离子(Fe2+)在pH为3~9的水溶液中,可与 邻菲啰啉生成极稳定的血红色的螯合阳离子,其最大 吸收波长在508nm附近。测总铁时,需要用盐酸羟胺 将Fe3+离子还原成Fe2+离子后,才能显色。不加盐酸 羟胺,被测定的只是亚铁离子。在用盐酸羟胺还原的 情况下,用本法测定的实际上是水中的Fe3+、Fe2+及 在该pH条件下能参与反应的胶态铁和配位铁离子。 以1cm比色皿测定时,最低检出限为0.03 mg/L ,线 性浓度范围为0~4.5mg/L。本方法显色迅速,加入显 色剂后立即显色,且颜色稳定。
实验七、活性磷的测定
目的要求
1. 掌握钼蓝光度比色法测定磷酸盐的方法原理及实验条件。 2. 了解水体中各种不同形态磷的分离处理过程。 3. 验证盐度对吸光值的影响(设计)。
概述
水体中的磷主要以颗粒态和溶解态存在,以孔径为0.45μm醋 酸纤维滤膜为界。不通过的为颗粒态,主要为含有机磷和无机磷 的生物体碎屑及某些磷酸盐矿物颗粒;能通过0.45μm滤膜的为 溶解态磷酸盐,包括有机磷和无机磷,其中溶解态无机磷是正磷 酸盐,主要以HPO42-和PO43-的离子形式存在。
磷(总磷、溶解性磷酸盐和溶解性总磷)

一般天然水中磷酸盐含量不高.化肥、冶炼、合成洗涤剂等行业地工业废水及生活污水中常含有较大量磷.磷是生物生长必需地元素之一.但水体中磷含量过高(如超过),可造成藻类地过度繁殖,直至数量上达到有害地程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏.磷是评价水质地重要指标.个人收集整理勿做商业用途
磷酸盐贮备液:将优级纯磷酸二氢钾()于℃干燥,在干燥器中放冷.称取溶于水,移入容量瓶中.加()硫酸,用水稀释至标线,此溶液每毫升含μ磷(以计)个人收集整理勿做商业用途
磷酸盐标准溶液:吸取磷酸贮备液于容量瓶中,用水稀释至标线.此溶液每毫升含μ磷.临用时现配.个人收集整理勿做商业用途
配制
标准曲线地绘制
取数只具塞比色管,分别加入磷酸盐标准使用液、、、、、、,加水至.个人收集整理勿做商业用途
过硫酸钾消解法
仪器
医用手提式高压蒸汽消毒器或一般民用压力锅,.
电炉.
调压器,,.
(磨口)具塞刻度管.
试剂
过硫酸钾溶液:溶解过硫酸钾于水中,并稀释至.
步骤
吸取混匀水样(必要时,酌情少取水样,并加水至,使含磷量不超过μ)于具塞刻度管中,加过硫酸钾溶液,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出.将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或压力锅中加热,待锅内压力达(相应温度为℃)时,调节电炉温度使保持此压力后,停止加热,带压力表指针降至零后,取出放冷.如溶液混浊,则用滤纸过滤,洗涤后定容.个人收集整理勿做商业用途
总磷地测定,于水样采集后,加硫酸酸化至≤保存.溶解性正磷酸盐地测定,不加任何保存剂,与℃冷处保存,在内进行分析.个人收集整理勿做商业用途
总磷检测分析方法

总磷在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,它们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷酸盐,它们存在于溶液中,腐殖质粒子中或水生生物中。
天然水中磷酸盐含量较微。
化肥、冶炼、合成洗涤剂等行业的工业废水及生水污水中常含有较大量磷。
磷是生物生长的必需的元素之一。
但水体中磷含量过高(超过0.2mg/L)可造成藻类的过量繁殖,直至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
1.方法的选择水中磷的测定,通常按其存在的形式,而分别测定总磷、溶解性正磷酸盐和总溶解性磷,如下图所示消解2.样品的采集和保存总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。
溶解性正磷酸盐的测定,不加任何试剂。
于2—5℃冷处保存,在24h内进行分析。
水样的预处理采集的水样立即经0.45µm微孔滤膜过滤,其滤液可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测得可溶性总磷。
取混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
(一)过硫酸钾消解法仪器(1)医用手提式高压蒸汽消毒器或一般民用压力锅(1—1.5kg/cm2)。
(2)电炉,2kw。
(3)调压器、2kvA(0—220v)(4)50ml(磨口)具塞刻度管。
试剂5%(m/V)过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100 ml。
步骤(1)吸取25.00 ml混匀水样(必要时,酌情少取水样,并加水至25 ml,使含磷量不超过30µg)于50 ml具塞刻度管中,加过硫酸钾溶液4 ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或民用压力锅中加热,待锅内压力达1.0kg/cm2 (相应温度为120℃)时,调节电炉温度使保持此压力30min后,停止加热,待压力表指针将至零后,取出放冷。
(2)试剂空白和标准溶液系列也经同样的消解操作。
总磷检测分析方法

总磷在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,它们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷酸盐,它们存在于溶液中,腐殖质粒子中或水生生物中。
天然水中磷酸盐含量较微。
化肥、冶炼、合成洗涤剂等行业的工业废水及生水污水中常含有较大量磷。
磷是生物生长的必需的元素之一。
但水体中磷含量过高(超过0.2mg/L)可造成藻类的过量繁殖,直至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
1.方法的选择水中磷的测定,通常按其存在的形式,而分别测定总磷、溶解性正磷酸盐和总溶解性磷,如下图所示消解总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。
溶解性正磷酸盐的测定,不加任何试剂。
于2—5℃冷处保存,在24h内进行分析。
水样的预处理采集的水样立即经0.45μm微孔滤膜过滤,其滤液可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测得可溶性总磷。
取混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
(一)过硫酸钾消解法仪器(1)医用手提式高压蒸汽消毒器或一般民用压力锅(1—1.5kg/cm2)。
(2)电炉,2kw。
(3)调压器、2kvA(0—220v)(4) 50ml(磨口)具塞刻度管。
试剂5%(m/V)过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100 ml。
步骤(1)吸取25.00 ml混匀水样(必要时,酌情少取水样,并加水至25 ml,使含磷量不超过30μg)于50 ml具塞刻度管中,加过硫酸钾溶液4 ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或民用压力锅中加热,待锅内压力达1.0kg/cm2 (相应温度为120℃)时,调节电炉温度使保持此压力30min后,停止加热,待压力表指针将至零后,取出放冷。
(2)试剂空白和标准溶液系列也经同样的消解操作。
注意事项(1)如采样时水样用酸固定,则用过硫酸钾消解前将水样调至中性。
磷酸盐测定通用方法

磷酸盐测定通用方法(GB/T 9727—1988)1 适用范围本方法规定了用萃取-磷钼蓝比色法测定磷酸盐的通用方法。
本方法适用于化学试剂中微量正磷酸盐的测定。
分光光度法或目视比色法的检测范围在乙酸丁酯中为0.2~2μg/mL(以PO4计)。
2 原理在浓度c(HNO3)为0.4~1.4mol/L硝酸溶液中,正磷酸能定量与钼酸铵作用,生成磷钼杂多酸(磷钼黄),磷钼黄可被乙酸丁酯从1.0~1.4mol/L硝酸溶液中定量萃取,从而与干扰元素砷、硅及过量试剂钼酸铵分离。
加入氯化亚锡-抗坏血酸溶液,将磷钼黄还原为磷钼蓝。
根据磷钼蓝颜色的深浅,可用分光光度法或目测比色法测定磷酸盐的含量。
3 试剂本方法中所用杂质标准溶液,制剂及制品按GB 602、GB 603之规定配制。
实验用水应符合CB 6682中二级水的规格。
4 操作按产品标准的规定称取样品并制备试液(必要时用饱和2,4-二硝基酚指示液为指示剂调节试液的pH值)。
取10mL试液,加10mL硝酸(13%),此时溶液的酸度c(H﹢)应为1.0~1.2mol/L。
加2mL钼酸铵溶液(100g/L),室温下放置20min。
加入10mL乙酸丁酯,萃取;静置分层。
弃去水相,有机相用盐酸(5%)洗涤两次,每次5mL,分出水相。
在有机相中加入0.2mL氯化亚锡-抗坏血酸溶液,轻轻摇动,静置分层。
弃去水相,于有机相中加入lmL无水乙醇,混匀。
所呈蓝色与标准比对溶液比较。
标准比对溶液的制备是取含规定量的磷酸盐(PO4)标准溶液,稀释至10mL,与同体积试液同﹢时同样处理。
若用分光光度法测定,应按下述条件:测定波长为720nm,用lcm吸收池,以试剂空白为参比。
标准系列的配制:吸取含不同量的磷酸盐(P04)标准溶液,稀释至10mL,与同体积试液同时同样处理。
5 注意事项5.1 硅酸盐、砷酸盐、锗酸盐当存在硅酸盐、砷酸盐、锗酸盐时,这些盐类也能与钼酸铵发生类似的反应。
消除这种干扰的方法有:a)控制溶液的酸度当溶液的酸度c(H﹢)在0.8mol/L以上时,这些盐类不能与钼酸铵发生类似的反应。
1、2:TP、正磷酸盐的测定
TP、溶解性磷酸盐的测定废水中,磷几乎都以各种磷酸盐的形式存在,他们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷(如磷脂等),它们存在于溶液中,腐殖质粒子中或水生生物中。
工业废水及生活污水中常含有较大量磷。
磷是生物生长必需的元素之一。
但水中磷含量过高(如0.2mg/L超过),可造成藻类的过度繁殖,甚至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
磷是评价水质的重要指标。
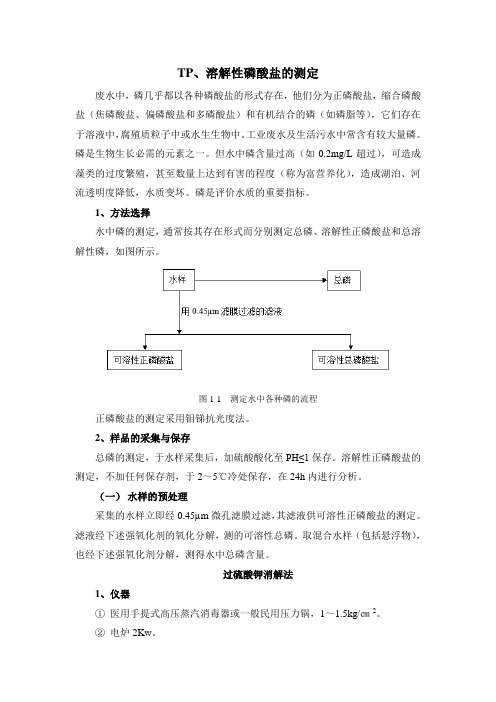
1、方法选择水中磷的测定,通常按其存在形式而分别测定总磷、溶解性正磷酸盐和总溶解性磷,如图所示。
图1-1 测定水中各种磷的流程正磷酸盐的测定采用钼锑抗光度法。
2、样品的采集与保存总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。
溶解性正磷酸盐的测定,不加任何保存剂,于2~5℃冷处保存,在24h内进行分析。
(一)水样的预处理采集的水样立即经0.45µm微孔滤膜过滤,其滤液供可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测的可溶性总磷。
取混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
过硫酸钾消解法1、仪器①医用手提式高压蒸汽消毒器或一般民用压力锅,1~1.5kg/㎝2。
②电炉2K W。
③调压器,2KV A,0~220V。
④50(磨口)具塞刻度管。
2、试剂5%过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100ml。
3、步骤①吸取25.0ml混匀水样(必要时,酌情少取水样,并加水至25ml,使含磷量不超过3 0µg)于50ml具刻度管中,加过硫酸钾溶液4ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或压力锅中加热,待锅内压力达1.1kg/cm2(相应温度为1200C)时,调节电炉温度保持此压力30min后,停止加热,待压力表指针降至零后,取出冷放。
如溶液混浊,则用滤纸过滤,洗涤后定容。
TP的测定
TP在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,它们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷酸盐,它们存在于溶液中,腐殖质粒子中或水生生物中。
天然水中磷酸盐含量较微。
化肥、冶炼、合成洗涤剂等行业的工业废水及生水污水中常含有较大量磷。
磷是生物生长的必需的元素之一。
但水体中磷含量过高(超过0.2mg/L)可造成藻类的过量繁殖,直至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
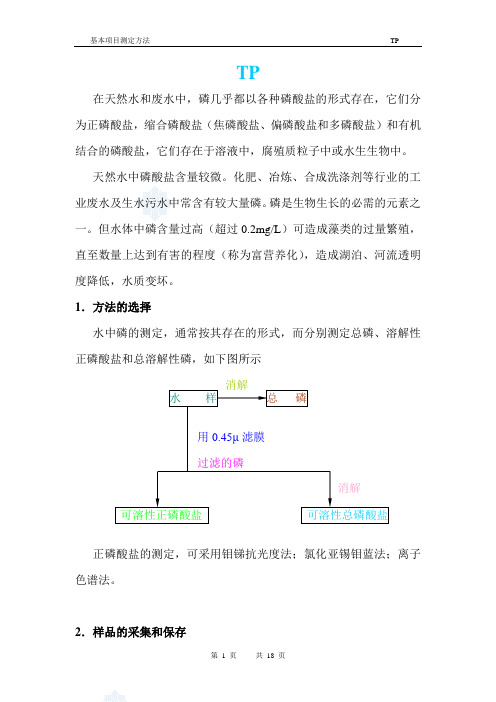
1.方法的选择水中磷的测定,通常按其存在的形式,而分别测定总磷、溶解性正磷酸盐和总溶解性磷,如下图所示正磷酸盐的测定,可采用钼锑抗光度法;氯化亚锡钼蓝法;离子色谱法。
2.样品的采集和保存总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。
溶解性正磷酸盐的测定,不加任何试剂。
于2~5℃冷处保存,在24h内进行分析。
水样的预处理采集的水样立即经0.45µm微孔滤膜过滤,其滤液可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测得可溶性总磷。
取混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
(一)过硫酸钾消解法仪器(1)医用手提式高压蒸汽消毒器或一般民用压力锅(1~1.5kg/cm2)(2)电炉,2kw(3)调压器、2kvA(0~220V)(4)50ml(磨口)具塞刻度管试剂5%(m/V)过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100 ml。
步骤(1)吸取25.00 ml混匀水样(必要时,酌情少取水样,并加水至25 ml,使含磷量不超过30µg)于50 ml具塞刻度管中,加过硫酸钾溶液4 ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或民用压力锅中加热,待锅内压力达1.0kg/cm2 (相应温度为120℃)时,调节电炉温度使保持此压力30min后,停止加热,待压力表指针将至零后,取出放冷。
污水磷酸盐和氨氮吸附能力实验

污水磷酸盐和氨氮吸附能力实验近年来,氮、磷等营养元素的过量排放所导致的水体富营养化现象日益严重,而另一方面,磷又是人类农业生产和生活必不可少的元素之一,由于其不可再生循环的特性和人类的过度消耗开发,导致全球磷矿将会在100~250a内消耗殆尽[1].因此,如何高效回收污水中的“氮磷资源”具有重要的现实意义.鸟粪石沉淀法被认为是回收污水中磷酸盐和氨氮行之有效的方法,已广泛应用于尿液、禽畜废水、污泥上清液和渗滤液等废水中.该方法不仅可以实现对水中氮磷的同步固定化回收,且其回收产物是一种性能优良的缓释肥料,可用于农田作物生产.但是,该方法仍在镁源投加和pH调控等方面存在成本较高问题以及回收困难的不足,限制了其工业推广应用.目前常用的镁源有MgCl2、MgSO4、Mg(OH)2、MgOolanghao等,其中,MgO由于其安全无毒且自碱性强等优点,在应用中具有一定碱性自调节作用,能满足鸟粪石的形成对pH的碱性需要,可实现镁源和碱源投加的减量化,从而降低成本.而选择合适的鸟粪石载体是弥补回收困难不足的有效途径之一,天然沸石作为一种多孔性架状铝硅酸盐矿物,无毒无害且价格低廉,不会造成二次污染,而且可作为晶种促使鸟粪石晶体的快速生成,且生成的鸟粪石可以很好地固载在沸石上,使其成为鸟粪石载体的首要选择对象.与此同时,天然沸石具有较强的阳离子交换能力和吸附性能,可协同鸟粪石法实现对污水中氮磷的高效回收. Huang等采用镁盐改性天然沸石同步去除模拟废水中的磷酸盐和氨氮,但其去除能力不甚理想且镁盐投加量大,成本较高.针对这一缺陷,本研究拟开发集氮磷回收性能、镁离子靶向供给、晶种作用和碱性自调控功能于一体的载镁天然沸石复合材料,构建MgO复合沸石-鸟粪石沉淀深度耦合技术,实现对污水中磷酸盐和氨氮的高效固定回收,着重考察了不同影响因素下载镁天然沸石复合材料对污水中磷酸盐和氨氮的吸附能力,并探讨了其回收机制,以期为载镁天然沸石复合材料应用于废水中氮磷的同步回收提供理论支撑.1材料与方法 1.1试剂及仪器供试天然沸石选自河南洛阳选矿厂,过60目筛备用,其化学组成列于表 1.表1天然沸石的化学组成供试试剂:磷酸二氢钾、氯化铵、六水氯化镁、酒石酸钾钠、抗坏血酸、钼酸盐、碘化钾、二氯化汞、过硫酸钾、盐酸、氢氧化钠,均为分析纯.仪器:QHZ-98A恒温振荡培养箱、XP6电子天平、FE20pH计、UV-2550紫外可见分光光度计(日本岛津公司)、ASAP2020自动吸附仪(美国Micromeritics公司)、Ultra55场发射扫描电子显微镜(德国Zeiss公司)、Nicolet5700傅立叶红外光谱仪(美国热电尼高力仪器公司)、X'pert Pro X射线衍射仪(德国Bruker公司)、XRF-1800波长色散型X射线荧光光谱仪(日本岛津公司).1.2实验设计 1.2.1载镁天然沸石复合材料的制备称取10g天然沸石,加入100mL1mol·L-1的氯化镁溶液,在恒温磁力搅拌器上搅拌1h后,按OH-/Mg2+摩尔配比为2配置一定浓度的氢氧化钠溶液缓慢滴加至混合溶液中,振荡浸渍3h后用去离子水反复冲洗过滤,得到浸渍复合物,在105℃条件下烘干脱去表层吸附水,得到载镁天然沸石的前驱物,最后放入马弗炉中于400℃焙烧5h,即制得载镁天然沸石复合材料(记为NZ-MgO).1.2.2实验方法取一定质量的NZ-MgO材料,投加到装有100mL氮磷混合模拟废水的250mL锥形瓶中,其中氨氮和磷酸盐的初始浓度皆为60mg·L-1,将其置于恒温震荡培养箱中于25℃以180 r·min-1转速反应8h,取溶液上清液过0.22μm滤膜,用分光光度法测定上清液的磷酸盐和氨氮浓度.通过测定反应前后溶液中磷酸盐和氨氮的浓度,计算单位吸附量.1.2.3分析方法(1)溶解性磷酸盐浓度测定采用GB11893-89钼酸铵分光光度法;氨氮浓度测定采用GB11893-89纳氏试剂分光光度法.(2)单位吸附量的计算:反应平衡时NZ-MgO对磷酸盐和氨氮的单位平衡吸附量通过下式计算:式中,qe为单位平衡吸附量,mg·g-1;c0为溶液中磷酸盐和氨氮的初始浓度,mg·L-1; ce为平衡时溶液中磷酸盐和氨氮的浓度,mg·L-1;V为溶液体积,L;m为NZ-MgO的质量, g.2结果与讨论 2.1NZ-MgO材料的特性图1为天然沸石(NZ)和NZ-MgO材料的XRD图谱,从中看出NZ-MgO材料较天然沸石出现了两处高强度衍射峰,分别是在42.9°(200)和62.3°(220)处,将其与MgO标准卡片(PDF#45-0946)对比,可以判定NZ-MgO材料中含有MgO组分.图2为天然沸石(NZ)和NZ-MgO材料的SEM图谱,从中可以看出,NZ-MgO材料表面较天然沸石出现了类似絮状的纳米氧化镁覆层,分散较为均匀,这为NZ-MgO复合材料同步回收溶液中的磷酸盐和氨氮提供了良好的条件.图1天然沸石(NZ)和NZ-MgO材料的XRD图谱图2天然沸石NZ和NZ-MgO材料的扫描电镜图天然沸石(NZ)和NZ-MgO材料的比表面及孔容孔径特性如表2所示.从中可知,负载纳米氧化镁后的天然沸石的比表面积、孔径和孔容分别为天然沸石的2.7、8.7和4.3倍,该特性可在一定程度上增加了材料对溶液中磷酸盐和氨氮的吸附能力.表2材料比表面积及孔容孔径特性2.2NZ-MgO投加量的优化图3为不同投加量对溶液中磷酸盐和氨氮回收性能的影响,从中可知,当投加量从0.1g·L-1增至0.4g·L-1时,NZ-MgO对溶液中的磷酸盐和氨氮的单位吸附量呈明显上升的趋势,当NZ-MgO的投加量为0.4g·L-1时,溶液磷酸盐和氨氮的单位吸附量分别高达120.3mg·g-1和48.1mg·g-1.当投加量超过0.4g·L-1时,两者的单位吸附量呈明显下降趋势,这表明反应过程中生成鸟粪石的动力下降,究其原因,可能是由于NZ-MgO投加量的增加导致溶液pH的进一步升高,从而抑制了鸟粪石晶体的形成和聚集.图3不同投加量对NZ-MgO材料回收溶液中磷酸盐和氨氮的影响2.3溶液pH的影响溶液pH是NZ-MgO回收溶液中磷酸盐和氨氮的重要影响因素,对鸟粪石晶体的形成至关重要.图4为在不同初始pH条件下投加NZ-MgO后溶液pH随反应时间的变化情况,从中可以看出,在反应初始阶段,溶液pH迅速上升,20min后溶液pH即可达到相对平衡状态,这说明NZ-MgO释放碱度较快.尤其值得注意的是,当溶液初始pH=3时,最终平衡pH可达到7.98,这说明NZ-MgO自碱性较强,无需外加碱源就可达到鸟粪石晶体的生长条件.图5为溶液初始pH对NZ-MgO回收溶液中磷酸盐和氨氮的影响,从中可知,当溶液初始pH在3~7的范围内,NZ-MgO对溶液中的磷酸盐和氨氮的吸附容量随着pH的上升而增加.当溶液初始pH升至7时,NZ-MgO对两者的吸附容量皆达到最大,分别高达118.9mg·g-1和49.3mg·g-1,而此时溶液最终平衡pH可达到9.55.Stratful等[19]指出当溶液pH>7.5时鸟粪石晶体开始生长;溶液pH≥8.5时,晶体中的鸟粪石含量可达到最大,本研究与此结果基本一致.当溶液初始pH>7时,磷酸盐和氨氮的单位吸附容量都急剧下降,这主要有以下两方面原因:①溶液中的NH4+在高pH条件下转变成NH3,导致鸟粪石溶解度升高[20];②沉淀物中存在其他沉淀物,Tao等[21]指出Mg3(PO4)2在高pH条件下较鸟粪石更容易沉淀,此外,当溶液中OH-浓度远大于PO43-浓度,也易生成Mg(OH)2沉淀[22].图4投加NZ-MgO后溶液pH随反应时间的变化图5溶液pH对NZ-MgO材料回收溶液中磷酸盐和氨氮的影响2.4动力学图6为不同反应时间对NZ-MgO回收溶液中磷酸盐和氨氮的影响,从中可知,在反应前60min内磷酸盐和氨氮的吸附容量随反应时间呈急剧上升的趋势,这可能是由于NZ-MgO可在短时间内快速释放大量的Mg2+,促使鸟粪石晶体的形成.反应60min后两者的吸附容量略有增加,反应120min后达到吸附平衡状态,此时,NZ-MgO对磷酸盐和氨氮的吸附容量分别达到119.2mg·g-1和48.5mg·g-1,还可以发现,NZ-MgO对磷酸盐和氨氮的吸附量均高于天然沸石,分别为天然沸石的56.6倍和2.2倍,这是由于载镁天然沸石表面活性吸附位点的增多以及鸟粪石晶体的大量生成.图6接触时间对回收溶液中磷酸盐和氨氮的影响为了进一步理解NZ-MgO对溶液中磷酸盐和氨氮的回收过程,采用了拟一级动力学模型[式(1)]和拟二级动力学模型[式(2)]对动力学实验数据进行拟合,式中,qe(mg·g-1)和qt(mg·g-1)分别表示平衡吸附量和时间t时的吸附量,k1(min-1)和k2[g·(mg·min)-1]分别表示拟一级和拟二级吸附速率常数.(1)(2)表3为溶液中磷酸盐和氨氮的动力学拟合参数,从中可以看出,拟二级动力学相关系数R2都高于拟一级动力学,且拟二级动力学的R2>0.99,可确定NZ-MgO对溶液中氮磷的吸附过程更适合用拟二级动力学模型来描述,这也说明该反应体系中固液界面存在一定的化学作用力,即NZ-MgO材料表面存在化学反应.表3NZ和NZ-MgO回收溶液中磷酸盐和氨氮的动力学参数2.5回收机制NZ-MgO对溶液中磷酸盐和氨氮的回收机制主要有以下4种:①物理吸附.具体来讲,天然沸石作为多孔性硅酸盐矿物,本身具有一定的吸附能力,其次,天然沸石表面负载的纳米MgO颗粒增加了孔径,有利于NZ-MgO对溶液中磷酸盐和氨氮的吸附.②离子交换.天然沸石晶格的孔穴中的部分碱金属或碱土金属离子(如:Ca2+、K+、Na+和Mg2+等)与沸石结合并不紧密,易与溶液中的NH4+发生交换.③静电吸附.当NZ-MgO投加到溶液中,材料表面的高度活性纳米MgO易在固液界面发生原位水解,形成,反应方程式如式(3)所示,在该条件下溶液中磷酸盐的主要存在形式为H2PO4-和HPO2-4[23],所以溶液中的磷酸盐极易被材料表面的正电荷所吸引,而氨氮易被排斥.④化学沉淀.根据有关研究可知[19,24],前3种机制对溶液中磷酸盐和氨氮的回收能力有限,其主要回收方式是鸟粪石沉淀法.水解产物在溶液中可以释放一定量的Mg2+,直至材料表面的[Mg2+]和[OH-]达到饱和[Ksp(Mg(OH)2)=5.61×10-12][25],当溶液中存在大量Mg2+、PO43-和NH4+时,在适宜pH 下易形成鸟粪石晶体,反应方程式如式(4~6)所示.由方程式可知,鸟粪石晶体的生成会释放一定量的H+,从而中和了溶液中的OH-,可促使材料表面活性纳米MgO的进一步水解,进而加快鸟粪石晶体的生长.(3)(4)(5)(6)图7为在最优反应条件下形成的回收产物的FTIR、XRD、SEM图谱,由图7(a)可知,谱图在波数为1007.8、571.2和471.6cm-1处存在明显的PO43-特征吸收峰,在波数为1 438.55cm-1处对应的是NH4+的变形振动,这说明磷酸盐和铵盐的组分均存在于回收产品中.由图7(b)可以看出回收产物在15.81°(020)、20.86°(111)、21.45°(021)和31.93°(040)处出现了高强度衍射峰,将其与鸟粪石的标准谱图(PDF#15-0762)对比,可发现两者所在强度峰的位置基本一致.从图7(c)可以看到回收产物表面聚集了密密麻麻的短棒状鸟粪石晶体,个别呈较大的楔状并相互黏结碰撞.综合以上分析,可确定NZ-MgO对溶液中磷酸盐和氨氮的同步回收机制主要为鸟粪石沉淀法.图7最优反应条件下回收产物的FTIR、XRD和SEM图谱2.6共存Ca2+的影响实际废水中存在较多非构晶离子杂质,影响方式主要是通过进入晶体,与构晶粒子发生化学沉淀,从而影响晶体的质量.常见的离子主要有Ca2+、Al3+、Na+和K+等,其中Ca2+对鸟粪石晶体的影响较为突出.图8为不同Ca2+浓度对NZ-MgO回收溶液中磷酸盐和氨氮的影响,从中可知,当溶液中Ca2+的浓度从0mg·L-1增至60mg·L-1时,NZ-MgO对溶液中磷酸盐的单位吸附容量逐步上升,而对溶液中氨氮的吸附量却急剧下降;当溶液中Ca2+浓度超过60mg·L-1时,两者变化不甚明显,平衡时磷酸盐的单位吸附量高达147.6mg·L-1,而氨氮的吸附量却低至1.96mg·L-1,这表明在高Ca2+浓度的情况下,以鸟粪石法同步回收溶液中的磷酸盐和氨氮几乎不可行.另外还可以发现溶液最终pH随着Ca2+浓度增加呈缓慢下降趋势,当Ca2+浓度达到120mg·L-1时,溶液pH降至8.0,这可能是由于Ca2+在溶液中发生水解,释放了一定量的H+.图8不同Ca2+浓度对去除溶液中磷酸盐和氨氮的影响图9为不同Ca2+浓度下回收产物的XRD图谱,从中可知,回收产物中的鸟粪石晶体特征峰随溶液中Ca2+浓度的增加呈弱化趋势,当Ca2+浓度超过100mg·L-1鸟粪石晶体的特征峰明显消失,这可能是由于Ca2+与磷酸盐反应生成了无定形的羟基磷灰石,而XRD通常无法鉴别.Yan等[26]指出在溶液pH在7.5~8.0之间,Ca2+在反应过程中会与鸟粪石竞争水中的磷酸盐生成羟基磷灰石[Ca10(PO4)6(OH)2],从而抑制脱氮效果,这和本研究结果相吻合.图10为Ca2+浓度为120mg·L-1下的回收产物的SEM图谱,从中可知,回收产物呈不规则的颗粒状,无明显的棒状鸟粪石晶体,这表明较高的Ca2+浓度会抑制鸟粪石晶体的形成,无法实现污水中磷酸盐和氨氮的同步回收.图9不同Ca2+浓度下回收产物的XRD图谱图10Ca2+浓度为120mg·L-1时回收产物的SEM图谱3结论(1)NZ-MgO具备高效的氮磷回收性能,其最佳回收条件为溶液初始pH=7,投加量为0.4g·L-1,该条件下NZ-MgO对溶液中磷酸盐、氨氮的吸附容量可分别高达119.2mg·g-1、48.5mg·g-1.(2)动力学研究表明,NZ-MgO在反应120min时对溶液中氮磷的回收达到平衡稳定状态,其回收过程符合拟二级动力学模型,R2>0.99.(3)NZ-MgO对溶液中氮磷的回收机制分为物理吸附、离子交换、静电吸附和化学沉淀这4种,其中以鸟粪石化学沉淀法为主.(4)共存Ca2+对NZ-MgO回收溶液中氨氮会产生明显抑制作用,Ca2+浓度的增加使得回收产物中鸟粪石含量急剧减少,磷酸钙等无定形副产物明显增加.。
城市污水中磷(总磷、溶解性磷酸盐和溶解性总磷)的测定方法

城市污水中磷(总磷、溶解性磷酸盐和溶解性总磷)测定方法在天然水和废水中,磷几乎都以各种磷酸盐的形式存在,他们分为正磷酸盐,缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐)和有机结合的磷(如磷脂等),它们存在于溶液中,腐殖质粒子中或水生生物中。
一般天然水中磷酸盐含量不高。
化肥、冶炼、合成洗涤剂等行业的工业废水及生活污水中常含有较大量磷。
磷是生物生长必需的元素之一。
但水中磷含量过高(如L超过),可造成藻类的过度繁殖,甚至数量上达到有害的程度(称为富营养化),造成湖泊、河流透明度降低,水质变坏。
磷是评价水质的重要指标。
1、方法选择水中磷的测定,通常按其存在形式而分别测定总磷、溶解性正磷酸盐和总溶解性磷,如图所示。
正磷酸盐的测定可采用离子色谱法、钼锑抗光度法、氧化亚锡还原钼蓝法(灵敏度较低,干扰较多),而孔雀绿–磷钼杂多酸法灵敏度较高,且容易普及的方法。
罗丹明6G荧光分光光度法灵敏度最高。
2、样品的采集与保存总磷的测定,于水样采集后,加硫酸酸化至PH≤1保存。
溶解性正磷酸盐的测定,不加任何保存剂,于2~50C冷处保存,在24h内进行分析。
(一)水样的预处理采集的水样立即经µm微孔滤膜过滤,其滤液供可溶性正磷酸盐的测定。
滤液经下述强氧化剂的氧化分解,测的可溶性总磷。
取混合水样(包括悬浮物),也经下述强氧化剂分解,测得水中总磷含量。
过硫酸钾消解法1、仪器①医用手提式高压蒸汽消毒器或一般民用压力锅,1~㎝2。
②电炉2K W。
③调压器,2KVA,0~220V。
④50(磨口)具塞刻度管。
2、试剂5%过硫酸钾溶液:溶解5g过硫酸钾于水中,并稀释至100ml。
3、步骤①吸取混匀水样(必要时,酌情少取水样,并加水至25ml,使含磷量不超过3 0µg)于50ml具刻度管中,加过硫酸钾溶液4ml,加塞后管口包一小块纱布并用线扎紧,以免加热时玻璃塞冲出。
将具塞刻度管放在大烧杯中,置于高压蒸汽消毒器或压力锅中加热,待锅内压力达cm2(相应温度为1200C)时,调节电炉温度保持此压力30s后,停止加热,待压力表指针降至零后,取出冷放。
总磷的测定
水体中总磷的测定-------钼酸铵分光光度法在天然水和废水中,磷几乎以各种磷酸盐形式存在。
如:正磷酸盐、缩合磷酸盐(焦磷酸盐、偏磷酸盐和多磷酸盐),和有机磷存在。
水体中磷过高(如超过0.2 mg/L),会造成富营养化。
磷是评价水质的重要指标。
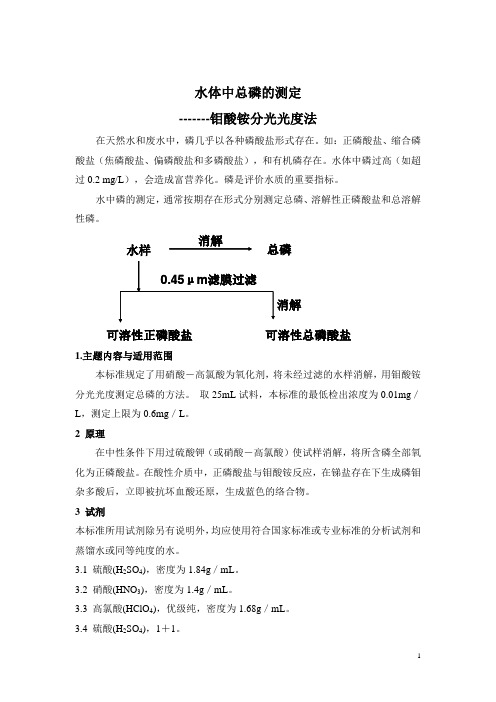
水中磷的测定,通常按期存在形式分别测定总磷、溶解性正磷酸盐和总溶解性磷。
1.主题内容与适用范围本标准规定了用硝酸-高氯酸为氧化剂,将未经过滤的水样消解,用钼酸铵分光光度测定总磷的方法。
取25mL试料,本标准的最低检出浓度为0.01mg/L,测定上限为0.6mg/L。
2 原理在中性条件下用过硫酸钾(或硝酸-高氯酸)使试样消解,将所含磷全部氧化为正磷酸盐。
在酸性介质中,正磷酸盐与钼酸铵反应,在锑盐存在下生成磷钼杂多酸后,立即被抗坏血酸还原,生成蓝色的络合物。
3 试剂本标准所用试剂除另有说明外,均应使用符合国家标准或专业标准的分析试剂和蒸馏水或同等纯度的水。
3.1 硫酸(H2SO4),密度为1.84g/mL。
3.2 硝酸(HNO3),密度为1.4g/mL。
3.3 高氯酸(HClO4),优级纯,密度为1.68g/mL。
3.4 硫酸(H2SO4),1+1。
3.5 硫酸,约c(1/2H2SO4)=1mo1/L:将27mL硫酸(3.1)加入到973mL水中。
3.6 氢氧化钠(NaOH),1mo1/L溶液:将40g氢氧化钠溶于水并稀释至1000mL。
3.7 氢氧化钠(NaOH),6mo1/L溶液;将240g氢氧化钠溶于水并稀释至1000mL。
3.8 过硫酸钾,50g/L溶液:将5g过硫酸钾(K2S2O8)溶解干水,并稀释至100mL。
3.9 抗坏血酸,100g/L溶液:溶解10g抗坏血酸(C6H8O6)于水中,并稀释至100mL。
此溶液贮于棕色的试剂瓶中,在冷处可稳定几周。
如不变色可长时间使用。
3.10 钼酸盐溶液:溶解13g钼酸铵[(NH4)6Mo7O24·4H2O]于100mL水中。
