颗粒自动包装机清洁验证报告
自动包装机报告

本报告所执行的验证方案是“自动包装机验证方案”,验证的目的是选取我公司水丸和冲剂的包装设备,并按GMP的要求进行安装,同时对设备的运行状况和模拟生产情况进行验证,以确保设备始终如一地生产出符合质量标准的产品。
一.设备资料1 资料档案1.1概述该设备为自动包装机,可包装冲剂和水丸,本机适用于中亚药业公司颗粒剂的包装。
1.2资料档案应有下列资料:设备使用说明书号码存放处档案室设备操作规程号码存放处档案室、三车间设备检修规程号码存放处档案室、动力车间设备清洗规程号码存放处档案室、三车间设备卡片号码存放处档案室2设备性能计量范围:1-80ml制袋尺寸:L:50-120W:40-85主电机功率:0.79kw主电机电压:380V主电机转速:1400转/分生产能力:40-60bag/min3设备材质部件要求实际材质表面材质表面量杯轨道不锈钢不锈钢光洁光洁不锈钢不锈钢光洁光洁检查人日期4 设备结构设备结构合理,方便拆卸,容易清洗。
检查人日期5 仪器仪表名称型号系列号横封温控仪0-300纵封温控仪0-4006评估结论:自动包装机的设备技术资料符合GMP要求,可以达到我公司水丸及冲剂包装的技术质量要求结果审查及批准部门签名日期生产部门质管部二. 运行确认1.概述在完成设备的安装工作后,为了证明设备能在预期的及设计范围内准确地运行,并完全达到规定的技术指标和使用要求,以确保生产出合格的产品,必须对设备的运行进行确认工作。
按照验证方案所制订的验证方法和验证项目,对自动包装机进行了详细验证。
2.验证结果数据综述验证项目可接受标准实测结果验证结论出料系统控制料门灵活可靠完全正常符合要求热合系统热封板网纹清洁、加热均匀可调完全正常符合要求热封切系统热封切刀清洁完好完全正常符合要求易撕口装置易撕口切刀锋利完好完全正常符合要求批号打印系统打印准确,位置适中,批号整齐、端正、清晰无歪斜完全正常符合要求SOP的适用性可遵照设备SOP来操作设备设备SOP适用于大蜜丸的生产符合要求3.运行确认验证结论经运行确认表明,所验证的自动包装机能在预期的及设计范围内准确地运行,且设备的各项运行参数能达到规定的技术要求和使用要求。
颗粒自动包装机验证方案(新版GMP-含风险评估)概要

颗粒分装机验证方案申请部门:审核人日期:审核人日期:批准人日期:目录1 引言2人员培训确认3概述4 验证的目的5 验证所需文件6 验证范围7 验证项目和时间安排9 设计确认10 供应商审计和评估11 安装确认IQ12 运行确认13 性能确认14 结果与评价15 验证周期16 设备使用阶段17设备报废阶段1 引言1.1 验证小组:姓名所在部门职务验证分工1.2 验证小组职责1.2.1负责验证方案的审批;1.2.2负责验证的协调工作,以保证验证方案规定项目顺利实施;1.2.3负责验证数据及结果的审核;1.2.4负责验证报告的审批;1.2.5负责发放验证证书;1.2.6负责验证周期的确认;1.2.7验证小组组长负责组织方案起草、方案实施全过程的组织和验证报告;1.2.8验证小组组员分别负责方案实施验证部分具体工作。
1.3工程部1.3.1负责颗粒自动包装机的调试,并做好相应记录;1.3.2负责提供颗粒自动包装机的档案、资料交档案室;1.3.4负责拟定验证周期;1.3.5负责收集各项验证、试验记录,并对数据进行分析、评估,起草验证报告,报验证小组;1.3.6确保验证设备的完好运行,为验证过程中提供有关的技术服务;1.3.7负责颗粒自动包装机的维护保养。
1.3.8负责设备的统筹管理,包括设备的配置、验收、建档、检修和报废等。
1.4 质量部1.4.1 负责对生产部提供的参数要求进行确认;1.4.2 各种检验的准备,取样及样品的测试工作;1.4.3 负责根据检验结果,出具检验报告单;1.4.4负责组织验证方案、验证报告、验证结果的会审会签;1.4.5负责对验证全过程实施监控。
负责验证的协调工作,以保证本验证方案规定项目的顺利实施;1.4.6负责建立验证档案,及时将批准实施的验证资料收存归档;1.4.7负责验证过程的取样、检验、测试及结果报告。
1.5 生产部1.5.1 负责提供与颗粒自动包装机有关的主要参数;1.5.2 负责指定颗粒自动包装机的管理人员及操作人员;1.5.3 负责验证中各种试验材料的准备工作,并派人参加验证工作对机器的操作和清洁维护保养工作;1.5.4组织实施验证方案,参加会签验证方案、验证报告,收集记录验证资料、数据。
全自动颗粒包装机验证报告

全自动颗粒包装机验证报告一、验证报告审批1 验证报告起草2 验证报告批准批准人:日期:年月日二、验证报告1 引言全自动颗粒包装机是用于颗粒剂生产中颗粒分装、热封成型的设备。
该设备于年月进行全面安装,年月完成安装调试。
根据生产工工艺和GMP要求,结合实际情况,决定于年月日~年月日对本设备进行验证。
2 目的该设备经安装调试后,检查并确认本设备是否符合技术参数要求,是否能满足生产工艺和GMP要求。
3 验证对象DXDK-80型全自动颗粒包装机安装验证、运行验证及清洗验证。
4 验证前准备4.1 文件检查检查人:检查日期:检查人:检查日期:4.3 有关全自动颗粒包装机的标准操作规程A DXDK-80型颗粒分装机标准操作规程B 颗粒分装标准操作程序C 颗粒分装机清洁标准操作程序5 验证实施检查人:检查日期:5.1.1 设备性能检查人:检查日期:检查人:检查日期:5.1.2 公用工程连接(配电)检查人:检查日期:5.2 运行验证5.2.1 性能测试(空运转)目的:保证全自动颗粒包装机在空转时符合设计要求。
接受范围:按照制造厂商的操作说明书每步操作均运行正常。
测试步骤:确认全自动颗粒包装机已经为性能测试做好一切准备,检查并保证设备可运行。
检查人:检查日期:5.2.2 功能测试(负载运转)目的:保证全自动颗粒包装机在负载运转时符合设计要求。
接受范围:按照制造厂商的操作说明书每步操作均运行正常。
测试步骤:确认全自动颗粒包装机已经为功能测试做好一切准备,包括:检查人:检查日期:测试人:测试日期:检查人:检查日期:6 结果分析和评价根据以上验证结果,写出验证评定。
7 最终审批验证报告由验证组长审核后,报验证总负责人批准,并签发验证证书。
根据验证评定,由厂长批准投入使用或禁止使用。
粉剂包装机清洁验证方案报告

粉剂包装机清洁验证方案报告DXD粉剂包装机清洁验证方案文件编号:YZJSABC有限责任公司ABC有限责任公司-清洁验证验证立项申请表立项部门立项题目验证原因生产制造部、质量管理部、化验室、饮片车间。
DXD粉剂包装机清洁验证包装机使用后要保持洁净。
申请日期要求完成日期类别验证验证要求完成目的:证明通过设定的清洁规程进行清洁后可以达到的“洁净”状态。
立项部门负责人签字:生产制造部意见质量管理部意见化验室意见饮片车间意见验证委员会的意见指定编制验证计划的部门和人员。
生产制造部:贾正龙质量管理部:刘政制作负责人:吴金兵计划要求:验证方案设计的各项指标一定要符合验收标准,尽量全面详实,所测数据如有偏差,应查明原因,立即解决。
验证完成要求及日期:核查结果经核查小组和核查委员会认可,出具核查报告后,核查视为完成,完成期限为2013年12月31日。
备注:负责人签署的方案申请书生效。
检定列入附表,由所涉及的单位和个人负责。
abc有限责任公司-清洁验证粉末包装机的清洁验证验证时间:年月日至年月日。
目的:设备清洁验证是采用目测、化验等方法来检查设备按清洁规程清洁后,设备上残留的污染物量是否符合规定的限度标准,证明本设备清洁规程的可行和可靠,从而消除了换品种时设备清洗不彻底,造成残留物对下一种生产药品污染的发生,有效地保证药品质量。
适用范围:dxd粉末包装机。
验证责任:一、验证小组1.负责审核方案的审批。
2.负责验证的协调工作,以保证本方案规定项目的顺利实施。
3.负责验证数据及结果的审核。
4.负责验证报告的审核。
5.负责发放验证证书。
二、生产制造部1.负责收集各项验证,试验记录,起草验证报告,报验证小组。
2.负责设备的维护。
三、质量管理部门1.负责验证所需的标准品、样品、试剂、试液等的准备。
2.负责各种理化检验和微生物检验的准备、取样和调试。
3.负责根据结果出具检验报告。
四、饮片车间1.负责制订清洁规程,并按规程清洁操作。
自动包装机验证报告

验证报告目录1. DXDK80C自动包装机验证报告2. DXDK80C自动包装机验证报告记录2.1安装确认2.1.1文件及技术资料2.1.2设备的材质2.1.3设备的结构2.1.4仪表的检查与校验2.1.5电气部分安装2.1.6安装确认小结2.2.运行确认2.2.1目的2.2.2运行前检查2.2.3运行检查2.2.4横封、纵封温度确认2.2.5运行确认小结2.3.性能确认2.3.1目的2.3.2方法2.3.3验证所需仪器及校验2.3.4合格标准2.3.5检测记录2.3.6性能确认小结DXDK80C自动包装机验证报告编号:WAL-XB-018-00 一、验证项目名称:DXDK80C自动包装机验证二、验证方案见DXDK80C自动包装机验证方案三、验证实施日期:2005年月日-2005年月日四、各验证项目结论:●安装确认:验证该设备的安装是否符合设备安装的要求.1、可接受标准:文件资料齐全,设备性能设计符合要求;设备安装符合设计规范.2、验证结果:查阅设备档案设文件齐全,设备性能设计符合要求;设备安装符合设计规范.(详见验证记录2.1.安装确认)3、安装确认结论: DXDK80C自动包装机安装符合要求●运行确认:验证该设备在空载运行时,符合设计要求,并检查设备操作规程的适用性1、可接受标准:按照设备操作规程空载运行,各项参数是否符合要求2、验证结果:按照设备操作规程空载运行,各项参数符合要求(详见验证记录2.2.运行确认)3、运行确认结论:DXDK80C自动包装机运行符合要求●性能确认:验证该设备在负载运行时,对工艺的适应性.1、可接受标准:本试验用三批淀粉颗粒,按该设备操作规程进行操作,外观质量、袋长、批号、封合及装量差异。
符合内控标准.2、验证结果:本试验用三批淀粉颗粒,按该设备操作规程进行操作,外观质量、袋长、批号、封合及装量差异一直符合内控标准(详见验证记录2.3.性能确认)3、性能确认结论:DXDK80C自动包装机性能符合要求五、评价与建议:1、该设备应按批准的标准操作、维护保养程序进行操作、维护和保养.2、再验证2.1该设备应在当前验证的条件下使用,使用条件发生变更,应报验证委员会审核,必要时重新验证.2.2该设备一年再验证一次.经验证,同意“DXDK80C自动包装机投入使用”。
5GHL-250型高效湿法混合制粒机清洁验证方案及报告

编号:TSP-YZ-QY-005-01GHL-250型高效湿法混合制粒机清洁验证方案及报告GHL-250型高效湿法混合制粒机清洁验证方案目录1.验证方案的起草与审批1.1验证方案起草1.2验证方案的审批2.概述3.验证目的4.验证小组职责5.验证方法5.1 验证所需文件资料5.2 参照检验对象的选择5.3物理外观检查5.4残留量和微生物检测5.4.1确定限量标准5.4.2取样点的确定5.4.3取样方法的确定5.4.4确定检验方法6.验证结果评定与结论7.验证周期8.最终批准1.验证方案的起草与审批1.1验证方案的起草1.2验证方案的审批2.概述GHL-250型高效湿法混合制粒机是一次完成混合、加湿、制粒工序的设备,为了保证产品质量,避免污染和交叉污染,我们建立了《GHL-250型高效湿法混合制粒机清洁标准操作规程》,清洁该设备后,以该设备表面药品最难溶活性成分的残留量及微生物数不超过预定的限量为指标,考察《GHL-250型高效湿法混合制粒机清洁标准操作规程》是否合理。
3.验证目的:为了确认使用《GHL-250型高效湿法混合制粒机清洁标准操作规程》对该设备进行清洁后,表面最难溶活性成分的残留量及微生物数不超过规定的限量,以达到防止发生污染与交叉污染的目的,特制定本验证方案进行验证。
4.验证小组职责:组长:生产技术部于海泉负责起草验证方案,整理验证报告负责组织该设备验证,制订验证进度,协调验证方案实施组员:生产技术部赵艳霞负责该设备清洁操作质量保证部庄金玲杨健成乔鲜云马兴白棠负责取样及检测5.验证方法:本方案选择最不利的清洁条件,对《GHL-250型高效湿法混合制粒机清洁标准操作规程》进行验证,首先确定最难溶活性成分残留量及微生物限量,然后用棉签擦拭取样,对所取样品进行检验,并将检验结果与可接受的限量进行比较,若检测结果均低于最难溶活性成分残留量及微生物可接受限量;则可证实清洁标准操作规程的有效性及稳定性.反之,则证实该清洁标准操作规程无效,需修改或重新编写清洁标准操作规程。
10.高速混合制粒机清洁验证方案及报告

编号高速混合制粒机清洁再验证方案药业有限公司验证方案1.概述GHL-250型高速混合制粒机是固体制剂车间西药线湿法制粒专用设备,为防止污染和交叉污染,需通过有效的清洗和消毒将上批药品残留在生产设备中的物质减少到不会影响下批药品疗效、质量和安全性的程度。
2.验证目的为确认GHL-250型高速混合制粒机的清洁规程程自上次验证以来,没有发生偏移,依旧能够使设备清洁后表面没有可见异物、微生物数在合格范围内,防止发生污染和交叉污染,特制定本验证方案,进行再验证。
3.职责3.1验证领导小组3.1.1负责验证方案的审批。
3.1.2负责验证数据及结果的审核。
3.1.3负责验证报告的审批。
3.1.4负责发放验证证书。
3.1.5负责再验证周期的确认。
3.2验证小组3.2.1负责起草验证方案。
3.2.2负责验证的协调工作。
3.2.3负责按验证方案规定项目实施验证。
3.2.4负责收集各项验证、试验记录。
3.2.5负责起草验证报告。
3.3生产技术部3.3.1负责起草设备清洁规程3.3.2负责设备的清洁。
3.3.3负责根据验证结果,修改设备清洁程序。
3.4设备动力部3.4.1负责组织试验所需设备的验证。
3.4.2负责仪器、仪表、量具等的校正。
3.5质量保证部3.5.1负责组织试验所需仪器的验证。
3.5.2负责验证所需标准品、样品、试剂、试液等的准备。
3.5.3负责取样及对样品的检验。
4.原理本验证方案选择最不利的清洁条件,对高速混合制粒机清洁规程进行验证。
本车间洁净区的设备最后冲洗用水为纯化水,并用75%乙醇或3%的双氧水的消毒。
为了验证清洗和消毒的效果,可以在高速混合制粒机按其清洁规程进行清洁后,进行下列检查4.1物理外观的检查。
在按相关规程进行清洁后,一看,设备内表面应无挂水现象;二闻,应无气味;三比浊,在最终冲洗纯化水中取样,于洁净的比色管中,目测冲洗水应无色透明,不得有混浊、可见异物。
则可证实设备清洗程序的有效性及稳定性。
颗粒自动包装机验证方案(新版GMP-含风险评估).总结

颗粒分装机验证方案申请部门:审核人日期:审核人日期:批准人日期:目录1 引言2人员培训确认3概述4 验证的目的5 验证所需文件6 验证范围7 验证项目和时间安排8 风险评估9 设计确认10 供应商审计和评估11 安装确认IQ12 运行确认13 性能确认14 结果与评价15 验证周期16 设备使用阶段17设备报废阶段1 引言1.1 验证小组:1.2 验证小组职责1.2.1负责验证方案的审批;1.2.2负责验证的协调工作,以保证验证方案规定项目顺利实施;1.2.3负责验证数据及结果的审核;1.2.4负责验证报告的审批;1.2.5负责发放验证证书;1.2.6负责验证周期的确认;1.2.7验证小组组长负责组织方案起草、方案实施全过程的组织和验证报告;1.2.8验证小组组员分别负责方案实施验证部分具体工作。
1.3工程部1.3.1负责颗粒自动包装机的调试,并做好相应记录;1.3.2负责提供颗粒自动包装机的档案、资料交档案室;1.3.3负责仪器仪表的校正;1.3.4负责拟定验证周期;1.3.5负责收集各项验证、试验记录,并对数据进行分析、评估,起草验证报告,报验证小组;1.3.6确保验证设备的完好运行,为验证过程中提供有关的技术服务;1.3.7负责颗粒自动包装机的维护保养。
1.3.8负责设备的统筹管理,包括设备的配置、验收、建档、检修和报废等。
1.4 质量部1.4.1 负责对生产部提供的参数要求进行确认;1.4.2 各种检验的准备,取样及样品的测试工作;1.4.3 负责根据检验结果,出具检验报告单;1.4.4负责组织验证方案、验证报告、验证结果的会审会签;1.4.5负责对验证全过程实施监控。
负责验证的协调工作,以保证本验证方案规定项目的顺利实施;1.4.6负责建立验证档案,及时将批准实施的验证资料收存归档;1.4.7负责验证过程的取样、检验、测试及结果报告。
1.5 生产部1.5.1 负责提供与颗粒自动包装机有关的主要参数;1.5.2 负责指定颗粒自动包装机的管理人员及操作人员;1.5.3 负责验证中各种试验材料的准备工作,并派人参加验证工作对机器的操作和清洁维护保养工作;1.5.4组织实施验证方案,参加会签验证方案、验证报告,收集记录验证资料、数据。
颗粒自动包装机再确认方案及报告

文件编号:VOL-FOP-028 版本号:00 颗粒自动包装机再确认方案安庆****制药有限公司文件编号:VOL-FOP-028 版本号:00 第 2 页共 2 页确认方案审批表确认方案名称颗粒自动包装机再确认方案确认方案编号VOL-FOP-028方案起草人起草日期方案审核部门审核人审核日期审核意见提取车间兹证明我已审核同意颗企管部粒自动包装机再确认方案,按此方案实施。
质量部批准意见批准人批准日期执行日期文件编号:VOL-FOP-028 版本号:00 第 3 页共 3 页目录1.确认概述2.确认目的3.确认内容3.1.预确认3.1.1文件资料3.1.2设备性能3.1.3设备材质3.1.4设备所用的仪表3.1.5电源3.1.6环境状况3.2.运行确认3.3性能确认4.再确认5.确认结果评定与结论6.确认报告总结书文件编号:VOL-FOP-028 版本号:00 第 4 页共 4 页1、概述本机为北京万德福泉新技术有限责任公司生产的颗粒自动包装机,主要用于颗粒剂的包装。
该设备主材采用不锈钢,拆装方便,易于清洁。
电机功率为0.6千瓦,生产能力55-100袋/h。
本机型号为DXDK80Z型。
本机器适用于食品、医药等产品中的松散状、无粘性细小颗粒物品的小剂量自动包装。
本机器具有自动制袋、可调量杯计量、充填、打印日期、封合部位打口、计数等功能。
2、确认目的:本再验证是通过对颗粒自动包装机的预确认及运行、性能确认等,对该设备准确性、适应性作评估,以证实该设备符合生产工艺的要求。
3、确认内容3.1. 预确认项目及标准3.1.1文件资料序号资料名称存放地点检查结果1 采购定单公司档案室2 操作手册公司档案室3 维修说明书公司档案室4 图纸公司档案室5 产品合格证公司档案室检查人:日期:复核人:日期:3.1.2. 设备性能名称标准检查情况型号DXDK80Z功率 1.6KW生产能力55-100袋/分纵封加热棒200W×2横封加热棒200W×2检查结果:检查人:日期:复核人:日期:3.1.3.设备材质文件编号:VOL-FOP-028 版本号:00 第 5 页共 5 页部件要求及标准检查结果料斗不锈钢、光滑料盘不锈钢、光滑量杯不锈钢、光滑制袋导槽不锈钢、光滑设备主架不锈钢、光滑确认结果:检查人:日期:复核人:日期:3.1.4.设备所用的仪表仪表名称型号合格证号检查结果横封温控仪TED-4301纵封温控仪TED-4301确认结果:检查人:日期:复核人:日期:3.1.5.电源设计要求安装情况检查结果单相220V 单相三线220V功率1.6KW 功率1.6KW频率50Hz 频率50Hz接地保护0.9Ω确认结果:检查人:日期:复核人:日期:3.1.6. 环境状况项目要求检查结果温度18~26℃湿度45~65%空气洁净度D级确认结果:检查人:日期:复核人:日期:3.2.运行确认在完成设备预确认后,根据设备标准操作程序对设备进行部份或整体空载运文件编号:VOL-FOP-028 版本号:00 第 6 页共 6 页转,来确保该设备能在要求的范围内准确运行并达到规定的技术指标。
自动颗粒包装机清洁验证

自动颗粒包装机清洁验证方案1适用范围本验证方案适用于三车间的DXDK40Ⅱ型自动颗粒包装机的清洁验证。
2职责生产技术部:负责清洁验证方案的起草及验证的实施。
质量部QC:负责按计划完成清洁验证中的相关检验任务,确保检验结果的正确可靠。
QA验证管理员:负责验证工作的管理,协助清洁验证方案的起草,组织协调验证工作,总结验证结果,起草验证报告。
质量部经理:负责清洁验证方案及报告的审核。
质量总监:负责清洁验证方案及报告的批准。
3概述3.1.我公司三车间的自动颗粒包装机是用于分装硫酸锌颗粒的专用性设备,为了防止不同批号之间由于颗粒包装机的清洁达不到要求而致下一批颗粒染菌,通过试验对《颗粒包装机清洁SOP》进行验证。
3.2.清洁后的评估项目:物理外观检查及微生物限度检查,如果清洁后各评估项目均达到预先设定的标准,则说明该清洁程序是可以达到要求的清洁消毒效果的。
(注:微生物验证的取样应在化学验证取样之前进行。
)4验证目的4.1通过物理外观检查(目检)来考查颗粒包装机的外观清洁效果,以证实本清洁方法能够满足要求。
4.2由于硫酸锌颗粒在成品质量标准中有卫生学指标的检测,为了保证不因颗粒包装机的清洁不彻底而污染下一批药物,通过检测消毒后颗粒包装机取样部位的菌落数来证明其消毒效果。
5清洁方法每批硫酸锌颗粒包装结束后,按《颗粒包装机清洁SOP》对设备进行清洁。
6取样部位确定6.1按《颗粒包装机清洁SOP》清洁包装机后,其清洁部位包括分装机料斗、料盘、成型器、量杯、出料口、辊、以及分装机外壳等。
6.2根据本包装机的特点,确定成型器内壁(M)、料盘(N)是最难清洁的部位,以这两个部位为棉签擦拭取样法的取样部位。
7化学验证物理外观检查取样:清洁结束后,在最难清洁的部位用清洁白稠布进行擦拭取样。
检验方法:目视检查法可接受标准:目视检查颗粒包装机料斗、成型器、料盘、量杯、接料盒、辊、以及包装机外壳等应无残留药粉,无污迹,用清洁白稠布抹后应无可见污迹。
清洁验证方案
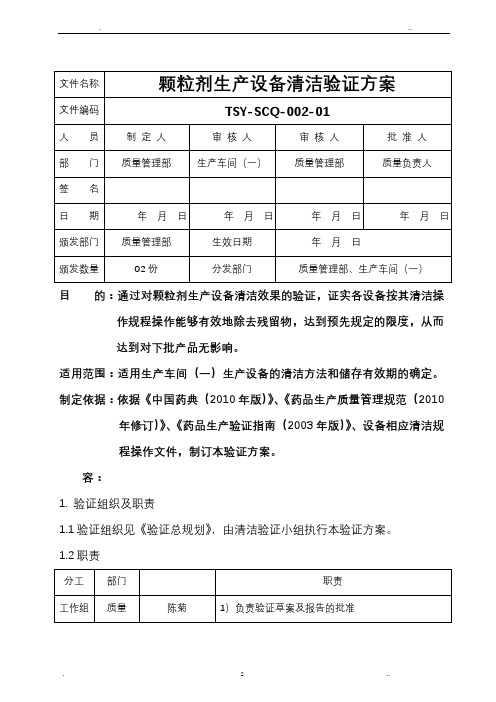
目的:通过对颗粒剂生产设备清洁效果的验证,证实各设备按其清洁操作规程操作能够有效地除去残留物,达到预先规定的限度,从而达到对下批产品无影响。
适用范围:适用生产车间(一)生产设备的清洁方法和储存有效期的确定。
制定依据:依据《中国药典(2010年版)》、《药品生产质量管理规范(2010年修订)》、《药品生产验证指南(2003年版)》、设备相应清洁规程操作文件,制订本验证方案。
容:1. 验证组织及职责1.1验证组织见《验证总规划》,由清洁验证小组执行本验证方案。
1.2职责2. 概述2.1根据GMP要求,在每次更换品种、批号或生产工序完成后,要认真按清洁规程,对设备、容器、生产场地进行清洁,以避免造成不同批号或不同品种产品之间的污染和交叉污染,有效地保证药品质量。
2.2设备清洁在制药生产中有特殊地位,生产设备的清洗是指从设备表面去除可见及不可见物质的过程。
这些物质包括活性成分及其衍生物、辅料、清洁剂、环境污染物质、水冲洗残留物及设备运行过程中释放出的异物。
为正确评估清洗程度的效果,需定期对直接接触药品的设备进行清洁验证。
3. 颗粒剂生产设备3.1颗粒剂生产设备清单3.2本次验证设备的主要材质为304不锈钢。
3.3本次验证设备及与产品接触面积4. 验证周期为了验证清洁方法的稳定性和可靠性,三批生产后,分别进行清洁验证。
5. 清洁验证准备工作5.1进行生产设备清洁验证前,所有与清洁验证有关的仪器、设备应进行过校验或确认。
仪表、计量器具等应校验合格,仪器、设备等应建立相应的操作、维护保养规程,对清洁验证的样品应建立相应的检验操作规程。
本次清洁验证中所使用设备的确认情况及QC检验过程中所使用的仪器、设备、仪表、计量器具等确认或校验情况见附表。
5.2设备清洁规程及文件编号5.3清洁介质及用品清洁介质:饮用水、纯化水、压缩空气、75%乙醇清洁用品:清洁布、一次性清洁布5.4清洁方式及取样部位5.4.1清洁方式:生产设备的清洁方式为手工清洁方式,由操作工持清洁工具,按预定的要求清洗设备,根据目测确定清洁的程序,直至清洁完成。
颗粒自动包装机清洁验证报告

颗粒剂生产工序设备清洁验证报告1.概述根据验证方案的时间安排验证小组于10月20日至23日随颗粒生产组织,颗粒自动包装机清洁验证工作。
2.验证目的验证“各设备清洁规程”的清洁效果是否符合要求,清洁剂选用是否合理。
3.验证使用的文件“设备清洁规程”、“周转容器具清洁规程”、“洁净区门窗、地面、墙面、台面、天花板清洁规程”及其相关文件。
4.验证范围颗粒自动包装机。
5.验证条件5.1设备条件:5.1.1颗粒自动包装机为经过设备验证的完好设备。
5.1.2凡接触药品的设备部位均为不锈钢,符合GMP要求。
5.2人员条件。
各岗人员均已经过GMP知识,药品管理法及其实施细则、产品质量法等法律法规的培训,经过了岗位SOP,工艺规程、清洁规程等培训,具有上岗证的熟练工人。
5.3 清洁剂条件:选用中性无磷等“白猫”牌洗洁精。
6.验证实施6.1颗粒自动包装机的清洁验证。
6.1.1清洗操作步骤:6.1.1.1拆下加料斗、计量盘、量杯、切刀、出料门,并清理残余颗粒粉尘,用饮用水冲洗干净后,再用纯水清洗干净。
6.1.1.2用饮用水擦洗干净机体外表面至清洁干净。
6.1.1.3用含乙醇的白绸布清洁电眼,用75%乙醇擦拭各部件及机体表面进行消毒。
6.1.2需验证的关键部位:6.1.2.1 加料斗、计量盘、量杯。
6.1.2.2 出料门、切刀。
6.1.3 清洗操作人员:20040801批清洗由操作。
20040802批清洗由操作。
20040803批清洗由操作6.1.4 清洁检查方法与结果:6.1.4.1 擦拭法:用含乙醇棉球擦拭颗粒自动包装机各键部件,检查结果为:无任何可见的残留物痕迹。
6.1.4.2 微生物检查:按设备表面附着菌检查标准操作规程进行检测,设备表面附着菌检出结果为:20040801批 10CFU/棉签、20040802批 20个/棉签、20040803批 10CFU/棉签。
6.1.5 清洁过程QA监控人员:6.1.6验证结论:从清洁检查结果表明:各项指标均符合合格标准。
038-ZL-200型快速整粒机清洗验证方案及报告

清洗验证方案****制药厂1. 验证方案的起草与审批1.1 验证方案的起草1. 2 验证方案的审批2. 验证小组成员名单3. 时间进度表4. 概述5. 验证目的6. 清洁标准操作规程7. 关键部位和参照产品7.1关键部位7.2参照产品8. 验证方法8.1 物理外现检查8.2化学测定8.2.1 考核指标的确定8.2.2 取样方法8.2.3 检验方法9.验证接受标准及检查结果10.再验证10.1 变更后再验证10.2验证周期11.最终评价及验证报告1验证方案的起草与审批1.1验证方案的起草1.2验证方案的审批2.验证小组成员名单3.时间进度表4.概述ZL-200 型快速整粒机用于多个产品颗粒干燥后的整粒生产,为了防止交叉污染,须对设备的清洗进行验证。
本验证以感冒通片整制粒生产后,按整粒机清洁标准操作规程进行清洗,用擦拭法取样,检测设备中人工牛黄的残留物,证实其结果在规定的许可范围之内,不会对下一品种的质量造成影响。
5.验证目的通过对本设备的清洗验证,证实设备按其清洁标准操作规程操作能达到设备的清洗要求。
6.清洁标准操作规程ZL-200 型快速整粒机清洁标准操作规程:SOP-CS-032-00。
7.关键部位和参照产品7.1关键部位设备清洗的关键部位为设备的边角,即最容易为固体残留物、液体玷污的地方。
本设备的关键部位为:刮刀、筛网和料斗内壁。
7.2参照产品721设备生产的一组产品7.2.2选择参照产品7.2.2选择参照产品最难清洗的产品就是水中溶解度最小的产品,所以参照产品是感冒通片中的人工牛黄,在设备生产该产品结束后,进行清洗验证。
8.验证方法8.1物理外观检查参照产品(感冒通片)整粒生产后,按规定的清洁程序清洗设备,检查应无人工牛黄残留物及残留气味。
8.2化学检测8.2.1考核指标的确定任何产品不能受到前一产品带来超过其 10ppm 的污染。
对于本验证,其它产品每公斤中许可含有人工牛黄 10mg ,即10ppm 。
DXDK40Ⅱ自动颗粒包装机清洁验证方案

DXDK40Ⅱ自动颗粒包装机清洁验证文件验证方案编号:V103C006-00 验证报告编号:B-V103C006-00目录1.验证立项申请表2.验证小组成员3.验证方案4.验证报告5.验证证书验证立项申请表验证小组人员DXDK40Ⅱ自动颗粒包装机清洁验证方案验证方案编号:V103C006-00起草人: 日期:年月日审核人: 日期:年月日日期:年月日日期:年月日批准人: 日期:年月日目录1.概述2.验证目的3.验证条件4.相关部门职责5. 验证进度计划6. 验证引用的文件7. 验证项目及合格标准8. 验证容与方法(包括取样方法和检测方法、如有偏差,详细说明偏差的处理情况)。
9. 验证结果与结论10. 附件1、概述本公司DXDK40Ⅱ自动颗粒包装机为直接接触药品的主要设备,目前主要用于颗粒包装,根据GMP要求每次更换品种要认真按清洁操作规程对设备、容器进行清洁和消毒。
DXDK40Ⅱ自动颗粒包装机的清洗是指从DXDK40Ⅱ自动颗粒包装机外去除可见及不可见物质的过程。
这些物质包括活性成分、清洁剂、微生物及环境污染物等,为正确评价清洗的效果,需进行清洁验证。
2、验证目的DXDK40Ⅱ自动颗粒包装机清洁验证是指从目检、化学和微生物角度试验并证明DXDK40Ⅱ自动颗粒包装机按规定的清洁规程清洗后,使用该设备生产产品时没有来自上批产品及清洗过程所带来的污染的风险。
3、验证条件D级洁净区环境应符合要求,与本程序相关的项目(空调系统、纯化水及相关检验方法等)都经过验证而且合格,操作人员均经专业岗位培训后上岗,操作人员技术熟练、职责明确、健康检查合格。
ZDXDK40Ⅱ自动颗粒包装机清洁验证的验证方法是选择最不利清洗情形,首先以考虑活性成分的无显著影响值入手,确定最大允许残留物浓度限度,然后对冲洗水样及取样棉签样品进行化学和微生物检验,对冲洗溶剂样品进行化学检验,将所得结果与可接受限度比较,若低于残留物浓度限度,则可证实清洗程序的有效性及稳定性。
自动颗粒包装机验证

烟台正方制药有限公司(中港合资)企业标准文件号: YZ-JS-021-01题目DXDK-80自动颗粒包装机的验证复印号:01,02,03,04,05,06,07,08,09,10,11,12,13,14,15,16,17,18,19,20……起草:审核:批准:1.0修订清单1.1.该文件所有的修订和发布情况均记录于下列表格中。
1.2.文件持有者必须将文件的修订情况填入相应位置,并且在接到修订版后,立即将原版本撤下,由QA收回或在QA人员的监督下销毁。
2.0目的:建立DXDK-80自动颗粒包装机的验证,保证设备符合生产要求3.0范围:DXDK-80自动颗粒包装机。
4.0依据:《药品生产质量管理规范》(1998)5.0责任:验证小组负责人、质量部负责人。
6.0内容:6.1.验证方案6.1.1.预确认6.1.1.1.概述本方案是根据公司实际生产要求、生产工艺标准、GMP的有关规定来制定的,目的是选择适合公司的颗粒剂包装设备。
为达到此目的,本方案制定了具体的设备选型条件,包括设备的技术指标及设计规范要求、合适的供应商等,以确保预确认实施工作的顺利进行。
6.1.1.2.验证内容6.1.1.2.1.验证目的确定欲购买颗粒剂包装的设备的技术指标、设计规范要求,选择适合公司的颗粒剂包装设备,同时选择合适的供货商。
6.1.1.2.2.验证方法根据公司颗粒剂包装生产的质量要求,定出欲购设备的技术指标,根据指标作广泛的市场调研,并选择合适的供货商和设备。
6.1.1.2.3.验证项目及可接受标准6.1.2.安装确认6.1.2.1.概述本阶段的验证方案是根据DXDK80自动颗粒包装机技术和操作资料及GMP的有关规定而制订的,本阶段确认的目的是对设备本身及其整个安装过程的有关技术指标是否符合要求进行确认,为设备的正式运行做好准备工作。
为达到以上目的,本方案制订了具体的验证条件,主要包括设备开箱验收、安装场地的准备、设备备件清单的制订、编写标准操作规程、编制各种设备运行记录、仪器的检验等,以确保安装确认工作的顺利进行。
GMP认证全套文件资料08-自动包装机清洗验证

SB-80型自动包装机清洗验证文件目录1、验证的目的与计划1.1验证目的1.2验证计划2、验证机构3、验证方案的起草与审批3.1验证方案的起草3.2验证方案的审核3.3验证方案的批准4、设备清洁验证方案4.1设备简介4.2清洁操作规程4.3需验证的关键部位和验证方法4.3.1关键部位4.3.2验证方法4.3.2.1物理外观检查4.3.2.2化学检测4.4设备与物料接触的表面积4.5考核指标和可接受的限度范围4.5.1外观检查标准4.5.2化学检测标准4.6 验证评估5、验证总结及批准5.1验证结果总结5.2验证结果的审查5.3验证结果的批准6、再验证6.1变更后的再验证6.2定期的再验证7、附录1、验证的目的与计划1.1验证的目的根据98版GMP的要求,必须对设备的清洁进行验证,以保证药品在生产过程中,设备清洁后的残留不会对下一批产品的质量造成污染,证明设备按其清洁SOP进行操作后能达到工艺要求。
1.2验证计划本验证以罗红霉素颗粒剂在全自动颗粒包装机中试生产后,按其清洁SOP 对设备进行清洁,并对设备上的罗红霉素残留进行检测,证明其残留量在规定的许可范围之内,不会对下一批罗红霉素颗粒剂的产品质量造成污染,并对验证结果进行总结。
2、验证机构验证参与部门:质量部、生产技术部、制剂车间验证负责部门:质量部3、验证方案的起草与审批3.2验证方案的审核审核意见:3.3验证方案的批准批准意见:批准人:批准日期:4、设备清洗验证方案4.2设备简介自动颗粒包装机主要用于颗粒的复合膜包装。
现制剂车间利用该机生产的品种为罗红霉素颗粒剂、牛磺酸颗粒剂。
4.2清洁操作规程本设备的清洁规程详见SOP—WS—2018—014.3需验证的关键部位及验证方法4.3.1关键部位设备清洁的关键部位必须选择设备的边角,即最容易为固体残留,液体玷污,又不易清洁的地方。
本设备清洁验证的关键部位为料斗、粉盘及下料装置等。
4.3.2验证方法生产结束后,必须及时按照设备清洁SOP的规定对设备进行清洁,对清洁结果应从以下两种方法进行检查。
高速自动包装机清洁验证报告

类别:验证管理编号: YZ-I-016-00部门:制剂车间页码:共 15 页第 1 页高速自动包装机清洁验证报告版次:□新订□替代:起草:年月日审核:年月日批准:年月日生效日期:年月日授权:现授权下列部门拥有并执行标准(复印数:份)生产经理、生产技术部、质量保证部、工程设备部、制剂车间复印序列号:目录1. 概述-------------------------------------------------------------------3页1.1 设备特性描述----------------------------------------------------------3页1.2 使用本设备生产的产品--------------------------------------------------4页2. 验证目的---------------------------------------------------------------4页3. 验证小组---------------------------------------------------------------4页4. 原理-------------------------------------------------------------------4页5. 验证内容---------------------------------------------------------------5页5.1验证的准备工作-------------------------------------------------------- 5页5.1.1验证所需文件资料----------------------------------------------------5页5.1.2验证所需试验条件----------------------------------------------------5页5.2 参照检验对象的选择---------------------------------------------------5页5.3 确定限量标准---------------------------------------------------------6页5.4 取样点的确定----------------------------------------------------------6页5.5取样方法的确定-------------------------------------------------- ------6页5.6确定检验方法----------------------------------------------------------6页5.7 验证实施--------------------------------------------------------------6页5.8验证结果评定与结论----------------------------------------------------7页5.9再验证周期------------------------------------------------------------7页5.10 验证小组领导意见-----------------------------------------------------7页6. 附件:--------------------------------------------------------------8-16页验证时间2018年12月10日---2018年12月13日1.概述高速自动包装机是制剂生产中用于内包的设备,为保证产品质量、避免污染及交叉污染,我们建立了高速自动包装机的清洁规程(附件1),该清洁规程必须能够保证按规程清洁后高速自动包装机最终冲洗水及微生物不超过预先确定的限量。
包装机验证方案及报告

******验证方案及报告安图绿科生物工程有限公司目录1、验证方案1、概述1.1概述1.2设备信息2、验证目的3、验证职责4、验证容4.1安装确认4.2运行确认4.3性能确认4.3.1封口参数确认432产品在参数的封口效果确认二、验证结果评价三、验证报告1、验证职责签字2、确认记录2.1安装确认2.2运行确认2.3性能确认一、验证方案1、概述1.1概述:********是一款集制袋、充填、封合、计数、打码、等一系列动作均自动完成的立式包装机,我公司主要用该设备对 ******进行包装,要求设备能持续稳定的生产出符合生产工艺要求的产品。
1.2设备信息:2、验证目的(1) 确认检查该设备各部件及资料齐全,安装良好。
(2) 调试设备,确认设备的功能运行能否达到设计标准,运行稳定可靠(3) 确认该设备运行参数,保证在参数围能持续稳定生产出合格的产品' 3、验证职责4、验证容4.1安装确认4.2运行确认4.3性能确认4.3.1封口参数确认根据设备调试情况,横封温度选择围为** C-*** C,纵封温度选择围为*** °C-*** °C,速度选择围为**-**包/分,对以上三个参数进行交叉试验,温度调整幅度为** C,速度调整幅度为5包/分,每种参数搭配至少取样**个进行取样检查,做密封性试验,并对合格率进行统计。
合格标准:1、用力握不漏气或发生清脆的爆裂声2、切口整齐、无粘连3、无变色、烤焦等影响外观现象4、纵封口整齐,无明显露白,无褶皱4.3.2产品在参数的封口效果确认取二十个易知盖检测管,在参数围选择几个参数搭配,在确认的参数围进行装载封口,并对包装合格结果进行统计。
合格标准:1、用力握不漏气或发生清脆的爆裂声2、切口整齐、无粘连3、无变色、烤焦等影响外观现象4、纵封口对齐,无明显露白无褶皱5、封的产品检验无问题、验证结果评价专业资料三、验证报告1、验证职责签字2、确认记录2.1安装确认2.2运行确认2.3性能确认2.3.1封口参数确认结果表:确认人:_______ 核人: _______ 认时间: ____ 年—月—日232产品在参数的封口效果确认记录:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
颗粒剂生产工序设备清洁验证报告
1.概述
根据验证方案的时间安排验证小组于10月20日至23日随颗粒生产组织,颗粒自动包装机清洁验证工作。
2.验证目的
验证“各设备清洁规程”的清洁效果是否符合要求,清洁剂选用是否合理。
3.验证使用的文件
“设备清洁规程”、“周转容器具清洁规程”、“洁净区门窗、地面、墙面、台面、天花板清洁规程”及其相关文件。
4.验证范围
颗粒自动包装机。
5.验证条件
5.1设备条件:
5.1.1颗粒自动包装机为经过设备验证的完好设备。
5.1.2凡接触药品的设备部位均为不锈钢,符合GMP要求。
5.2人员条件。
各岗人员均已经过GMP知识,药品管理法及其实施细则、产品质量法等法律法规的培训,经过了岗位SOP,工艺规程、清洁规程等培训,具有上岗证的熟练工人。
5.3 清洁剂条件:
选用中性无磷等“白猫”牌洗洁精。
6.验证实施
6.1颗粒自动包装机的清洁验证。
6.1.1清洗操作步骤:
6.1.1.1拆下加料斗、计量盘、量杯、切刀、出料门,并清理残余
颗粒粉尘,用饮用水冲洗干净后,再用纯水清洗干净。
6.1.1.2用饮用水擦洗干净机体外表面至清洁干净。
6.1.1.3用含乙醇的白绸布清洁电眼,用75%乙醇擦拭各部件及机体表面进行消毒。
6.1.2需验证的关键部位:
6.1.2.1 加料斗、计量盘、量杯。
6.1.2.2 出料门、切刀。
6.1.3 清洗操作人员:20040801批清洗由操作。
20040802批清洗由操作。
20040803批清洗由操作
6.1.4 清洁检查方法与结果:
6.1.4.1 擦拭法:用含乙醇棉球擦拭颗粒自动包装机各键部件,
检查结果为:无任何可见的残留物痕迹。
6.1.4.2 微生物检查:按设备表面附着菌检查标准操作规程进行检
测,设备表面附着菌检出结果为:20040801批 10CFU/棉签、20040802批 20个/棉签、20040803批 10CFU/棉签。
6.1.5 清洁过程QA监控人员:
6.1.6验证结论:从清洁检查结果表明:各项指标均符合合格标准。
因此判定清洗合格,即颗粒自动包装机的清洁规程是可行的,具有操作性,对产品质量无影响。
7.清洁过程QA监控。
