表面活性剂原理课件
合集下载
第三章表面活性剂-PPT

大多数聚氧乙烯表面活性剂得浊点在 70~100℃。
45
六 表面活性剂得生物学性质
1、对药物吸收得影响 表面活性剂得存在可能增加药物吸收,也可能降低药物
得吸收。 (1)若药物系被增溶在胶束内,且能顺利从胶束内扩散或胶
束本身迅速与胃肠粘膜融合,则可增加吸收,如吐温80 促进螺内酯口服吸收。 (2)表面活性剂得浓度亦有重要影响,如0、01%吐温80可 增加司可巴妥吸收,而1%吐温80反而降低了司可巴妥 吸收。
图解表面张力
三、表面活性剂得种类
根据极性基团得解离性质进行分类: ①离子型表面活性剂(阴离子型活性剂;阳离子
型活性剂,两性离子型); ②非离子型表面活性剂。
混合型得
11
大家应该也有点累了,稍作休息
大家有疑问的,可以询问和交
12
根据分子量大小进行分类: ①低分子表面活性剂; ②高分子表面活性剂[如海藻酸钠、聚乙烯醇(PVA)、
酸碱酶得作用下易水解。
23
24
第二节 表面活性剂得基本特性
一、胶束(micelles)
溶液得表面正吸附达到饱与后,当溶液内表面活性剂 分子数目不断增加时,分子转入溶液中,其疏水部分 相互吸引,缔合在一起。
表面活性剂分子自身依靠范德华力相互聚集,形成亲 油基向内,亲水基向外,在水相中温度分散,大小在胶 体粒子范围得缔合体,称为胶束。
表面活性剂浓度变大
C < CMC
分子在溶液表面 定向排列,表面张 力迅速降低
C = CMC
溶液表面定向排 列已经饱与,表面 张力达到最小值。 开始形成小胶束
C > CMC
溶液中得分子得憎水 基相互吸引,分子自 发聚集,形成球状、 层状胶束,将憎水基 埋在胶束内部
45
六 表面活性剂得生物学性质
1、对药物吸收得影响 表面活性剂得存在可能增加药物吸收,也可能降低药物
得吸收。 (1)若药物系被增溶在胶束内,且能顺利从胶束内扩散或胶
束本身迅速与胃肠粘膜融合,则可增加吸收,如吐温80 促进螺内酯口服吸收。 (2)表面活性剂得浓度亦有重要影响,如0、01%吐温80可 增加司可巴妥吸收,而1%吐温80反而降低了司可巴妥 吸收。
图解表面张力
三、表面活性剂得种类
根据极性基团得解离性质进行分类: ①离子型表面活性剂(阴离子型活性剂;阳离子
型活性剂,两性离子型); ②非离子型表面活性剂。
混合型得
11
大家应该也有点累了,稍作休息
大家有疑问的,可以询问和交
12
根据分子量大小进行分类: ①低分子表面活性剂; ②高分子表面活性剂[如海藻酸钠、聚乙烯醇(PVA)、
酸碱酶得作用下易水解。
23
24
第二节 表面活性剂得基本特性
一、胶束(micelles)
溶液得表面正吸附达到饱与后,当溶液内表面活性剂 分子数目不断增加时,分子转入溶液中,其疏水部分 相互吸引,缔合在一起。
表面活性剂分子自身依靠范德华力相互聚集,形成亲 油基向内,亲水基向外,在水相中温度分散,大小在胶 体粒子范围得缔合体,称为胶束。
表面活性剂浓度变大
C < CMC
分子在溶液表面 定向排列,表面张 力迅速降低
C = CMC
溶液表面定向排 列已经饱与,表面 张力达到最小值。 开始形成小胶束
C > CMC
溶液中得分子得憎水 基相互吸引,分子自 发聚集,形成球状、 层状胶束,将憎水基 埋在胶束内部
表面活性剂作用原理 PPT

聚氧乙烯型
HLB值=
皂化值不易得到的
离子型
HLB=∑(亲水基团HLB)+∑(亲油基团HLB)+7
混合型 HLB混合=∑(HLBi ×qi)
2.3.1.2 HLB与表面活性剂应用关系
亲油 | 亲水
HLB值 0 1 3 6 7 8 10 12 13 15 18 | |消泡| — | | 润湿剂 |—增溶剂——|
2.2 表面活性剂胶束
2.2.1 胶束的形成
胶束结构示意图
2.2.2 临界胶束浓度 CMC Critical Micell Concentration
表面活性剂在水中随着浓度增大,表面上聚集的活性剂分 子形成定向排列的紧密单分子层,多余的分子在体相内部 也三三两两的以憎水基互相靠拢,聚集在一起形成胶束, 这开始形成胶束的最低浓度称为临界胶束浓度。
第二章
表面活性剂的作用原理
2.1 表面张力与表面活性
当任意两相接触时, 两相之间决非是一个没有厚 度的纯几何面,而是一个具有相当厚度的过渡区体,这种界面通常称为表面。 但由于历史的原因, 这两个概念常常混用。 常见的界面有:气-液界面,气-固界面,液-液 界面,液-固界面,固-固界面。
表面活性剂的碳氢链长 碳氢链分支 极性基团的位置 碳氢链中其它取代基的影响 疏水链的性质 亲水基团的种类 温度 离子型 Krafft point 非离子型 浊点 cloud point
2.2.3 胶束的形状和大小
球 状
2.2.4 胶束的作用
乳化作用 泡沫作用 分散作用 增溶作用
催化作用
2.3 表面活性剂结构与性能的关系
气-液界面
气-固界面
液-液界面
液-固界面
固-固界面
表面活性剂课件课件

第5页,此课件共47页哦
2.4 生物表面活性剂:利用微生物在一定条件下,将某些 物质转化为具表面活性剂特性的代谢物.
▪ 如:海藻糖脂,磷脂类,鼠李糖,蛋白脂-多糖聚合物
3、特征、结构与性质 3.1 特征 ①两亲性:亲水亲油性 ②溶解性:溶于液相中的某一相
第6页,此课件共47页哦
③界面吸附:达到平衡时,其在界面上的浓度要大 于其作为溶质在溶液整体中的浓度
N a O HC H 81 7
C H S -O H 3
C H 71 5
C H S -O N 3a
7.1.2.4 α-烯烃磺酸盐-AOS
第一步:
+ R-CH2-CH2 CH=CH2 SO3
第二步:
R-CH2=CHCH2 CH2SO3 H 含量42%
R-CH2-CH-CH2 CH2 1, 3烷 烃 磺酸 内酯
3.2 结构及性质 ①不对称结构:亲水亲油基团一般分处两端,
使其一部分可溶于水而另一部分易自水中逃 逸。 ②疏水基团:脱离水包围的趋势,自身互相靠 近并聚集,致使其在水溶液表面上吸附,并 在溶液内部形成胶束。 ③表面张力γ与lgC:作图可确定CMC
第8页,此课件共47页哦
γ
( 表 面 张 力 )
▪ 至少涉及气、液、固三相。
▪ 首先是采用能大量起泡的表面起泡剂。 ▪ 当在水中通人空气或由于水的搅动引起空气进入水中时,表面活
性剂的憎水端在气—液界面向气泡的空气一方定向, 亲水端 仍在溶液内,形成了气泡。
▪ 另一种起捕集作用的表面活性剂(一般都是阳离子表面活性剂, 也包括脂肪胺),吸附在固体矿粉的表面。这种吸附随矿物性质的 不同而有一定的选择性。其基本原理是利用晶体表面的晶格缺陷。 而向外的憎水端部分地插入气泡内。这样在浮选过程中气泡就 可把指定的矿粉带走,达到选矿的目的。
2.4 生物表面活性剂:利用微生物在一定条件下,将某些 物质转化为具表面活性剂特性的代谢物.
▪ 如:海藻糖脂,磷脂类,鼠李糖,蛋白脂-多糖聚合物
3、特征、结构与性质 3.1 特征 ①两亲性:亲水亲油性 ②溶解性:溶于液相中的某一相
第6页,此课件共47页哦
③界面吸附:达到平衡时,其在界面上的浓度要大 于其作为溶质在溶液整体中的浓度
N a O HC H 81 7
C H S -O H 3
C H 71 5
C H S -O N 3a
7.1.2.4 α-烯烃磺酸盐-AOS
第一步:
+ R-CH2-CH2 CH=CH2 SO3
第二步:
R-CH2=CHCH2 CH2SO3 H 含量42%
R-CH2-CH-CH2 CH2 1, 3烷 烃 磺酸 内酯
3.2 结构及性质 ①不对称结构:亲水亲油基团一般分处两端,
使其一部分可溶于水而另一部分易自水中逃 逸。 ②疏水基团:脱离水包围的趋势,自身互相靠 近并聚集,致使其在水溶液表面上吸附,并 在溶液内部形成胶束。 ③表面张力γ与lgC:作图可确定CMC
第8页,此课件共47页哦
γ
( 表 面 张 力 )
▪ 至少涉及气、液、固三相。
▪ 首先是采用能大量起泡的表面起泡剂。 ▪ 当在水中通人空气或由于水的搅动引起空气进入水中时,表面活
性剂的憎水端在气—液界面向气泡的空气一方定向, 亲水端 仍在溶液内,形成了气泡。
▪ 另一种起捕集作用的表面活性剂(一般都是阳离子表面活性剂, 也包括脂肪胺),吸附在固体矿粉的表面。这种吸附随矿物性质的 不同而有一定的选择性。其基本原理是利用晶体表面的晶格缺陷。 而向外的憎水端部分地插入气泡内。这样在浮选过程中气泡就 可把指定的矿粉带走,达到选矿的目的。
表面活性剂ppt课件教学教程

消泡剂(antifoaming agent):在稳定的泡沫中加入一 些HLB值为1~3的表面活性剂使泡沫破坏。
Surfactant
去污作用(HLB值为13~16)
➢ 油酸钠和脂肪酸的钠盐、钾盐、十二烷基硫酸钠或烷基 磺酸钠等阴离子性表面活性剂。
➢ 机理:包括对污物表面的润湿、分散、乳化或增溶、起 泡等多种过程。
➢ 溶液的性质如渗透压、界面
张力等都存在突变现象
胶态电解质溶液—十二烷 基硫酸钠的性质
临界胶束浓度的测定
表
摩
面 张
尔 电 导
力
率
浓度
庚基乙二醇十二烷基醚的 表面张力与浓度的关系
浓度
十二烷基磺酸钠水溶液 的电导率与浓度的关系
Surfactant
2 亲水亲油平衡值 HLB
Hydrophile-lipophile balance 定义:表面活性剂分子中亲水和亲油基团对水或油 的综合亲和力 HLB值范围 :O~40 非离子型混合表面活性剂的HLB值: HLB值的理论计算 HLB=∑(亲水基团HLB数)-∑(亲油基团HLB数)+7
剂、乳化剂、分散剂和润湿剂、常与司盘配伍 。
CR
Surfactant
聚氧乙烯脂肪酸酯(商品名:卖泽Myrij)
通式:R.COO.CH2(CH2OCH2)nCH2OH
聚 特点:较强水溶性、增溶剂、用作O/W型乳化
氧 乙
剂和栓剂的基质。
烯 常用:polyoxyl 40 stearate。
型
聚氧乙烯脂肪醇醚(商品名:苄泽Brij)
剂
高分子表面活性剂
Surfactant
1•代离表子:硫表酸面化蓖活麻性油(剂土耳其红油);SDS 。
Surfactant
去污作用(HLB值为13~16)
➢ 油酸钠和脂肪酸的钠盐、钾盐、十二烷基硫酸钠或烷基 磺酸钠等阴离子性表面活性剂。
➢ 机理:包括对污物表面的润湿、分散、乳化或增溶、起 泡等多种过程。
➢ 溶液的性质如渗透压、界面
张力等都存在突变现象
胶态电解质溶液—十二烷 基硫酸钠的性质
临界胶束浓度的测定
表
摩
面 张
尔 电 导
力
率
浓度
庚基乙二醇十二烷基醚的 表面张力与浓度的关系
浓度
十二烷基磺酸钠水溶液 的电导率与浓度的关系
Surfactant
2 亲水亲油平衡值 HLB
Hydrophile-lipophile balance 定义:表面活性剂分子中亲水和亲油基团对水或油 的综合亲和力 HLB值范围 :O~40 非离子型混合表面活性剂的HLB值: HLB值的理论计算 HLB=∑(亲水基团HLB数)-∑(亲油基团HLB数)+7
剂、乳化剂、分散剂和润湿剂、常与司盘配伍 。
CR
Surfactant
聚氧乙烯脂肪酸酯(商品名:卖泽Myrij)
通式:R.COO.CH2(CH2OCH2)nCH2OH
聚 特点:较强水溶性、增溶剂、用作O/W型乳化
氧 乙
剂和栓剂的基质。
烯 常用:polyoxyl 40 stearate。
型
聚氧乙烯脂肪醇醚(商品名:苄泽Brij)
剂
高分子表面活性剂
Surfactant
1•代离表子:硫表酸面化蓖活麻性油(剂土耳其红油);SDS 。
第二章 表面活性剂的作用原理课件

也是增加单位表面积时所必须对系统做的功,单位
J/m2
Chapter Two
10
表面张力
从力的角度:作用于表面单位长度边
缘的力; 从能量角度:单位表面的表面自由能
Chapter Two
11
表面张力测定方法
滴重法:精确简便 毛细管上升法:精确度高,最常用 环法 吊片法 最大气泡压力法 滴外形法:表面吸附速率很慢的溶液
第二章 表面活性剂的作用原理
Chapter Two
1
基本内容
2.1 2.2 2.3
表面张力与表面活性 表面活性剂胶束 表面活性剂结构与性能的关系
Chapter Two
2
2.1 表面张力与表面活性
当任意两相接触时,两相之间是一个具 有相当厚度的过渡区,这一过渡区通常 称之为界面。
若其中一相为气体,这种界面通常称为表面。 但由于历史的原因, 这两个概念常常混用。
37
胶束的结构
胶束的基本结构分为两部分:内核和外层, 在水溶液中,胶团的内核由彼此结合的疏 水基构成,形成胶团水溶液中的非极性微 区。胶团内核与溶液间为水化的表面活性 剂极性基构成的外层。
a.离子型表面活性剂胶束; b.非离子型表面活性剂胶束 Chapter Two
38
胶束的结构
对离子型表面活性剂, 胶束内核由疏水的碳氢 链构成,双电层最内层 不仅包含极性头,还固 定一部分与极性头结合 的反离子和不足以铺满 一单分子层的水化层; 离子胶束有一反离子扩 散层,即双电层外围的 扩散层部分。
0 -纯溶剂的表面张力;
cmc -溶液在cmc时的表面张力。
34
Chapter Two
34
《表面活性剂》课件
阳离子表面活性剂的缺点是价格较高,洗涤性能较差。
5.3 非离子表面活性剂
非离子表面活性剂在水溶液中不电离,其亲水基 主要是由具有一定数量的含氧基团(一般为醚基和 羟基)构成。正是这一特点决定了非离子表面活性 剂在某些方面比离子型表面活性剂优越:因为在溶 液中不是离子状态,所以稳定性高,不易受强电解 质无机盐类存在的影响,也不易受酸、碱的影响; 与其它类型表面活性剂的相容性好,能很好地混合 使用;在水及有机溶剂中皆有较好的溶解性能(视 结构不同而有所差别)。由于在溶液中不电离,故 在一般固体表面上亦不易发生强烈吸附。
同构成的。而且两部分分处两端,形成不对称的结
构。是一种两亲分子如:C12H25SO4- Na+ (OC2H4)6OH
C12H25
这种分子就会在水中采取采取独特的定向排列,这
种情况发生于表面活性剂溶液体系,即表现为两种
主要的基本性质:溶液表面的吸附与溶液内部的胶
团形成。
第 五 章 表面活性剂的分类和化学结构
现时采用“磺氧化”的合成方法:
经工艺等各方面的改进,产品质量大大提高,消 除前法的缺点,不需用氯气,副产物减少,纯 化操作工艺大大简化,成本降低;而且此种表 面活性剂毒性较小,易于生物降解。因此,近 年来生产上有所发展,产量逐渐增加。
活性的化合物,R的碳原子数为4—8。二辛酯(2-乙 基已酯)化合物可溶于水及有机溶剂(包括烃类), 故可用于干洗溶剂中。此类表面活性剂水溶液的表 面张力较低,故为良好的润湿剂。
表面活性剂
第四章 绪 论
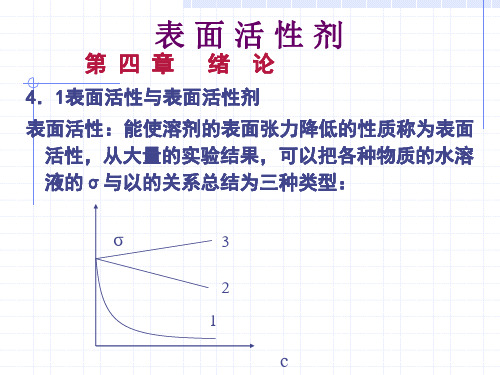
4.1表面活性与表面活性剂
表面活性:能使溶剂的表面张力降低的性质称为表面 活性,从大量的实验结果,可以把各种物质的水溶 液的σ与以的关系总结,洗涤剂等物有曲线1的性质;乙醇、乙酸、丁 醇等物的水溶液有曲线2的性质;NaCl、KNO3、HCl、 NaOH等无机物的水溶液则有曲线3的性质。
5.3 非离子表面活性剂
非离子表面活性剂在水溶液中不电离,其亲水基 主要是由具有一定数量的含氧基团(一般为醚基和 羟基)构成。正是这一特点决定了非离子表面活性 剂在某些方面比离子型表面活性剂优越:因为在溶 液中不是离子状态,所以稳定性高,不易受强电解 质无机盐类存在的影响,也不易受酸、碱的影响; 与其它类型表面活性剂的相容性好,能很好地混合 使用;在水及有机溶剂中皆有较好的溶解性能(视 结构不同而有所差别)。由于在溶液中不电离,故 在一般固体表面上亦不易发生强烈吸附。
同构成的。而且两部分分处两端,形成不对称的结
构。是一种两亲分子如:C12H25SO4- Na+ (OC2H4)6OH
C12H25
这种分子就会在水中采取采取独特的定向排列,这
种情况发生于表面活性剂溶液体系,即表现为两种
主要的基本性质:溶液表面的吸附与溶液内部的胶
团形成。
第 五 章 表面活性剂的分类和化学结构
现时采用“磺氧化”的合成方法:
经工艺等各方面的改进,产品质量大大提高,消 除前法的缺点,不需用氯气,副产物减少,纯 化操作工艺大大简化,成本降低;而且此种表 面活性剂毒性较小,易于生物降解。因此,近 年来生产上有所发展,产量逐渐增加。
活性的化合物,R的碳原子数为4—8。二辛酯(2-乙 基已酯)化合物可溶于水及有机溶剂(包括烃类), 故可用于干洗溶剂中。此类表面活性剂水溶液的表 面张力较低,故为良好的润湿剂。
表面活性剂
第四章 绪 论
4.1表面活性与表面活性剂
表面活性:能使溶剂的表面张力降低的性质称为表面 活性,从大量的实验结果,可以把各种物质的水溶 液的σ与以的关系总结,洗涤剂等物有曲线1的性质;乙醇、乙酸、丁 醇等物的水溶液有曲线2的性质;NaCl、KNO3、HCl、 NaOH等无机物的水溶液则有曲线3的性质。
第三章-表面活性剂PPT课件

7)阴离子表面活性剂是家用洗涤剂、工业 洗涤剂、干洗剂和润湿剂的重要成分。
2021
8
3.2.1 阴离子表面活性剂
分类
1、肥皂类
系高级脂肪酸的盐,通式: (RCOOˉ)n M。脂肪酸烃R一 般为11~17个碳 的长链,常见有硬脂酸、油酸、月桂酸。 根据M代表的物质不同,又可分为碱金属皂、碱土金属皂 和有机胺皂。它们均有良好的乳化性能和分散油的能力。 但易被破坏,碱金属皂还可被钙、镁盐破坏,电解质亦可 使之盐析。
胶束聚集数增大
形成新的胶团
临界胶束浓度:表面活性剂分子缔合形成胶束的最低浓度
0.002%-0.5% (0.0001mol/L-0.02mol/L)
2021
20
3.4 临界胶束浓度
2021
21
3.4 临界胶束浓度
CMC是表面活性剂表面活性的一种度量。 形成胶束所需要的浓度愈低;
CMC愈小
达到表面饱和吸附的浓度愈低; 使表面张力降到最低值所需浓度愈低;
2021
阴离子型
RCOONa
R洗SO涤3N、a R去OS污O3性Na
好
ROPO3Na
4
3.2.1 阴离子表面活性剂
起作用的部分是阴离子
特性
1)溶解度随温度的变化存在明显的转折点,即 在较低的一段温度范围内溶解度随温度上升非常 缓慢,当温度上升到某一定值时溶解度随温度上 升而迅速增大,这个温度叫做表面活性剂的克拉 夫点(Krafft point)。一般离子型表面活性剂 都有Krafft点。
②如果表面活性剂的疏水基相同,亲水基使cmc增大的顺序是:
离子型
C O O ->S O 3 ->O S O 3 -
非离子型 聚氧乙烯单元数目增大,cmc略有增大。
2021
8
3.2.1 阴离子表面活性剂
分类
1、肥皂类
系高级脂肪酸的盐,通式: (RCOOˉ)n M。脂肪酸烃R一 般为11~17个碳 的长链,常见有硬脂酸、油酸、月桂酸。 根据M代表的物质不同,又可分为碱金属皂、碱土金属皂 和有机胺皂。它们均有良好的乳化性能和分散油的能力。 但易被破坏,碱金属皂还可被钙、镁盐破坏,电解质亦可 使之盐析。
胶束聚集数增大
形成新的胶团
临界胶束浓度:表面活性剂分子缔合形成胶束的最低浓度
0.002%-0.5% (0.0001mol/L-0.02mol/L)
2021
20
3.4 临界胶束浓度
2021
21
3.4 临界胶束浓度
CMC是表面活性剂表面活性的一种度量。 形成胶束所需要的浓度愈低;
CMC愈小
达到表面饱和吸附的浓度愈低; 使表面张力降到最低值所需浓度愈低;
2021
阴离子型
RCOONa
R洗SO涤3N、a R去OS污O3性Na
好
ROPO3Na
4
3.2.1 阴离子表面活性剂
起作用的部分是阴离子
特性
1)溶解度随温度的变化存在明显的转折点,即 在较低的一段温度范围内溶解度随温度上升非常 缓慢,当温度上升到某一定值时溶解度随温度上 升而迅速增大,这个温度叫做表面活性剂的克拉 夫点(Krafft point)。一般离子型表面活性剂 都有Krafft点。
②如果表面活性剂的疏水基相同,亲水基使cmc增大的顺序是:
离子型
C O O ->S O 3 ->O S O 3 -
非离子型 聚氧乙烯单元数目增大,cmc略有增大。
表面活性剂原理课件

d ,或简称表面自由能或 ⊿d 表面能,用符号γ表示
,单位为J·m-2。
液体表面张力
f 2l
G ( A)p,T
,nB
J=N·m,J/m2= N/m
γ 从力的角度是作用于单位长度上的力,叫表 面张力.
f 2l
从能量的角度是单位表面的表面自由能,是 增加单位表面积液体时自由能的增值,也就是 单位表面上的液体分子比处于液体内部的同 量分子的自由能过剩值.
水溶液的表面张力与溶 质浓度的几种典型关系
表面活性剂的结构特点
表面活性剂是如何降低表面张力的呢?
亲油基
亲水基
表面活性剂的结构特点
a
b
c
表2.1 常见液体的表面张力
表面活性与表面活性剂
1无机盐和蔗糖等多 羟基化合物。
这些物质的离子有水合 作用,趋向于把水分子拖 入水中,非表面活性物质 在表面的浓度低于在本体 的浓度。
胶束(Micelle)的结构
离子型表面活性剂的胶束结构示意图
疏水内核:疏水的碳氢链 极性基层:表面活性剂的极性基团、反离子、水化层 反离子扩散层:反离子在溶剂中的扩散层
斯特恩(stern)双电层理论 特点:扩散反离子在溶液中的分布为紧密层和分散层。
斯特恩(stern)双电层模型
胶束(Micelle)的结构
量形成胶束的浓度,是表
面活性剂主要的性能参数。
当表面活性剂的浓度到达C
MC后,溶液的各种性能发
生明显的变化。
表面活性剂的表面张力浓度-曲线
洗涤作用 高频电导 密度
与温度有关:温度升高, 值减小。当液体沸腾时表 面张力系数为零。
与液体内所含杂质有关:在液体内加入杂质,液体的 表面张力系数将显著改变,有的使其值增加;有的 使其值减小。使值减小的物质称为表面活性物质。
,单位为J·m-2。
液体表面张力
f 2l
G ( A)p,T
,nB
J=N·m,J/m2= N/m
γ 从力的角度是作用于单位长度上的力,叫表 面张力.
f 2l
从能量的角度是单位表面的表面自由能,是 增加单位表面积液体时自由能的增值,也就是 单位表面上的液体分子比处于液体内部的同 量分子的自由能过剩值.
水溶液的表面张力与溶 质浓度的几种典型关系
表面活性剂的结构特点
表面活性剂是如何降低表面张力的呢?
亲油基
亲水基
表面活性剂的结构特点
a
b
c
表2.1 常见液体的表面张力
表面活性与表面活性剂
1无机盐和蔗糖等多 羟基化合物。
这些物质的离子有水合 作用,趋向于把水分子拖 入水中,非表面活性物质 在表面的浓度低于在本体 的浓度。
胶束(Micelle)的结构
离子型表面活性剂的胶束结构示意图
疏水内核:疏水的碳氢链 极性基层:表面活性剂的极性基团、反离子、水化层 反离子扩散层:反离子在溶剂中的扩散层
斯特恩(stern)双电层理论 特点:扩散反离子在溶液中的分布为紧密层和分散层。
斯特恩(stern)双电层模型
胶束(Micelle)的结构
量形成胶束的浓度,是表
面活性剂主要的性能参数。
当表面活性剂的浓度到达C
MC后,溶液的各种性能发
生明显的变化。
表面活性剂的表面张力浓度-曲线
洗涤作用 高频电导 密度
与温度有关:温度升高, 值减小。当液体沸腾时表 面张力系数为零。
与液体内所含杂质有关:在液体内加入杂质,液体的 表面张力系数将显著改变,有的使其值增加;有的 使其值减小。使值减小的物质称为表面活性物质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• 表面张力:液体的表面层中有一种使液面尽可能收缩 成最小的宏观张力。
学习交流PPT
15
表面张力产生的微观本质 • 分子力观点:
• 表面张力是由于液体表面层内分子间相互作用与液体内部分子间相互作用不 同。
• 分子力:在液体內部的分子之间,彼此互相吸引力,忽略了斥力;
• 分子作用球(约10-8 m) :在液体内部P点任取一分子A ,以A为球心,以分子有 效作用距离为半径作一球,称为分子作用球 。球外分子对A 无作用力,球内 分子对A 的作用力对称分布,合力为零。
与液体内所含杂质有关:在液体内加入杂质,液体的 表面张力系数将显著改变,有的使其值增加;有的 使其值减小。使值减小的物质称为表面活性物质。
学习交流PPT
23
影响表面张力系数的因素
学习交流PPT
24
表面张力的测定方法
滴重法(滴体积法)
W2r f
学习交流PPT
25
❖ 毛细管上升法
将一洁净的半径为 r 的均匀 毛细管插入能润湿该毛细管的 液体中,则由于表面张力所引 起的附加压力, 将使液柱上 升,达平衡时,附加压力与液 柱所形成的压力大小相等,方 向相反:
2
行凌 走波 在微 水步 面: 上为 ?什
么 蜥 蜴 能
学习交流PPT
3
学习交流PPT
形的? 荷叶上的 露 珠 为 什 么 是 球
4
学习交流PPT
会既水
浸不黾
湿会的
自划 己破
高
的水明
腿面之
,处
也 不
:
5
学习交流PPT
珠为 是什 圆么 形蜘 的蛛 ?网
上 的
水
6
一枚硬币上可承受几滴水?
学习交流PPT
第二章 表面活性剂的作用原理
2.1表面张力与表面活性 2.2表面活性剂胶束 2.3表面活性剂结构与性能的关系
学习交流PPT
1
有趣的现象
2007年11月23日,英国伦敦博物馆,Sam Heath(右
),又被称为泡泡人Sam,用一个巨大的肥皂泡将50名
学生罩起来:为什么肥皂学膜习交能流PP被T 拉的很大而不破裂?
学习交流PPT
19
γ 从力的角度是作用于单位长度上的力,叫表 面张力.
f 2l
从能量的角度是单位表面的表面自由能,是 增加单位表面积液体时自由能的增值,也就是 单位表面上的液体分子比处于液体内部的同 量分子的自由能过剩值.
(GA) 学习交流PPT
p,T,nB
20
表2.1 常见液体的表面张力
学习交流PPT
• 发现液体表面存在张力,且方向在液面内 。
学习交流PPT
10
为什么液体表面会形成一张有弹性的膜?
作用在液体表面,使液体表面收缩到最小面 积的力,叫做「液体表面张力 」。
生活中,许多 地方都有它!
学习交流PPT
11
2.1 表面张力和表面活性
界面与表面的概念 表面:液体或固体与气体的接触面称为液 体或固体的表面。 界面:液-液、固-固和液-固的接触面称为 界面。
在宏观上就表现为学液习交体流P表PT 面有收缩的趋势
16
表面张力产生的微观本质
• 从能量观点来分析
力把作分功子,从分液子体势内能部增移加到,即表表面面层层,内需分克子服的f势⊥ 能作比功液;外
体内部分子的势能大,表面层为高势能区; 表面层内,各个分子势能增量的总和称为液体的表
面能,用E 表示。
任何系统的势能越小越稳定,所以表面层内的分子 有尽量挤入液体内部的趋势,即液面有收缩的趋势, 使液面呈紧张状态,宏观上就表2.2 一些液液体系的界面张力
液液界面的 界面张力小
学习交流PPT
22
影响表面张力系数的因素
与液体的性质有关:不同液体, 值不同;密度小、 易挥发的液体值较小。如:酒精、乙醚的值很小,金 属熔化后的值很大。
与相邻物质化学性质有关:同一液体与不同物质交界 , 值不同。
与温度有关:温度升高, 值减小。当液体沸腾时表 面张力系数为零。
• 从表面层中Q、R、S点任取一分子,其分子作用球一部分在液体外,空气密 度比水小,破坏了表面层的分子受力的球对称性;
• 其受合力与液面垂直,指向液体内部,这使得表面层内的分子与液体内部的
分子不同,都受一个指向液体内部的合力 f • 越的靠趋近势表。面,受到的f越大;在f作用下,液体表面的分子有被拉进液体内部
体积一定, 球体的表面积最小;
学习交流PPT
17
2.1.1表面张力与表面自由能
空气
m
m′
液体
液体内部和表面分子的受力情况
在两相(特别是气-液)界面上,处处存在着一种张力,它垂
直于表面的边界,指向液体方向并与液面相切。把作用于单位边
界线上的这种力称为表面张力,用γ表示,单位是N/m,通常为
mN/m 。
rro f 0 引力起主要作用
rR f 0 R—分子有效作用半径 108 m
分子力是短程力!
学习交流PPT
14
液体的表面张力
• 现象:液体表面有收缩到最小的趋势 液面像紧绷的弹性薄膜。
• 说明:液面上存在沿表面的收缩力作用,这种力只存 在于液体表面。
• 表面层:在液体与气体交界面,厚度等于分子有效作 用距离(=10-8 m) 的一层液体。
7
结论:水面是一张有弹性的膜
提问:为什么液体表面会形成一张有弹性的膜?
学习交流PPT
8
为什么液体表面会形成一张有弹性的膜?
• 圆形金属框上沾有肥皂泡沫,若将膜面上的棉线圈内部 的膜戳破,那么棉线圈将被拉成圆形;
学习交流PPT
9
为什么液体表面会形成一张有弹性的膜?
• 把系有棉线的铁环放入肥皂水中,拿出时,铁 环上布满一层肥皂膜。刺破一侧肥皂膜,另一 侧肥皂膜收缩,棉线向该侧完成弧形 。
学习交流PPT
12
液体表面张力产生的原因
1.汽
1.表面层
• 表面层是一个厚 度大概为10-9m 的薄层,液体分
子间距比较大。
1.液体
液体表面微观图
学习交流PPT
13
分子间既有引力作用 又有斥力作用
rro
rro
v12
f
斥力
f 0 平衡位置
d
o•
r0
f 0 斥力起主要作用 引力
v12=0
r
R
r
d
d 分子有效直径 1010m
1Rghr
2 3
学习交流PPT
学习交流PPT
18
2.1.1表面张力与表面自由能
a
c l
b
保持温度、压力和组成
不变,每增加单位表面积
时,Gibbs自由能的增加值
称为表面Gibbs自由能,
或简称表面自由能或表面 d 能,用符号γ表示,单位
⊿d 为J·m-2。
f
液体表面张力
f 2l
G ( A)p,T,nB
J=N·m,J/m2= N/m
学习交流PPT
15
表面张力产生的微观本质 • 分子力观点:
• 表面张力是由于液体表面层内分子间相互作用与液体内部分子间相互作用不 同。
• 分子力:在液体內部的分子之间,彼此互相吸引力,忽略了斥力;
• 分子作用球(约10-8 m) :在液体内部P点任取一分子A ,以A为球心,以分子有 效作用距离为半径作一球,称为分子作用球 。球外分子对A 无作用力,球内 分子对A 的作用力对称分布,合力为零。
与液体内所含杂质有关:在液体内加入杂质,液体的 表面张力系数将显著改变,有的使其值增加;有的 使其值减小。使值减小的物质称为表面活性物质。
学习交流PPT
23
影响表面张力系数的因素
学习交流PPT
24
表面张力的测定方法
滴重法(滴体积法)
W2r f
学习交流PPT
25
❖ 毛细管上升法
将一洁净的半径为 r 的均匀 毛细管插入能润湿该毛细管的 液体中,则由于表面张力所引 起的附加压力, 将使液柱上 升,达平衡时,附加压力与液 柱所形成的压力大小相等,方 向相反:
2
行凌 走波 在微 水步 面: 上为 ?什
么 蜥 蜴 能
学习交流PPT
3
学习交流PPT
形的? 荷叶上的 露 珠 为 什 么 是 球
4
学习交流PPT
会既水
浸不黾
湿会的
自划 己破
高
的水明
腿面之
,处
也 不
:
5
学习交流PPT
珠为 是什 圆么 形蜘 的蛛 ?网
上 的
水
6
一枚硬币上可承受几滴水?
学习交流PPT
第二章 表面活性剂的作用原理
2.1表面张力与表面活性 2.2表面活性剂胶束 2.3表面活性剂结构与性能的关系
学习交流PPT
1
有趣的现象
2007年11月23日,英国伦敦博物馆,Sam Heath(右
),又被称为泡泡人Sam,用一个巨大的肥皂泡将50名
学生罩起来:为什么肥皂学膜习交能流PP被T 拉的很大而不破裂?
学习交流PPT
19
γ 从力的角度是作用于单位长度上的力,叫表 面张力.
f 2l
从能量的角度是单位表面的表面自由能,是 增加单位表面积液体时自由能的增值,也就是 单位表面上的液体分子比处于液体内部的同 量分子的自由能过剩值.
(GA) 学习交流PPT
p,T,nB
20
表2.1 常见液体的表面张力
学习交流PPT
• 发现液体表面存在张力,且方向在液面内 。
学习交流PPT
10
为什么液体表面会形成一张有弹性的膜?
作用在液体表面,使液体表面收缩到最小面 积的力,叫做「液体表面张力 」。
生活中,许多 地方都有它!
学习交流PPT
11
2.1 表面张力和表面活性
界面与表面的概念 表面:液体或固体与气体的接触面称为液 体或固体的表面。 界面:液-液、固-固和液-固的接触面称为 界面。
在宏观上就表现为学液习交体流P表PT 面有收缩的趋势
16
表面张力产生的微观本质
• 从能量观点来分析
力把作分功子,从分液子体势内能部增移加到,即表表面面层层,内需分克子服的f势⊥ 能作比功液;外
体内部分子的势能大,表面层为高势能区; 表面层内,各个分子势能增量的总和称为液体的表
面能,用E 表示。
任何系统的势能越小越稳定,所以表面层内的分子 有尽量挤入液体内部的趋势,即液面有收缩的趋势, 使液面呈紧张状态,宏观上就表2.2 一些液液体系的界面张力
液液界面的 界面张力小
学习交流PPT
22
影响表面张力系数的因素
与液体的性质有关:不同液体, 值不同;密度小、 易挥发的液体值较小。如:酒精、乙醚的值很小,金 属熔化后的值很大。
与相邻物质化学性质有关:同一液体与不同物质交界 , 值不同。
与温度有关:温度升高, 值减小。当液体沸腾时表 面张力系数为零。
• 从表面层中Q、R、S点任取一分子,其分子作用球一部分在液体外,空气密 度比水小,破坏了表面层的分子受力的球对称性;
• 其受合力与液面垂直,指向液体内部,这使得表面层内的分子与液体内部的
分子不同,都受一个指向液体内部的合力 f • 越的靠趋近势表。面,受到的f越大;在f作用下,液体表面的分子有被拉进液体内部
体积一定, 球体的表面积最小;
学习交流PPT
17
2.1.1表面张力与表面自由能
空气
m
m′
液体
液体内部和表面分子的受力情况
在两相(特别是气-液)界面上,处处存在着一种张力,它垂
直于表面的边界,指向液体方向并与液面相切。把作用于单位边
界线上的这种力称为表面张力,用γ表示,单位是N/m,通常为
mN/m 。
rro f 0 引力起主要作用
rR f 0 R—分子有效作用半径 108 m
分子力是短程力!
学习交流PPT
14
液体的表面张力
• 现象:液体表面有收缩到最小的趋势 液面像紧绷的弹性薄膜。
• 说明:液面上存在沿表面的收缩力作用,这种力只存 在于液体表面。
• 表面层:在液体与气体交界面,厚度等于分子有效作 用距离(=10-8 m) 的一层液体。
7
结论:水面是一张有弹性的膜
提问:为什么液体表面会形成一张有弹性的膜?
学习交流PPT
8
为什么液体表面会形成一张有弹性的膜?
• 圆形金属框上沾有肥皂泡沫,若将膜面上的棉线圈内部 的膜戳破,那么棉线圈将被拉成圆形;
学习交流PPT
9
为什么液体表面会形成一张有弹性的膜?
• 把系有棉线的铁环放入肥皂水中,拿出时,铁 环上布满一层肥皂膜。刺破一侧肥皂膜,另一 侧肥皂膜收缩,棉线向该侧完成弧形 。
学习交流PPT
12
液体表面张力产生的原因
1.汽
1.表面层
• 表面层是一个厚 度大概为10-9m 的薄层,液体分
子间距比较大。
1.液体
液体表面微观图
学习交流PPT
13
分子间既有引力作用 又有斥力作用
rro
rro
v12
f
斥力
f 0 平衡位置
d
o•
r0
f 0 斥力起主要作用 引力
v12=0
r
R
r
d
d 分子有效直径 1010m
1Rghr
2 3
学习交流PPT
学习交流PPT
18
2.1.1表面张力与表面自由能
a
c l
b
保持温度、压力和组成
不变,每增加单位表面积
时,Gibbs自由能的增加值
称为表面Gibbs自由能,
或简称表面自由能或表面 d 能,用符号γ表示,单位
⊿d 为J·m-2。
f
液体表面张力
f 2l
G ( A)p,T,nB
J=N·m,J/m2= N/m
