霉菌酵母菌检验.
霉菌和酵母菌的鉴定方法(2016.10.12)
霉菌酵母菌计数常用的培养基是孟加拉红(虎红),其中加入了一定量的氯霉素可有有效地抑制绝大多数细菌菌落的生长。但是由于一些难以预计的因素,例如培基的质量等。在孟加拉红培基上也可能生长出细菌菌落来,有时候未凸出琼脂表面的霉菌菌落也不太好判断。前面有很多网友以及在培训中碰到的许多学员都有问到这个问题。马群飞老师也曾做过专门的介绍鉴别的方法。我在马老师的基础上,专门针对这一问题做了一些比较性的实验。希望大家看了之后能有所收获。
可见明显的菌丝体
(三)染色法
挑取菌落用亚甲基蓝或革兰氏染色,酵母菌或霉菌在低倍镜下即可见到孢子或菌丝,而细菌不可见。
若是肉眼观察菌落形态还无法判断的话可以采用马老介绍的方法用普通光学显微镜观察菌落的边缘较薄较透光的部分。观察是否菌落
霉菌菌落
边缘交规整,调节聚焦螺旋可见到细腻如细沙的结构。若无法确认可用接种从边缘稍稍刮开菌落,即可在镜下见到卵圆形的孢子。
菌落紧密,边缘整齐,不易透光,几乎看不到细沙粒样的结构
(一)观察菌落特征
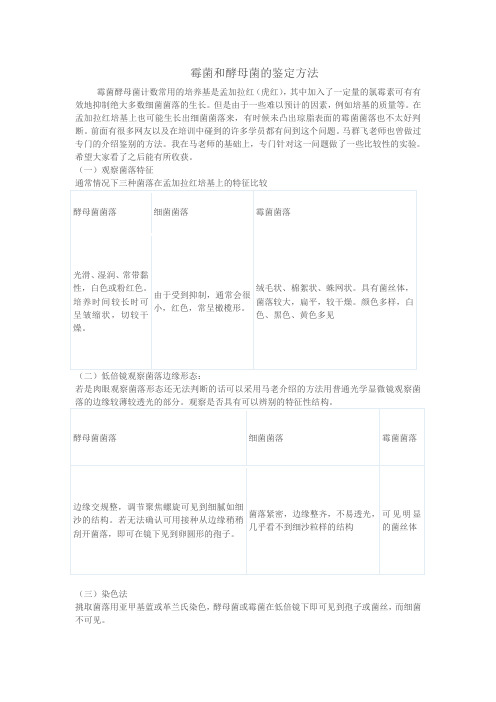
通常情况下三种菌落在孟加拉红培基上的特征比较
酵母菌菌落
细菌菌落
霉菌菌落
光滑、湿润、常带黏性,白色或粉红色。
培养时间较长时可呈皱缩状,切较干燥。
由于受到抑制,通常会很小,红色,常呈橄榄形。
绒毛状、棉絮状、蛛网状。具有菌丝体,菌落较大,扁平,较干燥。颜色多样,白色、黑色、黄色多见
(二)低倍镜观察菌落边缘形态:
9.5.1食品霉菌酵母菌测定

谢谢观看
目录/Contents
01 霉菌、酵母菌的定义 02 检验程序 03 操作步骤 04 结果与报告 05 实验后整理
霉菌、酵母菌的定义
什么是食品中的霉菌、酵母菌菌落数?
食品检样经过处理,在一定条件下培养后(这个条件如培养基、 培养温度、培养时间),所得每g(mL)检样中形成的霉菌、酵 母菌菌落数。
霉菌、酵母菌的检验程序
位数字,后面用0代替位数;也可用10的指数形式来表示,按“四舍五入”原则 修约后,采用两位有效数字。 3 若空白对照上有菌落生长,则此次检测结果无效。
4 称重取样以CFU/g为单位报告,体积取样以CFU/mL为单位报告。
实验后整理
实验后整理
将使用过的所有玻璃器皿按要求清洗干净,沥干水后放回原 处。将操作台清理干净。
霉菌、酵母作步骤
3 菌落计数
取菌落数在10~ 150CFU之间平板 霉菌蔓延生长 ( 覆 盖整个平板的 ) 可 记录为菌落蔓延。 菌落数应采用两个 平板的平均数。
霉菌、酵母菌的结果与报告
结果
1 若只有一个稀释度平板上的菌落数在适宜计数范围内,计算两个平板菌落数的平 均值,再将平均值乘以相应稀释倍数,作为每g(mL)样品中霉菌、酵母菌结果。
5 若所有稀释度(包括液体样品原液)平板均无菌落生 长,则以小于1乘以最低稀释倍数计算。
6 若所有稀释度的平板菌落数均不在10~150CFU之间, 其中一部分小于10 CFU或大于150CFU时,则以最接 近10或150CFU的平均菌落数乘以稀释倍数计算。
霉菌、酵母菌的结果与报告
报告
1 菌落数小于100 CFU时,按“四舍五入”原则修约,以整数报告。 2 菌落数大于或等于100CFU时,第3位数字采用“四舍五入”原则修约后,取前2
国标食品微生物学检验 霉菌酵母菌计数

1、检验食品中的霉菌、酵母菌有何意义?试举例食品中产毒素的霉菌、酵母菌?酵母菌是人类较早应用于制作面包、酿酒等的一类微生物。
近年来的应用越来越广,酵母菌体可供食用和作饲料,并可提取核酸、辅酶A、细胞色素C、凝血质等贵重药品;利用其代谢产物,制取维生素、有机酸和酶制剂等;同时,也可用于石油发酵和石油脱蜡等;霉菌除用于传统的酿酒、制酱和做其他发酵食品外,近年来在发酵工业中广泛用来生产酒精、柠檬酸、青霉素、灰黄霉素、赤霉素、淀粉酶、发酵饲料等。
腐生型酵母能使食物、纺织品和其他原料腐败变质;少数嗜高渗压酵母菌如鲁氏酵母、蜂蜜酵母可使蜂蜜、果酱败坏;有的是发酵工业的污染菌,它们消耗酒精,降低产量或产生不良气味,影响产品质量。
面包内含有淀粉,容易滋生霉菌,霉菌会分解淀粉,产生有毒黄曲霉素,是强致癌物质。
根霉经常出现在淀粉质食品上,引起食品霉烂变质,有些曲霉菌能产生对人体有害的物质,如黄曲霉毒素。
2、如何在菌落形态上鉴定霉菌、细菌、酵母菌?细菌:小而突起,大而平坦,透明或半透明,易挑取,粘稠,有臭味,质地均匀菌落正反面或边缘与中央部位颜色一致,圆形菌落,颜色有白色、黄色等。
放线菌:正面有白点而且正背面颜色不同,干燥,小而紧密,与培养基结合牢固(难以挑取),不透明,泥香味,菌落背面有同心圆形纹路。
这点可以和细菌菌落区分。
酵母菌:菌落为淡黄色,光滑,半透明,比细菌菌落大。
霉菌:有菌丝,干燥,大而疏松,有霉味而且透明,菌落大型,肉眼可见许多毛状物,如绒毛状或棉絮状,棕色、青色等,可见黑色的分生孢子群。
菌落最初往往是浅色或白色,当菌落上长出各种颜色的孢子后,由于孢子有不同形状、构造和色素,菌落表面常出现肉眼可见的不同的结构和色泽,如黄、绿、青、黑、橙等各色。
有的霉菌由于产生的色素能扩散到培养基内,使培养基正面和反面显示出不同颜色,故菌落特征也是鉴定霉菌的主要依据之一。
3、该实验只进行霉菌总数的测定而如何进行霉菌的分离与鉴定?(在土壤中,将10-2、10-3各1ml稀释液接于马丁氏培养基)一、配制培养基(根据试剂瓶上的配比)每个培养皿装15~20ml,有7个培养皿,每组近似配150ml(20*7=140ml取最大范围);二、取两个100或150ml的三角瓶,其中一个用于装90ml的蒸馏水,使用硅胶塞(用于配样品),另一个用于装50~60ml蒸馏水(五根试管,5*9=45ml),用报纸包扎;三、包扎枪头(10个),将培养基放置于一个铁笼子,再将枪头和两瓶水放置于另一个铁笼子,进行湿热灭菌。
霉菌和酵母菌介绍及检测方法

霉菌和酵母菌介绍及检测方法一、霉菌和酵母菌介绍:霉菌和酵母菌及其检验酵母菌是真菌中的一大类,通常是单细胞,呈圆形,卵圆形、腊肠形或杆状。
霉菌也是真菌,能够形成疏松的绒毛状的菌丝体的真菌称为霉菌。
霉菌和酵母广泛分布于自然界并可作为食品中正常菌相的一部分。
长期以来,人们利用某些霉菌和酵母加工一些食品,如用霉菌加工干酪和肉,使其味道鲜美;还可利用霉菌和酵母酿酒、制酱;食品、化学、医药等工业都少不了霉菌和酵母。
但在某些情况下,霉菌和酵母也可造成中腐败变质。
由于它们生长缓慢和竞争能力不强,故常常在不适于细菌生长的食品中出现,这些食品是pH低、湿度低、含盐和含糖高的食品、低温贮藏的食品,含有抗菌素的食品等。
由于霉菌和酵母能抵抗热、冷冻,以及抗菌素和辐照等贮藏及保藏技术,它们能转换某些不利于细菌的物质,而促进致病细菌的生长;有些霉菌能够合成有毒代谢产物-霉菌毒素.霉菌和酵母往往使食品表面失去色、香、味.例如,酵母在新鲜的和加工的食品中繁殖,可使食品发生难闻的异味,它还可以使液体发生混浊,产生气泡,形成薄膜,改变颜色及散发不正常的气味等。
因此霉菌和酵母也作为评价食品卫生质量的指示菌,并以霉菌和酵母计数来制定食品被污染的程度。
目前已有若干个国家制订了某些食品的霉菌和酵母限量标准.我国已制订了一些食品中霉菌和酵母的限量标准。
二、检验方法:霉菌和酵母的计数方法,与菌落总数的测定方法基本相似。
主要步骤为:将样品制作成10倍梯度的稀释液,选择3个合适的稀释度,吸取1mL于平皿,倾注培养基后,培养观察,计数.对霉菌的计数,还可以采用显微镜直接镜检计数的方法。
具体检测标准参见:GB4789.15—94,《中华人民共和国国家标准食品卫生微生物检验霉菌和酵母计数》三、说明:1.样品的处理。
为了准确测定霉菌和酵母数,真实反映被检食品的卫生质量,首先应注意样品的代表性。
对大的固体食品样品,要用灭菌刀或镊子从不同部位采取试验材料,再混合磨碎.如样品不太大,最好把全部样品放到灭菌均质器杯内搅拌2min。
菌落总数、霉菌和酵母菌总数等微生物检验方法

菌落总数、霉菌和酵母菌总数等微生物检验方法下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!一、引言微生物检验是食品行业中非常重要的环节,能够确保食品产品的质量和安全性。
霉菌及其酵母菌

1、样品的稀释培养
(1)以无菌操作将检样25mL(或25g)放于含
有225mL灭菌蒸馏水的三角瓶中,振摇30min,
即为1:10稀释液。
(2)用1mL灭菌吸管吸取1:10稀释液1mL,
沿管壁徐徐注入含有9mL灭菌蒸馏水的试管内,
振摇试管混合均匀,制成1:100的稀释液。
(3)另取1mL灭菌吸管,按上项操作顺序,
制10倍递增稀释液,如此每递增稀释一次即换
用1支1mL灭菌吸管。
(4)根据标准要求或对污染情况的估计,选
择3个适宜稀释度,分别在制10倍递增稀释的
同时,以吸取该稀释度的吸管移取1mL稀释液
于灭菌平皿中,每个稀释度做两个平皿。
及时将15mL~20mL 冷却至46℃的马铃薯-葡 萄糖-琼脂或孟加拉红培养基(可放置于 46℃±1℃恒温水浴箱中保温)倾注平皿,并转 动平皿使其混合均匀。 待琼脂凝固后,将平板倒置,28℃±1℃培养 5d,观察并记录。
制片镜检观察,可见分生孢子梗很粗糙。顶囊 呈烧瓶形或近球形。分生孢子在小梗上呈链状着 生,分生孢子的周围有小突起、球形、粗糙。 制片镜检观察,可见分生孢子梗很粗糙。顶囊呈 烧瓶形或近球形。分生孢子在小梗上呈链状着生 ,分生孢子的周围有小突起、球形、粗糙。
二、黄曲霉毒素检测方法
可归纳为化学方法、生物学方法和免疫学方法 三大类。 1、生物学方法 1. 抑菌试验 通过平皿中抑菌圈大小来衡量AFT含量 2. 荧光测定法 将待检菌株接种于培养基中,28—30 ℃培养48 ~72h,产生的毒素便浸入培养基中,在紫外灯光 下照射培养基会呈现出特异的荧光。此法操作简便 对AFT最低检出量为5pg/mL(拷贝数/毫升)。 3. 动物试验 大白鼠试验法、鸡胚试验、鸭雏试验
霉菌、酵母菌的测定意义

霉菌、酵母菌的测定意义
霉菌和酵母菌是一类微生物,它们在自然界中广泛存在并在人类的生产和生活中扮演着重要的角色。
测定霉菌和酵母菌的数量和种类对于食品、药品、日用化学品、环境卫生等方面具有重大的意义。
首先,在食品加工和储藏过程中,霉菌和酵母菌可能会导致食品变质、腐败和产生毒素,对食品质量和安全造成威胁。
因此,对于食品的生产和贮存过程中进行霉菌和酵母菌的测定是非常必要的,以确保食品的质量和安全。
其次,在药品生产过程中,霉菌和酵母菌的存在可能会导致某些药品降解,影响药品的稳定性和有效性。
因此,在药品生产过程中进行霉菌和酵母菌的测定也是非常必要的。
另外,在日用化学品生产和使用过程中,霉菌和酵母菌也可能会导致产品变质和污染,对人体健康和环境造成危害。
因此,对于日用化学品的生产和使用过程中进行霉菌和酵母菌的测定也是非常重要的。
最后,在环境卫生方面,测定霉菌和酵母菌的数量可以帮助人们了解空气、水体和土壤的微生物污染情况,从而采取相应的措施进行环境治理和保护。
综上所述,测定霉菌和酵母菌的数量和种类对于食品、药品、日用化学品、环境卫生等方面都具有重要的意义,可以保障人们的生命健康和环境的可持续发展。
- 1 -。
牙膏中霉菌和酵母菌总数检验方法

牙膏中霉菌和酵母菌检验方法Molds and Yeasts Count in Toothpaste1范围本规范规定了牙膏中霉菌和酵母菌的检验方法。
本规范适用于牙膏中霉菌和酵母菌的测定。
2定义霉菌和酵母菌数测定Molds and yeasts count牙膏检样经过处理,在一定条件下培养后,1g检样中形成的霉菌和酵母菌总数,藉以判明牙膏被霉菌和酵母菌污染程度及其一般卫生状况。
本方法根据霉菌和酵母菌特有的形态和培养特性,在虎红培养基上,置28℃±2℃培养5d,计算所生长的霉菌和酵母菌数。
3仪器和设备3.1恒温培养箱:28℃±2℃。
3.2振荡器。
3.3三角瓶:250mL。
3.4试管:18mm×150mm。
3.5灭菌平皿:直径90mm。
3.6无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或者移液器及吸头。
3.7量筒:200mL。
3.8酒精灯。
3.9高压灭菌器。
3.10恒温水浴箱。
4培养基和试剂4.1SCDLP液体培养基见总则中3.1。
4.2虎红(孟加拉红)培养基成分:蛋白胨5g葡萄糖10g磷酸二氢钾1g硫酸镁(无水)0.5g琼脂20g1/3000虎红溶液100mL(四氯四碘荧光素)蒸馏水加至1000mL氯霉素100mg制法:将上述各成分(除虎红外)加入蒸馏水中溶解后,再加入虎红溶液。
分装后,121℃高压灭菌20min,另用少量乙醇溶解氯霉素,溶解过滤后加入培养基中,若无氯霉素,使用时每1000mL加链霉素30mg。
5操作步骤5.1样品稀释牙膏样品的稀释分别见牙膏中菌落总数检验方法5.1。
5.2取5.1的样品稀释液各2mL,分别注入2个灭菌平皿内,每皿1mL,注入融化并冷却至44℃~48℃的虎红培养基,充分摇匀。
凝固后,翻转平板,置28℃±2℃培养5d,观察并记录。
同时吸取1mL空白稀释液加入灭菌空平皿中,加入约15mL虎红培养基,待琼脂凝固后,翻转平皿,置28℃±2℃培养箱内培养5d,为空白对照。
项目十八 酵母菌、霉菌检验

项目十八 酵母菌、霉菌检验
项目知识点
1.设备和材料 恒温培养箱 冰箱 恒温振荡器 架盘药物天平0g~500g 显 微镜10×、100×灭菌玻塞三角瓶300mL 灭菌试管 15mm×150mm 灭菌平皿 直径9cm 酒精灯 灭菌吸管 1mL、10mL 载玻片 盖玻片 灭菌广口瓶 500mL 牛皮纸袋 金属勺 刀 试管架 接种针 橡皮乳头
项目十八 酵母菌、霉菌检验
2.培养基和试剂
孟加拉红培养基 马铃薯-葡萄糖琼脂培养基 灭菌蒸馏水 乙醇
项目十八 酵母菌、霉菌检验
3.检验程序
检样
取25g或25mL,加入225mL无菌水
做成几个适当倍数的稀释样
选择3个适宜稀释度,各以1mL加入灭脂培养基
项目十八 酵母菌、霉菌检验
6.报告 每克(或每毫升)食品所含霉菌和酵 母数以个/g(或个/mL)表示。
项目十八 酵母菌、霉菌检验
4)培养 倒置于25~28℃温箱中,3d后开始观察,共培养 观察5d。 5)计数 选取菌落数10~150之间的平板进行计数。(稀释 度选择和菌落报告方式参考菌落总数的测定)
项目十八 酵母菌、霉菌检验
5.计算方法 通常选择菌落数在10~150之间的平皿进行计 数,同稀释度的2个平皿的菌落平均数乘以稀释 倍数,即为每克(或每毫升)检样中所含霉菌和 酵母数。
项目十八 酵母菌、霉菌检验
学习任务: 任务1.学习霉菌、酵母菌的检验方法。 任务2.学习配制孟加拉红培养基。 任务3.学习对霉菌、酵母菌的判断及计数。
项目十八 酵母菌、霉菌检验
任务要求
掌握霉菌、酵母菌的检验方法。 掌握孟加拉红的配制。 掌握霉菌、酵母菌的判断及计数。
霉菌酵母菌检验知识分享

5)作平皿内菌落计数时,可用肉眼观察,必要时用放大镜检查,以防遗漏。
二、平皿菌落总数计算CFU/g(ml)
(1)若有两个连续稀释度的平板菌落总数在适宜计数范围(10CFU~150CFU)内时,按式(Ⅰ)计算:
N= ∑C/(n1+0.1n2)d………………(Ⅰ)
有时在标准视野中出现极细的菌丝丛或小菌落,则以其直径来计算,超过视野直径1/6为阳性视野,否则为阴性视野。阳性视野用“+”表示;阴性视野用“-”表示之。
对初次学习菌计测法者,作记录前,先在记录纸上划出计测室上50视野均匀分布的小格,观察一个标准视野,立即在相应的方格内作“+”或“-”的记录,或“-”以空格表示之。
如均大于150CFU,则取最高稀释度的平均菌落数乘以稀释倍数报告之。
如均小于10CFU,则以最低稀释度的平均菌落数乘稀释倍数报告之。
如菌落数有的大于150CFU,有的又小于10CFU,但均不在10~150CFU之间,则应以最接近150CFU或10CFU的平均菌落数乘以稀释倍数报告之。
如所有稀释度(包括液体样品原液)均无菌落生长,则应按小于1乘以最低稀释倍数报告。
液体样品:以无菌吸管吸取25ml样品置盛有225ml无菌稀释液(蒸馏水或磷酸盐缓冲液或生理盐水)的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中混匀,为1:10样品匀液。
用灭菌吸量管吸取1∶10稀释液10mL,注入试管中,另用带橡皮乳头的1mL灭菌吸量管反复吹吸50次,使霉菌孢子充分散开。
取1mL1∶10稀释液注入含有9mL灭菌水的试管中,另换一支1mL灭菌吸量管吹吸5次,此液为1∶100稀释液。
琼脂凝固,正置平板。
培养
样品28℃±1℃培养
霉菌和酵母菌检测方法

霉菌和酵母菌检测方法
常见的霉菌和酵母菌检测方法包括以下几种:
1. 直接镜检法:采集被检物表面样品,然后在显微镜下直接观察样品中是否存在霉菌和酵母菌。
2. 培养法:将样品分别接种在含有适当营养物质的培养基中,然后在一定条件下培养,观察生长情况,判断其中是否有霉菌和酵母菌。
3. PCR检测法:对样品中的霉菌和酵母菌的特定基因进行PCR扩增,并通过电泳等技术检测扩增产物的种类和数量。
4. 气相色谱法:通过分析样品中的挥发性有机化合物,判断其中是否存在霉菌和酵母菌。
5. 快速检测法:利用特定化学试剂或生物标记物,在短时间内快速检测样品中的霉菌和酵母菌。
食品微生物能力验证霉菌酵母菌计数—检验方法比较

食品微生物能力验证霉菌酵母菌计数—检验方法比较霉菌酵母菌在自然界中分布极广,种类繁多,食品中易受到不同程度的污染。
食品中霉菌酵母菌的增殖一般会导致营养价值下降、酸败变味或外观恶化等,影响货架期及口感,若霉菌、酵母菌含量较高,且日摄入量较多,会影响人体肠胃内的微生物平衡,甚至造成肠胃不适,可能引起疾病发生。
霉菌对干食品的最大风险主要是在适宜的条件下(产毒株、数量、温度、湿度、水分活度等),能产生霉菌的有毒代谢产物—霉菌毒素,引起过敏反应等各种急、慢性中毒及可能的致癌作用。
因此,人们愈来愈重视食品中霉菌及酵母菌污染对人体造成的危害。
在我国国家部分食品产品及卫生标准中,把霉菌和酵母菌作为常见指示菌进行监测和控制,如饮料、坚果制品、米面制品、糕点类等食品。
霉菌和酵母的检测被列入国标4789 系列食品安全微生物常规检测项目之一 , 霉菌酵母菌的检验方法看似简单,但由于食品种类繁多成分复杂,食品中存在的霉菌种类较多,对环境温湿度及营养成分的要求有所不同,要在同等条件下把所有的霉菌培养出来,反映出样品的真实情况,实属不易,且霉菌前期生长速度缓慢,后期菌丝急剧增加,特别是毛霉的蔓延,给霉菌和酵母菌的同时计数带来一定的困难,如何能更准确、快速提离食品中霉菌检测数目是食品卫生部门面临的一个严峻问题。
能力验证是利用实验室间的比对判定实验室的特定校准、检测能力,以考察实验室检验能力的外部质量活动,组织方提供试验的样本,一般会考虑增加检测难度。
为了更准确更全面得出能力验证结果,本实验室综合了多种方法进行同步检测,主要是考虑霉菌、酵母菌总数检测是通过平板中生长的菌落数目直接计数推算,培养基的质量和培养方式直接影响了检测的结果,因此,选择两种常用的霉菌酵母培养基,采用正置和倒置培养法进行试验,比较分析不同培养基、不同培养方式对霉菌酵母菌计算结果的差异,进而得出较为准确的试验结果进行上报。
2 材料与方法2.1 样品能力验证样品:中国检验检疫科学研究院测试评价中心提供,样品编号为15-G068。
霉菌(酵母菌)总数测定方法

霉菌(酵母菌)总数测定方法
设备和材料:高压灭器、恒温水浴45℃、吸管1mL和10mL、试管20mL、三角瓶500mL和250mL、培养箱30~35℃、菌落计数器、放大镜
培养箱:25~28℃,培养基选用玫瑰红钠琼脂培养基。
1.供试液与稀释按细菌总数测定项下规定得方法进行
取供试液1:100和1:1000的稀释液个1mL分别注入平皿内,每个稀释液各用2~3个平皿,加入稀释液后,将熔化并冷却至45~50℃的虎红琼脂培养基倾入平皿内,充分摇匀,凝固后,翻转平板至25~28℃培养72小时,24、48、72小时计数,以72小时为准,计算平板内生长的霉菌落数。
若有根霉或毛霉蔓延已生长,为避免影响其它霉菌的同时,应及时将此平板取出计数。
2.酵母养菌霉菌菌数报告
酵母菌、霉菌计数,应选取带有菌丝体的菌落和酵母菌菌落进行点数,先点清每个平板上生长的菌落数,再求出每一稀释度的平均菌落数。
判定结果时,应选取平板上的菌落数即清楚可数,平均又在30~100个范围以内的菌落数,乘以稀释倍数后,做为供试品的霉菌总数报告之。
若有两个稀释度的菌落数皆在30~100个以内或三个稀释度皆不在此范围之内,应参照细菌总数测定的规则报告之。
若不合格同细菌总数测定。
依据:中国药典2005年版二部附录ⅪJ。
霉菌和酵母菌检验方法验证报告

方法验证报告方法验证报告一、方法依据/原理1.1方法依据:化妆品安全技术规范(2015)第五章 6 霉菌和酵母菌检验方法1.2原理:化妆品检样在一定条件下培养后,1g或1mL化妆品中所污染的活的霉菌和酵母菌数量,藉以判明化妆品被霉菌和酵母菌污染程度及其一般卫生状况。
本方法根据霉菌和酵母菌特有的形态和培养特性,在虎红培养基上,置28℃±2℃培养5d,计算所生长的霉菌和酵母菌数。
二、使用范围2.1适用于化妆品霉菌和酵母菌的测定。
三、设备情况表1使用仪器设备一览表表2标准物质和关键物料登记表四、环境条件情况表3环境条件五、人员能力情况表4相关人员六、方法验证/确认情况6.1 实验步骤6.1.1样品前处理6.1.1.1液体样品:水溶性的液体样品,用灭菌吸管吸取 10mL 样品加到 90mL 灭菌生理盐水中,混匀后,制成 1:10检液。
6.1.1.2油性液体样品:取样品10g,先加5mL灭菌液体石蜡混匀,再加10mL灭菌的吐温80,在40℃—44℃水浴中振荡混合10min,加入灭菌的生理盐水75mL(在40℃—44℃水浴中预温),在40℃—44℃水浴中乳化,制成1:10的悬液。
6.1.1.3膏、霜、乳剂半固体状样品:亲水性的样品:称取10g,加到装有玻璃珠及90mL灭菌生理盐水的三角瓶中,充分振荡混匀,静置 15min。
用其上清液作为 1:10 的检液。
疏水性样品:称取10g,置于灭菌的研钵中,加10mL灭菌液体石蜡,研磨成粘稠状,再加入10mL灭菌吐温 80,研磨待溶解后,加70mL灭菌生理盐水,在40℃—44℃水浴中充分混合,制成 1:10 检液。
6.1.1.4固体样品:称取10g,加到90mL灭菌生理盐水中,充分振荡混匀,使其分散混悬,静置后,取上清液作为1:10 的检液。
使用均质器时,则采用灭菌均质袋,将上述水溶性膏、霜、粉剂等,称10g 样品加入90mL灭菌生理盐水,均质1min—2min;疏水性膏、霜及眉笔、口红等,称10g样品,加10mL灭菌液体石蜡,10mL吐温80,70mL 灭菌生理盐水,均质3min—5min。
霉菌和酵母菌菌数检验技术

28±1℃ 5天
4.结果计数
案例---蜂蜜中霉菌数测定
菌落计数应于培养后的72 h进行第一次观察。培养过程中观察平板时,动作稍重,生长快速的 霉菌孢子就会在培养基内扩散,导致二次污染,结果异常。
一般以第五天的读数为最终计数。
案例---蜂蜜中霉菌数测定
5.结果报告 例次 1
不同稀释度的平均菌落数
GB 4789.15-2016 标准解读
5 操作步骤
5.1.3 取1 mL 1:10样品匀液注入含有9 mL 无菌稀释液的试管中, 另换一支1 mL无菌吸管反复吹吸,或在 漩涡混合器上混匀,此液为1:100的样品匀液。 5.1.4 按5.1.3操作程序,制备10倍系列稀释样品匀液。每递增稀释一次,换用1次1mL无菌吸管。 5.1.5 根据对样品污染状况的估计,选择2个~3个适宜稀释度的样品匀液(液体样品可包括原液),在进 行10倍递增稀释的同时,每个稀释度分别吸取1 mL样品匀液于2个无菌平皿内。同时分别取1 mL样品稀 释液加入2个无菌平皿作空白对照。 5.1.6 及时将20 mL~ 25mL冷却至46 ℃的马铃薯-葡萄糖-琼脂或孟加拉红培养基(可放置于46℃±1℃ 恒温水浴箱中保温)倾注平皿,并转动平皿使其混合均匀,置水平台面待培养基完全凝固。
计算公式:
备注:
注意事项
培养基的选择 在霉菌和酵母计数中,主要使用以下几种选择性培养基: ① 马铃薯-葡萄糖-琼脂配有计算(PDA):霉菌和酵母在PDA培养基上生长良 好。用PDA做平板计数时,必须加入抗菌素以抑制细菌。 ② 孟加拉红(虎红)培养基:该培养基中的孟加拉红和抗菌素具有抑制细菌的 作用。孟加拉红还可以抑制霉菌菌落的蔓延生长。在菌落背面由孟加拉红产生的 红色有助于霉菌和酵母菌落的计数
06-食品中酵母菌、霉菌测定

知识点:果汁中酵母菌、霉菌测定情境:微生物检测技术任务:酵母菌、霉菌测定课程:食品微生物技术酵母菌、霉菌测定原理一、霉菌、酵母菌什么叫霉菌、酵母菌?❞霉菌:为丝状真菌的统称。
凡是在营养基质上能形成绒毛状、网状或絮状菌丝体的真菌(除少数外),统称为霉菌。
❞酵母菌:一些单细胞真菌。
一种肉眼看不见的微小单细胞微生物,能将糖发酵成酒精和二氧化碳,分布于整个自然界,是一种典型的兼性厌氧微生物,在有氧和无氧条件下都能够存活,是一种天然发酵剂。
二、霉菌、酵母菌测定原理❞霉菌和酵母菌菌数的测定是指食品检样经过处理,在一定条件下培养后,所得1g或1mL检样中所含的霉菌和酵母菌菌落数(粮食样品是指1g粮食表面的霉菌总数)。
❞霉菌和酵母数主要作为判定食品被污染程度的标志,以便对被检样品进行卫生学评价时提供依据。
本方法适用于所有食品。
酵母菌、霉菌测定原理与菌落总数测定类似,选用平板菌落计数法。
平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。
统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。
酵母菌、霉菌测定步骤1.液体样品稀释以无菌吸管吸取25 mL样品至盛有225mL无菌稀释液(蒸馏水或生理盐水或磷酸盐缓冲液)的适宜容器内(可在瓶内预置适当数量的无菌玻璃珠)或其他无菌均质袋中,充分振摇或用拍击式均质器拍打1 min~2min,制成1:10 的样品匀液。
2.梯度稀释❞取1 mL 1:10 样品匀液注入含有9 mL 无菌稀释液的试管中,另换一支1 mL 无菌吸管反复吹吸,或在漩涡混合器上混匀,此液为1:100 的样品匀液。
❞按上述操作程序,制备10 倍系列稀释样品匀液。
每递增稀释一次,换用1 次1 mL 无菌吸管或吸头。
四、倒平板❞根据对样品污染状况的估计,选择2 个~3 个适宜稀释度的样品匀液(液体样品可包括原液),在进行10 倍递增稀释时,吸取1 mL 样品匀液于无菌平皿内,每个稀释度做两个平皿。
细菌、霉菌、酵母菌检查标准操作规程

细菌、霉菌、酵母菌检查标准操作规程全文共四篇示例,供读者参考第一篇示例:细菌、霉菌、酵母菌检查是食品安全和环境卫生领域中非常重要的一项工作。
为了确保检查结果的准确性和可靠性,需要遵守一系列标准操作规程。
下面将介绍一份关于细菌、霉菌、酵母菌检查的标准操作规程,以供参考。
一、检测方法选择在进行细菌、霉菌、酵母菌检查之前,首先需要确定检测的目的和样品种类。
根据具体情况选择适合的检测方法,一般可以选择培养基法、PCR法、免疫学法等方法进行检测。
不同方法的灵敏度和准确度有所差异,需要根据具体要求选择合适的检测方法。
二、样品采集在进行细菌、霉菌、酵母菌检查之前,需要首先采集样品。
样品的采集应该遵循以下原则:1. 样品应该代表性,能够反映整个检测对象的真实情况;2. 样品的采集方法应该符合标准操作规程,避免污染;3. 采样器具和容器应该经过消毒处理,避免样品受到外界干扰。
三、样品处理在采集到样品后,需要进行样品处理以提取目标微生物。
样品处理的方法应该符合标准操作规程,避免样品受到外界污染。
常用的样品处理方法包括过滤法、萃取法、富集法等。
四、培养条件设置对于细菌、霉菌、酵母菌的检测,需要设置合适的培养条件以促进目标微生物的生长。
培养条件的设置应该考虑到目标微生物的生长特性和适宜条件,并严格控制培养环境的温度、湿度和氧气等因素。
五、培养基选择在进行微生物检测时,需要选择适合的培养基以促进目标微生物的生长。
不同微生物对培养基有不同的选择性,需要选择适合的培养基进行培养。
常用的培养基包括普通培养基、选择性培养基、差异培养基等。
六、检测结果解读在检测完成后,需要进行检测结果的解读。
根据实验结果判断目标微生物的存在与否,对结果进行合理解读和分析。
检测结果应该符合标准操作规程的要求,确保检测结果的准确性和可信度。
七、结果报告在完成检测后,需要对检测结果进行报告。
检测报告应该包括检测方法、样品信息、检测结果、结论和建议等内容。
细菌、霉菌、酵母菌检查标准操作规程

细菌、霉菌、酵母菌检查标准操作规程细菌、霉菌、酵母菌检查是微生物学实验室常用的一项技术,用于确定食品、饮料、药品、环境样品等中是否存在这些微生物。
细菌、霉菌、酵母菌都是常见的微生物,它们在生物学和工业上具有重要的作用。
本文将以标准操作规程的形式详细介绍细菌、霉菌、酵母菌检查的步骤和要求。
一、实验前准备1.环境准备:实验室环境要保持清洁、无尘、无飞虫等干扰因素,确保实验的准确性。
2.器材准备:准备好必要的实验器材,包括培养基、试剂、仪器设备等。
3.样品准备:样品应遵循卫生标准及实验要求,确保样品的可靠性和代表性。
二、样品处理1.样品消毒:将样品进行适当的消毒处理,以消除外源性微生物的干扰。
2.预培养:将样品接种到含有适宜培养基的试管中,进行预培养,以增加微生物的数量。
三、分离与纯化1.罩口接种:将样品中微生物接种到含有相应培养基的平板上,通过罩口接种的方式,避免次生污染。
2.培养条件:根据微生物的特性,设置适宜的培养温度、时间和培养基组成等条件,促进微生物的生长。
3.单菌分离:观察接种后的菌落形态和特征,选取单菌落转接到新的培养基上,以实现纯化。
四、鉴定与检测1.形态观察:观察菌落形态、边缘、颜色、透明度等特征,与已知细菌、霉菌、酵母菌的特征进行比对。
2.生理生化试验:通过一系列的生理生化指标和试验,如盖氏染色、革兰氏染色、培养基反应等,对菌株进行进一步鉴定。
3.分子生物学检测:采用PCR、序列比对等分子生物学技术,对菌株进行分子水平的鉴定。
五、结果处理与分析1.定量分析:根据菌落的数量和菌落形状比例,计算并报告样品中细菌、霉菌、酵母菌的数量。
2.图像记录:对鉴定结果进行拍照记录,确保结果的真实性和可追溯性。
六、质量控制1.消毒控制:实验室应定期对实验环境进行消毒处理,保持无菌状态。
2.正负对照:每次实验都应设置正、负对照,确保实验结果的准确性和可靠性。
3.重复实验:对怀疑结果的样品可以进行重复实验,验证结果的可靠性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实训项目教程
适合专业(群):食品加工技术专业群
教师:万国福
行动领域 任务一 菌落总数测定 任务二 大肠菌群检验 任务三 霉菌、酵母菌检验 任务四 乳酸菌检验
任务三 霉菌、酵母菌检验
一、目的要求
1、学习测定食品中霉菌、酵母菌检测程序、方法; 2、掌握霉菌、酵母菌检测结果的报告方式。
二、实验原理
五、实验数据及结果
• 通常选择菌落数在10-150之间的平皿进行计数,一个稀 释度使用两个平板,采用两个平板的平均数;选择稀释度 也选择平均菌落数在10-150之间的稀释度,菌落平均数 乘以稀释倍数,即为每克(或毫升)检样中所含霉菌和酵 母数。
待琼脂凝固后,倒 置于25-28℃温箱 中,3d后开始观察, 共培养观察5d。
(1)将各稀释平板上的菌落数填入下表。 霉菌测定报告
稀释度 平板号 1
1:10
2 平 均 1
1:100
2 平均 1
1:1000
2 平 均
霉菌菌落数
根据试验结果,报告检测结果: 每1mL(g)食品中的霉菌数是
。
酵母菌测定报告
稀释度 稀释度 平板号 酵母菌落数 1 1:10 2 平 均 1 1:100 2 平 均 1 1:1000 2 平 均
根据试验结果,报告检测结果: 每1mL(g)食品中酵母菌数是__________。
(3)取1mL 1:100稀 释液注入含有9mL 灭菌水的试管中, 另换一支1mL灭菌 吸量管,此液为 1:1000稀释液。
2、接种培养 • 根据对样品污染情 况的估计,选择3个 合适的稀释度,分 别在做10倍稀释的 同时,吸取1mL稀 释液于灭菌平皿中 ,每个稀释度做2个 平皿,然后将凉至 45 ℃左右的培养基 注入平皿中,待琼 脂凝固后,倒置于 25-28℃温箱中, 3d后开始观察,共 培养观察5d。
四、操作步骤
1、采样 选取有代表 性的样品并避免采 样时的污染。本实 验用的是开封的脉 动饮料。
(1)以无菌操作称取 检样25mL,放入含 有225mL灭菌水的 玻塞三角瓶中,振 摇30 min,即为 1:10稀释液。
(2)取1mL 1:10稀释 液注入含有9mL灭 菌水的试管中,另 换一支1mL灭菌吸 量管此液为1:100稀 释液。
• 霉菌和酵母菌菌数的测定是指食品检样经过处理,在一定 条件下培养后,所得1g或1mL检样中所含的霉菌和酵母菌 菌落数(粮食样品是指1g粮食表面的霉菌总数)。
三、实验器材
1、培养基:马铃薯-葡萄糖琼脂培养基 2、器皿:已灭菌的平皿(9套/组),1mL吸管(6支/组), 试管(15×150)(6/组),三角锥瓶500mL、三角锥瓶 500mL(内装蒸馏水250mL),10mL吸管 3、其他:牛皮纸或报纸,酒精灯,棉花,高压蒸汽菌锅, 电烘箱,线绳,毛刷等
