10.元素的分类
元素周期表的基本结构和特点

元素周期表的基本结构和特点一、元素周期表的起源和发展•1869年,门捷列夫发现了元素周期律,并编制出第一个元素周期表。
•随着化学元素的不断发现和核反应技术的进步,周期表逐渐完善和扩展。
二、元素周期表的基本结构•横行称为周期,竖列称为族。
•周期表共有7个周期,从第1周期到第7周期。
•周期表共有18个族,包括7个主族、7个副族、1个0族和1个第Ⅷ族。
三、周期表的排列规律•周期表中,元素的原子序数依次增加。
•周期表中,同一周期的元素电子层数相同,同一族的元素最外层电子数相同。
四、元素周期表的特点•周期表反映了元素的原子结构与元素性质之间的关系。
•周期表中,周期与周期的交界处往往是一些特殊元素的所在,如超铀元素。
•周期表中,族与族之间的过渡元素往往具有相似的化学性质。
五、元素周期表的应用•周期表是化学领域的重要工具,可以查找到元素的物理和化学性质。
•周期表有助于预测和解释新元素的发现及其可能的性质。
•周期表为化学教育和研究提供了系统的分类和归纳方式。
六、元素的命名和符号•元素以化学符号表示,符号通常由一个或两个字母组成。
•元素符号的第一个字母大写,第二个字母小写。
•元素名称通常以英文表示,也有一些元素的名称来源于其他语言。
七、周期表的拓展•周期表还包括了一些具有特定性质的元素,如过渡元素、镧系元素和锕系元素。
•周期表的研究还涉及到同位素、元素周期律的微观解释等方面。
以上是关于元素周期表的基本结构和特点的知识点介绍,希望对你有所帮助。
习题及方法:1.习题:元素周期表中有多少个周期?解题方法:回顾元素周期表的基本结构,周期表共有7个周期。
答案:7个周期。
2.习题:元素周期表中有多少个族?解题方法:根据元素周期表的基本结构,周期表共有18个族。
答案:18个族。
3.习题:请列举出周期表中的7个主族。
解题方法:根据元素周期表的基本结构,主族元素位于周期表的左侧。
答案:第1主族(碱金属族)、第2主族(碱土金属族)、第3主族(硼族)、第4主族(碳族)、第5主族(氮族)、第6主族(氧族)、第7主族(卤素族)。
第十章1环境地球化学简介

环境地球化学简介
大气环境飘尘的自然去除 • 干沉降(碰撞和吸附) • 湿沉降
环境地球化学简介
4.森林植被对环境的净化作用 除调节气候,保持水土外,有以下作用: (1)保持氧和CO2的平衡 一人的氧气量需要150m2的叶面
环境地球化学简介
(2)降低大气中的有害气体浓度 可吸收HF、SO2、Cl、NO2、NH3、O3、Hg、 乙烯、过氧乙酰硝酸酯,醛,酮等。 如SO2通过高15m宽15m的法国梧桐林带, 其含量可降低25-75%。
环境地球化学简介
(2)土壤背景值 是母岩、气候、生物、水系、地形等综合 作用的产物,在研究或评价土壤的污染 程度时必须考虑原始地球化学背景。
环境地球化学简介
各地区土壤中有害元素的背景值 As Cd Hg <0.24-1.0 0.01-0.09 英国 0.02-0.55 挪威 0.09-0.56 0.01-0.16 加拿大 6.3 0.47-10.8 0.01-0.7 0.03-0.86 芬兰 0.22 0.004-0.99 瑞典 0.085 2.5 苏联 3.5-52 0.4 0.04-0.33 日本 1-7.5 0.05-0.52 0.01-0.16 美国 Pb 9.4-39 5.2-14.1 2.5-8.9 6.3-21 3.4 5.2-14.1
环境地球化学简介
2.毒性元素: • 毒性:Cd、Ge、Sn、Sb、Te、Hg、Pb、 Ga、In、As、Li(?) • 潜在和放射性毒性元素:Be、Tl、Th、 U、Po、Ra、Sr(?)、Ba(?)
环境地球化学简介
3.无毒性稳定元素:(多为氧化物矿物或 自然元素) Ti、Zr、Hf、Sc、Y、Nb、Ta、Ru、Os、 Rb、Ir、Pd、Pt、Ag、Au 4.中间性元素:B、Al
化学竞赛培训元素化学部分第10章f区元素

水体污染
通过地表径流和地下水渗透,f区元素可能进入水体,造成水体污 染。
大气污染
某些f区元素在大气中不易分解,可长时间悬浮,造成大气污染。
使用时的注意事项与安全性
防护措施
使用f区元素时,应穿戴防护服、手套、口罩等防护用品,以减少 与有害物质的直接接触。
1940s
通过核反应和粒子加速 器等手段,科学家成功 合成了一些超重元素, 进一步证实了f区元素的 存在。
制备方法
高能核反应
通过高能核反应合成超重元素,如使用粒子加速 器轰击重元素靶。
放射性衰变
某些长寿命f区元素可以由放射性衰变产生,如铹 元素。
高温高压合成
在极端条件下合成超重元素,如使用激光或离子 束技术。
新材料探索
利用f区元素的特性,探索和开发具有优异性能的新材料, 如超导材料、磁性材料、发光材料等,为科学技术进步做 出贡献。
生命科学研究
某些f区元素(如镧系元素和锕系元素)具有与生物活性相 关的特性,在生物标记、药物设计和生物成像等领域有潜 在应用价值。
日常生活中的应用
1 2
照明和显示技术
利用某些f区元素的发光特性,制造高效、环保 的照明和显示产品,如LED灯具、液晶显示器等。
03 f区元素的化合物
氧化物
定义
f区元素氧化物是指该元素与氧元 素结合形成的化合物。
特性
f区元素氧化物大多数具有较高的 熔点和沸点,因为它们是离子型化 合物,且f区元素的离子半径较小, 使得离子键更加强健。
举例
例如,镧的氧化物La2O3是一种白 色固体,熔点高达2465°C。
氢氧化物
定义
f区元素的氢氧化物是指该元素与 氢和氧结合形成的化合物。
火线100天(广西专版)中考化学 第10讲 元素、化学式与化合价复习-人教版初中九年级全册化学试题

第10讲元素、化学式和化合价考试说明1.认识氢、碳、氧、氮等与人类关系密切的常见元素。
2.记住并能正确书写一些常见元素的名称和符号。
3.知道元素的简单分类。
4.能根据元素的原子序数在元素周期表中找到指定的元素。
5.形成“化学变化过程中元素不变”的观念。
6.能说出几种常见元素的化合价。
7.能用化学式表示某些常见物质的组成。
8.利用相对原子质量、相对分子质量进行物质组成的简单计算。
9.能看懂某些商品标签上标示的组成元素及其含量。
元素1.元素是具有相同____________(即________)的一类原子的总称。
2.性质:①元素是宏观概念,它只能组成物质,而不能构成分子或原子;②元素只讲________,不讲________;③化学变化中,元素的________和________保持不变。
3.分类:元素可分为________元素、________元素、____________元素三大类。
4.含量:①在地壳中,________最多,其次为硅、铝、铁等元素;②在空气中,________最多,其次是________;③在生物体细胞中,________最多,其次是碳、氢元素。
5.国际上统一采用元素的拉丁文名称的第一个大写字母来表示元素,若第一个字母相同,就再附加一个小写字母来区别。
6.元素符号的意义(1)宏观:表示一种________;如O表示氧元素。
(2)微观:表示这种元素的____________;如O表示一个氧原子。
(3)金属、稀有气体和部分非金属的元素符号还表示这种物质;如Na、He、S表示相应物质。
7.元素与原子的区别与联系项目元素原子定义具有相同____________(即________)的同一类原子的总称____________的最小粒子区别含义宏观概念,只表示______,不表示______微观粒子,既表示______,又表示______使用X围表示物质的宏观组成,如水是由氢元素和氧元素组成的表示物质的微观构成,如1个水分子是由2个氢原子和1个氧原子构成的联系只要核电荷数相同的一类原子就是同一种元素,原子是元素的最小单位,而元素则是原子的一个归类“集体”8.物质、元素、分子、原子间的关系:元素周期表1.元素周期表的结构:________个周期、________个族、________个区间。
化探10元素-概述说明以及解释

化探10元素-概述说明以及解释1.引言化探10元素是指在地球化学勘探中具有重要意义的十种元素,包括钍、铀、镝、钕、铈、钷、镧、镨、钕和铥。
这些元素在地球上广泛分布,具有独特的性质和应用价值。
本文将对这些元素的特性、用途以及它们在地质勘探中的重要性进行深入探讨,以期为读者展示化探10元素的重要性和潜在价值。
编写文章1.1 概述部分的内容1.2 文章结构文章结构部分应该包括对整篇文章的框架和主要内容进行概述,提供读者一个整体的导向。
在这里,可以简要介绍本文的结构安排,指出每个部分所涉及的内容和重点,让读者对接下来要讨论的话题有一个清晰的预期。
内容示例:在文章结构部分,我们将依次介绍化探10元素的概述、性质和应用以及在地质勘探中的重要性。
首先,我们会从化探10元素的基本概念和分类入手,介绍这些元素的特点和作用。
然后,我们将深入探讨这些元素在实际应用中的价值和影响,包括其在环境保护、工业生产和科学研究中的应用情况。
最后,我们将探讨化探10元素在地质勘探中的作用和重要性,以及其对资源勘探、矿物探测和地质灾害监测方面的贡献。
通过对这些内容的全面讨论,我们希望读者能够更好地了解化探10元素的真正价值和未来发展趋势。
1.3 目的本文旨在探讨化探10元素在地质勘探领域中的重要性和应用。
通过对10元素的简介、性质和应用进行深入分析,希望能够全面了解这些元素在地质勘探中的价值和作用。
同时,通过对10元素在地质勘探中的实际案例进行研究和总结,探讨其在未来的应用前景。
最终旨在为地质勘探工作者提供有益的参考和启示,促进地质勘探技术的发展和应用。
2.正文2.1 化探10元素简介化探10元素是指在矿产勘查和地质勘探中具有重要作用的10种元素,它们是铅(Pb)、锌(Zn)、铜(Cu)、镍(Ni)、锡(Sn)、铼(Re)、钨(W)、钼(Mo)、银(Ag)和金(Au)。
这些元素通常在地质构造和矿床成因中起着重要作用,它们的存在形式和分布特征对于判断矿床类型、勘探方向和储量规模具有重要的指导意义。
元素周期表的起源和应用

4f3 6s2 60 Nd 4f4 6s2 61 Pm 4f5 6s2 62 Sm 4f6 6s2 63 Eu 4f7 6s2 64 Gd
1 H 1s1 2 He 1s2 3 Li 2s1 4 Be 2s2 5 B 2s2 2p1 6 C 2s2 2p2 7 N 2s2
2p3 8 O2s2 2p4 9 F 2s2 2p5 10 Ne 2s2 2p6 11 Na 3s1 12 Mg 3s2 13 Al
4p3 34 Se 4s2 4p4 35 Br 4s2 4p5 36 Kr 4s2 4p6 37 Rb 5s1 38 Sr 5s2 39
Y 4d1 5s2 40 Zr 4d2 5s2 41 Nb 4d4 5s1 42 Mo 4d5 5s1 43 Tc 4d5 5s2 44
4f7 5d1 6s2 65 Tb 4f9 6s2 66 Dy 4f10 6s2 67 Ho 4f11 6s2 68 Er 4f12 6s2
69 Tm 4f13 6s2 70 Yb 4f14 6s2 71 Lu 4f14 5d1 6s2 72 Hf 5d2 6s2 73 Ta
A:质量数 (Mass number) ,即在数量上等于原子核(质子加中子)的粒子数目。 Z:原子序数,即是质子的数目。由于它是固定的,一般不会标示出来。
e:净电荷,正负号写在数字后面。
n:原子数目,元素在非单原子状态(分子或化合物)时的数目。除此之外,部份较高级的周期表更会列出元素的电子排布、电负性和价电子数目。
钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī) 67 钬(huǒ) 68
元素周期表

H氢Li锂Be铍Na钠Mg镁K钾Ca钙Sc钪Ti钛V钒Cr铬Rb铷Sr锶Y钇Zr锆Nb铌Mo钼Cs铯Ba钡*Hf铪Ta钽W钨Fr钫Ra镭**Rf鈩Db(钅杜)Sg(钅喜) *La镧Ce铈Pr镨Nd钕**Ac锕Th钍Pa镤U铀14Si硅归283s2,3p2 15P磷林313s2,3p3 16S硫留323s2,3p4 17Cl氯绿35.53s2,3p5 18Ar氩亚403s2,3p6 19K钾假394s1 20Ca钙盖404s2 21Sc钪抗钪453d1,4s2 22Ti钛太483d2,4s2 23V钒凡513d3,4s2 24Cr铬个52锰3d5,4s1 25Mn锰猛553d5,4s2 26Fe铁铁563d6,4s2 27Co钴古593d7,4s2 28Ni镍臬593d8,4s2 29Cu铜同63.53d10,4s1 30Zn锌辛65.53d10,4s2 31Ga镓家69.74s2,4p1 32Ge锗者72.64s2,4p2 33As砷申754s2,4p3 34Se硒西794s2,4p4 35Br溴秀794s2,4p5 36Kr氪克83.84s2,4p6 37Rb铷如85.55s1 38Sr锶思87.55s2 39Y钇乙894d1,5s2 40Zr锆告914d2,5s2 41Nb铌尼934d4,5s1 42Mo钼目964d5,5s1 43Tc锝得984d5,5s2 44Ru钌liǎo1014d7,5s1 45Rh铑老1034d8,5s1 46Pd钯把106.54d10 47Ag银吟1084d10,5s1 48Cd镉隔112.54d10,5s250Sn锡西118.55s2,5p2 51Sb锑梯1225s2,5p3 52Te碲帝127.55s2,5p4 53I碘典1275s2,5p5 54Xe氙仙131.35s2,5p6 55Cs铯色1336s156Ba钡贝137.36s257La镧兰1395d1,6s2 58Ce铈市1404f1,5d1,6s2 59Pr镨普1414f3,6s2 60Nd钕女1444f4,6s2 61Pm钷叵1454f5,6s2 62Sm钐衫150.54f6,6s2 63Eu铕有1524f7,6s2 64Gd钆轧1574f7,5d1,6s2 65Tb铽特1594f9,6s2 66Dy镝滴162.54f10,6s2 67Ho钬火1654f11,6s2 68Er铒耳1674f12,6s2 69Tm铥丢1694f13,6s2 70Yb镱意1734f14,6s271Lu镥鲁1754f14,5d1,6s272Hf铪哈178.55d2,6s2 73Ta钽坦1815d3,6s2 74W钨乌1845d4,6s2 75Re铼来1865d5,6s2 76Os锇鹅1905d6,6s2 77Ir铱衣1925d7,6s2 78Pt铂伯1955d9,6s1 79Au金今1975d10,6s1 80Hg汞拱200.65d10,6s2 81Tl铊他204.56s2,6p1 82Pb铅千2076s2,6p2 83Bi铋必2096s2,6p3 84Po钋泼2096s2,6p4B硼Al铝Mn锰Fe铁Co钴Ni镍Cu铜Zn锌Ga镓Tc锝Ru钌Rh铑Pd钯Ag银Cd镉In铟Re铼Os锇Ir铱Pt铂Au金Hg汞Tl铊Bh(钅波)Hs(钅黑)Mt䥑(钅麦)Ds鐽Rg錀Cn鎶Pm钷Sm钐Eu铕Gd钆Tb铽Dy镝Ho钬Np镎Pu钚Am镅Cm锔Bk锫Cf锎Es锿周期表列表质4主/类Silicon['silikən]地壳中含量仅次于氧-3,3,5主/非/其Phosphorus['fɔsfərəs]白磷有剧毒-2,4,6主/非/其Sulfur['sʌlfə]质地柔软,轻,与氧气燃-1,1,3,5,7主/非/卤Chlorine['klɔ,ri,n]有毒,活泼主/非/稀Argon['ɑ,ɡɔn]稀有气体,在空气中含量1主/碱Potassium[pə'tæ,sjəm]活泼,与空气或水接触发2主/碱土Calcium['kæ,lsiəm]骨骼主要组成成分3副/金/过Scandium['skæ,ndiəm]一种柔软过渡金属,常与4副/金/过Titanium [tai'teiniəm]能在氮气中燃烧,熔点高5副/金/过Vanadium [və'neidiəm]高熔点稀有金属3,6副/金/过Chromium['krəumjəm]硬度最高的金属2,4,6,7副/金/过Manganese ['mæ,ŋɡə,ni,s]在地壳中分布广泛2,3副/金/过Iron['aɪən]地壳含量第二高金属,开2,3副/金/过Cobalt[kəu'bɔ,lt]有毒,放射性元素2,3副/金/过Nickel['nikəl]有磁性和良好可塑性1,2副/金/过Copper['kɔpə]人类发现最早金属之一2副/金/过Zinc[ziŋk] 3主/金/其Gallium['ɡæ,liəm]4主/类Germanium [dʒə,'meiniəm]-3,3,5主/类Arsenic['ɑ,sənik]有毒-2,4,6主/非/其Selenium [si'li,niəm]-1,7主/非/卤Bromine['brəumi,n]活泼主/非/稀Krypton['kriptɔn]1主/碱Rubidium [ru,'bidiəm]活泼2主/碱土Strontium ['strɔntiəm]3副/金/过Yttrium['itriəm]4副/金/过Zirconium [zə,'kəuniəm]5副/金/过Niobium [nai'əubiəm]6副/金/过Molybdenum [mɔ'libdinəm]7副/金/过Technetium [tek'ni,ʃiəm]放射,人造3,8副/金/过Ruthenium [ru,'θi,niəm]3,4副/金/过Rhodium['rəudiəm]2,4副/金/过Palladium [pə'leidiəm]1副/金/过Silver['silvə] 2副/金/过Cadmium['kæ,dmiəm]2,4主/金/其Tin[tin]-3,3,5主/类Antimony['æ,ntiməni]-2,2,4,6主/类Tellurium [te'ljuəriəm]-1,7主/非/卤Iodine['aiəudi,n]活泼4,6,8主/非/稀Xenon['zenɔn]1主/碱Cesium['si,ziəm]活泼2主/碱土Barium['bεəriəm]3副/金/镧Lanthanum ['læ,nθənəm]3,4副/金/镧Cerium['siəriəm]3副/金/镧Praseodymium[,preiziəu'dimiəm]3副/金/镧Neodymium [,ni,əu'dimiəm]3副/金/镧Promethium [prəu'mi,θiəm]放射3副/金/镧Samarium [sə'mɛəriəm]3副/金/镧Europium [juə'rəupiəm]3副/金/镧Gadolinium['ɡæ,dəliniəm]3副/金/镧Terbium['tə,biəm]3副/金/镧Dysprosium [dis'prəusiəm]3副/金/镧Holmium['həulmiəm] 3副/金/镧Erbium['ə,biəm]3副/金/镧Thulium['θju,liəm]3副/金/镧Ytterbium[i'tə,biəm]3副/金/镧Lutetium [lju,'ti,ʃiəm]4副/金/过Hafnium['hæ,fniəm]5副/金/过Tantalum['t æ,ntələm]6副/金/过Tungsten['tʌŋstən]熔点最高7副/金/过Rhenium['ri,niəm]4,6,8副/金/过Osmium['ɔzmiəm]密度最大的金属3,4副/金/过Iridium[ai'ridiəm]2,4副/金/过Platinum['pl æ,tinəm]1,3副/金/过Gold[ɡəuld]原子结构最稳定1,2副/金/过Mercury['mə,kjuri] 3主/金/其Thallium['θæ,liəm] 2,4主/金/其Lead[led] 3,5主/金/其Bismuth['bizməθ]-2,6主/类Polonium [pə'ləuniəm]放射['He氦C碳N氮O氧F氟Ne氖Si硅P磷S硫Cl氯Ar氩Ge锗As砷Se硒Br溴Kr氪Sn锡Sb锑Te碲I碘Xe氙Pb铅Bi铋Po钋At砹Rn氡Fl鈇Lv鉝Uuo Er铒Tm铥Yb镱Lu镥Fm镄Md钔No锘Lr铹。
元素周期表个知识点归纳

人教版化学必修2第一章第一节元素周期表38个知识点归纳1、元素定义:核电荷数相同的同一类原子的总称,一种元素可能有多种形式的原子存在H)、H+、H-。
形式,如:氢元素的几种形式:H、D(21H)、T(312、元素符号:在元素周期表中每个小格分四层,元素符号在第一层,黑色字体,用拉丁文大写字母表示,当大写字母相同时,加一个小写字母予以区别。
例如:H(氢)、He(氦);C(碳)、Cl(氯)、Ca(钙);N(氮)、Ne(氖)、Na (钠);Al(铝)、Ar(氩)。
3、元素名称:在元素周期表中每个小格分四层,元素名称在第二层,黑色字体,大多数元素的名称是由形声字构成,气态非金属的名称有气字头,固态非金属的名称有石头旁,液态非金属用三点水旁(溴),液态金属用水字底(汞),金属的名称都有金字旁,个别的元素的名称不是形声字,例如:氮不读“炎”音。
4、元素分类:(1)按元素所在的周期分类:同周期元素和不同周期元素同周期元素共同点:电子层数相同,在元素周期表中处于同一行中,处于左右关系。
不同周期元素不同点:电子层数不相同,在元素周期表中不处于同一行中。
(2)根据元素的原子序数分类:前20号元素或第n号元素(3)按元素所在的族分类:主族元素、副族元素、第VIII族元素、0族元素(4)按元素周期表(新课标人教版化学必修2)分类:金属、非金属、过渡元素其中金属元素专指主族元素的金属元素,非金属包括主族非金属和稀有气体,过渡元素是指所有副族金属元素和Ⅷ族金属元素,。
5、元素的特有数值:元素的原子序数和元素的相对原子质量。
(1)原子序数=核电荷数=质子数,原子序数在核组成符号中处于元素符号的左下角位置,在元素周期表中每个小格内的第一层,位于元素符号的左下角,数字呈鲜红色。
(2)元素的相对原子质量就是按照元素各核素原子的相对原子质量所占的一定百分比计算出的平均值(见课本P10),元素的相对原子质量在元素周期表中每个小格内的第四层,通常保留有效数字4位,数字呈黑色。
《元素周期表》最新版本

6,54,86. • 记住1~20号元素的名称和符号
.
方法指引
根据原子序数推算主族元素在周期表中的位置 将该原子序数同与之最相近的惰性元素的序数相 减:
1、若比相应惰性元素大1-2,则应处在下一周期 的ⅠA- ⅡA 2、若比相应惰性元素小1-5,则应处在同一周期 H
1
1氢 IIA
Li Be
2
3锂 4铍
Na Mg
3
11钠 12镁
K Ca
4
19钾 20钙
A:主族
IIIA B 5硼 Al 13铝
B:副族
IVA C 6碳 Si 14硅.
VA N 7氮 P 15磷
VIA O 8氧 S 16硫
VIIA F 9氟 Cl
17氯
0 He 2氦 Ne 10氖 Ar 18氩
周 期I
.
(3)从上到下,由于电子层数递增,原子半径逐渐 增大,原子核对最外层电子的吸引力逐渐减弱,原 子得电子能力逐渐减弱,因此,卤族元素的非金属 性逐渐减弱,单质的氧化性逐渐减弱。
表现:①与H2反应渐难; ②生成的HX的稳定性逐渐减弱; ③最高价氧化物的水化物(HXO4)的酸性逐渐减 弱:HClO4>HBrO4>HIO4 (F无正价)
越 难
以
通式:X2 + H2O==HX+HXO
发 生
(X:Cl、Br、I)
.
卤素与氢气的反应
名称 反应条件
方程式
F2 Cl2 Br2
冷暗处爆炸
H2+F2==2HF
光照
光照或点燃 H2+Cl2点=燃=2HCl
高温
500℃
H2+Br2==2HBr
金属元素在元素周期表中位置

10 8
109 110 111 112
1
8M
8
3 6 N 18
5 4 O 18
8 6 P 32
练习:完成下表
主族元素的族序数=其原子最外层电子数
练习:已知某主族元素的原子结构 示意图如下,判断其位于第几周期, 第几族?分别是什么元素?
金属在周期表中的位置
1.推算原子序数为6、13、34、 53、88的元素在元素周期表中的 位置(用周期和族来表示)。
[实验]
滴有酚 酞的水
+Na 常温 +Mg
+Al
1.Na在常温下,与水剧烈反应,浮 于水面在水面四处游动,同时产生 大量无色气体,溶液变红。
2.Mg在常温下,与水的反应无明显 现象;加热时,镁带表面有大量气 泡出现,溶液变红。
3.Al在常温或加热下,遇水无明显 现象。
[实验] +Mg条
1 mol/L盐酸
26
周期
号
核外电 子层数
1 2 3 4 5 6 7
2.族
主族——由短周期元素和长周期元 素共同构成的族( 用A表示,有7 个主族,1-2 、13-17纵行)
副族——完全由长周期元素构成的 族(用B表示,有7个副族,3-7、 11-12纵行)
一个零族(18纵行)和一个第Ⅷ 族 (8、9、10纵行)
过渡元素——元素周期表 的中部从ⅢB族到ⅡB族10 个纵行,包括了第Ⅷ族和 全部副族元素,共六十多 种元素。
c
Th Pa U Np Pu Am Cm Bk Cf Es 0 Md 2 r
锕
Fm
No 铹
一、元素周期表的结构(7个横行18个纵行)
1、周期—具有相同电子层数的元素 按照原子序数递增的顺序 排列的 一个横行
元素周期表
越来越困难
稳定性↓ 还原性↓
三、位、构、性的关系
质子数Z 电子层数 最外层电子数
电子层数
=周期序数
决
定
最外层电子数
=主族序数
原子结构
元素性质由最
外层电子数和
决 电子层数共同
反
反
定
决定。主要由 原子最外层电
映
映 子数决定。
周期表中位置
相似性,递变性
元素性质
推断
7个周期 16个族
同一周期 同一主族
1 H →He 2
1
2 Li→Ne 8
2
3 Na→Ar 8
3
4 K →Kr 18
4
5 Rb→Xe 18
5
6 Cs→Rn 32
6
7 Fr→… 26
7
(2)族:
①概念:元素周期表共有18列。周期表中的第8、
9、10三个纵列是一个族,叫做第Ⅷ族,其余15
个纵列,每个纵列成为一族。共16个族。 ②族的分类及表示:七主七副一零族一Ⅷ族
M L k
8 8 2
4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
5 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54
57
6 55 56 - 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
4、下表是元素周期表的一部分,针对所给的10种元素, 完成下列各小题。
主族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 周期
2
①② ③
九年级化学化学元素周期表顺口溜
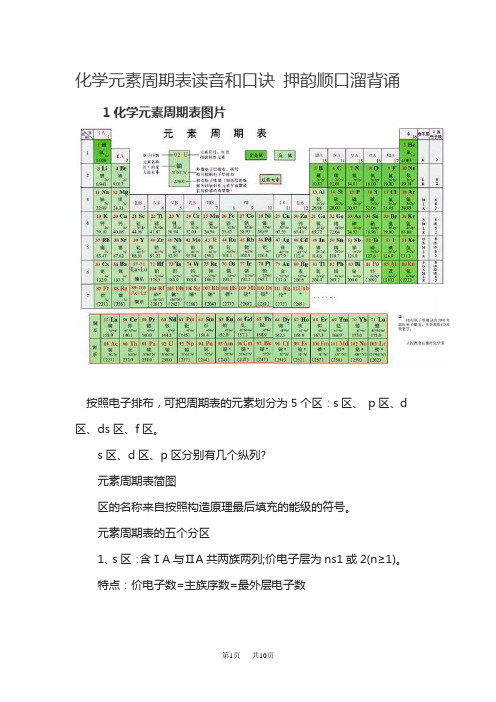
化学元素周期表读音和口诀押韵顺口溜背诵1化学元素周期表图片按照电子排布,可把周期表的元素划分为5个区:s区、p区、d 区、ds区、f区。
s区、d区、p区分别有几个纵列?元素周期表简图区的名称来自按照构造原理最后填充的能级的符号。
元素周期表的五个分区1、s区:含ⅠA与ⅡA共两族两列;价电子层为ns1或2(n≥1)。
特点:价电子数=主族序数=最外层电子数注意:①并不是所有价电子层为ns1或2的元素都在S区,He 除外(它在p区).②除H外,都是金属元素2、p区:含ⅢA至ⅦA及零族共六族六列;价电子层为ns2 np1-6(n≥2) 。
特点:①价电子总数=主族序数(零族除外);②以非金属元素为主。
注意:He在p区,但它无p电子元素周期表3、d区:含ⅢB至ⅦB和Ⅷ族共六族八列。
(镧系和锕系属f区);价电子层为(n-1)d1-9ns1-2。
特点:①均为金属元素;②价电子总数=副族序数;若价电子总数为8、9、10,则为Ⅷ族。
注意:有元素在d区但并不符合(n-1)d1-9ns1-2规则,如:46Pd 4d10。
4、ds区:含ⅠB与ⅡB共两族两列;价电子层为(n-1)d10ns1或2特点:①价电子总数=所在的列序数;②均为金属元素;且d轨道电子全充满,一般不参与化学键的形成。
5、f区:包括镧系与锕系;价电子层(n-2)f0-14(n-1)d0-2ns2。
说明:由于最外层电子数基本相同,(n-1)d电子数也基本相同,一般是(n-2)f的电子数不同,因此镧系元素化学性质相似;锕系元素化学性质也相似。
2化学元素周期表读音20个常考化学元素1氢(qīng) 2氦(hài) 3锂(lǐ) 4铍(pí)5 硼(péng) 6碳(tàn) 7氮(d àn) 8氧(yǎng) 9氟(fú) 10氖(nǎi) 11钠(nà) 12镁(měi) 13铝(lǚ) 14硅(guī) 15磷(lín) 16硫(liú) 17氯(lǜ) 18氩(yà) 19钾(jiǎ) 20钙(gài)不常考化学元素21钪(kàng) 22钛(tài)23 钒(fán) 24铬(gè) 25锰(měng) 26铁(ti ě) 27钴(gǔ)28 镍(niè)29 铜(tóng)30 锌(xīn) 31镓(jiā) 32锗(zh ě) 33砷(shēn) 34硒(xī) 35溴(xiù) 36 氪(kè) 37铷(rú) 38锶(s ī) 39钇(yǐ) 40锆(gào) 41铌(ní) 42钼(mù) 43锝(dé) 44钌(liǎo) 45铑(lǎo) 46钯(bǎ) 47银(yín) 48镉(gé) 49铟(yīn) 50锡(xī) 51锑(tī) 52碲(dì) 53碘(diǎn) 54氙(xiān) 55铯(sè) 56钡(bèi) 57镧(lán) 58铈(shì) 59镨(pǔ) 60 钕(nǚ) 61钷(pǒ) 62钐(shān) 63铕(yǒu) 64钆(gá) 65铽(tè) 66镝(dī) 67钬(huǒ) 68 铒(ěr) 69铥(diū)70 镱(yì) 71镥(lǔ) 72铪(hā) 73 钽(tǎn) 74钨(wū) 75铼(l ái) 76锇(é) 77铱(yī) 78铂(bó) 79 金(jīn) 80汞(gǒng) 81铊(t ā) 82铅(qiān)83 铋(bì) 84钋(pō) 85砹(ài) 86氡(dōng) 87钫(fāng) 88镭(léi) 89 锕(ā) 90钍(tǔ) 91 镤(pú) 92铀(yóu) 93镎(n á)94 钚(bù) 95 镅(méi) 96锔(jú)97 锫(péi) 98锎(kāi) 99锿(āi) 100镄(fèi) 101钔(mén) 102锘(nuò) 103铹(láo) 104 钅卢(lú) 105钅杜(dù) 106钅喜(xǐ)107钅波(bō)108 钅黑(hēi)109 钅麦(mài)110 钅达(dá) 111钅仑(lún)3巧记化学元素周期表口诀先用2分钟时间看一个不伦不类的小故事:侵害:从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。
元素化学主族部分

元素化学主族部分主族元素部分卤素⼀、通性卤素位于周期表第七主族, 价层电⼦构型ns 2np 5,包括F 、Cl 、Br 、I 、At 五种元素(⼀)卤素原⼦的物理性质 1. 从上到下,原⼦半径、离⼦半径增⼤2. 易得电⼦形成阴离⼦1/2X 2+e -→X-3. 第⼀电离能从 F →I 依次减⼩4. 电负性从F →I 减⼩ 5.Φθ(X 2/X-)值从F→I 逐渐减⼩6. 氧化值: F (-1,0)Cl ,Br ,I (-1,0,+1,+3,+5,+7)(⼆)卤素的存在卤素以X-负⼀价离⼦的形式存在于矿⽯和海⽔中 F: 存在于萤⽯CaF 2、冰晶⽯Na 3AlF 6、氟磷灰⽯Ca 5F(PO 4)3Cl: 主要存在于海⽔、盐湖、盐井,盐床中,主要有钾⽯盐KCl 、光卤⽯KCl ·MgCl 2.6H 2O Br: 主要存在于海⽔中 I: 主要被海藻所吸收 At: 放射性元素,⼈⼯合成X 2+H 2=2HX (反应条件)发⽣氧化反应⽽放出氧⽓ 2X 2+2H 2O=4H ++4X -+O 2↑F 2,Cl 2,Br 2能与⽔发⽣氧化反应,⽽I 2不能发⽣此反应能发⽣:4I -+O 2+4H +=2I 2+2H 2O卤素元素符号 F Cl Br I 价电⼦构型 2s 22p 5 3s 23p 5 4s 24p 5 5s 25p 5 常见氧化态 -I-I,0,I,III,V ,VII -I,0,I,III,V ,VII -I,0,I,III,V ,VII 共价半径/pm 64 99 114.2 133.3电负性 3.98 3.16 2.96 2.66 电离能/(kJ/mol )1681 1251 1140 1008X 2+H2O=H ++X -+HXO 歧化反应时X 2发⽣异裂的结果 X -+X ++OH -+H +=HX+XOH∵Cl +→I +得电⼦能⼒减弱∴歧化程度越来越⼩ K(Br 2)=7.2×10-9 ; K(I 2)=2.0×10-13 通常所⽤的氯⽔、溴⽔和碘⽔主要成分是单质。
化学元素周期表

的1表示最外层电子的数目(是电子自旋态以及pauli原理决定的)。
详情请参考量子力学。
1 H 1s12 He 1s23 Li 2s14 Be 2s25 B 2s2 2p16 C 2s2 2p27 N 2s2 2p38 O2s2 2p49 F 2s2 2p510 Ne 2s2 2p611 Na 3s112 Mg 3s213 Al 3s2 3p114 Si 3s2 3p215 P 3s2 3p316 S 3s2 3p417 Cl 3s2 3p518 Ar 3s2 3p619 K 4s120 Ca 4s221 Sc 3d1 4s222 Ti 3d2 4s223 V 3d3 4s224 Cr 3d5 4s125 Mn 3d5 4s226 Fe 3d6 4s227 Co 3d7 4s228 Ni 3d8 4s229 Cu 3d10 4s130 Zn 3d10 4s231 Ga 4s2 4p132 Ge 4s2 4p233 As 4s2 4p334 Se 4s2 4p435 Br 4s2 4p536 Kr 4s2 4p637 Rb 5s138 Sr 5s239 Y 4d1 5s240 Zr 4d2 5s241 Nb 4d4 5s142 Mo 4d5 5s143 Tc 4d5 5s244 Ru 4d7 5s145 Rh 4d8 5s146 Pd 4d1047 Ag 4d10 5s148 Cd 4d10 5s249 In 5s2 5p150 Sn 5s2 5p251 Sb 5s2 5p352 Te 5s2 5p453 I 5s2 5p554 Xe 5s2 5p655 Cs 6s156 Ba 6s257 La 5d1 6s258 Ce 4f1 5d1 6s259 Pr 4f3 6s260 Nd 4f4 6s261 Pm 4f5 6s262 Sm 4f6 6s263 Eu 4f7 6s264 Gd 4f7 5d1 6s265 Tb 4f9 6s266 Dy 4f10 6s267 Ho 4f11 6s268 Er 4f12 6s269 Tm 4f13 6s270 Yb 4f14 6s271 Lu 4f14 5d1 6s272 Hf 5d2 6s273 Ta 5d3 6s274 W 5d4 6s275 Re 5d5 6s276 Os 5d6 6s277 Ir 5d7 6s278 Pt 5d9 6s179 Au 5d10 6s180 Hg 5d10 6s281 Tl 6s2 6p182 Pb 6s2 6p283 Bi 6s2 6p384 Po 6s2 6p485 At 6s2 6p586 Rn 6s2 6p687 Fr 7s188 Ra 7s289 Ac 6d1 7s290 Th 6d2 7s291 Pa 5f2 6d1 7s292 U 5f3 6d1 7s293 Np 5f4 6d1 7s294 Pu 5f6 7s295 Am 5f7 7s296 Cm 5f7 6d1 7s297 Bk 5f9 7s298 Cf 5f10 7s299 Es 5f11 7s2100 Fm 5f12 7s2101 Md (5f13 7s2) 102 No (5f14 7s2) 103 Lr (5f14 6d17s2) 104 Rf (6d2 7s2)105 Db (6d3 7s2)106 Sg 5f146d47s2 107 Bh 5f146d57s2 108 Hs 5f146d67s2 109 Mt 5f146d77s2 110 Ds 5f146d97s1 111 Rg 5f146d107s1112 Cn 5f146d107s2113 Uut 5f146d107s27p1114 Uuq 5f146d107s27p2115 Uup 5f146d107s27p3116 Uuh 5f146d107s27p4117 Uus 5f146d107s27p5118 Uuo 5f146d107s27p61 原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
专题10元素及物质的分类-2022年中考化学二模分类汇编(上海)-

专题10元素及物质的分类2022年中考化学二模分类汇编(上海)一、单选题(共0分)1.(2022·上海奉贤·统考二模)氯元素以游离态存在的物质是A.Cl2B.HCl C.KClO3D.FeCl2【答案】A【详解】单质中的元素以游离态存在,故氯气中的氯元素以游离态存在,故选A。
2.(2022·上海虹口·统考二模)氧元素以游离态存在的是A.臭氧B.双氧水C.二氧化锰D.食盐水【答案】A【详解】A、氧气是由氧元素组成的纯净物,属于单质,氧元素以游离态存在,故符合题意;B、双氧水(过氧化氢)是由两种元素组成的化合物,则氧元素以化合态存在,故不符合题意;C、二氧化锰是由氧元素和锰元素组成的的纯净物,属于化合物,其中氧元素以化合态存在,故不符合题意;D、食盐水由氯化钠和水两种物质组成,水是由氢元素和氧元素组成,其中氧元素以化合态存在,故不符合题意;.故选A。
3.(2022·上海长宁·统考二模)空气的成分中氧元素以游离态存在的是A.氧气B.氮气C.二氧化碳D.水蒸气【答案】A【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成。
纯净物又分为单质和化合物。
由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物。
氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素。
元素以单质形式存在叫游离态,元素以化合物的形式存在叫化合态。
【详解】A、氧气中氧元素只以游离态存在,故选项正确;B、氮气中氮元素只以游离态存在,故选项错误;C、二氧化碳中氧元素只以化合态存在,故选项错误;D、水蒸气中氧元素只以化合态存在,故选项错误。
故选:A。
4.(2022·上海金山·统考二模)物质中氮元素以游离态形式存在的是A.N2B.HNO3C.NH4Cl D.NO2【答案】A【分析】元素以游离态存在即是以单质形式存在。
人教版九年级上册化学 第三单元 物质构成的奥秘 知识点总结

课题一分子和原子一、物质由微观粒子构成1.物质是由分子、原子等微观粒子构成的。
2.分子的性质:(微观粒子均有以下几点性质)①分子的质量和体积很小。
②分子总是在不断运动的。
(温度越高,分子能量越高,分子运动速率越快)③分子间有间隔。
物质三态:固—液—气分子间隔:小→大(热胀冷缩)物质的三态变化,只是分子间间隔发生了改变,分子本身不变,分子本身的质量、大小均不变。
④同种分子性质相同,不同种分子性质不同。
3.用分子观点解释纯净物与混合物。
(例如:该物质由分子构成)纯净物:由一种分子构成的物质。
混合物:由两种或两种以上分子构成的物质。
二、分子可以分为原子1.分子、原子的定义及关系:⑴分子是保持物质化学性质的最小粒子。
(该物质由分子构成)注:①最小:不可再分,发生化学变化时可分。
②当物质由原子构成,原子保持该物质的化学性质。
⑵原子是化学变化中的最小粒子。
注:①最小:化学变化中不可再分,物理变化时可分。
⑶分子是由原子构成的。
原子可以构成分子,原子也可以直接构成物质。
①有些分子由同种原子构成。
②大多数分子由两种或两种以上原子构成。
③不同的分子、原子的质量和大小不能直接拿来比较。
同一分子中原子的质量和大小小于该分子。
④分子、原子的本质区别:在化学变化中,分子可分,原子不可再分。
⑤化学变化的实质:分子破裂成原子,原子重新组合构成新的分子。
2.用分子观点来解释物理变化与化学变化。
(该物质由分子构成)物理变化的实质:分子本身不变、分子间隔改变。
化学变化的实质:分子本身改变,分子间隔改变。
同:分子间隔都改变。
异:物理变化中分子不变。
物质在发生化学变化的过程中,会同时发生物理变化。
3.物质的构成:⑴⑵分子、原子都是构成物质的粒子。
4.物质构成分分类⑴分子构成的物质①常见气体(除稀有气体):氮气、氧气、氢气、氯气、二氧化碳、氯化氢、氨气、甲烷。
②某些液体:水、过氧化氢、乙醇③某些固体:五氧化二磷⑵原子构成的物质①金属:铜、铁、铝、银、汞②常温下呈固态的某些固态非金属:碳、磷、硫、硅③稀有气体:氦、氖、氩、氪、氙、氡。
元素和元素符号

12 Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar
这个表是依据什么而画出来的呢?
1. 电子层数相同的元素,排在同一横行 2. 最外层电子层数相同的元素,排在同一纵行。 假如我们用这样的方法将已知的100多种元素排列 起来,列成一个表,那这个表就叫做元素周期表。
元素周期表
使用 范围 联系
元素的概念建立在原子的基础上,即具有相同核电荷数 的一类原子的总称。 原子的核电荷数(质子数)决定元素的种类。
举例
水里含有氢元素和氧元素。 一个水分子是由两个氢 水是由氢元素和氧元素组成的。原子和一个氧原子构成的。
1~18号元素的性质研究
1H 3 Li 11 Na 4 Be 5B 6C 7N 8O 9F 2 He 10 Ne
57L
a 镧 89A c 锕
58 Ce
59 Pr
60 Nd
61 62 Pm Sm
63 Eu
64 Gd
65 Tb
66 Dy
67 Ho
90
Th
91
Pa
92
U
93
Np
94
Pu
95
Am
96
Cm
97
Bk
98
Cf
99
Es
6 69 70 71Lu 8 Tm Yb 镥 Er 10 10 10 103Lr 0 1 2 铹
金属元素主要分布在元素周期表的 左边。每一周期开头都是金属元素。
非金属元素主要分布在元素周期表的 右边。
稀有气体元素分布在元素周 期表的最后一纵行。
推测:元素的性质,新元素等。
2 . 作用: 查找:元素符号,相对原子质量等。
推测:元素的性质,新元素等。
中考总复习化学2-第10讲 构成物质的微粒、元素 (2)

3.元素周期表的规律 (1)同一周期的元素,原子的电子层数相同;由左往右,最外层电子数依次从 1递增至8(第一周期除外);第一周期为气体元素,其他周期的元素种类依次 为金属→非金属→稀有气体。 (2)同一族的元素,最外层电子数相同,化学性质相似(氢除外);从上到下, 电子层数递增。
【归纳总结】 周期数=原子核外电子层数,如钠原子核外有3个电子层,则钠元素位于元素 周期表的第三周期。
知识考点清单 考点 1 构成物质的微粒
1.构成物质的微粒有① 分子、原子、离子 。 2.由② 分子 构成的物质,如氢气、氧气、水、二氧化碳等。 由③ 原子 构成的物质,如铁、铜、氦气、金刚石、硫等。 由④ 离子 构成的物质,如氯化钠、硫酸铜等。
【归纳总结】各微粒之间的关系:
考点 2 分子和原子 1.分子和原子的异同
B.
——铝原子
C. 2He——2个氦元素
D. 2NO2——2个二氧化氮分子
9
10
返回命题点导航
10.(2014·河北6题,2分)分析推理是化学学习中常用的思维方法。下列分 析推理正确的是 ( B ) A.浓硫酸具有吸水性,所以浓盐酸也具有吸水性 B.O2和O3的分子构成不同,所以它们的化学性质不同 C.离子是带电荷的微粒,所以带电荷的微粒一定是离子 D.酸雨的pH小于7,所以pH小于7的雨水一定是酸雨
分子
原子
定 义
分子是⑤ 保持物质化学性质 的最 小粒子
原子是⑥ 化学变化中 的最小粒子
性 质
质量小、体积小;不断运动;有间隔;同种粒子的化学性质相同
联 系
分子是由原子构成的。分子、原子都是构成物质的微粒
区 别
在化学变化中,⑦
分子
可以再分,而⑧
化学元素周期表(最新最全)
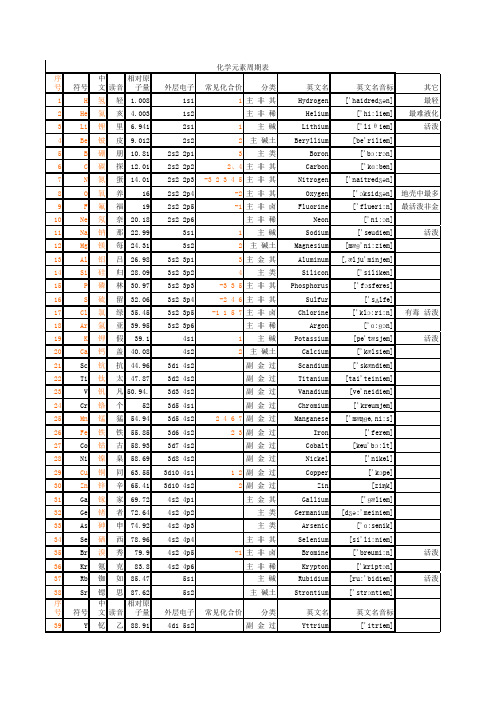
12 Mg 镁 每 24.31
13 Al 铝 吕 26.98
14 Si 硅 归 28.09
15
P 磷 林 30.97
16
S 硫 留 32.06
17 Cl 氯 绿 35.45
18 Ar 氩 亚 39.95
19
K 钾 假 39.1
20 Ca 钙 盖 40.08
21 Sc 钪 抗 44.96
22 Ti 钛 太 47.87
主类
Antimony
['æntiməni]
52 Te 碲 帝 127.6 5s2 5p4
主 类 Tellurium [te'ljuəriəm]
53
I 碘 典 126.9 5s2 5p5
主非卤
Iodine
['aiəudi:n]
54 Xe 氙 仙 131.3 5s2 5p6
主非稀
Xenon
['zenɔn]
1副 金 过
Silver
['silvə]
48 Cd 镉 隔 112.4 4d10 5s2
副金过
Cadmium
['kædmiəm]
49 In 铟 因 114.8 5s2 5p1
主金其
Indium
['indiəm]
50 Sn 锡 西 118.7 5s2 5p2
主金其
Tin
[tin]
51 Sb 锑 梯 121.8 5s2 5p3
91 Pa 镤 仆 231 5f2 6d1 7s2
92
U 铀 由 238 5f3 6d1 7s2
93 Np 镎 拿 [237] 5f4 6d1 7s2
94 Pu 钚 不 [244] 5f6 7s2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
稀有气体元素: “ 气 ” 氦(He)、氖(Ne)、氩(Ar)、氪(Kr)、氙(Xe)、氡(Rn)
元素
ቤተ መጻሕፍቲ ባይዱ
元素的分布: 1、空气中含量位居前两位的元素:
氮(N)、氧(O)
2、地壳中含量位居前四位的元素: 氧(O)、硅(Si)、铝(Al)、铁(Fe)
地壳中含量最高的非金属元素和金属元素 分别是什么?
元素的分类
预习导入微课
元素——宇宙大爆炸
(安装flash播放器插件后,播放幻灯片点击▶按钮,等待加载播放)
金属元素:“ 钅”(除汞) “汞”是唯一一个在常温下呈液态的金属
非金属元素: 气态非金属元素:“ 气 ”,如:氧(O)、氮(N) 液态非金属元素:“ 氵”,如:溴(Br) 固态非金属元素:“ 石 ”,如:碳(C)、磷(P)
非金属元素: 氧(O) 金属元素: 铝(Al)
元素的分布: 1、空气中含量位居前两位的元素:
氮(N)、氧(O)
2、地壳中含量位居前四位的元素: 氧(O)、硅(Si)、铝(Al)、铁(Fe)
3、生物细胞当中含量位居前四位的元素: 氧(O)、碳(C)、氢(H)、氮(N) (非金属元素)
