13CNMR 核磁共振碳谱化学位移总览表+++
合集下载
13C-NMR

整理ppt
13C-核磁共振波谱的特点
• ②给出不与氢相连的碳的共振吸收峰。季碳、C=
O、C=C=C、C≡C、N=C=O、C≡N等基团中的碳不与 氢直接相连,从氢谱中得不到直接的信息,只能靠分子式 及其对相邻基团值的影响来判断。而在碳谱中均能给出各 自的特征吸收峰。
整理ppt
13C-核磁共振波谱的特点
整理ppt
4. 门控去偶
质子噪声去偶失去了所有的偶合信息,偏共振去偶也 损失了部分偶合信息,而且都因NOE不同而使信号的相 对强度与所代表的碳原子数目不成比例。为了测定真正 的偶合常数或做各类碳的定量分析,可以采用门控去偶 或反转门控去偶的办法。
在脉冲傅立叶变换核磁共振波谱仪中有发射门(用以 控制射频脉冲的发射时间)和接受门(用以控制接受器 的工作时间)。门控去偶是指用发射门及接受门来控制 去偶的实验方法,用这种方法与用单共振法获得的13CNMR谱较为相似,但用单共振法得到同样一张谱图,需 要累加的次数更多,耗时很长。门控去偶法借助于NOE 的帮助,在一定程度上补偿了这一方法的不足。
δ C 2 5 0 .3
2 2 0 .2
1 9 1 .1
整理ppt
3.助电子基团及其密集性
①卤素 (主要为诱导效应。电负性基团会使邻近13C
核去屏蔽。基团的电负性越强,去屏蔽效应越大。)
F Cl Br I 电负性δC-F >δC-Cl >δC-Br >δC-I,
其中 I 的效应是屏整蔽理pp效t 应(高场)
偶的碳谱,各个裂分的谱线彼此交叠,很难识别。故常规 的碳谱都是质子噪声去偶谱,去掉了全部13C-1H偶合,
得到的各种碳的谱线都是单峰。
整理ppt
13C-核磁共振波谱的特点
13C-核磁共振波谱的特点
• ②给出不与氢相连的碳的共振吸收峰。季碳、C=
O、C=C=C、C≡C、N=C=O、C≡N等基团中的碳不与 氢直接相连,从氢谱中得不到直接的信息,只能靠分子式 及其对相邻基团值的影响来判断。而在碳谱中均能给出各 自的特征吸收峰。
整理ppt
13C-核磁共振波谱的特点
整理ppt
4. 门控去偶
质子噪声去偶失去了所有的偶合信息,偏共振去偶也 损失了部分偶合信息,而且都因NOE不同而使信号的相 对强度与所代表的碳原子数目不成比例。为了测定真正 的偶合常数或做各类碳的定量分析,可以采用门控去偶 或反转门控去偶的办法。
在脉冲傅立叶变换核磁共振波谱仪中有发射门(用以 控制射频脉冲的发射时间)和接受门(用以控制接受器 的工作时间)。门控去偶是指用发射门及接受门来控制 去偶的实验方法,用这种方法与用单共振法获得的13CNMR谱较为相似,但用单共振法得到同样一张谱图,需 要累加的次数更多,耗时很长。门控去偶法借助于NOE 的帮助,在一定程度上补偿了这一方法的不足。
δ C 2 5 0 .3
2 2 0 .2
1 9 1 .1
整理ppt
3.助电子基团及其密集性
①卤素 (主要为诱导效应。电负性基团会使邻近13C
核去屏蔽。基团的电负性越强,去屏蔽效应越大。)
F Cl Br I 电负性δC-F >δC-Cl >δC-Br >δC-I,
其中 I 的效应是屏整蔽理pp效t 应(高场)
偶的碳谱,各个裂分的谱线彼此交叠,很难识别。故常规 的碳谱都是质子噪声去偶谱,去掉了全部13C-1H偶合,
得到的各种碳的谱线都是单峰。
整理ppt
13C-核磁共振波谱的特点
13C核磁共振波谱及谱图解析示例

12 2021/4/15
谱图去偶作用对比
13 2021/4/15
谱图去偶作用对比
14 2021/4/15
四、13C NMR谱图
1.C7H14O 1H 4H 4H
6H 13C
S
2.3 1.5 0.9
210
2021/4/15
q t t
43 18 12
15
13C NMR谱图2
2.C9H10O 1H
θ=90 。, CH的最大正信号,其它无信号
θ=90。 θ=45。
θ=135
。
, CH,
CH3非最大正信号,CH2最大负
信号
因此,取θ=135,。可确定CH;θ=135,。可确
定CH、CH3和CH2(倒峰)
20 2021/4/15
碳-氢相关谱
ONO
21 2021/4/15
谱图的综合解析 例1: 某含氧化合物分子无对称性,根据13C NMR确定其结构
3 2021/4/15
溶剂的化学位移
• CDCl3: 77.0 (t);
• CD3COCD3: 30.0(7)、206.8(s);
• CD3OD: 49.3(7);
• C6D6:
128.7(t);
• CD3SOCD3: 39.7(7);
4 2021/4/15
化学位移规律:烷烃
碳数n >4 端甲基 C=13-14
O OH
22 2021/4/15
例2:
某化合物C8H8O,根据13C NMR解析其结构
CH 3 O
23 2021/4/15
例3:
某化合物C9H12,根据13C NMR解析其结构
CH3
CH2CH3
谱图去偶作用对比
13 2021/4/15
谱图去偶作用对比
14 2021/4/15
四、13C NMR谱图
1.C7H14O 1H 4H 4H
6H 13C
S
2.3 1.5 0.9
210
2021/4/15
q t t
43 18 12
15
13C NMR谱图2
2.C9H10O 1H
θ=90 。, CH的最大正信号,其它无信号
θ=90。 θ=45。
θ=135
。
, CH,
CH3非最大正信号,CH2最大负
信号
因此,取θ=135,。可确定CH;θ=135,。可确
定CH、CH3和CH2(倒峰)
20 2021/4/15
碳-氢相关谱
ONO
21 2021/4/15
谱图的综合解析 例1: 某含氧化合物分子无对称性,根据13C NMR确定其结构
3 2021/4/15
溶剂的化学位移
• CDCl3: 77.0 (t);
• CD3COCD3: 30.0(7)、206.8(s);
• CD3OD: 49.3(7);
• C6D6:
128.7(t);
• CD3SOCD3: 39.7(7);
4 2021/4/15
化学位移规律:烷烃
碳数n >4 端甲基 C=13-14
O OH
22 2021/4/15
例2:
某化合物C8H8O,根据13C NMR解析其结构
CH 3 O
23 2021/4/15
例3:
某化合物C9H12,根据13C NMR解析其结构
CH3
CH2CH3
核磁共振碳谱汇总.

13C化学位移的分布范围比1H大。
由于具有长的T1值以及NOE效应的存在,在常规13C谱中,峰的 强度不能反映碳原子的数量。
13C核的天然丰度和灵敏度比1H核低得多,所以需要大量的样品 和较长的采样时间。 在同一种氘代溶剂中,13C和1H溶剂峰的多重性不同。
13C
NMR 较之1H NMR的一些主要区别
Granrt-Paul Corrective terms Skl (Branched chain alkanes)
Skl(ppm) 1。(3。) 1。(4。) Al(ppm) 9.1± 0.10 9.4± 0.10 -2.5± 0.10 0.3± 0.10 0.1± 0.10 2。(3。) 2。(4。) -1.10±0.20
c (k ) 2.3 Al nkl Skl
19F
- 13C偶合常数
1J F
C
2J
CF
31P
- 13C偶合常数
1J
CP
2J
CP
3J
CP
2H
- 13C偶合常数
1J
CD
13C
NMR 较之1H NMR的一些主要区别
在常用的CPD(连续序列组合脉冲)或宽带去偶的13C谱中,峰 型呈单峰,除非分子中含有其他磁性核,如2H,31P,19F。
13C化学位移的分布范围比1H大。
由于具有长的T1值以及NOE效应的存在,在常规13C谱中,峰的 强度不能反映碳原子的数量。
13C核的天然丰度和灵敏度比1H核低得多,所以需要大量的样品 和较长的采样时间。 在同一种氘代溶剂中,13C和1H溶剂峰的多重性不同。
1H
Chemical Shifts of Common Structures
由于具有长的T1值以及NOE效应的存在,在常规13C谱中,峰的 强度不能反映碳原子的数量。
13C核的天然丰度和灵敏度比1H核低得多,所以需要大量的样品 和较长的采样时间。 在同一种氘代溶剂中,13C和1H溶剂峰的多重性不同。
13C
NMR 较之1H NMR的一些主要区别
Granrt-Paul Corrective terms Skl (Branched chain alkanes)
Skl(ppm) 1。(3。) 1。(4。) Al(ppm) 9.1± 0.10 9.4± 0.10 -2.5± 0.10 0.3± 0.10 0.1± 0.10 2。(3。) 2。(4。) -1.10±0.20
c (k ) 2.3 Al nkl Skl
19F
- 13C偶合常数
1J F
C
2J
CF
31P
- 13C偶合常数
1J
CP
2J
CP
3J
CP
2H
- 13C偶合常数
1J
CD
13C
NMR 较之1H NMR的一些主要区别
在常用的CPD(连续序列组合脉冲)或宽带去偶的13C谱中,峰 型呈单峰,除非分子中含有其他磁性核,如2H,31P,19F。
13C化学位移的分布范围比1H大。
由于具有长的T1值以及NOE效应的存在,在常规13C谱中,峰的 强度不能反映碳原子的数量。
13C核的天然丰度和灵敏度比1H核低得多,所以需要大量的样品 和较长的采样时间。 在同一种氘代溶剂中,13C和1H溶剂峰的多重性不同。
1H
Chemical Shifts of Common Structures
13C-核磁共振光谱 -2

CH3 CH3 1 CH 2 CH2 3 CH2 4 Cl
例2.有两个有机物A、B,分子式均为C5H10,由气相色谱分离, 其13C谱数据如下: A:13(q),17(q),26(q),118(d),132(s) B:13(q),22(q),31(t),108(t),147(s) 解: 1、两个碳氢化合物均含有一个Ω,可知其分子内含有一个 双键(在100~160范围内均有两个峰)。 2、它们都没有等价的碳原子,由各峰的多重性可指示出分 子中所需的的10个氢原子; A化合物中含有3个甲基及1个 sp2杂化的CH;而B中有两个甲基,1个sp3的CH2和一个sp2 的CH2
酮,醛>羧酸>羧酸衍生物(酰胺、酰氯、酸酐、酯)
苯环碳谱出峰数目:
无对称性: 单取代: 对位取代: 6个峰 4个峰 4个峰
X
X
Y X Y
R
Y
邻位相同取代基: 3个峰 间位三相同取代基:2个峰 单个苯环不可能只有5个碳峰!
X X
X X X
例1. C5H11Cl ,COM如图。
22.0q 25.7d 41.6t 43.1t
2
照射3.91,7.40有NOE增益
3 1 2
1
1
COOH
OCH3 C 6 H4
1Hale Waihona Puke 0503、 C5H10O
HOCH2-CH2-CH2CH=CH2
C4H6O2 1
CH3-CH=CH-COOH
3 1
注:1H-NMR中,δ12处的积分高度对应于1个H的吸收峰未画出来。
解: 1、不饱和度Ω=0,所以,该化合物为链状饱和氯代烷。 2、13C-NMR谱中共有四个峰,而分子式中有五个碳,故分子结 构中有对称因素。 δ22.0处的甲基峰强度很大,表明有两个等价 的甲基(CH3)。 3、根据偏共振去偶13C谱中的裂分情况可知,分子中有如下的结 构单元: CH3(22.0q),CH(25.7d),CH2(41.6t),CH2(43.1t)
例2.有两个有机物A、B,分子式均为C5H10,由气相色谱分离, 其13C谱数据如下: A:13(q),17(q),26(q),118(d),132(s) B:13(q),22(q),31(t),108(t),147(s) 解: 1、两个碳氢化合物均含有一个Ω,可知其分子内含有一个 双键(在100~160范围内均有两个峰)。 2、它们都没有等价的碳原子,由各峰的多重性可指示出分 子中所需的的10个氢原子; A化合物中含有3个甲基及1个 sp2杂化的CH;而B中有两个甲基,1个sp3的CH2和一个sp2 的CH2
酮,醛>羧酸>羧酸衍生物(酰胺、酰氯、酸酐、酯)
苯环碳谱出峰数目:
无对称性: 单取代: 对位取代: 6个峰 4个峰 4个峰
X
X
Y X Y
R
Y
邻位相同取代基: 3个峰 间位三相同取代基:2个峰 单个苯环不可能只有5个碳峰!
X X
X X X
例1. C5H11Cl ,COM如图。
22.0q 25.7d 41.6t 43.1t
2
照射3.91,7.40有NOE增益
3 1 2
1
1
COOH
OCH3 C 6 H4
1Hale Waihona Puke 0503、 C5H10O
HOCH2-CH2-CH2CH=CH2
C4H6O2 1
CH3-CH=CH-COOH
3 1
注:1H-NMR中,δ12处的积分高度对应于1个H的吸收峰未画出来。
解: 1、不饱和度Ω=0,所以,该化合物为链状饱和氯代烷。 2、13C-NMR谱中共有四个峰,而分子式中有五个碳,故分子结 构中有对称因素。 δ22.0处的甲基峰强度很大,表明有两个等价 的甲基(CH3)。 3、根据偏共振去偶13C谱中的裂分情况可知,分子中有如下的结 构单元: CH3(22.0q),CH(25.7d),CH2(41.6t),CH2(43.1t)
CNMR

γ 2π
C 0
各类碳的化学位移范围
羰基碳>150
饱和碳原子:0~100 不直接与杂原子 C相连的<55 50 0
烯碳和芳碳:90~160
不饱和碳原子:90~200 200 150 100
13C
Chemical Shift Ranges
3.影响化学位移的因素
• • • • • • (1)杂化状态 (2)诱导效应 (3)空间效应 (4)共轭效应 (5)重原子效应 (6)分子内氢键
合,谱复杂难解析
1.质子噪音去偶
• (全氢去偶,宽带去偶)
消除了质子对13C偶合,不同碳都是单峰,除季碳外信号强度增强。
2.偏共振去偶:
偏共振去偶
3.质子选择性去耦
• 用一个很小功率的射频以某一特定质子 的共振频率进行照射,观察碳谱,结果 与该质子直接相连的碳会发生全部去耦 而变成尖锐的单峰,并且由于NOE,峰 信号增强。对于分子中其他的碳核,仅 受到不同程度的偏移照射(△ν≠0),产 生不同程度的偏共振去耦。 • 2—苄基—丙二酸二乙酯的选择性去耦谱。
205.5
(4)共轭效应
•
NH2
147.7 116.1 129.8
119.0
128.5
• -CO-H • -CO-CH3 • -COOH • -CONH2 • -COCl
201 204 177 172 170
(5)重原子效应
(6)分子内氢键
O O
191.5 O H O 196.9
195.7 O H O 204.1
1. H-H COSY
Y 3 CH2 X CH CH2 CH3 1 2 4
2. C-H COSY (乙苯)
4. DEPT实验
C 0
各类碳的化学位移范围
羰基碳>150
饱和碳原子:0~100 不直接与杂原子 C相连的<55 50 0
烯碳和芳碳:90~160
不饱和碳原子:90~200 200 150 100
13C
Chemical Shift Ranges
3.影响化学位移的因素
• • • • • • (1)杂化状态 (2)诱导效应 (3)空间效应 (4)共轭效应 (5)重原子效应 (6)分子内氢键
合,谱复杂难解析
1.质子噪音去偶
• (全氢去偶,宽带去偶)
消除了质子对13C偶合,不同碳都是单峰,除季碳外信号强度增强。
2.偏共振去偶:
偏共振去偶
3.质子选择性去耦
• 用一个很小功率的射频以某一特定质子 的共振频率进行照射,观察碳谱,结果 与该质子直接相连的碳会发生全部去耦 而变成尖锐的单峰,并且由于NOE,峰 信号增强。对于分子中其他的碳核,仅 受到不同程度的偏移照射(△ν≠0),产 生不同程度的偏共振去耦。 • 2—苄基—丙二酸二乙酯的选择性去耦谱。
205.5
(4)共轭效应
•
NH2
147.7 116.1 129.8
119.0
128.5
• -CO-H • -CO-CH3 • -COOH • -CONH2 • -COCl
201 204 177 172 170
(5)重原子效应
(6)分子内氢键
O O
191.5 O H O 196.9
195.7 O H O 204.1
1. H-H COSY
Y 3 CH2 X CH CH2 CH3 1 2 4
2. C-H COSY (乙苯)
4. DEPT实验
核磁共振碳谱-2014

N para N
故直接影响
依次增大.
δ C-C < δ C ≡ C < δ C = C < δ C = O δ sp3 δ sp3 : δ sp < δ sp < δ sp2 0 ~ 60ppm 70 ~ 90ppm 100 ~ 160ppm 160 ~ 220ppm
-CH3 , -CH2 , - >CH -, >C = C< (烯烃,芳烃) >C = O
SOCH3
N
OCH3
5.羰基化合物 羧酸, 酯类, 酰胺, 酰氯:
160~ 180ppm
醛类, 酮类: 180~220ppm
25.1 27.1 41.9 211.3
129.0
192.4 CHO 136.4
172.6 COOH 130.2 133.7 128.4 129.4
134.2
O
167.1 COOCH3
C O C C C N C O
2. 氢谱的δ值一般不超过10ppm,而碳谱的变化范围 可超过200ppm。因此,分子量在三四百内、无对称性的有 机分子的每一个碳原子,均可找到相应的谱线。但对氢谱 而言,经常出现谱线的重叠。
3.碳谱有多种多重共振方法,可区别碳原子 级数(如DEPT谱),因此,较之氢谱信息丰 富、结论清楚。
CH2 CH CH2 CH2 CH3 114.3 138.5 CH3 CH3 CH CH CH2 CH3 123.2 132.7
CH2 CH CH CH2CH2CH2CH3 129.3 130.5
烯烃对分子中sp3碳的化学位移影响较小。 例:
31.6 30.4
CH3
CH3
CH3
CH3
24.7
故直接影响
依次增大.
δ C-C < δ C ≡ C < δ C = C < δ C = O δ sp3 δ sp3 : δ sp < δ sp < δ sp2 0 ~ 60ppm 70 ~ 90ppm 100 ~ 160ppm 160 ~ 220ppm
-CH3 , -CH2 , - >CH -, >C = C< (烯烃,芳烃) >C = O
SOCH3
N
OCH3
5.羰基化合物 羧酸, 酯类, 酰胺, 酰氯:
160~ 180ppm
醛类, 酮类: 180~220ppm
25.1 27.1 41.9 211.3
129.0
192.4 CHO 136.4
172.6 COOH 130.2 133.7 128.4 129.4
134.2
O
167.1 COOCH3
C O C C C N C O
2. 氢谱的δ值一般不超过10ppm,而碳谱的变化范围 可超过200ppm。因此,分子量在三四百内、无对称性的有 机分子的每一个碳原子,均可找到相应的谱线。但对氢谱 而言,经常出现谱线的重叠。
3.碳谱有多种多重共振方法,可区别碳原子 级数(如DEPT谱),因此,较之氢谱信息丰 富、结论清楚。
CH2 CH CH2 CH2 CH3 114.3 138.5 CH3 CH3 CH CH CH2 CH3 123.2 132.7
CH2 CH CH CH2CH2CH2CH3 129.3 130.5
烯烃对分子中sp3碳的化学位移影响较小。 例:
31.6 30.4
CH3
CH3
CH3
CH3
24.7
13CNMR核磁共振碳谱化学位移总览表

1) INEPT法
由于核磁共振本身信号灵敏度很低,尤其是低天然丰度的核 (如13C、15N等)更为突出。INEPT法是在具有两种核自旋的系统 中,以CH为例,通过脉冲技术,把高灵敏1H核的自旋极化传递到 低灵敏的13C核上去,这样由1H到与其偶合的13C的完全极化传递可 使,13C信号强度增强4倍。
的峰的裂分应全部去除。如果还有谱线的裂分不能去除,应考虑分
子中是否含F或P等元素。 (6)从分子式和可能的结构单元,推出可能的结构式。利用化学位移 规律和经验计算式,估算各碳的化学位移,与实测值比较。 (7)综合考虑1H NMR、IR、MS和UV的分析结果,必要时进行其他 的双共振技术及τ 1测定,排除不合理者,得到正确的结构式。
δ值范围在100-150ppm,sp杂化碳的δ值范围在60-95ppm。
2.诱导效应
当电负性大的元素或基团与碳相连时,诱导效应使碳的核外 电子云密度降低,故具有去屏蔽作用。随着取代基电负性增强, 或取代基数目增大,去屏蔽作用也增强, δ值愈向低场位移。
3.共轭效应
共轭作用会引起电子云分布的变化,导致不同位置碳的共 振吸收峰向高场或低场移动。
5.弛豫时间τ1可作为化合物结构鉴定的波谱参数
在化合物中,处于不同环境的13C核,它们的弛豫时间τ1数
值相差较大,可达2-3个数量级,通过τ1可以指认结构归属,
窥测体系运动状况等。
4.2.1
脉冲傅里叶变换法
原理同1H NMR。
4.2.2
核磁共振碳谱中几种去偶技术
在有机化合物的13C NMR中,13C-13C之间的偶合由于13C的天然丰 度很低,可以不予考虑。但13C-1H核之间的偶合常数很大,如1JCH高达 120-320Hz,13C的谱线会被与之偶合的氢按n+1规律裂分成多重峰,这 种峰的裂分对信号的归属是有用的,但当谱图复杂时,加上2JCCH、
碳谱化学位移0-15

碳谱化学位移0-15
碳谱化学位移是指分子中的一个碳原子所产生的化学位移。
它通常由下式表示:
δ = (ν - νref)/νref x 10^6
其中,δ是化学位移,ν是分子中该碳原子与天然碳的共振频率,νref是参考物质的共振频率。
在常见有机分子的^13C NMR谱中,参考物质通常为二氯甲烷(CDCl3),其共振频率为77.0 MHz。
对于有机分子中的碳,它的化学位移范围通常在0到220 ppm之间。
其中,0 ppm对应的是甲基羰基碳(如乙酰基中的CH3CO-),220 ppm对应的是芳香环上的氢化碳(如苯环上的C-H)。
在其中,常见的一些化学位移值如下:
- 0-60 ppm:sp3杂化碳(如甲基、乙基、异丙基等)
- 60-90 ppm:α-烯丙基、β-烯丙基碳等
- 90-120 ppm:芳香环上的杂环、烷基等
- 120-150 ppm:烯烃、α,β-不饱和羰基、α,β-不饱和酮、α,β-不饱和酸等
- 150-220 ppm:芳香环上的加成基团(如酰基、烷氧基等)
需要特别说明的是,不同的分子、不同的实验条件(如溶剂、温度等)可能导致化学位移发生变化。
因此,在实际实验中,需要结合分子的结构和实验条件来解读^13C NMR谱。
核磁共振碳谱

反转门去偶谱表明,既达到了全去偶,S/N 提高,
又因NOE的抑制,使峰面积正比于碳原子的数目。 如下图: (a) 质子宽带去偶谱, (b) 反转门去偶谱.
ATP (attached proton test) J调制法
通过调节脉冲序列的时间间隔,使季碳和亚甲基
(CH2)碳的相位向上(正信号),次甲基(CH)和甲基
1 13
1
1H 2 13C
13C 2 1H
= 1.989 = 0.126
f
H{ C} =
(1) 因 NOE 增强不等,导致谱峰的强度与碳的数目 不成比例。 (2) 有用的偶合信息丢失,无法识别碳级。 CH3 CH2 CH C
偏共振去偶
( Off Resonance Decoupling )
,σ dai)
顺磁屏蔽(paramagnetic sielding ,σpara)
抗磁屏蔽(σ
dai)
在B0的诱导下,核外电子环流产生的与
B0场方向相反的感生磁场,σ 子云密度的增加而增加。
N dai随核外电
n C ppm
1.200 96
1.000 128.5
0.857 150
根据 Lamb 公式:
= /2 ·B0( 1-σ i)
一、屏蔽原理
抗磁屏蔽(σ 顺磁屏蔽(σ
dai)
para)
各 向 异 性 溶剂、浓度、pH值的影响
原子核的屏蔽, 是核外围电子( 原子本身的
电子和其它原子的电子)对核产生屏蔽的总和. 表
达式如下:
σ
N
=σ
N
dia
+σ
N
para
+σ
N
n
13C谱图

C=O: 160-220
3
必记基础数据
C=O: 160-220
酮: 195-220
醛: 185-205
醌: 180-190
羧酸: 160-180
酯及内酯: 165-180
酰胺及内酰胺: 160-170
4
碳谱(13C-NMR)化学位移的影响因素
a. 碳的杂化方式 sp3 < sp < sp2 10-80 60-120 90-200
37
1H-
NMR
-CH3×3 活泼氢2 活泼氢1
38
13C-NMR
-CH3×3
-C-O O-C-O
39
1H-1H
COSY
H-4
H-11
H-12 H-15 H-13
O OH
H-3β
3 4
O
OH
片断1
15
13
片断2 11
12
40
HMBC
H-15
1-OH H-14a
H-9β
H-6
H-9α
H-2α
C-14 C-10
29
30
13C-1H
COSY Spectrum(HMQC)
HMQC:归属直接相连的碳氢之间关系。
31
32
33
13C-1H远程
COSY Spectrum(HMBC)
HMBC:设定偶合常数J在10Hz左右,使2JCH 和3JCH引起的相关信号出现在图谱上,其中以
间隔三键( 3JCH )的碳氢相关为主,也可观
2. DEPT的用途:区分 -CH3 、 -CH2、-CH或季 C信号
特点:不同类型13C信号呈单峰分别朝上或向下,可 识别CH3、CH2、CH、C. 脉冲宽度 =135°CH3, CH , CH2 (常用) =90°CH , =45°CH3, CH2 , CH , 季碳不出现
碳谱图 C13

15
67.9
3.92(1H, brd, J=12.0Hz) 3.95(1H, brd, J=12.0Hz)
Note: 1. 400 MHz for 1H-NMR, 100MHz for 13C-NMR.
50 2. Using CD3OD as a solvent, TMS is the internal standard, the chemical shifts (δ)
1
O
OH
5
48
NOESY
1-OH
H-11 H-9α
H-4
H-14b
H-14a
H-12
O OH
O
c8的平面结构
H
OH
HH
14
O OH
H H
1
9
O OH
4
H
11
49
转化产物c8
O OH
O OH
1α-hydroxy-10β, 14epoxy curcumol
No.
Carbon signals
Proton signals
别伯、仲、叔、季碳。 CH3, q, CH2, t, CH, d, C, s。
11
4、选择氢去偶谱(SPD): 用很弱的能量选择性地照射特定氢核,消除它对 相关碳的偶合影响,使峰简化。
12
5、DEPT谱:改变照射氢核的第三脉冲宽度( ) 所测定的13C-NMR图谱
特点:不同类型13C信号呈单峰分别朝上或向下,
10-80 60-120 90-200
b. 碳核的电子云密度 电子云密度, 高场位移
5
影响因素
c. 取代基的诱导效应和数目
取代基数目,影响,
诱导效应随相隔键的数目增加而减弱;
波谱分析-研究生-13C化学位移
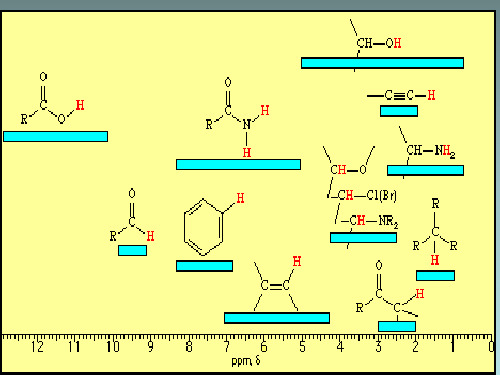
这种技术称为质子宽带去偶,也称质子噪声去偶或全 部质子去偶。(Proton noise decoupling, full proton decoupling, Proton broad band decoupling)
若化合物中不含31P、19F等,则所有碳均呈单峰,由于 13C的驰豫时间一般较长,所以每个碳峰谱线半宽度很小, 几乎都是单峰( 与T 2成反比 )。
2 2( x 2 )
x为核x的共振频率,在质子偏共振去偶实验中,核x 为质子,ν2为H2的频率。这样照射的结果,13C出现峰的分 裂,但其裂距要小于JCH,下降为Jr,Jr为剩余偶合常数, 伯,仲,叔碳分别分长为四、三、二重峰。
Jr 0 ~JCH
Proton resonance offset
是13C和1H自旋量子化方向的夹角
当 0 时,即不进行双照射时,cos 1 ,
JCH(表观)最大,为13C和1H之间的真正的偶合系数。
当 900 时,即进行双照射时, cos 0,
JCH(表观)=0 ,即为13C和1H的偶合被去除。
二.量子理论 当干扰场H2照射1H时引起的1H自旋能级上的快速
空间位置靠近(<0.5 nm)的两个原子核,当其中一个核 的自旋被干扰达到饱和时,另一个核的谱线强度也发生变 化,这就是核Overhauser效应(Nuclear Overhauser Enhancement, NOE)。 NOE的强度与核间距的六次方成 反比
由于NOE的强弱直接与两个核之间的距离有关,因此它 是立体化学和蛋白质的溶液结构测定中最重要的约束条件 NOE (max) = S/(2* I) 同核NOE,最大增强 = 50% 异核NOE,最大增强 = 200%
② 异核双共振
AX
若化合物中不含31P、19F等,则所有碳均呈单峰,由于 13C的驰豫时间一般较长,所以每个碳峰谱线半宽度很小, 几乎都是单峰( 与T 2成反比 )。
2 2( x 2 )
x为核x的共振频率,在质子偏共振去偶实验中,核x 为质子,ν2为H2的频率。这样照射的结果,13C出现峰的分 裂,但其裂距要小于JCH,下降为Jr,Jr为剩余偶合常数, 伯,仲,叔碳分别分长为四、三、二重峰。
Jr 0 ~JCH
Proton resonance offset
是13C和1H自旋量子化方向的夹角
当 0 时,即不进行双照射时,cos 1 ,
JCH(表观)最大,为13C和1H之间的真正的偶合系数。
当 900 时,即进行双照射时, cos 0,
JCH(表观)=0 ,即为13C和1H的偶合被去除。
二.量子理论 当干扰场H2照射1H时引起的1H自旋能级上的快速
空间位置靠近(<0.5 nm)的两个原子核,当其中一个核 的自旋被干扰达到饱和时,另一个核的谱线强度也发生变 化,这就是核Overhauser效应(Nuclear Overhauser Enhancement, NOE)。 NOE的强度与核间距的六次方成 反比
由于NOE的强弱直接与两个核之间的距离有关,因此它 是立体化学和蛋白质的溶液结构测定中最重要的约束条件 NOE (max) = S/(2* I) 同核NOE,最大增强 = 50% 异核NOE,最大增强 = 200%
② 异核双共振
AX
13C-NMR课件分析

13C-核磁共振波谱法
Nuclear Magnetic Resonance Spectroscopy
2020/10/17
一、概述
核磁矩:1H=2.79270; 13C=0.70216
磁旋比为质子的1/4;
相对灵敏度为质子的1/5600; PFT-NMR(1970年),实用化技术;
(pulse fourier transform )
醛、酮﹥酸﹥酯≈酰氯≈酰胺﹥酸酐
减小
210
170
羰基邻位有吸电基团将使它向低场位移;
芳香和α,β-不饱和羰基化合物,由于共 轭和诱导作用将增加羰基的电子云密度, 使它向高场位移。
2020/10/17
化学位移表1 chemical shift table
2020/10/17
化学位移表2 chemical shift table
2020/10/17
三、偶合与弛豫
13C-13C偶合的几率很小(13C天然丰度1.1%);
13C- 1H偶合;偶合常数1JCH:100-250 Hz;峰裂分;谱图复杂;
去偶方法: (1)质子噪声去偶或宽带去偶(proton noise decoupling or boradband decoupling) : 文献中均使用之
decoupling, DD)
2020/10/17
(3)交叉极化方法(cross polization,CP) (4)魔角旋转(magic angle spinning,MAS)
2020/10/17
2020/10/17
2020/10/17
固体物质中原子核受到的各种相互作用,主要有以下几项:
(1)在外磁场作用下,核外电子云对核的屏蔽 作用和产生的诱导局部磁场,产生的化学位移 各向异性,它会使谱带增宽﹤10kHz。
Nuclear Magnetic Resonance Spectroscopy
2020/10/17
一、概述
核磁矩:1H=2.79270; 13C=0.70216
磁旋比为质子的1/4;
相对灵敏度为质子的1/5600; PFT-NMR(1970年),实用化技术;
(pulse fourier transform )
醛、酮﹥酸﹥酯≈酰氯≈酰胺﹥酸酐
减小
210
170
羰基邻位有吸电基团将使它向低场位移;
芳香和α,β-不饱和羰基化合物,由于共 轭和诱导作用将增加羰基的电子云密度, 使它向高场位移。
2020/10/17
化学位移表1 chemical shift table
2020/10/17
化学位移表2 chemical shift table
2020/10/17
三、偶合与弛豫
13C-13C偶合的几率很小(13C天然丰度1.1%);
13C- 1H偶合;偶合常数1JCH:100-250 Hz;峰裂分;谱图复杂;
去偶方法: (1)质子噪声去偶或宽带去偶(proton noise decoupling or boradband decoupling) : 文献中均使用之
decoupling, DD)
2020/10/17
(3)交叉极化方法(cross polization,CP) (4)魔角旋转(magic angle spinning,MAS)
2020/10/17
2020/10/17
2020/10/17
固体物质中原子核受到的各种相互作用,主要有以下几项:
(1)在外磁场作用下,核外电子云对核的屏蔽 作用和产生的诱导局部磁场,产生的化学位移 各向异性,它会使谱带增宽﹤10kHz。
核磁共振碳谱及二维谱汇总.

例:红霉素
NOE 二维谱 (NOESY)
� 两轴均为氢核的化学位移 � 空间距离较近,并有NOE相关的两种(组)
氢核在图谱上出现相关峰
The End
二维核磁共振波谱的表现形式
� 堆积图 � 等高线图:常用
1H-1H COSY 谱
� 横轴和纵轴均设定为1H 的化学位移,互相偶合的 两个(组)
� 1H 核在图谱上出现相关 峰
� 两个坐标轴上则画有通常 的一维谱
� 峰的解析
– 对角峰:45°对角线上的峰 – 相关峰:对称于对角角线
上的峰,表示偶合关系
No. Atom 9 2' 10 6' 11 5 12 4' 13 9 14 7 15 5
(ppm) 130.02 130.02 158.55 163.84 164.65 167.56 197.86
19/11/2001 12:50:34
32768
Sw eep Width (Hz)
18314.44
HO
• 伯碳和叔碳不变化 • 仲碳峰倒置
CH2
CH2 CH2
200 180 160 140 120 100 80 60ห้องสมุดไป่ตู้40 20 0
Chemical shift (d, ppm)
13C-NMR的化学位移
� 变化规律与1H有一定对应性,但并不完全相同
芳碳 烯碳
==CC==OO
CC==CC
糖糖区区
糖端
sspp3杂3杂化化
基C
220 200 180 160 140 120 100 80 60 40 20 0
90~110
13C-NMR的化学位移
碳的类型 δ (ppm)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.5
核磁共振碳谱解析及应用
13C
4.5.1 核磁共振碳谱谱图解析程序
NMR谱的解析并没有一个成熟、统一的程序,应该根据 具体情况,结合其他物理方法和化学方法测定的数据,综合分 析才能得到正确的结论。 通常解析按以下步骤进行: (1)确定分子式并根据分子式计算不饱和度。 (2)从13C NMR的质子宽带去偶谱,了解分子中含C的数目、类型和 分子的对称性。如果13C的谱线数目与分子式的C数相同,表明分 子中不存在环境相同的含C基团,如果13C的谱线数小于分子式中 的C数,说明分子式中存在某种对称因素,如果谱线数大于分子中 C数,则说明样品中可能有杂质或有异构体共存。 (3)分析谱线的化学位移,可以识别sp3、sp2、sp杂化碳和季碳,如 果从高场到低场进行判断,0-40ppm为饱和烃碳,40-90ppm为与O、 N相连的饱和碳,100-150ppm为芳环碳和烯碳,大于150ppm为羰 基碳及叠烯碳。
有机波谱分析
4.1
核磁共振碳谱的特点
13C核磁共振谱的信号是1957年由P.
C. Lauterbur首先观察到
的。碳是组成有机物分子骨架的元素,人们清楚认识到13C NMR对于化学研究的重要性。由于13C的信号很弱,加之1H 核的偶合干扰,使13C NMR信号变得很复杂,难以测得有实 用价值的谱图。20世纪70年代后期,质子去偶和傅里叶变换 技术的发展和应用,才使13C NMR的测定变成简单易得。20 多年来,核磁共振技术取得巨大发展,目前,13C NMR已广 泛应用于有机化合物的分子结构测定、反应机理研究、异构
4.3
13C的化学位移
化学位移范围:0~250ppm;核对周围化学环境敏感,重叠 少氢谱与碳谱有较多共同点;
碳谱化学位移规律:
(1) 高场低场 碳谱:饱和烃碳原子、炔烃碳原子、烯烃碳原子、羧基碳原子 氢谱:饱和烃氢、炔氢、烯氢、醛基氢; (2) 与电负性基团,化学位移向低场移动; 4.3.1 屏蔽常数
比乙醛(199.6ppm)处较高场
δ值比苯 (128.5ppm)大
4.立体效应
13C化学位移对分子的立体构型十分敏感。只要碳核间空间比
较接近,即使间隔几个化学键,彼此还会有强烈的影响。如在 Van der Waals效应中,通常1H是处于化合物的边缘或外围,当2 个氢原子靠近时,由于电子云的相互排斥,使1H核周围的电子云 密度下降,这些电子云将沿着C-H键移向碳原子,使碳的屏蔽 作用增加,化学位移向高场移动。
3.能给出不连氢碳的吸收峰 在1H NMR中不能直接观察到C=O、C=C、C≡C、C=N、季 碳等不连氢基团的吸收信号,只能通过相应基团的化学位移值、 分子式不饱和度等来判断这些基团是否存在。而13C NMR谱可 直接给出这些基团的特征吸收峰。由于碳原子是构成有机化合 物的基本元素,因此从13C NMR谱可以得到有关分子骨架结构 的信息。 4.不能用积分高度来计算碳的数目 13C NMR的常规谱是质子全去偶谱。对于大多数碳,尤其是 质子化碳,它们的信号强度都会由于去偶的同时产生的NOE效 应而大大增强,如甲酸的去偶谱与偶合谱相比,信号强度净增 近2倍。季碳因不与质子相连,它不能得到完全的NOE效应, 故碳谱中季碳的信号强度都比较弱。由于碳核所处的环境和弛 豫机制不同,NOE效应对不同碳原子的信号强度影响差异很大, 因此不等价碳原子的数目不能通过常规共振谱的谱线强度来确 定。
2.13C-31P的偶合常数 13C与31P的偶合也符合n+1规律,其偶合常数与磷的价数有关,一
般五价磷与碳的1JCP为50-180Hz,2JCP、3JCP在5-15Hz,三价磷的
1J CP
< 50Hz,2JCP、3JCP为3-20Hz。
3.13C-D的偶合常数
在13C NMR中常使用氘代溶剂,因此常遇到碳与氘的自旋偶合。 13C-D的偶合常数比13C-1H的偶合常数小得多,1JCH/1JCD与两种 核旋磁比的比值相近,即1JCD只有1JCH的1/6左右。 氘的自旋量子数为1,所以-CD3-、-CD2-、-CD-的共振 峰按2nI+1规律分别显示七、五、三重峰,峰的裂距即为其偶合常数。 氘代溶剂的1JCD值约为18一34Hz。
5.弛豫时间τ1可作为化合物结构鉴定的波谱参数
在化合物中,处于不同环境的13C核,它们的弛豫时间τ1数
值相差较大,可达2-3个数量级,通过τ1可以指认结构归属,
窥测体系运动状况等。
4.2.1
脉冲傅里叶变换法
原理同1H NMR。
4.2.2
核磁共振碳谱中几种去偶技术
在有机化合物的13C NMR中,13C-13C之间的偶合由于13C的天然丰 度很低,可以不予考虑。但13C-1H核之间的偶合常数很大,如1JCH高达 120-320Hz,13C的谱线会被与之偶合的氢按n+1规律裂分成多重峰,这 种峰的裂分对信号的归属是有用的,但当谱图复杂时,加上2JCCH、
4.13C金属原子的偶合常数
13C与金属原子核的偶合有时产生很大的偶合常数,如1J C-Hg可大
于100Hz,在进行有机金属化合物的NMR研究时应给予注意。
5.13C-15N的偶合常数
由于15N的天然丰度很小,只有14N的0.37%,因此13C与15N直 接相连的概率很低,偶合常数也很小。一般13C与15N的偶合常数在 1-15Hz。
取代基处于直立键比处平 伏键时δ位碳的占值小约 5ppm。
分子中存在空间位阻,常会影响共轭效应的效果,导致化学位移的变化, 如邻位烷基取代的苯乙酮,随着烷基取代基数目增加,烷基的空间位阻使羰 基与苯环的共轭效应减弱,羰基碳δ值向低场位移。
5.测定条件
测定条件对13C的化学位移有一定的影响,如溶解样品的溶 剂、溶液的浓度、测定时的温度等。
4.3.3
各类化合物的13C化学位移
1.饱和碳的化学位移值
饱和烷烃:饱和烷烃的碳为sp3杂化,其化学位移值一般在-2.5-55ppm。
与1H NMR相似,也可进行经验计算,这里不做详细介绍。
2.烯碳的化学位移值
烯碳为sp2杂化,其化学位移为100-165ppm。
3.炔烃的化学位移值
炔基碳为sp杂化,其化学位移介于sp3与sp2杂化碳之间,为 67-92ppm。
3 3 4 4
2 1
5
6
5 612Fra bibliotek谱图去偶作用对比
6.INEPT谱和DEPT谱
常规的13C NMR谱是指宽带质子去偶谱。在去偶的条件下,
失去了全部C-H偶合的信息,质子偶合引起的多重谱线合并, 每种碳原子只给出一条谱线。虽然用偏共振去偶技术可以分辨 CH3、CH2、CH及季C的归属,但由于偏共振去偶谱中偶合常 数分布不均匀,多重谱线变形和重叠,在复杂分子的研究中仍 然受到限制。随着现代脉冲技术的发展,产生了一些新的能确 定碳原子级数的新方法,如J调制法、APT法、INEPT法和 DEPT法等,其中INEPT法和DEPT法已被广泛应用。
δ值范围在100-150ppm,sp杂化碳的δ值范围在60-95ppm。
2.诱导效应
当电负性大的元素或基团与碳相连时,诱导效应使碳的核外 电子云密度降低,故具有去屏蔽作用。随着取代基电负性增强, 或取代基数目增大,去屏蔽作用也增强, δ值愈向低场位移。
3.共轭效应
共轭作用会引起电子云分布的变化,导致不同位置碳的共 振吸收峰向高场或低场移动。
3J CCCH也有一定的表现,使各种谱峰交叉重叠,谱图难以解析。为了
提高灵敏度和简化谱图,人们研究了多种质子去偶测定方法,以最大 限度地获取,13C NMR信息。
1.质子宽带去偶法
2.偏共振去偶法
3.门控去偶法 4.反转门控去偶法 5.选择质子去偶
谱图去偶作用对比
3 3 4
2 1
5
6
4
5 6
1
2
(4)分析偏共振去偶谱和DEPT谱,了解与各种不同化学环境的碳直
接相连的质子数,确定分子中有多少个CH3、CH2、CH和季碳及其 可能的连接方式。比较各基团含H总数和分子式中H的数目,判断
是否存在一OH、一NH2、一C(X)H、一NH一等含活泼氢的基团。
(5)如果样品中不含F、P等原子,宽带质子去偶谱图中的每一条谱线 对应于一种化学环境的碳,对比偏共振去偶谱,全部偶合作用产生
INEPT谱中不出现季 碳的信号
CH3和CH为正峰,而 CH2为负峰
只出现CH的正峰
CH3、CH2、CH为正值
2)DEPT法
DEPT谱中也不 出现季碳的信号
DEP-45°谱,CH3、 CH2和CH的峰均为正峰 DEPT-90°谱,只出现 CH的正峰 DEPT-135°谱,CH3 和CH为正峰,而CH2的 峰为负 常规宽带质子去偶13C谱
不同环境的碳,受到的屏蔽作用不同,δ值不同,其共振频率
νC也不同。
4.3.2
影响13C化学位移的因素
碳原子的杂化轨道状态(sp3、sp2、sp)很大程度上决定13C
1.碳杂化轨道
化学位移。sp3杂化碳的共振信号在高场,sp2杂化碳的共振信号
在低场,sp杂化碳的共振信号介于前二者之间。以TMS为标准, 对于烃类化合物来说,sp3碳的δ值范围在0-60ppm;sp2杂化碳的
1) INEPT法
由于核磁共振本身信号灵敏度很低,尤其是低天然丰度的核 (如13C、15N等)更为突出。INEPT法是在具有两种核自旋的系统 中,以CH为例,通过脉冲技术,把高灵敏1H核的自旋极化传递到 低灵敏的13C核上去,这样由1H到与其偶合的13C的完全极化传递可 使,13C信号强度增强4倍。
体判别、生物大分子研究等方面,成为化学、生物化学、药
物化学及其他相关领域的科学研究和生产部门不可缺少的分 析测试手段,对有关学科的发展起了极大的促进作用。
4.2 核磁共振碳谱的测定方法 1.灵敏度低 13C核的天然丰度很低,只有1.108%,而1H的天然丰度为 99.98%。13C核的旋磁比γC也很小,只有γH核翔的1/4。信号 灵敏度与核的旋磁比γC的立方成正比,因此,相同数目的1H 核和13C核,在同样的外磁场中,相同的温度下测定时,其信 噪比为11.59 × 10-4,即13C NMR的灵敏度大约只有1H NMR的 1/6000。所以,在连续波谱仪上是很难得到13C NMR谱的,这 也是13C NMR在很长时间内未能得到广泛应用的主要原因。 2.分辫能力高 1H NMR的化学位移通常在0-15ppm,而13C NMR的常用范 围为0-300ppm,约为1H谱的20倍。同时13C自身的自旋-自旋裂 分实际上不存在,虽然,13C-1H之间有偶合,但可以用质子去 偶技术进行控制。因此13C谱的分辨能力比1H谱高得多,结构 不对称的化合物、每种化学环境不同的碳原子通常可以得到特 征的谱线。
