物理化学课件分压定律和分体积定律.共23页
《气体分压定律》课件

目录
• 气体分压定律简介 • 气体分压定律的原理 • 气体分压定律的实验验证 • 气体分压定律的应用实例 • 气体分压定律的局限性
气体分压定律简介
01
定义与性质
定义
气体分压定律描述了在恒温、恒 容条件下,混合气体的总压等于 各组分气体的分压之和。
性质
气体分压定律是气体定律之一, 它反映了气体压力与其组分和温 度之间的关系。
工业生产
在化工、制药、环保等领域,气体分压定律被广泛应用于气 体分离、气体净化、气体反应等工艺流程的设计和控制。
气体分压定律的原
02
理
理想气体定律
1 2
理想气体定律
理想气体在一定温度和压力下,其性质与分子间 相互作用力和分子本身无关,只与分子数有关。
理想气体定律的数学表达式
PV=nRT,其中P表示压力,V表示体积,n表示 气体分子数,R表示气体常数,T表示温度。
4. 重复实验多次,以获得更 准确的结果。
实验数据记录与处理
数据记录 每种气体的压力数据。
实验温度数据。
实验数据记录与处理
数据处理 分析分压与总压的关系。
计算每种气体的分压。 比较不同温度下的分压数据。
实验结果分析与结论
结果分析
01
比较不同温度下的分压数据,探讨温度对 分压的影响。
03
02
分析分压与总压的比例关系,验证气体分压 定律。
03
验验证
实验装置与实验步骤
恒温槽
用于维持气体温度恒定。
压力计
用于测量气体的压力。
实验装置与实验步骤
真空泵
用于抽取气体。
混合室
用于混合不同种类的气体。
物理化学课件分压定律和分体积定律.

(2) 压力修正
器 壁
内部分子
靠近器壁的分子
分子间相互作用减弱了分子对器壁的碰撞, 所以:
2018/12/7
p= p理-p内 p内= a / Vm2 p理= p + p内= p + a / Vm2
a为范氏常数,其值与各气体性质有关,均为正 值。一般情况下,分子间作用力越大, a值越大。 将修正后的压力和体积项引入理想气体状态方 程:
VB y BV
y B=1
理想气体混合物的总体积V为各组分分体积VB*之和: yB = 1 V= VB*
n RT n B RT B V VB p p p B B n B RT VB p 理想气体混合物的总体积,等于气体B在与气体混 合物具有相同温度及压力条件下所占有体积的总和。 阿玛格分体积定律
注:该定律仅适用于理想气体,低压真实气体近似 服从该定律
2018/12/7
n
B
RT
气体混合物的平均摩尔质量 假定混合气体各组分之间不发生任何化学反应 , 组分A的物质的量为 nA,摩尔质量为MA;组分B的物 质的量为nB,摩尔质量为MB,则由A和B组成的混合 物体系的摩尔质量M,令nA+nB=n,则有
l2018/12/7 继续增加外压,液体被压缩,体积变化不大。
在敞口容器中,液体的饱和蒸气压等于外压时, 液体发生剧烈的汽化现象,称为沸腾,此时的温 度称为沸点 饱和蒸气压 1个大气压时的温度称为正常沸点 (373.15K) 饱和蒸气压 1个标准压力( 1个标准压力=100kPa, p)时的温度称为标准沸点(372.78K)
第一章 气体的pVቤተ መጻሕፍቲ ባይዱ性质
理想气体混合物的分压定律和分体积定律
分压定律理想气体混合物

解: 排水法收集气体时,通常将所收集气体中的 水蒸气看作饱和蒸气.由化学手册中查出18℃,
在湿氢气中,氢的分压为
p(H2O) 15.477 mmHg
p1(H2 ) (753 .8 15.477 )mmHg 738 .3mmHg
p1(H 2 )
738 .3mmHg 760 mmHg
11
p1(O2) p1(He) 0.10MPa,V1(O2) 46L,V2(He) 121L
混合气体总体积V=5.0L,则其中
p(O2 ห้องสมุดไป่ตู้
p1 (O2 )V1 (O2 ) V2 (O2 )
0.1MPa 46 L 5.0L
9.2 10 2 KPa
p(He) 0.1MPa12L 2.4102 KPa 5.0L
pV = nRT n = m/M pV = mRT/M (3) 气体密度的计算
6
M m RT PV
M RT
P
m
V
pM
RT
7
§1-2 气体混合物
理想气体混合物 组分气体 组分气体的分压 Dalton分压定律
8
§1-2 气体混合物
1.2.1、分压定律 理想气体混合物:当几种不同的气体在同一容 器中混合时,相互间不发生化学反应,分子本 身的体积和它们相互间的作用力都可以忽略不 计,这就是理想气体的混合物。 组分气体:理想气体混合物中每一种气体叫做 组分体。 组分气体的分压:对于理想气体来说,某组分气 体的分压力等于在相同温度下该组分气体单独 占有与混合气体相同体积时产生的压力.
2
§1.1 理想气体状态方程式
气体的基本物理特性:可压缩性和扩散性。 1.1.1、理想气体状态方程式 理想气体是分子之间没有相互吸引和排斥,分 子本身的体积相对于气体所占有体积完全可以 忽略的一种假想情况。对于真实气体,只有在 低压高温下,才能近似的看成理想气体。
物理化学课件分压定律和分体积定律.

2023/11/10
压缩因子法
由Z的定义式可知, pV=ZnRT
维里方程
pVm=RT(1+B/Vm+C/Vm2+D/Vm3+•••)
气体的液化与液体的饱和蒸汽压
实际气体分子间存在吸引力, 从而能发生一种理 想气体不可能发生的变化——液化.气体的液化一般 需要降温和加压. 降温可减小分子热运动产生的离 散倾向, 加压则可以缩小分子间距从而增大分子间 引力.
值.
00-7-22
20
普遍化压缩因子图
将对比状态参数的表达式引入压缩因子 Z 的定义中, 得
def Z
pVm RT
pCVC prVr RTC Tr
ZC
pr Vr Tr
式中右方第一项为临界点处的压缩因子ZC, 实验 表明多数实际气体的 ZC 在 0.270.29 的范围内(参
阅表1-2), 可看作常数;根据对应状态原理,在Tr和pr 一定时, pr也一定,因而,压缩因子Z近似为一定值,即 处于对比状态的各种气体具有相同的压缩因子,它是
分压力:混合气体中某一组分B的分压力pB是该
组份单独存在并具有与混合气体相同温度和体积
时所具有的压力。
注: 总压是构成该混合物的各组分对压力所做的贡 献之和; 气体混合物中每一种气体叫做组分气体。
yB = 1
p = pB
混合理想气体:
pB (nA nB
B
nC
) RT V
B
nB
Tr和pr的一个双变量函数.
00-7-22
21
VB yBV
y B=1
V 混合气体总体积, yB 组分B的物质的量分数
气体物理化学PPT课件

14
第14页/共32页
一些物质的临界参数
物质 6m3·mol-1
He
Tc/K 5.26
pc/MPa 0.229
Vm,c/1058
H2
33.3
1.30
N2
126.2
3.39
O2
154.4
5.04
H2O
647.4
22.12
CH4
190.7
4.64
C2H 4
283.1
5.12
C6H6
562.6
4.92
C2H5 OH 516.3
5
第5页/共32页
4. 理想气体的微观模型
• 理想气体是指任意压力和任意温度下其状态均符合 pV = nRT 的气体。
• 若要具有这种性质,理想气体必须有如下特征: (1)分子本身没有体积
若有体积,在T恒定、压力p→∞ 时(pVm)不能保证为常数。 (2)分子间无相互作用力
若有相互作用,在T恒定时,压力p = (n/V) RT ∝ n无法满足,因为分子间的 相互作用会影响压力。 • 实际气体性质:压力小,温度高时分子间相互作用小,体积较大,所以行为接近理 想气体。难液化的气体如H2、N2、O2等通常可认为是理想气体 。
1mol气体的体积
3
第3页/共32页
2. 理想气体的定义
•
任何温度、任何压力下均符合状态方程 pV = nRT 的气体。
• 理想气体的状态方程:pV = nRT
• 其它形式:已知气体的质量m、摩尔质量M、密度, 利用关系式 摩尔体积Vm = V / n,n = m / M, = m / V 则改写为: pVm = RT pV =(m/M)RT
度——将理想气体方程用压缩因子加以修正:PVm = ZRT
1. 2 混合气体的分压定律

解:设 t 时间后发生反应,玻璃 管中产生白烟的位置距 NH3 端 x cm, 则距 HCl 端( 100 - x )cm。
x
100 - x
NH3
NH4Cl
HCl
x
100 - x
NH3
NH4Cl
HCl
由公式 得
A B
即组分气体的分压,等于总压 与该组分气体的体积分数之积。
例 1. 1 某温度下,将 2 105 Pa 的 O2 3 dm3 和 3 105 Pa 的 N2 6 dm3 充入 6 dm3 的真空容器中。
求各组分气体的分压及 混合气体的总压。
解:根据分压的定义求组分气体的分压,
O2 V1 = 3 dm3 , p1 = 2 105 Pa ,
ni n
= xi
故
pi = p总•xi
即组分气体的分压等于总压 与该组分气体的摩尔分数之积。
p总 Vi = ni R T
p总V总 = n R T
(3) 又 (1) 得
Vi V总
=
ni n
(3) (1)
Vi V总
=
ni n
= xi
又有
pi = p总•xi
故
pi
=
p总•
Vi V总
pi
=
p总•
Vi V总
第 i 种组分气体的分体积, 用 Vi 表示
应有下面关系式 p总Vi = n i R T
第 i 种组分气体的分体积 Vi ,
与混合气体的总体积 V总 之比
Vi V总
称为该组分气体的体积分数。
1. 2. 2 分压定律 —— 分压与总压的关系
(完整版)2分压定律和分体积定律

2008---2009学年第二学期第1周第1页(共5页)第二节理想气体混合物的两个定律复习回忆:1、理想气体状态方程的数学表达式;2 、理想气体微观模型的特征。
讲授新课:一、分压定律1、基本概念(1)道尔顿分压定律:低压下气体混合物的总压等于组成该气体混合物的各组分的分压力之和,这个定律称为道尔顿分压定律。
(2)分压力:所谓分压力是指气体混合物中任一组分B单独存在于气体混合物所处的温度、体积条件下所产生的压力P B。
2、道尔顿分压定律的数学表达式P(T,V) P A仃,V) P B仃,V) L或p P B(1-4)B对于理想气体混合物,在T、V 一定条件下,压力只与气体物质的量有关,根据理想气体状态方程,有PV ,n 门人n B n c LRTP A V P B V P c V LRT RT RT(P A P B P c L)V / RT故有P (P A P B P c L )或P P BB适用范围:理想气体混合物或接近于理想气体性质的气体混合物。
3、气体物质的量分数与分压力的关系气体混合物中组分B的分压力与总压力之比可用理想气体状态方程得出P B n B RT /V n By BP nRT/V n即P B y B P (1-5)式中yB ――组分B的物质的量分数式(1-5 )表明,混合气体中任一组分的分压等于该组分的物质的量分数与总压的乘积。
例题1-3某烃类混合气体的压力为100kPa,其中水蒸气的分压为20 kPa,求每100mol2008---2009学年第二学期第1周第2页(共5页)该混合气体中所含水蒸气的质量。
解:p=100kPa , p(H2O)=20kPa , n=100mol , M (H2O)=18 x10-3kg/molB2008---2009学年 第二学期 第1周第3页(共5页)y(H 2。
)営而。
2n(H 2。
) y(H 2O)n 0.2 100 20mol100mol 混合气体中水蒸气的质量 m (H 2。
(完整版)2分压定律和分体积定律

2008---2009学年第二学期第1周第1页(共5页)第二节理想气体混合物的两个定律复习回忆:1、理想气体状态方程的数学表达式;2 、理想气体微观模型的特征。
讲授新课:一、分压定律1、基本概念(1)道尔顿分压定律:低压下气体混合物的总压等于组成该气体混合物的各组分的分压力之和,这个定律称为道尔顿分压定律。
(2)分压力:所谓分压力是指气体混合物中任一组分B单独存在于气体混合物所处的温度、体积条件下所产生的压力P B。
2、道尔顿分压定律的数学表达式P(T,V) P A仃,V) P B仃,V) L或p P B(1-4)B对于理想气体混合物,在T、V 一定条件下,压力只与气体物质的量有关,根据理想气体状态方程,有PV ,n 门人n B n c LRTP A V P B V P c V LRT RT RT(P A P B P c L)V / RT故有P (P A P B P c L )或P P BB适用范围:理想气体混合物或接近于理想气体性质的气体混合物。
3、气体物质的量分数与分压力的关系气体混合物中组分B的分压力与总压力之比可用理想气体状态方程得出P B n B RT /V n By BP nRT/V n即P B y B P (1-5)式中yB ――组分B的物质的量分数式(1-5 )表明,混合气体中任一组分的分压等于该组分的物质的量分数与总压的乘积。
例题1-3某烃类混合气体的压力为100kPa,其中水蒸气的分压为20 kPa,求每100mol2008---2009学年第二学期第1周第2页(共5页)该混合气体中所含水蒸气的质量。
解:p=100kPa , p(H2O)=20kPa , n=100mol , M (H2O)=18 x10-3kg/molB2008---2009学年 第二学期 第1周第3页(共5页)y(H 2。
)営而。
2n(H 2。
) y(H 2O)n 0.2 100 20mol100mol 混合气体中水蒸气的质量 m (H 2。
物理化学课件分压定律和分体积定律

在敞口容器中,液体的饱和蒸气压等于外压时, 液体发生剧烈的汽化现象,称为沸腾,此时的温 度称为沸点
饱和蒸气压 1个大气压时的温度称为正常沸点 (373.15K)
饱和蒸气压 1个标准压力( 1个标准压力=100kPa, p)时的温度称为标准沸点(372.78K)
饱和蒸气压是物质在一定温度下处于液气平衡共 存时蒸汽的压力,是纯物质特有的性质,由其本 性决定;其大小是温度的函数,是衡量液体蒸发 能力或液体分子逸出能力的一个物理量。
组分A的物质的量为nA,摩尔质量为MA;组分B的物 质的量为nB,摩尔质量为MB,则由A和B组成的混合 物体系的摩尔质量M,令nA+nB=n,则有
M
m n
nAMA nBMB n
nA n
MA
nB n
MB
即
M yAMA yBMB
该公式对多组分气体也同样适用,也适用于液体和
固体混合物,对任意组分,其计算平均摩尔质量通
第一章 气体的pVT性质
理想气体混合物的分压定律和分体积定律
真实气体的液化与液体的饱和蒸汽压 对应状态原理与压缩因子图
理想气体混合物的分压定律和分体积定律
道尔顿(Dalton)分压定律
鉴于热力学计算的需要,提出了既适用于理
想气体混合物,又适用于非理想气体混合物的分
压力定义 pB yBp
y B=1
压缩空间减小1。mol气体的可压缩空间以 (Vm - b)表示。 b为一范氏常数,恒为正值,其大小与气体性
质决定。 一般情况下,气体本身体积越大,b值也 越大。
对2020体/5/7积修正后,p(Vm - b)=RT。
(2) 压力修正
器 壁
2020/5/7
内部分子
道尔顿定律和阿玛格定律
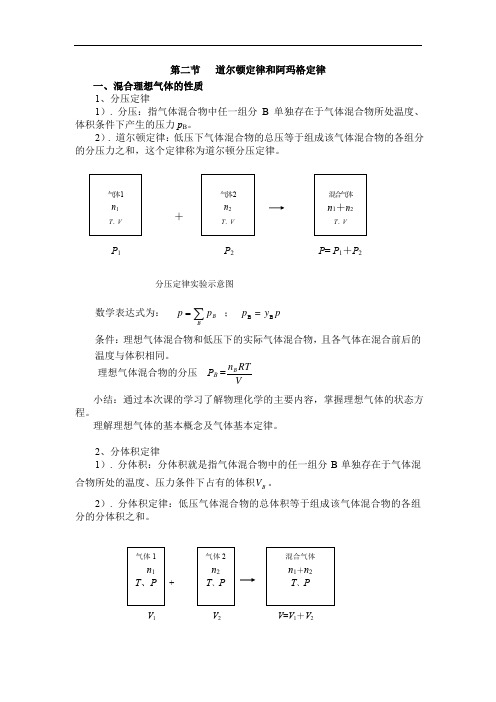
第二节 道尔顿定律和阿玛格定律 一、混合理想气体的性质
1、分压定律
1). 分压:指气体混合物中任一组分B 单独存在于气体混合物所处温度、体积条件下产生的压力p B 。
2). 道尔顿定律:低压下气体混合物的总压等于组成该气体混合物的各组分数学表达式为: ∑=B
B p p ; p y =p B B
条件:理想气体混合物和低压下的实际气体混合物,且各气体在混合前后的温度与体积相同。
理想气体混合物的分压 P B =
V
RT n B
小结:通过本次课的学习了解物理化学的主要内容,掌握理想气体的状态方程。
理解理想气体的基本概念及气体基本定律。
2、分体积定律
1). 分体积:分体积就是指气体混合物中的任一组分B 单独存在于气体混合物所处的温度、压力条件下占有的体积B V 。
2). 分体积定律:低压气体混合物的总体积等于组成该气体混合物的各组分的分体积之和。
+
V 1 V 2 V =V 1+V 2
+
P 1 P 2 P = P 1+P 2
分压定律实验示意图
气体1 n 1
T 、P 气体2 n 2 T 、P 混合气体 n 1+n 2 T 、P
气体 2 n 2 T 、V 混合气体 n 1+n 2
T 、V
气体 1
n 1
T 、V。
(完整版)2分压定律和分体积定律

第二节 理想气体混合物的两个定律复习回忆:1、理想气体状态方程的数学表达式;2、理想气体微观模型的特征。
讲授新课:一、分压定律1、基本概念(1)道尔顿分压定律:低压下气体混合物的总压等于组成该气体混合物的各组分的分压力之和,这个定律称为道尔顿分压定律。
(2)分压力:所谓分压力是指气体混合物中任一组分B 单独存在于气体混合物所处的温度、体积条件下所产生的压力p B 。
2、道尔顿分压定律的数学表达式(,)(,)(,)A B p T V p T V p T V =++L或 B B p p=∑ (1-4)对于理想气体混合物,在T 、V 一定条件下,压力只与气体物质的量有关,根据理想气体状态方程,有()/A B C C A B A B C pV n n n n RTp V p V p V RT RT RTp p p V RT ==+++=+++=+++L L L 故有 ()A B C p p p p =+++L 或 B B p p=∑适用范围:理想气体混合物或接近于理想气体性质的气体混合物。
3、气体物质的量分数与分压力的关系气体混合物中组分B 的分压力与总压力之比可用理想气体状态方程得出//B B B B p n RT V n y p nRT V n=== 即 B B p y p = (1-5) 式中 yB ——组分B 的物质的量分数式(1-5)表明,混合气体中任一组分的分压等于该组分的物质的量分数与总压的乘积。
例题1-3 某烃类混合气体的压力为100kPa ,其中水蒸气的分压为20 kPa ,求每100mol 该混合气体中所含水蒸气的质量。
解:p=100kPa ,p(H 2O)=20kPa ,n=100mol ,M (H 2O )=18×10-3kg/mol由式(1-5)得22()20()0.2100p H O y H O p === 又 22()()n H O y H O n= 所以 22()()0.210020n H O y H O n mol ==⨯= 100mol 混合气体中水蒸气的质量m(H 2O)为3222()()()2018100.36m H O n H O M H O kg -==⨯⨯=课堂练习题1、某气柜内贮有气体烃类混合物,其压力p 为104364Pa ,气体中含水蒸气的分压力p(H 2O)为3399.72Pa 。
分压定律体积和压强的关系

分压定律体积和压强的关系【摘要】分压定律是描述气体在混合气体中的压强分布规律的基本原理。
体积和压强的关系是通过分压定律来解释的,即每种气体分别占据一定的体积并独立地施加压强。
实验验证表明,当一种气体与另一种气体混合时,它们的压强分别与其在混合物中所占体积的比例成正比。
理论推导可以通过理想气体定律和Dalton气体混合物分压定律进行推导。
数学表达式可以表示为P= P1 + P2 + ... + Pn,其中P为总压强,P1、P2、...、Pn分别为各个气体的分压。
体积和压强之间的关系遵循分压定律的规律。
结论指出,分压定律是解释气体混合物中压强分布的重要定律,对于理解气体的行为和性质具有重要意义。
【关键词】引言、分压定律的基本原理、体积和压强的关系、实验验证分压定律、理论推导、数学表达式、结论1. 引言1.1 引言分压定律是研究气体在容器中受力时压强和体积的关系的基本定律之一。
根据分压定律,在给定温度下,气体在封闭容器中均匀地承受压力,每种气体对压力的贡献与其分压成正比。
这个定律具有很强的普适性,在许多自然现象和科学实验中都有重要应用。
体积和压强是气体性质的两个重要参数,它们之间的关系在分压定律中得到了明确的描述。
当气体受到外部压力作用时,其体积会相应地收缩,而压强则会增大。
通过实验验证和理论推导,可以得出体积和压强之间的具体关系,这有助于我们更深入地理解气体的行为规律。
在本文中,将介绍分压定律的基本原理、体积和压强的关系、实验验证方法、理论推导过程以及数学表达式。
通过深入研究这些内容,我们可以更好地理解气体在不同条件下的性质表现,为相关领域的研究和应用提供重要参考。
在接下来的内容中,我们将逐一探讨以上提到的各个方面,以期加深对分压定律体积和压强关系的理解,为后续研究工作奠定基础。
2. 正文2.1 分压定律的基本原理分压定律是描述气体在混合状态下的压强与各个气体分压之间的关系。
在一个封闭容器中,装有两种不同气体A和B,分别的压强分别为P_A和P_B。
2分压定律和分体积定律

第二节 理想气体混合物的两个定律复习回忆:1、理想气体状态方程的数学表达式;2、理想气体微观模型的特征。
讲授新课:一、分压定律1、基本概念(1)道尔顿分压定律:低压下气体混合物的总压等于组成该气体混合物的各组分的分压力之和,这个定律称为道尔顿分压定律。
(2)分压力:所谓分压力是指气体混合物中任一组分B 单独存在于气体混合物所处的温度、体积条件下所产生的压力p B 。
2、道尔顿分压定律的数学表达式(,)(,)(,)A B p T V p T V p T V =++或 B B p p=∑ (1-4)对于理想气体混合物,在T 、V 一定条件下,压力只与气体物质的量有关,根据理想气体状态方程,有()/A B C C A B A B C pV n n n n RTp V p V p V RT RT RTp p p V RT ==+++=+++=+++ 故有 ()A B C p p p p =+++ 或 B Bp p =∑适用范围:理想气体混合物或接近于理想气体性质的气体混合物。
3、气体物质的量分数与分压力的关系气体混合物中组分B 的分压力与总压力之比可用理想气体状态方程得出//B B B B p n RT V n y p nRT V n=== 即 B B p y p = (1-5) 式中 yB ——组分B 的物质的量分数式(1-5)表明,混合气体中任一组分的分压等于该组分的物质的量分数与总压的乘积。
例题1-3 某烃类混合气体的压力为100kPa ,其中水蒸气的分压为20 kPa ,求每100mol 该混合气体中所含水蒸气的质量。
解:p=100kPa ,p(H 2O)=20kPa ,n=100mol ,M (H 2O )=18×10-3kg/mol由式(1-5)得22()20()0.2100p H O y H O p === 又 22()()n H O y H O n= 所以 22()()0.210020n H O y H O n mol ==⨯= 100mol 混合气体中水蒸气的质量m(H 2O)为3222()()()2018100.36m H O n H O M H O kg -==⨯⨯=课堂练习题1、某气柜内贮有气体烃类混合物,其压力p 为104364Pa ,气体中含水蒸气的分压力p(H 2O)为3399.72Pa 。
