血钙浓度检测试剂盒使用说明
钙测试盒说明书
空白管 钙测试盒说明书
(甲基百里香酚蓝比色法)
一、实验仪器:分光光度计(610 nm)、微量移液器、漩涡混匀器
二、适用范围:本试剂盒可测各种动物血清(浆)、组织等样本中钙的含量; 三、操作过程:
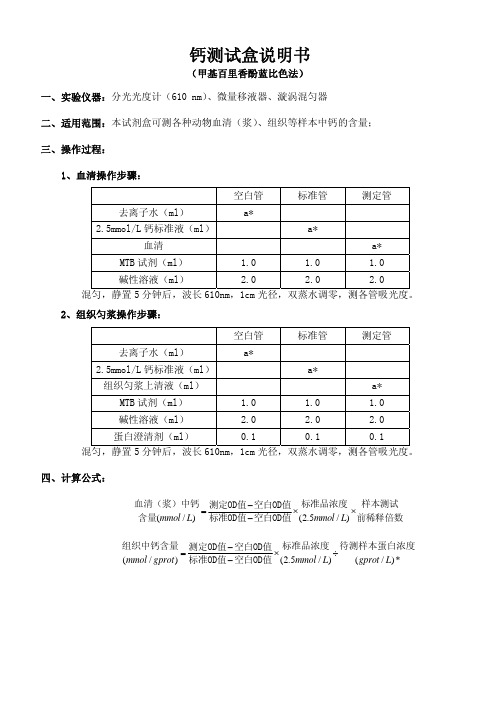
1、血清操作步骤:
标准管
测定管
去离子水(ml) a*
2.5mmol/L 钙标准液(ml)
a* 血清 a* MTB 试剂(ml) 1.0 1.0 1.0 碱性溶液(ml)
2.0
2.0
2.0
混匀,静置5分钟后,波长610nm,1cm 光径,双蒸水调零,测各管吸光度。
2、组织匀浆操作步骤:
空白管 标准管
测定管
去离子水(ml) a* 2.5mmol/L 钙标准液(ml) a* 组织匀浆上清液(ml)
a* MTB 试剂(ml) 1.0 1.0 1.0 碱性溶液(ml) 2.0 2.0 2.0 蛋白澄清剂(ml)
0.1
0.1
0.1
混匀,静置5分钟后,波长610nm,1cm 光径,双蒸水调零,测各管吸光度。
四、计算公式:
(/)(2.5/)mmol L mmol L −=××
−样本测试血清(浆)中钙标准品浓度测定OD值空白OD值标准OD值空白OD值前稀释倍数含量
(/)(2.5/)(/)*
mmol gprot mmol L gprot L −=×÷
−组织中钙含量标准品浓度待测样本蛋白浓度测定OD值空白OD值标准OD值空白OD值。
钙测定试剂盒(偶氮砷 III 法)产品技术要求haifeng

钙测定试剂盒(偶氮砷 III 法)
适用范围:本产品适用于体外定量测定人血清中的钙含量。
1.1 产品规格
1.2 主要组成成分
2.1外观
2.1.1试剂盒标签标识清晰,外包装完整无破损;
2.1.2试剂为紫红色液体,目测不得有任何沉淀及絮状悬浮物。
2.2净含量
净含量不低于标示值。
2.3空白吸光度
在主波长660nm、副波长750nm、37℃条件下:试剂空白吸光度A≤0.5。
2.4线性范围
[1.0,4.0]mmol/l范围内,线性相关系数r≥0.990,相对偏差不超过±10.0%。
2.5分析灵敏度
在产品说明书规定参数设定条件下,浓度为2.5mmol/L时,吸光度变化△A≥0.30。
2.6 精密度
2.6.1批内重复性
CV≤3.0%。
2.6.2批间差
相对极差R≤5.0%。
2.7 准确度
测定参考物质GBW09152,测定结果应不超过标称值的±5%。
2.8 稳定性
未开封试剂2℃~8℃储存,有效期为12个月。
取到效期后2个月内产品进行检测, 检测结果应满足2.4和2.7的规定。
钙测试预装试剂盒说明书

Millipore- 1.00858页码 1 的 9The life science business of Merck operates as MilliporeSigma in the US化学品安全技术说明书按照GB/T 16483、GB/T 17519编制版本6.2修订日期18.09.2022打印日期18.09.2022最初编制日期19.07.2017SDS 编号Millipore - 1.00858产品编号Millipore - 1.00858钙测试预装试剂盒第1部分:化学品及企业标识1.1 产品标识产品名称: 钙测试预装试剂盒Calcium Cell Test Method: photometric 10 -250 mg/l Ca14 - 350 mg/l CaO25 - 624 mg/l CaCO₃ Spectroquant®产品编号: 1.00858产品编号: 100858品牌: Millipore1.2 安全技术说明书提供者的详情制造商或供应商名称: Sigma-Aldrich (Shanghai) Trading Co.Ltd.509 Renqing RoadZhangjiang High Tech East Park, PudongSHANGHAI201201 SHANGHAICHINA西格玛奥德里奇(上海)贸易有限公司上海市浦东新区仁庆路509号10幢邮政编码:201201默克股份两合公司64271 达姆施塔特德国Millipore - 1.00858 页码 2 的 9The life science business of Merck operates as MilliporeSigma in the USPhone:+49(0)6151 72-2440电话号码 : +86 21 6141-5566 传真: +86 21 6141-55671.3 应急咨询电话紧急联系电话: +86 532 838890901.4 物质或混合物的推荐用途和限制用途已确认的各用途 : 分析用试剂这是此产品概括的物质安全资料表(SDS),如需第16项中所列的每一成分完整的物质安全资料表(SDS),请浏览我们的网站.第2部分:危险性概述2.1 GHS 危险性类别易燃液体 (类别 3), H226 金属腐蚀物 (类别 1), H290严重眼睛损伤/眼睛刺激性 (类别 2A ), H319 生殖毒性 (类别 1B ), H360本部分提及的健康说明(H-)全文请见第16部分。
血清里钙的检测

试剂准备: 血清、血浆样本
耗材准备:
96孔板 吸头 一次性手套
使用方法:
使用注意事项:
溶血样本对检测有干扰,尽量避免采用溶血样本; 在本试剂盒条件下,建议待测样品中钙离子浓度应大于 0.5mmol/L 为宜,否则有可能造成检测误
差;
本法也可以用于自动生化分析仪终点检测法;
彻底清除残留清洁剂。 6. 实验后完成后所有样品及接触过的器皿应按照规定程序处理。
产品简介:
贝博®血清钙检测试剂盒(甲基麝香草酚蓝微板法)是利用血清中钙离子在碱性条件下 能与甲基麝香草酚蓝(MTB)结合,生成蓝紫色的复合物,加入镁离子螯合剂,去除镁离 子背景干扰,通过酶标仪检测 610nm 处的吸光度,根据公式计算出总钙含量。
本试剂盒仅用于科研领域,不可用于临床诊断或其他用途。 贝博® BBcellProbe® 可以提供细胞凋亡、增殖、毒性、活性氧、细胞代谢、氧化应激、 细胞膜流动性、膜通透性转换孔、细胞耗氧率、细胞内 pH、细胞粘附、细胞自噬等数百种 检测试剂盒产品。 贝博® BBcellProbe® 可以为您提供各种颜色的 BBcellProbe® M 系列、N 系列、L 系列、 E 系列、G 系列等细胞膜、细胞质、细胞核、溶酶体、线粒体、内质网、高尔基体、骨架、 微管等细胞、细胞亚结构荧光染色试剂盒产品,以及钙离子、钠离子、氩离子等各种荧光染 色试剂盒产品。 贝博® BBcellProbe® 可以提供动物、植物、微生物、酵母、水产、家禽、兽类、土壤 等样本的各种生化指标检测的数百种试剂盒产品。
货号:BB-474253
血清钙检测试剂盒
(甲基麝香草酚蓝微板法)
试剂盒储存条件:
2-8℃ 保存。
【注】: 开盖后组份按要求条件保存。 拆封后请尽快使用完!
钙测定试剂盒(偶氮胂Ⅲ法)产品技术要求huayuyikang

钙测定试剂盒(偶氮胂Ⅲ法)适用范围:本试剂用于体外定量测定人血清中钙的含量。
1.1 产品型号/规格1×25 ml;1×50 ml;2×50 ml;4×50 ml;8×50 ml;5×50 ml;9×70 ml;6×50 ml;2×100 ml;6×100 ml;4×70 ml;2×125 ml;4×125 ml。
1.2 划分说明偶氮胂Ⅲ 1 mmol/LPB缓冲液 100 mmol/L表面活性剂适量2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;中文包装标签应清晰、准确、牢固。
2.1.2 试剂应为紫红色液体。
2.2 净含量不少于标示值。
2.3 试剂空白吸光度在光径1 cm、主波长660 nm下,以蒸馏水为检测样本时,吸光度应不大于1.500。
2.4 分析灵敏度Ca含量为2.5 mmol/L时,测定吸光度差值(△A)应在0.275 ~0.510 范围内。
2.5 线性范围Ca试剂在线性范围(0~4.00] mmol/L内:(a)回归系数r应不小于0.990;(b)在(0~1.00] mmol/L范围内,线性绝对偏差应不大于±0.10 mmol/L;(c)在(1.00~4.00] mmol/L范围内,线性相对偏差应不大于±10%。
2.6 测量精密度2.6.1 重复性变异系数(CV)均应不大于3%。
2.6.2 批间差相对偏差(R)应不大于5%。
2.7 准确度采用GBW09152 冷冻人血清中无机成分分析标准物质对试剂盒进行测试,相对偏差应不超过±5%。
2.8 稳定性Ca试剂盒贮存于2 ℃~8 ℃、避光环境中,有效期为12个月。
有效期满后应满足2.1、2.3、2.4、2.5、2.6.1、2.7的要求。
钙(CA)测定试剂盒(偶氮胂III法)产品技术要求百奥泰康

钙(CA)测定试剂盒(偶氮胂III法)适用范围:该试剂盒用于体外定量测定人血清中钙的浓度。
1.1 产品规格1.2 组成成分该试剂盒由试剂1(R1)、校准品(选配)组成。
1.2.1试剂组成试剂1:磷酸盐缓冲液≥50.0mmol/L偶氮胂III ≥0.1mmol/L1.2.2 校准品组成钙离子目标浓度:2.20mmol/L该校准品为水基质液体校准品2.1 外观a) R1应为紫色溶液,无混浊,无未溶解物。
b) 校准品应为无色溶液,无混浊,无未溶解物。
2.2 净含量液体组分不少于标示值。
2.3 试剂空白2.3.1试剂空白吸光度应不大于1.000。
2.4 分析灵敏度CA试剂盒测定浓度2.50mmol/L的被测物时,吸光度差值(ΔA)应不小于0.150。
2.5 准确度测定参考物质,测定结果的相对偏差不超过±5%。
2.6 精密度2.6.1重复性变异系数应不大于3%。
2.6.2批间差批间相对极差(R)应不大于5%。
2.7 线性在[0.20,4.50]mmol/L范围内,CA试剂盒的线性相关系数r应不低于0.9900;在[0.20,1.00]范围内绝对偏差应不超过0.10mmol/L,在(1.00,4.50]范围内相对偏差应不超过±10%。
2.8 校准品溯源性依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品控制物质赋值的计量学溯源性》及有关规定提供钙校准品的来源、赋值过程以及测量不确定度等内容。
校准品溯源至国家标准物质GBW09152。
2.9 稳定性原包装的CA试剂盒在2℃~8℃避光保存,有效期为18个月。
试剂在规定的条件下保存到有效期末,产品的性能应符合2.3、2.4、2.5、2.6.1和2.7的要求。
钙测定试剂盒(邻甲酚酞络合酮法)产品技术要求beihuakangtai

钙测定试剂盒(邻甲酚酞络合酮法)
适用范围:本试剂盒用于体外定量检测人血清中钙离子的含量。
1.1包装规格:
试剂1:100ml×1;试剂2:100ml×1。
1.2组成成份:
试剂1:邻甲酚酞络合酮 0.16mmol/L,8-羟基喹啉 6.89mmol/L;
试剂2:2-氨基-2甲基-正丙醇 3.5mol/L。
2.1 外观:均为澄清溶液,外包装完整。
2.2 净含量:不少于标示值。
2.3 试剂空白吸光度:A≤0.6(波长575nm,光径10mm)。
2.4 分析灵敏度:浓度为2.5mmol/L时,吸光度变化△A≥0.10。
2.5 线性区间
2.5.1线性相关系数:[1.00,
3.75]mmol/L范围内,线性相关系数r≥ 0.990。
2.5.2线性偏差:[1.00,1.25]mmol/L时,绝对偏差不超过±0.125mmol/L;(1.25,
3.75]mmol/L时,相对偏差不超过±10%。
2.6 精密度
2.6.1重复性:重复测定质控血清,变异系数(CV)≤
3.0%。
2.6.2批间差:用质控血清测试3个不同批号的试剂,相对极差≤5.0%。
2.7 准确度:测定国家标准物质,相对偏差在±5.0%范围内。
2.8 稳定性:试剂盒在2℃~25℃避光贮存有效期为18个月。
保存至有效期末进行测定,试验结果满足2.1、2.3、2.4、2.5、2.6.1、2.7的要求。
钙测定试剂盒(邻甲酚酞络合酮法)产品技术要求baiding

钙测定试剂盒(邻甲酚酞络合酮法)适用范围:本试剂用于体外定量测定人血清钙的含量。
1.1型号规格
产品组成:
2.1 外观
2.1.1 试剂1为黄色透明液体,无混浊,无未溶解物。
2.1.2 试剂2为无色透明液体,无混浊,无未溶解物。
2.1.3 校准品为无色透明液体,无浑浊,无未溶解物。
2.1.4 标签内容清晰,字迹牢固不易脱落。
2.2 试剂装量
液体试剂的净含量不少于标示值。
2.3 试剂空白吸光度
A≤0.30(光径1.0cm,570nm±20nm 波长)。
2.4 分析灵敏度
测定2.5mmol/L样本,吸光度变化在0.500~0.875范围内。
2.5 线性区间
2.5.1 [0.4,
3.75]mmol/L。
在规定的线性范围内,测定值与样本浓度值的相关系数(r)应不低于0.990。
2.5.2 [0.4,1.0]mmol/L范围内,线性绝对偏差应不超过±0.1mmol/L;(1.0,
3.75]mmol/L范围内,线性相对偏差应不超过±10%。
2.6 精密度
2.6.1 重复性
变异系数CV≤3.0%。
2.6.2 批间差
批间差≤5.0%。
2.7 准确度
相对偏差在±5.0%范围内(测试国家标准物质GBW09152)。
2.8 稳定性
原装试剂2℃~8℃保存,有效期12个月,有效期满后2个月内测定结果应符合2.1、2.3、2.4、2.5、2.6.1、和2.7要求。
钙测定试剂盒(偶氮砷Ⅲ法)产品技术要求haomai
钙测定试剂盒(偶氮砷Ⅲ法)
适用范围:本试剂用于体外定量测定人血清中钙[Ca]的浓度。
1.1包装规格
1.2主要组成成分
本试剂由试剂1(R1)组成
试剂1(R1):
醋酸钠 90mmol/L
偶氮砷 500μmol/L
二甲基亚砜 5ml/L
叠氮钠 0.5g/L
2.1 外观
试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰;R1试剂应为紫色澄清液体。
液体试剂不得有沉淀和絮状物。
2.2 净含量
用通用量具测量,液体试剂的净含量应不少于标示值。
2.3 试剂空白
在660nm处测定试剂空白吸光度,应≤1.2A。
2.4 分析灵敏度
测试2.5mmol/L的被测物时,吸光度变化(ΔA)应不低于0.2A。
2.5 准确性
用参考物质对试剂盒进行测试,相对偏差不超过±5%。
2.6 重复性
用一个水平的样本检测,检测结果批内变异系数(CV)应不超过3%。
2.7 线性
2.7.1在[0.24,4.25]mmol/L范围内,线性相关系数r应不低于0.990;
2.7.2在[0.24,0.43)mmol/L范围内绝对偏差不超过±0.04mmol/L;
[0.43,4.25]mmol/L范围内相对偏差不超过±10%。
2.8 批间差
对同一份样品进行重复测定,相对极差≤5%。
2.9 稳定性
该产品在2℃~8℃条件下贮存有效期为12个月,取到效期后的产品进行检测,应符合2.1、2.3、2.4、2.5、2.6、2.7的要求。
钙离子试剂盒测定说明书

<BioVision>Calcium Colorimetric Assay Kit钙比色生物试剂盒(Catalog #K380-250; 250 assays; Store kit at 4°C)1.钙相关介绍Calcium is essential for all living organisms, where Ca2+ sequestration and release into and out of the cytoplasm functions as a signal for many cellular processes. 99% of calcium is found in bones and teeth with the remaining 1% found in the blood and soft tissue. Serum calcium levels are tightly controlled (8.4-11.4 mg/dL) and any variation outside this range can have serious effects. Calcium plays a role in mediating the constriction and relaxation of blood vessels, nerve impulse transmission, muscle contraction, and hormone secretion.Calcium ion channels control the migration of calcium ions across cell membranes,permitting the activation and inhibition of a wide variety of enzymes. Causes of low calcium levels include chronic kidney failure, vitamin D deficiency, and low blood magnesium levels that can occur in severe alcoholism. BioVision’s Colorimetric Calcium Assay Kit utilizes thechromogenic complex(λ=575 nm) formed between calcium ions and0-cresolphthalein to provide a simple assay in the physiologically important range of calcium concentration 0.4-100 mg/dL (0.1-25 mM).4℃下避光保存,保质期一年。
血钙浓度检测试剂盒说明书 可见分光光度法

血钙浓度检测试剂盒说明书可见分光光度法注意:正式测定前务必取2-3个预期差异较大的样本做预测定。
货号:BC0720规格:50T/48S 产品内容:试剂一:液体10mL×1瓶,4℃保存。
试剂二:液体10mL×1瓶,4℃保存。
试剂三:液体×1瓶(空瓶,试剂自备)。
取30mL 试剂瓶,依次加入27mL 无水甲醇和3mL 丙酮,盖紧混匀即可。
标准液:液体1mL×1支,2μmol/mL CaCl 2•2H 2O 溶液,4℃保存。
临用前进行10倍稀释得到0.2μmol/mL 标准溶液。
产品说明:血钙几乎全部存在于血浆中,所以血钙主要指血浆钙。
血浆钙有离子钙和结合钙两种形式,其中只有离子钙直接起生理作用,它与结合钙处于动态平衡,并受血液pH 的影响。
血钙水平与多种重要的生理功能相关,过高或过低都会影响正常生理功能。
本试剂盒用于检测血液中游离钙浓度。
在强碱溶液中游离钙与GBHA 反应生成红色钙-GBHA 复合物,在520nm 有吸收峰;通过测定520nm 吸光度,计算游离钙浓度。
自备仪器和用品:可见分光光度计、可调式移液枪、1mL 玻璃比色皿、无水甲醇、丙酮和蒸馏水。
操作步骤:1.分光光度计预热30min 以上,调节波长到520nm,蒸馏水调零。
2.加样表:名称(μL)空白管标准管测定管血浆--50蒸馏水50--0.2μmol/mL标品-50-试剂一200200200试剂二200200200试剂三400400400混匀;静置5min后于520nm测定吸光度A,记为A测定管、A空白管、A对照管。
血钙浓度计算:血钙含量(μmol/dL)=[C标准液×(A测定管-A空白管)÷(A标准管-A空白管)]×100=20×(A测定管-A空白管)÷(A标准管-A空白管)C标准液:0.2μmol/mL;100:单位换算系数,1dL=100mL。
钙测定试剂盒(偶氮胂Ⅲ法)产品技术要求meigaoyi

钙测定试剂盒(偶氮胂Ⅲ法)
适用范围:用于体外定量检测人血清中钙(Ca)的浓度。
1.1包装规格
4×50ml;4×30ml;3×300ml;12×24ml;2×60ml;1×30ml。
1.2主要组成成分
2.1 外观和性状
2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰。
2.1.2 试剂应为紫红色液体,无沉淀、无悬浮物、无絮状物。
2.2 净含量
液体试剂的净含量应不少于标示值。
2.3 试剂空白吸光度
在630nm处测定试剂空白吸光度,应≤1.1。
2.4 分析灵敏度
测试2.5mmol/L的被测物时,吸光度(A)应不低于1.2。
2.5 准确性
测定国家标准品(360018),测定值与靶值相对偏差应不超过±5%。
2.6 重复性
对正常值浓度的样本进行重复测试,批内变异系数(CV)应≤3%。
2.7 线性
2.7.1在[0.50,4.00]mmol/L区间内,线性相关系数|r|应不低于0.990;
2.7.2 在(1.00,4.00]mmol/L区间内,相对偏差不超过±10%;测试浓度
[0.50,1.00]mmol/L的区间内,绝对偏差不超过±0.10mmol/L。
2.8 批间差
抽取3个不同批号试剂,对同一浓度样品进行重复检测,批间相对极差应≤5%。
2.9 稳定性
该产品在2℃~8℃条件下贮存有效期为18个月,取效期末的产品进行检测,应符合2.1、2.3、2.4、2.5、2.6、2.7之规定。
钙测定试剂盒(偶氮胂Ⅲ法)产品技术要求北检·新创源

钙测定试剂盒(偶氮胂Ⅲ法)
适用范围:本产品用于体外定量测定人血清中钙的含量。
1.1 规格
具体产品规格见下表:
1.2 组成成分
偶氮胂Ⅲ≥200μmol/L
三乙醇胺缓冲液≥100mmol/L
表面活性剂≥0.1%
2.1 外观
2.1.1 外包装完整无破损;
2.1.2 试剂:紫红色澄清液体。
2.2 净含量
净含量不低于标示值。
2.3 试剂空白吸光度
在660nm波长、37℃条件下,试剂空白吸光度应小于0.5。
2.4 线性
2.4.1 线性范围
[1.00,4.00]mmol/L,相关系数r≥0.990。
2.4.2 线性偏差
[1.00,4.00]mmol/L线性范围内,相对偏差不超过±10%。
2.5 分析灵敏度
检测浓度为2.46mmol/L的样本时,吸光度变化不小于0.161。
2.6 重复性
测试(2.50±0.50)mmol/L的样本或质控品,重复测试至少10次,CV ≤3%。
2.7 批间差
用三个不同批号的试剂测试(2.50±0.50)mmol/L的同一样本,重复测试3次,相对极差R≤5%。
2.8 准确度
测定360018标准物质水平2,测定结果应不超过标示值的±5%。
2.9 稳定性
原包装试剂2~8℃避光储存,有效期12个月。
取到效期后两个月内产品进行检测, 检测结果应符合2.4和2.8的要求。
钙测定试剂盒(偶氮胂III法)产品技术要求ruizhengshanda
钙测定试剂盒(偶氮胂III法)
适用范围:本试剂盒用于体外定量测定人血清中钙的含量。
1.1产品型号/规格及其划分说明
1.2主要组成成分
2.1外观
2.1.1 试剂(R)应为深紫色透明溶液,无混浊,无未溶解物;
2.1.2 校准液应为无色透明溶液,无混浊,无未溶解物;
2.1.3 试剂盒标签标识清晰,外包装完整无损。
2.2 净含量
试剂(R)和校准液的净含量不少于标示值。
2.3 试剂空白吸光度
在主波长660nm、副波长750nm处(光径1cm),试剂空白吸光度A ≤2.2。
2.4分析灵敏度
测量1mmol/L的被测物时,吸光度变化△A应≥0.10。
2.5 线性范围
在[1.0,4.0]mmol/L线性范围内,线性相关系数r≥0.990。
在[1.0,4.0]mmol/L线性范围内,相对偏差不超过±10%。
2.6 精密度
2.6.1 重复性
重复测定(2.5±0.5)mmol/L的样品,变异系数CV≤3%。
2.6.2 批间差
相对极差≤5%。
2.7 准确度
测定有证参考物质GBW09152,测定值与靶值的相对偏差不超过±5%。
2.8 稳定性
原包装的Ca试剂盒在2℃~8℃避光保存,有效期为18个月。
试剂盒在规定的储存条件下保存至有效期满后,检测2.3、2.4、2.5、2.6.1、2.7项,结果应符合各项目的要求。
2.9 校准液溯源性
按GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,试剂盒校准液溯源至NIST SRM909b。
组织内质网内钙离子浓度荧光检测试剂盒产品说明书中文版

组织内质网内钙离子浓度荧光检测试剂盒产品说明书(中文版)主要用途组织内质网内钙离子浓度荧光检测试剂是一种旨在通过内质网钙离子特异性荧光探针Mag-Fluo--AM,与钙离子结合后,其荧光强度显著增强,在荧光分光光度仪下观察相对荧光峰值的变化,来测定内质网中总钙离子浓度的权威而经典的技术方法。
该技术经过精心研制、成功实验证明的。
其适用于各种组织(动物、人体等)内内质网钙离子的浓度检测。
产品严格无菌,即到即用,操作简捷,性能稳定,检测敏感。
技术背景钙是人体中的一种重要电介质和矿物质,占1150克。
其中99%的钙以氟磷灰石钙(calcium fluorophosphate apatite)形式存在于骨组织中。
非骨组织钙成分主要存在于细胞内。
钙具有两种主要形式:一种是非弥散型蛋白结合钙,其构成约40%至50%的血清中的总钙含量;另一种为弥散型游离钙,其进一步分成具有活性的复合钙(complexed calcium)和离子钙(ionized calcium)。
钙对神经肌肉兴奋性(neuromuscular excitability)、血液凝固、酶的激活、离子跨膜运输、释放神经传导介质、信使传导等方面起着重要作用。
在细胞内,钙离子主要储存在线粒体和内质网等细胞器中。
其中内质网钙离子储存在控制细胞活化、调控信号通路、蛋白分子转录后修饰,维持细胞内环境钙离子平衡方面起着重要作用。
内质网钙的检测包括沉淀法、EDTA鳌合滴定法、火焰光度法(flame photometry)、原子吸收分光光度法等技术,但容易受到钠、钾、磷酸盐、硫酸盐的干扰,或者受限于仪器的特殊的要求,以及需要内质网纯化。
Mag-Fluo--AM染料是一种钙离子低亲和性的荧光标记染料,特异性地由内质网捕获,可以检测内质网内的游离钙离子浓度的变化。
在荧光分光光度仪下,激发波长490nm,散发波长525nm,来定量测定内质网的钙浓度。
产品内容清理液(Reagent A)毫升染色液(Reagent B)微升介导液(Reagent C)微升饱和液(Reagent D)毫升阴性液(Reagent E)毫升产品说明书1份保存方式保存GENMED染色液(Reagent B)和GENMED介导液(Reagent C)在-20℃冰箱里,避免光照;其余的保存在4℃冰箱里,有效保证6月用户自备1.5毫升离心管:用于工作液配制的容器细胞培养箱:用于染色孵育96孔培养板:用于样品操作的容器荧光酶标仪:用于荧光分析(共聚焦)荧光显微镜:用于荧光染色观察实验步骤一、测定准备1.设定好荧光酶标仪(22℃):激发波长490nm,散发波长525nm2.准备好纯化的内质网样品,置于冰槽里融化3.测定开始前,将-20℃冰箱里的试剂盒中的GENMED染色液(Reagent B)室温下融化,然后分别移出微升GENMED介导液(Reagent C)和微升GENMED染色液(Reagent B)到新的1.5毫升离心管,标记为GENMED染色工作液,并放在暗室里备用。
钙测定试剂盒(邻甲酚酞络合酮法)产品技术要求haomai

钙测定试剂盒(邻甲酚酞络合酮法)适用范围:本试剂盒用于体外定量测定人血清中钙(Ca)的含量。
1.1包装规格1.2主要组成成分本试剂由试剂1(R1)、试剂2(R2)和校准品(STD)组成试剂1(R1):赖氨酸缓冲液80mmol/L试剂2(R2):8-羟基喹啉0.09g/L 邻甲酚酞络合铜0.14g/L盐酸10g/L校准品:无机钙(基质:水溶液:浓度:2.0mmol/L)2.1 外观试剂盒外观应整洁,文字符号标识清晰;R1、R2为无色透明液体,校准品为无色透明液体。
液体试剂不得有沉淀和絮状物。
2.2 装量试剂瓶内液体装量应不少于标示值。
2.3 空白吸光度以生理盐水为样品,在37℃、570nm波长、1cm光径条件下,吸光度≤0.5。
2.4 分析灵敏度浓度为2.5mmol/L的样本,吸光度差值ΔA>0.2。
2.5 准确性用参考物质(GBW09152)对试剂盒进行测试,相对偏差不超过±5%。
2.6 重复性重复测试浓度在(2.5±0.5)mmol/L的控制血清,所得结果的重复性(变异系数,CV)应不超过3%。
2.7 线性2.7.1在[1.00,3.75]mmol/L范围内,线性相关系数r应不低于0.990;2.7.2 在[1.00,3.75]mmol/L范围内相对偏差不超过±10%。
2.8 批间差用三个批号的试剂盒测定同一份样本,试剂盒批间相对极差应不超过5%。
2.9 稳定性试剂盒在2~8℃避光保存,可稳定21个月。
取到效期后的样品检测准确度、线性范围应分别符合2.5、2.7的要求。
钙测定试剂盒(偶氮胂Ⅲ法)产品技术要求danda

钙测定试剂盒(偶氮胂Ⅲ法)
适用范围:该产品用于体外定量测定人血清中钙(Ca)的含量。
1.1规格
规格1(试剂1:20mL);
规格2(试剂1:40mL);
规格3(试剂1:60mL);
规格4(试剂1:60mL×2);
规格5(试剂1:60mL×3) 。
1.2组成
试剂盒组成见表1
表1 钙测定试剂盒组成
2.1试剂
2.1外观
试剂盒外观应整洁,文字符号标识清晰, 组分齐全,液体无漏液;液体单试剂为紫红色液体。
2.2装量
每瓶不少于标示值。
2.3试剂空白吸光度
用指定的空白样品测试试剂(盒),在光径1cm下,在A660nm处测定试剂空白吸光度A≤1.0A。
2.4分析灵敏度
测定2.5mmol/L的样品,吸光度变化≥0.10A。
2.5线性范围
在[1,4] mmol/L内,相关系数R≥0.990,线性相对偏差不超过±10%。
2.6 重复性
重复测试(2.5±0.5)mmol/L的样本,所得结果的变异系数(CV%)应不大于3%。
2.7批间差
测定(2.5±0.5)mmol/L样本,所得结果的批间相对极差(R)应不大于5 %。
2.8准确度
测定国家标准物质相对偏差不超过±5%。
2.9 效期稳定性
试剂(所有组份)有效期为12个月到效期后一个月内进行检测,测定结果应符合2.3、2.4、2.5、2.6、2.8要求。
钙离子(Ca)测定试剂盒(邻甲酚酞络合酮法)产品技术要求利德曼

钙离子(Ca)测定试剂盒(邻甲酚酞络合酮法)适用范围:本产品用于体外定量测定人体血清中钙离子的含量。
1.1规格试剂1(R1):2×60mL、试剂2(R2):2×20mL;试剂1(R1):2×60mL、试剂2(R2):2×12mL;试剂1(R1):4×60mL、试剂2(R2):2×40mL;试剂1(R1):3×40mL、试剂2(R2):3×10mL;试剂1(R1):2×300mL、试剂2(R2):1×200mL;试剂1(R1):2×80mL、试剂2(R2):2×16mL;试剂1(R1):5×60mL、试剂2(R2):5×12mL;试剂1(R1):2×45mL、试剂2(R2):2×15mL;试剂1(R1):1×60mL、试剂2(R2):1×12mL;试剂1(R1):1×45mL、试剂2(R2):1×15mL;试剂1(R1):1×15mL、试剂2(R2):1×5mL;272T:【试剂1(R1):48.96mL、试剂2(R2):16.32mL】;68T:【试剂1(R1):12.24mL、试剂2(R2):4.08mL】。
校准品(选配):1×3mL。
1.2 组成试剂盒由试剂、校准品(选配)组成。
试剂1:乙醇胺:0.5mol/L;稳定剂:0.1%;试剂2:盐酸: 50mmol/L;邻甲酚酞络合剂:0.35mmol/L;8-羟基喹啉:15.17mmol/L;校准品:单个水平的液体校准品,在水基质中添加碳酸钙(纯度:大于95%)。
定值范围:(2.0-3.0 )mmol/L2.1 外观液体双试剂:R1:无色透明液体,R2:黄色透明液体。
校准品:无色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
钙测定试剂盒(邻甲酚酞络合酮法)1产品技术要求zhongshengbeikong

钙测定试剂盒(邻甲酚酞络合酮法)适用范围:本产品用于体外定量测定人血清中钙的浓度。
1.1包装规格液体双剂型(液体Ⅰ型)试剂1(R1):60mL×4,试剂2(R2):60mL×41.2主要组成成分1.2.1 试剂1(R1)(液体)乙醇胺 100mmol/L1.2.2 试剂2(R2)(液体)邻甲酚酞络合酮(OCPC)0.175mmol/L8-羟基喹啉 7.8mmol/L2.1 外观试剂盒中各组件的外观应满足:2.1.1 试剂1(R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损;2.1.2 试剂2(R2)应为浅黄色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.2 净含量液体试剂净含量应不少于标示值。
2.3 试剂空白吸光度在波长600nm(光径1cm)处,试剂空白吸光度(A)应≤0.300。
2.4 准确度测定锂、钠、钾、镁、钙、氯复合电解质冰冻人血清国家标准品(编号:360018),相对偏差应不超过±5%。
2.5 分析灵敏度对应于浓度为2.5mmol/L (10mg/dL)的Ca所引起的吸光度差值(△A)的绝对值应在0.200~0.500的范围内。
2.6 重复性重复测试同一样本,变异系数(CV)应≤3%。
2.7 批间差测定同一样本,批间差(R)应≤5%。
2.8 线性范围在[0.60,3.75]mmol/L范围内,线性相关系数(r)应≥0.990;线性相对偏差应不超过±10%。
2.9 试剂稳定性2.9.1 效期稳定性:原包装的试剂盒在2℃~8℃避光贮存,有效期为24个月。
试剂有效期满后3个月以内,试剂性能应符合2.1、2.3、2.4、2.5、2.6、2.8的要求。
2.9.2 开盖稳定性:开盖后,在2℃~8℃避光保存,稳定期为12天;稳定期满后3天内,试剂性能应符合2.1、2.3、2.4、2.5、2.6、2.8的要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
血钙浓度检测试剂盒使用说明
分光光度法货号:BC0720
规格:50管/48样
产品内容:
试剂一液体×1瓶,4℃保存。
试剂二液体×1瓶,4℃保存。
试剂三液体×1瓶(空瓶,试剂自备)。
取30mL试剂瓶,依次加入27mL无水甲醇和3mL丙酮,盖紧混匀即可。
标准液液体×1瓶3μmol/L,4℃保存。
产品说明:
血钙几乎全部存在于血浆中,所以血钙指血浆钙。
血浆钙有离子钙和结合钙两种形式,其中只有离子钙直接起生理作用,它与结合钙处于动态平衡,并受血液PH的影响。
血钙水平与多种重要的生理功能相关,过高或过低都会影响正常生理功能。
本试剂盒用于检测血液中游离钙浓度。
在强碱溶液中游离钙与GBHA反应生成红色钙-GBHA复合物在520nm有吸收峰;通过测定520nm吸光度计算游离钙浓度。
自备仪器和用品:
可见分光光度计、可调式移液枪、1mL玻璃比色皿、无水甲醇、丙酮和蒸馏水。
血钙浓度测定操作
1.分光光度计预热30min以上调节波长到520nm蒸馏水调零。
2.空白管:1mL玻璃比色皿依次加入蒸馏水50μL试剂一200μL混匀后再加入试剂二
200μL,混匀;最后加入试剂三400μL,混匀;静置5min后于520nm测定吸光度A空白管。
做一个空白管即可。
3.标准管:1mL玻璃比色皿依次加入标准液50μL试剂一200μL混匀后再加入试剂二
200μL,混匀;最后加入试剂三400μL,混匀;静置5min后于520nm测定吸光度A标准管。
做一个标准管即可。
4.测定管:1mL玻璃比色皿依次加入血液样品50μL试剂一200μL混匀后再加入试剂
二200μL,混匀;最后加入试剂三400μL,混匀;静置5min后于520nm测定吸光度A测定管。
注意:加试剂三后应该在30min内完成该管的测定。
血钙浓度计算:
血钙含量(μmol/dL血液)=[C标准液×(A测定管-A空白管)÷(A标准管-A空白管)]×V样品总=300×(A测定管-A空白管)÷(A标准管-A空白管)
C标准液:3μmol/mL;V样总样品总体积,1dL=100mL。
注意事项:
1、宜早晨空腹采血并且采血后应该尽快完成测定。
2、静止5分钟后立即测定。
3、加入试剂三后,应该在30min内完成该管的测定。
4、最低检出限为1mmol/L。
