2018年广东省药品监督管理局
广东省关于食品从业人员健康检查的管理办法

---------------------------------------------------------------范文最新推荐------------------------------------------------------ 广东省关于食品从业人员健康检查的管理办法除了此前已经实施的餐饮行业,未来我省包括保健食品、食用农产品在内的所有食品生产经营单位都经实行食品安全管理员、从业人员健康检查制度,在国内率先实现两项制度对食品生产经营全环节的覆盖。
《广东省食品药品监督管理局关于食品安全管理员的管理办法》及《广东省食品药品监督管理局关于食品从业人员健康检查的管理办法》(以下简称两项办法)已于今年6月1日起正式实施。
以下是小编给大家提供的广东省关于食品从业人员健康检查的管理办法,一起来看看吧。
广东省食品药品监督管理局关于食品从业人员健康检查的管理办法(广东省食品药品监督管理局2018年4月19日以粤食药监规〔2018〕2号发布自2018年6月1日起施行)第一条为规范广东省食品生产经营(含保健食品,下同)从业人员健康检查管理工作,根据《中华人民共和国食品安全法》及其实施条例的规定,结合本省实际,制定本办法。
第二条凡从事接触直接入口食品工作的从业人员应当每年进行健康检查,并取得《广东省食品从业人员健康证明》(以下简称《健康证明》)后方可上岗工作。
《健康证明》有效期内在全省范围内通用。
1/ 17第三条食品药品监督管理部门负责食品从业人员健康检查工作的监督管理。
广东省食品药品监督管理局应对全省食品从业人员的健康检查表和《健康证明》样式进行统一规定。
第四条广东省食品从业人员健康检查工作实行信息化管理。
具备健康检查条件的医疗卫生机构应当向所属区(县)级食品药品监督管理部门提出自愿纳入全省食品从业人员健康检查信息化管理系统的书面申请,由属地食品药品监督管理部门上报省、市食品药品监督管理部门。
广东省食品药品监督管理局应当根据各地上报名单,及时公布承担食品从业人员健康检查工作的医疗卫生机构的名单。
医疗器械注册人制度的产业影响及新机遇

医疗器械注册人制度下主题分享:汪家卫医疗器械注册人制度系列产业影响及新机遇探讨纲要回顾:注册人制度的基本介绍冲击:注册人制度对产业的影响展望:注册人制度有哪些新的机遇4分享:注册人制度成功案例321汪家卫Ø十余年医疗器械法规相关工作经验,专注于医疗器械合规战略管理;Ø深圳医疗器械质量促进会法规技术成员、广东医疗器械审评认证技术协会专家成员Ø曾就职于医疗器械知名的上市公司从事注册、体系、质量、生产等相关工作;Ø近5年多主导完成有源、口腔、软件、无菌等二三类医疗器械产品注册和辅导数十个项目;Ø主导医疗器械注册人制度项目近10个,成功完成广东省较典型的非集团委托项目一个;Ø熟悉医疗器械产品注册、临床评价、质量体系及合规审核等。
Ø擅长医疗器械合规制造及先进制造水平提升,包括有源、无菌、口腔类制造企业1医疗器械注册人制度的介绍定义:医疗器械注册人制度(Marketing Authorization Holder ),是指符合条件的医疗器械注册申请人可以单独申请医疗器械注册证,然后委托给有资质和生产能力的生产企业生产,从而实现医疗器械产品注册和生产许可的“解绑”。
该定义指出了注册人制度要实现的直接目标是“医疗器械产品注册和生产许可的解绑”,这将有利于破除产品注册审评和生产管理的障碍性因素!产品注册证生产许可证解绑2012--2015p 2012年7月启动相关课题研究p 2015年4月形成初步试点方案并上报总局p 2015年11月受权试点后,组建上海市药物创新企业促进联盟,搭建平台促进企业对接试点p 2015年8月,国务院发布《关于改革药品医疗器械审评审批制度的意见》,提出推进药品上市许可人制度。
p 2016年6月国务院办公厅正式出台了《药品上市许可持有人制度试点方案》10省市(北京、天津、河北、上海、江苏、浙江、福建、山东、广东、四川)进入试点,试点期到2018年11月4日止p 截至2016年12月25日,据食药监统计,10个试点省份药品上市许可持有人试点品种申报数量共165。
医疗器械2019年度管理评审报告全套资料

总经理 、各部门经理和各部门主管
2019年7月06日8:30,会议室
1.公司组织结构的适合性,包括部门职责、人员和其他资源。
2.产品的质量和服务与相关法规的符合性。
3.顾客反馈的信息(包括投诉、客户满意调查)。
4.生产控制、设备运行、材料供应的情况。
5.基础设施及人员培训。
10.影响质量管理系统的变更
11.适用的新的或修订的法规要求
12.组织机构设置,资源配置状况信息(人员、设备、办公环境等)
13. 各部门工作运行报告,包括以下内容:(各部门)
① 部门质量目标达成情况的总结和分析;
② 改善的建议
③ 资源需求
编制: 批准: 日期:2019年03月07日
二、
一、评审目的:
已建立程序
2018年09月07日
3.4.2内部审核结果:
于2019年05月10至05月11日进行2019年内审,质量管理体系的运行情况总体上符合ENISO13485:2016的要求,内审中发现的问题已按要求制定和实施纠正预防措施。(内部审核报告)
不符合项及整改情况如下说明:
本次内审共发现2个建议项,已开出不符合项报告,属一般不符合项。
c)生产货物按类别摆放,不合适品单独划分区域,能够达到识别及追溯性目地,实现追溯性,主要靠人员的记录及日期,出库货物都有入库日期和规格等信息。
3.5过程的监视和测量
3.5.1
纠正措施:供应商送原材料时通过抽样的方式对品质进行检验,并做出判断该批产品是允收还是拒收。当发现为不合格时,对不合格批次出具该批的《不合格品报告》,并进行处理:退货、挑选使用、让步接收。
三、评审时间:2019年07月06日
国家市场监督管理总局通告2018年第12号——市场监管总局关于18批次食品不合格情况的通告

国家市场监督管理总局通告2018年第12号——市场监管总局关于18批次食品不合格情况的通告文章属性•【制定机关】国家市场监督管理总局•【公布日期】2018.06.04•【文号】国家市场监督管理总局通告2018年第12号•【施行日期】2018.06.04•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】食品安全正文国家市场监督管理总局通告2018年第12号市场监管总局关于18批次食品不合格情况的通告近期,原国家食品药品监督管理总局组织抽检炒货食品及坚果制品,方便食品,糕点,酒类,肉制品,食用油、油脂及其制品,蔬菜制品,蜂产品,水果制品,特殊膳食食品和食用农产品等11类食品556批次样品,抽样检验项目合格样品538批次,不合格样品18批次,检测项目见附件。
根据食品安全国家标准,个别项目不合格,其产品即判定为不合格产品。
具体情况通告如下:一、总体情况:炒货食品及坚果制品45批次,不合格样品2批次。
方便食品36批次,不合格样品3批次。
糕点26批次,不合格样品3批次。
酒类38批次,不合格样品1批次。
肉制品20批次,不合格样品1批次。
食用油、油脂及其制品18批次,不合格样品1批次。
蔬菜制品113批次,不合格样品1批次。
食用农产品156批次,不合格样品6批次。
蜂产品34批次,水果制品35批次,特殊膳食食品35批次,均未检出不合格样品。
二、不合格产品情况如下:(一)宁波市鄞州下应美购超市销售的标称厦门好士多食品有限公司出品、龙海市真好意食品有限公司生产的青豆(蒜香味),酸价(以脂肪计)检出值为5.2mgKOH/g,比国家标准规定(不超过3mgKOH/g)高出73.3%。
初检机构为宁波出入境检验检疫局检验检疫技术中心,复检机构为福建中检华日食品安全检测有限公司。
(二)深圳沃尔玛百货零售有限公司成都交大路分店销售的标称贵阳恒昌生态农业有限公司生产的巴旦木,二氧化硫残留量检出值为0.85g/kg。
国家标准规定不得使用。
广东省食品药品监督管理局药品零售企业分级分类的管理办法

各地级以上市食品药品监管局:《广东省食品药品监督管理局药品零售企业分级分类的管理办法(试行)》经2017年9月30日省食品药品监督管理局局务会审议通过,并经广东省人民政府法制办公室审查通过。
现印发给你们,请遵照执行。
广东省食品药品监督管理局2018年3月12日广东省食品药品监督管理局关于药品零售企业分级分类的管理办法(试行)第一章总则第一条为落实《国务院办公厅关于进一步改革完善药品生产流通使用政策的若干意见》(国办发〔2017〕13号),推进分级分类管理,规范药品零售企业经营行为,促进我省医药产业有序发展,根据《中华人民共和国药品管理法》及其实施条例、《药品经营质量管理规范》及《药品经营许可证管理办法》等规定,结合我省实际,制定本管理办法。
第二条本标准适用于广东省行政区域内药品零售企业(含药品零售连锁企业门店,以下简称“企业”)《药品经营许可证》的核发、换证、变更。
第三条本标准中的分级分类管理,是指食品药品监督管理部门根据企业经营场地规模、药品经营范围、药学技术人员配置情况、药品质量管理、药品追溯管理、信息化管理水平、药学服务能力等因素,对其经营资质和风险管控实施动态分类管理的活动。
第四条省食品药品监督管理部门负责制定本管理办法,指导地级市食品药品监督管理部门开展分级分类管理工作。
全省各地级市食品药品监督管理部门可结合本辖区实际依法制定具体有关细则,并指导区、县级食品药品监督管理部门具体实施。
地级市级食品药品监督管理部门负责本辖区内药品零售企业《药品经营许可证》的管理工作。
各级食品药品监管部门按照属地管理原则负责药品零售企业的日常监督管理工作。
第二章分级分类第五条根据药品零售企业设置条件与药品经营范围、经营规模的适应程度,核定的经营范围从小到大分为一类、二类和三类,相对应的企业分别简称为一类店、二类店和三类店。
(一)一类店经营范围限定为非处方药。
(二)二类店经营范围限定为非处方药、处方药(注射剂、肿瘤治疗药、抗生素、生物制品、二类精神药品、医疗用毒性药品、罂粟壳、中药饮片等除外),《药品经营许可证》经营范围标注“必须凭处方销售的药品除外”字样,同时注明上述必须凭处方销售的药品除外的类别。
广东省市场监督管理局(知识产权局)挂牌成立

龙源期刊网
广东省市场监督管理局(知识产权局)挂牌成立
作者:
来源:《中国知识产权》2018年第11期
10月19日,广东省市场监督管理局(知识产权局)挂牌成立。
根据《广东省机构改革方案》,新组建的广东省市场监督管理局整合了原省工商行政管理局、原省质量技术监督局、原省食品药品监督管理局、原省知识产权局的职责,以及省发改委的价格监督检查与反垄断执法职责、省商务厅的经营者集中反垄断职责等。
不再保留省工商行政管理局、省质量技术监督局、省食品药品监督管理局,不再保留单设的省知识产权局。
省市场监督管理局加挂省知识产权局牌子。
省食品安全委員会具体工作由省市场监督管理局承担。
同时,组建广东省药品监督管理局,作为省市场监督管理局的部门管理机构;组建广东省知识产权保护中心,为省市场监督管理局管理的事业单位。
广东省药品监督管理局也于同日挂牌成立。
国家药品监督管理局公告 2018年第97号

国家药品监督管理局公告2018年第97号关于批准发布YY0042-2018《高频喷射呼吸机》等27项医疗器械行业标准的公告国家药监局2018年12月20日序号YY0042-20072018-12-202020-06-012YY0290.3-2018眼科光学人工晶状体第3部分:机械性能及测试方法YY0290.3-20084YY0778-2018射频消融导管YY0778-20102018-12-202020-06-01无菌医疗器械包装试验方法第1部分:加速老化试验指南YY/T0681.1-20092018-12-202020-01-017YY/T0734.2-2018清洗消毒器第2部分:对外科和麻醉器械等进行湿热消毒的清洗消毒器YY/T0734.3-20092018-12-202020-01-019YY/T0865.2-2018超声水听器第2部分:40MHz以下超声场用水听器的校准2020-01-0111YY/T1043.2-2018牙科学牙科治疗机第2部分:气、水、吸引和废水系统YY/T0630-2008 YY/T0725-20092018-12-202020-01-01YY/T1090-2018超声理疗设备YY1090-20092018-12-202020-01-0114人类免疫缺陷病毒抗体检测试剂盒(免疫层析法)2018-12-202020-01-01YY/T1625-2018移动式X射线计算机体层摄影设备专用技术条件18YY/T1631.1-2018输血器与血液成分相容性测定第1部分:血液成分残留评定2018-12-202020-01-01关节置换植入物肩关节假体关节盂松动或分离动态评价试验方法2018-12-202020-01-0121YY/T1635-2018 多道生理记录仪2020-01-0123YY/T1637-2018牙科学磁性附着体2018-12-202019-06-01YY/T1640-2018外科植入物磷酸钙颗粒、制品和涂层溶解性的试验方法2018-12-202020-01-0126YY/T1641-20182018-12-20 2020-01-01。
国家食品药品监督管理总局公告 2018年第8号

国家食品药品监督管理总局公告2018年第8号关于批准发布YY0645-2018《连续性血液净化设备》等9项医疗器械行业标准的公告(2018年第8号)YY0645-2018《连续性血液净化设备》等9项医疗器械行业标准已经审定通过,现予以公布。
标准自2019年1月1日起实施,标准编号、名称如下:YY0645-2018《连续性血液净化设备》YY/T0514-2018《牙科学气动牙科手机用软管连接件》YY/T0744-2018《移动式C形臂X射线机专用技术条件》YY/T1600-2018《医疗器械湿热灭菌的产品族和过程类别》YY/T1601-2018《超声骨组织手术设备》YY/T1602-2018《牙科学根管预备机》YY/T1603-2018《医用内窥镜内窥镜功能供给装置摄像系统》YY/T1604-2018《牙科学旋转抛光器械》YY/T1610-2018《麻醉和呼吸设备医用氧气湿化器》上述标准适用范围见附件。
特此公告。
附件:YY0645-2018《连续性血液净化设备》等9项医疗器械行业标准适用范围食品药品监管总局2018年1月19日序号标准编号标准名称代替标准号发布日期实施日期1YY0645-2018连续性血液净化设备YY0645-20082018-01-192019-01-012YY/T0514-2018牙科学气动牙科手机用软管连接件YY/T0514-20092018-01-193YY/T0744-2018移动式C形臂X射线机专用技术条件YY/T0744-20092018-01-192019-01-014YY/T1600-2018医疗器械湿热灭菌的产品族和过程类别2018-01-195YY/T1601-2018超声骨组织手术设备2018-01-192019-01-016YY/T1602-2018牙科学根管预备机2018-01-192019-01-017YY/T1603-2018医用内窥镜内窥镜功能供给装置摄像系统2018-01-192019-01-018YY/T1604-2018科学旋转抛光器械2018-01-192019-01-019YY/T1610-2018麻醉和呼吸设备医用氧气湿化器2018-01-192019-01-01。
国家药品监督管理局公告第

国家药品监督管理局公告2018年第87号关于批准发布YY0060-2018《热敷贴(袋)》等14项医疗器械行业标准和1项修改单的公告YY0060-2018《热敷贴(袋)》等14项医疗器械行业标准和YY0650-2008《妇科射频治疗仪》第1号修改单已经审定通过,现予以公布。
其中,YY0060-2018《热敷贴(袋)》等2项强制性行业标准自2020年5月1日起实施,YY/T0449-2018《超声多普勒胎儿监护仪》等12项推荐性行业标准自2019年11月1日起实施,YY0650-2008《妇科射频治疗仪》第1号修改单自发布之日起实施。
标准编号、名称、适用范围及修改单内容见附件。
特此公告。
附件:1.YY0060-2018《热敷贴(袋)》等14项医疗器械行业标准编号、名称及适用范围2.YY0650-2008《妇科射频治疗仪》第1号修改单国家药监局2018年11月7日序号标准编号标准名称代替标准号发布日期实施日期1YY0060-2018热敷贴(袋)YY0060-19912018-11-072020-05-012YY0585.3-2018压力输液设备用一次性使用液路及附件第3部分:过滤器YY0585.3-20052018-11-072020-05-013超声多普勒胎儿监护仪YY/T0449-20092018-11-072019-11-014YY/T0590.1-2018医用电气设备数字X射线成像装置特性第1-1部分:量子探测效率的测定普通摄影用探测器YY/T0590.1-20052018-11-072019-11-015医用诊断X射线管组件通用技术条件YY/T0609-20072018-11-072019-11-016YY/T0616.3-2018一次性使用医用手套第3部分:用仓贮中的成品手套确定实际时间失效日期的方法2018-11-072019-11-01YY/T0681.14-2018无菌医疗器械包装试验方法第14部分:透气包装材料湿性和干性微生物屏障试验2018-11-072019-11-018YY/T0734.1-2018清洗消毒器第1部分:通用要求和试验YY/T0734.1-20092018-11-072019-11-01YY/T1615-2018外科植入物钛及钛合金阳极氧化膜通用要求2018-11-072019-11-0110YY/T1616-2018组织工程医疗器械产品生物材料支架的性能和测试指南YY/T0606.5-20072018-11-072019-11-0111YY/T1617-2018血袋用聚氯乙烯压延薄膜2018-11-072019-11-0112YY/T1622.1-2018牙科学牙周探针第1部分:通用要求2018-11-072019-11-0113YY/T1627-2018急性创面用敷贴、创贴通用要求2018-11-072019-11-0114YY/T1629.2-2018电动骨组织手术设备刀具第2部分:颅骨钻头2018-11-072019-11-0116YY0650-2008《妇科射频治疗仪》第1号修改单2018-11-072018-11-07。
2018年广东食品药品监督管理局直属单位拟录用参公管理
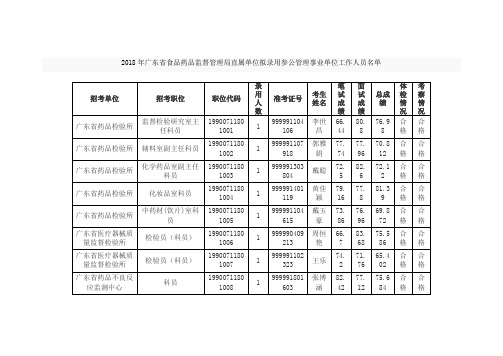
招考单位
招考职位
职位代码
录用
人数
准考证号
考生
姓名
笔试
成绩
面试
成绩
总成绩
体检
情况
考察
情况
广东省药品检验所
监督检验研究室主任科员
19900711801001
1
999991104106
李世昌
66.44
80.8
76.98
合格
合格
广东省药品检验所
1
999991401119
黄佳颖
79.16
77.8
81.39
合格
合格
广东省药品检验所
中药材(饮片)室科员
19900711801005
1
999991104615
戴玉豪
73.86
76.96
69.872
合格
合格
广东省医疗器械质量监督检验所
检验员(科员)
19900711801006
1
999990409213
周恒艳
66.7
83.68
75.586
合格
合格
广东省医疗器械质量监督检验所
检验员(科员)
19900711801007
1
999991102323
王乐
74.2
71.76
65.402
合格
合格
广东省药品不良反应监测中心
科员
19900711801008
1
999991801603
张博涵
82.42
77.12
75.684
合格
国家市场监督管理总局通告2018年第25号——市场监管总局关于28批次食品不合格情况的通告

国家市场监督管理总局通告2018年第25号——市场监管总局关于28批次食品不合格情况的通告文章属性•【制定机关】国家市场监督管理总局•【公布日期】2018.08.27•【文号】国家市场监督管理总局通告2018年第25号•【施行日期】2018.08.27•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】食品安全正文国家市场监督管理总局通告2018年第25号市场监管总局关于28批次食品不合格情况的通告近期,国家市场监督管理总局组织抽检蔬菜制品、调味品、保健食品、茶叶及相关制品、豆制品、罐头、乳制品、糖果制品、酒类和食用农产品等10类食品735批次样品。
根据食品安全国家标准检验和判定,其中合格样品707批次,不合格样品28批次(见附件)。
具体情况通告如下:一、京东商城泓翔食品专营店(经营者为北京泓翔优选商贸有限责任公司)在京东商城(网站)销售的标称湖南开口爽食品有限公司生产的馋恋猫萝卜(香辣味),防腐剂混合使用时各自用量占其最大使用量的比例之和检出值为1.829,比国家标准规定(不超过1)高出82.9%。
检验机构为山东省食品药品检验研究院。
二、京东商城桃潭兰花旗舰店(经营者为安徽泾县家乡好味道食品有限公司)在京东商城(网站)销售的标称安徽泾县家乡好味道食品有限公司委托安徽省泾县丁渡酱制品有限公司生产的鲜嫩生姜,防腐剂混合使用时各自用量占其最大使用量的比例之和检出值为1.319,比国家标准规定(不超过1)高出31.9%。
检验机构为山东省食品药品检验研究院。
三、京东商城泓翔食品专营店(经营者为北京泓翔优选商贸有限责任公司)在京东商城(网站)销售的标称湖南开口爽食品有限公司生产的馋恋猫金针菇(香辣味),山梨酸及其钾盐(以山梨酸计)检出值为0.657g/kg,比国家标准规定(不超过0.5g/kg)高出31.4%;防腐剂混合使用时各自用量占其最大使用量的比例之和检出值为2.311,比国家标准规定(不超过1)高出1.311倍。
国家市场监督管理总局通告2018年第39号——市场监管总局关于33批次食品不合格情况的通告

国家市场监督管理总局通告2018年第39号——市场监管总局关于33批次食品不合格情况的通告文章属性•【制定机关】国家市场监督管理总局•【公布日期】2018.11.06•【文号】国家市场监督管理总局通告2018年第39号•【施行日期】2018.11.06•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】食品安全正文国家市场监督管理总局通告2018年第39号市场监管总局关于33批次食品不合格情况的通告近期,市场监管总局组织抽检肉制品、水产制品、乳制品、婴幼儿配方食品和食用农产品等5类食品1209批次样品。
根据食品安全国家标准检验和判定,其中抽样检验项目合格样品1176批次、不合格样品33批次(见附件)。
具体情况通告如下:一、四川省成都市大邑百伦商贸有限公司销售的标称成都利顿食品有限公司生产的烤卤鸡翅(香辣味),菌落总数不符合食品安全国家标准规定。
检验机构为南京市产品质量监督检验院。
二、中兴_沈阳商业大厦(集团)股份有限公司中兴超市大东店销售的标称金百味集团·大连金百味食品有限公司生产的金百味里脊火腿,菌落总数不符合食品安全国家标准规定。
检验机构为黑龙江省质量监督检测研究院。
三、天猫汉味黑鸭旗舰店(经营者为武汉汉哈哈食品有限公司)在天猫(网站)销售的标称武汉汉哈哈食品有限公司生产的汉味黑鸭(全鸭),菌落总数不符合食品安全国家标准规定。
检验机构为国家肉类食品质量监督检验中心。
四、1号店(经营者为上海京东才奥电子商务有限公司)在1号店(网站)销售的标称佳木斯市哈尔香食品有限公司生产的林道斯哈尔滨风味红肠,菌落总数不符合食品安全国家标准规定。
检验机构为国家肉类食品质量监督检验中心。
五、京东桂花鸭官方旗舰店(经营者为南京桂雨鸭食品有限公司)在京东商城(网站)销售的标称南京桂雨鸭食品有限公司生产的490g盐水鸭,菌落总数不符合食品安全国家标准规定。
检验机构为国家肉类食品质量监督检验中心。
六、天猫互惠食品专营店(经营者为福建沙县郑湖垚香胡记板鸭食品厂)在天猫(网站)销售的标称福建沙县郑湖垚香胡记板鸭食品厂生产的板鸭,菌落总数不符合食品安全国家标准规定。
广东省食品药品监督管理局互联网药品经营监督管理办法

广东省食品药品监督管理局互联网药品经营监督管理办法文章属性•【制定机关】广东省食品药品监督管理局•【公布日期】2016.11.22•【字号】粤食药监局药通〔2016〕231号•【施行日期】2016.12.24•【效力等级】地方规范性文件•【时效性】失效•【主题分类】药政管理正文广东省食品药品监督管理局互联网药品经营监督管理办法(广东省食品药品监督管理局2016年11月22日以粤食药监局药通〔2016〕231号发布自2016年12月24日起施行)第一条为加强广东省内互联网药品、医疗器械经营的监督管理,保障药品、医疗器械安全,依据《中华人民共和国药品管理法》及其实施条例、《医疗器械监督管理条例》、《药品经营质量管理规范》、《医疗器械经营质量管理规范》、《互联网药品信息服务管理办法》、《互联网药品交易服务审批暂行规定》等法律法规,制定本办法。
第二条互联网药品经营企业包括下列三种类型:(一)为药品生产企业、药品经营企业和医疗机构之间的互联网药品交易提供服务的,简称A证企业;(二)药品生产企业、药品批发企业通过自身网站与本企业成员之外的其他企业进行互联网药品交易的,简称B证企业;(三)向个人消费者提供互联网药品交易服务的,简称C证企业。
第三条互联网药品经营企业应当坚持诚实守信,依法经营。
禁止任何虚假、欺骗行为。
第四条互联网药品经营监督管理,应当推进诚信体系建设,推动部门协作,鼓励举报违法行为;充分发挥行业协会、消费者权益保护协会等机构的作用,促进社会共治。
第五条各级食品药品监督管理部门应当加强安全合理用药的公益宣传,及时发布消费警示,保障消费者合法权益。
第六条互联网药品经营企业应在其网站首页显著位置标明《互联网药品交易服务资格证》证书号码,以及《药品经营许可证》、《医疗器械经营许可证》或备案凭证证书号码(A证企业除外),并提供与食品药品监督管理部门政府网站的电子链接。
第七条互联网药品经营企业的交易服务信息系统应当设置监管子系统,以便食品药品监督管理部门对在系统中发生的药品、医疗器械经营行为进行数据查询、汇总。
广州柏赛罗药业有限公司与广州市花都区市场监督管理局食品药品安全其他行政行为纠纷上诉案

广州柏赛罗药业有限公司与广州市花都区市场监督管理局食品药品安全其他行政行为纠纷上诉案【案由】行政行政行为种类其他行政行为【审理法院】广州铁路运输中级法院【审理法院】广州铁路运输中级法院【审结日期】2020.06.29【案件字号】(2020)粤71行终878号【审理程序】二审【审理法官】陈作斌张珣王硕【审理法官】陈作斌张珣王硕【文书类型】判决书【当事人】广州柏赛罗药业有限公司;广州市花都区某某监督管理局【当事人】广州柏赛罗药业有限公司广州市花都区某某监督管理局【当事人-公司】广州柏赛罗药业有限公司广州市花都区某某监督管理局【法院级别】中级人民法院专门人民法院【原告】广州柏赛罗药业有限公司【本院观点】《中华人民共和国药品管理法》(2015年修正)第六十三条第一款、《药品生产监督管理办法》(2017年修正)第三十八条第一款、第三十九条规定,药品监督管理部门有权按照法律、行政法规的规定对药品的生产、经营进行监督检查,有关单位和个人不得拒绝;省食品药品监督管理部门应当建立实施监督检查的运行机制和管理制度,并明确设区的市级食品药品监督管理部门的监督检查职责,该监督检查包括现场检查、日常监督检查等。
【权责关键词】其他行政行为合法违法管辖合法性维持原判【指导案例标记】0【指导案例排序】0【本院查明】经审查,原审法院查明事实清楚,且有相应证据证实,本院予以确认。
【本院认为】本院认为《中华人民共和国药品管理法》(2015年修正)第六十三条第一款、《药品生产监督管理办法》(2017年修正)第三十八条第一款、第三十九条规定,药品监督管理部门有权按照法律、行政法规的规定对药品的生产、经营进行监督检查,有关单位和个人不得拒绝;省食品药品监督管理部门应当建立实施监督检查的运行机制和管理制度,并明确设区的市级食品药品监督管理部门的监督检查职责,该监督检查包括现场检查、日常监督检查等。
为落实监管职责,广东省药品监督管理局制定了《广东省2019年药品生产环节监督检查计划》,该计划明确由各地市局负责A级、B级、C级风险药品生产企业的日常监督检查工作,由各地市局按照分类监管及有关文件规定要求,科学制定年度日常监督检查计划。
国家市场监督管理总局通告2018年第37号——市场监管总局关于22批次食品不合格情况的通告

国家市场监督管理总局通告2018年第37号——市场监管总局关于22批次食品不合格情况的通告文章属性•【制定机关】国家市场监督管理总局•【公布日期】2018.10.29•【文号】国家市场监督管理总局通告2018年第37号•【施行日期】2018.10.29•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】食品安全,市场规范管理正文国家市场监督管理总局通告2018年第37号市场监管总局关于22批次食品不合格情况的通告近期,国家市场监督管理总局组织抽检食用油、油脂及其制品,肉制品,豆制品和食用农产品等4类食品744批次样品。
根据食品安全国家标准检验和判定,其中抽样检验项目合格样品722批次、不合格样品22批次(见附件)。
具体情况通告如下:一、哈尔滨新世纪家得乐商贸有限公司志华店销售的标称黑龙江省建三江农垦荣氏粮油工贸有限公司生产的仁义大豆油,酸值(KOH)不符合食品安全国家标准规定。
检验机构为国家肉类食品质量监督检验中心。
二、沈阳沃尔玛百货有限公司太原街分店销售的标称辽宁智胜食品有限公司生产的哈尔滨风味红肠,菌落总数不符合食品安全国家标准规定。
检验机构为黑龙江省质量监督检测研究院。
三、沃尔玛华东百货有限公司销售的标称佳木斯市哈尔香食品有限公司生产的林道斯哈尔滨风味红肠,菌落总数不符合食品安全国家标准规定。
检验机构为宁波出入境检验检疫局检验检疫技术中心。
四、上海农工商川沙超市有限公司川沙店销售的标称辽宁智胜食品有限公司生产的智胜哈尔滨风味红肠,菌落总数不符合食品安全国家标准规定。
检验机构为宁波出入境检验检疫局检验检疫技术中心。
五、广西华联综合超市有限公司销售的标称广州市粤秀食品有限公司委托广州市富农食品有限公司生产的牛肉干(咖喱味),菌落总数不符合食品安全国家标准规定。
检验机构为国家糖业质量监督检验中心。
六、哈尔滨市道外区利隆食品经销部销售的标称黑龙江省佳木斯市羽琨食品有限公司生产的哈尔滨风味红肠,菌落总数不符合食品安全国家标准规定。
广东省食品药品监督管理局政务服务中心(企业信用报告)- 天眼查

/
注册时间:
/
注册地址:
/
营业期限:
/至/
经营范围:
/
登记机关:
/
核准日期:
/
1.2 分支机构
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参
3
4.3 核心团队
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参 考。
4.4 企业业务
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参 考。
5.6 严重违法
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参 考。
5.7 股权出质
考。
1.3 变更记录
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参 考。
1.4 主要人员
截止 2018 年 09 月 15 日,根据国内相关网站检索及天眼查数据库分析,未查询到相关信息。不排除因信 息公开来源尚未公开、公开形式存在差异等情况导致的信息与客观事实不完全一致的情形。仅供客户参 考。
广东省食品药品监督管理局药品零售企业分级分类的管理办法

各地级以上市食品药品监管局:《广东省食品药品监督管理局药品零售企业分级分类的管理办法(试行)》经2017 年9 月30 日省食品药品监督管理局局务会审议通过,并经广东省人民政府法制办公室审查通过。
现印发给你们,请遵照执行。
广东省食品药品监督管理局2018 年3 月12 日广东省食品药品监督管理局关于药品零售企业分级分类的管理办法(试行)第一章总则第一条为落实《国务院办公厅关于进一步改革完善药品生产流通使用政策的若干意见》(国办发〔2017 〕13 号),推进分级分类管理,规范药品零售企业经营行为,促进我省医药产业有序发展,根据《中华人民共和国药品管理法》及其实施条例、《药品经营质量管理规范》及《药品经营许可证管理办法》等规定,结合我省实际,制定本管理办法。
第二条本标准适用于广东省行政区域内药品零售企业(含药品零售连锁企业门店,以下简称“企业”)《药品经营许可证》的核发、换证、变更。
第三条本标准中的分级分类管理,是指食品药品监督管理部门根据企业经营场地规模、药品经营范围、药学技术人员配置情况、药品质量管理、药品追溯管理、信息化管理水平、药学服务能力等因素,对其经营资质和风险管控实施动态分类管理的活动。
第四条省食品药品监督管理部门负责制定本管理办法,指导地级市食品药品监督管理部门开展分级分类管理工作。
全省各地级市食品药品监督管理部门可结合本辖区实际依法制定具体有关细则,并指导区、县级食品药品监督管理部门具体实施。
地级市级食品药品监督管理部门负责本辖区内药品零售企业《药品经营许可证》的管理工作。
各级食品药品监管部门按照属地管理原则负责药品零售企业的日常监督管理工作。
第二章分级分类第五条根据药品零售企业设置条件与药品经营范围、经营规模的适应程度,核定的经营范围从小到大分为一类、二类和三类,相对应的企业分别简称为一类店、二类店和三类店。
(一)一类店经营范围限定为非处方药。
(二)二类店经营范围限定为非处方药、处方药(注射剂、肿瘤治疗药、抗生素、生物制品、二类精神药品、医疗用毒性药品、罂粟壳、中药饮片等除外),《药品经营许可证》经营范围标注“必须凭处方销售的药品除外”字样,同时注明上述必须凭处方销售的药品除外的类别。
国家市场监督管理总局通告2018年第24号——市场监管总局关于26批次食品不合格情况的通告

国家市场监督管理总局通告2018年第24号——市场监管总局关于26批次食品不合格情况的通告文章属性•【制定机关】国家市场监督管理总局•【公布日期】2018.08.20•【文号】国家市场监督管理总局通告2018年第24号•【施行日期】2018.08.20•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】食品安全正文国家市场监督管理总局通告2018年第24号市场监管总局关于26批次食品不合格情况的通告近期,国家市场监督管理总局组织抽检炒货食品及坚果制品,蜂产品,薯类和膨化食品,肉制品,食用油、油脂及其制品,蔬菜制品,水果制品,食用农产品和婴幼儿配方食品等9类食品750批次样品,抽样检验项目合格样品724批次,不合格样品26批次,检测项目见附件。
根据食品安全国家标准,个别项目不合格,其产品即判定为不合格产品。
具体情况通告如下:一、天猫商城纤手食品旗舰(经营者为江苏正林食品有限公司)在天猫(网站)销售的标称江苏正林食品有限公司生产的原味香瓜子,过氧化值(以脂肪计)检出值为2.5g/100g,比国家标准规定(不超过0.80g/100g)高出2.1倍。
检验机构为哈尔滨市产品质量监督检验院。
二、天猫商城好迪食品旗舰店(经营者为常州市吕蒙商贸有限公司)在天猫(网站)销售的标称江苏茂兴食品有限公司生产的焦糖味瓜子,过氧化值(以脂肪计)检出值为0.92g/100g,比国家标准规定(不超过0.80g/100g)高出15.0%。
检验机构为哈尔滨市产品质量监督检验院。
三、天猫商城信礼坊旗舰店(经营者为上海索伊贸易有限公司)在天猫(网站)销售的标称江苏味冠食品有限公司生产的五香花生,二氧化硫残留量检出值为0.10g/kg。
国家标准规定不得使用。
初检机构为哈尔滨市产品质量监督检验院,复检机构为国家加工食品及食品添加剂质量监督检验中心(南京)。
四、天猫商城华味亨旗舰店(经营者为杭州华味亨食品有限公司)在天猫(网站)销售的标称杭州华味亨食品有限公司生产的淮盐花生(油炸类炒货),过氧化值(以脂肪计)检出值为0.68g/100g,比国家标准规定(不超过0.50g/100g)高出36.0%。
广东省药品监督管理局第二类创新医疗器械特别审查程序.doc

广东省药品监督管理局第二类创新医疗器械特别审查程序(第二次修订稿)第一条为了鼓励广东省医疗器械的研究与创新,促进我省医疗器械新技术的推广和应用,推动我省医疗器械产业健康发展,根据《医疗器械监督管理条例》《中共中央办公厅国务院办公厅印发〈关于深化审评审批制度改革鼓励药品医疗器械创新的意见〉的通知》(厅字〔2017〕42号)和国家药品监督管理局《关于发布创新医疗器械特别审查程序的公告》(2018年第83号)等有关规定,制定本程序。
第二条省药品监督管理局(以下简称省局)对同时符合下列情形的医疗器械实施特别审查:(一)申报产品为第二类医疗器械,申请人住所在我省辖区内,申报产品拟由申请人生产。
(二)申报产品具有如下知识产权或获奖证明之一:1.国家级发明奖、科技进步奖;2.省级科技进步奖二等奖以上;3.市级科技进步奖一等奖;4.核心技术发明专利;5.实用新型专利(与临床应用相关)。
(三)申报产品具有显著的临床应用价值,产品技术为国内领先,或可填补省内该品种医疗器械的空白,或可替代同类进口产品。
(四)申请人已完成申报产品的前期研究并具有基本定型产品,研究过程真实和受控,研究数据完整和可溯源。
第三条省局及相关技术机构,根据各自职责和本程序规定,按照早期介入、专人负责、科学审查的原则,在标准不降低、程序不减少的前提下,对创新医疗器械予以优先办理,并加强与申请人的沟通交流。
第四条经国家药品监督管理局医疗器械技术审评中心审查同意进行特别审查的第二类医疗器械注册申请项目,可直接按本程序执行。
第五条申请人应当在医疗器械首次注册申请前填写《广东省第二类创新医疗器械特别审查申请表》(见附件1),并提交支持拟申报产品符合本程序第二条要求的相关证明文件及所提交资料真实性的自我保证声明。
包括:(一)申请人企业法人资质证明文件。
(二)产品知识产权或获奖证明文件。
对于提交产品核心技术发明专利的,还应满足以下之一:1.依法取得发明专利权或者其使用权;2.发明专利申请已由国务院专利行政部门公开,并由国家知识产权局专利检索咨询中心出具检索报告或由具备资质的查新机构出具查新报告,报告载明产品核心技术方案具备新颖性和创造性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2018年广东省药品监督管理局部门决算报告目录第一部分广东省药品监督管理局概况一、部门主要职责二、部门决算单位构成第二部分广东省药品监督管理局2018年部门决算表一、收入支出决算总表二、收入决算表三、支出决算表四、财政拨款收入支出决算总表五、一般公共预算财政拨款支出决算表六、一般公共预算财政拨款基本支出决算表七、一般公共预算财政拨款“三公”经费支出决算表八、政府性基金预算财政拨款收入支出决算表第三部分广东省药品监督管理局2018年部门决算情况说明第四部分名词解释第一部分广东省药品监督管理局概况(一)部门主要职责1.负责药品、医疗器械和化妆品安全监督管理。
拟定监督管理政策规划,组织起草有关地方性法规、规章草案,并监督实施。
研究拟定鼓励药品、医疗器械和化妆品新技术新产品的管理与服务政策。
2.负责监督实施药品、医疗器械和化妆品标准以及分类管理制度。
组织制定药品、医疗器械地方性标准。
配合实施国家基本药物制度。
3.负责药品、医疗器械和化妆品生产环节的许可,以及药品批发许可、零售连锁总部许可、互联网销售第三方平台备案,依职责承担药品、医疗器械和化妆品注册管理工作。
4.负责药品、医疗器械和化妆品质量管理。
监督实施生产质量管理规范、药品批发(含零售连锁)经营质量管理规范,指导实施其他经营、使用质量管理规范。
5.负责药品、医疗器械和化妆品上市后风险管理。
组织开展药品不良反应、医疗器械不良事件和化妆品不良反应的监测、评价和处置工作。
依法承担药品、医疗器械和化妆品安全风险监测和应急管理工作。
(六)负责组织指导药品、医疗器械和化妆品监督检查。
依法查处药品、医疗器械和化妆品生产环节,以及药品批发、零售连锁总部、互联网销售第三方平台的违法行为。
7.负责执业药师资格准入管理。
组织实施执业药师资格准入制度,指导监督执业药师注册工作。
8.负责指导省药监局粤东、粤西、粤北、广州、深圳药品稽查办公室工作。
9.负责指导市县市场监督管理部门承担的药品、医疗器械、化妆品经营和使用环节的监督管理工作。
10.完成省委、省政府和国家药监局交办的其他任务。
(二)部门决算单位构成按照部门决算编报要求,纳入广东省药品监督管理局2018年部门决算编制范围的单位共9个,包括局本级和下属8个预算单位,分别是:⒈广东省食品药品监督管理局(本级)⒉广东省药品检验所⒊广东省医疗器械质量监督检验所⒋广东省食品药品监督管理局审评认证中心⒌广东省食品检验所⒍广东省食品药品监督管理局政务服务中心⒎广东省药品不良反应监测中心⒏广东省执业药师注册中心⒐广东省医疗器械质量监督检验包装材料容器检验中心其中广东省食品检验所因省级机构改革,2018年12月划转省市场监管局。
按照经费划转有关规定并结合单位实际,该所2018年经费未划转至省市场监管局,按照决算编制统一口径,其2018年部门决算仍在我局编报。
第二部分广东省药品监督管理局2018年部门决算表表1收入支出决算总表部门:广东省药品监督管理局单位:万元6收入支出决算总表部门:广东省药品监督管理局单位:万元7收入支出决算总表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度的总收支和年末结转情况。
8表2收入决算表部门:广东省药品监督管理局单位:万元9表2收入决算表部门:广东省药品监督管理局单位:万元10表2收入决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度取得的各项收入情况。
表3支出决算表部门:广东省药品监督管理局单位:万元表3支出决算表部门:广东省药品监督管理局单位:万元表3支出决算表部门:广东省药品监督管理局单位:万元表3支出决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度各项支出情况。
表4财政拨款收入支出决算总表部门:广东省药品监督管理局单位:万元表4财政拨款收入支出决算总表部门:广东省药品监督管理局单位:万元表4财政拨款收入支出决算总表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度财政拨款的总收支和年末结转结余情况。
表5一般公共预算财政拨款支出决算表部门:广东省药品监督管理局单位:万元表5一般公共预算财政拨款支出决算表部门:广东省药品监督管理局单位:万元表5一般公共预算财政拨款支出决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度一般公共预算财政拨款实际支出情况。
表6一般公共预算财政拨款基本支出决算表部门:广东省药品监督管理局单位:万元表6一般公共预算财政拨款基本支出决算表部门:广东省药品监督管理局单位:万元表6一般公共预算财政拨款基本支出决算表部门:广东省药品监督管理局单位:万元表6一般公共预算财政拨款基本支出决算表部门:广东省药品监督管理局单位:万元表6一般公共预算财政拨款基本支出决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度一般公共预算财政拨款基本支出明细情况。
表7一般公共预算财政拨款“三公”经费支出决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度财政拨款“三公”经费支出情况。
其中,预算数为“三公”经费年初预算数,决算数是包括当年一般公共预算财政拨款和以前年度结转资金安排的实际支出。
表8政府性基金预算财政拨款收入支出决算表部门:广东省药品监督管理局单位:万元表8政府性基金预算财政拨款收入支出决算表部门:广东省药品监督管理局单位:万元注:本表反映部门本年度政府性基金预算财政拨款收入、支出及结转结余情况。
第三部分广东省药品监督管理局2018年部门决算情况说明一、 2018年度收入支出决算总体情况说明(一)年度收入总体情况广东省药品监督管理局2018年度总收入 100,683.30万元,其中本年收入 85,149.73万元。
具体情况如下:1.财政拨款收入 61,670.19万元,比上年决算数增加5,268.21万元,增长9.34%,主要原因是2018年按照统一的人员工资政策,人员经费较上年增加。
2.上级补助收入 0.00万元,与上年决算数持平。
3.事业收入 22,953.54万元,比上年决算数增加2,533.99万元,增长12.41%,主要原因是省食品检验所、省医疗器械检验所和包材检测中心检验能力提升,事业收入较上年有一定增幅。
4.经营收入 0.00万元,与上年决算数持平。
5.其他收入 526.01万元,比上年决算数增加42.44万元,增长8.78%,主要原因:一是部分直属单位承担的课题项目经费较上年增加;二是部分直属单位银行存款利息较上年增加。
(二)年度支出总体情况广东省药品监督管理局2018年度总支出 100,683.30万元,其中本年支出 75,785.28万元。
具体情况如下:1.基本支出 32386.23万元,比上年决算数增加5,143.15万元,增长18.88%,主要原因是2018年按照统一的人员工资政策,人员经费较上年增加。
2.项目支出 43,399.05万元,比上年决算数减少7,278.53万元,下降14.36%,主要原因:一是因“数字政府”改革,智慧食药监信息化项目暂缓建设,省局本级项目支出较上年减少;二是省药品检验所因迁建项目接近尾声,仅剩部分尾款支付,与去年实施阶段相比项目开支大幅下降;三是根据国家停征收费有关规定,医疗器械检验涉非税收入经费较上年下降,相应的项目支出较上年减少。
3.上缴上级支出 0.00万元,与上年决算数持平。
4.经营支出 0.00万元,与上年决算数持平。
5.对附属单位补助支出 0.00万元,与上年决算数持平。
二、 2018年度财政拨款收入支出总表说明(一) 2018年度财政拨款收入说明广东省药品监督管理局2018年度财政拨款收入合计61,670.19万元。
其中:一般公共预算财政拨款收入 61,670.19万元,比上年决算数增加5,268.21万元,增长9.34%,主要原因是2018年按照统一的人员工资政策,人员经费较上年增加。
;政府性基金预算财政拨款收入 0.00万元,比上年决算数增加0万元,与上年决算数持平。
(二) 2018年度财政拨款支出说明广东省药品监督管理局2018年度财政拨款支出合计59,283.14万元。
其中:一般公共预算财政拨款支出 59,283.14万元,比年初预算数增加6,281.84万元,增长11.85%,主要原因:一是国家局年中下达了公共卫生服务补助资金,支出随之增加;二是财政部门按照人员工资政策统一追加的人员经费,支出随之增加;政府性基金预算财政拨款支出 0.00万元,比年初预算数增加0万元,与年初预算数持平。
三、 2018年度财政拨款“三公”经费支出决算情况说明(一)“三公”经费财政拨款支出决算总体情况说明广东省药品监督管理局2018年度“三公”经费财政拨款支出决算为 91.17万元,完成预算 223.26万元的 40.84%。
其中:因公出国(境)费支出决算为 5.62万元,完成预算 16.76万元的 33.56%;公务用车购置及运行费支出决算为 72.43万元,完成预算 154.60万元的 46.85%;公务接待费支出决算为 13.13万元,完成预算 51.90万元的 25.29%。
2018年度“三公”经费支出决算小于预算数的主要情况:一是因工作任务调整,部分出国团组取消;二是因省级机构改革,收缩出境参加会议人数,暂停公务用车购置,外省兄弟单位来粤学习交流减少,对应的“三公”经费支出较预算少。
(二)“三公”经费财政拨款支出决算具体情况说明2018年“三公”经费财政拨款支出决算中,因公出国(境)费 5.62万元,占 6.17%;公务用车购置及运行费支出 72.43万元,占79.44%;公务接待费支出 13.13万元,占14.40%。
具体情况如下:1.因公出国(境)费支出 5.62万元。
全年使用财政拨款安排局机关及下属1个单位出国团组 7个、累计 13人次。
开支内容包括:(1)参加会议支出5.54万元,主要用于参加国际标准化组织的ISO/TC 106国际年会、2018年抗菌素耐药性区域研讨会、第四届传统中医药国际合作论坛、粤港澳三地食品专家讲座、香港GMP研讨会、粤澳合作中医药科技产业园合作推荐会等;(2)签证费0.08万,主要用于抽调参加国家药品监管局境外检查人员的签证费。
2.公务用车购置及运行维护费支出 72.43万元,其中:公务用车购置支出为 0.00万元, 2018年公务用车购置数 0辆。
公务用车运行及维护支出 72.43万元, 2018年局机关及下属8个单位公务用车保有量为 20辆,主要用于省局机关和下属单位机要文件交换、开展食品药品行政执法监督检(核)查、食品药品抽样检验等工作所需燃料费、维修费、过桥过路费、保险费等。
3.公务接待费支出 13.13万元,主要用于国内来访团组接待支出。
2018年,局机关及下属8个单位共接待国外来访团组0个,来访外宾 0人次;发生国内接待 119次,接待人数共 1059人,省局机关及下属单位与省(内)外单位开展食品药品监管工作交流及接受相关部门检查指导工作等发生的接待支出。
