外消旋体拆分的方法共15页
外消旋体

5: 色谱分离 用非对称的淀粉,乳糖粉等作柱色层的吸附剂,
选择性地吸附一种异构体.
6: 优先富集法 (新)
参考文献: [3] R.Temura etal chirality. 1997,9:220
OH NO2- -SO3Me3N NH- -O OEt
O
抗过敏药
混合晶体优先析出, 与优先结晶法相反.
差异而分离,常用于酸或碱的外消旋体分离.
例 : 分离(+)-酸 (-)-碱
(+)-酸 (-)-碱 非对映
(天然生物碱) (-)-酸 (-)-碱 体的盐
重结晶等法 分步结晶分离 强酸HCl (+)-酸 + (-)-碱 HCl 分解盐 (-)-酸 + (-)-碱 HCl
见参考文献 [2] (化学拆分法)
水解
C C RM
O RL
OH CH3 C COOH
COOH CH3 ROH
得 R构型 α -苯基乳 酸占优势
A 为 (-)-薄荷醇时反应为:
O
H Rs RM
C C O RL
O
CH(CH3)2
①CH3MgI CH3 ②H2O/OH-
③H2O/H+
OH CH3
C
+
COOH
R-(-)-α 苯基乳酸
CH3 OH C COOH
参考文献 [2] 顾可权,周新琢.<应用化学>,1989,6(4):20
=
H
(+) 反式
H
COOH
(+)(+)A +
(-)(-) A
(-) NH3 15%甲醇,异丙 醚
回流 2h
(+)(+) A (-) NR3 母液 H+ (-)HA (+)NR3
外消旋体拆分方法

外消旋体的性质
总结词
外消旋体具有旋光性,但整体呈中性。
详细描述
由于外消旋体由左旋和右旋对映体混合而成,因此它具有旋光性。然而,由于 左旋和右旋成分相互抵消,外消旋体的整体性质呈中性。
06 外消旋体拆分方法的比较 与选择
各种方法的优缺点比较
化学拆分法
优点是分离效果好,适用于大多数外消 旋体;缺点是需要使用化学试剂,可能
对环境造成污染。
生物拆分法
优点是环保无污染,选择性高;缺点 是分离周期较长,需要特定的生物资
源和培养条件。
物理拆分法
优点是环保无污染,操作简便;缺点 是分离效果相对较差,需要较高的技 术和设备支持。
详细描述
重结晶拆分法是一种常用的外消旋体拆分方法。它是利用外消旋体与纯的左旋或右旋体 在溶剂中的溶解度不同,通过多次重结晶过程将它们分离。在重结晶过程中,外消旋体 与纯的左旋或右旋体的溶解度差异逐渐增大,从而实现分离。该方法需要选择合适的溶
剂和结晶条件,以确保拆分的效率和纯度。
热拆分法
要点一
总结词
植物提取法
利用植物中存在的对映异构体选 择性吸收和代谢,通过植物提取 实现外消旋体的拆分。
动物选择性吸收法
利用动物体内对不同对映异构体 的选择性吸收和代谢,通过动物 实验实现外消旋体的拆分。
物理拆分法
溶解度差异法
利用不同对映异构体在溶剂中的溶解 度差异,通过选择性溶解实现外消旋 体的拆分。
蒸馏法
色谱法
利用外消旋体与纯的左旋或右旋体在加热过程中的稳定性 差异进行分离。
要点二
外消旋体的拆分

外消旋体的拆分021131090 王新珏Louispasteur在100多年前曾指出:“宇宙是非对称的,如果把构成太阳系的全部物体置于一面跟随着它们的各种运动而移动的镜子前面,镜子中的影像不能和实体重合。
……”生命由非对称作用所主宰。
在自然界中存在许多光学对映体,这些物质就像人的左右手,立体结构对称,左右相反,绝不能重合,故称为手性化合物。
在漫长的化学演化过程中,地球上出现了无数手性化合物构成生命体的有机分子,无论在种类上或在数量上,绝大多数是手性分子。
手性分子的对映体可以有几乎完全相同的物理化学性质,甚至有相同的光谱,但是它们之间仍然存在有重要的差别——手性分子间反应性的差别。
其气味、味道以及作用大相径庭:一方有益,而另一方就有害。
因此寻求和研究外消旋体拆分方法,与有利于对映体之一的合成方法,特别是得到所需要的纯粹单一对映体的化学合成方法不对称合成成为当前有机化学研究的热点与前沿。
手性物质我们周围的世界是手性的,构成生命体系的生物大分子的大多数重要的构件仅以一种对映形态存在。
生命体系有极强的手性识别能力,不同构型的立体异构体往往表现出极不相同的生理效能。
药物分子的两个对映体以不同的方式参与作用并导致不同的效果。
生物体的酶和细胞表面受体是手性的,外消旋药物的两个对映体在体内以不同的途径被吸收,活化或降解。
这两种对映体可能有相等的药理活性;或者一种可能是活性的,另一种可能是无活性的甚至有毒的,或者二者可能有不同程度或不同种类的活性。
例1.氯霉素,其中的D-对映体具有杀菌作用,而L-对映体却完全没有药效。
例2.有时一对对映体在体内可能具有相反的作用,这可以用在20世纪60年代发生在欧洲的一个悲剧来说明外消旋的反应:反应停(Thalidomide)曾是镇静剂和止吐药,用作减轻孕妇早期妊娠反应的药物,后来才发现有些曾服用过这种药的孕妇产下了畸形婴儿,进一步的研究表明,其致畸形是由该药的(S)-异构体所引起的,而(R)-异构体被认为即使在高剂量时在动物中也不引起畸变。
实验二十三外消旋α-苯乙胺的合成和拆分

实验二十三外消旋α-苯乙胺的合成和拆分实验二十三外消旋α-苯乙胺的合成和拆分一、实验目的1、学习外消旋α-苯乙胺的合成方法。
2、掌握外消旋体的拆分的基本原理和方法、学习旋光度的测定方法 3二、基本原理在非手性条件下,由一般合成反应所得的手性化合物为等量的对映体组成的外消旋体,故无旋光性。
利用拆分的方法,把外消旋体的一对对映体分成纯净的左旋体和右旋体,即所谓的消旋体的拆分。
拆分外消旋体最常用的方法是利用化学反应把对映体变为非对映体。
如果手性化合物分子中含有一个易于反应的极性基团,如羧基,氨基等,就可以使它与一个纯的旋光化合物(拆解剂)反应,从而把一对对映体变成两种非对映体。
由于非对映体具有不同的物理性质,如溶解性,结晶性等,利用结晶等方法将他们分离、精制,然后再去掉拆解剂,就可以得到纯的旋光化合物,达到拆分目的。
常用的拆解剂有马钱子碱、奎宁和麻黄素等旋光纯的生物碱(拆分外消旋的有机酸)以及酒石酸、樟脑磺酸等旋光纯的有机酸(拆分外消旋的有机碱)。
外消旋的醇通常先与丁二酸酐或邻苯二甲酸酐形成单酯,用旋光醇的碱把酸拆分,再经碱性水解得到单个的旋光性的醇。
对映体的完全分离当然是最理想的,但是实际工作中很难做到这一点,常用光学纯度表示被拆分后对映体的纯净程度,它等于样品的比旋光除以纯对映体的比旋光。
光学纯度(op)=样品的[a]/纯物质的[a]*100%。
本实验用(+)-酒石酸为拆解剂,它与外消旋α-苯乙胺形成非对映异构体的盐。
旋光纯的酒石酸在自然界颇为丰富,它是酿酒过程中的副产物。
由于(-)-胺(+)-酸非对映体的盐比另一种非对映体的盐在甲醇中的溶解度小,故易从溶液中呈结晶析出,经稀碱处理,使(-)-α-苯乙胺游离出来。
母液中含有(+)-胺(+)-酸盐,原则上经提纯后可以得到另一个非对映体的盐,经稀碱处理后得到(+)-胺。
本实验只分离对映异构体之一,即左旋异构体,因右旋异构体的分离对学生来说显得困难。
本实验用(+)-酒石酸为拆解剂,它与外消旋α-苯乙胺形成非对映异构体的盐。
第七章-化学手性制药工艺 第二节 外消旋体拆分

二、化学拆分法
外消旋底物 拆分试剂
非对映异构体 混合物
单一对映异 构体底物
水解
化学拆分
(结晶或柱层析)
单一非对映 异构体
7
二、化学拆分法
★ 常用拆分试剂:
1)能分别与对映异构体反应,所生成的非对映异构体 有显著的物理性质差异;
2)所用拆分试剂自身具有足够高的光学纯度; 3)所用拆分试剂成本较低,便于回收。
4
一、结晶拆分法 ✓ 优点:不需要加入拆分试剂,母液可以套用
多次,原料损耗小、设备简单,成本较低, 是比较理想的大规模拆分方法。 ✓ 缺点:必须采用间断式结晶,生产周期长, 拆分所得光学异构体的纯度不够高而需进一 步纯化。
5
★ 注意: 所拆分的外消旋体属于外消旋混合物,而
非外消旋化合物。
➢ 外消旋混合物:是等量的两种对映异构体晶体的机 械混合物,虽然该混合物没有光学活性,但每个晶核 仅包含一种对映异构体; ➢ 外消旋化合物:晶体是两种对映异构体分子完美有 序的排列,每个晶核包含等量的两种对映异构体。
外消旋体 酸 碱 醇
醛、酮
光学拆分剂 麻黄碱、奎宁、α-苯乙胺等 酒石酸、扁桃酸、樟脑等 转化为酸性酯后,用活性碱拆分
光学活性的肼、酰肼等
8
例如:度洛西汀合成中的化学拆分
9
★ 不对称转换法制备D-脯氨酸:
10
三、动力学拆分法 利用两个对映异构体在手性试剂或性催
化剂作用下反应速率的不同而使其分离。 ➢ 过程简单,生产效率高; ➢ 可以通过调整转化程度提高剩余底物的对映 体过量。
第七章 化学手性制药工艺
第一节 概述 第二节 外消旋体拆分 第三节 不对称合成反应
1
推荐阅读: 《手性药物质量控制研究技术指导原则》
有机化学上第六章-立体化学

第三十四页,共63页。
注意
• 外消旋体与内消旋体都没有旋光性,但 它们有本质的不同:
• 外消旋体是等量左旋体和右旋体的混合 物,可拆分;
• 内消旋体是分子内有对称面的单一化合 物,不可拆分。
第三十五页,共63页。
(六) 手性中心的产生
• 〔2〕判断分子中有无对称面和对称中心 在立体化学中有重要意义。
第九页,共63页。
(三) 手性分子的性质——光学活性
光学活性:手性分子可以使平面偏振光发生偏转的性质〔旋光性〕
(1) 偏振光
• 光是一种电磁波,光波的振动方向与其前进方向垂直。
• 普通光在所有垂直于其前进方向的平面上振动。
• 偏振光——只在一个平面上振动。
手性中心的产生与手性合成有密切关系。
(1) 第一个手性中心的产生 (自学)
产 生 第 一 手 性 碳
CH3CH2CH2CH3 Cl2
CH3*CHCH2CH3 +其 他 产 物 Cl
前 手 性 碳
外 消 旋 体
当产生第一个手性中心时,两个氢原子被取代的概率
均等,生成的对映体的量相等,产物没有旋光性,是一 个外消旋体。即从非手性反响物合成手性产物时常得到 外消旋体。
HO CH3 赤式
前后
H
H3C
Cl
HO
CH3
H
赤式 前后
前后碳旋转方向不同
前后碳旋转方向相同
“苏式〞、“赤式〞的概念在研究有机反响的立体化 学关系和反响机理时常会遇到。
第三十三页,共63页。
(2) 具有两个相同手性碳原子的对映异构
酒石酸分子中含有2个*C,可能的异构体有:
西他列汀外消旋体的合成及拆分

西他列汀外消旋体的合成及拆分叶飞;高仁孝;沈宁;丁志新【摘要】以2-氯吡嗪与2,4,5-三氟苯乙酸为原料,经亲核取代、环化、氢化等6步反应合成了制备西他列汀的重要中间体--4-氧代-4-{3-(三氟甲基)-5,6-二氢-[1,2,4]三唑并[4,3-a]哌嗪-7(8H)-基}-1-(2,4,5-三氟苯基)丁烷-2-烯胺(6);以NaBH4为还原剂,甲基磺酸为辅助添加剂,还原6制得西他列汀外消旋体(7); 7经(-)-二对甲苯酰-L-酒石酸拆分制得光学纯度高于93%的西他列汀,其结构经1H NMR, IR和MS 表征.【期刊名称】《合成化学》【年(卷),期】2010(018)006【总页数】4页(P767-770)【关键词】西他列汀;化学拆分;(-)-二对甲苯酰-L-酒石酸;合成【作者】叶飞;高仁孝;沈宁;丁志新【作者单位】西安建筑科技大学,理学院,化学系,陕西,西安,710055;西安建筑科技大学,理学院,化学系,陕西,西安,710055;西安瑞联近代电子材料有限责任公司,陕西,西安,710077;西安瑞联近代电子材料有限责任公司,陕西,西安,710077;西安瑞联近代电子材料有限责任公司,陕西,西安,710077【正文语种】中文【中图分类】O626.26;R914.5西他列汀{8,化学名7-[(3R)-3-氨基-1-氧-4-(2,4,5-三氟苯基)丁基]-3-三氟甲基-5,6,7,8-四氢[1,2,4]三唑并[4,3-a]哌嗪磷酸水合物}是默克公司研发并于2006年经美国食品药品管理局批准,用于治疗Ⅱ型糖尿病的首个DDP-Ⅳ抑制剂,其商品名为Januvia。
8主要通过保护胰高血糖素样肽-1(GLP-1)和肠抑胃肽(GIP)以达到治疗糖尿病的目的[1]。
Scott等[2]的研究显示,8具有良好的耐药性和安全性。
8的合成方法较多,工业上主要采用默克公司[3~6]的最新方法:以[(COD)RhCl]2和Josiphos SL-J002-1为手性催化剂不对称氢化烯胺(氢化转化率82%~89%, ee 值89%~95%);再与磷酸生成8的磷酸盐。
立体化学-外消旋体的拆分

这种 别,达 选择 应, 关系。 来 光学 光学 动 学 应 。 , 对光 产源自应 对备, 来
7
(3)晶种结晶法
在少数情况下,可能是受外界现尚不清楚的某 种手性因素的影响,一对对映体中有一光活异构 体会少量的先结晶出来,发生了晶种的作用,同 时另一个过剩的对映体又转变为等量的(+)和 时另一个过剩的对映体又转变为等量的(+)和(-) 的消旋体而达到平衡,并且转变的速率比结晶的 速率更快一些,因此理论上讲,由一对对映体可 以转变为一个纯的光活体。
如外消旋化合物既不是酸也不是碱,可以将 化合物接上一个羧基然后再进行拆分,如一个外 消旋醇与邻苯二甲酸酐反应,得到外消旋酸,再 用光活性的拆分剂——碱处理,形成非对映体再 用光活性的拆分剂——碱处理,形成非对映体再 进行分离。
(2)酶解法
有时用酶解的方法,可以将外消旋体分开,酶对底物具有 非常严格的空间选择反应性能。例如合成的DL— 非常严格的空间选择反应性能。例如合成的DL—丙氨酸经乙 酰化后,通过由猪肾内取得的一个酶,水解L 酰化后,通过由猪肾内取得的一个酶,水解L型丙氨酸的乙酰 化物的速率要比D型的快得多。因此就可以把Dl— 化物的速率要比D型的快得多。因此就可以把Dl—乙酰化物变 为L—(+)—丙氨酸和D—(-)—乙酰丙氨酸,由于这二者在乙 (+)—丙氨酸和D 醇中的溶解度区别很大,可以很容易地分开。这一系列的关 系可用下式表示:
外消旋体的拆分
LOGO
简介及意义
简介:外消旋体是由一对对映体等量混合而成, 简介:外消旋体是由一对对映体等量混合而成,对映体 除旋光方向外,其它物理性质均相同。 除旋光方向外,其它物理性质均相同。用一般的物理方 蒸馏、分馏、结晶等)不能把一对对映体分离开来。 法(蒸馏、分馏、结晶等)不能把一对对映体分离开来。 必须用特殊方法。 必须用特殊方法。 外消旋体的拆分: 外消旋体的拆分:将外消旋体分离成旋光体的过程叫 拆分” “拆分”。 意义:根据药物的不同,有些药物是其多个对映体之一, 意义:根据药物的不同,有些药物是其多个对映体之一, 而有些药物则为外消旋体。 而有些药物则为外消旋体。事前必须就药物对映体的药 理学效果作验证,以减少危险发生。 理学效果作验证,以减少危险发生。
外消旋化合物的分离
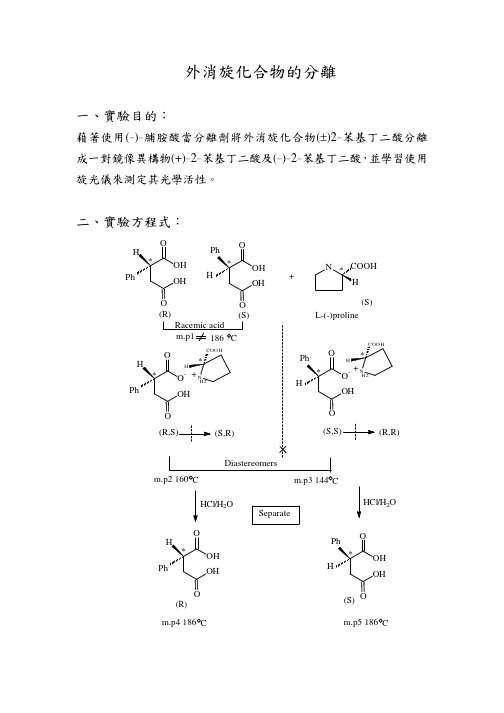
外消旋化合物的分離一、實驗目的:藉著使用(-)-脯胺酸當分離劑將外消旋化合物(±)2-苯基丁二酸分離成一對鏡像異構物(+)-2-苯基丁二酸及(-)-2-苯基丁二酸,並學習使用旋光儀來測定其光學活性。
二、實驗方程式:H HH H +(R)HCl/H 2O HCl/H 2O SeparateH HH H(S)(R)m.p2 160Cm.p3 144 m.p4 186m.p5 186(S)H(R,R)三、實驗原理:1、異構物的分類:1異構物(isomer ):具相同分子式的不同化合物,可區分為結構異構物及立體異構物。
2結構異構物(constitution isomers ):原子以不同之次序連接而成不3立體異構物(stereoisomers ):分子內的組成各原子以相同的次序連接,但其原子在空間中排列不相同。
立體異構物又可區分為對掌異構物及非對映異構物。
順-2-丁烯 反-2-丁烯4對掌異構物(enantiomers ):分子間互成鏡像的立體異構物。
對掌HCH 3H CH C CH CH CH 3異構物只發生在分子有對掌性(chiral )的化合物。
對掌性分子之定義為:互為鏡像且不能重疊之化合物,例如我們的左右手互為鏡像,但卻無法重疊。
一個碳原子連結四個不同取代基時,此碳原子是為”對掌中心”(掌性碳),然而幾乎所有的對掌異構物都含有對掌中心,相同的,含有對掌中心的分子大都為對掌異構物。
下圖中心碳為掌性碳,且互為對掌異構物(兩者無法重疊)。
5非對映異構物(diastereomers):分子間彼此不成鏡像的立體異構物。
2、對掌異構物的性質:具有相同的熔點、沸點、折射率、溶解度甚至連密度也相同。
一種容易觀察對掌異構物的方法是他們對平面偏極光偏轉方向之不同,當平面偏極光通過等量的R 型及S 型對掌異構物時,偏轉的角度相同但方向卻完全相反。
能使平面偏極光偏極面轉動者又稱為光學活性化合物。
1R 型及S 型:依照順序規則將鍵結在掌性碳上之四個原子基團大小排列,將最小的基團遠離我們,再觀察其餘3個基團,若以順時鐘排列則為R 型;若以逆時鐘排列則為S 型。
