青蒿素类药物的药理和毒理_综述_
2012执业西药师药理学辅导:青蒿素药物简介

【性状】为无色针状结晶,味苦。
在丙酮、醋酸乙酯、氯仿、苯或冰醋酸中易溶,在甲醇、乙醇、稀乙醇、乙醚及石油醚中溶解,在水中几乎不溶。
熔点150~153℃。
【药理及应用】为一种高效、速效的抗疟药,主要作用于疟原虫的红内期,用于间日疟,恶性疟特别是抢救脑型疟有良效,其退热时间及疟原虫转阴时间都较氯喹短,对氯喹有抗药性的疟原虫,使用本品亦有效。
但对间日疟原虫的近期复燃率比氯喹高20%~30%。
与伯氨喹合并应用,可使复燃率降至10%左右。
本品对血吸虫亦有杀灭作用。
【用法】
(1)直肠给药:1次0.4~0.6g,1日0.8~1.2g。
(2)深部肌注:第1次200mg,6~8小时后再给100mg,第2,3日各肌注100mg,总剂量500mg(个别重症第4天再给100mg)。
或连用3日,每日肌注300mg,总量900mg.小儿15mg /kg,按上述方法3日内注完。
(3)口服:先服1g,6~8小时再服0.5g,第2,3日各服0.5g,疗程3日,总量为2.5g.小儿15mg/kg,按上述方法3日内服完。
青蒿素类药物的药理和毒理学研究

青蒿素类药物的药理和毒理学研究前言青蒿素是一种用于治疗疟疾的天然药物。
它的发现被认为是现代中药学中最重要的突破之一。
在青蒿素的发现和广泛使用之后,科学家们开始深入研究这种药物的药理和毒理学特性。
青蒿素类药物已被证明是治疗疟疾的最有效药物之一,但它们的作用机制和相应的毒性仍有争议。
在本文中,我们将讨论青蒿素类药物的药理和毒理学特性。
青蒿素类药物的药理学研究作用机制青蒿素是一种强有效的抗疟药物,它的作用机制一直被广泛研究。
以下是青蒿素的作用机制:1.破坏疟原虫细胞膜青蒿素可以使疟原虫细胞膜高度活性,并形成过氧化物,导致疟原虫死亡。
2.抑制疟原虫生物合成青蒿素可以抑制疟原虫的DNA合成和蛋白质合成等过程,从而杀死疟原虫。
3.抵消疟原虫毒素青蒿素可以在治疗疟疾时中和疟原虫毒素,从而防止疟疾的恶化。
青蒿素类药物的药代动力学药代动力学研究了药物在人体内的吸收、分布、代谢和排泄的过程。
青蒿素类药物在体内的吸收和代谢速率与其他药物相比较是快速的。
青蒿素经过口服或静脉注射后,肝脏是主要的代谢器官,青蒿素代谢产物的半衰期约为1.3小时。
青蒿素通过胆汁排泄,在48小时内约60%的药物从体内自然排出。
青蒿素类药物的毒理学研究青蒿素类药物的毒性与它们的药理学作用及其剂量密切相关。
虽然青蒿素类药物广泛应用于临床治疗,但在某些情况下青蒿素类药物的毒性可能会引起轻微或严重的副作用。
常见的副作用1.胃肠反应青蒿素类药物可能导致恶心、呕吐、胃肠不适和腹泻等副作用,其中以腹泻最为常见。
这些副作用通常是轻微的,并随药物停止或减少剂量后迅速消失。
2.中枢神经反应青蒿素类药物可能引起头痛、头晕、失眠和焦虑等中枢神经反应。
这些反应可能与药物剂量有关,并随着药物停止或减少剂量而消失。
3.血液学反应在极少数情况下,青蒿素类药物可能导致脾肿大、贫血、血小板减少和白细胞减少等血液学反应。
这些反应比较严重并数量较少,随着药物停止或减少剂量后也可能迅速消失。
青蒿素综述

青蒿素综述刘兵情(井冈山大学11级药本(1)班学号:111116023)摘要:青蒿素类抗疟药物的发现是全球抗疟药物发展史上继奎宁之后的又一里程碑[1], 是目前治疗疟疾的特效药.本文简要介绍青蒿素的发现过程、药源、生物合成、应用前景和青蒿素及其衍生物药理活性,重点在于介绍青蒿素生物合成过程。
关键词:青蒿素发现过程药源生物合成药理活性前景引言:青蒿素是在科研计划组织下,全国多部门、多学科专家尽心协作、相互配合取得的重大成果,是继承发扬我国传统医药宝库的成功范例[2]。
青蒿素主要有抗疟、抗孕、抗纤维化、抗吸血虫等药理作用[3]。
青蒿素生物合成三个阶段分为从乙酰辅酶A 到法呢基焦磷酸的“上游”途径、从法呢基焦磷酸到双氢青蒿酸的“中游”途径和从双氢青蒿酸到青蒿素的“下游”途径,其中上游途径青蒿及其他高等植物与酵母等真核微生物完全相同,因而只需在酵母中额外增加一个青蒿素合成代谢支路, 就能让酵母全合成青蒿素。
而中游的酶促反应在酵母中已经完全建立,下游途径的反应条件在酵母中则未建立[4]。
而且青蒿素及其衍生物在抗肿瘤和葡萄膜炎免疫治疗上也具有应用前景。
一.青蒿素药物来源1967 年北京《5·23 抗疟计划》付诸实施, 1969 年1 月北京中医研究院加入5·23 计划,任命屠呦呦为科研组组长, 在全国多个研究单位协作下, 组织植物化学与药理学等专业200 多人参加, 并与中医药工作者密切合作[5].从追索我国历代抗疟方剂入手, 科研组调查了 2 000 种中草药制剂, 从中选出可能具抗疟活性的达640 种. 余亚纲梳理开列了有808 个中药的单子,其中有乌头、乌梅、鳖甲、青蒿等[6]共用约200种国产草药制成380 多种抽提物, 再筛查它们对小鼠疟疾模型的疗效,但实验不易获得明显结果[7]军事医学科学院用鼠疟模型筛选了近百个药方,青蒿提取物的抑制率虽达60%~80%, 而效力不够稳定[6]继后, 研究组经余亚纲和顾国明复筛, 肯定了青蒿的抗疟作用[8]他们也研究了中药常山,其抗疟作用虽强, 但呕吐的副作用亦强而妨碍推广应用. 转折点出现在黄花蒿的抽提物. 传统中药青蒿包括两个品种: 学名黄花蒿(Artemisia an-nua L.)的抽提物能对小鼠疟原虫的生长显示良好的抑制作用;而学名青蒿(Artemisia apiaceaHance)则无任何抗疟作用[7][9],继后的实验中, 上述结果未能重复, 这同中医文献的记载相矛盾. 为解开此疑惑, 再深入查阅古代医学文献, 最后在晋朝葛洪著《肘后备急方》中找到“青蒿一握, 以水二升渍, 绞取汁, 尽服之”的抗疟记录. 惯常煎熬中药的高温抽提法已破坏了抗疟的活性组分;温度高于60 ℃将使青蒿素完全分解. 在较低温度下进行青蒿抽提后, 获得了很满意的效果[7][9][10],.研究组将青蒿的抽提物分成酸性与中性物部分. 移除了不具抗疟活性且有害的酸性部分, 重点抽提黄花蒿的叶片, 使有效成分的产量提高, 并能大幅度地降低其毒性[6],1971年下半年, 于190次实验失败后, 他们在60 ℃用乙醚萃取, 制成了一种无毒性的第191 号中性抽提物[7].它对感染伯氏疟原虫(Plasmodium berghei) 小鼠以及感染猴疟原虫(Plasmodium cyomolgi) 猴的疟原虫血症(parasitemia) 显示100%的疗效. 此喜讯宣告了青蒿素课题的新突破. 研究组将191 号中性抽提物最先在全体组员身上试服, 确定了其安全性.1972 年 3 月, 向“5·23 计划”南京会议报告了试服的结果. 会后不久, 研究组即远赴海南省安排临床试验. 在选试的21 例疟疾患者中, 感染恶性疟或间日疟(subtertian or tertian malaria)者各占半数. 经治疗后, 患者的发热症状可迅速消失, 血中疟原虫的数目锐减;而接受氯喹的对照组患者则无效.受到临床试验疗效的鼓舞, 研究组再回头专攻青蒿素活性组分的分离与纯化. 钟裕容等通过抽提物的层析, 1972 年11 月8 日成功分离出一种相对分子质量0.282 kD的无色结晶, 测得其分子式为C15H22O5, 熔点156~157 ℃, 即“青蒿素Ⅱ”,后命名为青蒿素(artemisinin).1972 年在得知北京科研组有关青蒿粗提物的信息后, 山东寄生虫病研究所与山东省中医药研究所合作, 还有云南省药物研究所分别独立进行黄花蒿的提取, 亦获得有效抗疟单体, 各自命名为“黄花蒿素”(山东)及“黄蒿素”(云南). 1974 年初, 上述两种单体被初步确证与北京的青蒿素属相同的药物[6]。
近年来对青蒿素的研究

中药青蒿近年来的研究(综述)摘要:青蒿素的发现被国际上誉为“20世纪后半叶最伟大的医学创举”,青蒿素被世界卫生组织称为“是世界上唯一有效的疟疾治疗药物”。
近年来中外对青蒿素及其衍生物的研究越来越热,从其分子结构研究到它的生理生化特征及它的应用等等。
国内外已有千余篇论文报道该类化合物的化学,药学,药理和临床的研究结果。
本文汇总近年来青蒿素类药物的研究进展。
关键词:青蒿素衍生物研究作用青蒿素。
青蒿是一种菊科植物,长久以来以其退烧的能力而闻名。
因为现阶段疟疾寄生虫对大多数抗疟疾药物都产生了抵抗力,青蒿素以及青蒿的其他几种衍生物最近很受欢迎,如青蒿琥酯,蒿甲醚,双氢青蒿素等等。
青蒿药物,是抗击疟疾的关键,青蒿类药物是中国人自主研发的拥有自主知识产权的化学药,其原料是我国西南山区的青蒿草中提取的青蒿素,我国研发的青蒿类药物在治疗疟疾等疾病中效果显著,当前已经成为国际抗疟疾首选药。
而且青蒿素及其衍生物的抗肿瘤作用也受到广泛关注,美国国家癌症研究所(NCI)已将其纳入抗癌药物筛选与抗癌活性研究计划。
中医中青蒿的功效及作用:功效:清热解暑、退虚热、宣化湿热。
作用:临床常用于暑热外感、发热无汗或温热病发热恶寒等证,还可用于治疗疟疾。
因青蒿能退虚热,故还可用于阴虚发热或原因不明的低热。
临床常用的蒿芩清胆汤、青蒿鳖甲汤、清骨散都是以青蒿为主药而制成的。
其主治阴虚潮热骨蒸,外感温热暑湿,头目昏晕,疟疾,黄疸,泻痢,疥癣,皮肤瘙痒。
近年来青蒿的研究1.青蒿资源的研究(包括野生、引种、杂交培育以及生物合成青蒿素)(1)青蒿野生植物资源:据相关人士对黄花蒿的青蒿素含量与气候、土壤诸生态因子的相关性进行的研究。
结果表明,华中地区中亚热带常绿阔叶林武陵山地区内的黄花蒿含量普遍较高,平均在4.847%。
~8.853%0之间,最高可达10.221‰。
(2)生物合成:据报道的生物合成青蒿素的研究:a.组织器官培养:通过愈伤组织和细胞培养;青蒿发根培养;青蒿芽培养,结果发现青蒿发根及转基因丛生芽培养有较好的前景。
有关青蒿素近年研究综述

有关青蒿素近年研究综述【摘要】:青蒿素是目前我国唯一的得到国际承认的具有自主知识产权的抗疟新药。
因此在我国的研究领域占有很特别的地位。
近些年,随着青蒿素的发现,国内外的各个研究组织分别对其及其衍生物,在不同的方面进行了很多的研究与实验。
本文便是对有关青蒿素的分离提取,合成制备,作用用途等方面的研究作简要说明。
【关键词】:青蒿素,提取,制备。
【正文】青蒿素是目前我国唯一的得到国际承认的具有自主知识产权的抗疟新药。
因此在我国的研究领域占有很特别的地位。
青蒿入药最先现于马王堆三号汉墓出土的帛书《五十二方书》上,大约是在公元前168年左右。
后发现在《神农本草经》、《大观本草》、《本草纲目》等均有记录。
青蒿素最先是于1972年在研究青蒿治疗疟疾等病特性时从青蒿中分离出来的活性物资。
近些年,随着青蒿素的发现,国内外的各个研究组织分别对其及其衍生物,在不同的方面进行了很多的研究与实验。
现便对有关青蒿素的分离提取,合成制备,作用用途等方面的研究作简要说明。
1、青蒿素的理化性质简要介绍青蒿素的分子式是C5H22O5,有7个手性中心,分子量为282.34,化学名称为(3R,5As,6R,8As,9R,12S,12aS)八氢-3,6,9-三甲基-3,12-桥氧-12H-吡喃{4,3-J}-1,2-苯并二塞平-10-酮。
它是一种无色针状晶体,熔点为156~157`C。
它是一种含有过氧基的新型倍半菇内酯。
所以由于其具有特殊的过氧基团,其对热不稳定,易受湿、热和还原性物质的影响而分解。
它易溶于氯仿、丙酮、乙酸乙酯和苯,可溶于乙醇和乙醚,微溶于冷石油醚,几乎不溶于水。
2、青蒿素的分离提取与合成制备目前,随着研究的深入,从各个方面萌生出了各种制备青蒿素的方法,以下简要介绍一下获得青蒿素的传统与新型方法。
2.1分离提取方法2.2.1传统提取方法所谓提取对象主要是针对天然药用成分比如青蒿等植物。
一般是用试剂以浸渍,渗滤,煎煮等方法对天然药物的化学成分进行抽提。
青蒿素的药理作用

青蒿素的药理作用【摘要】青蒿素是从植物黄花蒿中提取的抗疟疾的活性成份,目前在临床上广泛用于治疗疟疾。
近些年研究发现青蒿素不仅可以抗寄生虫,包括疟原虫、血吸虫,而且具有显著的抗炎、调节免疫和抗肿瘤等多方面的药理作用。
本文在介绍青蒿素抗疟疾作用、应用和作用机制的基础上,对近年来青蒿素类药物的其它主要生物学作用研究的现状进行综述。
青蒿素的药理学研究1 抗疟疾作用1.1二价铁离子依赖的抗疟疾作用用与青蒿素的化学结构密切相关。
在疟原虫破坏红细胞并吞噬血红蛋白后,疟原虫体内的血红蛋白酶,主要是天冬氨酸蛋白酶、半胱氨酸蛋白酶将吸收的血红蛋白催化降解成游离氨基酸,同时释放出血红素和游离的二价铁离子;二价铁离子再催化青蒿素类物质中的过氧桥裂解,产生大量以青蒿素炭原子为中心的自由基和活性氧,它们将修饰或抑制疟原虫生长所需要的大分子物质或破坏疟原虫生物膜结构,最终导致疟原虫死亡。
1.2抑制血红素的内化氯喹对血红素具有较强的亲和力,它通过竞争性结合血红素从而拮抗青蒿素的抗疟作用,但青蒿素能抑制血红素的内化,从而阻断疟原虫对铁离子和蛋白质的利用。
1.3 与抗炎作用有关血红素是迄今所知生物体内最强的脂质过氧化反应的催化剂,具有刺激单核巨噬细胞释放炎症细胞因子的作用。
青蒿素可显著抑制诱导性合酶的合成、促炎细胞因子的释放,其作用可能与其抑制核转录因子的激活有关,因为已经证实多种倍半萜内酯化合物包括青蒿素类药物是NO合酶基因表达的强抑制剂,它们可通过烷化NF-kB 或阻断抑制性蛋白IkB的降解削弱NF-kB的活性。
2 抗肿瘤作用2.1 诱导肿瘤细胞凋亡青蒿素主要作用是诱导肿瘤细胞凋亡,而不是坏死,而且在铁转运蛋白的协助下,青蒿素的诱导凋亡作用更显著。
青蒿素衍生物青蒿琥酯不但能抑制人肝癌细胞H22和BEL-7402的增殖,而且能诱导肿瘤细胞凋亡。
2.2 二价铁离子介导的细胞毒作用示,青蒿素的抗肿瘤作用机制与其抗疟机制十分相似。
研究表明,二价铁和铁转运蛋白在红细胞和肿瘤细胞中的含量较正常细胞高。
青蒿素综述

青蒿素综述刘兵情(井冈山大学11级药本(1)班学号:111116023)摘要:青蒿素类抗疟药物的发现是全球抗疟药物发展史上继奎宁之后的又一里程碑[1], 是目前治疗疟疾的特效药.本文简要介绍青蒿素的发现过程、药源、生物合成、应用前景和青蒿素及其衍生物药理活性,重点在于介绍青蒿素生物合成过程。
关键词:青蒿素发现过程药源生物合成药理活性前景引言:青蒿素是在科研计划组织下,全国多部门、多学科专家尽心协作、相互配合取得的重大成果,是继承发扬我国传统医药宝库的成功范例[2]。
青蒿素主要有抗疟、抗孕、抗纤维化、抗吸血虫等药理作用[3]。
青蒿素生物合成三个阶段分为从乙酰辅酶A 到法呢基焦磷酸的“上游”途径、从法呢基焦磷酸到双氢青蒿酸的“中游”途径和从双氢青蒿酸到青蒿素的“下游”途径,其中上游途径青蒿及其他高等植物与酵母等真核微生物完全相同,因而只需在酵母中额外增加一个青蒿素合成代谢支路, 就能让酵母全合成青蒿素。
而中游的酶促反应在酵母中已经完全建立,下游途径的反应条件在酵母中则未建立[4]。
而且青蒿素及其衍生物在抗肿瘤和葡萄膜炎免疫治疗上也具有应用前景。
一.青蒿素药物来源1967 年北京《5·23 抗疟计划》付诸实施, 1969 年1 月北京中医研究院加入5·23 计划,任命屠呦呦为科研组组长, 在全国多个研究单位协作下, 组织植物化学与药理学等专业200 多人参加, 并与中医药工作者密切合作[5].从追索我国历代抗疟方剂入手, 科研组调查了 2 000 种中草药制剂, 从中选出可能具抗疟活性的达640 种. 余亚纲梳理开列了有808 个中药的单子,其中有乌头、乌梅、鳖甲、青蒿等[6]共用约200种国产草药制成380 多种抽提物, 再筛查它们对小鼠疟疾模型的疗效,但实验不易获得明显结果[7]军事医学科学院用鼠疟模型筛选了近百个药方,青蒿提取物的抑制率虽达60%~80%, 而效力不够稳定[6]继后, 研究组经余亚纲和顾国明复筛, 肯定了青蒿的抗疟作用[8]他们也研究了中药常山,其抗疟作用虽强, 但呕吐的副作用亦强而妨碍推广应用. 转折点出现在黄花蒿的抽提物. 传统中药青蒿包括两个品种: 学名黄花蒿(Artemisia an-nua L.)的抽提物能对小鼠疟原虫的生长显示良好的抑制作用;而学名青蒿(Artemisia apiaceaHance)则无任何抗疟作用[7][9],继后的实验中, 上述结果未能重复, 这同中医文献的记载相矛盾. 为解开此疑惑, 再深入查阅古代医学文献, 最后在晋朝葛洪著《肘后备急方》中找到“青蒿一握, 以水二升渍, 绞取汁, 尽服之”的抗疟记录. 惯常煎熬中药的高温抽提法已破坏了抗疟的活性组分;温度高于60 ℃将使青蒿素完全分解. 在较低温度下进行青蒿抽提后, 获得了很满意的效果[7][9][10],.研究组将青蒿的抽提物分成酸性与中性物部分. 移除了不具抗疟活性且有害的酸性部分, 重点抽提黄花蒿的叶片, 使有效成分的产量提高, 并能大幅度地降低其毒性[6],1971年下半年, 于190次实验失败后, 他们在60 ℃用乙醚萃取, 制成了一种无毒性的第191 号中性抽提物[7].它对感染伯氏疟原虫(Plasmodium berghei) 小鼠以及感染猴疟原虫(Plasmodium cyomolgi) 猴的疟原虫血症(parasitemia) 显示100%的疗效. 此喜讯宣告了青蒿素课题的新突破. 研究组将191 号中性抽提物最先在全体组员身上试服, 确定了其安全性.1972 年 3 月, 向“5·23 计划”南京会议报告了试服的结果. 会后不久, 研究组即远赴海南省安排临床试验. 在选试的21 例疟疾患者中, 感染恶性疟或间日疟(subtertian or tertian malaria)者各占半数. 经治疗后, 患者的发热症状可迅速消失, 血中疟原虫的数目锐减;而接受氯喹的对照组患者则无效.受到临床试验疗效的鼓舞, 研究组再回头专攻青蒿素活性组分的分离与纯化. 钟裕容等通过抽提物的层析, 1972 年11 月8 日成功分离出一种相对分子质量0.282 kD的无色结晶, 测得其分子式为C15H22O5, 熔点156~157 ℃, 即“青蒿素Ⅱ”,后命名为青蒿素(artemisinin).1972 年在得知北京科研组有关青蒿粗提物的信息后, 山东寄生虫病研究所与山东省中医药研究所合作, 还有云南省药物研究所分别独立进行黄花蒿的提取, 亦获得有效抗疟单体, 各自命名为“黄花蒿素”(山东)及“黄蒿素”(云南). 1974 年初, 上述两种单体被初步确证与北京的青蒿素属相同的药物[6]。
青蒿素的作用

1、青蒿的药理作用1.抗疟作用:青蒿乙醚提取中性部分和其稀醇浸膏对鼠疟、猴疟和人疟均呈显著抗疟作用。
体内试验表明,青蒿素对疟原虫红细胞内期有杀灭作用,而对红细胞外期和红细胞前期无效。
青蒿素具有快速抑制原虫成熟的作用。
蒿甲醚乳剂的抗疟效果优于还原青蒿素琥珀酸钠水剂,是治疗凶险型疟疾的理想剂型。
青蒿琥酯2.5、5、10、15mg/kg,2次/天,连续3天,皮肤外搽,治疗猴疟均有不同程度疗效。
5、10mg/kg,2次/天,连续10天,皮肤外搽即可使猴疟转阴。
加入适量促透氮酮,可提高抗疟作用。
脱羰青蒿素和碳杂脱羰青蒿素对小鼠体内的伯氏疟原虫K173株的ED50和ED90分别为12.6mg/kg和25.8mg/kg。
体外试验表明,青蒿素可明显抑制恶性疟原虫无性体的生长,有直接杀伤作用。
青蒿素、蒿甲醚和氯喹对恶性疟原虫的IC50分别为75.2,29.4.和43.2nmol/L。
青蒿素酯钠对恶性疟原虫6个分离株(包括抗氯喹株)有抑制作用。
2.抗菌作用:青蒿水煎液对表皮葡萄球菌、卡他球菌、炭疽杆菌、白喉杆菌有较强的抑菌作用,对金黄色葡萄球菌、绿脓杆菌、痢疾杆菌、结核秆菌等也有一定的抑制作用。
青蒿挥发油在0.25%浓度时,对所有皮肤癣菌有抑菌作用,在1%浓度时,对所有皮肤癣菌有杀菌作用。
青蒿素有抗流感病毒的作用。
青蒿酯钠对金葡萄、福氏痢疾杆菌、大肠杆菌、卡他球菌,甲型和乙型副伤寒秆菌均有一定的抗菌作用。
青蒿中的谷甾醇和豆甾醇亦有抗病毒作用。
3.抗寄生虫作用:青蒿乙醚提取物、稀醇浸膏及青蒿素对鼠疟、猴疟、人疟均呈显著抗疟作用。
体外培养提示,青蒿素对疟原虫有直接杀灭作用。
电镜观察证明,青蒿素主要作用于疟原虫红细胞内期无性体的膜相结构,首先作用于食物色膜、表膜和线粒体膜,其次是核膜和内质网。
此外对核内染色体亦有影响。
由于食物泡膜发生变化,阻断了疟原虫摄取营养的早期阶段,使疟原虫迅速发生氨基酸饥饿,形成自噬泡,并不断排出体外,使泡浆大量损失,内部结构瓦解而死亡。
青蒿素原理

青蒿素原理
青蒿素,也称为阿蒿素,是从蒿属植物中提取的一种药物成分。
它是一种有效的抗疟药物,特别是对于疟原虫的成熟血红素型有很强的杀灭作用。
青蒿素的作用机制是通过干扰疟原虫的代谢活动来抑制其生长繁殖。
具体来说,青蒿素可以与寄生虫中的血红素结合,形成稳定的血红素-青蒿素蛋白复合物。
这个复合物会积累在疟原
虫的食物液泡中,并与脂质双层相互作用,导致液泡内外压力不平衡,最终破裂。
此外,青蒿素还可以干扰疟原虫内部的氨基酸、核酸和脂类的合成过程,进一步破坏寄生虫的正常代谢途径,致使其死亡。
青蒿素还具有抗炎和免疫调节等作用。
研究表明,青蒿素可以抑制炎症反应的发生,减轻炎症症状,并通过调节免疫细胞的活化和分泌等途径,增强机体免疫力。
总的来说,青蒿素是一种多效性药物,具有广谱的抗疟活性,且作用机制复杂多样。
它的发现和应用为疟疾的治疗提供了重要的突破,对于全球范围内的抗疟工作具有重要意义。
青蒿素——精选推荐
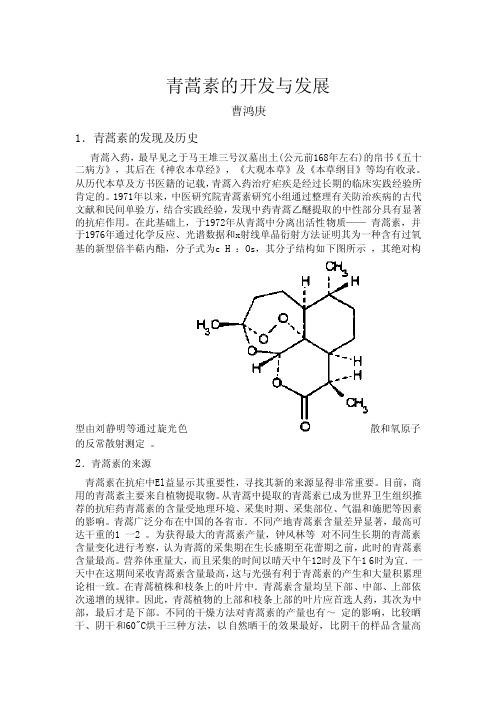
青蒿素的开发与发展曹鸿庚1.青蒿素的发现及历史青蒿入药,最早见之于马王堆三号汉墓出土(公元前168年左右)的帛书《五十二病方》,其后在《神农本草经》,《大观本草》及《本草纲目》等均有收录。
从历代本草及方书医籍的记载,青蒿入药治疗疟疾是经过长期的临床实践经验所肯定的。
1971年以来,中医研究院青蒿素研究小组通过整理有关防治疾病的古代文献和民间单验方,结合实践经验,发现中药青蒿乙醚提取的中性部分具有显著的抗疟作用。
在此基础上,于1972年从青蒿中分离出活性物质——青蒿素,并于1976年通过化学反应、光谱数据和x射线单晶衍射方法证明其为一种含有过氧基的新型倍半萜内酯,分子式为c H :Os,其分子结构如下图所示,其绝对构型由刘静明等通过旋光色散和氧原子的反常散射测定。
2.青蒿素的来源青蒿素在抗疟中El益显示其重要性,寻找其新的来源显得非常重要。
目前,商用的青蒿紊主要来自植物提取物。
从青蒿中提取的青蒿素已成为世界卫生组织推荐的抗疟药青蒿素的含量受地理环境、采集时期、采集部位、气温和施肥等因素的影响。
青蒿广泛分布在中国的各省市.不同产地青蒿素含量差异显著,最高可达干重的1 一2 。
为获得最大的青蒿素产量,钟风林等对不同生长期的青蒿素含量变化进行考察,认为青蒿的采集期在生长盛期至花蕾期之前,此时的青蒿素含量最高。
营养体重量大,而且采集的时间以晴天中午12时及下午1 6时为宜.一天中在这期间采收青蒿素含量最高,这与光强有利于青蒿素的产生和大量积累理论相一致。
在青蒿植株和枝条上的叶片中.青蒿素含量均呈下部、中部、上部依次递增的规律。
因此,青蒿植物的上部和枝条上部的叶片应首选人药,其次为中部,最后才是下部。
不同的干燥方法对青蒿素的产量也有~定的影响,比较晒干、阴干和60"C烘干三种方法,以自然晒干的效果最好,比阴干的样品含量高23.76 在人工栽培中稍加肥料,青蒿植株高大。
青蒿索的含量较野生的略高,且嫩叶比老叶的含量高。
青蒿素的药理作用及其临床应用

青蒿素的药理作用及其临床应用青蒿素是一种从药用植物青蒿中提取出来的有效成分,具有较强的抗疟疾作用。
自从1970年以来,在治疟疾方面被广泛应用,成为世界卫生组织推荐的一线治疗药物之一。
除了治疟疾,青蒿素还具有其他广泛应用的药理作用。
本文将从药理作用及其临床应用方面来介绍青蒿素。
一、药理作用1、抗疟疾作用青蒿素的明显药理作用是抗疟疾。
当细胞内存在铁离子和高浓度的氧,青蒿素分子会发生还原反应,生成较为活性的碳质自由基,并与寄生虫血红蛋白释放的ADP-铁络合物形成螯合物,使疟原虫细胞膜受损,从而使其失去菌体进一步生长的条件,杀灭病原体。
青蒿素不仅能对疟原虫的雌雄配子体产生杀灭作用,也对出血性疟原虫和恶性疟原虫等多种传统难治疟原虫产生杀灭作用。
2、抗癌作用青蒿素不仅对疟疾有很好的疗效,它还具有抗癌作用。
青蒿素能够促进癌细胞的凋亡,抑制癌细胞的生长和分裂,减少癌细胞的转移。
毒性试验显示,青蒿素对正常人类细胞的影响较小,只有在治疗剂量下才有明显的细胞毒性,相较于传统抗癌药物,它的毒副作用相对较小,不易出现耐药性。
3、抗炎作用青蒿素对于抗炎有很好的作用,通过约束肿瘤坏死因子(TNF)的生成来减少炎症反应。
青蒿素通过抑制炎性细胞介导的细胞因子的产生、减轻炎症反应的程度,抑制炎症提振了免疫系统的功能。
同时还能抑制白细胞趋化性因子的生成,减少白细胞聚集,防止炎症加重,减轻感染的严重程度。
4、抗病毒作用青蒿素还具有抗病毒作用。
2015年,在中国科学院微生物研究所的一项研究中发现,青蒿素能够杀死人体细胞中的乙型冠状病毒(MERS-CoV),并在小鼠体内潜在地防止乙型冠状病毒的感染。
该研究成果发表在美国国家科学院院刊《Proceedings of the National Academy of the United States of America》上。
二、临床应用1、治疟疾青蒿素被广泛应用于治疟疾。
1967年,中国科学院中药研究所的屠呦呦首次从药用植物青蒿中分离出青蒿素,成功治疗恶性疟疾,重新挽救了无数生命。
浅谈青蒿素的药理作用和临床应用

青蒿素的药理学研究张红蕊河南省邓州市中医院药剂科474150【摘要】:青蒿为菊科植物黄花蒿(artemisia annua L)的干燥地上部分, 青蒿素由植物黄花蒿中提取,活性较强,由于其良好的解热作用,目前在临床上广泛用于治疗疟疾。
近些年研究发现青蒿素不仅可以用于疟原虫、血吸虫等寄生虫的治疗,并且在其他方面(如抗炎、增强免疫)具有较强的药物作用。
本文在介绍青蒿素抗疟疾作用、应用和作用机制的基础上,也对近年来青蒿素类药物的其它主要生物学作用研究的现状进行综述,尚有多方面的药理作用和临床应用。
【关键词】:青蒿素化学性质药理作用衍生物青蒿素的化学性质:青蒿素是一种具有过氧基的新型倍半萜类化合物。
具有过氧键和δ—内酯环,它的分子中包括7个手性中心。
其结构的分子式为C15H22O5,分子量为282.34,化学名称为(3R,5aS,6R,8aS,9R,12S,12Ar)—八氢—3,6,9—三甲基—3,12—桥氧—12H—吡喃〔4,3—J〕—1,2—苯并二塞平—10(3H)—酮。
青蒿素的物理性质:青蒿素为无色针状结晶,熔点约为156℃,水溶性较差,近乎不溶于水。
易溶于苯、氯仿、丙酮,可溶于酒精、乙醚,微溶于冷石油醚。
由于其组成中含过氧基团,较为特殊,故受热受潮后易分解。
与还原性物质反应较活泼。
【青蒿素的药理学研究】1. 抗疟疾作用青蒿素是药效较强的抗疟药物,具有作用效果显著、作用速度较快、毒副作用较低等特点。
其衍生物蒿甲醚、青蒿酯钠与其作用类似,对鼠疟、猴疟和人疟均有明显的抑制作用。
微生物学试验显示,青蒿素仅对疟原虫红细胞内期具有直接的杀灭作用,对红细胞前期和外期无明显影响。
其作用机理主要是通过破坏疟原虫的膜结构而抑制其生长繁殖,即影响表膜、食物泡膜、线粒体膜的正常功能,破坏核膜、内质网膜的结构,使其功能异常。
且其对遗传物质的复制,转录,翻译有一定影响。
研究表明,青蒿素独有的过氧基是抗疟的必要基团2.抗孕作用实验显示,青蒿琥酯及双氢青蒿素对小鼠及兔有抗孕作用,青蒿琥酯连续使用可使处于妊娠状态的小鼠血清孕酮含量降低,并通过损伤母体的蜕膜和胎盘而破坏发育中的胚胎,使妊娠中止;人类细胞试验说明青蒿素对体外培养的人蜕膜细胞亦有直接杀伤作用。
青蒿素综述

优化或平衡控制代谢途径
法尼基焦磷酸合酶(FPPS) 该酶为1,4-异戊二烯转移酶,可催化合
成FPP,FPP是倍半萜、三萜、多萜的共同 前体,要提高青蒿素的产量,提高FPP的量 是至关重要的。
优化或平衡控制代谢途径
紫穗槐-4-11-二烯合酶(ADS) 该酶是将倍半萜通用前体 DAA 代谢流
引导至青蒿素生物合成下游途径的关键酶。
✓第三步是在紫穗槐 -4, 11- 二烯氧化酶 (amorpha-4, 11-diene oxidase, AMO) 的作用下, 紫穗槐-4, 11-二烯进一步被 氧化形成青蒿醇、青蒿醛,进而合成青蒿 酸或二氢青蒿酸;
✓第四步是青蒿酸或二氢青蒿酸通过一系列 酶反应或酶反应形成青蒿素。
优化或平衡控制代谢途径
Anhui Agri. Sci.2010,38( 4) :1698 -1701. [7]青蒿素生物合成研究进展综述;吴代娟,罗桂甫;精细化工中间体FINE
CHEMICAL INTERMEDIATES,2008 年 12 月,第 38 卷第 6 期. [8]青蒿素生物合成与基因工程研究进展;刘万宏,黄玺;中草药 Chinese
Traditional and Herbal Drugs 2013 年 1 月.
谢谢大家
学学报,1999年12月. [4]青蒿素生物合成的研究进展,卢文婕;陕西中医学院学报,2009年第12期. [5]青蒿素生物合成途径基因组织表达分析与青蒿素积累研究;向礼恩,严
铮辉; 中国中药杂志,2012 年 5 月第 37 卷第 9 期. [6]青蒿素生物合成研究进展;静一,罗安才;安徽农业科学,Journal of
简述青蒿素(Artemisinin)
发酵工程1班 13809015 陈迪迪
有关青蒿素类药物的研究

有关青蒿素类药物的研究摘要:为了解青蒿素类药物的药理和毒理学研究进展,笔者查阅有关文献,综述了青蒿素类药物的药理与毒理学研究进展。
研究结果说明:药动学研究显示此类药物吸收快、散布广、代谢与排泄快;青蒿素类药物除具有抗疟作用外,还有免疫调剂、抗肿瘤、抗炎、抗血吸虫及其它寄生虫等作用;无严峻的不良反映。
【关键词】青蒿素;药效学;药动学;毒理学青蒿素是我国药学工作者于1971年从植物黄花蒿Atemisia annua L.叶中提取分离取得的一个具有过氧桥的倍半萜内酯,经化学改造可生成多种衍生物,如蒿甲醚、双氢蒿甲醚、青蒿酯钠、青蒿琥酯等均具有高效低毒的抗疟活性,尤其对具有抗氯喹能力的脑疟和急性疟有效,同时,对青蒿素类药物的研究引发了全世界药学工作者的关注,发觉了青蒿素类药物许多新的药理活性和一些毒理作用,作者就最近几年来青蒿素类药物的药理和毒理学方面的研究进展作一综述。
1 青蒿素的药理学研究药代动力学中国青蒿素研究小组经大鼠实验证明[1],大鼠口服青蒿素150mg/kg后,吸收迅速完全,但血药浓度低,维持时刻短,显示有首过效应。
静脉注射青蒿素混悬水溶液150mg/kg血药时程符合二室模型,t1/2为30min,Vd为kg,说明青蒿素在体内散布普遍,排除迅速。
在人体肌内注射蒿甲醚油剂kg,kg,和kg后,血药浓度达峰时刻为4h~6h,平均潴留时刻别离为、和,显示经肌内注射后蒿甲醚可在体内存留较长时刻[2],在人体静脉注射青蒿琥酯钠kg和kg后,血药时程符合二室模型,t1/2别离为30min和36min~48min.给药后7h内尿中积存排出原型药物仅占给药量的%~%,说明该药在体内的排除方式主若是代谢转化。
文献报导[2]青蒿琥酯进入体内后专门快就转化成二氢青蒿素。
用家免法测定体液中的药物浓度,难以对二氢青蒿素和青蒿琥酯作出区别,所测的浓度极可能是二种物质浓度的总和。
青蒿素类药物的药效学研究抗肿瘤作用文献报导[3]青蒿酯钠在体外对小鼠P388细胞、HeLa细胞、人肝癌SMMC-7721细胞、人鼻咽低分化鳞癌CNE二、SUNE-1及体内抑瘤实验对肝癌、网状红细胞肉瘤及裸鼠移植人鼻咽癌等有肿瘤抑制作用。
青蒿素的药理作用及其合成研究

青蒿素的药理作用及其合成研究青蒿素,是一种从传统中药草青蒿中分离出来的药物,被广泛应用于对疟疾等疾病的治疗。
自20世纪70年代起,青蒿素已经被世界卫生组织列为治疟疾的首选药物之一。
然而,青蒿素还具有许多其他的药理作用,并且在多种疾病的治疗中也显示出了良好的效果。
本文将从青蒿素的药理作用及其合成研究两个方面,深入探讨这一药物的应用前景。
一、青蒿素的药理作用1. 抗菌作用青蒿素具有良好的抗菌作用,能够有效杀灭多种细菌。
据研究表明,青蒿素对葡萄球菌、肺炎链球菌、金黄色葡萄球菌等细菌的MIC值都非常低,仅为0.5-2ug/ml。
因此,可以将其用于这些细菌引起的感染的治疗中。
2. 抗病毒作用青蒿素还具有一定的抗病毒作用,能够有效地抑制病毒的复制。
研究表明,青蒿素可以抑制HIV等病毒的复制,且具有较好的耐受性。
因此,可以将其用于治疗HIV感染等疾病。
3. 抗肿瘤作用除了上面两个作用外,青蒿素还具有重要的抗肿瘤作用。
据研究表明,青蒿素能够通过多种途径抑制肿瘤细胞的生长和分裂,抑制细胞周期、引起细胞凋亡并促进免疫反应,进而达到抗肿瘤的效果。
与目前的常规肿瘤治疗方法相比,青蒿素的优势在于更加强调对人体的安全性和副作用的降低。
二、青蒿素的合成研究青蒿素的结构复杂,合成难度大,因此,其在药物工业中的制备一直是一个热门的研究课题。
目前,人们已经开发出了多种方法来合成青蒿素。
1. 双氧水法双氧水法是一种产生活性氧的方法,通过活性氧在青蒿素链的氧化反应来合成青蒿素。
这种合成方法的优点在于简单,因此适用于小规模的合成工作。
不过,其缺点在于易受污染等因素的影响。
2. 醛醇法醛醇法是一种生产青蒿素的经典方法,通过反应来合成青蒿素。
这种合成方法最早是由荷兰学者Philips等人于1977年提出的。
该方法的优点在于可实现大规模的合成,并且可以方便地对青蒿素的结构和形状进行调整,使其适合于不同的药物应用。
3. 酮共轭质子转移反应法酮共轭质子转移反应法是一种新型的青蒿素合成方法,其基本原理是利用特殊的催化剂将酮转化为活性亚甲素,进而与其他反应物结合形成青蒿素。
青蒿素文章归纳总结

青蒿素文章归纳总结青蒿素是一种有效的抗疟药物,以其迅速和有效地治疗疟疾而闻名。
自从第一次分离出青蒿素以来,人们对其进行了广泛的研究和应用。
本文将对青蒿素的历史背景、药理作用、临床应用和发展前景进行归纳总结。
一、历史背景青蒿素是由中国科学家屠呦呦于1971年从中草药青蒿中提取出来的。
屠呦呦的发现对疟疾的治疗做出了重大贡献,她因此成为首位获得诺贝尔生理学或医学奖的中国科学家。
青蒿素的发现不仅极大地推动了疟疾的治疗,也为中草药研究树立了榜样。
二、药理作用青蒿素在体内通过两种主要机制发挥药理作用:抑制寄生虫生物合成和破坏寄生虫细胞膜。
青蒿素能够进入寄生虫红细胞内部,与寄生虫生物合成过程中的铁进行反应,形成活性氧,从而抑制寄生虫的生长和繁殖。
同时,青蒿素还能破坏寄生虫细胞膜,使其发生破裂,这进一步导致寄生虫的死亡。
三、临床应用青蒿素是世界卫生组织推荐的首选抗疟药物之一。
青蒿素及其衍生物已广泛用于疟疾治疗和预防。
临床试验证明,青蒿素具有迅速和高效的杀虫作用,可以有效地清除寄生虫,缩短疟疾的持续时间,并减少并发症和病死率。
同时,青蒿素还对多种疟疾株型具有广谱杀虫作用,减少了疟疾耐药性的发展。
青蒿素不仅对疟疾治疗具有重要作用,还展现了在其他领域的潜力。
近年来,青蒿素被发现具有抗癌、抗病毒和抗寄生虫等多种药理作用。
一些研究表明,青蒿素可以有效抑制癌细胞的生长和分化,并促使癌细胞进入凋亡。
此外,青蒿素还显示出对艾滋病病毒、疟原虫和其他寄生虫感染的抗病毒和抗寄生虫作用。
这些发现为青蒿素在其他疾病治疗中的应用提供了新的思路和研究方向。
四、发展前景尽管青蒿素在疟疾治疗中已取得显著成果,但仍面临一些挑战和问题。
首先,长期使用青蒿素可能导致疟疾耐药性的发展,因此需要不断寻找新的治疗方法和替代药物。
其次,青蒿素的制备和提取成本较高,限制了其在一些贫困地区的应用。
此外,对青蒿素的毒副作用和安全性问题仍需进一步研究。
未来的发展方向包括开发新的青蒿素衍生物、合成更便宜的类似物以及寻找其他具有相似药理作用的天然产物。
青蒿素的作用

青蒿素的作用青蒿素是一种有效的抗疟药物,广泛用于治疗疟疾。
它具有抗原虫、抗炎和抗癌等多种药理作用。
本文将详细介绍青蒿素的作用机制、临床应用、药理特点以及未来的发展方向。
青蒿素作为一种天然产物,最初从中草药青蒿中分离出来。
青蒿素对疟原虫有很强的抗原虫活性,可以破坏疟原虫的红细胞寄生阶段和疫病原体引起的内在性过程。
其作用机制是通过靶向对疟原虫的红细胞期进行杀菌,从而达到治疗疟疾的效果。
青蒿素的抗炎作用是其另一个重要的药理作用。
青蒿素通过下调炎症介质的生成,抑制炎症因子的释放,阻断炎症细胞的活化,从而发挥抗炎作用。
这种抗炎作用对于治疗炎症性疾病,如风湿性关节炎、炎症性肠病等具有积极的意义。
除了抗原虫和抗炎作用,青蒿素还具有抗癌的药理作用。
研究表明,青蒿素可以干扰肿瘤细胞的生长和分裂,诱导肿瘤细胞凋亡,抑制肿瘤细胞的侵袭性和转移能力。
这种抗癌作用使得青蒿素成为一种很有潜力的抗肿瘤药物。
在临床应用方面,青蒿素已经成功地用于疟疾的治疗。
疟疾是一种由寄生虫引起的传染病,严重威胁人类健康。
青蒿素与其他药物联合使用,形成了有效的联合疗法,成功地治疗了疟疾。
这种联合疗法不仅增加了治疗的疗效,还减少了抗药性产生的可能性。
此外,青蒿素的抗癌作用也引起了科研人员的关注。
初步的研究结果表明,青蒿素对多种肿瘤具有杀伤作用,包括乳腺癌、肺癌、结肠癌等。
虽然青蒿素在抗癌方面的研究还处于早期阶段,但是其潜力引起了人们的期待。
青蒿素作为一种天然产物,具有较好的安全性和耐受性。
在正常剂量下,青蒿素的不良反应和毒性很小。
然而,长期高剂量使用可能会导致一些不良反应,例如中毒和神经系统损伤。
因此,使用青蒿素时需要慎重,按照医生的指导进行用药。
青蒿素的发展前景在于进一步挖掘其多种药理作用和疾病治疗潜力。
目前,科研人员正在努力寻找更好的制剂和用药方法,以提高青蒿素的疗效和减少副作用。
此外,还有研究人员在探索青蒿素在其他疾病治疗中的应用,如自身免疫性疾病和神经系统疾病等。
青蒿素的药理学研究与应用

青蒿素的药理学研究与应用青蒿素是一种独特的化合物,其拥有重要的抗疟功效,因此被誉为“疟疾的奇迹药物”。
除此之外,现代医学已经确认了青蒿素在抗癌、抗感染、促进血管生成等众多医学领域的应用价值。
本文将简单阐述青蒿素的药理学研究与应用进展。
青蒿素的药理学研究自20世纪70年代中国科学家屠呦呦发现青蒿中含有抗疟成分后,国际上开始逐步注重研究青蒿素的药理学。
研究中发现,青蒿素产生抗疟作用的机制主要是通过抑制疟原虫的生命周期,进而实现治疗目的。
青蒿素可以迅速地杀死红细胞内的疟原虫血泊体,同时还具有抑制疟原虫的生长的能力,因此可以完全消除疟原虫的感染。
除了抗疟作用外,青蒿素具有广泛的抗癌作用。
研究表明,青蒿素可以促进癌细胞凋亡,抑制癌细胞的生长和扩散,同时还可以刺激机体内生成免疫细胞,对癌细胞的免疫的攻击也具有重要意义。
青蒿素的抗癌作用远不止这些,在未来的医学研究中,还有很多有待发现的作用。
青蒿素的应用青蒿素在国际医学领域的应用非常广泛,已经成为疟疾治疗的首选药物。
除此之外,青蒿素对其他疾病的治疗也具有重要的意义。
青蒿素在抗癌治疗中应用比较广泛。
目前,许多抗癌药物都是从青蒿素中分离出来的,如阿霉素、多柔比星等。
不仅如此,青蒿素还被用于治疗不同种类的癌症,如肺癌、肝癌、乳腺癌、前列腺癌等。
青蒿素在抗感染中的应用也非常广泛。
青蒿素可以抑制各种细菌的生长和扩散,同时能够刺激人体免疫系统,增强机体抵御抗菌的能力。
目前,青蒿素已经成为一种重要的治疗多种感染病的有效药物,如肺炎、性传播疾病、结核病等。
青蒿素在感染疾病防治方面的重要性也不容小觑。
青蒿素还在其他医学领域的应用中表现出了出色的效果。
最新的科学研究已经表明,青蒿素可以促进血管生成、维护肝脏和胰岛的正常功能等方面具有重要价值。
青蒿素的广泛应用,将进一步推动其在医学领域中的应用研究和发展。
小结青蒿素是一种神奇的药物,具有独特的化学结构和多种药理学特性。
青蒿素通过抑制疟原虫和其他病原体的生长、促进癌细胞凋亡和自噬,刺激人体免疫系统等方面展现了广泛的应用前景。
青蒿素的药理研究及其临床应用

青蒿素的药理研究及其临床应用青蒿素是一种有效的抗疟疾药物,它是从中国产生的蒿属植物青蒿(Artemisia annua)中提取得到的。
在20世纪70年代,以青蒿素为主要成分的疟疾新药——“青蒿素组合疗法”被发明出来,其治愈率和预防复发率同样突出,且对于复合病原体所致的疟疾均有效。
本文详细介绍青蒿素的药理研究和其在临床应用中的发展历程。
一、药理研究1. 青蒿素的化学结构与作用机理青蒿素是一种内酯型二萜类化合物,分子式为C15H22O5。
它的作用主要是通过抗氧化、抗炎、抗癌、抑菌等多种作用来实现的。
首先,青蒿素治疗疟疾的作用机理是破坏疟原虫进入红细胞的机制。
根据疟原虫的生命周期分为:早期和晚期疟原虫。
早期疟原虫进入红球后,通过突变而不断进化,从而能够抵抗疟疾药物,而青蒿素针对的正是这一环节。
早期疟原虫通过外周血单核细胞和肝细胞亚细胞膜的特定结合蛋白与红细胞结合,进入红细胞后,加速其衰竭,降低疟原虫进一步生存的能力。
其次,青蒿素对于恶性肿瘤的治疗有一定的作用。
它能够干扰肿瘤细胞的代谢过程,使其处于自我消耗和缺血状态,同时促进肿瘤细胞凋亡和细胞自噬,从而对恶性肿瘤具有一定的治疗作用。
最后,青蒿素还具有广谱抗菌作用,对于多种细菌和真菌均有效。
它能够穿透细胞壁进入细胞内破坏细菌的DNA和RNA,从而起到了抑菌的作用。
2. 研究进展自青蒿素被发现以来,各国研究者对它的发挥作用、药物代谢和副作用等方面的研究取得了长足进展。
目前,青蒿素已成为当前世界上应用最广泛的抗疟疾药物之一,同时也已应用于药物肝损伤、骨髓抑制、类风湿性关节炎、糖尿病等多种疾病的治疗中。
二、临床应用1. 青蒿素的应用历程青蒿素的应用历程可以追溯至1972年,当时中国科学家屠呦呦通过研究青蒿叶提取出青蒿素,并发现它对疟原虫有很强的杀灭作用。
但当时由于中国走向科技封锁,青蒿素对于疟疾治疗的意义并没有被外界广泛认知,直到20世纪80年代初才被引入了海外市场,以其良好的疗效而为世界所熟知。
青蒿素药理与危害

氧自由基的来源
自由基含有一个不成对电子的原子团
氧自由基的危害
细胞质膜
细胞核膜
线粒体膜
氧自由基
蛋白质、脂类
氧自由基破坏细胞结构
破坏疟原虫食物泡结构
疟原虫以食物泡形式摄取营养物质
青蒿素耐药性问题
改变生活周期、暂时进入休眠状态 规避敏感杀虫期
1.延长用药时间 2.更换辅助药物
青蒿素药理作用总结
1. 干扰疟原虫表膜-线粒体,阻断其营养获取 2.虫体不断吐出自噬泡
诺贝尔桂冠获得者:青蒿素
---药理作用
疟原虫的种类
疟原虫主要有四类
疟原虫什么样呢?
我是一只小虫子
疟原虫生活习性
疟原虫是一类单细胞、寄生性的原生动物
血红蛋白结构
Fe2+使血红蛋白分子具有载氧功能
疟原虫以红细胞血红蛋白为食
疟原虫进入到红细胞
青蒿素抗S)
Fe2+裂解青蒿素过氧桥产生氧自由基
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
进一步的研究。
1.5对免疫功能的影响近年来国内外有
很多文章报道青篙素及其衍生物对免疫系统
的影响,所得结论并不一致。林培英等「’用
多种动物模型、多项免疫指标.对青篙素、青
篙唬酷和篙甲醚进行较系统的研究,发现青
篙素、青篙唬醋对体液免疫有抑制作用,篙甲
慢静脉注射。
1.3抗血吸虫及其它寄生虫的作用青篙
素类药物是一种具有抗血吸虫作用的新型化
合物。其中篙甲醚和篙乙醚疗效较好,毒性较
低,此两药对日本血吸虫d7童虫、d35成虫的
减虫作用能使肝期童虫和成虫体内糖原含量急剧减
少,碱性磷酸醋酶活性减弱,对肝期血吸虫童
性L20一,还可见内脏广泛淤血,甚至出血.尤其
是胃肠粘膜溃疡,粘液血便,胃肠功能严重紊
乱等,并可引起视网膜的器质性损伤。停药后
各种变化亦可基本恢复正常。
2.3生殖毒性大鼠于孕后第1~6夭
(d,一。)灌胃青篙素一/25LDS。(223mg/kg),
几乎全部胎鼠发育正常;孕d6一。给药,6.1%
2.5中毒机理青篙唬酷的主要毒性作用
机理之一L,3一,可能是该药在代谢过程中产生
自由基以攻击不饱和脂肪酸,引发脂质过氧
化,导致细胞膜结构损伤和细胞功能紊乱.从
而表现出其毒性作用。
3结语
青篙素及其衍生物的药理作用是多方面
的,它除了有高效低毒的抗疟作用外,动物实
验亦证明有抗血吸虫、弓浆虫等作用。体外实
醚对体液免疫无此作用;三者对特异性细胞
免疫功能有增强作用,对非特异性免疫功能
具有抑制作用;青篙素、青篙唬酷能增强效应
阶段Ts细胞的活性,Ts细胞是青篙素、青篙
唬醋的效应靶细胞,但TS细胞不参与篙甲
醚的体液免疫反应,三者均能使补体C3含量
增加,使炎症部位PGE的合成量减少。此外,
青篙素、青篙唬酷和篙甲醚对免疫功能的影
(l),17〔随rivativesasAntimalarials.JTradCh,nMed,1982,2
5.殷静雯,等.中国药理学报,i,91,12(5):478(i):31
6.欧阳,等.中国人兽共患病杂志,1991.7(5):6317.乐文菊,等.药学学报,1982,7(3):187
7.邓定安,等.有机化学,1991,11(5):54015.李泽琳,等.中药通报,1988,13(4):234
形成钠盐后溶于水,因其给药方便,抗疟作用
又较青篙素为好,近年来对其研究较多,它在
免疫调节及抗孕作用方面也有一定开发前
景。总之,关于青篙素及其衍生物的研究目前
仍在深入。
参考文献
1.C卜i们奋一CooperarivesResearellGrouponQingh左一osuandl丫s
1尧rivativesasAnrlmala石als.JTradChinMed,1982,2
合成了百余种衍生物,其中二氢青篙素、篙甲
醚和青篙唬酷的抗疟作用比青篙素还大。目
前我国青篙素和青篙唬酷已有商品供应。青
篙素片剂:100mg/片,第l日口服1.09,第
2、3日各服0.59。青篙唬醋(注射用):60
mg,临用前用所附5%碳酸氢钠溶解,再以葡
萄糖注射液稀释成10mg/ml的溶液,作缓
知,青篙素及其衍生物有较明显的胚胎毒作
用,在较小剂量即可引起胚胎吸收,对存活动
物致畸性较小或无致畸性,且在不同孕期给
药时对胚胎的作用亦不同。
2.4致突变作用经Ames试验、微核试验
未发现青篙素具有诱变性。经Ames试验、微
核试验及哺乳动物培养细胞染色体畸变试
验,均未发现青篙唬醋钠具致突变作用「22。
胎鼠出现脐庙,其余发育正常;孕d卜,l给药,
胎鼠全部被吸收仁“一。以小鼠进行的实验也有
类似结果L21),小鼠于孕后d卜15每夭肌注篙甲
醚5.4mg/kg,对胎鼠的生长发育无明显影
响,肌注10.7mg/kg和21.4mg/kg则分别
有30%和100%胚胎被吸收。大鼠和兔在相
应的低剂量时对胎仔生长发育亦无影响,在
(l):25
2.赵凯存,等.中国临床药理学杂志,1988,4(2):76
3.杨树德.等.中国临床药理学杂志,1985,1(2):1()6
4.ChinaCooperativesResearebGrouponQinghaosuandItsDerivativesasAntimalarials.JTradChinMed,1982.216.C卜inaCooPerat一vesResearehGrouponQinghaosuandIts
mg/kg、48mg/kg、96mg/kg、192mg/kg分
为小、中、大、特大剂量组,于停药后3夭,其中96mg/kg和192mg/kg组引起多种脏器
组织的损伤。表现为骨髓红系和粒系细胞数
减少,成熟发育障碍,巨核细胞增生;心肌细
胞变性和灶性坏死(以超微结构病变为主);
肝、肾营养不良性改变;淋巴组织萎缩;注射
抑制而非杀灭。临床用青篙煎剂治疗登革热
病人.疗效显著且优于吗琳双肌,治愈率可达
100%「’‘。实验研究证明{‘5一,青篙唬醋有保
肝、降酶、抗病毒、调节免疫和增加还原型谷
胧甘肤等作用,其在治疗肝炎尤其是慢性肝
炎方面可能有其前途,但尚待临床证实。
2青篙素类药物的毒理学研究
2.1急性毒性对青篙素及其衍生物篙甲
皮炎、多形性日光疹及植物日光性皮炎均有
治愈作用。在用三种青篙制剂治疗50例盘形
红斑狼疮的观察中.总有效率达90%‘一‘2。青
篙素类物质无皮质激素样副作用,也没有抗
组胺药的嗜睡作用,可以作为一种新型的免
疫调节剂用于临床L“。
1.6其他药理作用在鸡胚感染试验中显
示‘,’,青篙素有抗流感病毒作用,其作用为
子、豚鼠、兔、猫及狗可表现出阵挛性和强直
性的惊厥,死前均有频繁抽搐,先呼吸停止.
然后心跳停止。鸽子对青篙素毒性最敏感,大
鼠最耐受。存活动物一般在10h一24h后逐
渐恢复正常。
2.2长期毒性恒河猴肌注青篙素的亚急
性毒性病理学研究表明{”一恒河猴连续14
天肌注青篙素油悬剂,按每天肌注青篙素24
药量的0.1%一6.8%汇,二,说明该药在体内的
消除方式主要是代谢转化。文献报告L3二,青篙
唬醋进入体内后很快就转化成二氢青篙素。
用放免法测定体液中的药物浓度,难以对青
篙唬酷和二氢青篙素作出区别,所测得的浓
度很可能是二种物质浓度的总和。
1.2抗疟作用青篙素具抗疟作用,临床上
青篙素对间日疟、一般恶性疟及抗氯喳地区
mg/kg,其混悬液灌胃的LDS。为977mg/kg
士114mg/kg。青篙唬醋钠小鼠静注的LDS。
为520mg/kg,肌注为475mg/kg,大鼠皮下
注射的LDS。则为438mg/kg。
不同种类动物大剂量单次肌注青篙素的
急性毒性症状有[’‘一:动物懒动,发抖,运动失
调,呼吸缓慢,感觉迟钝及翻正反射消失。鸽
醚、青篙唬醋的急性毒性研究发现L’6一‘8,小
鼠、大鼠口服青篙素水混悬液的LDS。分别为
4228mg/kg及5576mg/kg。肌注青篙素油
混悬液的IJDS。分别为3840mg/kg及2571
mg/kg。小鼠肌注篙甲醚油剂的LDS。为263
mg/kg,皮下注射的LDoo为391mg/kg土60
相应高剂量时大量胚胎被吸收。小鼠受孕后
d6一15肌注篙甲醚,对第二代胎鼠生长发育无
不良影响。青篙唬酷对大鼠出现胚胎毒性作
用的剂量非常小[,,几,当剂量为l/809LD。。
(0·5mg/kg)时,对母体完全无害的情况下,
仍有32.8%胎鼠被吸收,说明胚胎对青篙唬
醋钠的敏感性明显高于母鼠。由以上结果可
部位损伤等,其中以骨髓和心肌损伤较为明
显。于停药后35天,上述病变明显减轻或消
失,表明青篙素的毒副作用是可逆性的。每夭
肌注青篙素24mg/kg和48mg/kg为轻微
中毒剂量;96mg/kg为严重中毒剂量;192
mg/kg为致死剂量,致死原因为严重心肌损
伤。青篙琉酷钠静脉注射对犬的亚急性毒
kg后,血药浓度达峰时间为4h一gh,平均
储留时间分别为一0.Zh、15.6h和19.oh,
显示经肌内注射后篙甲醚可在体内存留较长
时间tZ二。在人体静脉注射青篙唬醋钠2.。
mg/kg和3.8mg/kg后,血药时程符合二室
模型,‘专。分别为30min和36min一45min。
给药后7h内尿中累积排出原型药物仅占给
大鼠实验表明“,大鼠口服青篙素150mg/
kg后,吸收迅速完全,但血药浓度低,维持时
间短,显示有首过效应。静脉注射青篙素混悬
水溶液150mg/kg,血药时程符合二室模型,
t合。为30min,Vd为4.IL/kg,表明青篙素在
体内分布广泛,消除迅速。在人体肌内注射篙
甲醚油剂3.Zmg/kg、6.omg/kg和10.0mg/
8.邓定安,等.药学学报,1992,27(4):31719.王德文,等.解放军医学杂志,1983,8(4):257
9.周金黄,等编.免疫药理学进展.基础与临床.中国科技20.宁殿玺,等.中国药理学与毒理学杂志,1987,l(2):
出版社.1993:325~538135
黄花篙中分离出有效单体青篙素。随着青篙
