高校液相色谱法测定吲达帕胺片的含量
化学药吲达帕胺片2013年的检验结果分析

1 . 1 品种来源 : 吲达 帕胺片收载于 《 中国药典 1 2 0 1 0年版二部 , 3 3. L 有关物质 : 检验 的 3 6批样品有 关物质全部 合格 。样 品分 处方 主要成分为 吲达 帕胺 。检验规格 均为每片 2 . 5 mg , 根据抽 离 度符合要求 , 对3 6批 吲达帕胺 片进行有关 物质分析 , 趋 势
格率为 9 7 . 2 %, 不合 格率 为 2 . 8 %。 实测值 图 对3 6} L L  ̄I 达 帕胺 片进 行 有 关 物 质 分 析 图 2抽 样 情 况 分析 从上 图可 以看 出,各生产企业在有关 物质控制方面情况 2 . 1 规格 、 剂型 、 包装种类 : 收到全 区 1 2个盟市抽 样总批数 3 8 令人满意。绝 大部分产 品控制在 了 0 . 1 %~ 0 . 3 %之间。 批, 规格分 为 3 种( 见表 1 ) 。 表 1 吲达 帕胺 规 格 统 计 表 3 . 3 . 2含 量 均 匀 度 : 检验的 3 6 批 吲达 帕 胺 片 含 量 均 匀 度 全 部 合 格。对 3 6批吲达帕胺 片进 行含量均匀度分析 , 趋势 图如下 。
北方药学 2 0 1 4年第 1 1 卷第 3 期
1 5 9
化 学药 吲达帕胺片 2 0 1 3年的检验结果分析
裴 春梅 丁 华 ( 内 蒙古 鄂尔多斯市 食品 药品 检验研究中 心 鄂 尔多斯 0 1 7 0 0 0 )
摘要 : 目的: 分析化 学药吲达 帕胺 片的检验情况。方法 : 依据《 中国药典) 2 0 1 0年版二部 对 3 6批抽 验吲达帕胺 片片剂 实验结果进 行调 查评 价、 汇总分析及探 索性研 究。结果 : 3 6批吲达帕胺片合格率为 9 7 . 2 %, 不合格 率为 2 . 8 %。结论 : 现行质控标准虽可较好 地控 制该化 学药质 量, 但还可做进 一步提 高与 完善 。
吲达帕胺原料药中DCC和DCU含量的检测方法[发明专利]
![吲达帕胺原料药中DCC和DCU含量的检测方法[发明专利]](https://img.taocdn.com/s3/m/b0ed930b102de2bd970588c5.png)
专利名称:吲达帕胺原料药中DCC和DCU含量的检测方法专利类型:发明专利
发明人:詹志斌,秦巨波,谢秀萍,陈小波,龚明峰,张志刚
申请号:CN201911130294.9
申请日:20191118
公开号:CN111595954A
公开日:
20200828
专利内容由知识产权出版社提供
摘要:本发明涉及吲达帕胺原料药中DCC和DCU含量的检测方法,其是利用高效液相色谱法对吲达帕胺原料药中的DCC和DCU进行检测,包括以下步骤:(1)配制吲达帕胺原料药供试品溶液;(2)分别配制DCC对照品溶液、DCU的对照品溶液和DCC&DCU对照品溶液;(3)进样,按以下条件对步骤(1)供试品溶液和步骤(2)中的对照品溶液分别进行检测:色谱条件:流动相:乙腈‑水;梯度洗脱:
0‑30min乙腈比例由10‑40%逐渐升至90‑98%;柱温为33‑37℃;流速为1.4‑1.6ml/min;检测波长为190‑210nm;(4)将供试品DCC、DCU对应的峰面积与对照品溶液计算得到DCC、DCU的含量。
本发明所提供的吲达帕胺原料药中DCC和DCU含量的检测方法,使用的试剂毒性小,杂质干扰少,检测方法可靠稳定。
申请人:远大医药(中国)有限公司
地址:430000 湖北省武汉市硚口区硚口路160号1幢23层1-6号
国籍:CN
代理机构:武汉蓝宝石专利代理事务所(特殊普通合伙)
代理人:王振宇
更多信息请下载全文后查看。
吲达帕胺缓释微球的体外释放性能及机制考察
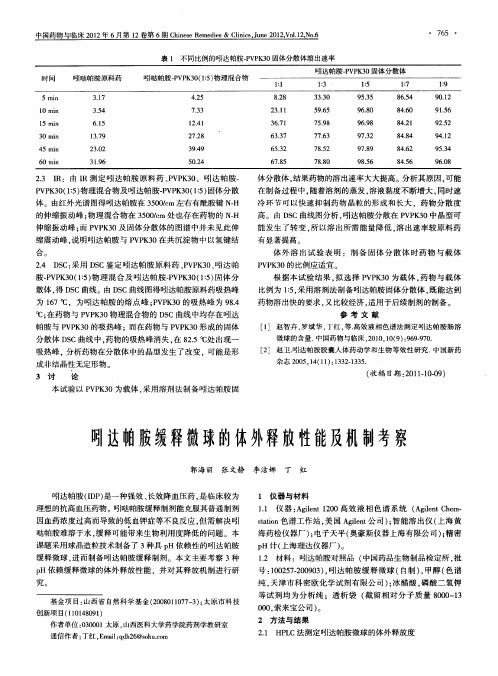
21 色谱条件[: .. 1 1 色谱柱 : gl t 1 (5 rx . m ] A i n 8柱 10mn 46 m, e C 5I ; m)流动相 : x 甲醇 : 醋酸 (55 :.)柱 温 :5℃; 水: 4 : 01 ; 5 2 流速 : 08ml i; . / n检测波长 :4 m; m 2 0a 进样量 2 l 0 。 21 标准曲线 的制备 : .. 2 分别配制 p .、H 45 p .、H H 1 p .、H 68 p 2 78的吲达帕胺对照品储备液 , . 稀释成系列质量浓度的溶液 , 进 行测定 , 以峰面积 ) 为纵坐标 , 质量浓度 ( ) G 为横 坐标 , 进 行线性 回归 , 结果 : 栅28 .8 + . 4Ap 8 .1C 82 7 A = 5 C 09 、 4 96 2 + . 、 5 4 H= 5 0
本试验 以 P P 3 V K 0为载体 , 采用溶剂法制备 吲达帕胺 固
吲达帕胺缓释微球的体外释放-能及机制考察 性
郭海丽 张文静 李洁娜 丁 红 吲达 帕胺 (D ) I P 是一种强效 、 长效降血压药 , 临床较为 是 理想的抗高血压药物。吲哒帕胺缓释制剂能克服其普通制剂 因血药浓度过高而导致 的低血钾症等不 良反应 . 但需解 决吲 哒帕胺难溶于水 , 缓释可能带来生物利用度降低的问题。本 课题采用球 晶造粒技术制备 了 3种具 p H依赖性的吲达帕胺
[ ] 赵智卉 , 1 罗斌华 , 丁红 , 高效液相色谱法 测定吲达帕胺肠溶 等. 微球的含量. 中国药物与l ,00 1 ( ) 6 . 0 床 2 1 , 9 : 99 . 0 9 7
10r n考察微球 的释放度 。 胃溶 微球 于释放 0 5 1 ,0 0 mi / , ,5 3 ,
基于HPLC法的吲达帕胺片有关物质测定

医药界 2020年06月第12期—115—临床经验基于HPLC 法的吲达帕胺片有关物质测定曹 祺 潘翠萍(广东安诺药业股份有限公司,广东 普宁 515300)【摘要】:目的:基于HPLC 法测定吲达帕胺片有关物质。
方法:采用高效液相色谱设备,流动相为甲醇(CH 3OH )-水(H 2O )-冰醋酸(CH 3COOH )比例为30:40:0.2,流速为2ml/min ,检测波长为260nm 。
结果:通过测定得出,实验组的测定误差在0.70μg/ml~0.90μg/ml 范围内,而对照组的测定误差最小值也超过了1.00μg/ml 。
结论:基于HPLC 法的吲达帕胺片有关物质测定方法具有可有效降低测定结果误差,进一步提高测定方法的准确性,保障药品制备的质量。
【关键词】:HPLC 法;吲达帕胺片;有关物质;测定;【中图分类号】R 927 【文献标识码】A 【文章编号】2095-4808(2020)12-115-010.引言吲达帕胺片是一种常见治疗高血压的药物,吲达帕胺的化学名称为:N-(3-甲基-2,3-二氢-1H-吲哚基)-3-氨磺酰基-4-氯-苯甲酰胺,尤其化学名称可以看出,该药物是一种携带吲哚环的磺胺衍生物[1]。
除了治疗高血压疾病外,吲达帕胺片还可通过抑制远端肾小管皮质稀释段对钠元素的重吸收,从而促进尿液中钠元素的排泄量增加,同时在一定程度上增加钾元素的排泄量,具备一定的利尿效果。
其次,该药物还具备一定的降压作用,但目前由于研究较浅,吲达帕胺片在降压作用中的相关机制尚未作出明确的判断。
当前在医药市场当中,吲达帕胺片主要作为利尿和降压的药物,且需求量较大,是各大零售药店和医院终端的畅销药物[2]。
随着药物生产技术的不断更新,该药物的生产规模也将逐步扩大,并且含有吲达帕胺的口服缓控释制剂也具备良好的应用前景,当前国内外药物市场中吲达帕胺主要以普通片、缓释片和缓释胶囊等类型药剂为主。
针对吲达帕胺片的有关物质组成成分,本文提出一种基于HPLC 法的吲达帕胺片有关物质测定方法。
HPLC法测定吲哒帕胺片的含量及含量均匀度

21 0 0年第 2 3卷第 3 期 ・药学研 究 ・
HP C法测定 吲哒帕胺 片的含量及含量均匀度 L
闰 韶 华 ( 河南 省周 口市食 品药 品检验 所 周 口 4 6 0 ) 6 0 0
摘 要 : 建立了高效液相色谱法测定 吲哒帕胺片中吲哒帕胺 的含量及含量均匀度 的方法 。该方法主要参数为 : 色谱柱为 Kr— o mai 1( 5mm>4 6 sC8 2 0 l < . mm, “ , 5 m) 流动相 为 甲醇一 (O 4 ) 冰醋酸调 节 p 至 3 5 水 6 :0 用 H . O±0 0 , . 5 检测 波长为 2 0 m, 4 n 流速为 l m1. rj- 该方法对吲哒帕胺 的平均 回收率为 9. 8 , D为 0 9 %( 一5 。结果 提示 , nn 1 95 RS .0 n ) 该方法结果准 确 , 专属性强 , 可用于含量及 含量 均匀度的测定。 关键词 : HP C法 ; 吲哒帕胺片 ; 吲哒帕胺 L
23 重复性实验 . 取同一批 号样 品适量 ( 约相当于吲哒帕胺 5 ) 份 , mg 3 精密 称定 , 按样 品测定项 下 的方法 , 定吲 哒帕胺 片 的含 量 , S 测 R D
为 0 7 。 .5 24 稳 定 性 实 验 .
取重复性 实验 中的第 一份 溶液 , 室温 下在 0 1 2 3 4小 、 、、 、 时测定 , 结果表明 , 品的供试品溶液在 室温 4小时 内基本 稳 本
精密称取吲哒帕胺对 照品 00 1g 置于 5 ml 瓶中 , .17 , 0 量 加
吲达帕胺片质量标准检测方法修订探讨

参考。
【关键词】高效液相色谱法;吲达帕胺质量控制标准研究
[ 中图分类号 ]R927
[ 文献标识码 ]A
[ 文章编号 ]2096-5249(2020)17-0212-02
吲达帕胺片为磺胺类利尿药,具有利尿和钙拮抗作用, 是一种强效、长效的降压药。依据 2015 年版的《中国药典》[1], 吲达帕胺片均匀度 ( 含量 )、含量、溶出度测定均实施紫外分 光光度法。伴随检验标准不断提升,相关研究文献也大量增 多,作为本次研究的参考 , [2-4] 通过试验研究发现,吲达帕 胺片均匀度 ( 含量 )、含量、溶出度测定对 HPLC 法进行利用, 从研究结果中显示,此测定方法具有较好的重复性、较强的 专属性、较高的灵敏度,且可保证可靠、准确的测定结果, 在吲达帕胺片均匀度 ( 含量 )、含量、溶出度测定中使用,可 有效控制质量。
55:0.1),检测波长:240nm。结果:吲达帕胺在 5.22~52.18ug/mL 范围内线性关系良好 (r=0.999),平均回收率为 99.5%(RSD=0.1%,n=9)。
结论:所建立的 HPLC 方法符合方法学考查要求,可用于吲达帕胺片中含量、含量均匀度和溶出度的检测,可为该药品质量标准修订提供
2.8 稳定性试验 以上文方法供试品溶液进行制备,在色 谱条件下,在 0~24h,每隔 2 个 h 进行 1 次测定,测定结果显 示,峰面积的 RSD 为 0.17%(n=8),在 24h 供试品溶液呈现稳 定的状态。
2.9 加样回收率试验 对 B 样品进行精密称取 ( 约 20mg 含 吲达帕胺 ),量取 9 份,在量瓶 (100mL) 中置入,每 3 份,将
品、对照品,在液相色谱仪中注入,图 1 显示结果。
a
b
c
吲达帕胺固体分散体的制备及体外溶出特性考察

体分散体 , 结果药物的溶 出速率大大提高。分析其 原因, 可能
在制备过程 中, 随着溶剂 的蒸发 , 溶液黏度不断增 大 , 同时速
冷 环 节 可 以 快 速 抑 制 药 物 晶粒 的 形 成 和 长 大 ,药 物 分 散 度
P P 3 ( :) V K 0 1 物理混合物及吲达帕胺.V K 0 1 ) 5 P P 3 (: 固体分散 5
吲达 帕胺 一V K 0物理混合 物及吲达 帕胺一V K 0固体 分 PP 3 PP3
1 . 标准 曲线的绘制 :精密量取吲达帕胺储备液 05 1 、 .2 3 .、. 0
20 50 8 1 .、2 1 .、.、. 0 1 . m 分别置于 10m 容量瓶 中 , 0、 0 0 0 l 用水定 容, 摇匀 , 2 2n 在 4 m波长处测定其吸光度值 ( , A)绘制标准 曲
缓 释 微 球 , 而 制 备 吲 达 帕 胺 缓 释 制 剂 。 本 文 主要 考 察 3种 进
体 。由红 外 光 谱 图得 吲达 帕 胺 在 3 0/m左 右 有 酰 胺 键 N H 5 0c —
的伸缩振 动峰 ; 物理混合物在 30 /m处也存 在药物的 N H 50c — 伸缩振动峰 : P P 3 固体 分散体的 图谱 中并未见此伸 而 V K 0及 缩震动峰 。 说明吲达帕胺与 P P 3 V K 0在共沉淀物 中以氢键结 合。 24 S : . D C 采用 D C鉴定吲达帕胺原 料药 、V K 0 吲达 帕 S PP 3 、 胺.V K 0 1 ) 理混 合及吲 达帕胺.V K 0 1 ) P P 3 (: 物 5 P P 3 (: 固体分 5
HPLC检测中药中非法添加化学降压药物

HPLC检测中药中非法添加化学降压药物随着高血压疾病的普遍发生,化学降压药物被广泛应用于临床治疗中。
然而,一些不良商家为增加中药的功效,非法向中药中添加化学降压药物,这既影响患者的健康,也破坏了中药的药性。
因此,如何检测中药中是否存在非法添加化学降压药物成为了一个重要的研究问题。
目前,高效液相色谱(HPLC)已经成为检测中药中非法添加化学降压药物的常用方法之一。
HPLC技术基于物质在固体与液体之间的相互作用而实现物质的分离和检测。
常见的液相色谱柱包括反相柱、离子交换柱和大小排列柱等。
而检测中药中非法添加化学降压药物则需要选用特定的柱型和检测条件。
具体来说,针对不同的化学降压药物,需要选择适当的检测波长和检测方法。
以利福平为例,通常采用反相柱(C18)作为固相,流动相则是甲醇-水混合液。
在此条件下,利福平的检测波长通常为254 nm。
如果中药中非法添加了利福平,那么就会出现具有特征波长和保留时间的峰。
而利福平的峰面积和峰高则可用来计算其含量。
其他化学降压药物的检测方法也类似,唯一不同的是某些药物需要特殊的检测条件。
当然,在HPLC检测过程中,需要注意一些技巧和细节。
首先,样品的前处理至关重要,自然干燥和无菌破碎等操作是必须的。
其次,需要根据样品的特点选用不同的提取方法,比如超声波法、微波法和微量萃取法等。
如此,才能有效提取化学降压药物并减少杂质的干扰。
最后,在完成HPLC检测后,还需要对检测结果进行质量评估,如判断峰的对称程度、峰面积和峰高等。
总的来说,HPLC检测是一种可靠的手段,用于检测中药中非法添加化学降压药物。
当然,在实际检测中,也需要结合其它检测手段,如质谱分析或核磁共振成像,从而更好地保护人民的健康和安全。
吲达帕胺缓释片的制备及体外释放度测定

吲达帕胺缓释片的制备及体外释放度测定谢清春;陈燕忠;吕竹芬;何敏【摘要】目的制备吲达帕胺缓释片并测定其释放度.方法以进口市售片为对照片,以高效液相色谱法为测定释放度的方法,以释放度为指标筛选缓释片处方,考察填充剂类型(乳糖、可溶性淀粉及微晶纤维素)及羟丙基甲基纤维素(HPMC K4M)用量对释放度的影响;并对自制片和对照片的释放曲线进行相似性评价.结果以乳糖作填充剂,HPMC K4M的质量分数为25%时,自制缓释片的释放度与对照片比较差异无统计学意义.释放度测定方法:吲达帕胺的质量浓度在0.2~1.5 μg·mL-1范围内与峰面积线性关系良好,低、中、高3个浓度的回收率分别是100.08%、99.67%、99.58%.结论自制缓释片处方工艺简单、经济,释放曲线与对照片相似.【期刊名称】《广东药学院学报》【年(卷),期】2010(026)006【总页数】3页(P561-563)【关键词】吲达帕胺;缓释片;高效液相色谱法;体外释放【作者】谢清春;陈燕忠;吕竹芬;何敏【作者单位】广东药学院,药物研究所/广东省药物新剂型重点实验室,广东,广州,510006;广东药学院,药物研究所/广东省药物新剂型重点实验室,广东,广州,510006;广东药学院,药物研究所/广东省药物新剂型重点实验室,广东,广州,510006;广东药学院,药物研究所/广东省药物新剂型重点实验室,广东,广州,510006【正文语种】中文【中图分类】R94吲达帕胺(indapamide)属于噻嗪类利尿药,降压作用强而利尿作用弱,其抗高血压和排钠利尿作用是分离的:低剂量时降低血压,较高剂量时其附加的利尿作用才显著[1]。
该药由法国Servier公司首先研制[2],《中国药典》2010年版收载了其普通片剂。
目前国内临床应用较多的缓释片是进口的纳催离(natrilix SR),它能在24 h内很好地控制血压,且在服药后的25~30 h之间仍能稳定降压。
HPLC法测定吲达帕胺片的含量

UV 2 5 一 5 0型 紫 外 分光 光 度 计 ( 日本 ) 9 S 2 2 ,2 M一 0 A双 量
供 试 品 溶液 的制 备 方法 制 成 阴 性溶 液 。遵 照 指定 的色 谱 条 件, 分别 准确 进 样 2 l进行 图谱 分 析 。 0 , 结果 显 示 , 色谱 在该 条 件 下 , 保 留时 间 t 41rn处 , 试 品 和 对 照 品溶 液 中 在 R .a = i 供
24 专 属 性 试 验 问 .
础 上 。 立 了测 定 吲达 帕胺 的 高效 液 相 色 谱 法 , 于 原有 的 建 优 紫 外 分光 光度 法 . 可用 于该 品种 的质 量控 制 。
1仪器 与试 药
去掉 吲 达 帕胺 , 他 按 处 方 和工 艺 制 成 阴性 对 照 , 照 其 按
CHEN pu Yu
J ou s t t frF o n r g C n rl Hen n P o ic , io u 4 4 0 , h n i z o I t ue o o d a d D u o t , a r vn e Ja z o 5 0 0 C i a a n i o
【 关键词1 高效液相 色谱 法; 吲迭帕胺 片; 含量 【 中图分类号】 9 71 R 2 .1 【 文献标识码】 A 【 文章编号】1 7 — 2 02 1 )1a 一 8 — 2 6 3 7 1 (0 1 ( )0 3 0 1
HPLC法测定全血中吲达帕胺的浓度

rn e o 5 0~1 0 0 n / , =0. 9 4 T elw s d tcinl t a . g n wi i—a db t e n d y a g f . 6 . g ml r 9 8 . et ee t mi w s 0 n /  ̄, t n d ya ew e -a h o o i 5 h n
Dee m i a in o n a m i e i m a hoe Bl o y HPLC t r n to fI d pa d n Hu n W l o d b
L U Jny n. I i-a WU il n J—i g a
( ua nvrt aiMei l colW hnH bi 30 1C i W h nU i syB s d a ho, ua ue4 07 ,hn ei c c S a)
回收率为 7.% ~ 02 。结论 本 文建 立的测定全血 中吲达帕胺浓度的 H L 26 8.% PC方法简便 易行 、 快捷 。 方便
关键词 : 吲达帕胺; P C 全血药物浓度 ; HL; 药代 动力 学
中图分类号 : 97 2 R 2 . 文献标识码 : A 文章编号 :0 80 3 (0 10 -300 10 - 5 2 1 )50 9 -5 6
clm mprtr a e a 2 ℃ , em bl p aew scmpsdo popa u e p . ) m tao o nt ea ew s t t 0 t oi hs a o oe f hsht bfr( H3 0 : ehnl u e u s h e e
:spoy l hl( 4 4 : ) t o a fI / i ,n eU e c o aeeg a e a 2 1m. i rp l c o 5 :0 6 a af w rt o mlm n a dt V d t tn w vl t w sst t 4 o ao l e h ei nh n
HPLC法测定吲达帕胺片的含量

HPLC法测定吲达帕胺片的含量作者:陈玉璞来源:《中国医药导报》2011年第31期[摘要] 目的:建立测定吲达帕胺片含量的方法。
方法:采用HPLC法,C18柱(150mm×6 mm,5 μm),流动相为甲醇-水-冰醋酸(45∶55∶0.1),检测波长为240 nm。
结果:吲达帕胺在1.65~16.48 μg/ml浓度范围内线性关系良好(r=0.999 9),平均回收率为99.20%,RSD=0.53%。
结论:本方法简便、快速、准确,专属性强,可作为吲达帕胺片的含量测定方法。
[关键词] 高效液相色谱法;吲达帕胺片;含量[中图分类号] R927.11 [文献标识码] A [文章编号] 1673-7210(2011)11(a)-083-02Content determination of Indapamide Tablets by HPLCCHEN YupuJiaozuo Institute for Food and Drug Control, He′nan Province, J iaozuo 454000, China[Abstract] Objective: To establish a method to determine the content of Indapamide Tablets. Methods: HPLC with C18 chromatographic column (150 mm×6.0 mm, 5 μm) was used. The mobile phase was methanol-water-acetic acid glacial (45∶55∶0.1), the wavelength for detection was 240 nm. Results: The linear range of Indapamide Tablets was 1.65-16.48 μg/ml (r=0.999 9). The average recovery was 99.20% (RSD=0.53%). Conclusion: The method is simple, rapid, accurate and specific. It can be used as the quantitative determination of Indapamide Tablets.[Key words] HPLC; Indapamide Tablets; Content吲达帕胺片为抗高血压药物,用于治疗原发性高血压及充血性心力衰竭引起的水钠潴留。
HPLC法测定吲达帕胺片的含量

HPLC法测定吲达帕胺片的含量江苏省淮药品检验所杨鲲摘要:目的用HPLC法测定吲达帕胺片中吲达帕胺的含量。
方法采用HPLC法测定。
以C18为固定相,甲醇-水-冰醋酸(45:5:0.1)为流动相,检测波长为240nm。
结果平均回收率为99.81%,RSD为1.30%。
结论本方法稳定、可靠、快速、准确,可以用于吲达帕胺片的含量测定。
关键词:吲达帕胺;HPLC;含量测定吲达帕胺片用于治疗高血压。
《中华人民共和国药典》采用紫外分光光度法测定其含量。
因紫外检测的专属性不强,故本文拟定了HPLC法测定其含量,并获得比较满意的效果。
1仪器与试药、试剂1.1 仪器日本岛津LC-10ATVP 高效液相色谱仪,SPD-10ATVP紫外检测器,AnaStar色谱工作站,Sartorius电子天平(BP211D)。
1.2 试药、试剂吲达帕胺片(1、新疆哈密戈泉药业有限责任公司,批号:20061127;2、上海华中药业有限公司,批号:061202;3、天津力生制药股份有限公司,批号:0701014;4、山西亚宝药业集团股份有限公司,批号:060103;5、山东方明药业股份有限公司,批号:060528;6、东莞万成制药有限公司,批号:20070107)吲达帕胺对照品(中国药品生物制品检定所,批号100257-200002)冰醋酸为分析纯;甲醇为色谱纯;重蒸馏水自制。
2方法与结果2.1 色谱条件色谱柱:C18、4.6*150mm;流动相:甲醇-水-冰醋酸(45:5:0.1);检测波长:240nm;流速:0.8ml/min;理论塔板数按吲达帕胺峰计不低于2500。
2.2 对照品溶液的制备精密称取吲达帕胺对照品(105℃干燥2小时)约20mg,置100ml量瓶中,加甲醇5ml溶解,用流动相稀释至刻度,摇匀,备用。
2.3 供试品溶液的制备取本品20片,精密称定,研细,精密称取适量(约相当于吲达帕胺20mg),置100ml量瓶中,加甲醇5ml,充分振摇使吲达帕胺溶解,加流动相稀释至刻度,摇匀,滤过,精密量取续滤液10ml置50ml量瓶中,加流动相稀释至刻度,作为供试品溶液。
吲达帕胺氨氯地平缓释片含量测定的研究

吲达帕胺氨氯地平缓释片含量测定的研究徐万升【摘要】目的:建立吲达帕胺氨氯地平缓释片中吲达帕胺的含量测定方法。
方法:采用高效液相色谱法,Nucleosil C18(150×4.6mm,5滋m);流动相:水-乙腈-异丁醇-三乙胺-十二烷基硫酸钠溶液,用磷酸调节pH值至2.5;柱温:35℃;检测波长:242nm;流速:1.2ml· min-1;进样量:20μl。
结果:HPLC能准确测定吲达帕胺的含量,测得吲达帕胺的线性范围为15.28~152.84μg·mL-1,R=0.99995;平均回收率为99.74%,RSD(%)=0.18%。
结论:该方法准确、灵敏,能有效控制吲达帕胺氨氯地平缓释片的质量。
【期刊名称】《黑龙江科技信息》【年(卷),期】2016(000)012【总页数】1页(P74-74)【关键词】吲达帕胺氨氯地平缓释片;HPLC;吲达帕胺【作者】徐万升【作者单位】黑龙江省边防总队医院,黑龙江哈尔滨 150000【正文语种】中文吲达帕胺氨氯地平缓释片为吲达帕胺和氨氯地平的复方制剂,为治疗原发性高血压的药物。
按照化学药品制剂的研究要求,结合本品的理化性质,参考进口药品注册标准,选用高效液相色谱法进行测定研究。
具体实验内容如下:吲达帕胺对照品:中检所,批号:100257-200903,含量:99.7%;乙腈、异丁醇、三乙胺、十二烷基硫酸钠为色谱纯,其他试剂为分析纯,水为去离子水;吲达帕胺氨氯地平缓释片:市售样品(批号:20140901、20140902、20140903,规格:2.0mg)。
仪器:Waters2695,二极管阵列检测器;色谱柱:Nucleosil C18 (150×4.6mm,5μm);流动相:水-乙腈-异丁醇-三乙胺-十二烷基硫酸钠溶液,用磷酸调节pH值至2.5;柱温:35℃;检测波长:242nm;流速:1.2ml·min-1;进样量:20μl。
高效液相色谱法测定吲达帕胺的含量及其有关物质的研究

高效液相色谱法测定吲达帕胺的含量及其有关物质的研究胡雅斐;沈元永;高永贵
【期刊名称】《药物分析杂志》
【年(卷),期】1998(0)S1
【总页数】2页(P167-168)
【关键词】吲达帕胺;有关物质;高效液相;色谱法测定;乙酰苯胺;流动相;中间体;原料药;保留时间;归一法
【作者】胡雅斐;沈元永;高永贵
【作者单位】天津市药品检验所;天津医科大学药学院
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.高效液相色谱法测定吲达帕胺片的含量和含量均匀度 [J], 罗亚虹;陈莹;周颖
2.高效液相色谱法测定吲达帕胺肠溶微球的含量 [J], 赵智卉;罗斌华;丁红;范博;阎志飞
3.高效液相色谱法测定吲达帕胺缓释片含量 [J], 冷晓燕;刘向红;许靖
4.高效液相色谱法测定吲达帕胺肠溶微球的含量分析 [J], 谭汉添
5.高效液相色谱法测定吲达帕胺肠溶微球的含量分析 [J], 谭汉添
因版权原因,仅展示原文概要,查看原文内容请购买。
吲达帕胺片含量测定方法改进研究

吲达帕胺片含量测定方法改进研究王洪萍;郑婷婷;王芝;曾凡明【期刊名称】《中国药业》【年(卷),期】2017(026)018【摘要】目的对吲达帕胺片的含量测定方法进行研究,找出分析方法的关键控制点.方法按照2015年版《中国药典(二部)》吲达帕胺片含量测定方法,将吲达帕胺片研细后的粉末全部过6号筛,加乙醇适量,水浴加热溶解一定时间,按紫外-可见分光光度法[2015年版《中国药典(四部)》(通则0401)],在242 nm波长处测定吸光度.结果吲达帕胺片的含量在90.0%~110.0%之间,符合《中国药典》的要求.结论经过改进的测定方法能确保在不同实验室、不同型号的仪器,以及不同分析人员等影响因素下,始终能准确地检测出吲达帕胺片的含量.%Objective To study the method for content determination of Indapamide Tablets,and to find out the critical point control of analytical methods. Methods According to the method of China Pharmacopoeia(2015 Edition,Volume Ⅱ)to determine the content of Indapamide Tablets,the porphyrization powder of Indapamide Tablets was over the No. 6 sieve,the right amount of alcohol was added and heated up in water bath for a certain time. Absorbance was measured at the wavelength of 242 nm by ultraviolet-visible spec-trophotometry of China Pharmacopoeia(2015 Edition,Volume Ⅳ,General 0401). Results The content of Indapamide Tablets ranged from 90. 0% to 110. 0%,which was in accordance with the requirements of Chinese Pharmacopoeia. Conclusion The improved method can always accurately determine thecontent of Indapamide Tablets in influence factor of different laboratories,different types of instru-ments and different analysts.【总页数】4页(P11-14)【作者】王洪萍;郑婷婷;王芝;曾凡明【作者单位】远大医药<中国>有限公司,湖北武汉 430040;远大医药<中国>有限公司,湖北武汉 430040;远大医药<中国>有限公司,湖北武汉 430040;远大医药<中国>有限公司,湖北武汉 430040【正文语种】中文【中图分类】R927.2;R972+.4【相关文献】1.含硫铁矿石中全铁含量测定方法的改进研究 [J], 王越蕾2.含硫铁矿石中全铁含量测定方法的改进研究 [J], 王越蕾3.水稻赖氨酸含量测定方法改进及其最优动态分类研究 [J], 陈庭木;李景芳;邢运高;徐波;王宝祥;徐大勇4.知柏地黄丸含量测定方法改进研究 [J], 张晓萍;朱仁愿;戚鹏飞;李志俊5.替米考星含量测定方法的改进研究 [J], 王轩;杨秀玉;韩宁宁;戴青;汪霞;赵晖因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高校液相色谱法测定吲达帕胺片的含量石家庄杏林锐步医药科技股份有限公司河北石家庄050000
摘要:目前,吲达帕胺片质量标准已收载入中国药典2020年版二部中,其含
量测定采用紫外分光光度法。
本文主要论述采用高效液相色谱法测定吲达帕胺片
的含量。
用十八烷基硅烷键合硅胶为填充剂(Agilent ZORBAX SB-C18,
4.6mm×150mm,5µm);以0.1%磷酸水溶液-乙腈-甲醇(60:30:10)为流动相;
柱温25℃;流速为每分钟1.5ml;检测波长240nm。
关键词:高效液相色谱法;吲达帕胺;含量测定;
吲达帕胺为磺胺类利尿药,临床上主要用于治疗原发性高血压。
目前,吲达帕胺片质量标准已收载入中国药典2020年版二部、国外药典(USP、BP、JP)中。
ChP2020吲达帕胺片的含量测定分析方法为紫外分光光度法,USP、BP、JP中采用的为高校液相色谱法。
优先考虑专属性好、灵敏度高的HPLC 法。
考虑USP、BP的含量测定中均采用离子对试剂作为流动相,而JP中选择0.1%磷酸溶液-乙腈-甲醇(6:3:1)作为流动相,成分简单,且易于冲洗,我们选择
在JP基础上建立吲达帕胺片的含量测定分析方法。
一、主要仪器与试剂
高效液相色谱仪、分析天平、超声波清洗仪。
水、乙腈(色谱纯)、甲醇
(色谱纯)、磷酸、无水乙醇、吲达帕胺对照品。
二、分析方法建立
1.流动相及色谱柱的确认
参考JP中吲达帕胺片质量标准,我们选择十八烷基硅烷键合硅胶为填充剂,经筛选,以Agilent ZORBAX SB-C18(4.6mm×150mm,5µm)作为色谱柱;并采用JP中的流动相0.1%磷酸溶液-乙腈-甲醇(6:3:1)。
1.检测波长的选择
根据吲达帕胺对照品的全波长扫描图谱,吲达帕胺在208nm、240nm附近均有吸收,但208nm波长较低,考虑到空白辅料可能带来的干扰以及紫外灯寿命问题,选定本方法的检测波长为240nm。
1.流速的选择
参照JP吲达帕胺片质量标准,在柱温30℃条件下,分别设置流速为每分钟1.5 ml、1.8ml,采集色谱图,其主峰保留时间依次为5.9min、4.9min,均可,我们选择1.5ml/min作为本方法的流速。
1.柱温的选择
筛选不同柱温:25℃、30℃、35℃、40℃。
结果发现各温度条件下理论板数与对称因子未有显著变化,但柱温高于30℃时,主峰前未知杂质与主峰无法达到分离,因此选定本方法的柱温为分离效果更好的25℃。
1.进样浓度的选择
分别配制浓度为10μg/ml、25μg/ml供试品溶液进行含量测定,两个浓度的样品含量依次101.2%、99.7%,基本一致;对称因子与理论板数无显著差别,但浓度为10μg/ml时信噪比仅为737.6,远低于2000,因此本方法样品浓度选用25μg/ml。
1.进样体积的选择
考察进样体积为10μl、20μl及50μl。
进样体积50μl时,理论板数显著降低;进样体积10μl和20μl时的信噪比均大于2000,符合要求,但进样体积10μl时理论板数较高,因此本方法选择进样体积为10μl。
1.最终确定的分析方法
色谱条件用十八烷基硅烷键合硅胶为填充剂(Agilent ZORBAX SB-C18,4.6×150mm,5µm,或效能相当的色谱柱);以0.1%磷酸水溶液-乙腈-甲醇(60:30:10)为流动相;柱温25℃;流速为每分钟1.5ml;检测波长240nm。
供试品配制取本品20片,精密称定,研细,精密称取细粉适量(相当于
吲达帕胺2.5mg),置100ml量瓶中,加溶剂适量,振摇超声至少30min使溶解,用溶剂稀释至刻度,摇匀,经0.45μm有机针式过滤器滤过,取续滤液,即得。
对照品溶液:取吲达帕胺对照品适量,精密称定,加50%乙醇溶解并稀释制
成每l ml中约含25µg的溶液。
三、分析方法验证
1.系统适用性
取对照品溶液,连续进样6针,吲达帕胺峰面积的相对标准差为0.1%,小于2%。
系统适用性良好。
2.专属性
经酸、碱、氧化、高温、高湿、光照破坏后,空白溶液、空白辅料在吲达帕
胺主峰位置均无干扰;降解产物峰与主峰之间的分离度介于1.07~25.15,符合
要求;以二极管阵列检测器检测主峰纯度,角度均小于阈值,符合要求。
专属性
良好。
3.线性与范围
配制不同浓度(40%、50%、60%、75%、125%、100%、150%)的对照品溶液,
测定,得出回归方程为y=0.3804x-0.0144,R2为0.9998,线性良好。
图1 吲达帕胺线性关系图
4.准确度
配制80%、100%、120%浓度的加标溶液,每个浓度平行配制3份,进行测定。
平均回收率为100.1%,RSD(n=9)为0.6%,准确度较高。
5.精密度
由不同操作者分别在不同日期使用不同仪器,配制6份供试品溶液,并测定。
RSD=0.9%、0.6%(n=6),RSD=0.8%(n=12)。
精密度良好。
6.耐用性
该方法在流动相中磷酸水溶液比例(±5%)、乙腈比例(±5%)、甲醇比例(±3%)、配制磷酸水溶液磷酸加入量(±0.2ml)、柱温(±5℃)、波长
(±5nm)、流速(±20%)及同一厂家同一型号不同批号色谱柱各条件变化之后,吲达帕胺片的含量测定RSD 为 0.8%,测定结果均在 94%~96%之间,符合规定,
耐用性良好。
四、总结
综上所述,根据《化学药物质量控制分析方法验证技术指导原则》及相关指
导原则,对建立的吲达帕胺片含量测定方法,从专属性、线性与范围、精密度、
准确度、耐用性等方面进行方法学验证,结果表明:本方法专属性好、精密度好、准确度高、线性良好、耐用性好,适用于吲达帕胺片含量测定。
参考文献:
[1]国家药典委员会.中华人民共和国药典2020年版二部.中国医药科技出
版社,2020.05:589.
[2]国家药典委员会.中华人民共和国药典2020年版四部.中国医药科技出
版社,2020.05:480-483.
[3]课题研究组.化学药物质量控制分析方法验证技术指导原则. 2005.03:1-13.
[4]JP18:1049-1050.
[5]USP40:115-116.
[6]BP2018.。
