糖类化合物
糖类化合物

环糊精
O
CH2OH O OH HO
O
HOCH2 HO O HO O OH HOH2C O HO O
环糊精( 环糊精(CD) 通常由6、 、 个 通常由 、7、8个 OH 葡萄糖单元环合 O CH2OH 而成,分别称为 HO 而成, α-、 β和r-CD。 、 。 O 许多有机反应底 OH 物可以嵌入其空 O 腔中进行位置选 OH CH2OH 择反应。
三、糖类化合物的命名
分类( 分类(Classifications) )
糖
低聚糖(寡糖) 低聚糖(寡糖) 麦芽糖 蔗糖 单糖 多糖 淀粉 纤维素 其它
aldose 醛糖
ketose 酮糖
triose tetrose pentose hexose 丙糖 丁糖 戊糖 己糖
l
二、单糖的结构 1、 单糖的构造式的确定 、
动物 物 ,为 供能
碱性弱氧化剂: 碱性弱氧化剂:
•Tollens试剂: [Ag(NH3)2+]OH-(氨水过量) 试剂: 氨水过量) 试剂 •Benedict试剂:CuSO4+柠檬酸 试剂: 柠檬酸+Na2CO3(蓝色) 蓝色) 试剂 柠檬酸 •Fehling试剂: CuSO4+酒石酸钾钠 试剂: 酒石酸钾钠+NaOH(蓝色) 试剂 酒石酸钾钠 (蓝色)
纤维素经上述处理后的再生纤维素, 纤维素经上述处理后的再生纤维素,其长纤维 称做人造丝,供纺织和针织用;其短纤维称人造棉, 称做人造丝,供纺织和针织用;其短纤维称人造棉, 供纯纺或混纺用。 供纯纺或混纺用。
乙、纤维素酯
(CH3CO)2O
C 2O H H O H O O H n O
H2SO4
C 2O O H H C C 3 O O HC O 3 C O O O H C C 3
有机化学_第14章糖类化合物

HOH2C HO HO
4
O OH
1
OH
β-D-(+)-吡喃葡萄糖的构象中,体积大的取代基-OH和CH2OH,都在 键;而在α-D-(+)-吡喃葡萄糖中有一个-OH在a键上。故β型的构象更 稳定,因而在平衡体系中的含量多于α-D-(+)-吡喃葡萄糖。 所有的 D-吡喃己醛糖的优势构象为4C1 型椅式构象。 因此β-D-葡萄糖在自然界有最广泛的存在 !
第二节
单糖
1、根据分子中所含碳的个数,单糖可分为己糖、戊糖等。 2、分子中含醛基的糖称为醛糖,含有酮基的糖称为酮糖。 例:
CHO 2 CHOH
3 4 1 1 2 3 4
CH2OH C=O CHOH CHO 2 CHOH
3 4 1
CHOH
CHOH 5 CHOH 6 CH2OH
己醛糖 4个* C
16个对映异构
5、脱水及显色反应
了解
单糖与醇一样在浓酸的作用下可发生分子内的脱水反应生 成α-呋喃甲醛(也称糠醛)类化合物
呋喃甲醛类化合物可以和酚或芳胺类缩合,生成有色化 合物,经常用于糖类的鉴定
莫利胥反应 (了解):
所有糖
浓H2SO4 α-萘酚
紫色或紫红色
阴性反应是糖类化合物肯定不存在的确证, 而阳性反应则不一定说明含有糖类化合物
变旋现象 由变旋现象说明,单糖并不仅仅以开链式存在 ,还有其它的存在形式。 1925-1930年,由X射线等现代物理方法证明,葡萄糖主要 以氧环式(环状半缩醛结构)存在。
1.氧环式结构
六元氧环(吡喃型)
H 1 OH C O
5
H
1C
O
HO 1 H C O
OH
5
α-D-(+)-吡喃葡萄糖
糖类化合物

黄色晶体
R
除C1和C2外,其余相同的化合物得相同的糖脎
6. 环状缩醛和缩酮的形成
处于糖环上的顺式邻二醇可与醛或酮生成环状的缩醛或缩酮,常用于某些
合成反应中保护糖上的羟基。C1和C6的羟基也可分别与C2与C4的羟基发生 类似反应,反式邻二醇不反应。
H 3C H2SO4 H 3C O O O H3C CH3 C6 H 5 O H OCH3 -D-葡萄糖甲甙 + C6H5CHO H
R=H 或CH2OH R' =分子其余部分
果糖是2-羰基酮糖,本身不具有能被氧化的醛基,但因在试剂的碱性条件 下可异构成醛糖,因此也发生正反应:
还原糖:能发生上述氧化反应的糖 非还原糖:不反应的称为
(2)与溴水的反应: 溴(或其它卤素)的水溶液可很快地与醛糖反应,选择性地将其醛基氧化成羧基, 先生成醛糖酸,然后很快生成内酯。
+
OH O H OH -D-半乳糖
O
O + 2 CH3CCH3
OH O H
OH
O O H OCH3
H
O
第二节 寡糖和多糖 寡糖是水解后能生成2~9个单糖的化合物 一、双 糖 双糖的苷键有两种形式:
糖基 配基或苷元
O OH OO H 氧苷键 氧苷(尿兰母, 存在于静兰植物中) NH OH OS H 硫苷键 硫苷(黑芥子甙) H 氮苷键 CH2CH CH2 N OSO3K HO HN O O N CH3 HO HN O O
O HN
H 碳苷键 碳苷 (伪尿嘧啶核苷)
氮苷(脱氧胸苷)
• 糖苷中已无半缩醛(酮)羟基,不能转变为开链的结构 • 糖苷无变旋现象,也无还原性。
③ D-葡萄糖:IR:无羰基峰;NMR:无醛基氢(H—CO—)
第十九章 糖类化合物

H HO HO H H
OH O H H OH OH
β -D-葡萄糖构象
α -D-葡萄糖构象
ห้องสมุดไป่ตู้
从两种异构体的构象可以看出在-D-葡萄糖构 象中所有大基团都处于 e 键,所以这是 D-(+)-葡 萄糖的最稳定构象。
4.变旋光现象的解释
α -D-葡萄糖的比旋光度为+112°, -D-葡萄 β 糖的比旋光度为+19°,在常温下用水或乙醇结晶 的葡萄糖的 m.p.为 146℃,主要是α -异构体, 20 新 配 制 的 水 溶 液 D +112°,在高温下用 CH3COOH 或吡啶结晶的葡 20 D 萄糖的 m.p.为 150℃,主要是β -异构体,所以 新配制的水溶液+19°,以上两种葡萄糖溶液经放 置达到平衡后其比旋光度都是+52°,这种现象称 做变旋现象。
CHO HO HO H H H H OH OH CH2OH
CHO H HO H H OH H OH OH CH2OH
D-(+)-葡萄糖 D-(+)-甘露糖 象这样的两种立体异构体称差向异构体, 这种现象称为 差向异构现象。
几点说明:
①D、L只表示单糖的相对构型与甘油醛的关 系,与旋光方向无关。 ②自然界中存在的糖都是D型,L型多为人工 合成的。 ③1951年,用X射线衍射法证明,单糖的真实 构型正好同原来规定的相对构型一致。
有一个手性碳原子的构型相反,其他手性碳原子构型完全相同 的异构体,称为差向异构体。 差向异构化:含多个手性碳原子的化合物,通过化学反应 ,使其中一个手性碳原子转变为其相反构型过程。
单糖在碱性溶液中会发生差向异构化反应,反应过 程是在碱性溶液中羰基发生烯醇化,通过烯醇式中间 体和其差向异构体达成平衡。
糖类化合物的正确定义

糖类化合物的正确定义1. 引言糖类化合物是一类重要的有机化合物,它们在生物体内起着多种重要的生理功能。
本文将对糖类化合物进行正确定义,并介绍其结构、分类、性质和生理功能等方面的内容。
2. 糖类化合物的定义糖类化合物是指由碳、氢和氧三种元素组成的有机化合物,其分子结构中含有一个或多个羟基(-OH)与一个或多个醛基(-CHO)或酮基(-C=O)相连。
糖类化合物包括单糖、双糖、寡糖和多糖等不同类型。
3. 糖类化合物的结构糖类化合物的分子结构通常以环式结构存在。
单糖分子可以存在于直链式或环式,其中环式又可分为六元环和五元环两种形式。
葡萄糖是一种六元环的单糖,而果糖则是一种五元环的单糖。
4. 糖类化合物的分类根据单糖分子中所含有的羟基个数,可以将单糖分为三种类型:三羟酮糖、二羟醛糖和多羟醛糖。
三羟酮糖是指含有一个酮基和三个羟基的单糖,如葡萄糖;二羟醛糖是指含有一个醛基和两个羟基的单糖,如果糖;多羟醛糖是指含有一个醛基和多个羟基的单糖,如戊糖。
另外,根据单糖分子中所含有的碳原子数目,可以将单糖分为五碳糖、六碳糖和其他碳数的糖类化合物。
五碳糖是指单糖分子中含有五个碳原子的化合物,如葡萄糖;六碳糖是指单糖分子中含有六个碳原子的化合物,如果糖。
5. 糖类化合物的性质5.1 溶解性大部分单糖在水中具有良好的溶解性。
葡萄糖在室温下可以完全溶解于水中形成透明溶液。
5.2 甜味许多单糖具有甜味,如葡萄糖、果糖等。
这是由于单糖分子的结构特点,使其能够与人类的甜味受体结合,从而产生甜味感受。
5.3 还原性单糖具有还原性,可以与一些氧化剂发生反应,并被氧化为相应的酸。
这是由于单糖分子中含有醛基或酮基,可以进行氧化反应。
6. 糖类化合物的生理功能6.1 能量供应作为生物体内重要的能量来源之一,糖类化合物可以通过新陈代谢过程转化为ATP (三磷酸腺苷),从而为细胞提供能量。
6.2 结构组成部分糖类化合物参与生物体内重要结构的形成。
糖类化合物名词解释

糖类化合物名词解释
糖类化合物是一类由多个碳原子和氢原子组成的有机物质,可以分为简单糖、复糖和非糖类物质三大类。
简单糖:又称单糖,它是一种由单个糖分子组成的糖类物质,主要包括葡萄糖、果糖、乳糖、半乳糖、麦芽糖、玉米糖、蔗糖、糖原等,其中葡萄糖、果糖和乳糖是人体最常摄入的三种糖类物质。
复糖:又称多重糖,在糖分子结构上比简单糖更复杂,可以分为淀粉、纤维素、凝胶聚糖、聚糖酶和环糊精等五大类。
淀粉是由多个葡萄糖分子链接而成的糖分子,是人体重要的热量来源;纤维素可以促进消化道的正常功能;凝胶聚糖是植物中的重要组成部分,有助于提高食物中的营养含量;聚糖酶是人体内分泌的一种肠道消化酶;环糊精是一种可以用作食品添加剂的复杂糖分子。
非糖类物质:它是糖原、淀粉和聚糖等糖类物质的一个分支,主要包括木糖醇、半乳糖苷、磷脂类、脂肪酸等,它们不像糖类物质那样可以直接被人体消化吸收,但是它们也是人体重要的营养物质。
糖类化合物

糖类化合物
糖类化合物又叫碳水化合物。
是自然界广泛存在的一类化合物,如淀粉、纤维素、蔗糖、葡萄糖等都属于糖类。
葡萄糖、麦芽糖、淀粉、纤维素等都叫碳水化合物(carbohydrate),它们都是由碳、氢和氧三种元素组成,而且其中的氢氧比和水一样,都是2:1,因此称为碳水化合物。
机体中碳水化合物的存在形式主要有三种,葡萄糖、糖原和含糖的复合物(淀粉、纤维素等)。
任何的碳水化合物在体内经过系列生化反应后最终都分解为糖(比如葡萄糖、果糖),又称为糖类。
糖类的主要功能是为机体提供生理活动和体力活动所需要的能量。
每克糖在体内可以产生4千卡的能量。
我们每天吃的食物中,碳水化合物的供能应该占55-65%。
虽然每天进食这么多的碳水化合物,但是直接储存在体内的只有1-2%,大部分都作为能量提供给机体活动。
糖类化合物

证明:分子中的碳链为一直链
(2)
C6H12O6
+ CH3COCl ( 过量) [or (CH3CO)2O] OH ,且分别连在五个碳原子上
五乙酸酯
证明:有五个
(3)
C6H12O6
NH2OH (or C6H5NHNH2) C= O 存在
肟(或腙)
证明:有
(4)
C6H12O6
Br2 H2O 弱氧化剂 or Tollens试剂 证明: 为 CHO
弱碱
HO H H
H OH OH CH2OH
弱碱
HO H H
D-葡萄糖
烯二醇
D-甘露糖
CH2OH O HO H H H OH OH CH2OH
D-果糖
第二节 单糖
四、单糖的化学性质
2. 氧化反应 (1)溴水氧化
H HO H H CHO OH H OH OH CH2OH Br2 H2O H HO H H COOH OH H OH OH CH2OH Br2 H2O CH2OH C O HO H H OH H OH CH2OH
第十五章
糖类化合物
主要内容
第一节 第二节 第三节 第四节 概述 单糖 寡糖(低聚糖) 多糖
第一节 概述
一、糖的定义和分类 • 糖类化合物是天然有机化合物,它 们对维持动植物的生命起着重要的 作用。 • 人类的遗憾——自身没有生产糖类 化合物的本领。 • 植物的骄傲——通过光合作用产生 糖类化合物。
~ 36 %
112。
~ 64 %
19。
第二节 单糖
三、单糖的环状结构
2. 环状结构 因为是δ- C上的-OH与-CHO缩合成环,故称δ氧环式。上式为Fischer投影式,其另一种表示方 法是用Haworth式来表示——即用六元环平面表 示氧环式各原子在空间的排布方式。
糖类化合物的定义

糖类化合物的定义糖类化合物是一类结构非常复杂的有机化合物,它们是有机物质的重要组成部分,包括多种不同类型的糖分子,如糖原、糖类多糖、糖酵素、糖苷和糖类混合物等。
它们不仅是有机生物体的能量来源,还可以作为许多其他应用的重要原料。
糖类化合物的化学定义是指一类具有多种糖分子结构的有机化合物,它们包括一个或多个糖类单体,它们可能是糖原、多糖、糖苷、糖酵素等不同类别的糖类分子,以及由它们构成的复杂大分子物质。
糖类化合物由各种不同的糖分子组成,其中糖原是最重要的,分子中存在着多个单糖(仅含一种单糖的分子称为非混合糖)和多种结构不同但具有相同糖基的混合糖,它们可能由碳水糖、葡萄糖、糖胺等单糖构成。
糖原是小分子的,体积小,溶解度好,并且可以通过酶的作用被渐渐分解和水解,从而提供能量。
糖类多糖是由多种糖基组合而构成的大分子化合物,它们不仅包括糖原,还包括许多其他常见的多糖,如植物多糖、细菌多糖、海洋多糖、真菌多糖、病毒多糖和胞外多糖等,不仅能提供有机物质的结构支持,还可以用于许多生物过程。
糖苷是由糖原和酸的氧化物酯反应而形成的,具有较高的分子量,有一个或多个糖基与一个或多个酸的酯基结合而形成糖苷分子,具有特定的染料性和芳香性。
糖苷大多以植物和微生物体内的糖原为原料,它们可以用于多种用途,如染料、抗菌剂等。
糖酵素是一类特殊的糖类化合物,它们是由蛋白质和糖类分子组成的复合物,具有特定的酶作用,可以进行特定的水解反应,如糖胺水解、蛋白质水解、淀粉水解等,可以加快生物代谢速度,对人类生活和工业生产有重要意义。
糖类混合物是一种由多种糖原混合而成的复合物,它们既能提供能量,又能提供抗癌和抗炎作用,并能作为营养补充剂等多种用途,混合物中有效成分的组成不同,应用于不同的领域。
总之,糖类化合物是一类具有复杂结构的有机化合物,它们包括糖原、糖类多糖、糖苷、糖酵素和糖类混合物等。
它们不仅是有机生物体的能量来源,还可以作为许多其他应用的重要原料,它们的化学反应性质也被广泛用于工业和医药领域,发挥着重要的作用。
大学本科有机化学40_糖类化合物

OH
Kiliani-Fischer醛糖碳链增长法 Kiliani-Fischer醛糖碳链增长法
♦ 与羟胺的加成及Wohl降解 与羟胺的加成及Wohl降解
CHO H HO H H OH H OH OH CH2OH H NH2OH HO H H AcO CH NOH OH H OH OH CH2OH C CH3ONa CH3OH H HO H H N O H H OH OH CH2OH OCH3 − CN HO H H 6 Ac2O NaOAc H C H AcO H H N OAc OAc H OAc OAc CH2OAc
互为差向异构体 可互变
互为差向异构体 不能互变
HO HO H
葡萄糖的六员环环状结构
CHO H HO H H OH H OH OH CH2OH H OH HO OH H H CH2OH H CHO OH a b CH2OH H O OH H H OH O H H OH H H OH OH CH2OH O H H H OH OH H CH2OH OH CHO H b H HO OH H OH a
HC NHNHPh C OH H OH OH CH2OH
CH2OH C O HO H H H OH OH CH2OH D−(−)−果糖 − CHO HO HO H H H H OH OH CH2OH D−(+)−甘露糖 − 3 PhNHNH2 HO H H 3 PhNHNH2 较慢 CH NNHPh
CN H HO H H OH H OH OH CH2OH (1) Ba(OH)2 (2) H3O+
CH2OH O H H OH H OH H OH + CH2OH HO HO OH HCHO H OH HO H H H O OH OH CH2OH D−(+)−葡萄糖 −
糖类化合物

需记住的糖
2 3 4 5*
1
C=O
6
*
*
*
*
D -葡萄糖 D -果糖 D-glucose D-fructose
D -甘露糖 D-mannose
D -半乳糖 D -核糖 D-galactose D-ribose
2. 单糖的环状结构
▲单糖的变旋现象(Mutarotation) D-葡萄糖
在低温乙醇溶液中结晶 在高温吡啶溶液中结晶 溶于水 溶于水 [α]= +112° [α]= +18.7°
左右翻转 180°
α-D-葡萄糖
旋转180°
如何辨别环状单糖的构型?
1.找半缩醛羟基 → 与氧相邻碳上的羟基 2.判断环碳排列方式 → 顺、逆时针 3.找尾基,判断D,L→顺,尾基在上,D 逆,尾基在上,L 4.判断α、β →尾基与半缩醛羟基同侧β 尾基与半缩醛羟基异侧α 5.写出糖的名称
练习:
戊醛糖
已酮糖
已醛糖
二、单糖的结构 ( Structure of monosaccharides ) (Structure monosaccharides)
1. 单糖的开链式结构
葡萄糖
H HO H H CHO OH H OH OH CH2OH
果糖
CH2OH C=O H HO H OH H OH CH2OH
α-D-甘露糖
HOH2C H
O H H
OH H
β-D-脱氧核糖
OH H H
H HOH2C
O OH H
CH2OH
OH H OH
OH OH HO β-L-果糖 OH H H O H α-D-葡萄糖 H CH2OH
(3)单糖的构象:
糖类 有机化合物

糖类有机化合物
糖类是一种有机化合物,也被称为碳水化合物。
它包括蔗糖、葡萄糖、果糖、半乳糖、乳糖、麦芽糖、淀粉等。
这些糖类在自然界中广泛存在,是一切生命体维持生命活动所需能量的主要来源。
糖类可根据能否水解以及水解的产物进一步分类,主要有单糖、二糖和多糖等。
其中,单糖是不能再被水解的糖,如葡萄糖、果糖和半乳糖等;二糖则是能水解生成两个单糖的糖,如蔗糖和麦芽糖;多糖则是能水解生成多个单糖的糖,如淀粉和纤维素等。
除了葡萄糖、果糖和半乳糖能被人体直接吸收外,其余的糖类在人体内需要转化为基本的单糖后才能被吸收利用。
例如,淀粉在口腔中被唾液淀粉酶水解成麦芽糖,然后进入小肠被麦芽糖酶进一步分解为葡萄糖而被身体吸收。
需要注意的是,含糖饮料中的糖主要是单糖,会快速被身体吸收。
这些被快速吸收的糖一旦无法及时消耗,可能会对身体带来负面影响,如增加罹患心脏病和糖尿病的风险等。
因此,保持适量的糖摄入和注意均衡饮食对于健康至关重要。
第十四章糖类化合物

五碳糖:
CHO H H H OH OH OH CH 2OH H H H CHO H OH OH CH 2 OH
D-核糖
D-2-脱氧核糖
氨基糖: 甲壳素 -D-2-氨基葡萄糖的高聚物
HOH 2C HO HO O NH2
OH
维生素C
CH 2OH C O NHNH 2 (过量)
HC
C
NNH NNH
果糖
果糖脎=葡萄糖脎
D-葡萄糖 苯肼 D-果糖 D-甘露糖
D-葡萄糖脎
糖脎都是不溶于水的亮黄色结晶体,不同的糖 脎具有不同的结晶形态和熔点,因此可用糖脎的 生成对糖进行鉴定。
四、苷的生成
苷是糖的环式结构中苷羟基的氢原子被烃基取代后 形成的产物,也叫配糖体。
1
H 2C HO
3C
H H5
HO H 4 H OH 3 H OH
H 4C
H, OH
H 5C OH
6CH2 OH
OH H CH 2OH
CH 2OH O OH OH OH
~ H, OH
CHO OH HO OH OH CH 2 OH
5 4 3 2 6
OH HOH 2C
6 5 4 3 2
CHO
1
OH OH
葡萄糖酸
酮糖不与溴水反应,可用溴水来区别醛糖和酮糖。
2、硝酸氧化
CHO (CHOH)4 CH 2OH
HNO 3 , H 2O 100℃
COOH (CHOH)4 COOH
葡萄糖二酸
应用:根据生成的糖二酸是否具有旋光性来推测 糖的构型
例: D-四碳糖
H H
HNO3
糖类化合物
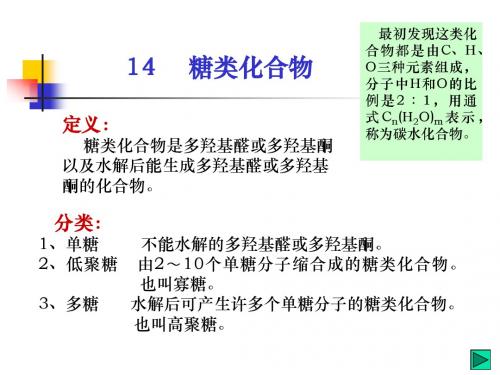
CH 2OH CHO
CH 2OH OH
α-D-葡萄糖
CHO
CH 2OH O OH H
β-D-葡萄糖
14 糖类化合物 果糖的Haworth式
HOH 2C H O CH 2OH OH
O CH2OH
α-D-呋喃果糖
HOH 2C H O OH CH 2OH
CH 2OH O
OH
α-D-吡喃果糖
O OH CH2OH
14
定义:
糖类化合物
糖类化合物是多羟基醛或多羟基酮 以及水解后能生成多羟基醛或多羟基 酮的化合物。
最初发现这类化 合物都是由C、H、 O三种元素组成, 分子中H和O的比 例是2∶1,用通 式 Cn(H2O)m 表 示 , 称为碳水化合物。
1、单糖 不能水解的多羟基醛或多羟基酮。 2、低聚糖 由2~10个单糖分子缩合成的糖类化合物。 也叫寡糖。 3、多糖 水解后可产生许多个单糖分子的糖类化合物。 也叫高聚糖。
H HO H H
CHO OH H OH OH CH2OH
D型糖
CH2OH C=O H HO H OH H OH CH2OH
自然界存在的单糖大多是D型糖。
14 糖类化合物
单糖的几种简写式:
HO CHO OH OH OH CH2OH CHO
CH2OH
CHO CHO HO H CH2OHL-(-)-甘源自醛CHOCH2OH O
CH2OH
CH2OH
CH2OH
L型糖
14 糖类化合物 D型糖与L型糖是对映体,根据D型糖可写出 相应的L型糖。 CHO CHO CHO CHO HO H OH H OH H HO H OH HO H OH CH 2OH CH 2OH CH 2OH CH 2OH L-葡萄糖 半乳糖
第14章 糖类化合物
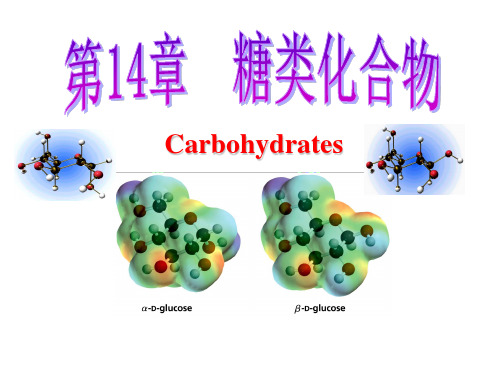
HO
H
HO
H
H
OH
H
OH
CH2OH
D甘露糖
CHO
H
OH
HO
H
HO
H
HO
H
CH2OH
L阿卓糖
CHO
H
OH
H
OH
HO
H
HO
H
CH2OH
L甘露糖
CHO
H
OH
H
OH
HO
H
H
OH
CH2OH
D古罗糖
CHO
HO
H
HO
H
H
OH
HO
H
CH2OH
L古罗糖
CHO
HO
H
H
OH
HO
H
H
OH
CH2OH
D艾杜糖
CHO
H
OH
HO
H
OH
H
CH2OH
β-L-半乳糖
α-D-阿洛糖
β-L-艾杜糖
β-D-甘露糖
(三)单糖的哈沃斯式环状结构式 (Haworth)透视式
平面环状式(台面式)(H-透视式)
CH2OH
H
OH
H
OH H
OH
OH
H OH
α-D-(+)-吡喃葡萄糖
CH2OH
H
O OH
H
OH H
OH
H
H OH
β-D-(+)-吡喃葡萄糖
[α]= -21°
CH2OH O
HO
H
H
OH
H
OH
CH2OH
D-(-)-果糖
开链式
糖类化合物

化学教研室
有机化学
• 第一节:单糖 • 第二节:双糖 • 第三节:多糖
化学教研室
有机化学
第一节 单糖
单糖可分为醛糖和酮糖,也可以根据分子中碳原子的多少,可 分为丙糖、丁糖、戊糖、己糖。这两种分类命名的方法一般都 合并使用
单糖中最常见的是葡萄糖和果糖。这两种糖从结构和性质上 都可以作为各种单糖的代表。
三、糖原
糖原是动物体内的储备糖,就像淀粉是植物的储备糖一样, 所以又称为动物淀粉。以肝脏和肌肉中含量最大,因而也叫肝 糖。它是无定形粉末,比较容易溶解在热水中,不成糊状,而 成胶体溶液。分子量可达1亿。
化学教研室
有机化学
化学教研室
化学教研室
有机化学
2、环的大小 3、环状构型的表示方法 通常表示方法有两种:一种 是直立环状投影式,如D-葡萄糖半缩醛式。另一种 是是用透视式即哈武斯式。
4、α 型和β 型 D-葡萄糖形成了半缩醛式的环状结构 后,后来醛基的第一个碳原子变成了手性碳原子, 所以就有两种构型。
化学教研室
有机化学
六、重要的糖
化学教研室
有机化学 2、还原糖和非还原糖:
能被Tollen试剂或Fehling试剂氧化的糖叫还原糖。 反之叫非还原糖。所有的单糖都是还原糖;所有的多 糖都是非还原糖;部分双糖是还原糖,部分双糖是非 还原糖。
二、几种重要的双糖
麦 芽 糖 纤 维 食 品
化学教研室
有机化学
名称 性质 是甘蔗和甜菜的主要成分。为无色结晶体。易溶 于水。是非还原糖。水解得一分子葡萄糖和一分 子果糖 是纤维素的结构单位。有还原性。水解得两分子 葡萄糖。与麦芽糖相比,只是麦芽糖以α —苷键 相连,纤维二糖以β —苷键相连。 。
第十五章糖类化合物

*
H*
*
* *O
* H*
CH2OH
CH2OH
CH2OH
-D-(+)-葡萄糖 (~36%)
D-(+)-葡萄糖开链结构 -D-(+)-葡萄糖
(微量)
(~64%)
上述环状结构的表示方式称做直立氧环(或氧桥)式。
根据半缩醛羟基与决定构型的羟基 (氧环)的关系
-型——同侧
-型——异侧
-D-葡萄糖和-D-葡萄糖是一对非对映异构体。 像-D-葡萄糖和-D-葡萄糖那样,仅C1构型不相 同的一对非对映异构体,称做异头物或端基异构 体(anomers)。
.............................. ..............................
CH2OH
CH2OH
CH2OH
...............................................................................................................................
CH2OH
H
O
H OH H
HO
CH2OH
H
H
O
CH3OH 干HCl
H OH H
OH
H2O HO
H OH
H OH
H O CH3
-苷键
-D-吡喃葡萄糖
-D-甲基吡喃葡萄糖苷
CH2OH
CH2OH
H H OH
O OH
干HCl
H
CH3OH H2O
H H OH
O H
HO
H
HO
H OH
H OH
糖类化合物

2.氧化作用
• 所有单糖都能被弱氧化剂氧化。 如: 吐伦试剂、费林溶液和本尼迪特试剂 •D-葡萄糖与溴水反应,醛基就被氧化为羧基 而生成D-葡萄糖酸。酮糖在此条件下不反应, 因此可用溴水来区别醛糖和酮糖。 •较强氧化剂(如稀硝酸)氧化时,单糖碳链上的 羟甲基也被氧化为羧基,生成糖二酸。
第一节 单糖
•苷由糖和非糖部分组成。非糖部分叫做糖苷 配基(aglycone)。糖和糖苷配基脱水后一般通 过“氧桥”连接,这种键称为苷键 (glycosidic bond)。 •α-苷键,β-苷键
第一节 单糖
(二)化学性质
5.酯化作用
第一节 单糖
三、重要的单糖及其衍生物
(一)D-(-)-核糖和D-(-)-2-脱氧核糖 (二)D-(+)-葡萄糖 (三)D-(+)-半乳糖 (四)D-(-)-果糖 (五)氨基糖
(a)
HO C H (c) ( a ) C OH HO H OH H H OH CH2OH ( 烯二醇) (c) CH2OH C O H H O H H O CH2O D-果 糖 (31%)
HO ( b ) HO H H
CHO H H OH OH CH2OH D-甘露糖 (5%)
第一节 单糖
(二)化学性质
1
OH a H
e
OH
β -D- 吡喃葡萄糖
第一节 单糖
3. 哈沃斯 (Haworth)式和构象式
CH2OH C HO H H O H OH OH CH2OH
HO HO H
6
2
1
6
C C C C
CH2 OH H OH H O
HOH2C
5
O H
4
OH
2
第十五章 糖类化合物 - 复制

D-葡萄糖 葡萄糖
烯二醇
CH2OH O HO H H OH H OH CH2OH
D-甘露糖 甘露糖
D-果糖 果糖
(三) 成脎反应(不做要求) 三 成脎反应(不做要求) 醛糖或酮糖可与过量苯肼反应生成二苯腙, 醛糖或酮糖可与过量苯肼反应生成二苯腙 , 糖的 二苯腙称做糖脎(Osazone)——黄色晶体 二苯腙称做糖脎
(二) 在稀碱溶液中的异构化反应 二 用稀碱处理D-葡萄糖 葡萄糖、 果糖或 果糖或D-甘露糖中的任何 用稀碱处理 葡萄糖、D-果糖或 甘露糖中的任何 一种,都将得到这3种糖的混合物 种糖的混合物。 一种,都将得到这 种糖的混合物。
H C H HO H H OH H OH OH CH2OH O H C C OH HO H H OH H OH CH2OH OH H C HO HO H H H H OH OH CH2OH O
D− 果糖在溶液中 , 既可生成 α 和 β 两种 吡喃 − 果糖在溶液中, 既可生成α 两种吡喃 果糖,也可生成α 两种呋喃型糖 呋喃型糖. 型果糖,也可生成α和β两种呋喃型糖.
请写出D-核糖及D-2-脱氧核糖的Haworth式.
CHO H———OH H———OH H———OH CH2OH
DD-核糖
CH2OH C O C O
CH2OH
(-)- 果糖 (fructose,F)
(-)-果糖 3以下各手性碳原子的构型 果糖C 果糖 葡萄糖的完全一样。 与(+)-葡萄糖的完全一样。 + 葡萄糖的完全一样
CH2OH C O HO C H H C OH H C OH CH2OH
CH2OH C O H C OH HO C H H C OH CH2OH
CH2OH C O H C OH H C OH CH2OH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十六章糖类化合物一、本章的要点碳水化合物指多羟基醛或多羟基酮,以及它们的脱水缩合物和衍生物。
1、单糖单糖是最重要的糖,也是其他糖的基本结构单位。
根据分子中碳原子数目分为:丙糖、丁糖、戊糖、己糖等。
根据羰基的位置不同分为:醛糖、酮糖。
单糖的构型和标记法相对构型:规定了以甘油醛为标准,其他的单糖与甘油醛比较,如编号最大的手性碳原子的构型与D-甘油醛相同,就属D型,反之为L型。
注意:① D、L只表示单糖的相对构型与甘油醛的关系,与旋光方向无关。
②自然界中存在的糖都是D型,L型多为人工合成的。
构型的表示和标记方法构型的表示:常用费歇尔投影式表示糖的构型,可以做一些简化。
构型的绝对标记:用R/S标记出每一个手性碳原子的构型,但较为复杂。
(2)单糖的氧环式结构单糖溶液存在变旋现象。
糖的结构不是开链式的,而是形成环状半缩醛结构,且都是以五元或六元环的形式存在。
用Haworth透视式能比较真实的表现糖的氧环式结构。
注意:①α型—生成的半缩醛羟基与C5上的羟甲基处于环的两侧;β构型—生成的半缩醛羟基与C5上的羟甲基处于环的同侧。
②α-型糖与β-型糖是一对非对映体,α-型与β-型的不同在C1的构型上故有称为端基异构体和异头物。
③六元环的又称为吡喃糖,五元环的又称为呋喃糖。
(3)单糖的构象吡喃型葡萄糖的半缩醛环具有椅式构象。
在溶液中α-型和β-型可以通过开链式相互转化。
β-葡萄糖的构象中,所有大基团都处于e键,所以比α-葡萄糖稳定。
(4)单糖的化学性质氧化Tolling试剂、Fehling试剂和Benedict试剂能被这些氧化剂氧化的糖称为还原糖,否则为非还原糖。
酮糖也能被Tolling试剂、Fehling试剂或Benedict试剂氧化。
酮糖如果糖在稀碱溶液中可发生酮式-烯醇式互变,酮基不断地变成醛基(Tolling试剂、Fehling试剂和Benedict试剂都是碱性试剂)—差向异构化作用,所以酮糖也能被氧化。
溴水溴水能氧化醛糖,但不能氧化酮糖,因为酸性条件下,不会引起糖分子的异构化作用。
可用此反应来区别醛糖和酮糖。
硝酸稀硝酸的氧化作用比溴水强,能使醛糖氧化成糖二酸。
稀硝酸氧化酮糖时导致C1-C2键断裂。
高碘酸高碘酸氧化,碳碳键发生断裂。
反应是定量的,每破裂一个碳碳键消耗一摩尔高碘酸。
因此,此反应是研究糖类结构的重要手段之一。
还原脎的生成一分子糖和三分子苯肼反应,在糖的1,2-位形成二苯腙(称为脎)的反应称为成脎反应。
注意:①生成糖脎的反应是发生在C1和C2上,不涉及其它碳原子,对于差向异构体,则生成同一个脎。
例如,D-葡萄糖、D-甘露糖、D-果糖的C3、C4、C5的构型都相同,它们生成同一个糖脎。
不同。
因此,可根据糖脎的晶型和生成的时间来鉴别糖。
苷的生成单糖的半缩醛羟基与另一分子中的羟基、氨基或硫羟基等失水而产生的化合物称糖苷,也称配糖物。
(用甲醇的干燥盐酸反应发生缩醛反应,生成缩醛)糖苷是缩醛或缩酮,在水溶液中不再能转变为开链式。
在碱性条件下是稳定的,但在温和的酸性条件下水解。
酶也能促使糖苷水解,而且是立体专一的。
醚的生成在酸催化下,只有糖的半缩醛羟基能与另一分子醇反应形成苷键。
但用Williamson反应可使糖上所有的羟基(包括半缩醛的羟基)形成醚。
最常用的甲基化试剂是:30% NaOH+(CH3)2SO4或Ag2O+CH3I。
醇羟基形成的醚键在温和的酸性条件下是稳定的,只有在强的HX作用下才分解。
酯的生成(CH3CO)2O吡啶CH3CH33(5)脱氧糖单糖分子中的羟基脱去氧原子后的多羟基醛或多羟基酮。
(6)氨基糖氨基代替糖分子中的羟基而成的。
广泛存在于自然界中。
2、二糖水解后产生两分子单糖的低聚糖称为双糖。
双糖中两个单糖分子有两种可能的连接方式:①一分子单糖以半缩醛羟基和另一分子单糖的其他羟基缩合。
此种双糖有半缩醛羟基,具有还原性、变旋现象等。
②两个半缩醛羟基相互结合生成缩醛。
此种双糖没有半缩醛羟基,不具有还原性、变旋现象等。
(1)蔗糖蔗糖是非还原性双糖。
(2)麦芽糖麦芽糖是还原性双糖。
(3)纤维二糖纤维二糖是还原性双糖。
3、多糖多糖是重要的天然高分子化合物,是由单糖通过苷键连接而成的高聚体。
多糖无还原性,无变旋光现象,无甜味,大多难溶于水,有的能和水形成胶体溶液。
(1)淀粉淀粉的改性环糊精(2)纤维素粘胶纤维纤维素酯纤维素醚二、例题例1、①下列糖类物质不能发生银镜反应的是()A. D-葡萄糖B. D-果糖C. 麦芽糖D. 蔗糖分析:①只有蔗糖是非还原性糖。
②硝酸可把醛糖氧化成二酸。
解答:① D ② HNO3例2、写出D-(+)-甘露糖与下列物质的反应。
(1)羟胺(2)苯肼(3)溴水(4)HNO3(5)HIO4(6)NaBH4(7)CH3OH/HCl(生成缩醛),然后(CH3)2SO4/NaOH (8)苯甲酰氯/吡啶解答:例3、三个单糖和过量苯肼作用后,得到同样晶形的脎,其中一个单糖的投影式为HOCHOHHOHHH OH2OHOH,写出其它两个异构体的投影式。
解答:其它两个异构体为:例4、有两种化合物A和B,分子式均为C5H10O4,与Br2作用得分子式相同的酸C5H10O5,与乙酐反应均生成三乙酸酯,用HI还原A和B都得到戊烷,用HIO4作用都得到一分子H2CO 和一分子HCO2H,与苯肼作用A能生成脎,而B则不生成脎,推测A和B的结构。
找出A和B的手性碳原子,写出对映异构体。
分析:A和B与Br2作用得酸→A和B是醛糖;A和B与乙酐反应生成三乙酸酯→分子中含三个羟基;用HI还原得到戊烷→A和B是碳直链结构;用HIO4作用得一分子H2CO 和一分子HCO2H→A和B中只有一对羟基相邻;苯肼作用A能生成脎,B不生成脎→A的C1是醛基,C2上有羟基,B的C1是醛基,C2上无羟基。
解答:例5、柳树皮中存在一种糖苷叫做糖水杨苷,当用苦杏仁酶水解时得D-葡萄糖和水杨醇。
水杨苷用硫酸二甲酯和氢氧化钠处理得五-O-甲基水杨苷,酸催化水解得2,3,4,6-四甲基-D-葡萄糖和邻甲氧基甲酚。
写出水杨苷的结构式。
分析:水杨苷用苦杏仁酶水解得D-葡萄糖和水杨醇→葡萄糖以β-苷键与水杨醇结合;水杨苷用(CH 3)2SO 4和NaOH 处理得五-O-甲基水杨苷→水杨苷有五个羟基;五-O-甲基水杨苷酸化水解得2,3,4,6-四甲基-D-葡萄糖和邻甲氧基甲酚→葡萄糖以吡喃式存在并以苷羟基与水杨醇的酚羟基结合。
解答:水杨苷的结构式为:例6、一个D 型非还原性糖类化合物A ,分子式为C 7H 14O 6,无变旋光现象。
A 经稀盐酸水解得到还原性糖B ,分子式为C 6H 12O 6;B 经过硝酸氧化得到非光学活性的二元酸C ,分子式为C 6H 10O 8;B 经Ruff 降解得到还原性糖D ,分子式为C5H10O5;D 经硝酸氧化生成光学活性的二元酸E ,分子式为C 5H 8O 7。
当把A 用(CH 3O)2SO 2-NaOH 处理后再用稀盐酸处理,然后用硝酸加热,得到2,3-二甲氧基丁二酸和2-甲氧基丙二酸,请推测A 、B 、C 、D 、E 的结构,并给出相关的反应式。
解答: 例7、从一植物中分离得到化合物A(C 12H 16O 7),它可β-葡萄糖苷酶水解为D-葡萄糖和一化合物B(C 6H 6O 2)。
B 的1HNMR 数据如下:δ6.81(s,4H), 8.59(s,2H)。
A 在碱性条件下用(CH 3)2SO 4处理然后酸性水解得2,3,4,6-四甲基-D-葡萄糖和化合物C(C 7H 8O 2),C 在CH 3I/Ag 2O 作用下可转化为化合物D(C 8H 10O 2),其1HNMR 数据为:δ3.75(s,6H),6.83(s,4H)。
试给出化合物A 的稳定构象及B,C,D 的结构。
分析:B(C 6H 6O 2)→不饱和度是4,分子中可能有苯环; B 的1HNMR 数据δ6.81(s,4H)→含苯环,且为对二取代,8.59(s,2H)→两个-OH→B 为对二苯酚;D(C 8H 10O 2)的1HNMR 数据 6.83(s,4H)→对二取代苯环,δ3.75(s,6H)→两个-CH 3O-→D 为对二苯甲醚;C 在CH 3I/Ag 2O 作用下可转化为D→C 为对甲氧基苯酚。
A(C 12H 16O 7)在β-葡萄糖苷酶作用下水解→葡萄糖以β-苷键与对二苯酚结合; A 在碱性条件下用(CH 3)2SO 4处理然后酸性水解得2,3,4,6-四甲基-D-葡萄糖→葡萄糖以吡喃式存在并以苷羟基与对二苯酚结合。
解答:A 的稳定构象为:OHHO B C D OCH 3HO OCH 3CH 3O 三、习题和参考答案1、写出D-(+)-葡萄糖的对映体。
α和β的δ-氧环式D-(+)-葡萄糖是否是对映体?为什么? 解答:D-(+)-葡萄糖CHO H OH HO H H OH HOHCH 2OH 的对映体为C H 2O H H OHH H O O H H H O H C H O (L- (-)-葡萄糖)。
α和β的δ-氧环式D-(+)-葡萄糖不是对映体,因为α和β的δ-氧环式D-(+)-葡萄糖之间不具有实物与镜像的关系。
α和β的δ-氧环式D-(+)-葡萄糖分子中均含有五个手性碳原子,其中有四个手性碳的构型相同,只有苷原子的构型不同,所以它们互为差向异构体或异头物。
2、写出下列各化合物立体异构体的投影式(开链式):(1) OO HH O HO C H 2O H H (2)OO HH OC HO HH 2O H(3) OO HH OC H 2O HH 2O H解答:(1) C H 2O HO H HH O H H O H O H H C H O (2) C H 2O HO H HH O H H O H O H H C H O (3) C H 2O HHO H O H H N H 2H H O H C H O3、怎样能证明D-葡萄糖、D-甘露糖、D-果糖这三种糖的C 3、C 4和C 5具有相同的构型?解答:成脎反应发生在C 1和C 2上,这三种糖都能生成同一种脎D-葡萄糖脎,则可证明它们的C 3,C 4,C 5具有相同的构型: 4、完成下列反应式: 解答:(1)(2) (3)C H OH 2O HO H H H O H 3内消旋酒石酸(4)4CHO H 2OH O H H H O H 旋光性丁四醇(5)(6) (7) (8)(C H C O )O H O H 2O H C H 2O H H O C H 2H O H OO H O O H O H 2O O C C H 3C H 2O O C C H 3C H 3C O O C H 2C H 3C O O C H 3C O O O O O O C C H 3C H 3C C C H 3O蔗糖八乙酸酯5、回答下列问题:(1)单糖是否均是固体?都溶于水?都不溶于有机溶剂?都有甜味?都有变旋光现象?(2)下列两个异构体分别与苯肼作用,产物是否相同?(A)O H C C H 2C H C H C H C H 2H (B) C H 2C H C H C H 2CH HH H C H O(3)糖苷既不与Fehling 试剂作用,也不与Tollens 试剂作用,且无变旋光现象,试解释之。
