第五章脂环烃
第五章 脂环烃

脂环烃
36
5.4 环烷烃的结构与稳定性
♦ 环烷烃的稳定性与化学性质联系密切。环越稳定, 则化学性质越不活泼,不易发生化学反应;相反, 环越不稳定,化学性质越活泼。
♦ 在环烷烃中,环丙烷的性质是最活泼的,环丁烷 次之,但都易发生加成反应而开环,性质活泼, 而环己烷的性质最稳定。这是为什么?
有机化学
脂环烃
有机化学
脂环烃
28
2. 氧化反应
♦ 在更强烈的条件下,与强氧化剂及催化剂的作 用下,则可以被氧化成不同的产物。
环 酸 烷 钴 1.0~2.5MPa 150~160℃,
O
+
OH
醋 钴 酸 1.0MPa 95℃ ,
HOOC COOH
有机化学
脂环烃
29
3. 加成反应
——小环烷烃具有与烯烃类似的性质,可发生一 些加成反应。如催化加氢、加X2、加HX等。 (1)催化加氢: C3、C4、C5环烷烃可在金属Ni 催化下加氢,生成相应的开链烷烃,并随环的增 大,反应所需温度越高,反应越困难。如:
环戊烷的构象
46
4)环己烷的构象
在环己烷分子中,六个碳原子不在同一平面内, 碳碳键之间的夹角可以保持109.5°因此环很稳定。
有机化学
脂环烃
47
5)环己烷及其衍生物的构象
——在环己烷分子中,六个碳原子不在同一平面 内,碳碳键之间的夹角可以保持109.5°,因此环很稳定。 1.两种极限构象——椅式和船式
H3C CH3 O3 Zn
乙酸
5.臭氧化
O H C CH CH2 CH C H
O CH3 H3C
CH CH
or
CH2=CH CN
CN
有机化学
第五章 脂环烃

第五章脂环烃(cycloalkane)内容提要本章学习脂环烃的结构、命名、性质,其中环烷烃的顺反异构、对映异构、构象分析是本章的难点;掌握这类化合物的化学性质及其制备方法;同时与前面所学的脂肪烃作比较,从反应机理上理解它们化学性质的异同点。
5.1 脂环烃的分类、命名和异构环烷烃是指碳干为环状而性质和开链烃相似的烃类化合物。
单环烷烃的通式为C n H2n,双环烷烃的通式为C n H2n-2。
5.1.1 脂环烃的分类脂环烃按其成环特点可分为三类:单环烃、螺环烃及桥环烃(见表3.1)。
的数目而确定。
需要断开几个C—C键就是几环。
例如金刚烷(见右图),C10H16是三环。
桥环化合物中,碳环共用的两个碳原子叫桥头碳原子。
双环化合物可以看成是三条连在两个桥头上的桥所构成的。
5.1.2 脂环烃的命名5.1.2.1 单环化合物的命名根据饱和脂环烃环中碳原子的数目叫环某烷。
当环上有取代基时,在母体环烃名称的前面加上取代基的名称和位置。
环上碳原子的编号,应使表示取代基位置的数字尽可能小。
取代基的顺序与烷烃命名相同。
含有C=C双键的脂环烃叫环某烯,编号从双键碳原子开始,并考虑取代基位置。
5.1.2.2 桥环化合物的命名饱和桥环化合物命名时,首先根据环的数目确定双环或者三环等,叫“几环”,然后把与桥头碳原子相连的各桥所含碳原子的数目按由大到小的顺序写在方括号里(每个数目之间用点隔开),放在“几环”的后面;再根据组成所有环的碳原子金刚烷总数命名为“某烷”,放在方括号的后面。
从桥头碳原子开始,由大环到小环,依次编号。
对于相同大小的环,以取代基位置较小为佳。
将取代基的位置及名称写在最前面。
若环上含有双键,叫“某烯”,从桥头碳原子开始,由大环到小环依次编号,对于相同大小的环,以双键位置较小为宜,并标出双键位置。
5.1.2.3 螺环化合物的命名螺环化合物的命名,根据组成环的碳原子总数,命名为某烷,加上词头螺。
再把连接于螺原子的两个环的碳原子数目,按由小到大的次序写在螺与某烷之间的方括号里,数字用点分开。
第五章脂环烃

O +
环戊二烯
O O
O
O
O
丁烯二酸酐
三、卡宾(碳烯)合成法
CH2N2
重氮甲烷
光或热
: CH2 + N2
碳烯
CH3- CH=CH-CH3 + :CH2
CH3-CH -CH-CH3 CH2
+ :CH2
二环[4.1.0]庚烷
本章作业:
1(1,4,6,7), 2(3,5,7), 6, 9
Ni 180~250℃
+ 3 H2
+ H2
催化剂 四氢化萘
H2 催化剂
十氢化萘
二、分子内偶联法
1.武慈合成法——主要适合于制备三、四元环
CH2 CH2 Br
Na 或Zn
CH2
Br
Br
CH2
CH2 CH2
K
Br
2.格氏试剂合成法——主要适合于制备四~七元环
Cl
Mg
Cl 3 MgCl
3.狄尔斯-阿德尔合成法(双烯合成)
H + H COOCH3 COOCH3 具 有 顺丁烯二酸二甲酯 顺-环己烯-4,5-二甲酸二甲酯 立 体 COOCH3 专 CH3OOC H H 一 H + 性 COOCH3 H COOCH3
反-丁烯二酸二甲酯 反-环己烯-4,5-二甲酸二甲酯
H CO O CH 3 H CO O CH 3
但在530℃、Pd-C催化剂存在下,两者可达到动态平衡:
H H H H H H 9% 空间障碍大,能量高
530 C,Pd-C催化剂
。
H
H 91% 空间障碍小,能量低
不稳定
稳定
二、 环己烷的构象
第五章脂环烃

(2a)
反-1,4-二取代
若环上有不同取代基,则体积大的取代基连在 e键上的构象最稳定。
H C(CH3)3 HO H OH C(CH3)3 H
叔丁基在 e键上稳 定
H
OH
顺-4-叔丁基环己醇
C(CH3)3
5)环己烷构象的画法: 三组平行线
结论:
通过环己烷的构象分析可知:
环己烷椅式构象稳定; 取代基在e键上稳定; 处于e键的取代基越多,越稳定; 大取代基处于e键越多,越稳定。
2)环烯烃的命名(环某烯)
原则:先保证双键位次最小,再考虑取代基
2 1 6 5
H3C 3
4
环戊烯
3-甲基-1-环己烯
3)螺环烃的命名 定义:两个环共用一个碳原子的环烷烃称为螺环烃。
螺碳原子
规则:(a) 组成环的碳原子总数命名为“某烷”,加上 词头“螺”。 (b) 再把连接于螺原子的两个环的碳原子数(不 含螺原子),按由小到大的次序写在“螺”和“某烷” 之间的方括号里,数字用圆点分开。表示为螺[ . ]某 烷。
例如:
2 3 4 6 5 1 8
7 1 6
7
2 4
5
3
8-甲基-2-乙基双环[4.2.0]辛烷 2,7,7-三甲基双环[2.2.1]庚烷
练习:
6-甲基双环[3.2.2]壬烷
8,8-二甲基双环[3.2.1]辛烷
二、 脂环烃的性质 1、环烷烃的反应 1)取代反应
环烷烃与烷烃一样,在光或热引发下可发生卤代反应。
双环[2. 2. 1]-5-庚烯-2-羧酸甲酯
2)聚合反应
室温
+
双烯组分 亲双烯组分
H H
二聚环戊二烯
实质:双烯合成
第五章 脂环烃
应用:用高锰酸钾溶液来区别烯烃与环丙烷衍生物
CH2=CH 2
KMnO 4
紫色退去 不退色
§5.3 脂环烃的结构
实验事实: 环的稳定性:三元环<四元环<五元、六元环
反映了环的稳定性与环的结构有着密切的联系。
一、 张力学说
当碳原子的键角偏离109©28′时,会产生一种恢复正常键角的力量。 这种力就称为张力。键角偏离正常键角越多,张力就越大。 1、所有的碳都应有正四面体结构 2、所有成环的碳原子都处在同一平面上
H
C(CH3)3
扭船式 太大的取代基 要尽量避免取 a键。
5、 1,3-己二醇
形成氢键时,aa为优势构象。
OH
OH
四、十氢合萘的构象 1、 名称
8 7 6 5 4 1 2 3
8 7 6 Βιβλιοθήκη 91 2 39 8
10 1
2 3 4 5
10
6 7
4
萘
十氢合萘(暜通名)
二环[4.4.0]癸烷
naphthalene
室温 H2, Ni
+
>100 C
三、芳烃还原
H2 catalyst H2 catalyst
四、卡宾合成法(以后学到)
本章重点
1 、环的大小与其稳定性(三元、四元环不稳定, 易开环加成;五元、六元环稳定,不易开环加 成); 2、桥环、螺环化合物的命名; 3、环丙烷的结构、弯曲键的不稳定性; 4、环己烷的构象:船式、椅式
联环
4、根据环的连接方式 桥环 螺环
二、 脂环烃的异构
脂环烃的构造异构现象比脂肪烃复杂。
碳架异构体
顺反异构
写出符合分子式C6H10的化合物
COOH COOH
第五章 脂 环 烃课件

1,2-二甲基环丙烷
1-甲基-2-异丙基环戊烷
H
H
H
H
顺-1,4-二甲基环己烷
反-1,4-二甲基环己烷
2、环烯烃和环炔烃的命名
和命名烯烃,炔烃相似,只是把环某烷改 成环某烯(炔),同时双键或叁键也要标出最 小位次。
3,5-二甲基环己烯
1,3-环戊二烯
3-甲基环己炔
3、螺环及桥环化合物的命名
=
螺环[2.4]庚烷 螺环[2.2.1]庚烷 双环[2.2.2]-2,5-辛二烯
当环已烷分子中任一个H被其它原子或基团 取代后,就得到了环已烷的一元取代衍生物。 由于取代基既可占据a键,也占据e键,便有两 种不同的构象。例如甲基环已烷。
CH3 CH3
环已烷的二元取代衍生物,如二甲基环己烷, 除有1,1-;1,2-;1,3-;1,4一等位置异构 体外,还存在顺反异构体。例:
H H H H H H H H H H H H
80℃ 200℃
(2)加卤素
CCl4
R.T.
+ +
Br2
Br
Br
CCl4
Br2
Br
Br
(3)加卤化氢
+ +
IH
R.T.
I
IH
I
I
+ HI
3、氧化反应
常温下,环烷烃不与氧化剂反应,而烯烃则 与KmnO4 ,O3 等氧化剂反应,∴可利用KmnO4 的 颜色变化来鉴别环烷烃和烯烃。 但在强烈条件下,环烷烃也可被氧化:
H
H H
H H H H
H H C ( C H 3)3 H
反 -1 -甲 甲 -2 -叔 叔甲 叔叔 叔
H
H
第5章 脂环烃

高于开链烷烃的能量,称为张力能
大环/中环/普通环 > 四元环 > 三元环
第三节 构象
一、环丙烷、环丁烷和环戊烷的构象
2
3
1
4 3 2 1
四个碳不在同一 平面上,为折叠 式排列。
4
3
2
1
4
环丁烷的构象—蝴蝶型
稳定构象 • 角张力稍增加, 扭转张力明显减小
能量低, 稳定构象
环戊烷的构象
• 环戊烷分子中,碳碳键的夹角为108°,接近sp3杂化轨 道间夹角,角张力很小,是比较稳定的环。
9
4
C6H 37
34
CH3 2 7 1CH3 6 5
CH 3
32[4-.甲3.20基]壬1二烷环9 8
CH 3
34
5
2
16
CH 3
5,7,7-三甲基二环[2.2.1]庚-2-烯
对于相同大小的环, 以双键位置较小为宜
总结: 大前, 小后, 从大到小。(桥环)
11
10 4
5
3
2
1
6 7
9 8
环烃的命名关键是编号——应当遵循的原 则依次为: ①桥环、螺环的特定原则; ②官 能团位置最小原则; ③取代基最先碰面原则; ④先小后大原则。
第一节 • 分类和命名 第二节 • 小环烷烃的结构 第三节 • 构象 • 环丙烷、环丁烷和环戊烷的构象 • 环己烷的构象
第四节 • 脂环烃的物理性质 第五节 • 脂环烃的化学性质 第六节 • 脂环烃的制备
5.1 脂环烃的分类和命名(了解) 5.2 环烷烃的物理性质(了解) 5.3 环烷烃的结构与稳定性(掌握) 5.4 脂环烃的化学性质(重点掌握)
第一节 分类和命名
有机化学课件——第五章 脂环烃

(3)同一碳上有两个不同取代基时
同一碳上有两个不同取代基时,把母体官能团做“参 照基团”给予尽可能低位次号,其它取代基只择其“较 优基团”用顺或反表示与“参照基团”的立体关系。 例如:
1,顺-2-二氯-r-1-环戊基甲酸
4、环己烷及其衍生物的结构
(1)环己烷的构象 (2)a键和e键 (3)取代环己烷的结构
H3C H
反-1, 4-二甲基环己烷
例子
(二)螺环烃的命名
螺原子:两个碳环共用的碳原子 螺[2,4]庚烷
3-甲基-75]癸烷
(三)桥环烃的命名
桥头碳原子:两环共用的碳原子。 桥:两个桥头碳原子之间的碳链或一个键。
(1) 桥 (2) 桥
桥头碳
桥头碳 桥 (3)
例如
顺-1,3-二氯环戊烷
反-2-氯环戊基甲酸
(2)环上有两个以上位置各有一个取代 基时
环上有两个以上位置各有一个取代某时,则选择其中位次 最低者为“参照基团”.在位次前加“r”标记,其余取 代基位次前用顺或反表示它们与“参照基团”的立体关 系。例如
r-1,反-2,顺-4-三氯环己烷 反-5-氯-r-1,顺-3-环己基二甲酸
4-甲基环己烯
3-甲基-4-环丁基庚烷
3)顺、反环烷烃 受环的限制,σ键不能自由旋转。环上取代基在空间的 位置不同,产生顺反(几何)异构。
顺(cis): 两个取代基在环同侧;
反(trans): 两个取代基在环异侧。
H3C CH3
H3C H
CH3
H CH3
HH
H
顺-1, 4-二甲基环己烷
CH3
CH3
二环 [3.2.1] 辛烷
7
1
6
2
54 3
第五章 脂环烃
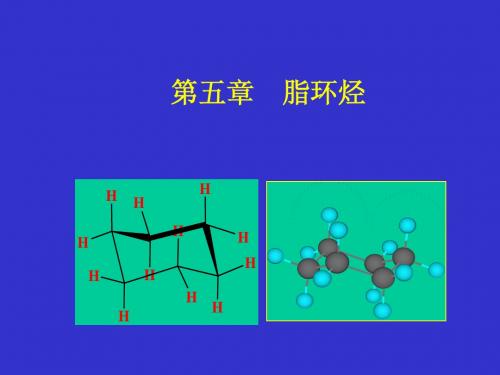
C C C
Fig. the Molecular Orbital of Cyclopropane
特点: )键角60℃;(2)轨道夹角105. 5℃; 特点:(1)键角 ℃;( )轨道夹角 ℃
(3)不等性 3杂化 形成 )不等性sp 杂化: 形成C-C键sp3杂化轨道具有较 键 成分。 多p成分。 成分
第五章
脂环烃
H H H H H H H H
H H H H
脂环烃: 由碳和氢两种元素组成的一类碳环化合物。 脂环烃 由碳和氢两种元素组成的一类碳环化合物。
一、脂环烃的分类
环烷烃 碳原子的饱和程度 环烯烃 环炔烃 单环脂环烃 碳环的数目 二环脂环烃 多环脂环烃
降冰片烷 立方烷
脂环烃的构造异构现象比脂肪烃复杂,如环烷烃 脂环烃的构造异构现象比脂肪烃复杂, C5H10的构造异构体 的构造异构体:
其沸点、熔点和密度较相同碳原子的开链脂肪烃高。 沸点、熔点和密度较相同碳原子的开链脂肪烃高 较相同碳原子的开链脂肪烃 环丁烷, 比水轻;常温常压下,只有环丁烷 环丙烷为气体, 比水轻;常温常压下,只有环丁烷,环丙烷为气体, 其余为液态。 其余为液态。
四、脂环烃的化学性质 (一)环烷烃的化学性 1.取代反应 1.取代反应
原因:由于角张力作用, 原因:由于角张力作用,使得环丙烷和环丁烷分子
定性下降,容易发生加成反应使环打开。 稳 定性下降,容易发生加成反应使环打开。
0.152nm 比烷烃中的 比烷烃中的C-C键长 键长0.154nm短 键长 短
H H H
H H H
H H
115°
H
H
H
H
重叠构象
六、环己烷及其衍生物的构象
7 5 5 6 1 4 3 2 3 2 1 4 6 7 7 6 5 1 8 4 2 3
有机化学第五章 脂环烃

三、脂环烃的结构与稳定性
为什么三、四元的小环化合物不稳定,易发生开环 的反应,而五元环、六元环相对稳定?
拜尔张力学说
键角: 60° 90°
当碳原子的键角偏离109°28′时,便会产生一种恢复
正常键角的力量。这种力就称为张力。键角偏离正常键角
越多,张力就越大。
C C
109.5 。
C
105.5 。
C
如果取代基更大,则空间效果更突出,叔丁基以e键与环
相连的构象近100%。
C
(2)二取代环己烷的构象
1,2-二甲基环己烷
CH3 CH3 CH3
CH3
CH3
CH3 CH3
CH3
反式
顺式
1,2-二甲基环己烷的平面表示法
顺式
CH3 H3 C CH3 CH3
稳定性相同 反式
CH3 CH3 CH3
CH3
更稳定
H 1 H H 5 2 H 4 2.50A H H 2.51A H H 3 H 2.49A H
H 6
H
a键
e键
a b b b a a a
a b b b a a a
b b a
b a a b
b
a
b
构象翻转,a键转变成e键,e键转变成a键;环 上原子或基团的空间关系保持。
2、环己烷椅式构象的书写
3、环己烷的船式构象
椅式
扭船式
船式
半椅式
1、环己烷的椅式构象
H 1 H H H
H 2 3 H H 4 H H
H 6 H H
5
锯架式
纽曼式
环己烷椅式构象的特点
环中相邻两个碳原子均为邻交叉。
C-H键分为两类,有6个直立键叫a (axial) 键,有6个 平伏键称e (equatorial)键。
第五章脂环烃

1
2 6
CH3
3
CH3
4
5
同碳数环烷烃与烯烃互为同分异构体 通式为CnH2n
其中1、2、3、4、5是构造异构体。分 子中原子的连接方式和次序不同。
6和7是顺反异构体,因成环碳原子单键不
7 5
CH3
CH3
能自由旋转而引起的。两个甲基相对于环
平面的位置不同。
6和7之间互相转变需要较高的能量,在室温 下不能实现,它们的物理性质也不相同。
键角
实际上,环烷烃(除三元环外)并不是一个平面结构, 实际上,环烷烃(除三元环外)并不是一个平面结构,这就使张 力学说失去了存在的基础。那么,如何解释小环的不稳定性呢? 力学说失去了存在的基础。那么,如何解释小环的不稳定性呢? 小环烷烃的结构
。 1 。09.5 60 24。4' 4
随着环的扩大,张力
H 1 H H 2 H H 3 H H 4 H
H H
H H
1 6
5
3 4
H
H 6 H H
5
H
H H
2
H
H
H
H
锯架式
纽曼式
环己烷椅式构象的特点
1. 有6个a (axial) 键,有6个e (equatorial)键。 个 个 键 2. 有C3对称轴。(过中心,垂直于 对称轴。(过中心,垂直于1,3,5平面和 。(过中心 平面和2,4,6 平面和 平面,两平面间距50pm) 平面,两平面间距 ) 3. 有构象转换异构体 。( 。(K=104-105/秒) 秒 4. 环中相邻两个碳原子均为邻交叉。 环中相邻两个碳原子均为邻交叉。
CH3
CH3
CH3
5 6 4 7 8
3 2 1
有机化学 第五章 脂环烃

(3) 其它方法
+
CHO
。
30 C
100%
OH
+ ZnBr2 CHO
环戊二烯的工业来源和制法
石油热裂解的C5馏分加热至100℃,其中的 环戊二烯聚合为二聚体,蒸出易挥发的 其他C5馏分,再加热至约200℃,使二聚 体解聚为环戊二烯:
。
+
100 C
。
200 C
(八) 萜类和甾族化合物
萜类化合物广泛存在于自然界,是植物香精 油的主要成分,广泛用于医药、香料工业。
CH +
CH
双烯体 亲双烯体
双环[2,2,1]-2,5-庚二烯
(四) 环烷烃的结构与稳定性
• 环的大小与环张力、环的稳定性 • 环丙烷的结构 • 环丁烷的结构 • 环戊烷的结构
(四) 环烷烃的结构与稳定性
实验事实: 环的稳定性:三元环<四元环<五元、六元环 why? 结构所致!环张力所致!
• 环烷烃的环张力越大,表明分子的能量越高, 稳定性越差,越容易开环加成。
(甲) 桥环烃 (乙) 螺环烃
(二) 脂环烃的命名
(1) 单环脂环烃
CH2 CH2 CH2
即
CH2 CH2
环戊烷
CH3
即
CH
H3C
CH3
CH3
CH3 CH3
甲基环丁烷
1,2-二甲基环戊烷
H CH3
H CH3
CH3 H
即
CH3 H
1-甲基-4-异丙基环己烷
CH3
反-1,4-二甲基环己烷
CH3
1-甲基-1-环己烯
环己烷的船式构象
船式与椅式翻转,环己烷二种椅式构象互换
取代环己烷的构象1
第五章 脂环烃

平伏键(e键):与分子的对称轴呈109 平伏键(e键):与分子的对称轴呈109。28, (e 与分子的对称轴呈 直立键( 键):与 直立键(a键):与y轴平行
C6 a
109° 28'
a键平行于 对称轴(共6个)
a a a e
109° 28' 109° 28'
稳定性: >(ii ii) iii) 稳定性: (Ⅳ) >(ii)≈(i)> (iii)
CH3 CH3 CH3 CH3
(△G<0)
a,a式
e,e式
CH3
CH3 CH3
CH3
(△G=0)
e,a式
e,a式
(2)1,4-二甲基环己烷 ) , 二甲基环己烷
(3)1,3-二甲基环己烷 ) , 二甲基环己烷
Ni 200℃ Pd >300℃
2.加卤素 .
CH2-CH2-CH2-CH2 Br Br
Br2/CCl4
不起加成,而是取代反应
3.加HX, H2SO4 .
注意: 加成方向遵循马氏规则; 注意:①加成方向遵循马氏规则; 开环位置: ②开环位置:C含H最多——C含H最少, 最多 最少 环的活泼性:三元环>四元环> 七元环。 ③环的活泼性:三元环>四元环>五、六、七元环。小 环烷烃易加成\难氧化 似烷似烯。 普通环以上难加成, 难氧化, 环烷烃易加成 难氧化 , 似烷似烯 。 普通环以上难加成 , 难氧化,似烷。 难氧化,似烷。 环烯烃、共轭二烯烃,各自具有其相应烯烃的通性。 ④环烯烃、共轭二烯烃,各自具有其相应烯烃的通性
(4)反-1-甲基-4-异丙基环己烷 甲基CH3
大的取代基位于e 大的取代基位于 键上的构象更稳定
第5章 脂环烃

例 写出1,3-二甲基环己烷的最稳定构象。
顺 式 反 式 ee
H3C
CH3
H3C CH3
ae
1,3-二甲基环己烷的顺式较反式稳定。
同理可推出:1,4-取代的反式较顺式稳定。
44
例 写出4-叔丁基环己醇的最稳定构象。
顺 式
C(CH3)3 OH
HO C(CH3)3
ae
HO
较稳定
OH
C(CH3)3
15
原 因
5-2 脂环烃的物理性质和化学性质
环烷烃的化学性质 取代反应 自由基取代历程
Br2
hv
Br
+
CH3
+
+
HBr
+
Cl2
hv
CH3 Cl
HCl
取代反应一般在五、六元环上易发生
16
环烷烃的化学性质
开环反应——加成反应 大环环烷烃和链状烷烃的化学性质很相像:
——对一般试剂表现得不活泼。
1-甲基-4-异丙基环己烷
5
④ 对于顺反异构体 顺式(cis):相同基团在环平面的同侧;
反式(trans):相同基团在环平面的两侧。
CH3CH3
CH3CH3
或
H H
H CH3
顺- 1,2-二甲基环丙烷
H H
CH3
反-1,3-二甲基环戊烷
H
CH3 CH2
CH(CH3)2
反-1-乙基-3-异丙基环戊烷
41
[2]多取代环己烷的构象
结论:
① 多取代环己烷, e取代基最多的构象最 稳定。 ② 多取代环己烷, 体积较大的取代基为e 型的构象最稳定。
42
例 写出1,2-二甲基环己烷的最稳定构象。
第五章脂环烃共55页

2019/9/22
环丙烷
HC H
1 0 5 .5
H C 0.1524nm C H
H
H 114
环丙烷为张力环,采取重叠式构象, 所以容易破环。此外,环丙烷C-C 键为弯曲键,有点类似于烯烃的键, 可以发生类似于烯烃的加成反应。
2019/9/22
二、环丁烷和环戊烷的构象 平 面 式
2019/9/22
C 6 H 12
Structural formulas of cyclic molecules -- Cyclohexane
Condensed formula
CH 2
CH 2
CH 2
CH 2
CH 2
CH 2
2019/9/22
C 6 H 12
Structural formulas of cyclic molecules -- Cyclohexane
2019/9/22
环己烷 的2种 典型构
象
四、环己烷的构象
CYCLO ALK ANE CO NFO RM ATIO N
CHAIR CYCLOHEXANE
561 432
椅式
BOAT CYCLOHEXANE
4
1
5 3
2
6
船式
1
3 2
56
4
邻位交叉式
STAGGERED
32 5 6 1 4
全叠式
ECLIPSED
1. 加氢开环
H2,Ni 80 C
CH3CH2CH3
H1220,NCi CH3CH2CH2CH3
H302,0NCi CH3CH2CH2CH2CH3
2. 加卤素、加卤化氢开环
+Br2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五章脂环烃学习要求1、掌握脂环烃的命名方法和基本结构。
2、熟练掌握环烷烃和环烯烃的化学性质。
3、熟练掌握环烷烃的顺、反异构现象和环己烷的构象。
§5~1 脂环烃的分类命名和异构现象一、分类饱和脂环烃,环烷烃如:()1、不饱和脂环烃环烯烃如:()环炔烃环的大小:小环(3~4元);普通环(5~7元);中环((8~12元)和2、大环(十二碳以上)。
环的多少:单环;多环(桥环,螺环)二、命名1、环烷烃的命名通式C n H2n与单烯烃互为同分异构体。
n=3 C3H6 同分异构体数目1个; n=4 C4H8 同分异构体数目2个;n=5 C5H10 同分异构体数目5个;环烷烃命名:⑴环上命名似烷烃,在名称前加上“环”字,叫环某烷;⑵环上有取代基时,一元取代——某基环某烷;二元取代——用“次序规则”决定基团的排列先后,环上编号以小基团优先,写法时“较优”基团排在后面;多个取代基时,方法类同。
⑶有顺反异构时,则在命名最前写出“顺”或“反”名称。
⑷较复杂时,则把碳环看作取代基,叫法“环某基”。
例如:环丙烷环丁烷环戊烷CH3 CH3CH3CH3CH3H2CCH3环已烷甲基环丙烷1,3-二甲基环丙烷1,1-二甲基环丙烷乙基环丙烷CH3H H 3CHCH 3HH 3CH 3H顺-1,2-二甲基环丙烷反-1,2-二甲基环丙烷OH H OH HOH H HOH顺-1,2-环已二醇反-1,2-环已二醇CH3CH 2CHCH 2CH 33-环丙基戊烷2、环烯烃的命名 (1)称为环某烯。
(2)以双键的位次和取代基的位置最小为原则。
例如:3、多环烃的命名(1) 桥环烃(二环、三环等) 分之中含有两个或多个碳环的多环化合物中,其中两个环共用两个或多个碳原子的化合物称为桥环化合物。
命名原则:A 、确定母体名称——某烷(根据环上碳原子总数目)。
A 、 注明环数——常用“双环”或“三环”等;B 、确定桥头碳原子——数出每条桥所含碳原子数(不包括桥头碳原子),按由多到少的次序写在“双环”和“某烷”之间 的方括号里,数字用圆点分开。
C 、 桥环碳原子编号,从桥头碳——大环——桥头碳原子——中环——小环。
D 、 如有取代基,在符合上述条件下,尽量使取代基编号为最少;如有双键时,也同上,叫某烯,还注明双键的位次。
例如: 上化合物名为 7,7-二甲基二环[2,2,1]庚烷(2)螺环烃 两个环共用一个碳原子的环烷烃称为螺环烃。
CH 3CH 3CH 3环戊烯1-甲基环戊烯3,4-=甲基 环己烯1,3-环戊烯2-甲基-1,3- 环己二烯桥头碳2CH 32-甲基-5-异丙基二环[3,1,0]己烷2-乙基-6-氯二环[3,2,1]辛烷23命名原则:A 、确定母体名称——某烷(根据环上碳原子总数目)。
B 、确定各环碳原子个数(除去螺原子)按由少到多的次序写在“螺”和“某烷”之间 的方括号里,数字用圆点分开。
C 、 桥环碳原子编号,小环——螺原子——大环。
D 、 如有取代基,在符合上述条件下,尽量使取代基编号为最少;如有双键时,也同上,叫某烯,还注明双键的位次。
E 、§ 5~2 脂环烃的性质一 、普通环的性质普通脂环烃具有开链烃的通性,环烷烃主要是起自由基取代反应,难被氧化。
环烯烃具有烯烃的通性二、小环烷烃的特性反应 1.加成反应 (1) 加氢螺碳原子1-溴-5-甲基螺[3,4]辛烷CH 3Br 2Cl 2BrCl CH 3HBr HCl H 2N i CH 3CH 2CH 3H 2Ni CH 3CH 2CH 2CH 3H 2Pd>300℃CH 3CH 2CH 2CH 2CH 3CH 3CH 3Br 2/CCl 43H O/Zn CH 3-C-CH 2CH 2CH 2CHOO 1mol Cl 2CH 3ClCl CH 3主次CH 3HCl CH 3ClCH 3Cl 1,4-加成1,2-加成(主)(2) 加卤素(3)加H X, H 2SO 42、氧化反应环丙烷对氧化剂稳定,不被高猛酸钾、臭氧等氧化剂氧化。
例如:故可用高猛酸钾溶液来区别烯烃与环丙烷衍生物。
环烃性质小结:(1) 小环烷烃(3,4元环)易加成,难氧化,似烷似烯。
普通环以上难加成,难氧化,似烷。
(2) 环烯烃、共轭二烯烃,各自具有其相应烯烃的通性。
§ 5~3 脂环烃的结构从环烷烃的化学性质可以看出,环丙烷最不稳定,环丁烷次之,环戊烷比较稳定,环己烷以上的大环都稳定,这反映了环的稳定性与环的结构有着密切的联系。
一、 环丙烷的结构与张力学说 1、环丙烷的结构理论上: 1° 饱和烃,C 为sp 3杂化,键角为109.5°自相 2° 三碳环,成环碳原子应共平面,内角为60° 矛盾故三元环的结构特殊。
现代物理方法测定,环丙烷分子中:键角 C-C-C = 105.5°; H-C-H =114°。
所以环丙烷分子中碳原子之间的sp 3杂化轨道是以弯曲键(香蕉键)相互交盖的。
Br 2/CCl 4CH 2-CH 2-CH 2Br BrCH CH Br 2/CCl 4C-CH-CH 2Br CH 3Br CH 3CH 3Br 2/CCl 4CH 2-CH 2-CH 2-CH 2Br BrBr 2/CCl 4溴褪色可用于鉴别环烷烃不起加成,而是取代反应HBr H 2SO 4C CH CH 3CH 3CH 3BrCH 3C CH CH 3CH 3CH 3OSO 3H CH 3C CH CH 3CH 3CH 3OH CH 3CH=C CH 33CH 3CH 3C=O由图可见,环丙烷分子中存在着较大的张力(角张力和扭转张力),是一个有张力环,所以易开环,所以易 开环,发生加成反应环丙烷的结构图2、张力学说 (见P 104~105)在环丙烷分子中,电子云的重叠不能沿着sp 3轨道轴对称重叠,只能偏离键轴一定的角度以弯曲键侧面重叠,形成弯曲键(香蕉键),其键角为 105.5°,因键角要从109.5°压缩到105.5°,故环有一定的张力(角张力)。
另外环丙烷分子中还存在着另一种张力——扭转张力(由于环中三个碳位于同一平面,相邻的C-H 键互相处于重叠式构象,有旋转成交叉式的趋向,这样的张力称为扭转张力)。
环丙烷的总张力能为114KJ/mol 。
二、环丁烷和环戊烷的构象 1、环丁烷的构象与环丙烷相似,环丁烷分子中存在着张力,但比环丙烷的小,因在环丁烷分子中四个碳原子不在同一平面上,见右图:根据结晶学和光谱学的证明,环丁烷是以折叠壮构象存在的,这种非平面型结构可以减 少C-H的重叠,使扭转张力减小。
环丁烷分子中 C-C-C 键角为 111.5°,角张力也比环丙烷 的小,所以环丁烷比环丙烷要稳定些。
总张力能 环丁烷的构象 为108KJ/mol 。
2、环戊烷的构象环戊烷分子中,C-C-C 夹角为108°,接近sp 3杂化轨道间夹角109.5°,环张力甚微,是比较稳定的环。
但若环为平面结构,则其C-H 键都相互重叠,会有较大的扭转张力,所以,环戊烷是以折叠式构象存在的,为非平面结 构,见右图,其中有四个碳原子在同一平面,另外一个碳原子在这个平面之外,成信封式构象。
这种构象的张力很小,总张力能25KJ/mol ,扭转张力在2.5KJ/mol 以下,因此,环戊烷的化 环戊烷的构象 学性质稳定。
三、环己烷的构象 在环己烷分子中,六个碳原子不在同一平面内,碳碳键之间的夹角可以保持109.5°因此环很稳定。
1、两种极限构象——椅式和船式HH 椅式船式 无角张力 无C-H 键间的扭转张力 无张力 环 常温下 99%无角张力有C-H 键间的扭转张力有张力环1%椅式构象稳定的原因:船式构象不稳定的原因:2、平伏键(e 键)与直立键(a 键)在椅式构象中C-H 键分为两类。
第一类六个C-H 键与分子的对称轴平行,叫做直立键或a 键(其中三个向环平面上方伸展,另外三个相换环平面下方伸展);第二类六个C-H 键与直立键形成接近109.5°的夹角,平伏着相环外伸展,叫做平伏键或e 键。
如下图:在室温时,环己烷的椅式构象可通过 C-C 键的转动(而不经过碳碳键的断裂), 由一种椅式构象变为另一种椅式构象,在互相转变中,原来的a 键变成了e 键,而原来的e 键变成了a 键。
当六个碳原子上连的都是氢时,两种构象是同一构象。
连有不同基团时,则构象不同。
3、取代环己烷的构象 1)一元取代环己烷的构象一元取代环己烷中,取代基可占据a 键,也可占据e 键,但占据e 键的构象更稳定。
例如:H 相邻碳上的C-H全部为重叠式H 相邻碳上的C-H键全部为交叉式环己烷的直立键和平伏键平伏键直立键对称轴键键键键两个椅式构象的互相转变393%内能比a 型少75.3KJ/mol7%原因:a 键取代基结构中的非键原子间斥力比e 键取代基的大(因非键原子间的距离小于正常原子键的距离所致)。
从下图中原子在空间的距离数据可清楚看出。
取代基越大e 键型构象为主的趋势越明显。
2)二元取代环己烷的构象 (1)1,2-二取代(2)1,3-二取代其他 二元、三元等取代环己烷的稳定构象,可用上述同样方法得知。
小结:1°环己烷有两种极限构象(椅式和船式),椅式为优势构象。
2°一元取代基主要以e 键和环相连。
3°多元取代环己烷最稳定的构象是e 键上取代基最多的构象。
4°环上有不同取代基时,大的取代基在e 键上构象最稳定。
§ 5~4 脂环烃的制备 (自学)甲基环己烷原子间的距离C CH CH C 3CH 3CH 3<0.1%>99.9%CH 3CH 333333(顺式)(反式)只能是 构象构象(优势构象)e,a a,a e,e 构象333e,a a,a 3CH 3CH 3CH 3CH 33e (顺式)(反式)构象只有 构象(其中有大的基团时,则在 键上)e,e 构象(优势构象)。
