腐蚀电化学常规测量方法讲义
高考化学电化学腐蚀讲义

高考化学—-电化学腐蚀—-讲义(1)对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐措施的腐蚀。
(2)对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液中。
(3)活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。
两种保护方法的比较外加电流的阴极保护法保护效果大于牺牲阳极的阴极保护法。
例题解析1、如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为A。
②①③④⑤⑥B。
⑤④③①②⑥C、⑤④②①③⑥D。
⑤③②④①⑥2、利用如图装置探究铁在海水中的电化学防护,下列说法不正确的是A、若X为锌棒,开关K置于M处,可减缓铁的腐蚀B、若X为锌棒,开关K置于M处,铁电极的反应:Fe−2e−Fe2+C、若X为碳棒,开关K置于N处,可减缓铁的腐蚀D。
若X为碳棒,开关K置于N处,铁电极的反应:2H++2e−H2↑3、利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间、下列说法正确的是A、左管中O2得到电子,右管中H+得到电子B。
一段时间后,左管液面低于右管液面C、a、b两处具有相同的电极反应式:Fe−3e−Fe3+D、a处溶液的pH增大,b处溶液的pH减小4、铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图所示。
下列说法不正确的是A、因铁的金属性比铜强,因此铁铆钉被氧化而腐蚀B、若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小C、铜极上的反应是2H++2e−H2↑、O2+4e−+4H+2H2OD、在金属表面涂一层油脂,能防止铁铆钉被腐蚀巩固练习1、[2019江苏][双选]下列说法正确的是A、反应N2(g)+3H2(g)2NH3(g)的ΔH< 0,ΔS >0B、地下钢铁管道用导线连接锌块能够减缓管道的腐蚀C。
腐蚀电化学研究方法常用技术讲义

一个实验电解池。
2、极化曲线
方法分类 装置和测量技术:一般用三电极体系 体系构成两个回路:一个是极化回路(电流测量回路)
一个是电位测量回路
极化电源
A
电位测量
二、Tafel直线外推法
极化曲线外延法测定腐蚀速度
对于活化极化控制体系,外加极化较大时,E与lgi间成线性关系,
1、线性极化方程
①活化极化控制的腐蚀体系,在自腐蚀电位附近,也
就是△E很小时(通常在±10mv左右),极化曲线是
线性关系,直线的斜率称极化电阻,Rp= d,E
icorr=
ba bc 2.303(ba bc )
1,线性极化方程式,SterdnI-Geary方
Rp
程式。
两电极系统:两个电极同等程度的极化,但方向相反, 所以两电极的极化值为2△E(V读数),则每个电极 极化值为△E,给定△E后测△I。
在弱极化区选三个适当的极化电位值△E,2△E和-2△E,测量出的相应的极化 电流密度,与极化电位值的关系分别为:
i(△E)=
icorr[exp(
2.3E ba
)-exp(
2b.3c E)]
i(2△E)=
icorr[exp(
4.6E ba
)-exp(
4b.6c E)]
i(-2△E)=
icorr[exp(
1、极化方法与方程式
方法:对腐蚀体系施加恒定电流(其数值应使极化电位不超过10mv),从自腐电 位开始极化,记录其极化电位—时间曲线,由充电曲线方程式计算出稳态时的极化 电位之IRp I已知,求出 Rp
a. 恒电流小极化时可得恒电流充电曲线方程式:
利用电化学法测定材料腐蚀速率的实验技巧

利用电化学法测定材料腐蚀速率的实验技巧Introduction材料腐蚀是一种常见问题,对于各个领域的材料应用都具有重要意义。
因此,准确测定材料的腐蚀速率对于材料科学和工程来说至关重要。
电化学法作为一种常用的测定方法,能够提供快速、准确的腐蚀速率数据,并广泛应用于各种材料腐蚀性能研究中。
本文将讨论利用电化学法测定材料腐蚀速率的实验技巧。
Materials and Methods首先,准备所需的实验材料和设备。
这包括待测材料的试样、电化学腐蚀测试仪器(如电极、电解池等)、参比电极和工作电极等。
试样的选择应根据研究对象的特点和预期实验结果进行,确保能够获得可靠的数据。
其次,在进行实验前,需要对实验装置进行校准。
校准方法包括校正电压、电流和电解液浓度等参数。
校准后,确保实验装置的稳定性和准确性。
实验过程在进行实验之前,需要清洗待测材料试样以去除表面的氧化物和杂质等。
清洗方法应根据材料的特性进行选择,可以采用酸洗、溶剂洗涤或者机械抛光等方式。
确保试样表面的纯净度,以提高实验结果的可靠性。
完成试样处理后,将其装入电化学腐蚀测试装置中。
注意保持试样与电解液的充分接触。
同时,为了保持实验的一致性,应将参比电极和工作电极置于相同条件下进行测试。
设置实验条件,包括温度、溶液类型和浓度等。
这些条件的选择应根据具体研究目的和材料性质来确定。
实验条件的选择对于腐蚀速率的测定具有重要影响,因此需要仔细考虑。
在实验过程中,需要记录电压、电流以及时间等参数。
这些数据将用于计算腐蚀速率。
为了提高数据的准确性,应进行多次重复实验,并取平均值作为最终结果。
结果和讨论通过实验测定,可以得到材料的腐蚀速率数据。
这些数据可以用于评估材料的耐腐蚀性能,并对材料设计和工程应用提供参考。
根据实验结果,可以分析材料的腐蚀机理和影响因素。
例如,通过观察腐蚀产物的形貌和组成,可以判断腐蚀的类型(如局部腐蚀、晶间腐蚀等)。
此外,还可以通过改变实验条件,如温度和溶液浓度等,来探究腐蚀速率的变化规律。
腐蚀电化学及电化学测量方法

腐蚀电化学及电化学测量方法绪在近几十年里腐蚀电化学基理研究在金属的钝化、小孔腐蚀、电化学噪声以及电化学阻抗谱等方面取得了丰硕的成果。
为解释腐蚀现象,解决生产中的实际问题奠定了理论基础。
在我们的日常生产和生活中所看到的腐蚀现象大多是电化学腐蚀,例如大气腐蚀、土壤腐蚀、海水腐蚀等自然环境腐蚀和炼油装置中的常减压塔塔顶腐蚀、冷却水腐蚀、储油罐罐顶腐蚀等等,都是电化学腐蚀。
因此了解电化学腐蚀原理以及电化学研究方法是非常有用的,首先,对进一步做好防腐工作有帮助,因为缓蚀剂作用原理、腐蚀的阴极保护原理所依据的理论基础都是腐蚀电化学;其次,有助于正确选择和有效运用电化学监测手段。
下面我们共同回顾和学习一些腐蚀电化学中最为基础和与电化学监测技术紧密关联的部分,以便于在实际工作中的运用。
电化学腐蚀就是在金属在腐蚀的过程中伴随着电子的移动。
第一章、电化学腐蚀原理一、电化学腐蚀机理:电化学腐蚀机理可归纳为电池作用:绝大多数属微电池作用,如金属的自腐蚀,肉眼看不到;少数情况是宏观电池作用,如电偶腐蚀,肉眼能分辨阴阳极。
电解作用:1.微电池腐蚀如上图,工业纯锌放在稀硫酸中,在金属锌晶粒溶解的同时,有气泡在锌中杂质上形成并逸出,这种气泡就是氢气,而且在杂质与锌晶粒之间有电流流动。
此现象同Zn-Cu与稀硫酸形成的原电池作用是完全相同的,在锌电极上发生锌的溶解,在铜电极上逸出氢气泡,两电极间有电流流动。
概念:阳极:发生溶解的电极(锌或锌晶粒)阴极:另一极(铜或杂质)电极反应式:阳极:Zn Zn2++2e电子从阳极流到阴极。
阴极:H++e HH+H H2 图2 腐蚀原电池示意图图1 锌在稀盐酸中腐蚀示意图△阴阳极概念的进一步:产生电池作用的推动力是电极之间存在着电位差。
电极电位较负者为阳极电极电位较正者为阴极小结:我们把微电池的腐蚀作用看作是金属中电极电位不同的两个微观部分直接作电接触,其表面又同时与电解质溶液接触的原电池作用。
化学检验工常见电化学涂层性能测试方法

化学检验工常见电化学涂层性能测试方法电化学涂层是一种常见的表面处理方法,可用于增加材料的耐腐蚀性能、改善导电性能等。
为了确保电化学涂层的质量,需要进行一系列的性能测试。
本文将介绍几种常见的电化学涂层性能测试方法。
1. 腐蚀性能测试电化学腐蚀测试是评估电化学涂层耐腐蚀性能的重要方法之一。
常用的测试方法包括极化曲线法和电化学阻抗谱法。
(1)极化曲线法极化曲线法是一种通过测量极化曲线来评估电化学涂层在腐蚀环境中的抗腐蚀性能的方法。
通过应用一定电位范围内的电流,可以观察到电流随电位的变化关系,从而评估涂层的耐腐蚀性能。
(2)电化学阻抗谱法电化学阻抗谱法是一种通过测量电化学阻抗谱曲线来评估电化学涂层耐腐蚀性能的方法。
该方法可以得到频率范围内的电阻和电容数值,通过分析这些数据可以评估涂层的耐腐蚀性能。
2. 导电性能测试导电性能是衡量电化学涂层质量的关键指标之一。
常用的测试方法有四探针法和电阻率测量法。
(1)四探针法四探针法是一种通过测量电阻来评估电化学涂层导电性能的方法。
在该方法中,四个探针被插入涂层中,通过测量电流和电阻的关系,可以计算涂层的电导率和电阻率。
(2)电阻率测量法电阻率测量法是一种通过测量涂层材料的电阻来评估导电性能的方法。
该方法使用导电传感器在涂层表面上测量电阻,通过计算电阻率可以评估涂层的导电性能。
3. 附着力测试附着力是评估电化学涂层质量的重要指标之一。
常用的测试方法包括划伤测试、拉伸测试和冲击测试。
(1)划伤测试划伤测试是一种通过使用硬度指针在涂层表面划伤,从而评估涂层与基材之间的附着力的方法。
通过观察划痕形状和痕迹深度,可以评估涂层的附着力。
(2)拉伸测试拉伸测试是一种通过施加拉伸力来评估涂层与基材之间的附着力的方法。
通过在涂层上施加力并测量力的变化,可以计算涂层与基材的附着力。
(3)冲击测试冲击测试是一种通过施加冲击力来评估涂层与基材之间的附着力的方法。
常用的冲击测试方法包括钢球落锤测试和冲击炮测试,通过观察涂层破损情况可以评估附着力。
电化学腐蚀
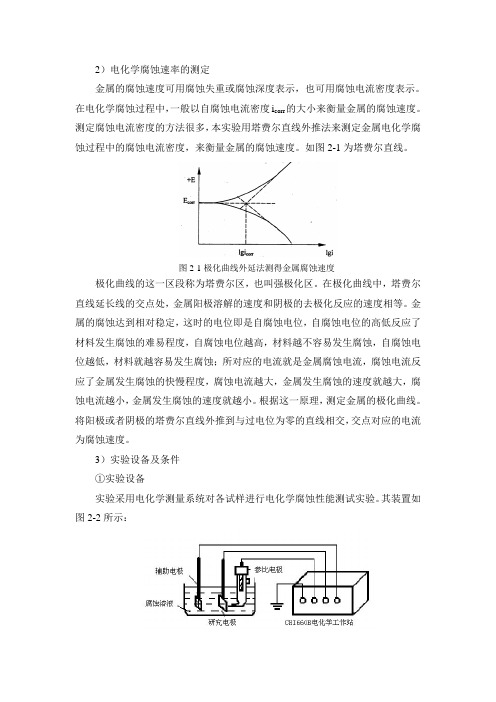
2)电化学腐蚀速率的测定金属的腐蚀速度可用腐蚀失重或腐蚀深度表示,也可用腐蚀电流密度表示。
在电化学腐蚀过程中,一般以自腐蚀电流密度i corr的大小来衡量金属的腐蚀速度。
测定腐蚀电流密度的方法很多,本实验用塔费尔直线外推法来测定金属电化学腐蚀过程中的腐蚀电流密度,来衡量金属的腐蚀速度。
如图2-1为塔费尔直线。
图2-1极化曲线外延法测得金属腐蚀速度极化曲线的这一区段称为塔费尔区,也叫强极化区。
在极化曲线中,塔费尔直线延长线的交点处,金属阳极溶解的速度和阴极的去极化反应的速度相等。
金属的腐蚀达到相对稳定,这时的电位即是自腐蚀电位,自腐蚀电位的高低反应了材料发生腐蚀的难易程度,自腐蚀电位越高,材料越不容易发生腐蚀,自腐蚀电位越低,材料就越容易发生腐蚀;所对应的电流就是金属腐蚀电流,腐蚀电流反应了金属发生腐蚀的快慢程度,腐蚀电流越大,金属发生腐蚀的速度就越大,腐蚀电流越小,金属发生腐蚀的速度就越小。
根据这一原理,测定金属的极化曲线。
将阳极或者阴极的塔费尔直线外推到与过电位为零的直线相交,交点对应的电流为腐蚀速度。
3)实验设备及条件①实验设备实验采用电化学测量系统对各试样进行电化学腐蚀性能测试实验。
其装置如图2-2所示:图2-2 电化学极化曲线测量装置示意图实验装置中三电极体系中以饱和甘汞(SCE)电极作为参比电极(reference electrode);Pt 电极作为辅助电极(auxiliary electrode);代测试样为研究电极(research electrode)。
参比电极和研究电极间用盐桥连接,鲁金毛细管(capiliary)距研究电极1~2毫米。
电化学工作站部分参数如下:初始电位(V):-2;终止电位(V):2.2;扫描段数:1;终止电位处保持时间:0;静置时间:2s;电流灵敏度(A/V):1.e-0.04。
②实验条件a.腐蚀试样:对1#到12#试样进行蜡封,即:在试样上用油性笔取1cm×1cm 的面积,并在其上放置橡皮,而后将烧化的蜡汁快速滴于试样表面,即蜡封处理。
第八章 腐蚀试验方法

Z Rs
Z
1 1 Q2 R
2
1 1 Q1 R
1
含锌Ni(OH)2碱性电池的EIS谱图
0%的DOD(放电深度)时不同Zn含量的Zn-Ni(OH)2碱性充电电池的EIS谱图 H.Chen,JQ Zhang, J Solid State Electrochem,2005 9:421-428
复合元件的CDC示例
按规则(1)将这一等效电路表示为: R1CE-1 按规则(2),CE-1可以表示为 (Q2CE-2). 因此整个电路可进一步表示为: R1(Q2CE-2) 将复合元件CE-2表示成: W3CE-3 整个等效电路就表示成: R1(Q2(W3CE-3)) 将简单的复合元件CE-3表示出来。应表 示为(R4C5),于是电路可以用如下的 CDC表示:R1(Q2(W3(R4C5)))
EIS测量的前提条件
因果性条件: 测定的响应信号是由输入的扰动信号引起的; 线性条件: 对体系的扰动与体系的响应成线性关系; 稳定性条件: 电极体系在测量过程中是稳定的,当扰动停止后, 体系将回复到原先的状态; 有限性条件: 在整个频率范围内所测定的阻抗或导纳值是有限的.
阻纳的复平面(Nyquist)图
用上图装置测量的极化曲线(Zn和Cu面积相等)
E
Eoc(cu) 欧姆电阻压降iR Ec(cu) Ea(Zn)
Eoa(Zn)
i
imax
Evans极化图及其应用
Evans极化图
E
Eoc Ecor Eoa
Icor
I
英国科学家 Evans 是 世界最著名的腐蚀专家, 大气腐蚀理论创始人 , 防腐包装技术的奠基者。 从事金属保护及金属电 化学研究工作。 1923 年 Evans 首先提出金属的大 气腐蚀理论 ,并阐述了 金属腐蚀的电化学特征, 特别强调了水蒸气的影 响。
腐蚀电化学常规测量方法共67页

21、静念园林好,人间良可辞。 22、步步寻往迹,有处特依依。 23、望云惭高鸟,临木愧游鱼。 24、结庐在人境,而无车马喧;问君 何能尔 ?心远 地自偏 。 25、人生归有道,衣食固其端。
41、学问是异常珍贵的东西,从任何源泉吸 收都不可耻。——阿卜·日·法拉兹
42、只有在人群中间,才能认识自 己。——德国
43、重复别人所说的话,只需要教育; 而要挑战别人所说的话,则需要头脑。—— 玛丽·佩蒂博恩·普尔
44、卓越的人一大优点ຫໍສະໝຸດ :在不利与艰 难的遭遇里百折不饶。——贝多芬
45、自己的饭量自己知道。——苏联
第五章 腐蚀电化学测试技术

化学成分不均一 组织结构不均一 电化学不均一性 物理状态不均一 表面膜不完整
综上所述,腐蚀电池实质上就是一个短路的原电 池。宏观腐蚀电池和微电池仅仅在形式上有区别,工 作原理完全相同。它们都是由阳极过程、阴极过程和 电流流动三个相互联系的环节构成的,三个环节缺一 不可。如果其中某个环节受到阻滞,则整个腐蚀过程 就会缓慢或完全停止。
四、金属电化学腐蚀的热力学条件
电位比较准则:
G nF nF( Ee,K Ee,A )
由腐蚀反应发生的条件G < 0,可得 E e, K – E e, A > 0 或 E e, K > E e, A 判断电化学腐蚀倾向的电位比较准则:
如果金属发生氧化反应的平衡电位Ee.A低于溶液中 某种氧化剂(即去极化剂)发生还原反应的平衡电位Ee.K ,则电化学腐蚀能够发生。二者的差值(Ee.K – Ee.A)愈 大,腐蚀的倾向愈大。
1 Zn O2 ZnO 2
2、电化学腐蚀:金属腐蚀的 氧化还原反应有着两个同时进行 却又相对独立的过程。例如金属 锌在含氧的中性水溶液中的腐蚀 。 金属放出自由电子成为阳离子 的反应称为阳极反应。金属发生 阳极反应的表面部位称为阳极区 。 接受电子的反应称为阴极反应 。发生阴极反应的表面部位称为 阴极区。 反应产物Zn(OH)2不是由氧分 子与锌原子直接碰撞结合形成的 ,而是通过了下列步骤:
0 K
0 A
第二节 腐蚀速度
一、极化与超电压 1、极化现象 (1)原电池中两电极的极化 曲线 原电池中,负极是阳 极,正极是阴极。随着电 流密度的增加,阳极析出 电势变大,阴极析出电势 变小。由于极化,使原电 池的作功能力下降。 但可以利用这种极化 降低金属的电化腐蚀速度
第二节 腐蚀速度
腐蚀测量及技术PPT学习教案

涂层测厚技术
第19页/共65页
点蚀深度的测量
测量孔深。
• 微米规与深度计:用带有刚性细长探针的微米规或 带尖针的深度计测定孔底部及边缘未腐蚀区的读数差, 作为孔深。
• 机械切削法:选定一未腐蚀面为基准,用机械加工 方法切削直至蚀孔消失。机床的行程表示孔深。
涡流检测法
• 原理:在具有一定导电率的工件上放置一检查线圈以产生 交变磁场,它在工件内感生涡流,后者同样也产生一交变磁场 。按照楞次定律,工件中产生的磁场与外磁场方向相反。材料 中局部缺陷会影响次级涡流的作用范围。利用这个效应,通过 检查这两个交互作用的磁场来发现材料内部的裂纹、鼓泡等腐 蚀现象 • 方法:用触头式线圈或环形线圈检测系统,在任意一无缺 陷的位置将阻抗调到某一零位。一旦线圈移到工件中有缺陷处 ,初级线圈在工件中产生的涡流就发生变化,使次级交变磁场 也发生变化,反过来又影响到初级激励磁场,使事先调整好的 阻抗零点发生位移。根据这种位移信号确定缺陷大小和位置 • 优缺点:方法简便,常用于储罐底板腐蚀检测,也用于测 厚,需专用仪器和定标技术
• 优缺点:本方法适用于各种腐蚀作用和类型,尤其在 系统内介质为气体或液体是更为适用。本方法操作容易、 结果准确。但测试监控的时间比较长,变化速度较慢,变 化过程无法详细了解。
第21页/共65页
热流法
• 透热法:先在容器或管壁一侧均匀加热,在加热过 程记录另一侧的温度变化。对相同材料而言,壁厚薄的 地方相对应的另一侧处温度上升较快。若材料中有缺陷 (如:裂纹或夹杂),其导热性比工件材料要差,使通 过该处热流减慢。利用这种热流差别来发现壁厚的局部 变化及内部缺陷。
第13页/共65页
直接称重法
• 原理:直接测定腐蚀后试样的质量变化来确定其发生的腐
腐蚀电化学常规测量方法讲义69页PPT

•
26、我们像鹰一样,生来就是自由的 ,但是 为了生 存,我 们不得 不为自 己编织 一个笼 子,然 后把自 己关在 里面。 ——博 莱索
•
27、法律如果不讲道理,即使延续时 间再长 ,也还 是没有 制约力 的。— —爱·科 克
•
28、好法律是由坏风俗创造出来的。 ——马 克罗维 乌斯
▪
27、只有把抱怨环境的心情,化为上进的力量,才是成功的保证。——罗曼·罗兰
▪
28、知之者不如好之者,好之者不如乐之者。——孔子
▪
29、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达·芬奇
▪
30、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华
谢谢!Biblioteka 69•29、在一切能够接受法律支配的人类 的状态 中,哪 里没有 法律, 那里就 没有自 由。— —洛克
•
30、风俗可以造就法律,也可以废除 法律。 ——塞·约翰逊
▪
26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭
基本的电化学腐蚀测量本的电化学腐蚀测量

基本的电化学腐介绍大多数金属腐蚀通过在金属与溶液层形成了溶液。
大桥中的钢筋发生发生在非水系统中。
腐蚀通常以正、逆反应达到平衡时一个是发生阴极反应,溶液中的离应达到平衡时,每个反应的电荷转同金属接触。
图1-1是上述过程的图解。
纵轴是曲线表示总电流—阴极电流和阳极点就是电流发生改变的地方,即反于将横轴对数化造成。
横轴对数化是由于钝化现象,电流值改变6个数图1-1 腐蚀过程中阳极和阴极电流金属电位 是阳极和阴极反应平衡时假设阳极反应产生过多电子只金属应。
这抵消了系统中的初始扰动在大多数腐蚀电化学试验中,第一偏向于开路电位。
腐蚀科学家在测量开路电位很重要定的开路电位表示所要研究的系统化学腐蚀测量与溶液界面上发生的电化学反应而产生。
对大气腐蚀而言金属筋发生腐蚀的电解液是潮湿的混凝土。
尽管大多数腐蚀发生在平衡时的速率发生。
首先是阳极反应,金属被氧化,释放离子中的离子(通常是O2 或 H+)被还原,吸收了来自金属的电电荷转移速度相等,没有净电流产生。
正、逆反应可发生在同纵轴是电位,横轴是电流的对数。
理想的阴、阳极反应电流如和阳极电流之和。
这是在用恒电位仪进行电位扫描时测得的电即反应从阳极反应转变成阴极反应或是阴极反应转变成阳极数化是必要的,因为在一个腐蚀试验中,较宽范围内的电流值个数量级不常见。
极电流部分平衡时的电位。
参照图1-1。
注意每个半反应的电流取决于金属只金属表面。
过剩电子使得金属电位向负向移动,减缓阳极反扰动。
第一步就是测量开路电位。
开路电位和腐蚀电位的关系通常很重要的一点就是在进行试验前给予足够时间使得开路电位达的系统处于稳定状态,即各种腐蚀反应的速度恒定。
有言金属表面薄的水分子发生在水中,也有腐蚀放离子至金属表面。
另属的电子。
当这两个反生在同一金属或两种不电流如图中直线所示。
得的电流。
图像中的尖成阳极反应。
尖点是由电流值需展示在图中。
于金属的电化学电势。
阳极反应,加快阴极反系通常可互换,但是更电位达到稳定状态。
电化学腐蚀实验

实验内容和步骤
A. 配制3%NaCl溶液 称取6克NaCl倒入烧杯,加入适量蒸馏水,搅拌至完全 溶解,移入容量瓶,并加蒸馏水到刻度线,配成均匀溶 液。
腐蚀电化学实验
电化学腐蚀 腐蚀电化学测试原理 动电位扫描实验
电化学腐蚀
定义:金属与电解质发生电化学反应而引起的变质或破坏过程。 原因:金属组织的不均匀性或电解质中的浓度差(例如氧)导致电
位不同而形成了腐蚀原电池。 电荷转移:电势较低的部位易失去电子而遭受氧化腐蚀,称此为阳
极,而电势较高的部位是阴极,它将阳极流来的电子传给电解质 中被还原的物质,发生还原反应,因此阴极仅起电子传递作用而 不受腐蚀。 阳极反应 :M→Mn++ne
I = f (E) 以电位为自变量,通过调节使电极恒定在某一电位,测量相应
的极化电流值; 然后把电位恒定在另一数值上再读取新的极化电流值, 这样逐点地测定,得到相应的极化电流随电位变化的函数关系。
控制电位以规定的速度连续线性变化,同步地记录相应
的电流随电位的变化,自动给出极化曲线,这就称为动 电位扫描法。这种方法具有恒电位的性质,故也称为恒
腐蚀电池:
组成和反应与原电池相同,但腐蚀电池为短路的 腐蚀电池仅是一个能进行氧化还原反应的电极体
系,电极反应的结果导致阳极金属氧化溶解而发生 腐蚀。
腐蚀原电池的组成
A
K
Zn
Cu
Zn
Cu
Cu Cu Cu
HCl溶液
HCl溶液
腐蚀电化学方法概述

CV和LSV扫描速度:0.000001-5,000V/s 电位扫描时电位增量:0.1mV@500V/s CA和CC脉冲宽度:0.0001-1,000sec CorrTest CA和CC阶跃次数:320 DPV和NPV脉冲宽度:0.0001-10sec SWV频率:1-100kHz ACV频率:0.1-10kHz SHACV频率:0.1-5kHz IMP频率:0.00001-100kHz 自动电位和电流零位调整 电位和电流测量低通滤波器,自动或手动设置, 覆盖八个数量级的频率范围 旋转电极控制输出:0-10V(以上型号) 电解池控制输出:通氮,搅拌,敲击 最大数据长度:128,000点-4,096,000点可选择 仪器尺寸:(宽)(深)(高) 仪器重量:
6. 电解池设计和电极位置:电力线分布均匀,有效工作面积=实际工作面积;
辅助电极和工作电极对称性;辅助电极和工作电极间的电阻; 7. 溶液电阻对稳态测量影响:高电流区极化曲线无线性范围畸变; 8. 溶液电阻对暂态测量影响:高电流脉冲对恒电位仪功率储备的影响;电解 池时间常数必须小于暂态测量时间标度,消除过渡过程的影响。
ZAHNER
Gamry
2.2 电化学测试有效性的检测
体系响应异常的可能性:恒电位仪器故障/电解池故障 1. 电子元件等效电路取代电解池方法 2. 参比电极问题:盐桥和鲁金毛细管问题;接触问题;准参比电极取代法;
3. 辅助电极和工作电极问题:连接;表面状态和表面膜变化;
4. 电化学阻抗高频响应进入第VI象限:恒电位仪响应不够导致相移; 5. 频率响应分析仪连接错误:V1/V2;软件和硬件检测;
① 腐蚀电化学测量体系
1. 电极电位和电池电动势 2. 三电极体系:
工作电极:金属电极、汞电极、碳电极;可重现表面;
金属的电化学腐蚀完整版PPT课件-2024鲜版

金属的电化学腐蚀过程
阳极过程
金属原子失去电子成为金属离子,进入电解质溶液。 阳极反应通常是金属的氧化反应。
阴极过程
电解质溶液中的氧化剂在阴极接受电子,发生还原反 应。阴极反应通常是氧或氢离子的还原。
电流回路
通过电解质溶液和金属内部的电子流动,形成闭合回 路,维持腐蚀反应的进行。
2024/3/28
2024/3/28
19
缓蚀剂的应用
无机缓蚀剂
如硅酸盐、磷酸盐等,通过与金 属表面发生化学反应形成保护膜,
减缓金属的腐蚀速率。
2024/3/28
有机缓蚀剂
如胺类、醛类、羧酸类等有机化合 物,通过吸附在金属表面形成保护 膜或改变金属表面的电化学性质来 抑制腐蚀。
复合缓蚀剂
将无机缓蚀剂和有机缓蚀剂复配使 用,发挥协同作用,提高缓蚀效果。
2024/3/28
表面改性
通过化学或物理方法改变 金属表面的性质,提高其 耐蚀性,如化学镀、激光 处理等。
表面合金化
在金属表面形成耐蚀性合 金层,提高金属的耐蚀性 能。
18
阴极保护与阳极保护
阴极保护
通过向金属施加负电位,使其成为阴 极而得到保护,如外加电流阴极保护 和牺牲阳极阴极保护等。
阳极保护
将金属连接到外加电源的正极上,使其 成为阳极并形成致密的氧化膜,从而防 止金属的进一步腐蚀。
可以缩短试验周期,降低成本,同时模拟多 种腐蚀因素的作用。
缺点
应用范围
模拟条件与实际使用环境可能存在差异,结 果仅供参考。
适用于金属材料的耐腐蚀性能评估和选材依 据。
2024/3/28
25
06
金属电化学腐蚀的案例分析与讨论
2024/3/28
电化学腐蚀试验

实验九极化曲线的测定【目的要求】1. 掌握稳态恒电位法测定金属极化曲线的基本原理和测试方法。
2. 了解极化曲线的意义和应用。
3. 掌握恒电位仪的使用方法。
【实验原理】1. 极化现象与极化曲线为了探索电极过程机理及影响电极过程的各种因素,必须对电极过程进行研究,其中极化曲线的测定是重要方法之一。
我们知道在研究可逆电池的电动势和电池反应时,电极上几乎没有电流通过,每个电极反应都是在接近于平衡状态下进行的,因此电极反应是可逆的。
但当有电流明显地通过电池时,电极的平衡状态被破坏,电极电势偏离平衡值,电极反应处于不可逆状态,而且随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。
由于电流通过电极而导致电极电势偏离平衡值的现象称为电极的极化,描述电流密度与电极电势之间关系的曲线称作极化曲线,如图2-19-1所示。
图2-19-1 极化曲线A-B:活性溶解区;B:临界钝化点B-C:过渡钝化区;C-D:稳定钝化区D-E:超(过)钝化区金属的阳极过程是指金属作为阳极时在一定的外电势下发生的阳极溶解过程,如下式所示:M→M n++n e此过程只有在电极电势正于其热力学电势时才能发生。
阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,但当阳极电势正到某一数值时,其溶解速度达到最大值,此后阳极溶解速度随电势变正反而大幅度降低,这种现象称为金属的钝化现象。
图2-19-1中曲线表明,从A点开始,随着电位向正方向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减至最小,这是因为在金属表面生产了一层电阻高,耐腐蚀的钝化膜。
B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流。
电势到达C点以后,随着电势的继续增加,电流却保持在一个基本不变的很小的数值上,该电流称为维钝电流,直到电势升到D点,电流才有随着电势的上升而增大,表示阳极又发生了氧化过程,可能是高价金属离子产生也可能是水分子放电析出氧气,DE段称为过钝化区。
腐蚀电化学常规测量方法共67页

END
Hale Waihona Puke 腐蚀电化学常规测量方法56、死去何所道,托体同山阿。 57、春秋多佳日,登高赋新诗。 58、种豆南山下,草盛豆苗稀。晨兴 理荒秽 ,带月 荷锄归 。道狭 草木长 ,夕露 沾我衣 。衣沾 不足惜 ,但使 愿无违 。 59、相见无杂言,但道桑麻长。 60、迢迢新秋夕,亭亭月将圆。
16、业余生活要有意义,不要越轨。——华盛顿 17、一个人即使已登上顶峰,也仍要自强不息。——罗素·贝克 18、最大的挑战和突破在于用人,而用人最大的突破在于信任人。——马云 19、自己活着,就是为了使别人过得更美好。——雷锋 20、要掌握书,莫被书掌握;要为生而读,莫为读而生。——布尔沃
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用腐蚀极化图分析腐蚀速率控制因素
腐蚀的原动力
I corr
E E PC PA R
e C e A
e e 其中: EC :阴、阳极间的初始电位差 EA Pc,PA:阴、阳极极化率 R:以及欧姆电阻R
• 在腐蚀过程中如果某一步骤的阻力与其他步骤相 比大很多,则这一步骤对于腐蚀进行的速率影响 最大,称其称为腐蚀的控制步骤,其参数称为控 制因素。
第四章
暂态测量方法
主要测量某一个电化学变量随时间的变化。
决定暂态变化所需要时间的重要参数是“时间常数 ” 从测量的电化学变量分类:暂态电流测量和暂态电 位测量。
1 暂态过程的等效电路
由于暂态过程是随时间而变化的,因而相当 复杂。因此常常将电极过程用等效电路来描述, 每个电极基本过程对应一个等效电路的原件。如 果我们得到了等效电路中某个元件的数值,也就 知道了这个元件所对应的电极基本过程的动力学 参数。这样,我们就将对电极过程的研究转化为 对等效电路的研究。
二、电化学测量的基本原则
要进行电化学测量,研究某一个基本过程, 就必须控制实验条件,突出主要矛盾,使该过程 在电极总过程中占据主导地位,降低或消除其他 基本过程的影响,通过研化学测量的主要步骤
• 1、实验条件的控制 • 2、实验结果的测量
• 3、实验结果的解析
第二章
电化学测量的基本方法
1 电化学测量的基本元件介绍
⑴参比电极:参比电极的性能直接影响着电极电势的测 量或控制的稳定性。 ⑵盐桥:当被测电极体系的溶液与参比电极的溶液不同 时,常用盐桥把研究电极和参比电极连接起来。盐桥的 作用主要有两个,一是减小液界电势,二是减少研究、 参比溶液之间的相互污染。
腐蚀极化图 用于分析腐蚀速率的影响因素
(1)腐蚀速率与腐蚀电池初 始电位差的关系: 当阴极反应及其极化曲线相 同时,如果金属阳极极化程 度较小,金属的平衡电位越 低,则腐蚀电池的初始电位 差越大,腐蚀电流越大。
腐蚀极化图 用于分析腐蚀速率的影响因素
(2)极化性能对腐蚀速 率的影响 如果腐蚀电池体系中的 欧姆电阻很小,则电极 的极化性能对腐蚀速率 必然有很大影响。在其 他条件相同时,极化率 越小,其腐蚀电流越大, 即腐蚀速率越大。
扫描电压呈等腰三角形。如果前半部扫描(电压上升部分)为 去极化剂在电极上被还原的阴极过程,则后半部扫描(电压 下降部分)为还原产物重新被氧化的阳极过程。因此.一次 三角波扫描完成一个还原过程和氧化过程的循环,故称为循 环伏安法。
循环伏安法常用的测量体系为三电极体系,如图所示
循环伏安法的应用
循环伏安法是一种很有用的电化学研究方法,可用于电极 反应的性质、机理和电极过程动力学参数的研究。但该法 很少用于定量分析。(1)电极可逆性的判断 循环伏安法 中电压的扫描过程包括阴极与阳极两个方向,因此从所得 的循环伏安法图的氧化波和还原波的峰高和对称性中可判 断电活性物质在电极表面反应的可逆程度。若反应是可逆 的,则曲线上下对称,若反应不可逆,则曲线上下不对称 。(2)电极反应机理的判断 循环伏安法还可研究电极吸 附现象、电化学反应产物、电化学—化学耦联反应等。对 于有机物、金属有机化合物及生物物质的氧化还原机理研 究很有用。
第三章
稳态测量方法
稳态测量主要测量腐蚀金属电极的电位E 与连接腐蚀金属电极外线路中德电流之间的关 系。测量方式主要有两种:控制电位的测量和 控制电流的测量。
1
控制电位的测量
两种方法
恒电位法
电位扫描法
2
控制电流的测量
在恒电流电路或恒电流仪的保证下,控制通过 研究电极的极化电流按照人们预想的规律变化, 不受电解池阻抗变化的影响,同时测量相应电极 电势的方法。
电路接通
腐蚀极化图:一种电位-电流图,它是把表征腐蚀电 流特征的阴、阳极极化曲线画在同一张图上构成的。
腐蚀极化图的应用
腐蚀极化图是研究电化学腐蚀的重要理论工具 • 解释腐蚀过程中所发生的现象 • 分析腐蚀过程的性质和影响因素 • 确定腐蚀的主要控制因素 • 计算腐蚀速率 • 研究防腐蚀剂的效果与作用机理 • „„„
腐蚀电化学测量方法
报告人:叶超
指导老师 :赵晴
第一章 绪论
一、电化学测量方法的分类
• 第一类:电化学热力学性质的测量方法 • 第二类:单纯依靠电极电势、极化电流的 的控制和测量进行动力学性质的测量。 • 第三类:在电极电势、极化电流的控制和测量的 同时引入光谱波谱技术、扫描探针显微技术 的体系电化学性质测量方法
3 腐蚀金属电极的E-I曲线
由强极化区的极化曲线测定Icorr、ba、bc
4、稳态测量方法在金属腐蚀方面的应用
在金属腐蚀方面,测量极化曲线可得出阴极保护电势,
阳极保护的致钝电势、致钝电流、维钝电流、击穿电势和再 钝化电势等。测量极化曲线,采用强极化区、线性极化区和 弱极化区的方法可快速测量金属的腐蚀速度,从而快速筛选 金属材料的缓蚀剂。测量阴极极化曲线和阳极极化曲线,可 用于研究局部腐蚀。分别测量两种金属的极化曲线,可推算 这两种金属连接在一起时的电偶腐蚀。测量腐蚀系统的阴阳 极极化曲线,可查明腐蚀的控制因素、影响因素、腐蚀机理 及缓蚀剂作用类型。
(3)研究电极:电化学测量的主体,其选用的材料、结构形 式、表面状态对于电极上的电化学反应影响很大。 (4)电解池:电解池的结构和安装对电化学测量影响很大, 电解池的各个部件需要由具有不同性能的材料制成,对 材料的选择要根据具体的使用环境,其要具有良好的稳 定性,避免材料的分解产生杂志,干扰被测电极的过程
图2.1 三电极体系电路示意图
2 伏安法
伏安法主要有脉冲伏安法和线性电势扫描伏安 法,其中后者应用较为广泛。我们本节主要讨论 循环伏安法。
循环伏安法是指在电极上 施加一个线性扫描电压, 以恒定的变化速度扫描, 当达到某设定的终止电位 时,再反向回归至某一设 定的起始电位,循环伏安 法电位与时间的关系如图 所示
3 恒电流法测定阴极极化曲线
将研究电极的电流密度恒定在所需的值以后, 测定电极的稳定电位。
4 恒电压法测定阳极极化曲线
就是控制电极电位为一定值,然后测出 该电位下的极化电流密度。
5 腐蚀极化图
原电池在短接后,阴阳极的极化曲线如下图所示。
+E EeC 阴极 EC EA 阳极 EeA 0 开路 接通后 t EC - E A EeC - EeA
